Анодная и катодная защита от коррозии: Электрохимическая защита
Содержание
Анодно-катодная защита для газгольдера
Чтобы продлить срок службы газгольдера, он должен быть защищён от коррозии при помощи системы электрохимической защиты.
Даже самого эффективного антикоррозийного покрытия недостаточно для того, чтобы полностью предотвратить коррозию подземного резервуара для хранения сжиженного газа. Без электрохимической защиты срок его службы окажется значительно короче.
Существует два основных метода электрохимической защиты газгольдеров: активный и протекторная. Первый используют преимущественно с газгольдерами, выпущенными в России — такими, как FAS или «Фасхиммаш» (иногда их называют немецкими или российско-германскими), РП, РПГ и украинским «Фобосом».
Все эти газгольдеры изготовлены из подверженной коррозии стали 09Г2С или ее модификаций. Чтобы отсрочить распространение ржавчины, как правило, используют станцию катодной защиты мощностью 0,75 кВт.
Это довольно накладный метод защиты от коррозии. Станция постоянно потребляет электроэнергию, однако другого выхода нет. Без защиты российский резервуар приходит в негодность уже через пять-семь лет.
Без защиты российский резервуар приходит в негодность уже через пять-семь лет.
Газгольдеры европейских производителей, в том числе газгольдеры АвтономГаз, изготовленные польским заводом Chemet, защищают при помощи протекторной анодно-катодной системы.
При использовании протекторной защиты в котловане устанавливают элементы, изготовленные из металлов с более электроотрицательным потенциалом, и соединяют их с подземным резервуаром проводом. После этого протектор «берёт удар» на себя: алюминий, из которого он сделан, окисляется, а железо резервуара, наоборот, восстанавливается.
Протекторная защита от коррозии не нуждается в электроэнергии, но требует периодической замены протектора. Чтобы заменить протектор, возле подземного резервуара вручную бурят шурф, укладывают туда новый протектор и переключают провода на него.
Срок службы протектора зависит от модели газгольдера.
- Протекторы, которые защищают российские резервуары с битумным покрытием или европейские резервуары с эпоксидным покрытием, которое не прошло проверки во время монтажа, нужно менять каждый год.
 Столь малый срок службы связан с проницаемостью покрытия и расходовании жертвенного анода на восстановление железа резервуара, не защищаемого покрытием.
Столь малый срок службы связан с проницаемостью покрытия и расходовании жертвенного анода на восстановление железа резервуара, не защищаемого покрытием. - Европейские газгольдеры с неповреждённым эпоксидным покрытием требуют замены протектора один раз в три-семь лет.
- Газгольдеры АвтономГаз, изготовленные из стали, которая не подвержена коррозии, и покрытие ударопрочным пластиком полиуретан, нуждаются в новом протекторе лишь один раз в пятнадцать лет.
Газгольдеры АвтономГаз изготовлены из материалов, которые не подвержены коррозии. Тем не менее, электрохимическая защита нужна. Она служит для подстраховки на случай непредвиденных ситуаций — например, таких, как повреждения покрытия во время земляных работ или вмешательства вандалов.
Кроме того, система защиты служит заземлителем. Заземление резервуара необходимо при заправке, так как при течении газа по шлангу возникает сильное статическое электричество. Обычное стальное заземление приводит к ухудшению антикоррозионных свойств резервуара, применение в качестве заземлителя анода в активаторе значительно улучшает стойкость резервуара к коррозии.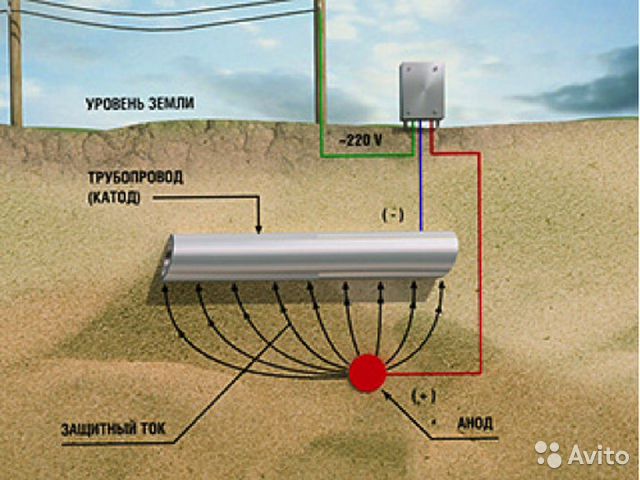
Каждый газгольдер АвтономГаз снабжён системой пассивной анодно-катодной защиты резервуара, состоящей из пятикилограммового магниевого анода и двенадцатикилограммового активатора Замена защиты осуществляется по результатам проверки при обслуживании. Клиентам, которые заправляются и обслуживаются в АвтономГаз, замена анодно-катодной защиты осуществляется бесплатно.
Решения для защиты судов и кораблей от коррозии — Корпорация ПСС
Вследствие коррозионно-механических разрушений выходит из строя большое количество корпусных конструкций судов и плавучих технических сооружений. Помимо экологической опасности при подобных авариях (загрязнение окружающей среды, потеря энергоресурсов), возникают значительные экономические убытки: потеря оборудования, затраты на ремонт, простой в работе. 10% металла теряется безвозвратно, рассеиваясь в виде продуктов окисления.
Производство оборудования для мониторинга и предотвращения коррозии на подводных частях корпуса судна является ключевой компетенцией Корпорации ПСС.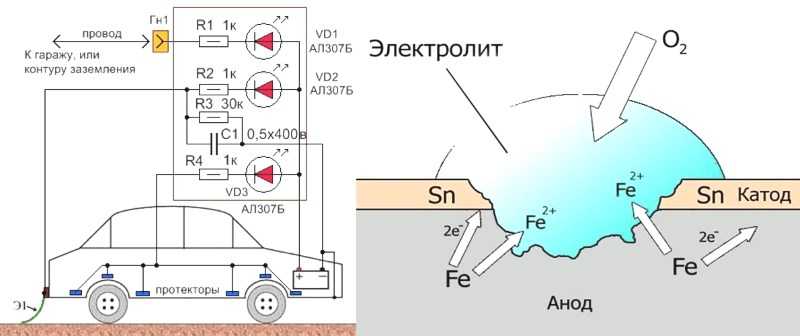
В зависимости от характера коррозии и условий ее протекания применяются различные методы защиты корпусных конструкций судов. Выбор того или иного способа определяется его эффективностью в данном конкретном случае, а также экономической целесообразностью. Любой метод защиты от коррозии изменяет ход коррозионного процесса, либо уменьшая скорость, либо прекращая его полностью. Надежным способом защиты от коррозионных разрушений стали в морской воде является электрохимическая защита.
Корпорация ПСС развивает два метода электрохимической защиты — протекторную (метод жертвенных анодов) и катодную (метод защиты наложенным током).
Сравнение методов
|
Протекторная защита Метод жертвенных анодов |
Катодная защита Метод защиты наложенным током |
|
+ работают независимо от источника электрической энергии |
— потребность в надежном источнике электропитания постоянного тока |
|
+ не могут быть неправильно прикреплены к конструкции |
— автоматическая работа, минимум внимания экипажа |
|
— незначительна эффективность при локальных формах коррозии |
+ возможность регулирования параметров защиты, в том числе и автоматического, что позволяет предотвратить коррозионные разрушения |
|
— необходимо наличие лакокрасочного покрытия |
+ достаточно установки относительно небольшого количества анодов даже для защиты больших конструкций без лакокрасочного покрытия в условиях высокого удельного сопротивления |
|
— ограниченный срок действия протекторов, необходима периодическая замена, в случае стационарного сооружения |
+ нет необходимости возобновления средств защиты, увеличивается междоковый период эксплуатации корпусов морских судов и сооружений |
|
— высокая стоимость установки анодов на месте |
+ сниженные расходы по обслуживанию, система обеспечивает защиту на весь срок службы |
|
— создает дополнительное сопротивление, имеют большую массу |
+ не создает дополнительного сопротивления |
Катодная защита
Это наиболее надежный и экономически выгодный способ предохранения от коррозии подводной части корпусов объектов морской инфраструктуры. Преимущества катодной защиты для защиты платформы:
Преимущества катодной защиты для защиты платформы:
- полное подавление коррозии обшивок и сварных швов
-
уменьшение запаса толщины обшивок на коррозионный износ - не требует замены в течение всего срока службы судна
-
удаленный мониторинг и контроль.
Опыт применения и расчеты показывают, что для судов с водоизмещением более 3400 тонн, оптимально использовать катодную защиту, ввиду значительного уменьшения массы по сравнению с протекторной, для судов с водоизмещением более 6000 тонн применение катодной защиты уменьшает суммарную стоимость защиты.
Корпорацией ПСС разработан целый комплекс для защиты судов методом наложенного тока. При использовании данного метода основными звеньями схемы являются:
- Станции катодной защиты (СКЗ) — защищает за счет сдвига потенциала на корпусе судна, на нем протекает только катодный процесс, коррозия замедляется.
 Станции производятся в разных модификациях и комплектациях. Включены в РМРС.
Станции производятся в разных модификациях и комплектациях. Включены в РМРС. - Аноды судовые — подключены к СКЗ и предназначены предназначены для стекания в воду защитного тока. Разработаны разные типы анодов для эксплуатации в разных районах плавания, в том числе в Арктике. Монтируются таким образом, чтобы не создавать помех при движении судна.
- Электрод сравнения хлорсеребряный производится в пластиковом корпусе или в защитном коффердаме. Они измеряют потенциал и используются в системах автоматического контроля и регулирования режима работы установок электрохимзащиты.
-
Кабель. Для систем ЭХЗ разработан кабель Elkaflex, который обладает стойкостью к маслобензопродуктам и другим агрессивным средам.
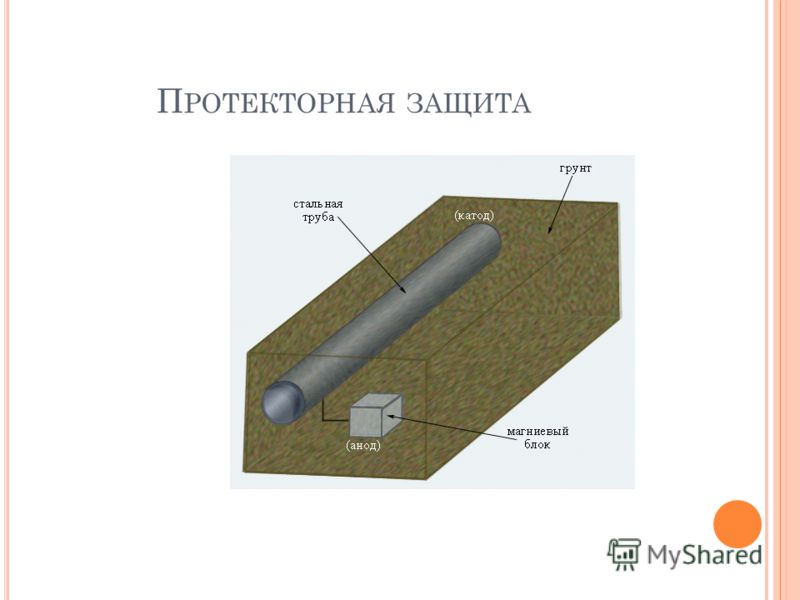
Протекторная защита
Протекторная защита экономична, проста и понятна. Протекторы медленно растворяются, защищая конструкцию, к которой они прикреплены. Представляют собой изделия из алюминиевого, цинкового или магниевого сплава с влитым стальным элементом для крепления. Отливаются из сплавов по ГОСТ 26251-84. Изготавливаются различных типоразмеров по требованиям заказчика. Форма определяется исходя из места и условии эксплуатации протектора. Так, на корпус судов оптимально использовать протекторы обтекаемых форм.
Отливаются из сплавов по ГОСТ 26251-84. Изготавливаются различных типоразмеров по требованиям заказчика. Форма определяется исходя из места и условии эксплуатации протектора. Так, на корпус судов оптимально использовать протекторы обтекаемых форм.
Корпорация ПСС предлагает широкий ассортимент протекторов для защиты судов:
П-НЛМ неотключаемый ленточный магниевый
П-НКМ неотключаемый концевой магниевый
П-ПОМ подвесной отключаемый магниевый
П-РОМ регулируемый отключаемый магниевый
П-КОМ короткозамкнутый отключаемый магниевый
П-КЛА короткозамкнутый линейный алюминиевый
П-ККА короткозамкнутый концевой алюминиевый
П-РОА регулируемый отключаемый алюминиевый
П-ПОА подвесной отключаемый алюминиевый
П-КОА короткозамкнутый одиночный алюминиевый
ПМФ межфланцевый
Морской климат, соленый воздух и вода разрушают не только части корабля, находящиеся в непосредственном контакте с водой, но и внутренние коммуникации. Для защиты труб применяются межфланцевые протекторы, а для исключения ржавления резьбовых соединений — болты-протекторы.
Для защиты труб применяются межфланцевые протекторы, а для исключения ржавления резьбовых соединений — болты-протекторы.
Разница между анодной и катодной защитой
Основное различие между анодной и катодной защитой заключается в том, что при анодной защите защищаемая поверхность действует как анод, тогда как при катодной защите защищаемая поверхность действует как катод .
Анодная и катодная защита — это два электрохимических процесса, которые мы используем для предотвращения коррозии или ржавления поверхностей. В электрохимическом процессе мы используем электрохимическую ячейку с двумя электродами в качестве анода и катода. В процессах анодной и катодной защиты мы используем защищаемую поверхность (подложку) в качестве анода или катода, что приводит к названию этих процессов как таковых. Протекторная защита — это тип катодной защиты, при котором мы используем металл в качестве расходуемого анода. В этом процессе этот жертвенный металл подвергается коррозии, избегая коррозии катода.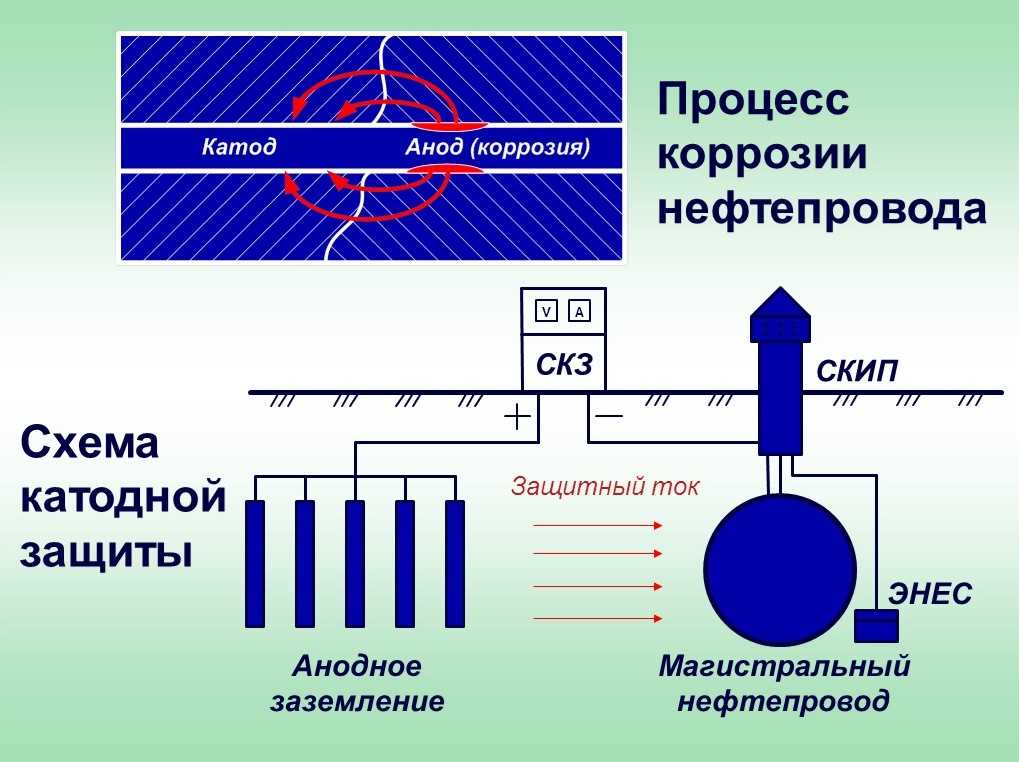
СОДЕРЖАНИЕ
1. Обзор и основные отличия
2. Что такое анодная защита
3. Что такое катодная защита
4. Прямые сравнения – анодная и катодная защита в табличной форме
5. Резюме
Что такое анодная защита ?
Анодная защита — это тип электрохимического процесса, при котором мы можем защитить металлическую поверхность, сделав ее анодом в электрохимической ячейке. Мы можем обозначить это как AP. Однако этот метод возможен только для комбинаций материала и среды, которые показывают довольно широкие пассивные области. то есть сталь и нержавеющая сталь в 98% серная кислота.
В АП нам нужно довести металл до высокого потенциала. Затем металл становится пассивным за счет образования защитного слоя. Однако AP не используется широко в качестве катодной защиты, поскольку он ограничен металлами, имеющими на поверхности достаточно надежный пассивный слой; например, нержавеющая сталь.
При применении AP необходимо учитывать два основных момента. Во-первых, нам нужно убедиться, что вся система находится в пассивном диапазоне. Во-вторых, нам необходимо иметь точное представление об ионах, что может привести к обширной точечной коррозии.
Во-первых, нам нужно убедиться, что вся система находится в пассивном диапазоне. Во-вторых, нам необходимо иметь точное представление об ионах, что может привести к обширной точечной коррозии.
Что такое катодная защита?
Катодная защита — это тип электрохимического процесса, при котором мы можем защитить металлическую поверхность, сделав ее катодом в электрохимической ячейке. Мы можем обозначить его как CP. CP может предотвратить коррозию металлических поверхностей. Существуют различные типы CP; например, гальваническая защита или протекторная защита, системы импульсного тока и гибридные системы.
Рисунок 01: Системы подаваемого тока
В этом методе корродирует жертвенный металл, а не защищаемый. Если мы используем катодную защиту для больших конструкций, таких как длинные трубопроводы, метода гальванической защиты недостаточно. Следовательно, нам необходимо обеспечить достаточный ток, используя внешний источник питания постоянного тока.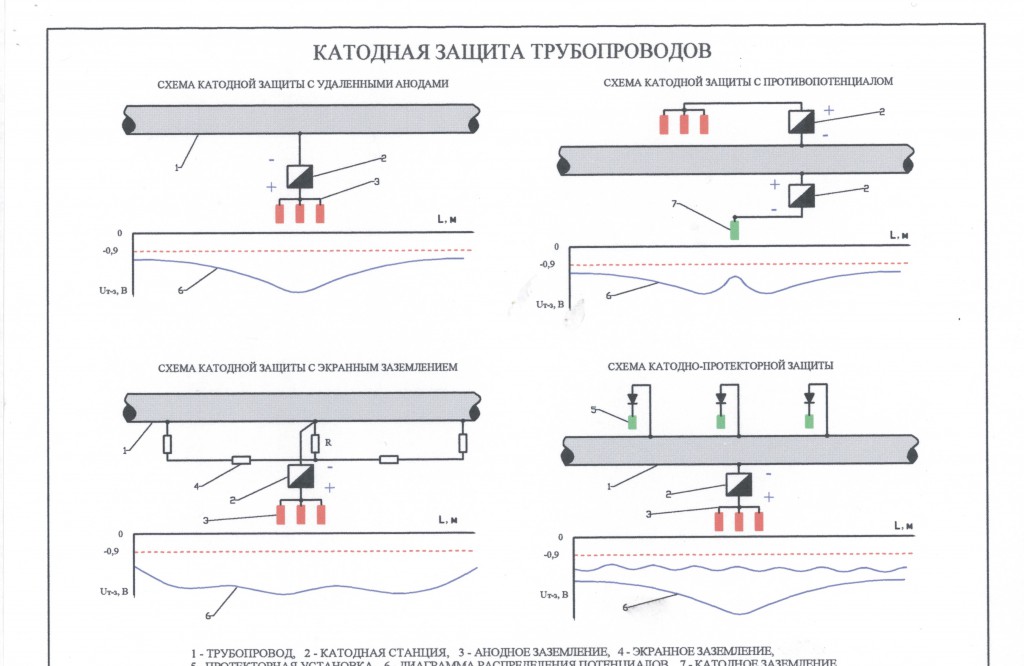
Рисунок 02: Жертвенный анод – слой цинка
Кроме того, мы можем использовать эту технику для защиты топливных или водопроводных трубопроводов, изготовленных из стали, резервуаров для хранения, корпусов кораблей и лодок, оцинкованной стали и т. д.
Что такое Разница между анодной и катодной защитой?
Анодная защита — это тип электрохимического процесса, в котором мы можем защитить металлическую поверхность, сделав ее анодом в электрохимической ячейке, а катодная защита — это тип электрохимического процесса, в котором мы можем защитить металлическую поверхность, сделав ее катодом. в электрохимической ячейке. Таким образом, ключевое различие между анодной и катодной защитой заключается в том, что при анодной защите защищаемая поверхность действует как анод, тогда как при катодной защите она является катодом.
Кроме того, анодная защита включает подавление реакционной способности металла путем регулирования потенциала более реакционноспособного металла; однако катодная защита включает изменение направления тока между двумя разнородными электродами. Следовательно, мы можем рассматривать и это как разницу между анодной и катодной защитой.
Следовательно, мы можем рассматривать и это как разницу между анодной и катодной защитой.
Резюме – Анодная и катодная защита
Анодная защита – это тип электрохимического процесса, в котором мы можем защитить металлическую поверхность, сделав ее анодом в электрохимической ячейке, а катодная защита – это тип электрохимического процесса, в котором мы может защитить металлическую поверхность, сделав ее катодом в электрохимической ячейке. Основное различие между анодной и катодной защитой заключается в том, что при анодной защите защищаемая поверхность действует как анод, тогда как при катодной защите она является катодом.
Ссылка:
1. «Что такое жертвенная защита? — Определение из Corrosionpedia». Corrosionpedia, доступно здесь.
Изображение предоставлено:
1. «Диаграмма катодной защиты» Кафе Нервоза — собственная работа (CC BY-SA 3.0) через Commons Wikimedia
2. «Жертвенный анод» Цвергельстерн (CC BY-SA 3.0) через Commons Wikimedia
Контроль коррозии с помощью анодной защиты
Контроль коррозии с помощью анодной защиты — technology. matthey.com
matthey.com
Защита от коррозии с помощью анодной защиты
Архив журнала
Platinum Metals Rev., 1960,
4 , (3), 86
Защита от коррозии с помощью анодной защиты
Поделиться этой страницей:
Твиттер
Фейсбук
LinkedIn
Реддит
Копать
СМЕШИВАНИЕ
Краткое содержание статьи
Метод катодной защиты хорошо известен и широко применяется для решения ряда проблем, связанных с коррозией. Не так хорошо известно, что коррозию можно также предотвратить в подходящих случаях с помощью анодной защиты с использованием системы платиновых электродов. Автор показывает, что при соответствующей предварительной лабораторной работе и надлежащем оборудовании использование анодной защиты может внести эффективный вклад в жизнь химического предприятия.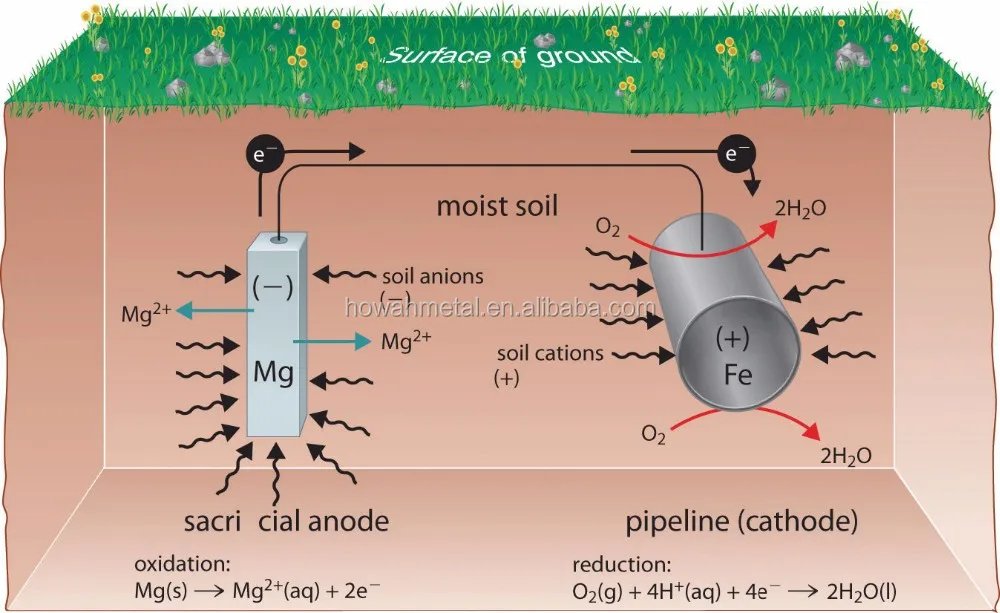
Хорошо известно, что коррозию иногда можно контролировать с помощью катодных токов, и даже при элементарных знаниях электрохимии легко понять, почему это должно быть так. Коррозия связана с окислением металла, и разумно ожидать, что катодная поляризация, препятствующая окислению и способствующая восстановлению на поверхности металла, должна обеспечивать защиту. На самом деле положение несколько сложнее, и во многих случаях другие факторы перевешивают этот, казалось бы, простой.
Не так хорошо известно, что коррозию можно также предотвратить в подходящих случаях с помощью анодной поляризации, и, конечно, гораздо труднее понять, почему это должно быть так, из несколько упрощенной теории коррозии, с которой неспециалист связан иметь. Вероятно, из-за этого этот чрезвычайно мощный метод, часто применимый именно тогда, когда катодная защита невозможна, не был легко принят в качестве практического предложения и до сих пор рассматривается только как лабораторная диковинка. Создается, кажется, ощущение, может быть, бессознательное, что метод в принципе несостоятелен, и цель настоящей статьи состоит в том, чтобы как можно проще объяснить, почему анодная защита возможна и когда ее можно ожидать. быть полезным.
быть полезным.
Общие принципы борьбы с коррозией
Если пренебречь методами «грубой силы» борьбы с коррозией, такими как пластик, стекло или другие покрытия, имеются два основных метода борьбы с коррозией. Во-первых, свести к минимуму движущую силу коррозии, а во-вторых, убедиться, что продукт коррозии сам подавляет реакцию, образуя подходящую защитную пленку.
Используя терминологию, предложенную Пурбэ (1), мы говорим, что в первом случае мы пользуемся иммунитетом, а во втором зависим от пассивности.
На практике мы можем добиться иммунитета, выполнив одно или несколько из следующих действий:
1 Использование подходящего благородного металла
2 Удаление ненужных окислителей (например, воздуха)
3 Добавление катодного ингибитора (снижение эффективности окислителей)
4 Нанесение катодной защиты
На химическом заводе часто нецелесообразно использовать благородные металлы, а если растворы сильно окисляются, другие методы неприменимы.
Пассивность достигается:
1 Использованием металла, содержащего оксид (или другой аналогичный продукт коррозии), который практически нерастворим в среде
2 Обеспечение постоянного наличия достаточного количества окислителя для образования оксида
3 Применение анодной поляризации для поддержания постоянного восстановления оксида
Таким образом, в принципе анодная защита имеет много общего с практикой добавления окисляющих веществ, таких как хроматы или нитриты, в качестве ингибиторов. С другой стороны, катодная защита в некотором роде связана с такими методами, как деаэрация.
Сходство можно продолжить. В системе металл/раствор, в которой коррозия низка из-за невосприимчивости, коррозия обычно усиливается либо добавлением окислителей, либо анодной поляризацией, тогда как в зависимости от пассивности опасно либо деаэрировать, либо применять катодную поляризацию. токи.
Защита черных металлов в кислых растворах
Анодная защита, вероятно, окажется наиболее полезной для сплавов на основе железа в кислых растворах, и по этой причине этот случай был выбран в качестве примера. На рис. 1 показана диаграмма Пурбе (1) для железа; указаны условия пассивности и иммунитета. Отсюда видно, что в кислых растворах имеется значительный разрыв потенциалов, при котором не устанавливается ни одно из этих условий и который должен приводить к сильной коррозии.
На рис. 1 показана диаграмма Пурбе (1) для железа; указаны условия пассивности и иммунитета. Отсюда видно, что в кислых растворах имеется значительный разрыв потенциалов, при котором не устанавливается ни одно из этих условий и который должен приводить к сильной коррозии.
Рис. 1
Диаграмма Пурбе для железа в водных растворах
Линии A и B на этой диаграмме относятся к нижнему и верхнему пределам стабильности воды. Выше А вода окисляется до кислорода, ниже А восстанавливается до водорода.
Если мы поместим железо в раствор сильной кислоты, то теоретически сможем защитить его катодно, снизив его потенциал до области иммунитета. Однако, поскольку вода нестабильна при таких низких потенциалах, будет происходить непрерывное и быстрое выделение водорода. Это непрактичный способ избежать коррозии как из-за очень высоких требований к току, так и из-за того, что нет смысла предотвращать коррозию, если для этого нам нужно разлагать раствор.
С другой стороны, повышение потенциала железа путем анодной поляризации или путем добавления подходящего окислителя до достаточно высоких значений пассивности кажется более многообещающим способом предотвращения коррозии. Это тем более так, что область пассивности для железа, и особенно для некоторых железо-хромовых сплавов, значительно больше, чем показано на рис. 1, полученном расчетным путем после некоторых допущений.
Это тем более так, что область пассивности для железа, и особенно для некоторых железо-хромовых сплавов, значительно больше, чем показано на рис. 1, полученном расчетным путем после некоторых допущений.
Фактическое соотношение между потенциалом и скоростью коррозии при заданном значении рН схематически показано в несколько упрощенном виде на рис. 2. Это экспериментально определяемая кривая для любого заданного раствора и сплава с использованием потенциостатических методов, которые становятся широко используемыми в коррозионные исследования (2). Из рис. 2, который типичен для многих случаев, видно, что как только потенциал поднимается достаточно, чтобы установить пассивность, скорость коррозии падает до действительно пренебрежимо малых значений. Например, для железа в нормальной серной кислоте скорость падает примерно до 0,1 мг/см 9 .0172 2 /сутки, а плотность тока, необходимая для поддержания пассивности, составляет 5 мкА/см 8 . Таким образом, скорость коррозии пассивного железа в этой кислоте незначительна, и железо может быть очень подходящим материалом для контейнеров.
Рис. 2
Связь между потенциалом и скоростью коррозии железа в серной кислоте
На данном этапе важно понимать, что скорость коррозии металла в данном растворе кислоты является точно определяемым свойством при условии, что указан потенциал. Сильно разбросанные и явно бессмысленные результаты, часто получаемые на обычных коррозионных «испытательных образцах», полностью обусловлены неконтролируемым блужданием потенциала, но как только для данной системы металл/раствор получены такие результаты, как на рис. 2, мы можем полностью зависят от них на практике, опять же при условии мы также гарантируем, что потенциал установки по отношению к раствору поддерживается на правильном уровне. В качестве альтернативы мы можем точно контролировать скорость коррозии, измеряя потенциал и обращаясь к рис. 2.9.0007
Из вышесказанного должно стать очевидным, что анодная защита — это просто способ гарантировать, что потенциал металла поддерживается достаточно высоким для стабильной пассивности.
Приборы
Если потенциал железа поднимается значительно выше линии А на рис. 1, происходит выделение кислорода (т. е. раствор начинает разлагаться и ток теряется), так что это накладывает верхний предел на желаемый потенциал. В нержавеющих сталях кислород обычно не выделяется, но скорость коррозии увеличивается выше определенного потенциала, так что снова существует верхний предел потенциала. С титаном (3) и некоторыми другими металлами, образующими непроводящие пленки, вообще существует гораздо большая свобода действий, и часто можно поднять потенциал на несколько десятков вольт, но и в этих случаях защита может выйти из строя, если потенциал поднят достаточно.
Важным фактом является то, что существует как верхний, так и нижний предел диапазона потенциалов, дающих удовлетворительные результаты. Это означает, что прибор, необходимый для анодной защиты, представляет собой «потенциостат», но точный характер прибора сильно зависит от системы.
Если диапазон удовлетворительных потенциалов велик, как в случае с титаном, очень простое устройство постоянного напряжения, такое как аккумулятор или даже сухой элемент, удовлетворит требованиям. В таком случае можно с уверенностью предположить, что потенциал инертного катода не будет отклоняться более чем на несколько сотен милливольт, каким бы ни был ток, и если потенциал между катодом и растением поддерживается достаточно высоким, то не будет опасности, что потенциал завода упадет до предела. Фактически Коттон нашел эту систему полностью удовлетворительной для титана в соляной кислоте.
В таком случае можно с уверенностью предположить, что потенциал инертного катода не будет отклоняться более чем на несколько сотен милливольт, каким бы ни был ток, и если потенциал между катодом и растением поддерживается достаточно высоким, то не будет опасности, что потенциал завода упадет до предела. Фактически Коттон нашел эту систему полностью удовлетворительной для титана в соляной кислоте.
Этот простой метод также может быть применим в некоторых случаях для ферросплавов, хотя полезный диапазон потенциалов составляет всего несколько сотен милливольт, но в целом было бы безопаснее использовать настоящий потенциостат. Этот прибор измеряет потенциал растения относительно стандартного электрода и поддерживает его на нужном уровне, пропуская поляризующий ток через инертный вспомогательный электрод.
Существует множество доступных схем потенциостатов, а лабораторные типы полностью электронные и могут очень точно контролировать потенциалы, но имеют довольно низкий выходной ток.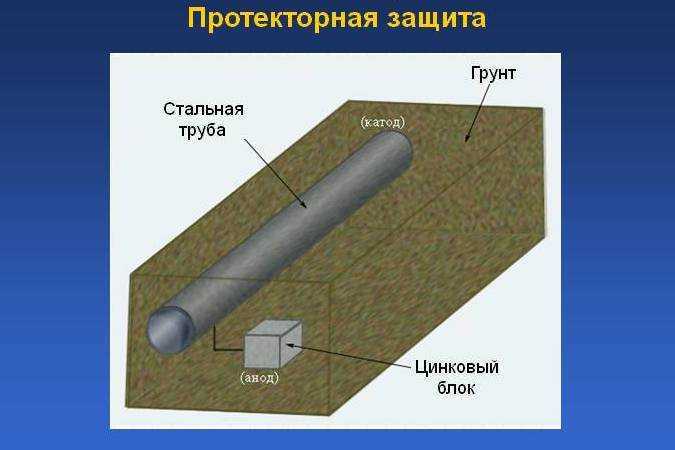 Для промышленного использования производительность является основным требованием, и инструмент с сервоприводом был бы более подходящим.
Для промышленного использования производительность является основным требованием, и инструмент с сервоприводом был бы более подходящим.
Стоимость оборудования для анодной защиты не должна быть высокой, даже если требуется настоящая потенциостатическая система, но, если метод будет использоваться с максимальной выгодой, стоит одновременно установить систему мониторинга. предоставить отчет о производительности установки с точки зрения коррозии (4). Это также может служить предупреждением, если произойдет что-то непредвиденное.
Позиция в точности аналогична использованию регулятора температуры, например, на печи, который защитит печь от перегрева, но без регистратора температуры или хотя бы индикатора система неполноценна.
Опасности и ограничения при применении анодной защиты
Метод особенно подходит для применения в тяжелой химической промышленности, но растворы, используемые на химическом заводе, настолько различаются, что каждый случай должен быть изучен в лабораторных масштабах перед анодной защитой.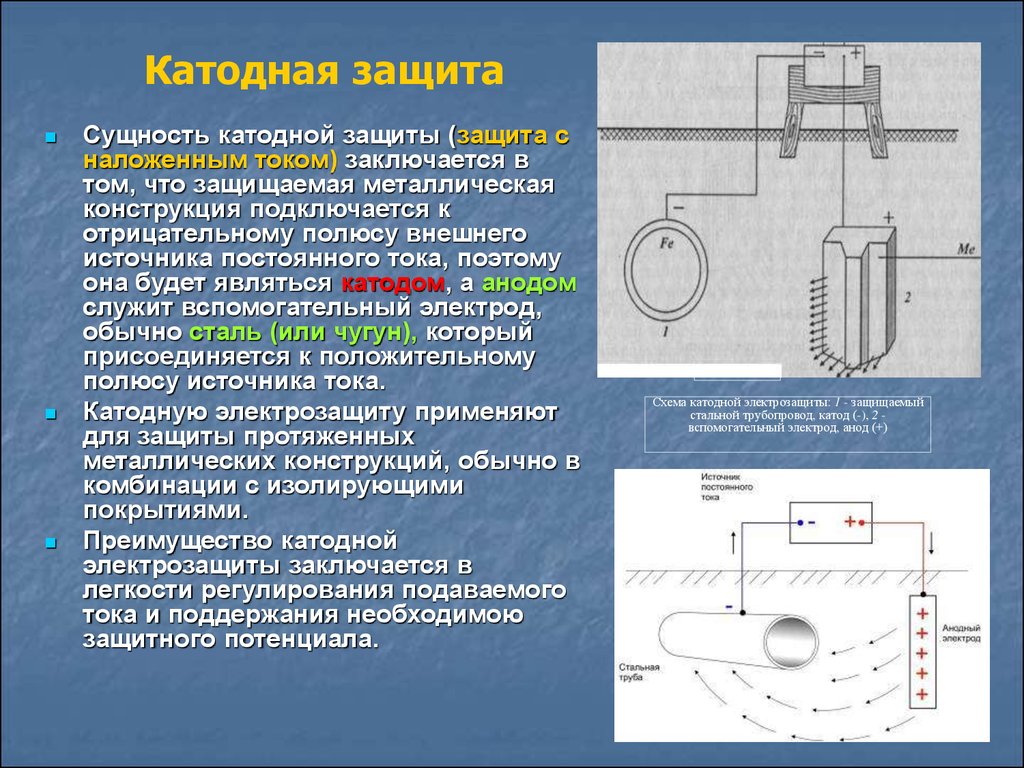 можно смело применять.
можно смело применять.
Эта предварительная работа должна включать металлографическое исследование, так как существуют различные типы коррозии, такие как межкристаллитная коррозия и селективная коррозия, которые могут ограничить использование сплавов меньшим диапазоном потенциала, чем можно было бы предположить (5).
Наибольшую опасность, однако, представляет форма кривой, изображенной на рис. 2. На ней видно, что при потенциалах чуть ниже тех, при которых устанавливается защита, скорость коррозии очень высока. В некоторых случаях эта скорость может быть на много порядков выше, чем у пассивного металла. Если бы сосуд стал активным, для восстановления пассивности защитное устройство должно было бы обеспечить ток, эквивалентный максимально возможной скорости коррозии. Это означает, что потенциостат должен быть в состоянии обеспечить ток на много порядков выше необходимого для защиты, и если он не может, он может потерять управление. По этой причине мониторинг считается целесообразным.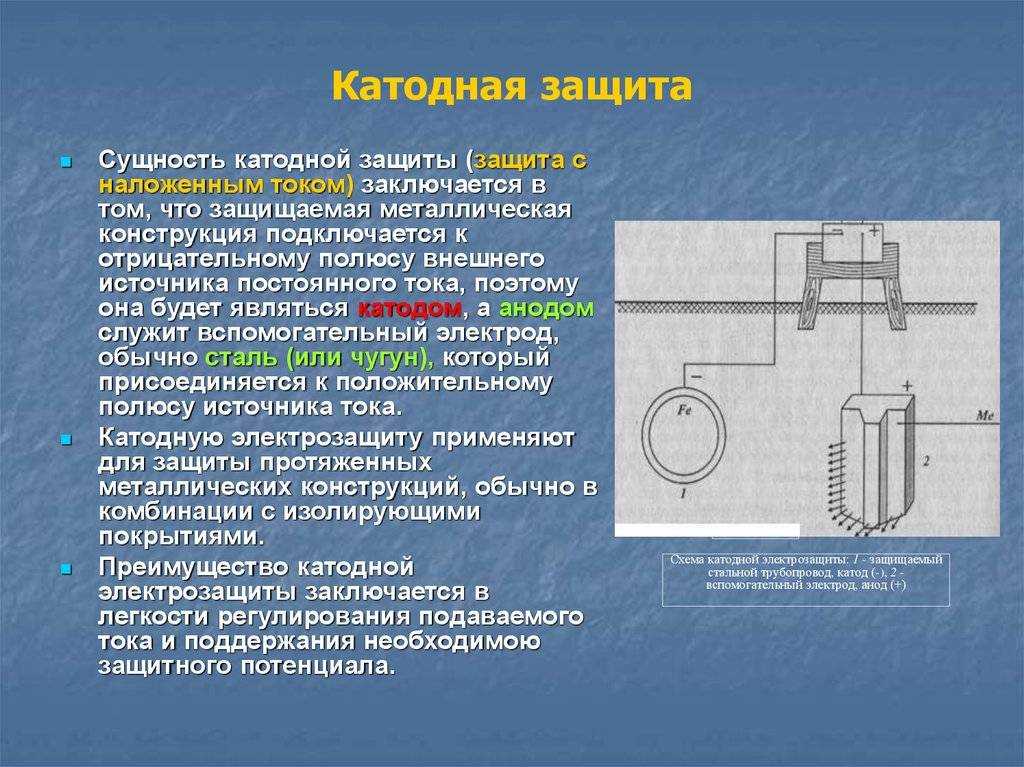 Эта опасность может быть одной из причин, по которой метод до сих пор не нашел широкой поддержки. Как бы серьезно это ни было, это, безусловно, было преувеличено, возможно, потому, что в попытке продемонстрировать впечатляющие возможности метода решение, использованное в первых экспериментах на пилотной установке, было одним из самых сложных в обращении (6). В этом случае доступный потенциостат был совершенно неадекватным для этой цели (он был сконструирован для лабораторных исследований на небольших образцах) и мог обеспечить ток, достаточно большой для защиты, но его было мало, чтобы учесть даже небольшие локальные аварии. Тем не менее установка успешно проработала многие сотни часов. Более поздняя американская работа (7, 8, 9) показал, что риск не слишком велик, и с помощью подходящего инструмента можно полностью преодолеть эту трудность.
Эта опасность может быть одной из причин, по которой метод до сих пор не нашел широкой поддержки. Как бы серьезно это ни было, это, безусловно, было преувеличено, возможно, потому, что в попытке продемонстрировать впечатляющие возможности метода решение, использованное в первых экспериментах на пилотной установке, было одним из самых сложных в обращении (6). В этом случае доступный потенциостат был совершенно неадекватным для этой цели (он был сконструирован для лабораторных исследований на небольших образцах) и мог обеспечить ток, достаточно большой для защиты, но его было мало, чтобы учесть даже небольшие локальные аварии. Тем не менее установка успешно проработала многие сотни часов. Более поздняя американская работа (7, 8, 9) показал, что риск не слишком велик, и с помощью подходящего инструмента можно полностью преодолеть эту трудность.
Невозможно перечислить все ограничения метода, но стоит только отметить, что не все металлы показывают достаточный диапазон пассивности и что при любом данном металле пассивность не будет стабильной во всех растворах. Этот метод зависит от электролитического тока, поступающего на металл, поэтому он неприменим выше линии промывки в сосуде или в подобных местах.
Этот метод зависит от электролитического тока, поступающего на металл, поэтому он неприменим выше линии промывки в сосуде или в подобных местах.
Применение анодной защиты
Хотя в технической прессе (9, 10) было несколько сообщений об использовании анодной защиты, а также было проведено несколько других испытаний, метод до сих пор почти не применялся на практике.
С точки зрения защиты от коррозии все химические установки, как правило, сильно перепроектированы, поскольку они подобны печи без регулятора температуры или самописца. Таким образом, возможности использования защиты и/или мониторинга огромны. Например, на заводе по производству нержавеющей стали обычно поддерживают концентрацию кислоты, температуру, давление или другие подобные переменные ниже значений, вызывающих проблемы. Поскольку, как правило, нет средств сказать, насколько близка установка к потере пассивности, материалы не используются на пределе своих возможностей. Другой способ сказать вышесказанное состоит в том, что для химических заводов обычно выбирают излишне дорогие сорта материалов, чтобы обеспечить некоторую степень безопасности.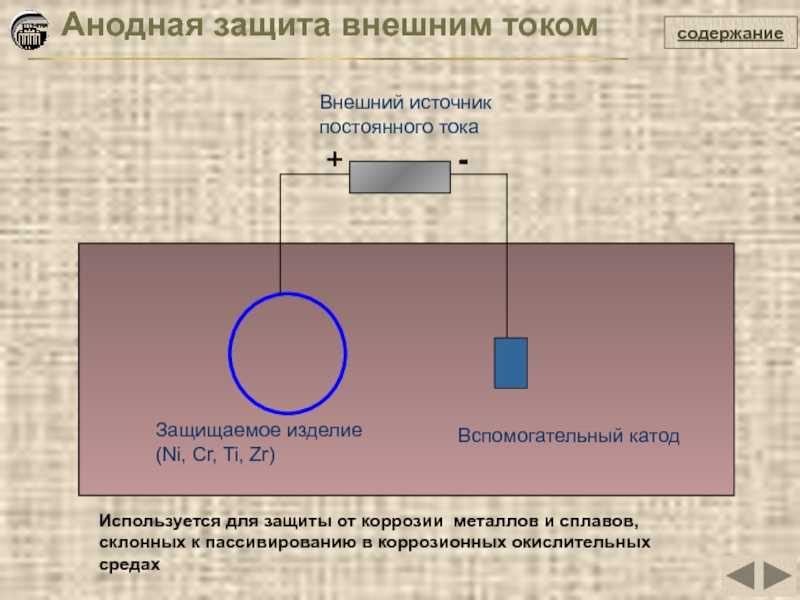
Кажется, можно провести различие между двумя видами использования анодной защиты. В первую очередь должна быть возможность использовать его, чтобы позволить использовать существующие установки и материалы на пределе их возможностей, с анодной защитой и/или мониторингом только в качестве предохранительного устройства. Однако при наличии мужества кажется, что нет никаких причин, по которым установка не должна быть специально спроектирована из материалов низкого качества, выживание которых полностью зависело бы от анодной защиты. В этом случае, конечно, система анодной защиты должна быть дорогой, но экономика может оказаться привлекательной, если бы была существенная экономия на строительных материалах или если бы завод мог работать в условиях, намного превосходящих все, что могло бы быть. визуализируется без защиты.
Конструкция установки и электрода
По-видимому, необходимо учитывать только одну особенность конструкции установки. Электролитический ток должен поступать на установку для защиты. Необходимый ток, как правило, ниже 10 мкА/см 2 , и относительно легко рассчитать, как далеко он «бросит», если известна проводимость раствора и установлен доступный диапазон напряжения. На практике обнаруживается, что сила броска огромна, как это было продемонстрировано недавними американскими работами (9).), а достаточно длинные трубы можно легко защитить, если решение является хорошим проводником. Естественно, что справиться со случайной поломкой на конце трубы несколько сложнее, чем внутри сосуда, но оценить связанные с этим риски относительно легко.
Необходимый ток, как правило, ниже 10 мкА/см 2 , и относительно легко рассчитать, как далеко он «бросит», если известна проводимость раствора и установлен доступный диапазон напряжения. На практике обнаруживается, что сила броска огромна, как это было продемонстрировано недавними американскими работами (9).), а достаточно длинные трубы можно легко защитить, если решение является хорошим проводником. Естественно, что справиться со случайной поломкой на конце трубы несколько сложнее, чем внутри сосуда, но оценить связанные с этим риски относительно легко.
Невозможно защитить выше линии промывки в сосуде, где коррозия может быть вызвана распылением. Некоторые детали клапанов и насосов также сложны, но нет никаких причин, по которым материалы, обладающие естественной устойчивостью, не следует использовать в опасных местах в сочетании с менее качественными материалами в других местах. При правильно подобранных материалах не должно быть осложнений, связанных с блуждающими токами.
Что касается электродов, то стандарт, если он используется, может быть подобен стандарту, который будет использоваться для измерения pH в той же среде. Принимая во внимание, однако, что точность, требуемая от стандарта для этого приложения, невелика, вместо этого можно использовать очень простые и надежные стандарты. Например, платиновая проволока, реагирующая на естественный окислительно-восстановительный потенциал раствора, была бы адекватной, если бы она была достаточно стабильной.
Что касается катода, то здесь опять-таки значительная широта, но стоит помнить об одном моменте. Если используется потенциостатическая система, могут быть короткие периоды, когда полярность тока меняется на противоположную, так что катод становится анодом. По этой причине, если этот электрод сделан, скажем, из меди или никеля, в надежде, что он будет защищен катодно, он вполне может исчезнуть во время этих перемен полярности, и по этой причине считается, что благородные металлы более удобны. . Платина является естественным выбором из-за ее хорошей электропроводности, низкого водородного перенапряжения, хорошей герметизации стекла и не в последнюю очередь простоты очистки от отложений, которые образуются в результате прохождения тока.
. Платина является естественным выбором из-за ее хорошей электропроводности, низкого водородного перенапряжения, хорошей герметизации стекла и не в последнюю очередь простоты очистки от отложений, которые образуются в результате прохождения тока.
Резюме и выводы
С точки зрения защиты от коррозии анодная защита для химического завода является тем же, чем регулятор температуры для печи. Без анодной защиты химическая установка должна быть перепроектирована, и материалы не могут быть использованы наилучшим образом.
Метод почти не применялся на практике, хотя и прост в применении. Вероятно, это отчасти связано с неадекватным пониманием того, как работает метод, и с ощущением, что это лабораторный курьез. На самом деле в защите анодным током нет ничего более странного, чем в защите общепризнанными окислителями типа хроматов.
Конечно, существуют опасности и ограничения, но при соответствующей лабораторной работе и подходящем оборудовании они не составляют серьезного возражения против метода.
Каталожные номера
- 1
M. Pourbaix Термодинамика разбавленных водных растворов, Арнольд, Лондон, 1949
- 2
с. Чихал и м. Празак
J. Iron & Steel Inst., 1959,
193 , 360 К.Эделяну
Дж. Металлургический институт, 1958 г.,
188 , 122- 3
Дж. Б. Хлопок
Хим. и Ind., , 1958, с. 68; 1958, с. 492 - 4
К. Эделяну
Технология коррозии, 1955 г.,
2 , 204 - 5
К. Эделяну
J. Iron & Steel Inst., 1957,
185 , 482 - 6
К. Эделяну
Металлургия, 1954 г.,
50 , 113 - 7
Дж. Д. Садбери, О. Л. Риггс и Д. А. Шок
Коррозия, 1960 г.,
16 , 91 - 8
Д. А. Шок, О. Л. Риггс и Дж. Д.

