Анодная и катодная защита от коррозии: Электрохимическая защита
Содержание
5.4 Катодная защита.
Катодная защита
конструкций от коррозии применяется
преимущественно в условиях следующих
агрессивных сред: морской и жесткой
речной воды, почвы и т.д. Эта защита
основана на использовании основных
законов процесса электролиза.
Суть катодной
защиты заключается в том, что защищаемую
деталь присоединяют к отрицательному
полюсу источника постоянного тока.
Анодом служит обычный электрод из
железа, установленный на определенном
расстоянии от объекта (Рис.8). Такие
железные бруски применяются в качестве
анодов для береговых сооружений. Такое
решение приводит к загрязнению водной
среды окислами Fе, а поэтому
оно не всегда может применяться (анод
лучше не растворимый). Анода расходуют
до 9кг в год и поэтому его
периодически заменяют. Из-за
неравномерности распределения тока на
поверхности защищаемого сооружения
величина защитного тока превышает
расчетную.
Рис.8 Катодная
защита для берегового сооружения
Нужно следить,
чтобы не произошла «перезащита
металла» это приводит к интенсивному
выделению водорода. Она очень опасна
Она очень опасна
для Zn, РЬ, А1,Sn,
т.к. произойдет подщелачивание прикатодного
участка:
О2+2Н2О+4е4ОН
эти металлы в
щелочной среде разрушаются.
Катодная защита,
по-видимому, наиболее важный метод
борьбы с коррозией. С ее помощью коррозию
фактически сводят к нулю, и поверхность
Ме не подвергается разрушению при
выдержке в агрессивной среде в течение
неограниченного времени. Электрохимическая
защита применяется для борьбы с коррозией
таких металлов как сталь, Сu,
Рb, А1, латунь во всех видах грунтовых и
особенно в водных средах. Она может
эффективно использоваться для
предотвращения коррозионного
растрескивания, коррозионной усталости
(но не просто усталости) межкристаллитной
коррозии.
Элементы системы
катодной защиты:
3
Рис.9: катодная
защита на судах
1. электрод
сравнения
2. щит управления
системы катодной защиты
3. анодный экран
анодный экран
4. аноды
Конструкция
делается катодом (корпус), а в
электропроводную среду (морскую воду)
помещается анод и подключается источник
тока. Источник питания(1) служит для
преобразования энергии судовой (или
береговой) сети переменного тока
напряжением 220 или 380В в постоянный ток
с напряжением 12-24В-такое напряжение
обычно используется в системах катодной
защиты.
В отечественном
судостроении в качестве источников
питания в настоящее время применяются
полупроводниковые выпрямители типа
ПАК (преобразователь автоматический
катодный). Электроды сравнения служат
для измерения потенциала подводной
части корпуса судна или любой защищаемой
конструкции.
В практике
электрохимической защиты морских судов
от коррозии наиболее широкое применение
получили хлорсеребряные электроды
сравнения.
Аноды в системах
катодной защиты служат для обеспечения
стекания защитного тока в морскую воду.
Стационарные аноды устанавливаются на
наружной обшивке корпуса судна. В
береговых системах применяются подвесные
аноды.
Для катодной защиты
корпуса корабля применение растворимых
анодов не эффективно, т.к. процесс их
замены громоздкая и дорогая операция.
Поэтому в судостроении применяются
нерастворимые аноды.
В настоящее время
наиболее распространены Рt-
аноды для
систем катодной
защиты судов. Однако дороговизна платины
заставляет искать способы, возможности
ее экономии. Она применяется в виде
тонкого покрытия на подложке из
пассивирующих металлов — Тi, Та, Nb.
Нанесение тонких
слоев Рtосуществляется
способами: гальваническим осаждением,
напылением расплавленного металла и
приваркой платиновой фольги. Рtи платинированный Тi могут применяться
в широком интервале плотностей тока до
5000 а/м2. Расход Рtпри этой
плотности тока составляет 6 мг/м.кв.
Ориентировочный срок службы анодов из
Рt и платинированного Тi -15-20 лет. Околоанодные
Околоанодные
экраны применяются с целью обеспечения
более равномерного распределения тока
по защищаемой поверхности корпуса (т.е.
чтобы электрическое поле анода не влияло
на распределение тока), а также с целью
защиты лакокрасочного покрытия вблизи
анодов от разрушения кислородом, хлором,
кислотами (НС1, НСlO).
Материалы
околоанодных экранов должны обладать
достаточной химической стойкостью,
механической прочностью и диэлектрическими
свойствами. Материалы околоанодных
экранов используются стеклопластики
холодного отверждения на эпоксидной
смоле. Они наформовываются непосредственно
на обшивку судна и в этом случае
обеспечивается плотное прилегание
экрана к обшивке при любом радиусе
кривизны.
Катодная защита
имеет преимущества:
возможность
применения к объекту, где уже есть очаги
коррозии;длительный срок
службы;снижается обрастание
корпуса судна.
Недостатки: наличие
дополнительного персонала.
ГОСТы, СНиПы Карта сайта TehTab.ru Поиск по сайту TehTab.ru | Навигация по справочнику TehTab.ru: главная страница / / Техническая информация/ / Химический справочник / / Электрохимическая коррозия металла. Катодная защита. Анодная защита. Пассивная защита. Электродные потенциалы — таблица.
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Нашли ошибку? Есть дополнения? Напишите нам об этом, указав ссылку на страницу. | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
TehTab.ru Реклама, сотрудничество: [email protected] | Обращаем ваше внимание на то, что данный интернет-сайт носит исключительно информационный характер. Информация, представленная на сайте, не является официальной и предоставлена только в целях ознакомления. Все риски за использование информаци с сайта посетители берут на себя. Проект TehTab.ru является некоммерческим, не поддерживается никакими политическими партиями и иностранными организациями. | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Разница между анодной и катодной защитой
Основное различие между анодной и катодной защитой заключается в том, что при анодной защите защищаемая поверхность действует как анод, тогда как при катодной защите защищаемая поверхность действует как катод .
Анодная и катодная защита — это два электрохимических процесса, которые мы используем для предотвращения коррозии или ржавления поверхностей. В электрохимическом процессе мы используем электрохимическую ячейку с двумя электродами в качестве анода и катода. В процессах анодной и катодной защиты мы используем защищаемую поверхность (подложку) в качестве анода или катода, что приводит к названию этих процессов как таковым. Протекторная защита — это тип катодной защиты, при котором мы используем металл в качестве расходуемого анода. В этом процессе этот жертвенный металл подвергается коррозии, избегая коррозии катода.
СОДЕРЖАНИЕ
1. Обзор и основные отличия
2. Что такое анодная защита
3. Что такое катодная защита
4. Прямые сравнения – анодная и катодная защита в табличной форме
5. Резюме
Что такое анодная защита ?
Анодная защита — это тип электрохимического процесса, при котором мы можем защитить металлическую поверхность, сделав ее анодом в электрохимической ячейке. Мы можем обозначить это как AP. Однако этот метод возможен только для комбинаций материала и среды, которые показывают довольно широкие пассивные области. то есть сталь и нержавеющая сталь в 98% серная кислота.
Мы можем обозначить это как AP. Однако этот метод возможен только для комбинаций материала и среды, которые показывают довольно широкие пассивные области. то есть сталь и нержавеющая сталь в 98% серная кислота.
В АП нам нужно довести металл до высокого потенциала. Затем металл становится пассивным за счет образования защитного слоя. Однако AP не используется широко в качестве катодной защиты, поскольку он ограничен металлами, имеющими на поверхности достаточно надежный пассивный слой; например, нержавеющая сталь.
При применении AP необходимо учитывать два основных момента. Во-первых, нам нужно убедиться, что вся система находится в пассивном диапазоне. Во-вторых, нам необходимо иметь точное представление об ионах, что может привести к обширной точечной коррозии.
Что такое катодная защита?
Катодная защита — это тип электрохимического процесса, при котором мы можем защитить металлическую поверхность, сделав ее катодом в электрохимической ячейке. Мы можем обозначить его как CP. CP может предотвратить коррозию металлических поверхностей. Существуют различные типы CP; например, гальваническая защита или протекторная защита, системы импульсного тока и гибридные системы.
CP может предотвратить коррозию металлических поверхностей. Существуют различные типы CP; например, гальваническая защита или протекторная защита, системы импульсного тока и гибридные системы.
Рисунок 01: Системы подаваемого тока
В этом методе корродирует жертвенный металл, а не защищаемый. Если мы используем катодную защиту для больших конструкций, таких как длинные трубопроводы, метода гальванической защиты недостаточно. Следовательно, нам необходимо обеспечить достаточный ток, используя внешний источник питания постоянного тока.
Рисунок 02: Жертвенный анод – слой цинка
Кроме того, мы можем использовать эту технику для защиты топливных или водопроводных трубопроводов, изготовленных из стали, резервуаров для хранения, корпусов кораблей и лодок, оцинкованной стали и т. д.
Что такое Разница между анодной и катодной защитой?
Анодная защита — это тип электрохимического процесса, в котором мы можем защитить металлическую поверхность, сделав ее анодом в электрохимической ячейке, а катодная защита — это тип электрохимического процесса, в котором мы можем защитить металлическую поверхность, сделав ее катодом. в электрохимической ячейке. Таким образом, ключевое различие между анодной и катодной защитой заключается в том, что при анодной защите защищаемая поверхность действует как анод, тогда как при катодной защите она является катодом.
в электрохимической ячейке. Таким образом, ключевое различие между анодной и катодной защитой заключается в том, что при анодной защите защищаемая поверхность действует как анод, тогда как при катодной защите она является катодом.
Кроме того, анодная защита включает подавление реакционной способности металла путем регулирования потенциала более реакционноспособного металла; однако катодная защита включает изменение направления тока между двумя разнородными электродами. Следовательно, мы можем рассматривать и это как разницу между анодной и катодной защитой.
Резюме – Анодная и катодная защита
Анодная защита – это тип электрохимического процесса, в котором мы можем защитить металлическую поверхность, сделав ее анодом в электрохимической ячейке, а катодная защита – это тип электрохимического процесса, в котором мы может защитить металлическую поверхность, сделав ее катодом в электрохимической ячейке. Основное различие между анодной и катодной защитой заключается в том, что при анодной защите защищаемая поверхность действует как анод, тогда как при катодной защите она является катодом.
Ссылка:
1. «Что такое жертвенная защита? — Определение из Corrosionpedia». Corrosionpedia, доступно здесь.
Изображение предоставлено:
1. «Диаграмма катодной защиты» Кафе Нервоза — собственная работа (CC BY-SA 3.0) через Commons Wikimedia
2. «Жертвенный анод» Цвергельстерн (CC BY-SA 3.0) через Commons Wikimedia
Что такое расходуемая анодная катодная защита (SACP)?
Что означает протекторная катодная защита анода (SACP)?
Катодная защита расходуемого анода (SACP) представляет собой тип катодной защиты, при котором менее благородный материал, действующий в качестве расходуемого анода, соединяется металлическими проводниками с защищаемой конструкцией. Материалами, используемыми для этой цели, являются магний, алюминий и цинк. Они обеспечивают электроны защищаемой структуре и расходуются.
Обычно SACP используется для защиты участков с хорошим покрытием, где требования к защитному току и удельное сопротивление почвы или воды низкое. Он также используется там, где площадь поверхности защищаемой конструкции относительно невелика.
Он также используется там, где площадь поверхности защищаемой конструкции относительно невелика.
Нажмите здесь, чтобы спроектировать кольцевую анодную систему резервуара!
Реклама
Corrosionpedia Объясняет катодную защиту расходуемого анода (SACP)
Расходуемые аноды представляют собой высокоактивные металлы, которые используются для предотвращения коррозии поверхности менее активного материала. В применении SACP для обеспечения защиты используются естественные электрохимические потенциалы различных металлов. Жертвенные аноды соединены с защищаемой конструкцией, и обычный ток течет от анода к конструкции до тех пор, пока анод более «активен», чем конструкция. При протекании тока вся коррозия происходит на аноде, который «жертвует» собой, чтобы обеспечить защиту конструкции от коррозии.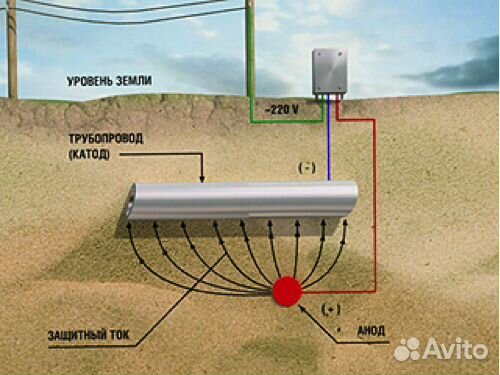
Особенности и преимущества SACP:
- Не требуется независимый источник электроэнергии
- Ограниченное воздействие на соседние конструкции
- Анодные соединения также защищены
- Правильный выбор материала обеспечивает отсутствие чрезмерной защиты, что позволяет избежать охрупчивания металла и повреждения покрытия
- Отсутствие возможности повреждения оборудования из-за неправильного подключения
- Простота установки, эксплуатации и обслуживания
Существует два типа катодной защиты на основе подачи электронов в конструкцию:
- Катодная защита расходуемого анода (SACP) — Менее благородный материал действует как расходуемый анод.
- Катодная защита от импульсного тока (ICCP) — используется внешний источник тока и выпрямитель.
Основное различие между ними заключается в том, что ICCP использует внешний источник питания с инертными анодами, а SACP использует естественную разность электрохимических потенциалов между различными металлическими элементами для обеспечения защиты.

 На практике, наибольший вред приносит т.н. электрохимическая коррозия, сопровождающаяся активным переносом вещества. Металлические поверхности подвержены электрохимическому разрушению (коррозии) при вступлении в контакт с электролитами ( агентами коррозии). Таковыми агентами могут служить атмосферные газы, такие как морской, городской или промышленный воздух ( т.е. диоксид серы, хлорид и сульфит водорода и т.д.) или активные жидкости – рассолы, щелочи, морская вода и т.д. (например –отпечатки потных рук).
На практике, наибольший вред приносит т.н. электрохимическая коррозия, сопровождающаяся активным переносом вещества. Металлические поверхности подвержены электрохимическому разрушению (коррозии) при вступлении в контакт с электролитами ( агентами коррозии). Таковыми агентами могут служить атмосферные газы, такие как морской, городской или промышленный воздух ( т.е. диоксид серы, хлорид и сульфит водорода и т.д.) или активные жидкости – рассолы, щелочи, морская вода и т.д. (например –отпечатки потных рук).
 Если на защищаемый объект подать некий дополнительный положительный потенциал = поддержать на нем некий отрицательный потенциал порядка десятой доли вольта, то вероятность окислительной реакции падает почти до нуля. Данный способ защиты подразумевается обычно, когда говорят о катодной защите.
Если на защищаемый объект подать некий дополнительный положительный потенциал = поддержать на нем некий отрицательный потенциал порядка десятой доли вольта, то вероятность окислительной реакции падает почти до нуля. Данный способ защиты подразумевается обычно, когда говорят о катодной защите.
 д.
д.
 68
68 14
14 50
50