Дать характеристику меди: Характеристика переходных элементов (меди, цинка, хрома, железа) по их положению в периодической системе химических элементов Д.И. Менделеева и особенностям строения их атомов / Справочник :: Бингоскул
Содержание
Переходные металлы — комплексы, строение переходных металлов, переходные металлы, галогениды переходных металлов
Переходные металлы, Переходные металлы. переходные металлы — простые и сложные комплексы переходных металлов. Переходные металлы (переходные элеме́нты) — элементы побочных подгрупп Периодической системы химических элементов Д. И. Менделеева, в атомах которых появляются электроны на d- и f-орбиталях. В общем виде электронное строение переходных элементов можно представить следующим образом: . На ns-орбитали содержится один или два электрона, остальные валентные электроны находятся на -орбитали. Поскольку число валентных электронов заметно меньше числа орбиталей, то простые вещества, образованные переходными элементами, являются металлами.
Общая характеристика переходных элементов. Все переходные элементы имеют следующие общие свойства:
Небольшие значения электроотрицательности.
Переменные степени окисления. Почти для всех d-элементов, в атомах которых на внешнем ns-подуровне находятся 2 валентных электрона, известна степень окисления +2.
Начиная с d-элементов III группы Периодической системы химических элементов Д. И. Менделеева, элементы в низшей степени окисления образуют соединения, которые проявляют основные свойства, в высшей — кислотные, в промежуточной — амфотерные. Например:
Для всех переходных элементов характерно образование комплексных соединений.
Подгруппа меди. Подгруппа меди, или побочная подгруппа I группы Периодической системы химических элементов Д. И. Менделеева, включает в себя элементы: медь Cu, серебро Ag и золото Au.
Для всех металлов характерны высокие значения плотности, температур плавления и кипения, высокая тепло- и электропроводность. [8]
Особенностью элементов подгруппы меди является наличие заполненного предвнешнего -подуровня, достигаемое за счёт перескока электрона с ns-подуровня. Причина такого явления заключается в высокой устойчивости полностью заполненного d-подуровня. Эта особенность обусловливает химическую инертность простых веществ, их химическую неактивность, поэтому золото и серебро называют благородными металлами. [9]
[9]
Медь, Медные группы. Медь представляет собой довольно мягкий металл красно-жёлтого цвета. В электрохимическом ряду напряжений металлов она стоит правее водорода, поэтому растворяется только в кислотах-окислителях (в азотной кислоте любой концентрации и в концентрированной серной кислоте):
таб?
В отличие от серебра и золота, медь окисляется с поверхности кислородом воздуха уже при комнатной температуре. В присутствии углекислого газа и паров воды её поверхность покрывается зелёным налётом, представляющим собой основной карбонат меди (II).
Для меди наиболее характерна степень окисления +2, однако существует целый ряд соединений, в которых она проявляет степень окисления +1.
Платиновые металлы
Основная статья: Металлы платиновой группы
Платиновые металлы — семейство из 6 химических элементов побочной подгруппы VIII группы Периодической системы, включающее рутений Ru, родий Rh, палладий Pd, осмий Os, иридий Ir и платину Pt. Эти металлы подразделяются на две триады: лёгкие — триада палладия (Ru, Rh, Pd) и тяжёлые — триада платины (Os, Ir, Pt).
Эти металлы подразделяются на две триады: лёгкие — триада палладия (Ru, Rh, Pd) и тяжёлые — триада платины (Os, Ir, Pt).
Нас находят по запросам:
— переходные металлы
— комплексы переходных металлов
— строение переходные металлы
— простые и переходные металлы
— галогениды переходных металлов
— нитриды переходных металлов
— комплексы переходных металлов
— сплав переходных металлов
— расчёт комплексов переходных металлов
— водорастворимые полимеры переходные металлы
— свойства комплексов переходных металлов
— структура переходных металлов
Минеральные вещества | Tervisliku toitumise informatsioon
В человеческом организме установлено наличие более 70 химических элементов. Достоверно установлена потребность в более чем 20 биоэлементах. Для обеспечения достаточного количества этих элементов крайне важно, чтобы питание было разнообразным.
Встречающиеся в организме минеральные вещества можно условно разделить на две группы:
- Содержание макроэлементов в организме составляет более 0,01%.
 Ими являются фосфор (P), кальций (Ca), натрий (Na), калий (K), магний (Mg), сера (S), хлор (Cl) (см Таблица 1).
Ими являются фосфор (P), кальций (Ca), натрий (Na), калий (K), магний (Mg), сера (S), хлор (Cl) (см Таблица 1). - Содержание микроэлементов – менее 0,01%, у некоторых даже 0,00001.
Потребность в некоторых микроэлементах установлена, это железо (Fe), цинк (Zn), медь (Cu), йод (I), селен (Se) , марганец (Mn), молибден (Mo), фтор (F), хром (Cr), кобальт (Co), кремний (Si), ванадий (V), бор (B), никель (Ni), мышьяк (As) и олово (Sn).
Помимо них в организме обнаружен целый ряд элементов, функция которых пока не ясна, их появление в организме может быть обусловлено загрязнением окружающей среды и частым соприкосновением с ними. Например, люди, работающие в теплицах, постоянно контактируют с химическими веществами, различные элементы могут быть признаком разного рода заболеваний. В числе таких элементов алюминий (Al), стронций (Sr), барий (Ba), рубидий (Rb), палладий (Pd), бром (Br).
В организм могут попадать и тяжелые, т.е. ядовитые металлы, такие как кадмий (Cd), ртуть (Hg) или свинец (Pb).
Минеральные вещества в нашем организме являются важными компонентами скелета, биологических жидкостей и энзимов и способствуют передаче нервных импульсов.
Люди и животные получают различные биологические элементы из пищи, воды и окружающего воздуха, самостоятельно синтезировать минеральные вещества живые организмы не могут. В растениях минеральные вещества накапливаются из почвы, и их количество зависит от места произрастания и наличия удобрений. В питьевой воде также имеются минеральные вещества, и их содержание зависит от места, откуда получают воду.
Несмотря на то, что человек нуждается в небольших количествах минеральных веществ (макроэлементов в миллиграммах и граммах, микроэлементов – в милли- и микрограммах), в его организме, тем не менее, отсутствуют достаточные запасы минеральных веществ, чтобы нормально перенести их долговременный дефицит. Потребность в минеральных веществах зависит также от возраста, пола и прочих обстоятельств (см Таблица 2). Например, повышенная потребность в железе у женщин связана с менструациями и беременностью, а спортсменам требуется больше натрия, потому что он интенсивно выводится с потом.
Например, повышенная потребность в железе у женщин связана с менструациями и беременностью, а спортсменам требуется больше натрия, потому что он интенсивно выводится с потом.
Чрезмерные количества минеральных веществ могут привести к сбоям в работе организма, потому что, будучи компонентами биоактивных соединений, они оказывают влияние на регуляторные функции. Получать чрезмерные количества минеральных веществ (за исключением натрия) с пищей практически невозможно, однако это может произойти при чрезмерном употреблении биологически активных добавок и обогащенных минеральными веществами продуктов.
Усвоению минеральных веществ могут препятствовать:
- злоупотребление кофе,
- употребление алкоголя,
- курение,
- некоторые лекарства,
- некоторые противозачаточные таблетки,
- определенные вещества, встречающиеся в некоторых продуктах, например, в ревене и шпинате.
Потери минеральных веществ при тепловой обработке продуктов питания значительно меньше, чем потери витаминов.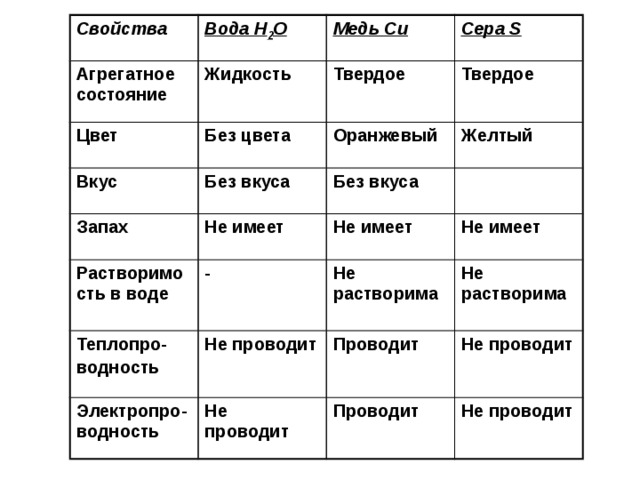 Однако при рафинировании или очистке часть минеральных веществ удаляется. Поэтому важно есть больше цельнозерновых и нерафинированных продуктов. Минеральные вещества могут образовывать соединения с другими веществами, содержащимися в продуктах питания (например, с оксалатами в ревене), в результате чего организм не может их усвоить.
Однако при рафинировании или очистке часть минеральных веществ удаляется. Поэтому важно есть больше цельнозерновых и нерафинированных продуктов. Минеральные вещества могут образовывать соединения с другими веществами, содержащимися в продуктах питания (например, с оксалатами в ревене), в результате чего организм не может их усвоить.
Таблица 1
Названия и источники важнейших минеральных веществ
Обозначение | Название | Лучшие источники * |
Макроэлементы | ||
Na | натрий | поваренная соль (NaCl), готовая еда, сыр, ржаной хлеб, консервы, мясные продукты, оливки, картофельные чипсы |
K | калий | растительные продукты: сушеные фрукты и ягоды, орехи, семена, топинамбур, картофель, редис, капуста, зеленые овощи, мука «Кама», свёкла, банан, ржаной хлеб, смородина, томаты |
Ca | кальций | молоко и молочные продукты (особенно сыр), миндаль, орехи, семена, рыба (с костями), шпинат |
Mg | магний | орехи, семена, мука «Кама», ржаной хлеб, шпинат, бобовые, греча, цельнозерновые продукты, свинина, говядина и курятина, банан, брокколи |
P | фосфор | семена, орехи, молочные продукты (особенно сыр), печень, птица, говядина, ржаной хлеб, рыба, цельнозерновые продукты, бобовые |
S | сера | продукты с белками, содержащими аминокислоты метионин (зерновые, орехи) и цистеин (мясо, рыба, соевые бобы, зерновые) |
Cl | хлор | поваренная соль |
Микроэлементы | ||
Fe | железо | печень, кровяная колбаса, семечки, яйца, изюм, ржаной хлеб, нежирная говядина и свинина, цельнозерновые продукты, греча, клубника |
Zn | цинк | печень, мясо, мука «Кама», семена, орехи, сыр, ржаной хлеб, бобовые, дары моря (крабы, салака), цельнозерновые продукты, яйца |
Cu | медь | печень, какао-порошок, мясо, бобовые, цельнозерновые продукты, семена, орехи, греча, ржаной хлеб, лосось, авокадо, свёкла, дары моря |
I | йод | йодированная соль, рыба и другие дары моря, сыр, яйца, некоторые виды ржаного хлеба и йогурта |
Se | селен | арахис, печень, рыба и дары моря, семена подсолнечника, мясо |
* Количество, содержащееся в 100 г продукта, покрывает не менее 10% суточной потребности взрослой женщины
Таблица 2
Рекомендуемые в зависимости от возраста суточные нормы потребления важнейших минеральных веществ
Возраст | Натрий, мг | Кальций, мг | Калий, г | Магний, мг | Железо, мг | Цинк, мг | Медь, мг | Йод, мкг | Селен, мкг |
Дети |
|
|
|
|
|
|
|
|
|
6–11 месяцев | до 650 | 550 | 1,1 | 80 | 8 | 5 | 0,3 | 60 | 15 |
12–23 месяца | до 830 | 600 | 1,4 | 85 | 8 | 6 | 0,3 | 90 | 25 |
2–5 лет | до 1580 | 600 | 1,8 | 120 | 8 | 6 | 0,4 | 90 | 30 |
6–9 лет | до 1580 | 700 | 2 | 200 | 9 | 7 | 0,5 | 120 | 30 |
Женщины |
|
|
|
|
|
|
|
|
|
10–13 лет | до 2400 | 900 | 2,9 | 300 | 11 | 8 | 0,7 | 150 | 40 |
14–17 лет | до 2400 | 900 | 3,1 | 320 | 15 | 9 | 0,9 | 150 | 50 |
18–30 лет | до 2400 | 900 | 3,1 | 320 | 15 | 9 | 0,9 | 150 | 50 |
31–60 лет | до 2400 | 800 | 3,1 | 320 | 15 | 9 | 0,9 | 150 | 50 |
61–74 лет | до 2400 | 800 | 3,1 | 320 | 10 | 9 | 0,9 | 150 | 50 |
> 75 лет | до 2400 | 800 | 3,1 | 320 | 10 | 9 | 0,9 | 150 | 50 |
Беременные | до 2400 | 900 | 3,1 | 360 | 15 | 10 | 1 | 175 | 60 |
Кормящие матери | до 2400 | 900 | 3,1 | 360 | 15 | 11 | 1,3 | 200 | 60 |
Мужчины |
|
|
|
|
|
|
|
|
|
10–13 лет | до 2400 | 900 | 3,3 | 300 | 11 | 11 | 0,7 | 150 | 40 |
14–17 лет | до 2400 | 900 | 3,5 | 380 | 11 | 12 | 0,9 | 150 | 60 |
18–30 лет | до 2400 | 900 | 3,5 | 380 | 10 | 9 | 0,9 | 150 | 60 |
31–60 лет | до 2400 | 800 | 3,5 | 380 | 10 | 9 | 0,9 | 150 | 60 |
61–74 лет | до 2400 | 800 | 3,5 | 380 | 10 | 10 | 0,9 | 150 | 60 |
> 75 лет | до 2400 | 800 | 3,5 | 380 | 10 | 10 | 0,9 | 150 | 60 |
* Для 18–20-летних рекомендуемая суточная доза составляет 900 мг кальция и 700 мг фосфора.
** Потребность в железе зависит от потери железа при менструациях. Для женщин в постменопаузе рекомендуемая дневная доза железа составляет 10 мг.
*** Для достижения сбалансированного содержания железа во время беременности в организме женщины должны иметься запасы железа как минимум на 500 мг больше, чем до беременности. В двух последних триместрах беременности, в зависимости от уровня железа в организме, может потребоваться дополнительный прием железа.
**** На самом деле, селена можно потреблять больше указанной в таблице рекомендованной дозы, поскольку селен по-разному всасывается из разных источников и происходит постоянное обеднение им поверхности, т.е. таблицы питательной ценности продуктов «не поспевают» за истинным положением дел (в них зачастую указываются значения больше реальных).
Максимальные разовые безопасные дозы минеральных веществ и пищевых добавок:
| Минеральное вещество | Доза |
|---|---|
| Кальций (мг) | 2500 |
| Фосфор (мг) | 3000 |
| Калий (мг) | 3,7* |
| Железо (мг) | 60 |
| Цинк (мг) | 25 |
| Медь (мг) | 5 |
| Йод (мкг) | 600 |
| Селен (мкг) | 300 |
* Только из биоактивных добавок или обогащенной пищи
Green Синтез и характеристика наночастиц меди и их влияние на функцию печени и гематологические параметры у мышей
Turk J Pharm Sci. 2020 авг.; 17(4): 412–416.
2020 авг.; 17(4): 412–416.
Опубликовано онлайн 2020 августа 28. DOI: 10.4274/tjps.galenos.2019.28000
, 1 , 2 , 3 , 4 и 5, *
Авторская статья. и информация о лицензии Отказ от ответственности
Цели:
Настоящее исследование основано на зеленом синтезе наночастиц меди (CuNP) из водного экстракта плодов Capparis spinosa L.. Оценивали их влияние на функцию печени и гематологические показатели у мышей.
Материалы и методы:
Был достигнут зеленый синтез CuNP с помощью экстракта C. spinosa . Для идентификации синтезированных наночастиц использовали ультрафиолетово-видимую спектроскопию, инфракрасную спектроскопию с преобразованием Фурье (FTIR), сканирующую электронную микроскопию (SEM) и энергодисперсионную рентгеновскую спектроскопию. Мышам BALB/c перорально вводили CuNP в дозах 1000, 2000 и 5000 мкг/кг в течение 2 недель. Позже влияние CuNP на функцию печени у обработанных мышей оценивали путем измерения уровней в сыворотке ферментов, таких как аланинаминотрансфераза, аспартатаминотрансфераза, щелочная фосфатаза и билирубин, а также гематологических параметров, включая гемоглобин, гематокрит, лейкоциты, эритроциты. количество клеток крови и тромбоцитов.
количество клеток крови и тромбоцитов.
Результаты:
Максимальный пик при длине волны 414 нм подтвердил биосинтез CuNP. Анализ спектра FTIR показал, что группы факторов формируют экстракт покрытия на поверхности наночастиц. Изображения SEM продемонстрировали размер частиц от 17 до 41 нм. Хотя некоторые ферменты печени и гематологические показатели увеличивались с увеличением дозы экстракта, достоверной разницы (p>0,05) между пероральным введением НЧ Cu в дозах 1000, 2000 и 5000 мкг/кг и контрольной группой не наблюдалось.
Заключение:
Полученные данные показали, что НЧ Cu, биосинтезированные из водного экстракта плодов C. spinosa , не оказывают токсического действия на функции печени и гематологические показатели мышей. Однако необходимы дополнительные исследования для оценки гепатопротекторных эффектов CuNP.
Ключевые слова: Наночастицы, медь, печень, гематология, Capparis spinosa, мыши BALB/c энергетика, электроника и космическая промышленность. В частности, эта технология применяется при лечении рака, аллергии, воспалений, диабета и других заболеваний. 1
В частности, эта технология применяется при лечении рака, аллергии, воспалений, диабета и других заболеваний. 1
Существуют различные физические и химические методы производства наночастиц, и они все еще исследуются с целью получения частиц определенного размера и меньшей токсичности. 2 Зеленый синтез считается новым подходом к предотвращению производства нежелательных или небезопасных побочных продуктов с помощью надежных, ремонтопригодных и экологически благоприятных методов синтеза. Между существующими зелеными процедурами синтеза наночастиц использование растительных экстрактов является подходящим и простым методом сбора наночастиц в больших масштабах по сравнению с синтезом, опосредованным бактериями и/или грибами. 2,3 Недавние исследования также показали, что синтез наночастиц металлов с использованием растительных экстрактов, т. е. зеленый синтез, имеет некоторые преимущества, такие как низкая стоимость и низкое токсическое воздействие при крупномасштабном производстве. 2,3,4
2,3,4
Медь (Cu) является одним из наиболее полезных элементов в медицине из-за ее многочисленных противовоспалительных, противораковых, обезболивающих и противомикробных эффектов. 5 В последние годы было доказано, что из-за высокого отношения поверхности к объему наночастицы Cu (CuNP) чрезвычайно реакционноспособны и просто взаимодействуют с другими частицами, что приводит к широкому спектру биологической активности. 5,6,7
Предыдущие обзоры на лабораторных животных показали, что печень считается ключевой тканью-мишенью токсичности лекарств. Следовательно, оценка функции этого органа является очень важным методом определения токсичности лекарств. 8 В настоящее время одним из основных критериев для определения повреждения печени является определение уровней в сыворотке крови таких ферментов, как аланинаминотрансфераза (АЛТ), аспартатаминотрансфераза (АСТ), щелочная фосфатаза (ЩФ) и билирубин. 9,10,11 Сообщалось, что пероральное употребление некоторых лекарственных средств может повлиять на гематологические параметры и привести к анемии, нейтропении и тромбоцитопении; поэтому необходимо оценивать эффекты новых лекарственных препаратов путем измерения гематологических параметров. 10 Соответственно, в настоящем исследовании изучался зеленый синтез CuNP из экстракта плодов Capparis spinosa и оценивалось их влияние на функцию печени и гематологические параметры у мышей.
10 Соответственно, в настоящем исследовании изучался зеленый синтез CuNP из экстракта плодов Capparis spinosa и оценивалось их влияние на функцию печени и гематологические параметры у мышей.
Зеленый синтез наночастиц меди
Плоды C. spinosa были собраны в сельских районах западного Ирана и затем экстрагированы методом перколяции с помощью метанола (80%) в течение 3 дней при комнатной температуре. 12 На следующем этапе был проведен зеленый синтез CuNP в соответствии с методом, описанным в другом месте. Вкратце, 75 мл полученного экстракта добавляли к 100 мл 0,01 М раствора сульфата меди. После перемешивания выдерживали при 60°С в течение 1 суток. На следующем этапе для удаления всех примесей его дважды центрифугировали при 12 000 об/мин в течение 20 мин. Наночастицы начали осаждаться, когда цвет раствора изменился с зеленого на янтарно-желтый. Синтезированные наночастицы подвергали термообработке в печи при 60°С для дальнейшего анализа.
Спектроскопический анализ в ультрафиолетовом и видимом (UV-Vis) диапазонах
Трансформация ионов Cu в CuNP была показана с помощью поверхностного плазмонного резонанса (SPR) CuNP. Для этого 0,3 мл образцов разводили 3 мл физиологического раствора и исследовали с помощью УФ-видимого спектра на спектрофотометре (JENWAY 6405) в диапазоне 300-700 нм. 13
Инфракрасная спектроскопия с преобразованием Фурье (FTIR)
После заливки и смешивания полученных образцов и гранул бромида калия в соотношении 1 к 100 (соотношение 1/100) и прессования их в таблетки был проведен анализ FTIR (модель Nicolet 32) в диапазоне 400-4000 см -1 и с разрешением 1-4 см -1 . 14
Сканирующий электронный микроскоп (СЭМ)
Для получения характеристик синтезированных наночастиц была проведена электронная микроскопия (Mira3, Чехия) при 15 кВ, увеличении 10х, разрешении 1 нм.
Животные и дизайн исследования
Всего 32 самца мышей BALB/c весом 25-30 г были предоставлены Тегеранским институтом Пастера и содержались при цикле свет/темнота 12:12 часов. Комнатная температура была 22±2°C, а у мышей было вволю доступ к воде и пище. Их помещали в лабораторные условия за 30 мин до начала эксперимента. Этическое одобрение, необходимое для этого исследования (IR.LUMS.REC.1398.247), было выдано Комитетом по этике Лорестанского университета медицинских наук, Лорестан, Иран. Тестируемых мышей разделили на следующие четыре группы:
Комнатная температура была 22±2°C, а у мышей было вволю доступ к воде и пище. Их помещали в лабораторные условия за 30 мин до начала эксперимента. Этическое одобрение, необходимое для этого исследования (IR.LUMS.REC.1398.247), было выдано Комитетом по этике Лорестанского университета медицинских наук, Лорестан, Иран. Тестируемых мышей разделили на следующие четыре группы:
Группа i: получали нормальный физиологический раствор перорально в течение 14 дней;
Группа ii: Получали CuNP в концентрации 1000 мкг/кг перорально в течение 14 дней;
Группа iii: Получали CuNP в концентрации 2000 мкг/кг перорально в течение 14 дней;
Группа IV: Получали CuNP в концентрации 5000 мкг/кг перорально в течение 14 дней.
Коллекция образцов
На 15-й день экспериментов мышей анестезировали кетамином-ксилазином с последующим сбором образцов крови у каждой мыши после вскрытия сердца. Собранные образцы крови помещали в пробирки с антикоагулянтом или без него для обработки сгустков, а затем их сыворотку отделяли центрифугированием при 5000xg в течение 10 мин.
Оценка ферментов печени в сыворотке
Для определения гепатопротекторных эффектов CuNP с помощью коммерческих диагностических наборов (Roche, Германия) были проанализированы различные параметры клинической химии, связанные с функцией печени, такие как АСТ, АЛТ, ЩФ и билирубин (прямой и общий). 10,15
Гематологические параметры
Для оценки влияния НЧ Cu на гематологические исследования всю собранную кровь помещали в пробирки, содержащие этилендиаминтетрауксусную кислоту. Затем с помощью Sysmex (KX-21, Япония) измеряли гематологические параметры, включая гемоглобин, гематокрит, количество лейкоцитов, эритроцитов и тромбоцитов (PLT).
Статистический анализ
SPSS версии 17.0 (SPSS Inc., Чикаго, Иллинойс, США) использовали для анализа полученных данных. Односторонний ANOVA и апостериорный критерий Тьюки были выполнены для оценки различий между экспериментальными группами, и p<0,05 считалось статистически значимым.
Анализ ультрафиолетового и видимого спектров
Полученные результаты показали, что наибольший пик синтезированных НЧ Cu приходится на длину волны 414 нм. Характеристика резонансной полосы ПП произошла для НЧ Cu при длине волны 414 нм ().
Открыть в отдельном окне
Спектр поглощения синтезированных наночастиц меди
Инфракрасный анализ с преобразованием Фурье
Данные FTIR показали, что биомолекулы в экстракте снижают концентрацию сульфата меди. Полосы 3380, 2928, 1741, 1604, 1400, 1050 и 1271 относятся к растяжению ОН спирта и фенола, растяжению С-Н алифатической группы, растяжению С=О сложноэфирного карбонила, растяжению С=С ароматического соединения. кольцо и растяжение сложного эфира C-O соответственно ().
Открыть в отдельном окне
FTIR-спектр синтезированных наночастиц меди
FTIR: инфракрасный Фурье-преобразование
Анализ с помощью сканирующего электронного микроскопа
После подтверждения синтезированных наночастиц с помощью модификации цвета, видимого УФ и ИК-Фурье характеристики наночастиц были определены с помощью СЭМ. Как показано на рисунке, синтезированные НЧ Cu представляют собой сферическую морфологию, тогда как размер частиц составляет от 17 до 41 нм ().
Как показано на рисунке, синтезированные НЧ Cu представляют собой сферическую морфологию, тогда как размер частиц составляет от 17 до 41 нм ().
Открыть в отдельном окне
Электронно-микроскопические изображения наночастиц меди, синтезированных с использованием водного экстракта Capparis spinosa Плоды x10000
Гепатопротекторные эффекты CuNPs
представлены результаты гепатопротекторного действия на биохимические показатели сыворотки крови мышей, получавших CuNP в дозах 1000, 2000 и 5000 мкг/кг в течение 14 дней. Как видно, хотя эти параметры увеличивались с увеличением дозы экстракта, статистически значимой разницы (p>0,05) между пероральным введением НЧ Cu в дозах 1000, 2000 и 5000 мкг/кг и контрольной группой не было.
Таблица 1
Влияние CuNP на ферменты печени в сыворотке после 2-недельного введения мышам. Результаты представлены в виде среднего ± стандартное отклонение
Открыть в отдельном окне
Влияние на гематологические параметры
Как показано в , после перорального введения CuNPs в используемых дозах 1000, 2000 и 5000 мкг/кг в течение 14 дней не было существенной разницы (p<0,05) между гематологическими параметрами по сравнению с контрольной группой.
Таблица 2
Гематологические параметры цельной крови мышей после перорального введения CuNP в течение 2 недель. Результаты представлены в виде среднего ± стандартное отклонение
Открыть в отдельном окне
В последние годы исследования в области нанотехнологий продемонстрировали, что физические и химические процедуры для создания наночастиц, несмотря на их исключительную биологическую активность, из-за наличия некоторых ограничения, такие как токсичность, заменены рядом новых методов, таких как зеленый синтез. 1 Сегодня, учитывая, что наночастицы широко используются значительной частью населения земного шара для лечения некоторых заболеваний, необходимо измерять токсичность этих продуктов различными методами. Поскольку недавние исследования показали, что НЧ Cu обладают широким спектром биологической активности, мы решили оценить их токсичность и гепатопротекторное действие на мышах.
Недавние исследования показали, что измерение ферментов печени является одним из ключевых диагностических тестов для оценки функции печени, а также воспалений и повреждений, таких как гепатит и цирроз. 8,10 НЧ Cu из-за высокого отношения поверхности к объему чрезвычайно реакционноспособны и просто взаимодействуют с другими частицами. Следовательно, они обладают многочисленными биологическими активностями. 17,18 Доказано, что некоторые лекарственные препараты могут вызывать непоправимые осложнения за счет снижения количества лейкоцитов и эритроцитов и количества тромбоцитов в крови; таким образом, необходимо оценивать эффекты новых лекарственных препаратов путем измерения гематологических параметров. 19
8,10 НЧ Cu из-за высокого отношения поверхности к объему чрезвычайно реакционноспособны и просто взаимодействуют с другими частицами. Следовательно, они обладают многочисленными биологическими активностями. 17,18 Доказано, что некоторые лекарственные препараты могут вызывать непоправимые осложнения за счет снижения количества лейкоцитов и эритроцитов и количества тромбоцитов в крови; таким образом, необходимо оценивать эффекты новых лекарственных препаратов путем измерения гематологических параметров. 19
По результатам настоящего исследования, после перорального введения мышам НЧ Cu в дозах 1000, 2000 и 5000 мкг/кг в течение 14 дней, хотя некоторые параметры увеличивались с увеличением дозы экстракта, не наблюдалось статистически значимое различие (p>0,05) между пероральным введением CuNP в этих дозах и контрольной группой. Кроме того, не наблюдалось статистически значимой разницы (p<0,05) в гематологических параметрах между мышами, получавшими CuNP, и контрольной группой.
Принимая во внимание изучение гепатопротекторных эффектов наночастиц и аналогичные нашим выводам, Zhang et al. 20 продемонстрировали, что наночастицы серебра, синтезированные с использованием Rhizophora apiculata , эффективно защищают печень от вредного воздействия четыреххлористого углерода.
Бхуванешвари и др. 21 сообщалось, что повышенные ферментативные уровни АСТ, АЛТ, ЩФ и билирубина под действием CCl 4 нормализовались при обработке наночастицами серебра, синтезированными с использованием экстракта плодов Embilica officinalis , что указывает на сильное гепатопротекторное действие этих наночастиц. В исследовании, проведенном Eftekhari et al. 22 , наночастицы кверцетина продемонстрировали замечательную гепатопротекторную активность за счет снижения уровней АСТ, АЛТ и ЩФ. Ghosh и Gomes 23 также недавно показали, что наночастицы золота, синтезированные экстрактом Trigonella foenum-graecum , значительно нормализуют повышенные ферментативные уровни АСТ, АЛТ, ЩФ и билирубина, вызванные CCl 4 , что указывало на гепатопротекторный потенциал этих наночастиц.
В настоящем исследовании мы применили C. spinosa для облегчения синтеза CuNP. Затем мы синтезировали CuNP, которые были сферическими и имели размер от 17 до 41 нм. На сегодняшний день существует широкий спектр растений, таких как Syzygium ароматический , Nerium oleander , Citrus medica Linn., Capparis zeylanica , Gloriosa superba L. и Vitis vinifera 9.0026 были применены в биосинтезе CuNP. Однако более детальное определение способности растения как биологического материала для синтеза наночастиц требует дополнительных исследований. 5,6,17,24,25,26,27
Полученные данные показали, что НЧ Cu, биосинтезированные из водного экстракта плодов C. spinosa , не оказывают токсического действия на печень исследованных мышей, а значимой токсичности не выявлено. наблюдаются по их гематологическим показателям. Однако необходимо провести дополнительные исследования для оценки гепатопротекторного действия CuNP.
Авторы выражают благодарность сотрудникам Исследовательского центра растительных лекарственных средств Рази, Хоррамабад, Иран, а также сотрудникам Бамского университета медицинских наук, Бам, Иран.
Конфликт интересов: Авторы заявляли об отсутствии конфликта интересов. Ответственность за содержание и написание статьи несут только авторы.
1. Boisseau P, Loubaton B. Наномедицина, нанотехнологии в медицине и нанотехнологии для медицины. Comptes Rendus Physique. 2011;12:620–636. [Академия Google]
2. Мано П.М., Карунаи С.Б., Джон Пол Дж.А. Зеленый синтез наночастиц серебра из экстрактов листьев Euphorbia hirta и Nerium indicum. Дайджест J Nanomat Biostruct. 2011; 6: 869–877. [Google Scholar]
3. Khatami M, Pourseyedi S. Водный экстракт косточки Phoenix dactylifera (финиковая пальма) опосредован новым путем синтеза высокостабильных наночастиц серебра с высокой противогрибковой и антибактериальной активностью. ИЭТ Нанобиотехнологии. 2015;9:184–190. [PubMed] [Google Scholar]
4. Хатами М., Мортазави С.М., Кишани-Фарахани З., Амини А., Амини Э., Хели Х. Биосинтез наночастиц серебра с использованием пыльцы сосны и оценка противогрибковой эффективности. Иран Дж. Биотехнология. 2017;15:95–101. [Бесплатная статья PMC] [PubMed] [Google Scholar]
Хатами М., Мортазави С.М., Кишани-Фарахани З., Амини А., Амини Э., Хели Х. Биосинтез наночастиц серебра с использованием пыльцы сосны и оценка противогрибковой эффективности. Иран Дж. Биотехнология. 2017;15:95–101. [Бесплатная статья PMC] [PubMed] [Google Scholar]
5. Сараняадеви К., Субха В., Равиндран Р.С., Ренганатан С. Синтез и характеристика наночастиц меди с использованием экстракта листьев Capparis Zeylanica. Int J Chem Tech Res. 2014;6:4533–4541. [Google Scholar]
6. Naika HR, Lingaraju K, Manjunath K, Kumar D, Nagaraju G, Suresh D, Nagabhushana H. Зеленый синтез наночастиц CuO с использованием экстракта Gloriosa superba L. и их антибактериальная активность. J Taibah Uni Sci. 2015;9:7–12. [Академия Google]
7. Angrasan J, Subbaiya R. Биосинтез наночастиц меди водным экстрактом листьев Vitis vinifera и его антибактериальная активность. Int J Curr Microbiol Appl Sci. 2014;3:768–774. [Google Scholar]
8. Махмудванд Х., Фаллахи С., Махмудванд Х., Шакибаи М. , Харанди М.Ф., Дезаки Э.С. Эффективность Myrtus communis L. для инактивации эхинококковой кисты протосколесов. J Invest Surg. 2016;29:137–143. [PubMed] [Google Scholar]
, Харанди М.Ф., Дезаки Э.С. Эффективность Myrtus communis L. для инактивации эхинококковой кисты протосколесов. J Invest Surg. 2016;29:137–143. [PubMed] [Google Scholar]
9. Fallahi S, Beyranvand M, Mahmoudvand H, Nayebzadeh H, Kheirandish F, Jahanbakhsh S. Химический состав, острая и подострая токсичность эфирного масла Satureja khuzestanica у мышей. Джей Рез Фарм. 2017;21:515–521. [Академия Google]
10. Mahmoudvand H, Oliaei RT, Mirbadie SR, Kheirandish F, Kareshk AT, Ezatpour B, Mahmoudvand H. Эффективность и безопасность Bunium Persicum (Boiss) для инактивации протосколесов во время операций на эхинококковых кистах. Surg Infect (лиственница). 2016;17:713–719. [PubMed] [Google Scholar]
11. Mahmoudvand H, Mahmoudvand H, Oliaee RT, Kreshk AT, Mirbadie SR, Aflatoonian MR. In vitro протосколицидные эффекты эфирного масла Cinnamomum zeylanicum и его токсичность у мышей. Фармакогн Маг. 2017; 13 (Приложение 3): S652–S657. [Бесплатная статья PMC] [PubMed] [Google Scholar]
12. Шираванд М., Эбрахими К., Махмудванд Х. Биосинтез наночастиц меди с использованием водного экстракта плодов Capparis spinosa и исследование его антибактериальной активности. Мармара Фарм Дж. 2017; 21:866–871. [Google Scholar]
Шираванд М., Эбрахими К., Махмудванд Х. Биосинтез наночастиц меди с использованием водного экстракта плодов Capparis spinosa и исследование его антибактериальной активности. Мармара Фарм Дж. 2017; 21:866–871. [Google Scholar]
13. Хатами М., Мортазави С.М., Кишани-Фарахани З., Амини А., Амини Э., Хели Х. Биосинтез наночастиц серебра с использованием пыльцы сосны и оценка противогрибковой эффективности. Иран Дж. Биотехнология. 2017;15:95–101. [Бесплатная статья PMC] [PubMed] [Google Scholar]
14. Солтани Неджад М., Хатами М., Шахиди Бонжар Г.Х. Внеклеточный синтез золотых нанотреугольников с использованием биомассы Streptomyces microflavus. ИЭТ Нанобиотехнологии. 2016;10:33–38. [Бесплатная статья PMC] [PubMed] [Google Scholar]
15. Mahmoudvand H, Kheirandish F, Dezaki ES, Shamsaddini S, Harandi MF. Химический состав, эффективность и безопасность Pistacia vera (разновидность Fandoghi) для инактивации протосколексов во время операции на эхинококковой кисте. Биомед Фармаколог. 2016; 82: 393–398. [PubMed] [Академия Google]
2016; 82: 393–398. [PubMed] [Академия Google]
16. Мурти С.К. Наночастицы в современной медицине: современное состояние и проблемы будущего. Int J Наномедицина. 2007; 2: 129–41. [Бесплатная статья PMC] [PubMed] [Google Scholar]
17. Гопинатх М., Суббайя Р., Селвам М.М., Суреш Д. Синтез наночастиц меди из водного экстракта листьев олеандра нериума и его антибактериальная активность. Int J Curr Microbiol Appl Sci. 2014;3:814–818. [Google Scholar]
18. Катха У. и Гаджера Х. Синтез наночастиц меди двумя разными методами и сравнение размеров. Int J Pharm Bio Sci. 2014;5:533–540. [Академия Google]
19. Муриити Н.Дж., Майна Г.С., Мугенди Н.М., Майна М.Б., Киамби М.Дж., Кельвин Дж.К., Умар А., Джон М.К., Энн Н.В., Ю.А., Пьеро Н.М., Элиуд Н.М. Определение гематологических эффектов метанольного экстракта листьев S. incanum у нормальных мышей. Фарм Анал Акта. 2015;6:10. дои: 10.4172/21532435.1000429. [Интернет]
20. Zhang H, Jacob JA, Jiang Z, Xu S, Sun K, Zhong Z, Varadharaju N, Shanmugam A. Гепатопротекторный эффект наночастиц серебра, синтезированных с использованием водного экстракта листьев Rhizophora apiculata. Int J Наномедицина. 2019;14:3517–3524. [Бесплатная статья PMC] [PubMed] [Google Scholar]
Гепатопротекторный эффект наночастиц серебра, синтезированных с использованием водного экстракта листьев Rhizophora apiculata. Int J Наномедицина. 2019;14:3517–3524. [Бесплатная статья PMC] [PubMed] [Google Scholar]
21. Бхуванесвари Р., Чидамбаранатан Н., Джегатесан К. Гепатозащитный эффект Embilica officinalis и его наночастиц серебра против гепатотоксичности, индуцированной ccl4, у белых крыс Wistar. Дайджест журнала наноматериалов и биоструктур. 2014; 9: 223–235. [Google Scholar]
22. Эфтехари А., Ахмадиан Э., Панахи-Азар В., Хоссейни Х., Табибиазар М., Дизай С.М. Гепатозащитное действие наночастиц кверцетина и удаление свободных радикалов при повреждении печени, вызванном афлатоксином B1: исследования in vitro/in vivo. Artif Cells, Nanomed Biotechnol. 2018;46:411–420. [PubMed] [Академия Google]
23. Ghosh S, Gomes A. Гепатопротекторная эффективность наночастиц золота, синтезированных зеленым методом с использованием экстракта семян Trigonella foenum-graecum. Transl Med (Саннивейл) 2016; 6:4. [Google Scholar]
Transl Med (Саннивейл) 2016; 6:4. [Google Scholar]
24. Субханкари И., Наяк П.Л. Синтез наночастиц меди с использованием водного экстракта Syzygium ароматического (гвоздики) с использованием зеленой химии. World J Nano Sci Technol. 2013;2:14–17. [Google Scholar]
25. Shende S, Ingle AP, Gade A, Rai M. Зеленый синтез наночастиц меди компанией Citrus medica Linn. (идилимбу) сок и его антимикробная активность. World J Microbiol Biotechnol. 2015; 31: 865–873. [PubMed] [Академия Google]
26. Джанакираман М. Защитная эффективность наночастиц серебра, синтезированных из силимарина, в отношении индуцированного цисплатином почечного окислительного стресса у белых крыс. Inter J Appl Pharm. 2018;10:110–116. [Google Scholar]
27. Нафари А., Черагипур К., Сепахванд М., Шахрохи Г., Габал Э., Махмудванд Х. Наночастицы: новые средства для лечения лейшманиоза. Эпидемиологический контроль паразитов. 2020;10:e00156. [Бесплатная статья PMC] [PubMed] [Google Scholar]
Биосинтез и характеристика наночастиц меди с использованием Shewanella oneidensis: Application for Click Chemistry
. 2018 март;14(10).
2018 март;14(10).
doi: 10.1002/smll.201703145.
Epub 2018 23 января.
Ричард Л. Кимбер
1
, Эдвард А. Льюис
2
, Фабио Пармеджани
3
, Курт Смит
1
, Хит Бэгшоу
1
, Тоби Старборг
4
, Нимиша Джоши
1
, Адриана I Фигероа
5
, Геррит ван дер Лаан
5
, Джанантонио Чибин
6
, Диего Джанолио
6
, Сара Дж. Хей
2
, Ричард А. Д. Паттрик
1
, Николас Дж. Тернер
Тернер
3
, Джонатан Р. Ллойд
1
Принадлежности
- 1 Школа наук о Земле и окружающей среде и Исследовательский центр молекулярных наук об окружающей среде Уильямсона, Манчестерский университет, Манчестер, M13 9PL, Великобритания.
- 2 Школа материалов Манчестерского университета, Манчестер, M13 9ПЛ, Великобритания.
- 3 Школа химии, Манчестерский институт биотехнологии, Манчестерский университет, Манчестер, M1 7DN, Великобритания.
- 4 Wellcome Center for Cell Matrix Research, Манчестерский университет, Манчестер, M13 9PT, Великобритания.

- 5 Группа магнитной спектроскопии, Алмазный источник света, Дидкот, Оксфордшир, OX11 0DE, Великобритания.
- 6 Алмазный источник света, Дидкот, Оксфордшир, OX11 0DE, Великобритания.
PMID:
29359400
DOI:
10.1002/смл.201703145
Ричард Л. Кимбер и соавт.
Небольшой.
2018 март
. 2018 март;14(10).
doi: 10.1002/smll.201703145.
Epub 2018 23 января.
Авторы
Ричард Л. Кимбер
1
, Эдвард А. Льюис
2
, Фабио Пармеджани
3
, Курт Смит
1
, Хит Бэгшоу
1
, Тоби Старборг
4
, Нимиша Джоши
1
, Адриана I Фигероа
5
, Геррит ван дер Лаан
5
, Джанантонио Чибин
6
, Диего Джанолио
6
, Сара Дж. Хей
2
, Ричард А. Д. Паттрик
1
, Николас Дж. Тернер
3
, Джонатан Р. Ллойд
1
Принадлежности
- 1 Школа наук о Земле и окружающей среде и Исследовательский центр молекулярных наук об окружающей среде Уильямсона, Манчестерский университет, Манчестер, M13 9PL, Великобритания.

- 2 Школа материалов Манчестерского университета, Манчестер, M13 9ПЛ, Великобритания.
- 3 Школа химии, Манчестерский институт биотехнологии, Манчестерский университет, Манчестер, M1 7DN, Великобритания.
- 4 Wellcome Center for Cell Matrix Research, Манчестерский университет, Манчестер, M13 9PT, Великобритания.
- 5 Группа магнитной спектроскопии, Алмазный источник света, Дидкот, Оксфордшир, OX11 0DE, Великобритания.
- 6 Алмазный источник света, Дидкот, Оксфордшир, OX11 0DE, Великобритания.
PMID:
29359400
DOI:
10.
 1002/смл.201703145
1002/смл.201703145
Абстрактный
Наночастицы меди (Cu-NPs) имеют широкий спектр применения в качестве гетерогенных катализаторов. В этом исследовании продемонстрирован новый путь зеленого биосинтеза для производства НЧ меди с использованием бактерии, восстанавливающей металлы, Shewanella oneidensis. Просвечивающая электронная микроскопия тонких срезов показывает, что НЧ Cu преимущественно внутриклеточные и присутствуют в типичном диапазоне размеров 20-40 нм. Серийная сканирующая электронная микроскопия с блочной поверхностью демонстрирует, что НЧ Cu хорошо распределены по трехмерной структуре клеток. Рентгеновская абсорбционная спектроскопия ближнего края и анализ расширенной рентгеновской абсорбционной спектроскопии тонкой структуры показывают, что наночастицы представляют собой Cu(0), однако изображения с атомарным разрешением и спектроскопия потерь энергии электронов предполагают частичное окисление поверхностного слоя до Cu 2 O при контакте с воздухом. Каталитическая активность Cu-NP демонстрируется в архетипической реакции «щелчковой химии», давая хорошие выходы во время азид-алкинового циклоприсоединения, скорее всего, катализируемого поверхностным слоем Cu (I) наночастиц. Кроме того, мутанты с делецией цитохрома предполагают, что новая система восстановления металлов участвует в ферментативном восстановлении Cu(II) и синтезе Cu-NP, который не зависит от пути Mtr, обычно используемого для восстановления других металлов с высокой степенью окисления в этой бактерии. Эта работа демонстрирует новый, простой, экологичный метод биосинтеза для производства эффективных катализаторов на основе наночастиц меди.
Каталитическая активность Cu-NP демонстрируется в архетипической реакции «щелчковой химии», давая хорошие выходы во время азид-алкинового циклоприсоединения, скорее всего, катализируемого поверхностным слоем Cu (I) наночастиц. Кроме того, мутанты с делецией цитохрома предполагают, что новая система восстановления металлов участвует в ферментативном восстановлении Cu(II) и синтезе Cu-NP, который не зависит от пути Mtr, обычно используемого для восстановления других металлов с высокой степенью окисления в этой бактерии. Эта работа демонстрирует новый, простой, экологичный метод биосинтеза для производства эффективных катализаторов на основе наночастиц меди.
Ключевые слова:
Shewanella oneidensis; КСАНЕС; биосинтез; нажмите химия; наночастицы меди.
© 2018 WILEY-VCH Verlag GmbH & Co. KGaA, Вайнхайм.
Похожие статьи
Усиление восстановления шестивалентного хрома с помощью Shewanella oneidensis MR-1 в присутствии наночастиц меди за счет стимуляции бактериального переноса внеклеточных электронов и адаптации к окружающей среде.

Чен Л., Ву И., Шен Ц., Чжэн С., Чен И.
Чен Л. и др.
Биоресурсная технология. 2022 окт.; 361:127686. doi: 10.1016/j.biortech.2022.127686. Epub 2022 25 июля.
Биоресурсная технология. 2022.PMID: 355
Исследование антибактериальных наночастиц меди, стабилизированных альгинатом, методами FT-IR и 2D-IR корреляционной спектроскопии.
Диас-Висуррага Х., Даса С., Посо С., Бесерра А., фон Плессинг С., Гарсия А.
Диас-Висуррага Дж. и др.
Int J Наномедицина. 2012;7:3597-612. дои: 10.2147/IJN.S32648. Epub 2012 11 июля.
Int J Наномедицина. 2012.PMID: 22848180
Бесплатная статья ЧВК.Уникальные свойства наночастиц церия, нанесенных на металлы: новые обратные катализаторы церий/медь для окисления СО и реакции конверсии водяного газа.

Сенанаяке С.Д., Стаккиола Д., Родригес Дж.А.
Сенанаяке С.Д. и др.
Acc Chem Res. 2013 авг. 20;46(8):1702-11. doi: 10.1021/ar300231p. Epub 2013 3 января.
Acc Chem Res. 2013.PMID: 23286528
Биоредуктивное осаждение высокодисперсных наночастиц Ag на углеродные нанотрубки с усиленной каталитической деградацией 4-нитрофенола с помощью Shewanella oneidensis MR-1.
Сонг Х, Ши Х.
Песня X и др.
Environ Sci Pollut Res Int. 2017 Январь; 24 (3): 3038-3044. doi: 10.1007/s11356-016-8076-0. Epub 2016 16 ноября.
Environ Sci Pollut Res Int. 2017.PMID: 27854056
Бактериальные реакции на наночастицы TiO(2), легированные медью.
Ву Б., Хуан Р., Саху М., Фэн С., Бисвас П., Тан Ю.Дж.
Ву Б и др.
Научная общая среда. 1 марта 2010 г .; 408 (7): 1755-8. doi: 10.1016/j.scitotenv.2009.11.004. Epub 2009 20 ноября.
Научная общая среда. 2010.PMID: 19931887
Посмотреть все похожие статьи
Цитируется
Неорганические наноматериалы, нацеленные на опухоль, синтезированные живыми клетками.
Яо И, Ван Д, Ху Дж, Ян С.
Яо Ю и др.
Наномасштаб Adv. 2021 12 апреля; 3 (11): 2975-2994. дои: 10.1039/d1na00155h. Электронная коллекция 2021 1 июня.
Наномасштаб Adv. 2021.PMID: 36133644
Бесплатная статья ЧВК.Рассмотрение.
Классификация наночастиц, физико-химические свойства, характеристика и применение: всесторонний обзор для биологов.
Джуде Н., Линке Д.

Джуде Н. и соавт.
J Нанобиотехнология. 2022 7 июня; 20 (1): 262. doi: 10.1186/s12951-022-01477-8.
J Нанобиотехнология. 2022.PMID: 35672712
Бесплатная статья ЧВК.Рассмотрение.
Зеленые металлические наночастицы: от биосинтеза до приложений.
Чопра Х., Биби С., Сингх И., Хасан М.М., Хан М.С., Юсафи К., Байг А.А., Рахман М.М., Ислам Ф., Эмран Т.Б., Кавалу С.
Чопра Х. и др.
Фронт Биоэнг Биотехнолог. 2022 6 апр;10:874742. дои: 10.3389/fbioe.2022.874742. Электронная коллекция 2022.
Фронт Биоэнг Биотехнолог. 2022.PMID: 35464722
Бесплатная статья ЧВК.Рассмотрение.
Внеклеточный перенос электронов обеспечивает клеточный контроль катализируемого Cu(I) алкин-азидного циклоприсоединения.
Партипило Г.

