Характеристика химического элемента меди: Характеристика переходных элементов (меди, цинка, хрома, железа) по их положению в периодической системе химических элементов Д.И. Менделеева и особенностям строения их атомов / Справочник :: Бингоскул
Содержание
Медь и её характеристики
Онлайн калькуляторы
На нашем сайте собрано более 100 бесплатных онлайн калькуляторов по математике, геометрии и физике.
Справочник
Основные формулы, таблицы и теоремы для учащихся. Все что нужно, чтобы сделать домашнее задание!
Заказать решение
Не можете решить контрольную?!
Мы поможем! Более 20 000 авторов выполнят вашу работу от 100 руб!
Общая характеристика меди
Общее содержание меди в земной коре сравнительно невелико [0,01% (масс.)], однако она чаще чем другие металлы, встречается в самородном состоянии, причем самородки меди достигают значительной величины.
Важнейшими минералами, входящими в состав медных руд, являются: халькозин, или медный блеск Cu2S; халькопирит, или медный колчедан CuFeS2; малахит (CuOH)2CO3.
Чистая медь – тягучий вязкий металл светло-розового цвета (рис. 1), легко прокатываемый в тонкие листы. Она очень хорошо проводит теплоту и электрический ток, уступая в этом отношении только серебру. В сухом воздухе медь почти не изменяется, так как образующаяся на её поверхности тончайшая пленка оксидов (придающая меди боле темный цвет) служит хорошей защитой от дальнейшего окисления. Но в присутствии влаги и диоксида углерода поверхность меди покрывается зеленоватым налетом карбоната гидроксомеди (CuOH)2CO3.
1), легко прокатываемый в тонкие листы. Она очень хорошо проводит теплоту и электрический ток, уступая в этом отношении только серебру. В сухом воздухе медь почти не изменяется, так как образующаяся на её поверхности тончайшая пленка оксидов (придающая меди боле темный цвет) служит хорошей защитой от дальнейшего окисления. Но в присутствии влаги и диоксида углерода поверхность меди покрывается зеленоватым налетом карбоната гидроксомеди (CuOH)2CO3.
Рис. 1. Медь. Внешний вид.
Атомная и молекулярная масса меди
Поскольку в свободном состоянии хром существует в виде одноатомных молекул Cu, значения его атомной и молекулярной масс совпадают. Они равны 63,546.
Изотопы меди
Известно, что в природе медь может находиться в виде двух стабильных изотопов 63Cu (69,1%) и 65Cu (30,9%). Их массовые числа равны 63 и 65 соответственно. Ядро атома изотопа меди 63Cu содержит двадцать девять протонов и тридцать четыре нейтрона, а изотоп 65Cu – столько же протонов и тридцать шесть нейтронов.
Существуют искусственные нестабильные изотопы меди с массовыми числами от 52-х до 80-ти, а также семь изомерных состояний ядер, среди которых наиболее долгоживущим является изотоп 67Cu с периодом полураспада равным 62 часа.
Ионы меди
Электронная формула, демонстрирующая распределение по орбиталям электронов меди выглядит следующим образом:
1s22s22p63s23p63d104s1.
В результате химического взаимодействия медь отдает свои валентные электроны, т.е. является их донором, и превращается в положительно заряженный ион:
Cu0 -1e → Cu+;
Cu0 -2e → Cu2+.
Молекула и атом меди
В свободном состоянии медь существует в виде одноатомных молекул Cu. Приведем некоторые свойства, характеризующие атом и молекулу меди:
|
Энергия ионизации атома, эВ
|
7,72
|
|
Относительная электроотрицательность
|
1,90
|
|
Радиус атома, нм
|
0,128
|
Сплавы меди
Важнейшими сплавами меди с другими металлами являются латуни (сплавы меди с цинком), медноникелевые сплавы и бронзы.
Латуни содержат до 45% цинка. Различают простые и специальные латуни. В состав последних входят другие элементы, например железо, алюминий, олово, кремний.
Медноникелевые сплавы подразделяются на конструкционные и электротехнические. К конструкционным относятся мельхиоры и нейзильберы. Мельхиоры содержат 20-30% никеля и небольшие количества железа и марганца, а нейзильберы содержат 5-35% никеля и 13-45% цинка. К электротехническим медноникелевым сплавам относятся константан (40% никеля, 1,5% марганца), манганин (3% никеля и 12% марганца) и копель (43% никеля и 0,5% марганца).
Бронзы подразделяются по основному входящему в их состав компоненту (кроме меди) на оловянные, алюминиевые, кремнистые и т.д.
Примеры решения задач
|
Понравился сайт? Расскажи друзьям! |
| ||
ЛЕКЦИЯ №4 «Характеристика переходных элементов» для учащихся 11 кл.
 (профиль)
(профиль)
ЛЕКЦИЯ №4 по химии для 11 класса (профиль)
Раздел 1 | ТЕОРЕТИЧЕСКИЕ ОСНОВЫ ХИМИИ |
Тема 2 | Периодический закон и периодическая система химических элементов Д.И. Менделеева. |
Тема 2.3. | «Характеристика переходных элементов — меди, цинка, хрома, железа по их положению в периодической системе химических элементов Д.И. Менделеева и особенностям строения их атомов» |
Элементы содержания, проверяемые заданиями КИМ: А4 | «Характеристика переходных элементов — меди, цинка, хрома, железа по их положению в периодической системе химических элементов Д.И. Менделеева и особенностям строения их атомов» |
Домашнее задание | |
План
|
Большинство элементов-металлов находится в побочных группах Периодической системы.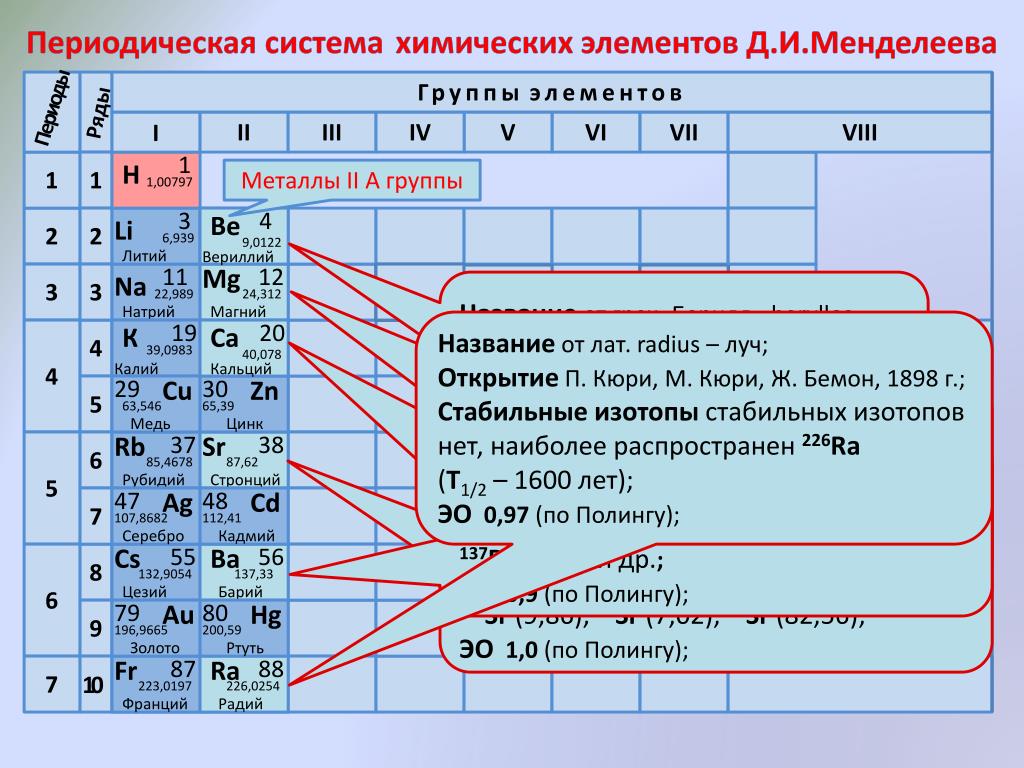
В четвертом периоде у атомов калия и кальция появляется четвертый электронный слой, заполняется 4s -подуровень, так как он имеет меньшую энергию, чем Зй-подуровень. К, Са — s-элементы, входящие в главные подгруппы. У атомов от Sc до Zn заполняется электронами Зd -подуровень.
Рассмотрим, какие силы действуют на электрон, который добавляется в атом при возрастании заряда ядра. С одной стороны, притяжение атомным ядром, что заставляет электрон занимать нижний свободный энергетический уровень. С другой строны, отталкивание уже имеющимися электронами. Когда на энергетическом уровне оказывается 8 электронов (заняты s- и р-орбитали), их общее отталкивающее действие так сильно, что следующий электрон попадает вместо расположенной по энергии ниже d-орбитали на более высокую s-орбиталь следующего уровня. Электронное строение внешних энергетических уровней у калия …3d°4s1, у кальция — …3d°4s2.
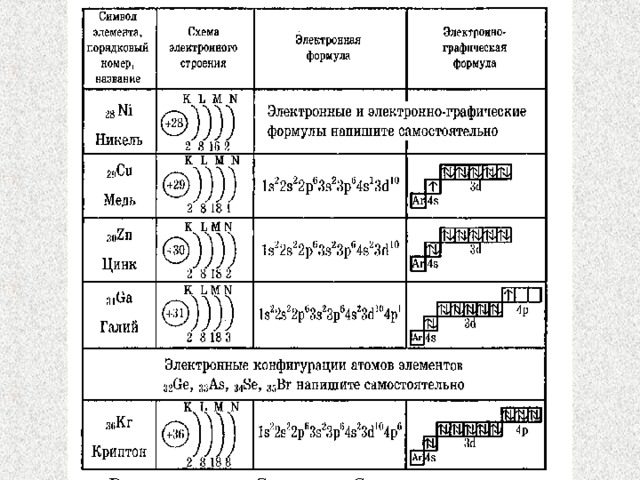
Последующее прибавление еще одного электрона у скандия приводит к началу заполнения Зd — орбитали вместо еще более высоких по энергии 4р-орбиталей.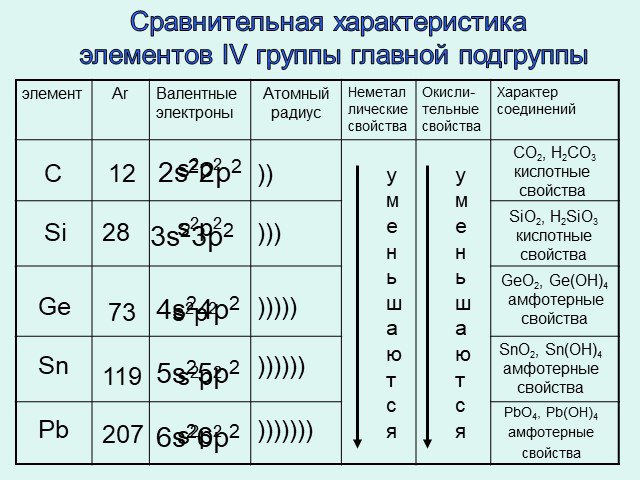 Это оказывается энергетически выгоднее. Заполнение Зd — орбитали заканчивается у цинка, имеющего электронное строение
Это оказывается энергетически выгоднее. Заполнение Зd — орбитали заканчивается у цинка, имеющего электронное строение
1s22s22p63s23p63d104s2. Следует отметить, что у элементов меди и хрома наблюдается явление «провала» электрона. У атома меди десятый d-электрон перемещается на третий Зd – подуровень.
Электронная формула меди …3d104s1.
У атома хрома на четвертом энергетическом уровне (s- орбиталь) должно быть 2 электрона. Однако один из двух электронов переходит на третий энергетический уровень, на незаполненную d-орбиталь, его электронная формула …3d54s1.
Таким образом, в отличие от элементов главных подгрупп, где происходит постепенное заполнение электронами атомных орбиталей внешнего уровня, у элементов побочных подгрупп заполняются
d-орбитали предпоследнего энергетического уровня. Отсюда и название: d-элементы.
Все простые вещества, образованные элементами подгрупп Периодической системы, являются металлами. Благодаря большему числу атомных орбиталей, чем у элементов-металлов главных подгрупп, атомы d-элементов образуют большое число химических связей между собой и потому создают прочную кристаллическую решетку. Она прочнее и механически, и по отношению к нагреванию. Поэтому металлы побочных подгрупп — самые прочные и тугоплавкие среди всех металлов.
Благодаря большему числу атомных орбиталей, чем у элементов-металлов главных подгрупп, атомы d-элементов образуют большое число химических связей между собой и потому создают прочную кристаллическую решетку. Она прочнее и механически, и по отношению к нагреванию. Поэтому металлы побочных подгрупп — самые прочные и тугоплавкие среди всех металлов.
Известно, если атом имеет более трех валентных электронов, то элемент проявляет переменную валентность. Это положение относится к большинству d-элементов. Максимальная их валентность как у элементов главных подгрупп, равна номеру группы (хотя есть и исключения). Элементы с равным числом валентных электронов входят в группу под одним номером (Fe, Co, Ni).
У d-элементов изменение свойств их оксидов и гидроксидов в пределах одного периода при движении слева направо, т. е. с увеличением их валентности, происходит от основных свойств через амфотерные к кислотным. Например, хром имеет валентности +2, +3, +6; а его оксиды: — Сг 0 — основной, Сг203 — амфотерный, СгОа — кислотный.
Источники информации:
- ЕГЭ. ХИМИЯ: Универсальный справочник/ О.В.Мешкова .- М.: ЭКСМО, 2010.- 368с.
- Химия. 11 класс. Профильный уровень: учеб. Для общеобразоват. учреждений / О.С.Габриелян, Г.Г.Лысова. – 10-е изд., перераб. – М.: Дрофа, 2008. – 398, (2) с.: ил.
Характеристики, применение и интересные факты
Горнодобывающая промышленность
Медь — элемент, который часто встречается в земной коре. Его можно найти в рудах, минералах, а также в твердом виде. Во всем мире есть медные рудники из-за огромного спроса в этой отрасли.
Медь в качестве легирующего элемента
Медь добавляется в качестве легирующего элемента только в несколько марок стали. В низколегированных и нелегированных сталях эффективно повышает устойчивость к атмосферным воздействиям. В высоколегированных кислотоупорных сталях добавка более 1 % элемента обеспечивает повышенную стойкость к соляной и серной кислотам.
Применение
Из-за мягкости металла его можно легко деформировать ковкой. Вот почему медь очень быстро стала популярным материалом для ювелирных изделий. Наряду с золотом и серебром, медь была одним из металлов, который очень рано перерабатывался в листовой металл.
Медь является очень хорошим проводником электричества и тепла. Эти свойства делают этот металл незаменимым для промышленности. Особенно в электронике он незаменим и может быть найден практически в каждом электрическом устройстве. В химии большое значение имеют соединения меди. Сульфат меди очень хорошо известен как химический катализатор, который добавляют в плавательные бассейны в качестве средства защиты от водорослей. Сульфат меди также используется в качестве средства защиты растений от грибковых поражений. Медный лист можно использовать в качестве материала для кровельных плит в строительной отрасли.
Медь подвержена коррозии в течение нескольких десятилетий. Это приводит к тонкой патине, которая с возрастом приобретает зеленый цвет. Химически он реагирует с кислородом воздуха, минералами и водой из осадков. При этом образуется минерал под названием малахит, который также встречается в природных месторождениях. Малахит имеет цвет от зеленого до зелено-голубого и придает крышам типичный вид.
Это приводит к тонкой патине, которая с возрастом приобретает зеленый цвет. Химически он реагирует с кислородом воздуха, минералами и водой из осадков. При этом образуется минерал под названием малахит, который также встречается в природных месторождениях. Малахит имеет цвет от зеленого до зелено-голубого и придает крышам типичный вид.
Статуя Свободы в Нью-Йорке выполнена французскими художниками и состоит из более чем 80 тонн меди. Он хорошо пережил долгое путешествие через Атлантику и с 1886 года бросает вызов соленому морскому воздуху. Естественная зеленая патина защищает его от коррозии.
Имущество | Влияние | Степень |
|---|---|---|
Устойчивость к ржавчине | Улучшение | + 1 |
твердость | Улучшение | + 1 |
Прочность | Улучшение | + 1 |
Предел текучести | Улучшение | + 2 |
Эластичность | нет подшипника | 0 |
Термостойкость | Улучшение | 0 |
Карбидообразование | нет подшипника | 0 |
Износостойкость | нет подшипника | 0 |
нитруемость | нет подшипника | 0 |
Напряжение | нет подшипника | 0 |
Уменьшение площади | нет подшипника | 0 |
Ударная вязкость с надрезом | нет подшипника | 0 |
Ковкость | Снижаться | — 3 |
Масштабирование | нет подшипника | 0 |
Обрабатываемость | нет подшипника | 0 |
См.
 также
также
Алюминий
Алюминий очень хорошо поддается формованию и механической обработке. Он особенно подходит для легких конструкций.
Подробнее
БРИНАР
BRINAR – это износостойкая сталь, которая используется в местах с высокой механической нагрузкой.
Подробнее
Конструкционная сталь
Конструкционная сталь обладает отличными механическими свойствами и хорошо поддается обработке.
Подробнее
Медь — Энциклопедия Нового Света
Медь (символ Cu , атомный номер 29) — один из старейших металлов, известных в истории человечества. Красновато-оранжевый цвет, он пластичен, податлив и является отличным проводником тепла и электричества. В своей ионной форме медь является эссенциальным элементом для высших растений и животных, а также для человеческого организма.
В своей ионной форме медь является эссенциальным элементом для высших растений и животных, а также для человеческого организма.
Содержание
- 1 Этимология и алхимический символ
- 2 История
- 3 источника
- 4 Примечательные характеристики
- 4.1 Изотопы
- 4.2 Сплавы
- 5 приложений
- 6 Биологическая роль
- 6.1 Токсичность
- 6.2 Прочие опасности
- 7 Соединения
- 8 Тесты на медь 2+ ионы
- 9 Примечания
- 10 Каталожные номера
- 11 кредитов
Медь и ее сплавы широко используются в электропроводке и машинах, электронных компонентах, конструкционных материалах, кухонной утвари и столовых приборах, чеканке монет, музыкальных инструментах и скульптурах. Кроме того, поскольку медь является биостатическим материалом, медные поверхности и дверные ручки используются в больницах для предотвращения переноса микробов, а сульфат меди (II) используется в качестве фунгицида.
Этимология и алхимический символ
Алхимический символ меди
Медь была важным ресурсом для древних греков и римлян. Греки назвали металл халкос (χαλκός). В римские времена он стал известен как aes Cyprium — aes , являющийся общим латинским термином для медных сплавов, таких как бронза (медь, сплавленная с оловом), и Cyprium , указывающий, что большая часть меди добывалась на Кипре. Отсюда латинское слово стало cuprum , который в конечном итоге был переведен на английский язык до меди .
В мифологии и алхимии медь ассоциировалась с богиней Афродитой/Венерой из-за ее блестящей красоты, ее древнего использования для изготовления зеркал и связи с Кипром, который был посвящен богине. В алхимии символ меди был также символом планеты Венера.
История
Древний медный слиток из Закроса, Крит, имеет форму шкуры животного, характерную для той эпохи
Медь была известна некоторым из древнейших цивилизаций, и ее история использования насчитывает не менее десяти тысяч лет. Медный кулон был найден на территории нынешнего северного Ирака и датируется 8700 90 161 годом до н. э. К 5000 г. г. до н.э. , имеются следы плавки меди, аффинажа меди из простых минералов, таких как малахит или азурит. Медь была первым металлом, выплавленным из руд.[1] Напротив, самые ранние признаки использования золота появляются около 4000 90 161 гг. до н. э.
Медный кулон был найден на территории нынешнего северного Ирака и датируется 8700 90 161 годом до н. э. К 5000 г. г. до н.э. , имеются следы плавки меди, аффинажа меди из простых минералов, таких как малахит или азурит. Медь была первым металлом, выплавленным из руд.[1] Напротив, самые ранние признаки использования золота появляются около 4000 90 161 гг. до н. э.
Самый древний известный литой медный предмет — это наконечник булавы, обнаруженный в Кан Хасане в южной Анатолии и датируемый примерно 5000 90 161 годом до н. э. Имеются артефакты из меди и бронзы (медь в сплаве с оловом, а иногда и с другими элементами) из шумерских городов, которые датируются 3000 годом до н. э. , а древнеегипетские артефакты из меди и бронзы почти такого же возраста. В одной пирамиде была обнаружена пятитысячелетняя медная водопроводная система.
Египтяне обнаружили, что добавление небольшого количества олова облегчает литье металла, поэтому бронзовые сплавы были найдены в Египте почти сразу же, как и медь. Использование меди в Древнем Китае датируется как минимум 2000 годом 9.0161 г. до н. э. К 1200 г. г. до н. э. , в Китае делали отличные бронзы. Обратите внимание, что на эти даты повлияли войны и завоевания, так как медь легко переплавляется и используется повторно.
Использование меди в Древнем Китае датируется как минимум 2000 годом 9.0161 г. до н. э. К 1200 г. г. до н. э. , в Китае делали отличные бронзы. Обратите внимание, что на эти даты повлияли войны и завоевания, так как медь легко переплавляется и используется повторно.
В Европе Эци Ледяной человек, хорошо сохранившийся мужчина, датируемый 3200 годом до н. э. , был найден вместе с топором с медным наконечником, металл которого имел чистоту 99,7%. Высокий уровень мышьяка в его волосах предполагает, что он занимался выплавкой меди. Латунь, сплав цинка и меди, была известна грекам, но впервые широко использовалась римлянами.
Различные цивилизации мира прошли через «Бронзовый век» в разные, но пересекающиеся периоды времени. Например, считается, что ближневосточный бронзовый век длился с 3500 по 1200 год 90 161 года до н. э. ; британский бронзовый век датируется с 2100 по 700 год г. до н.э. ; а центральноевропейский бронзовый век длился с 1800 по 700 год 90 161 года до н. э. Переходный период в некоторых регионах между предшествующим периодом неолита (новый каменный век) и бронзовым веком называется энеолитом, когда некоторые инструменты из меди высокой чистоты использовались наряду с каменными орудиями.
э. Переходный период в некоторых регионах между предшествующим периодом неолита (новый каменный век) и бронзовым веком называется энеолитом, когда некоторые инструменты из меди высокой чистоты использовались наряду с каменными орудиями.
West Mine at Alderley Edge
В эпоху бронзы медь добывалась на Британских островах в основном в следующих местах: South West County Cork, West Wales (например, шахта Cwmystwyth), North Wales (например, Great Orme) , Англси (гора Пэрис), Чешир (Олдерли-Эдж), Стаффордширские вересковые пустоши (например, шахта Эктон) и остров Мэн (между Англией и Северной Ирландией).
В Америке добыча меди началась с маргинальных разработок коренных американцев и некоторых разработок первых испанцев. Европейцы добывали медь в Коннектикуте еще в 1709 году.. Движение на запад также привело к расширению добычи меди с разработкой значительных месторождений в Мичигане и Аризоне в 1850-х годах и в Монтане в 1860-х годах.
Медь активно добывалась на полуострове Кевинау в Мичигане, а центром добычи был продуктивный рудник Куинси. В Аризоне было много известных месторождений, в том числе «Медная королева» в Бисби и «Юнайтед Верде» в Джероме. К 1886 году Анаконда в Бьютте, штат Монтана, стала главным поставщиком меди в стране. Медь также добывалась в Юте, Неваде и Теннесси, среди других мест.
Источники
Открытый медный рудник Эль-Чино в Нью-Мексико
Среднее содержание меди в породах земной коры составляет примерно 68 частей на миллион (млн) по массе. Источниками меди являются следующие минералы:
- сульфиды: халькопирит (CuFeS 2 ), борнит (Cu 5 FeS 4 ), ковеллит (CuS), халькоцит (Cu 2 S)
- карбонаты: азурит (Cu 3 (CO 3 ) 2 (OH) 2 ) и малахит (Cu 2 CO 3 (OH) 2 )
- оксид: куприт (Cu 2 O).

Самородная медь также образуется в нерентабельных россыпных месторождениях.
Медные руды в основном находятся в Чили, США, Индонезии, Австралии, Перу, России, Канаде, Китае, Польше, Казахстане и Мексике. [1]
Большая часть медной руды добывается или извлекается в виде сульфидов меди на крупных карьерах в медно-порфировых месторождениях (медные рудные тела в порфировых породах), содержащих 0,4–1,0% меди. Примеры открытых медных рудников включают Chuquicamata в Чили и шахту El Chino в Нью-Мексико.
Межправительственный совет стран-экспортеров меди (CIPEC), прекративший свое существование в 1992 году, когда-то пытался играть ту же роль в отношении меди, что и ОПЕК в отношении нефти. Однако такого же влияния она не добилась — не в последнюю очередь потому, что второй по величине производитель, Соединенные Штаты, никогда не был ее членом. Образована в 1967 году, ее основными членами были Чили, Перу, Заир и Замбия.
Примечательные характеристики
Медь существует в виде металлически связанного вещества, что позволяет ей иметь широкий спектр металлических свойств
В периодической таблице медь является переходным металлом в периоде 4, между никелем и цинком. Кроме того, он находится в группе 11 (бывшая группа 1В) вместе с серебром и золотом и имеет с ними ряд общих характеристик. Подобно серебру и золоту, медь обладает высокой тепло- и электропроводностью (среди чистых металлов при комнатной температуре только серебро имеет более высокую электропроводность). Все три являются пластичными и ковкими металлами, то есть их можно легко вытянуть в проволоку или раскатать в листы.
Кроме того, он находится в группе 11 (бывшая группа 1В) вместе с серебром и золотом и имеет с ними ряд общих характеристик. Подобно серебру и золоту, медь обладает высокой тепло- и электропроводностью (среди чистых металлов при комнатной температуре только серебро имеет более высокую электропроводность). Все три являются пластичными и ковкими металлами, то есть их можно легко вытянуть в проволоку или раскатать в листы.
Золото и медь являются единственными цветными металлическими элементами, кроме цезия, щелочного металла периода 6. Медь имеет свой характерный красновато-оранжевый цвет, поскольку отражает красный и оранжевый свет и поглощает другие частоты в видимом спектре. Под воздействием атмосферы поверхность металла превращается в карбонат меди (CuCO 3 ), вещество зеленого цвета, называемое патиной .
Чистота меди выражается как 4N для чистоты 99,9999% или 7N для 9Чистота 9,9999999%. Цифра показывает количество девяток после запятой.
Изотопы
Существует два стабильных изотопа меди: 63 Cu и 65 Cu. Кроме того, есть пара десятков радиоизотопов. Подавляющее большинство радиоизотопов имеют период полураспада порядка минут или меньше; самый долгоживущий, 64 Cu, имеет период полураспада 12,7 часов с двумя режимами распада, которые приводят к двум отдельным продуктам.
Кроме того, есть пара десятков радиоизотопов. Подавляющее большинство радиоизотопов имеют период полураспада порядка минут или меньше; самый долгоживущий, 64 Cu, имеет период полураспада 12,7 часов с двумя режимами распада, которые приводят к двум отдельным продуктам.
Сплавы
Существует множество сплавов меди: металлическое зеркало представляет собой сплав меди/олова, латунь представляет собой сплав меди/цинка, а бронза представляет собой сплав меди/олова (иногда с некоторыми другими элементами). Металлический монель представляет собой сплав меди и никеля, также называемый мельхиором. Хотя термин «бронза» обычно относится к сплавам меди и олова, он также является общим термином для любого сплава меди, такого как алюминиевая бронза, кремниевая бронза и марганцевая бронза.
Применение
Медь широко используется в самых разных продуктах, как указано ниже.
- Электрические и электронные товары:
- Электропроводка.
- Электромагниты.
- Электрические машины, особенно электромагнитные двигатели и генераторы.
- Электрические реле, шины и переключатели.
- Вакуумные трубки, электронно-лучевые трубки и магнетроны в микроволновых печах.
- Волноводы для микроволнового излучения.
- В интегральных схемах медь все чаще заменяет алюминий из-за его превосходной проводимости.
- В качестве материала для изготовления компьютерных радиаторов из-за его превосходной способности рассеивать тепло по сравнению с алюминием.
- Электропроводка.
- Конструкционный материал:
- Строительство статуи: Статуя Свободы, например, содержит 179 200 фунтов (81,3 тонны) меди.
- Легированный никелем, используется для коррозионно-стойких материалов в судостроении.
- Кровля, водосточные желоба и водосточные желоба на зданиях.
- Товары для дома:
- Медная сантехника.
- Дверные ручки и другие приспособления в домах.

- В кухонной утвари, такой как сковороды.
- Большинство столовых приборов (ножи, вилки, ложки) содержат некоторое количество меди (нейзильбер).
- пробы, если оно используется в столовой посуде, должно содержать несколько процентов меди.
Серебро
- Тираж:
- Медные сплавы используются в чеканке монет. Например, пенни США состоят из 2,5% меди и 97,5% цинка по весу; никель состоит из 75,0% меди и 25,0% никеля; Даймы и четверти состоят из 91,67% меди и 8,33% никеля.
- Медицинское применение:
- Бактерии не размножаются на поверхности меди, поскольку она является биостатической. Медные дверные ручки и медные поверхности используются в больницах для уменьшения передачи болезнетворных микробов.
- Болезнь легионеров подавляется медными трубками в системах кондиционирования воздуха.
- Сульфат меди(II) используется в качестве фунгицида и средства для борьбы с водорослями в домашних озерах и прудах.
 Он используется в садовых порошках и спреях для уничтожения плесени.
Он используется в садовых порошках и спреях для уничтожения плесени.
- Разное:
- В качестве компонента керамических глазурей и для окрашивания стекла.
- Сплав цинка с образованием латуни используется в музыкальных инструментах и декоративных предметах.
- Различные бронзы, состоящие из меди, олова и других элементов (таких как алюминий, марганец или кремний), используются для изготовления колоколов, тарелок, скульптур и промышленных компонентов.
- Соединения меди (например, раствор Фелинга) находят применение в химии.
- В качестве облицовки частей судов для защиты от скопления ракушек и мидий. Первоначально он использовался в чистом виде, но позже был заменен формой латуни, называемой металлом Мунца.
- Паровой двигатель Джеймса Уатта.
- Инуиты иногда использовали медь для изготовления режущего лезвия для ножей улу.
Биологическая роль
Медь необходима всем высшим растениям и животным. Медь в основном переносится кровью с помощью белка плазмы, называемого церулоплазмином. Когда медь впервые всасывается в кишечнике, она транспортируется в печень в связанном виде с альбумином. Медь содержится в различных ферментах, включая медные центры цитохром-с-оксидазы и фермента супероксиддисмутазы (содержащего медь и цинк). В дополнение к своим ферментативным функциям медь используется для биологического переноса электронов. Белки синей меди, которые участвуют в переносе электронов, включают азурин и пластоцианин. Название «голубая медь» происходит от их интенсивного синего цвета, возникающего из-за полосы поглощения переноса заряда лиганда на металл (LMCT) около 600 нанометров.
Медь в основном переносится кровью с помощью белка плазмы, называемого церулоплазмином. Когда медь впервые всасывается в кишечнике, она транспортируется в печень в связанном виде с альбумином. Медь содержится в различных ферментах, включая медные центры цитохром-с-оксидазы и фермента супероксиддисмутазы (содержащего медь и цинк). В дополнение к своим ферментативным функциям медь используется для биологического переноса электронов. Белки синей меди, которые участвуют в переносе электронов, включают азурин и пластоцианин. Название «голубая медь» происходит от их интенсивного синего цвета, возникающего из-за полосы поглощения переноса заряда лиганда на металл (LMCT) около 600 нанометров.
Большинство моллюсков и некоторые членистоногие, такие как мечехвост, используют для транспорта кислорода медьсодержащий пигмент гемоцианин, а не железосодержащий гемоглобин, поэтому их кровь при насыщении кислородом становится синей, а не красной.
Как отмечалось выше, медь является биостатическим материалом, и медные поверхности не позволяют размножаться бактериям.
Считается, что цинк и медь конкурируют за всасывание в пищеварительном тракте, поэтому диета с избытком одного из этих минералов может привести к дефициту другого. Рекомендуемая диетическая норма (RDA) меди для здоровых взрослых составляет 0,9.миллиграмм (мг)/день.
Токсичность
Со всеми соединениями меди, если не известно иное, следует обращаться так, как если бы они были токсичными. Для человека 30 граммов сульфата меди потенциально смертельны. Предлагаемый безопасный уровень меди в питьевой воде для человека варьируется в зависимости от источника, но, как правило, составляет от 1,5 до 2 мг/л. Верхний допустимый уровень потребления диетической меди (DRI) для взрослых из диетической меди из всех источников составляет 10 мг/день. При токсичности медь может ингибировать фермент дигидрофилгидратазу, фермент, участвующий в кроветворении.
Значительная часть токсичности меди связана с ее способностью принимать и отдавать отдельные электроны при изменении степени окисления. Это катализирует образование очень реакционноспособных «свободных радикалов», таких как гидроксильный (ОН) радикал, аналогично химии фентона. Эта каталитическая активность меди используется ферментами, с которыми она связана, и поэтому токсична только в том случае, если она не изолирована и не опосредована. Увеличение количества неопосредованных реактивных радикалов обычно называют «окислительным стрессом» и является активной областью исследований при различных заболеваниях, где медь может играть важную, но более тонкую роль, чем при острой токсичности.
Это катализирует образование очень реакционноспособных «свободных радикалов», таких как гидроксильный (ОН) радикал, аналогично химии фентона. Эта каталитическая активность меди используется ферментами, с которыми она связана, и поэтому токсична только в том случае, если она не изолирована и не опосредована. Увеличение количества неопосредованных реактивных радикалов обычно называют «окислительным стрессом» и является активной областью исследований при различных заболеваниях, где медь может играть важную, но более тонкую роль, чем при острой токсичности.
Наследственное заболевание, называемое болезнью Вильсона, заставляет организм удерживать медь, поскольку она не выводится печенью с желчью. Это заболевание, если его не лечить, может привести к поражению головного мозга и печени. Кроме того, исследования показали, что люди с психическими заболеваниями, такими как шизофрения, имеют повышенный уровень меди в организме. Однако на данном этапе неизвестно, способствует ли медь психическому заболеванию, пытается ли организм накапливать больше меди в ответ на болезнь, или высокий уровень меди является результатом психического заболевания.
Избыток меди в воде наносит ущерб морской жизни. Наблюдаемый эффект этих более высоких концентраций на рыб и других существ заключается в повреждении жабр, печени, почек и нервной системы.
Прочие опасности
В порошкообразном виде металл является пожароопасным. Кроме того, при концентрациях выше 1 мг/л медь может оставлять пятна на одежде и других предметах, выстиранных в воде.
Соединения
Самородная медь
Обычные степени окисления меди включают менее стабильное состояние меди (I), Cu 1+ и более стабильное состояние меди (II) Cu 2+ . Последний образует голубые или сине-зеленые соли и растворы. В необычных условиях можно получить состояние 3+ и крайне редкое состояние 4+. Медь (I) и медь (II) также называются их общими названиями, медь и медь, соответственно.
Карбонат меди(II) зеленого цвета. Этот состав придает уникальный вид покрытым медью крышам и куполам некоторых зданий. Сульфат меди (II) образует синий кристаллический пентагидрат, одно из наиболее известных соединений меди в лаборатории. В качестве фунгицида используется бордоская смесь.
Сульфат меди (II) образует синий кристаллический пентагидрат, одно из наиболее известных соединений меди в лаборатории. В качестве фунгицида используется бордоская смесь.
Существует два стабильных оксида меди: оксид меди(II) (CuO) и оксид меди(I) (Cu 2 O). Эти оксиды используются для получения оксида иттрия-бария-меди (YBa 2 Cu 3 O 7-δ ) или YBCO, который составляет основу многих нетрадиционных сверхпроводников.
- Соединения меди (I) : хлорид меди (I), оксид меди (I).
- Соединения меди (II) : карбонат меди (II), хлорид меди (II), гидроксид меди (II), нитрат меди (II), оксид меди (II), сульфат меди (II), медь ( II) сульфид.
- Медь (III) Соединения (редко): калий гексафторупрат (K 3 CUF 6 )
- ). CuF 6 )
Тесты на медь
2+ ионы
Добавьте водный раствор гидроксида натрия в тестируемый раствор. Если раствор содержит ионы меди 2+ , то замещением ионов меди ионами натрия будет образовываться голубой осадок гидроксида меди(II). Ионное уравнение:
Если раствор содержит ионы меди 2+ , то замещением ионов меди ионами натрия будет образовываться голубой осадок гидроксида меди(II). Ионное уравнение:
- Cu 2+ (водн.) + 2OH − (водн.) → Cu(OH) 2 (тв.)
В качестве альтернативы, добавьте к испытанному водному раствору аммиака. Если раствор содержит ионы меди 2+ , выпадет осадок, но он растворится при добавлении избытка аммиака, образуя темно-синий аммиачный комплекс, тетрааминомедь(II). Ионное уравнение:
- Cu 2+ (водн.) + 4NH 3 (водн.) → Cu(NH 3 ) 4 2+ (водный)
Примечания
- ↑ Коалиция по образованию в области минералов меди. Проверено 20 июня 2013 г.
Ссылки
Ссылки ISBN поддерживают NWE за счет реферальных сборов
- «Металлы, токсичность и окислительный стресс».
 Current Medicinal Chemistry 12(10) (май 2005 г.): 1161-1208.
Current Medicinal Chemistry 12(10) (май 2005 г.): 1161-1208. - Управление оценки технологий. Глава 6: «Технология производства меди». В Медь: технология и конкурентоспособность (резюме). 2005.
- «Роль химии Фентона в индуцированной тиолами токсичности и апоптозе». Рез. 145(5) (май 1996 г.): 542-53.
Авторы
Энциклопедия Нового Света авторов и редакторов переписали и дополнили статью Википедии
в соответствии со стандартами New World Encyclopedia . Эта статья соответствует условиям лицензии Creative Commons CC-by-sa 3.0 (CC-by-sa), которая может использоваться и распространяться с надлежащим указанием авторства. Кредит должен соответствовать условиям этой лицензии, которая может ссылаться как на Энциклопедия Нового Света участников и самоотверженных добровольных участников Фонда Викимедиа. Чтобы процитировать эту статью, щелкните здесь, чтобы просмотреть список допустимых форматов цитирования.
