Как обозначается латунь в таблице менделеева: Расшифровка марок латунных сплавов — МИР МЕТАЛЛА Тольятти
Содержание
Статьи
Алюминий: особенности металла, сплавы и их применение
Алюминий – это парамагнитный цветной металл, который носит название Al в таблице Менделеева, и ему присвоен порядковый номер 13. В соответствии с высшей электронной формулой алюминия, на орбите атома элемента содержится 13 протонов и 14 нейроно
Подробнее
Свойства дюралюмина
Дюралюминий – это собирательное название сплавов на основе меди и алюминия. Свойства дюралюмина (английский вариант названия сплава) зависят от массовой доли как основных ингредиентов, так и легирующих добавок, которые вводятся в состав веществ
Подробнее
Пруток для пайки меди: особенности, разновидности и применение
В частном жилом доме или современной квартире нередко используются медные трубы для прокладки инженерных коммуникаций. Такой материал не подвержен коррозии, долговечен, практичен и легко поддается ремонту. При необходимости соединения или ремонта под
Подробнее
Медь: особенности металла, производные и их применение
Медь является одним из наиболее популярных представителей группы цветных металлов, используемых в промышленности. В таблице Менделеева элемент имеет порядковый номер 29 и обозначается как Cu.
В таблице Менделеева элемент имеет порядковый номер 29 и обозначается как Cu.
Физические свойства
Данный металл имеет следующие фи
Подробнее
Дюралевые пластины
Дюралевые пластины – это металлические листы, выполненные из дюралюминиевого сплава и широко используемые как полуфабрикат во многих отраслях промышленности. Производство этих изделий в нашей стране было отлажено еще с советских времен, а техно
Подробнее
Химические свойства латуни
Латунь – это металлический сплав из меди и цинка. Химические свойства латуни зависят от процентного содержания цинка в смеси, которое может колебаться от 5% до 45%. Введение в сплав данного химического элемента снижает коэффициент трения матери
Подробнее
Свойства алюминиевых бронз
Алюминиевые бронзы представляют собой сплавы на основе меди, в которых главным легирующим металлом является алюминий. Материал обладает повышенными прочностными свойствами, не поддается коррозии и имеет небольшой коэффициент трения. Содержание алюмин
Содержание алюмин
Подробнее
Краткая информация о физических свойствах меди
Медь – представитель группы цветных металлов, широко используемый в промышленности и быту на протяжении многих столетий. В таблице Менделеева элемент представлен в 11 группе 4 периода и обозначается латинской маркировкой Сu. Представляет собой
Подробнее
Состав и свойства бронзы
Бронза известна человечеству более 3000 лет как высокопрочный сплав на основе меди и олова. Металл обладает повышенной прочностью, не подвержен коррозии, хорошо поддается ковке, из-за чего сфера его применения затрагивает большинство отраслей промышл
Подробнее
Физико-химические свойства меди
Медь широко использовалась человеком с древних времен. Данный металл залегает в недрах земной коры в виде крупных самородков и часто применяется в чистом виде. Благодаря физико-химическим свойствам меди и простоте в обработке, она нашла применение во
Подробнее
Влияния цинка на свойства латуней
Латунь представляет собой металлический сплав на основе меди и цинка. Последний элемент используется в качестве легирующей добавки, и от его содержания зависят свойства сплава. При концентрации цинка в сплаве в количестве 6% – 20% он называется
Последний элемент используется в качестве легирующей добавки, и от его содержания зависят свойства сплава. При концентрации цинка в сплаве в количестве 6% – 20% он называется
Подробнее
Алюминий АМЦ – ГОСТ и характеристики сплава
Алюминий АМЦ входит в систему Al – Mn и относится к сплавам, деформируемым при помощи давления.
В состав металла этой марки входит от 96 до 99% алюминия и от 1 до 1,5% марганца. В соответствии с нормами ГОСТ 4784-97 содержание других примесе
Подробнее
Алюминий В95 – характеристики дюрали и цена сплава
Алюминий В95 представляет собой термоупрочняемый сплав особо высокой прочности.
В состав металла входят алюминий (до 91,5%), медь (от 1,4 до 2%), цинк (от 5 до 7%) и магний (от 1,8 до 2,8%), также в него включено до 0,6% марганца, что делает В95 с
Подробнее
Алюминий Д16 -Д16АТ – ГОСТ, характеристики, свойства, цена сплава
Алюминий Д16 – это сплав высокой прочности, входящий в систему Аl–Сu–Мg.
Состав, свойства и характеристики сплава алюминия Д16 регламентированы ГОСТ 4784-97. В качестве легируемых элементов в него добавлены магний, марганец и мед
Подробнее
Алюминий АМГ6– характеристики, свойства сплава, цена
Сплав алюминия АМг6 относится к магналиям, имеющим высокую пластичность и прочность.
Химический состав, который должен иметь металл АМг6, прописан в ГОСТ 4784-97. В него входит алюминий (93%), магний (от 5,8 до 6,8%) и другие вещества. В этом спла
Подробнее
Алюминий АМг– характеристики марки и цена сплава
АМг – марка алюминия, включающая в себя разные сплавы системы Al-Mn.
Этот вид металла имеет повышенную устойчивость к возникновению пятен ржавчины, высокие прочностные и пластичные свойства.
Также он отличается:
универсальностью,
Подробнее
Алюминий АМг2 — марка, цена – купить в Москве
Алюминий АМг2 деформируемый давлением сплав системы Al–Mg.
Марка АМг2 характеризуется:
небольшим весом,
прекрасной свариваемостью,
высокими антикоррозийными и прочностными характеристиками.
Прочность этого сплава выше, чем у м
Подробнее
Алюминий АМг5- характеристики, марки, цена
Алюминий АМг5 представляет собой деформируемый сплав, главным легирующим элементом в нем выступает магний, доля которого составляет от 4,8 до 5,8%.
Марка алюминия АМг5 применяется для изготовления изделий способом горячей или холодной деформации.
Подробнее
Нержавеющая проволока – основные виды и классы
Нержавеющая проволока – это объединенное понятие для всех стальных металлоизделий с:
Полнотелым сечением (круг)
Высокой стойкостью к повреждению ржавчиной (антикоррозийность)
В своей категории, меж тем, данный нержавеющий проволочн
Подробнее
Применение бронзы — многокомпонентная специализация
Бронза – это второй промышленно востребованный сплав на основе меди после латуни. В бронзовых составах используются различные легирующие компоненты, а в латунных – это цинк. Основным же элементом для бронзовых соединений является ол
Подробнее
Виды и особенности нержавеющих сплавов
Нержавеющая сталь – собирательное понятие для ряда стальных сплавов, имеющих различные компонентные составляющие, но обладающие едиными параметрами антикоррозийной устойчивости.
На самом деле, главным элементом всех видов нержавейки, который
Подробнее
Применение титановых изделий
Титановые металлоизделия, вероятно, заменили бы собой все уже существующие виды металлопроката, если бы не очень высокая стоимость как производства самого металла, так и изделий из него. Ввиду этого, использование титановой продукции реализуется
Подробнее
Станки гидроабразивной резки: специфика, преимущества и область применения
Для производства сложных технических деталей из материалов любого физико-химического состава требуется применение современного оборудования по их обработке. Наиболее частым инструментом являются станки для резки. По конструкции, способу и назначению
Подробнее
Стеновой профлист – выбираем материал и монтируем его на стены
Рулонная сталь – самая популярная заготовка для производства листового проката. Она лежит в основе наиболее стойких к коррозии изделий. Данный материал не поддается влаге. Чтобы согнуть, разрезать или сварить лист потребуется применить большие
Подробнее
Стальные трубы: производство, сфера применения, ГОСТ 9941-81 и 9940-81
Труба – это вид промышленного изделия, представляющее собой вытянутый пустотелый предмет круглого, квадратного или прямоугольного сечения. Назначение материала: транспортировка сырья любого состояния и химического состава (вода, газ, нефть,
Назначение материала: транспортировка сырья любого состояния и химического состава (вода, газ, нефть,
Подробнее
Сталь и стекло
Строительство – одна из самых быстро прогрессирующих отраслей, которая регулярно пополняется инженерными новинками. За всю историю металлов наибольшую популярность в данной сфере заслужила именно нержавеющая сталь. Она используется в бытов
Подробнее
Рифленый лист из алюминия – специфика, марки, технологии
Металлопродукция – основная отрасль производства строительных материалов, проката используемого во всех отраслях и сферах жизнедеятельности, которая наибольшее применение имеет в строительной индустрии и машиностроении. Причина огромной по
Подробнее
Скорлупа для труб
Для уменьшения теплопотерь, особенно в холодное время года, требуется надежная теплоизоляция всех конструкций выступающих за пределы отапливаемого помещени.
Особое внимание уделяется теплоизоляции трубопроводов.
В качестве современного теплоизо
Подробнее
Рифленый лист: особенности и свойства проката
Металлопрокат – продукт не теряющий своей популярности и спроса даже в условиях кризиса.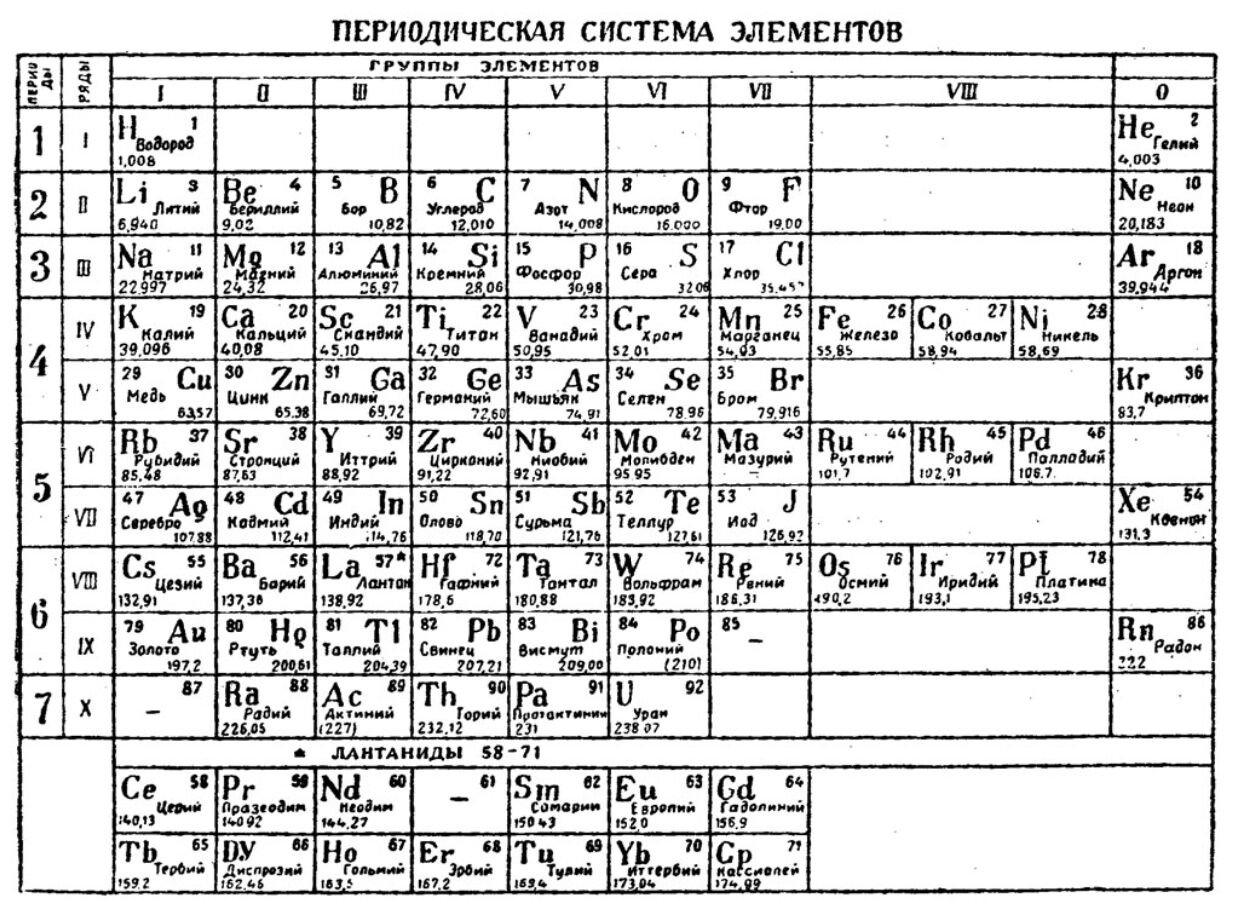 В современном строительстве незаменим, благодаря широкому сортаменту продукции и высоким эксплуатационным характеристикам.
В современном строительстве незаменим, благодаря широкому сортаменту продукции и высоким эксплуатационным характеристикам.
Среди сотен товаров мета
Подробнее
Виды металла: классификация и сферы применения
Металлы – обобщенное название химических элементов, объеденных по ряду признаков. В периодической таблице они занимают большую часть, однако до сих пор не существует документа, позволяющего разделить их на классы.
Отличаются металлы в первую очередь своими качественными характеристиками. Какие-то имеют высокую теплопроводимость, другие выдерживают высокие нагрузки на разрыв и растяжение. В зависимости от этих качеств определяется и сфера применения, но металлы в природном виде, даже очищенные, не обладают необходимыми показателями в достаточном виде, поэтому применяется технология сплавов, то есть соединения нескольких элементов в одну молекулярную решетку. Это позволяет существенно улучшить характеристики, и придать сплаву необходимые качества.
Простой пример: возьмем распространенный в промышленности сплав бронзу. Это соединение, где основным элементом выступает медь. В качестве легирующего, то есть улучшающего качество, компонента используется олово. В результате соединения получается новый металл, более твердый и упругий по сравнению с чистой медью, который часто используют для изготовления крепежа.
Это соединение, где основным элементом выступает медь. В качестве легирующего, то есть улучшающего качество, компонента используется олово. В результате соединения получается новый металл, более твердый и упругий по сравнению с чистой медью, который часто используют для изготовления крепежа.
Основные виды классификации металлов
Существует несколько видов классификации металлов. Начнем с основного типа – деления на две большие группы: черные и цветные. Черные металлы отличает высокая температура плавления, плотность и повышенная твердость. Цветные металлы, в большинстве случаев, плавятся при более низких температурах и обладают повышенной электро и теплопроводимостью.
Такое разделение обусловлено распространением элементов в природе. На добычу черных элементов приходится более 90 процентов от всей массы добываемых металлов, в то время как на цветную группу приходится не более 5-10 процентов. Необходимо отметить, что виды классификации являются условными, и используются в зависимости от назначения конечного продукта, который производят из этих металлов. Так, для изготовления крепежа используется классификация по техническим характеристикам, а для изготовления сложных сплавов химическая и кристаллическая. Рассмотрим эти виды подробнее.
Так, для изготовления крепежа используется классификация по техническим характеристикам, а для изготовления сложных сплавов химическая и кристаллическая. Рассмотрим эти виды подробнее.
Химическая классификация металлов
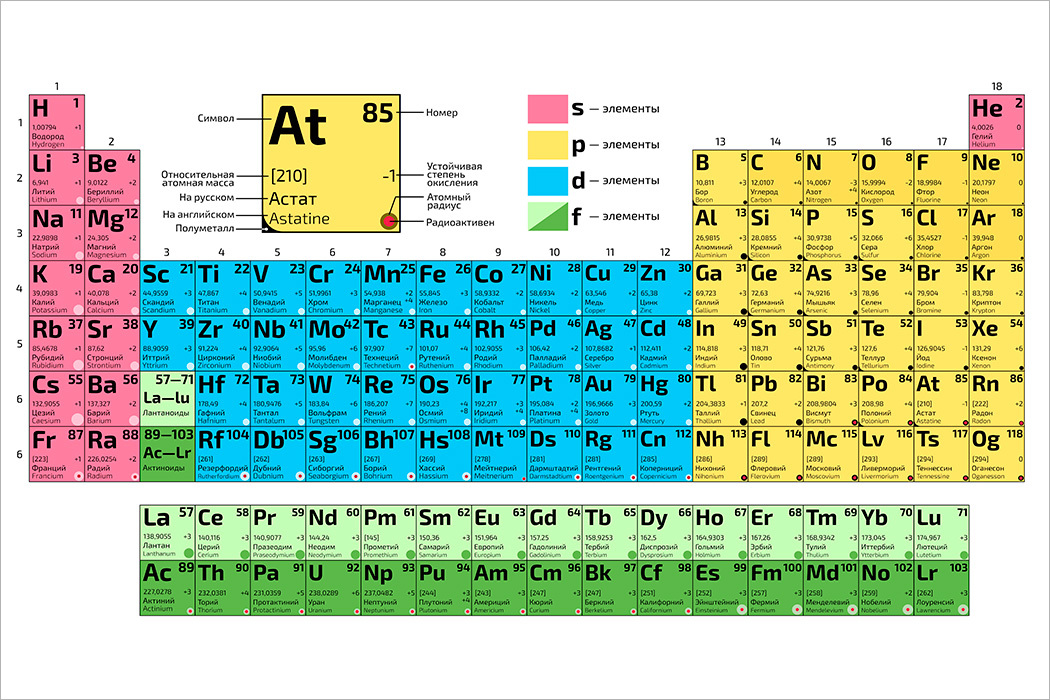
Все элементы в периодической таблице делятся на четыре основных группы, маркируемые латинскими буквами:
- S. Отмечены розовым цветом.
- P. Желтые элементы.
- D. Бирюзовый цвет.
- F. Зеленые элементы в таблице.
Каждая группа содержит в себе металлы. Элементы из первых двух категорий (S и P) называют простым видом, а элементы из групп D и F переходным. Также каждая группа делится еще на несколько категорий. В группу S входят щелочные и щелочеземеленые металлы, а в группы D и F платиновые, урановые и редкоземельные. При этом в каждой группе существуют исключения, из чего можно сделать вывод, что деление металлов по химическим группам является условностью, и редко применяется в практических сферах. Такое деление интересно только для научных изысканий, и практически не применимо в промышленности и производстве. Например, изготовление крепежа отталкивается от технических аспектов, и лишь в малой степени от химических.
Такое деление интересно только для научных изысканий, и практически не применимо в промышленности и производстве. Например, изготовление крепежа отталкивается от технических аспектов, и лишь в малой степени от химических.
Классификация металлов по кристаллической решетке
Все элементы имеют, так называемую, кристаллическую решетку. Абстрактная структура, определяющая расположение атомов и электронов, а также их привязку к ядру. В аморфных материалах, таких как стекло, атомы расположены хаотично, и не имеют строгой конструкции. В отличие от металлов, которые в твердом виде обладают строго структурированной решеткой, с четким построением молекулярных элементов. Всего разделяют 4 вида кристаллических решеток, которые проще представить в виде таблицы:
Это наиболее распространенные типы кристаллических решеток, часто встречающиеся у металлов. В общей сложности система классификации насчитывает 14 конфигураций, но у металлов они или встречаются крайне редко, или не встречаются вообще. Также следует отметить, что правильное построение решетки возможно только при естественном затвердевании металла, без искусственных ускорений. Если процесс остывания был ускорен, форма решетки изменится. В производстве это называют закаливанием, в результате которого меняется не только молекулярная структура, но и технические свойства.
Также следует отметить, что правильное построение решетки возможно только при естественном затвердевании металла, без искусственных ускорений. Если процесс остывания был ускорен, форма решетки изменится. В производстве это называют закаливанием, в результате которого меняется не только молекулярная структура, но и технические свойства.
Также, при нарушении норм производства металлического проката, может наблюдаться замена в кристаллической решетке. Это ведет к полному изменению качеств готового изделия. Чтобы условия производства соблюдались, были разработаны нормы стандартизации, гарантирующие четкое соответствие готового проката техническому описанию его свойств.
Техническая классификация металлов
Наиболее полную систему классификации предложил профессор Гуляев, хотя современные ученые и не согласны с некоторыми ее аспектами, ничего нового пока предложено не было. Итак, черные металлы делят на 5 основных подгрупп:
- Железные металлы. Сюда входят марганец, кобальт, никель, и конечно, железо.
 Наиболее распространенная в природе группа, используемая в сплавах как основной компонент.
Наиболее распространенная в природе группа, используемая в сплавах как основной компонент. - Тугоплавкие. Элементы, имеющие высокую температуру расплавления. В качестве эталона принята мера в 1539 градусов по Цельсию.
- Редкоземельные. Дорогостоящие в плане добычи и обработки элементы, к которым относят неодим, европий, самарий и другие металлы, используемые в качестве присадок к основному сплаву. Способны даже при небольшом проценте вмешательства существенно повысить или полностью изменить характеристики сплава.
- Щелочные. Особая группа, практически не применяемая в чистом виде. Чаще всего используются в атомной энергетике. Сюда относят: литий, барий, радий и другие.
- Урановые. Торий, уран, плутоний. Применяются исключительно в атомной энергетике.
Цветные металлы также делят на несколько подгрупп. Их три:
- Легкие. Алюминий, магний, бериллий. Обладают низким удельным весом и часто применяются в авиастроении и прочих сферах, где необходим твердый, но в то же время легкий материал.

- Легкоплавкие. Металлы с наиболее низкой температурой плавления: цинк, олово, свинец. Используются как в чистом виде, в качестве припоя и соединительного элемента, и как легирующие добавки, повышающие или изменяющие характеристики сплава.
- Благородные или драгоценные металлы. Наиболее редкие элементы, к которым относят: золото, серебро, палладий, платину. Обладают максимальной устойчивостью к коррозии и окислению, благодаря чему получают широкое распространение в различных промышленных сферах.
Практически все металлы из двух групп поддаются смешению, то есть производству из них сплавов с необходимыми техническими характеристиками.
Классификатор металлов по ГОСТ
Если рассматривать метлы с точки зрения геологии и распространения в природе, их делят на две большие группы: черные и цветные. Об этом мы уже говорили выше. В химии деление происходит по 4 направлениям, но чтобы привести виды металлов к общему знаменателю, необходимо более точное разделение. Начнем с основного типа классификации: металлы и сплавы. Металлы – это материалы, используемые в чистом, или практически чистом виде. Здесь допускаются примеси, но в незначительной степени, то есть те, которые не способны оказать влияния и изменить технические характеристики. Сплавами называют соединения, с высоким содержанием двух и более элементов.
Начнем с основного типа классификации: металлы и сплавы. Металлы – это материалы, используемые в чистом, или практически чистом виде. Здесь допускаются примеси, но в незначительной степени, то есть те, которые не способны оказать влияния и изменить технические характеристики. Сплавами называют соединения, с высоким содержанием двух и более элементов.
Для того чтобы сплав получил маркировку, в его составе должно быть не менее 50 процентов основного компонента. То есть, если мы берем бронзу, то понимаем, что в ее составе больше половины занимает медь, а остальное делится между другими металлическими компонентами. Чистые металлы, в свою очередь, делятся на стали и чугуны. Эти металлы имеют в составе углерод. Если его содержание не превышает 2,14 %, его называют сталью. Свыше этого значения уже чугун.
Классификация металлов
Чтобы привести все виды металлов к единому стандарту качества, необходимо разделить их на группы. Таких групп 3:
- Стали,
- Чугуны,
- Сплавы на основе цветных металлов.

Каждая группа имеет деление на подгруппы. У стали это:
- углеродистая,
- легированная,
- специальная.
Углеродистая сталь не имеют легирующих, то есть изменяющих структуру элементов. Допускаются примеси, но в незначительном количестве. Углеродистая сталь в свою очередь делится на инструментальную и конструкционную. Кардинальные различия заключаются в процентах содержания в составе углерода. Конструкционная сталь содержит не более 0,6%, а инструментальная от 0,7 до 1,5%. Далее конструкционная сталь делится на обычное качество и высокое. В обычном качестве допускаются примеси серы и фосфора, но в количестве, не превышающем 0,3 процента. Соответственно высококачественная сталь не предусматривает наличия этих элементов в составе, или их количество должно быть меньше установленной нормы.
Далее легированная сталь, то есть материал, имеющий в составе компонент, влияющий на качественные характеристики сплава. Список легирующих элементов довольно большой, и здесь его приводить не имеет смысла. Содержание легирующего элемента начинается от 2,5%. Такая сталь называется низколегированной. Если в составе от 2,5 до 10 процентов, это уже среднелегированная марка, а при содержании свыше 10 процентов, получается высоколегированная сталь.
Содержание легирующего элемента начинается от 2,5%. Такая сталь называется низколегированной. Если в составе от 2,5 до 10 процентов, это уже среднелегированная марка, а при содержании свыше 10 процентов, получается высоколегированная сталь.
Помимо этого легированные стали делятся по назначению. Здесь три группы:
- инструментальная,
- конструкционная,
- специальная
В стандартизации каждый элемент имеет буквенное обозначение, а для причисления легированной стали к тому или иному классу используется отдельный список. Все легированные стали обозначаются сочетанием букв и цифр. Для примера рассмотрим такое соединение: 10Г2СД.
Первая цифра здесь – это количество углерода в сотых долях процента. Далее буква Г, в классификаторе означающая марганец. Следующая за буквой Г цифра 2 говорит нам о том, что марганец в этом составе присутствует в двухпроцентной доле. И последние две буквы – это дополнительные элементы, процентная доля которых менее 1,5%.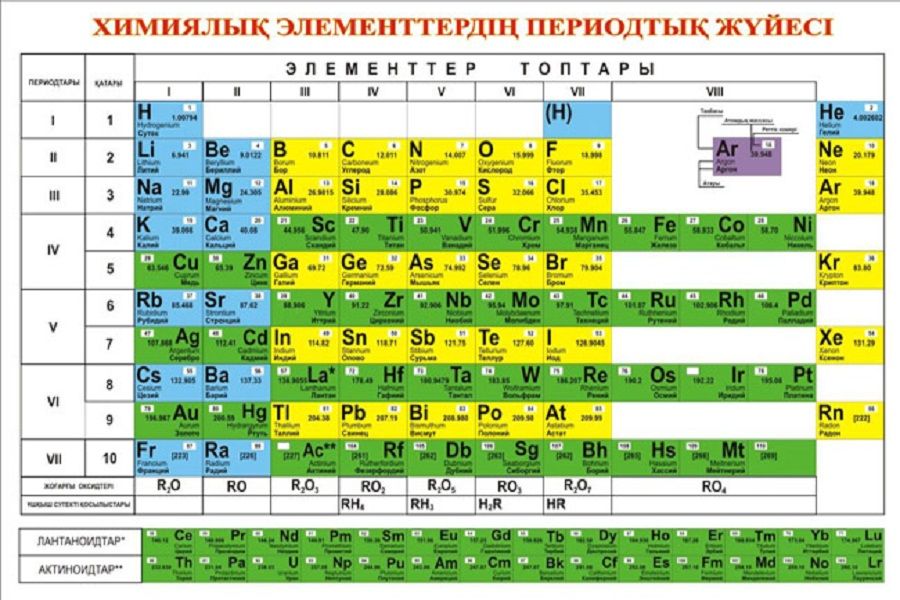 В данном случае сюда добавлены медь и кремний.
В данном случае сюда добавлены медь и кремний.
Последний вид стали – специальный. Он делится на несколько групп:
- строительная,
- подшипниковая,
- арматурная,
- котельная,
- автоматная.
Соответственно для каждой группы имеются свои стандарты.
Далее идут чугуны, делящиеся на три группы:
- белый,
- отбеленный,
- и графитизированный.
У каждой группы также имеется свое разделения, но наибольший интерес представляет графитизированный чугун, который делится на:
- серый,
- вермикулярный,
- ковкий
- и высокопрочный.
Отношение к какой-либо группе определяется процентным соотношением углерода к металлу в составе, а также наличию примесей, допустимых стандартами, то есть ГОСТами.
И, наконец, последняя крупная группа – сплавы на основе цветных металлов. Здесь очень много разделений и видов классификации, поэтому остановимся на трех основных категориях, и представим их в виде таблиц:
Алюминиевые сплавы:
Медные сплавы:
Поиск сплава в классификаторе ГОСТ
Государственные стандарты четко определяют не только виды металлов и сплавов, но и качество производства заготовок для дальнейшей обработки и производства металлоизделий. Реестр очень большой, и первый пункт, который нам нужен – металлы и металлические изделия.
Реестр очень большой, и первый пункт, который нам нужен – металлы и металлические изделия.
Далее переходим в необходимый раздел. Углеродистая и качественная сталь имеет маркировку В2 и В3 соответственно, а цветные металлы и их сплавы находятся в разделе В5. Также имеет смысл поискать в разделе В8, где перечислены стандарты литейных отливок.
Если мы говорим про изготовление крепежа, наибольший интерес представляет раздел В5, а внутри него подраздел В51.
Перед нами открывается список всех ГОСТов, связанных с этими определениями.
Он довольно большой, и не зная конкретного номера найти необходимую статью довольно сложно. Если же номер известен изначально, то на сайте ГосСтандарта есть готовый поиск, куда необходимо внести свой номер, чтобы сразу получить доступ к необходимому элементу.
Сферы применения основных металлов
Рассматривать радиоактивные и редкоземельные металлы не имеет смысла, так как в производстве крепежа они практически не принимают участия, как и в других сферах, не связанных с атомной энергетикой и некоторыми редкими видами промышленности. Нас интересуют основные металлы и сплавы рассмотренные выше.
Нас интересуют основные металлы и сплавы рассмотренные выше.
Сферы их применения очень разнообразны:
- строительство,
- авиастроение,
- машиностроение,
- производство инструментов,
- металлоконструкции,
- станкостроение.
И так далее. Изготовление крепежа можно отнести нескольким категориям, но по сути, это металлоконструкции, называемые в народе Метизы. Для производства метизов используются десятки различных металлов и сплавов, от конструкционной стали и чугуна, до сложных сплавов на основе титана и меди.
Коротко по каждому виду, применяемому для изготовления крепежей
Перед тем как перейти к описанию конкретных видов металлов и сплавов, необходимо определиться, какие основные технические требования предъявляются к продуктам, попадающим под категорию «крепеж». Их несколько:
- прочность учитывается прочность на разрыв и излом.
- Пружинистость. Возможность металла возвращать изначальную форму после сжатия.

- Устойчивость к коррозии и окислению. Актуально для всех видов крепежа.
И многое друге. Теперь поговорим о конкретных металлах и сплавах. Их список выглядит следующим образом:
- Алюминий и сплавы на его основе,
- Медь,
- Латунь,
- Бронза,
- Инструментальная сталь,
- Легированная сталь,
- Ковкий чугун,
- Сталь нержавеющая.
Начнем по порядку: первый пункт – это алюминий и сплавы на его основе. Он применяется при изготовлении клепок и различных зажимов. Также в клепках может быть использована медь для повышения качества метиза. Помимо этого из меди изготавливают гайки специального назначения. Они используются, в частности, при судостроении, так как медь при контакте с другими металлами не создает искру.
Латунь и бронза отличаются повышенной, по сравнению с медью, прочностью, поэтому из них изготавливают различные шпонки, элементы анкеров, а также болты, шурупы и винты. Еще одна особенность этих сплавов заключается в отсутствии скипания. То есть при электрическом замыкании, сталь сплавляется, а медь остается цельной и не разрушается.
Еще одна особенность этих сплавов заключается в отсутствии скипания. То есть при электрическом замыкании, сталь сплавляется, а медь остается цельной и не разрушается.
Из легированной и конструкционной стали изготавливаются барашковые гайки, струбцины и прочие удерживающие элементы. Это обусловлено высокой прочностью этих марок. Нержавеющая сталь, в свою очередь применяется там, где необходима максимальная устойчивость к коррозии. Что касается чугуна, то он чаще всего применяется при производстве запорной арматуры, то есть вентилей и запоров.
Вернуться обратно
ОПУБЛИКОВАТЬ В СОЦ.СЕТЯХ
Определение меди в латуни | Эксперимент
Попробуйте этот микромасштабный практический урок, чтобы определить, сколько меди содержится в латуни с помощью азотной кислоты
В этом эксперименте учащиеся определяют содержание меди в латуни (сплав меди и цинка), растворяя латунную стружку в азотной кислоте и сравнивая цвет раствора с растворами различных концентраций меди. Это должно занять примерно 25 минут.
Это должно занять примерно 25 минут.
Эксперимент имеет возможность использования в качестве оцениваемого практического. Доступны две версии рабочего листа для учащихся — версии A и B. В версии A учащимся в конце предлагаются расчеты. Эту версию можно использовать для оценки навыков проведения эксперимента/следования инструкциям. В версии B помощь с расчетами не предоставляется. Эту версию можно использовать для оценки навыков обработки результатов.
Оборудование
Аппаратура
- Защита глаз
- Рабочий лист для учащихся
- Лист белой бумаги
- Доступ к балансу
- Доступ к вытяжному шкафу
- Стакан, 10 см 3
- Мерная колба, 10 см 3
- Пластиковый планшет с лунками, 24 лунки (например, Sigma ref: CLS3526)
- Пластиковая пипетка (например, Aldrich ref: Z13, 503-8, тонкий наконечник)
Химические вещества
Примечание
Растворы должны содержаться в пластиковых пипетках. См. прилагаемое руководство по оборудованию и методам микрохимии, которое включает инструкции по приготовлению различных растворов.
См. прилагаемое руководство по оборудованию и методам микрохимии, которое включает инструкции по приготовлению различных растворов.
- Кислота азотная, 5 моль дм –3
- Вода деионизированная
- Медь азотнокислая раствор, 0,50 моль дм –3
- Латунная стружка
Здоровье, безопасность и технические примечания
- Прочтите наше стандартное руководство по охране труда и технике безопасности.
- Всегда используйте защитные очки (брызгозащитные очки в соответствии с BS EN166 3).
- Инструкции по приготовлению растворов см. в нашем руководстве по оборудованию и методам микрохимии.
- Азотная кислота, 5 М HNO 3 (водн.) (КОРРОЗИОННОЕ) – см. карточку опасности CLEAPSS HC067 и книгу рецептов CLEAPSS RB061. Рассмотрите возможность использования защитных перчаток.
- Раствор нитрата меди – см. карточку опасности CLEAPSS HC027B и книгу рецептов CLEAPSS RB031.
- УТИЛИЗАЦИЯ: собрать и сохранить растворы меди/цинка для соответствующей утилизации.
Процедура
Приготовление раствора латуни
- Точно взвесьте около 0,3 г латуни в 10-сантиметровом стакане 3 .
- Поместите стакан в вытяжной шкаф.
- Добавьте десять капель азотной кислоты.
- Когда реакция утихнет, добавить еще десять капель азотной кислоты.
- Повторяйте, пока вся латунь не растворится.
- С помощью пипетки перенесите раствор в мерную колбу 3 объемом 10 см. Добавьте капли воды в стакан, чтобы промыть, а затем перенесите промывные воды в колбу. Доведите объем в колбе до отметки с большим количеством воды. Закройте колбу пробкой и несколько раз переверните ее, чтобы перемешать.
Приготовление стандартных растворов меди
Источник: Королевское химическое общество
Используйте эту диаграмму, чтобы систематизировать различные реакции в этом эксперименте
Для использования с студенческим листом А (включает руководство по расчетам)
- Заполните луночный планшет (см.
 схему) растворами, как указано в таблице ниже. Всего в каждой лунке должно быть 40 капель.
схему) растворами, как указано в таблице ниже. Всего в каждой лунке должно быть 40 капель.
| Well # | A1 | A2 | A3 | A4 | A5 | A6 |
|---|---|---|---|---|---|---|
| Drops of 0.50 mol dm –3 copper nitrate solution | 8 | 22 | 24 | 10 | 12 | 14 |
| Капли воды | 32 | 30 | 28 | 26 | 24 | 22 |
| скважина # | C1 | C2 | C3 | C4 | C5 | C6 | 16 | 18 | 20 | 26 | 28 | 30 |
|---|---|---|---|---|---|---|
| Капли воды | 20 | 18 | 16 | 14 | 12 | 10 |
- Добавьте 40 капель раствора латуни в лунку B3 (см.
 схему).
схему). - Сравните интенсивность цвета вашего латунного раствора с лунками вокруг него. Ячейка, которая соответствует интенсивности цвета вашего раствора латуни, представляет собой концентрацию меди в вашем растворе латуни – например, если лунка A6 соответствует цвету вашего раствора латуни, тогда концентрация меди будет 0,50 × 18/40 моль дм -3 .
Для использования с студенческим листом B (без руководства по расчетам)
- Заполните луночный планшет (см. схему) растворами, как указано в таблице ниже. Всего в каждой лунке должно быть 40 капель.
| Well # | A1 | A2 | A3 | A4 | A5 | A6 |
|---|---|---|---|---|---|---|
| Drops of 0.50 mol dm –3 copper nitrate solution | 10 | 12 | 14 | 16 | 18 | 20 |
| Капли воды | 30 | 28 | 26 | 24 | 22 | 20 |
| Well # | C1 | C2 | C3 | C4 | C5 | C6 |
|---|---|---|---|---|---|---|
Drops of 0. 50 mol dm –3 copper nitrate solution 50 mol dm –3 copper nitrate solution | 22 | 24 | 26 | 28 | 30 | 32 |
| Капли воды | 18 | 16 | 14 | 12 | 10 | 8 |
- Добавьте 40 капель раствора латуни в лунку B3 (см. схему). Сравните интенсивность цвета вашего раствора латуни с лунками вокруг него.
- По вашим результатам рассчитайте содержание меди в латуни, выразив ответ в виде процентов.
Руководство по расчетам
- Рассчитать количество молей меди в 10 см 3 (объем раствора латуни).
- Умножьте значение, полученное в (1), на относительную атомную массу меди (63,5), чтобы получить массу меди в растворе латуни.
- Разделить на массу использованной латуни и выразить результат в процентах.
Вопросы учащихся
- Влияет ли цинк каким-либо образом на этот анализ? Обоснуйте свой ответ.

- Можете ли вы предложить способ повысить точность этого эксперимента?
Учебные заметки
Наблюдения
Латунь быстро растворяется, образуя раствор голубого цвета. Этот цвет обусловлен наличием меди в латуни. (Эта часть эксперимента должна проводиться в вытяжном шкафу, так как образуется диоксид азота.)
Интенсивность окраски этого раствора должна находиться в диапазоне интенсивностей окраски стандартных растворов. Учащиеся находят ближайшее цветовое соответствие, а затем вычисляют содержание меди в латуни.
Обсуждение
Большая часть латуни содержит около 60% меди (остальное — цинк). Латунь представляет собой интересный предмет для обсуждения структуры металлов и сплавов. Металлическая медь имеет гранецентрированную кубическую структуру (ГЦК), тогда как структура цинка является гексагональной. Когда цинк добавляется к меди, он замещается в решетке, образуя искаженную ГЦК-структуру (атомы цинка примерно на 13 % больше, чем у меди). Эту искаженную структуру трудно деформировать, что объясняет большую прочность латуни по сравнению с чистой медью.
Эту искаженную структуру трудно деформировать, что объясняет большую прочность латуни по сравнению с чистой медью.
Когда содержание цинка достигает примерно 36%, появляется новая объемно-центрированная кубическая фаза, и прочность заметно увеличивается, хотя пластичность снижается. Оптимальные свойства прочности и пластичности для большинства применений латуни достигаются при содержании цинка около 40%.
Дополнительная информация
Этот ресурс является частью нашей коллекции «Микромасштабная химия», в которой собраны эксперименты меньшего масштаба, чтобы заинтересовать ваших учащихся и изучить ключевые химические идеи. Ресурсы первоначально появились в книге Химия на микроуровне: эксперименты в миниатюре , опубликовано Королевским химическим обществом в 1998 г.
Международной исследовательской группе удалось получить новое представление о химических свойствах сверхтяжелого элемента флеровия — элемента 114 — на ускорительной установке GSI Helmholtzzentrum für Schwerionenforschung в Дармштадте. Измерения показывают, что флеровий является самым летучим металлом в периодической таблице. Таким образом, флеровий является самым тяжелым химически изученным элементом периодической таблицы. С результатами, опубликованными в журнале Frontiers in Chemistry , GSI подтверждает свои лидирующие позиции в области изучения химии сверхтяжелых элементов и открывает новые перспективы для строящейся международной установки FAIR (Facility for Antiproton and Ion Research).
Измерения показывают, что флеровий является самым летучим металлом в периодической таблице. Таким образом, флеровий является самым тяжелым химически изученным элементом периодической таблицы. С результатами, опубликованными в журнале Frontiers in Chemistry , GSI подтверждает свои лидирующие позиции в области изучения химии сверхтяжелых элементов и открывает новые перспективы для строящейся международной установки FAIR (Facility for Antiproton and Ion Research).
Под руководством групп из Дармштадта и Майнца два самых долгоживущих изотопа флеровия, известных в настоящее время, флеровий-288 и флеровий-289, были получены с использованием ускорительного оборудования GSI/FAIR и химически исследованы на экспериментальной установке TASCA. В периодической таблице флеровий стоит ниже тяжелого металла свинца. Однако ранние предсказания постулировали, что релятивистские эффекты высокого заряда в ядре сверхтяжелого элемента на его валентных электронах приведут к поведению, подобному благородному газу, в то время как более поздние предсказания скорее предполагали слабометаллическое поведение. Два ранее проведенных химических эксперимента, один из них в GSI в Дармштадте в 2009 г., привели к противоречивым толкованиям. В то время как три атома, наблюдаемые в первом эксперименте, использовались для вывода о поведении, подобном благородному газу, данные, полученные в GSI, указывали на металлический характер на основе двух атомов. Два эксперимента не смогли четко установить характер. Новые результаты показывают, что, как и ожидалось, флеровий инертен, но при подходящих условиях способен образовывать более прочные химические связи, чем инертные газы. Следовательно, флеровий является самым летучим металлом в периодической таблице.
Два ранее проведенных химических эксперимента, один из них в GSI в Дармштадте в 2009 г., привели к противоречивым толкованиям. В то время как три атома, наблюдаемые в первом эксперименте, использовались для вывода о поведении, подобном благородному газу, данные, полученные в GSI, указывали на металлический характер на основе двух атомов. Два эксперимента не смогли четко установить характер. Новые результаты показывают, что, как и ожидалось, флеровий инертен, но при подходящих условиях способен образовывать более прочные химические связи, чем инертные газы. Следовательно, флеровий является самым летучим металлом в периодической таблице.
Таким образом, флеровий является самым тяжелым химическим элементом, свойства которого были изучены экспериментально. Определением химических свойств GSI/FAIR подтверждает свое лидирующее положение в исследованиях сверхтяжелых элементов. «Изучение границ периодической таблицы было основой исследовательской программы GSI с самого начала и будет таковой в FAIR в будущем. Тот факт, что несколько атомов уже можно использовать для изучения первых фундаментальных химических свойств, дает указание на то, как будут вести себя большие количества этих веществ, увлекательно и возможно благодаря мощному ускорителю и опыту всемирного сотрудничества», — уточняет профессор Паоло Джубеллино, научный управляющий директор GSI и FAIR. «С FAIR мы переносим вселенную в лабораторию и исследуем пределы материи, а также химических элементов».
Тот факт, что несколько атомов уже можно использовать для изучения первых фундаментальных химических свойств, дает указание на то, как будут вести себя большие количества этих веществ, увлекательно и возможно благодаря мощному ускорителю и опыту всемирного сотрудничества», — уточняет профессор Паоло Джубеллино, научный управляющий директор GSI и FAIR. «С FAIR мы переносим вселенную в лабораторию и исследуем пределы материи, а также химических элементов».
Шесть недель экспериментов
Эксперименты, проведенные в GSI/FAIR для выяснения химической природы флеровия, длились в общей сложности шесть недель. С этой целью четыре триллиона ионов кальция-48 каждую секунду ускорялись до десяти процентов скорости света с помощью линейного ускорителя GSI UNILAC и обстреливались мишенью, содержащей плутоний-244, что приводило к образованию нескольких атомов флеровия в день.
Образовавшиеся атомы флеровия отскочили от мишени в газонаполненный сепаратор TASCA.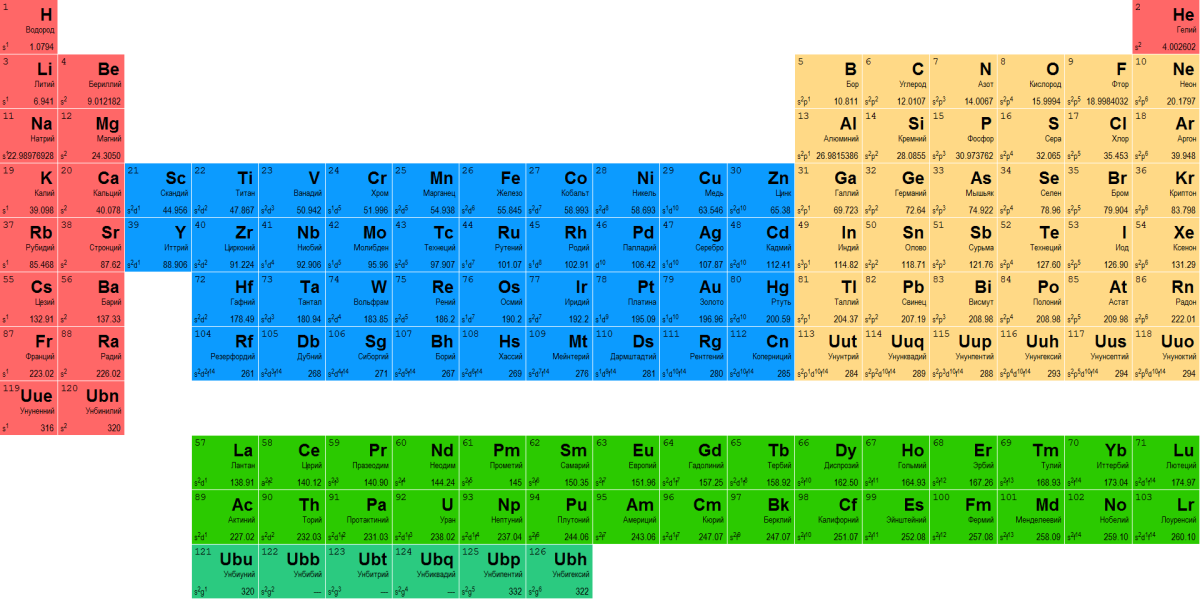 В его магнитном поле образуются изотопы флеровий-288 и флеровий-289., которые имеют время жизни порядка секунды, были отделены от интенсивного пучка ионов кальция и от побочных продуктов ядерной реакции. Они проникли через тонкую пленку и, таким образом, попали в химический аппарат, где были остановлены в газовой смеси гелия и аргона. Эта газовая смесь вытесняла атомы в аппарат газовой хроматографии COMPACT, где они впервые соприкасались с поверхностями оксида кремния. Если связь с оксидом кремния была слишком слабой, атомы переносились дальше, по золотым поверхностям — сначала по тем, которые хранились при комнатной температуре, а затем по все более холодным, вплоть до примерно -160 °C. Поверхности наносились в виде тонкого покрытия на специальные детекторы ядерного излучения, которые регистрировали отдельные атомы путем регистрации радиоактивного распада с пространственным разрешением. Поскольку продукты распада подвергаются дальнейшему радиоактивному распаду после короткого времени жизни, каждый атом оставляет характерную сигнатуру нескольких событий, из которых можно однозначно сделать вывод о присутствии атома флеровия.
В его магнитном поле образуются изотопы флеровий-288 и флеровий-289., которые имеют время жизни порядка секунды, были отделены от интенсивного пучка ионов кальция и от побочных продуктов ядерной реакции. Они проникли через тонкую пленку и, таким образом, попали в химический аппарат, где были остановлены в газовой смеси гелия и аргона. Эта газовая смесь вытесняла атомы в аппарат газовой хроматографии COMPACT, где они впервые соприкасались с поверхностями оксида кремния. Если связь с оксидом кремния была слишком слабой, атомы переносились дальше, по золотым поверхностям — сначала по тем, которые хранились при комнатной температуре, а затем по все более холодным, вплоть до примерно -160 °C. Поверхности наносились в виде тонкого покрытия на специальные детекторы ядерного излучения, которые регистрировали отдельные атомы путем регистрации радиоактивного распада с пространственным разрешением. Поскольку продукты распада подвергаются дальнейшему радиоактивному распаду после короткого времени жизни, каждый атом оставляет характерную сигнатуру нескольких событий, из которых можно однозначно сделать вывод о присутствии атома флеровия.
Один атом в неделю для химии
«Благодаря сочетанию сепаратора TASCA, химического разделения и обнаружения радиоактивного распада, а также технического развития аппарата газовой хроматографии с момента первого эксперимента мы нам удалось повысить эффективность и сократить время, необходимое для химического разделения, до такой степени, что мы могли наблюдать один атом флеровия каждую неделю», — объясняет д-р Александр Якушев из GSI/FAIR, представитель международной экспериментальной коллаборации.
При анализе данных было обнаружено шесть таких цепочек распада. Поскольку установка аналогична установке первого эксперимента GSI, вновь полученные данные можно было объединить с двумя атомами, наблюдаемыми в то время, и проанализировать их вместе. Ни одна из цепочек распада не появилась в пределах диапазона детектора с покрытием из оксида кремния, что указывает на то, что флеровий не образует существенной связи с оксидом кремния. Вместо этого все они были перенесены вместе с газом в покрытую золотом часть аппарата менее чем за десятую долю секунды. Восемь событий образовали две зоны: первую в области поверхности золота при комнатной температуре, а вторую в более поздней части хроматографа при настолько низких температурах, что золото покрывалось очень тонким слоем льда, так что происходила адсорбция. на льду.
Восемь событий образовали две зоны: первую в области поверхности золота при комнатной температуре, а вторую в более поздней части хроматографа при настолько низких температурах, что золото покрывалось очень тонким слоем льда, так что происходила адсорбция. на льду.
Из экспериментов с атомами свинца, ртути и радона, которые служили представителями тяжелых металлов, слабореакционноспособных металлов, а также благородных газов, было известно, что свинец образует прочную связь с оксидом кремния, а ртуть достигает детектора золота. Радон даже пролетает над первой частью детектора золота при комнатной температуре и лишь частично задерживается при самых низких температурах. Результаты флеровиума можно сравнить с таким поведением.
По-видимому, наблюдались два типа взаимодействия вида флеровия с поверхностью золота. Осаждение на золоте при комнатной температуре указывает на образование относительно прочной химической связи, которой нет в благородных газах. С другой стороны, некоторые атомы, по-видимому, никогда не имели возможности образовать такие связи и переносились на большие расстояния по поверхности золота вплоть до самых низких температур. Этот диапазон детектора представляет собой ловушку для всех элементарных частиц. Такое сложное поведение можно объяснить морфологией поверхности золота: она состоит из небольших кластеров золота, на границах которых находятся очень реактивные участки, по-видимому, позволяющие флеровию связываться. Тот факт, что часть атомов флеровия смогла достичь холодной области, указывает на то, что только атомы, попавшие в такие места, образовывали связь, в отличие от ртути, которая в любом случае сохранялась на золоте. Таким образом, химическая активность флеровия слабее, чем у летучего металла ртути. Имеющиеся данные не могут полностью исключить возможность того, что первая зона осаждения на золоте при комнатной температуре связана с образованием молекул флеровия. Однако из этой гипотезы также следует, что флеровий химически более активен, чем элемент благородного газа.
Этот диапазон детектора представляет собой ловушку для всех элементарных частиц. Такое сложное поведение можно объяснить морфологией поверхности золота: она состоит из небольших кластеров золота, на границах которых находятся очень реактивные участки, по-видимому, позволяющие флеровию связываться. Тот факт, что часть атомов флеровия смогла достичь холодной области, указывает на то, что только атомы, попавшие в такие места, образовывали связь, в отличие от ртути, которая в любом случае сохранялась на золоте. Таким образом, химическая активность флеровия слабее, чем у летучего металла ртути. Имеющиеся данные не могут полностью исключить возможность того, что первая зона осаждения на золоте при комнатной температуре связана с образованием молекул флеровия. Однако из этой гипотезы также следует, что флеровий химически более активен, чем элемент благородного газа.
Международное и междисциплинарное сотрудничество как ключ к пониманию
Экзотический плутониевый мишенный материал для производства флеровия был частично предоставлен Ливерморской национальной лабораторией Лоуренса (LLNL), США. На площадке TRIGA химического факультета Университета имени Иоганна Гутенберга в Майнце (JGU) материал был электролитически нанесен на тонкую титановую фольгу, изготовленную в GSI/FAIR. «В мире не так много этого материала, и нам повезло, что мы смогли использовать его для этих экспериментов, которые иначе были бы невозможны», — сказал д-р Дон Шонесси, руководитель отдела ядерных и химических наук в ЛЛНЛ. «Это международное сотрудничество объединяет навыки и опыт со всего мира для решения сложных научных проблем и ответов на давние вопросы, такие как химические свойства флеровия».
На площадке TRIGA химического факультета Университета имени Иоганна Гутенберга в Майнце (JGU) материал был электролитически нанесен на тонкую титановую фольгу, изготовленную в GSI/FAIR. «В мире не так много этого материала, и нам повезло, что мы смогли использовать его для этих экспериментов, которые иначе были бы невозможны», — сказал д-р Дон Шонесси, руководитель отдела ядерных и химических наук в ЛЛНЛ. «Это международное сотрудничество объединяет навыки и опыт со всего мира для решения сложных научных проблем и ответов на давние вопросы, такие как химические свойства флеровия».
«Наш эксперимент с ускорителем был дополнен подробным исследованием поверхности детектора в сотрудничестве с несколькими отделами GSI, а также с химическим факультетом и Институтом физики JGU. Это оказалось ключом к пониманию химического характера флеровия. «В результате данные двух предыдущих экспериментов теперь понятны и совместимы с нашими новыми выводами», — говорит Кристоф Дюльманн, профессор ядерной химии в JGU и руководитель исследовательской группы в GSI и Институте Гельмгольца в Майнце (HIM).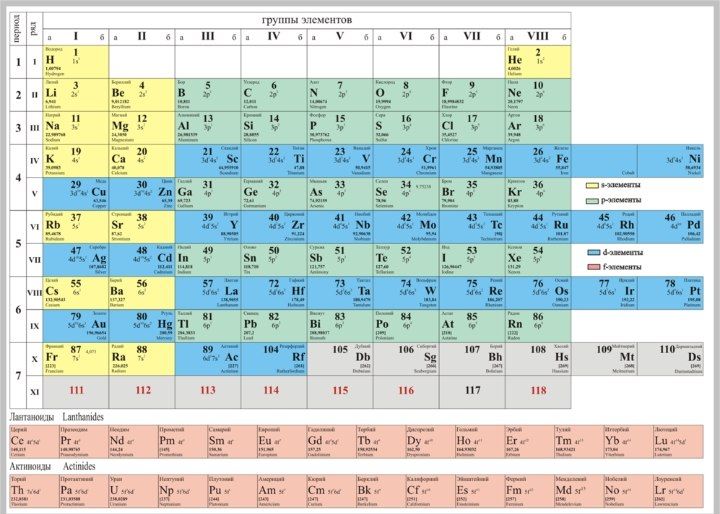 , результат сотрудничества GSI и JGU.
, результат сотрудничества GSI и JGU.
Как релятивистские эффекты влияют на его соседей, элементы нихоний (элемент 113) и московий (элемент 115), которые также были официально признаны только в последние годы, является предметом последующих экспериментов. Исходные данные уже получены в рамках программы FAIR Phase 0 в GSI. Кроме того, исследователи ожидают, что существуют значительно более стабильные изотопы флеровия, но они еще не обнаружены. Однако теперь исследователи уже знают, что они могут рассчитывать найти металлический элемент.
Помимо GSI/FAIR и JGU, HIM, Ливерпульского университета (Великобритания), Лундского университета (Швеция), Университета Ювяскюля (Финляндия), Университета Осло (Норвегия), Института электроники технологий (Польша), Ливерморской национальной лаборатории им. Лоуренса (США), Института ядерной физики Саха и Индийского технологического института в Рурки (Индия), Объединенного агентства по атомной энергии и Исследовательского центра RIKEN (Япония), а также Австралийского национального Университет (Австралия) были привлечены к эксперименту.