Какая теплопроводность у серы и меди: электропроводность :медь;сера,теплопроводность:медь;сера,плотность:медь сера; — Спрашивалка
Содержание
Не медью единой? Размышления Алексея Неаронова о влиянии меди в дистилляции…
«Англичане ружья кирпичом не чистят» (с)
Лесков Н.С., «Левша»
Недавно на встрече с Eddie Russell, мастер-дистиллером Wild Turkey, поднимался вопрос из чего изготовлено оборудование на дистиллерии. Эдди сказал, что всё — и колонна, и даблер — целиком медные, и его отец, легендарный Джимми Рассел, говорил, что на меди виски получается лучше и вкуснее, хотя, конечно, понятно, что за этим стоят определённые химические процессы. Как виски-энтузиаст, я часто езжу по винокурням, и действительно там меня окружает практически исключительно медь. Поэтому перегонные кубы из меди для меня совершенно естественны, я другого оборудования и не встречал. Нет, конечно, в какой-нибудь итальянской деревне до сих пор могут гнать граппу из виноградного жмыха, грубо говоря, в обычной кастрюле, но если говорить о тех, кто производит дистилляты не исключительно для потребления узким деревенским кругом, а претендует на то, чтобы его напитки оценивались другими, в выдержанном или в невыдержанном виде, то там обязательно присутсвует медь, в том числе и на ректификационных колоннах, даже на больших заводах, не говоря уже о микродистилериях.
Самый большой в Северной Америке завод Hiram Walker в Windsor, Канада
Микродистиллерия Stillwaters в Торонто, Канада.
Конечно, я тоже не раз задумывался о том, почему именно медь используется для дистилляции. Может быть, это просто историческое наследие, с тех времён, когда медь была наиболее удобным для ковки непростых форм металлом, одновременно обладающим замечательной теплопроводностью и износостойкостью? Но сейчас это уже не является однозначным преимуществом. Давайте же посмотрим, какие химические процессы делают медь полезной для дистилляции.
1. Сернистость
В процессе брожения в ходе дрожжевых метаболических реакций происходит преобразование соединений, содержащих серу. Сернистые соединения неизбежно остаются в браге, идущей на перегонку. Откуда сера, неорганическое соединение, попадает в брагу? Есть несколько путей. Один – в растворённом виде (ионы сульфатов) сера попадает в затор с водой, используемой в процессе производства. Второй – сера приходит с самим ячменём, который может обрабатываться пестицидами с содержанием серы. Сернистые соединения есть и в сами дрожжах в каких-то мизерных количествах, но, что более важно, достоверно известно, что количество сернистых соединений в браге значительно меняется в зависимости от того, какие дрожжи используются для сбраживания сусла, т.е. разные дрожжи с разной активностью метаболизируют сернистые соединения. Вот пример использования разных штаммов при брожении вина:
Второй – сера приходит с самим ячменём, который может обрабатываться пестицидами с содержанием серы. Сернистые соединения есть и в сами дрожжах в каких-то мизерных количествах, но, что более важно, достоверно известно, что количество сернистых соединений в браге значительно меняется в зависимости от того, какие дрожжи используются для сбраживания сусла, т.е. разные дрожжи с разной активностью метаболизируют сернистые соединения. Вот пример использования разных штаммов при брожении вина:
В любом случае, в браге сернистые соединения имеют те формы, которые могут ощущаться обонянием, а порог чувствительности для серы у человеческого обоняния очень низок, там речь идёт о количествах в ppb (части на миллиард). Запахи эти идентифицируются именно как серные (неожиданно, да?), можно привести в пример запах горелой спички, а также как «мясные» — ароматы свежего и/или иногда чуть «задохнувшегося» мяса; гнилостные запахи; ароматы варёных овощей.
Некоторый объём серных соединений, принимая форму сероводорода, уносится из бражного чана вместе с углекислым газом, всё остальное попадает в аламбик. Насколько контакт с медью может через образование сульфатов связать серу и очистить дистиллят от серных запахов? Обратимся к тем экспериментам, которые проводили учёные из Шотландского Института Исследований Виски.
Насколько контакт с медью может через образование сульфатов связать серу и очистить дистиллят от серных запахов? Обратимся к тем экспериментам, которые проводили учёные из Шотландского Института Исследований Виски.
Известный производитель медных кубов, компания Forsyths, изготовила для этих экспериментов два вида полностью аналогичного оборудования, бражные и спиртовые кубы небольшого размера, одну пару из меди, другую из нержавеющей стали.
В итоге, появилась возможность производить замену любой секции (разделение на части пронумеровано от 1 до 6 на фотографии выше) в ходе проведения двойной дистилляции на секцию из другого металла – при работе на нержавеющей стали вставлять секции из меди и наоборот. Далее полученный дистиллят (а делалось по три итерации в каждой сборке) предоставлялся оценочной панели для проверки на наличие серных или «мясных» ароматов. Давайте посмотрим на то, что из этого вышло.
Эксперимент на оборудовании из нержавеющей стали, для сравнения дан результат целиком на медном оборудовании («С») и целиком на оборудовании из нержавейки («S»).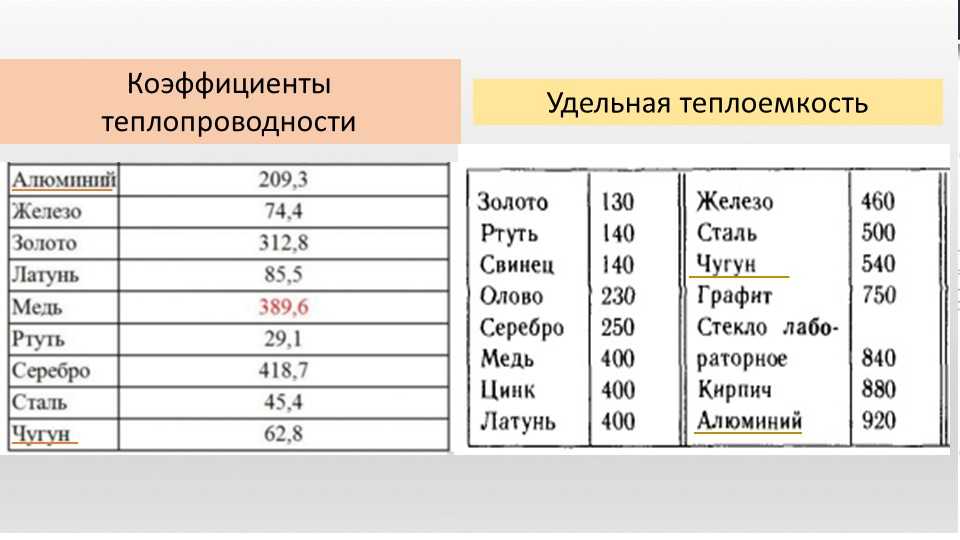 S1 – замена секции 1 на медную, S2 – замена секции 2 на медную, и так далее. Чёрный столбик – аромат серы, белый столбик – «мясной» запах.
S1 – замена секции 1 на медную, S2 – замена секции 2 на медную, и так далее. Чёрный столбик – аромат серы, белый столбик – «мясной» запах.
Как видно из графика, общий уровень сернистых соединений, влияющих на ароматические составляющие, при замене одной из секций из нержавейки на медную, значительно снижается, при этом наименее «влиятельной» в этом плане является последняя, 6-я секция, т.е. змеевик или кожухотрубный конденсатор, если говорить о виски-производстве. Таким образом, можно сделать вывод о том, что контакт с медью в ходе дистилляции крайне важен вообще, а рефлюкс на спиртовых кубах много важнее контакта с медью при конденсации паров. Что же касается кубов бражных, то там, несомненно, процесс конденсации вносит больше лепты в нейтрализацию серы.
Теперь посмотрим на эксперимент на оборудовании из меди. Также для сравнения дан результат целиком на медном оборудовании («С») и целиком на оборудовании из нержавейки («S»). С1 – замена секции 1 на секцию из нержавейки, С2 – замена секции 2 на нержавейку, и так далее.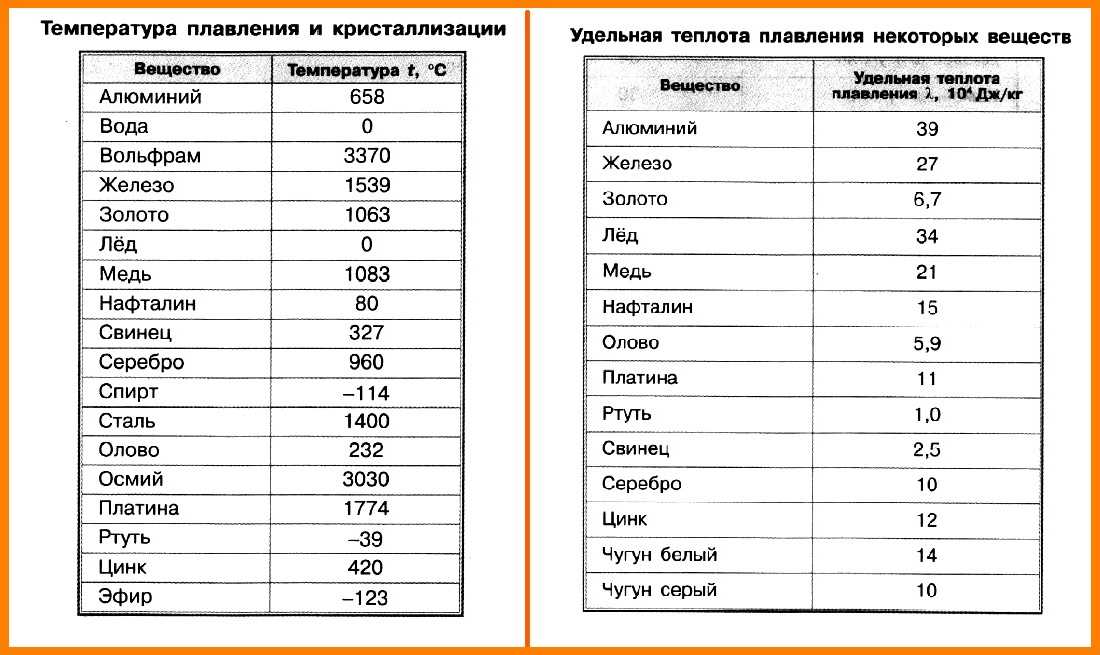 Чёрный столбик – аромат серы, белый столбик – «мясной» запах.
Чёрный столбик – аромат серы, белый столбик – «мясной» запах.
Видно, что уже общий уровень сернистости заметно ниже, чем на оборудовании из стали с вкраплениями меди. И видно, что замена последней секции, конденсатора паров, на стальную, даёт самый заметный всплеск сернистости в дистилляте.
Если отступить чуть в сторону, то этот момент представляет особенный интерес для споров о влиянии массовой замены змеевиков на кожухотрубные конденсаторы на шотландских винокурнях с конца 50-х по конец 60-х годов. Если посмотреть на графики, то видно, что, с одной стороны, при отсутствии контакта с медью во всём процессе, установка медного конденсатора ситуацию не исправит совершенно. С другой стороны, если убрать в «медном» процессе последний контакт, то это заметно повлияет на сернистость дистиллята. Но в случае замены змеевиков на конденсаторы мы говорим не о полном исключении контакта, так что, возможно, причины сернистости для некоторых винокурен надо искать не только в змеевиках, но и в других деталях их технологического процесса.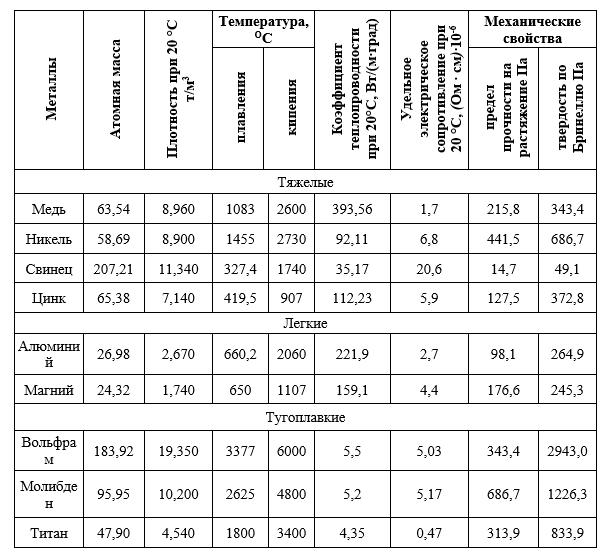
Кстати, этот эффект в своей работе используют и «скрытые гиганты» индустрии, новые дистиллерии Roseisle (10 миллионов литров, Diageo) и Ailsa Bay (12 миллионов литров, William Grant & Sons). При проектировании этих дистиллерий была поставлена задача, по некоторому подобию самодостаточных японцев, получать несколько видов дистиллятов. И если японцы идут через использование кубов различной формы, то шотландцы так далеко зайти не решились, и двинулись по пути работы с конденсаторами из нержавеющей стали. Посмотрите на фото цеха на Roseisle:
Обратите внимание, например, на второй куб в дальнем ряду. Это бражный куб, и у этого куба два конденсатора – один из меди, другой из стали. При необходимости изменить характеристики дистиллята, сбор паров осуществляется в тот или иной конденсатор. То же касается и спиртовых кубов, вот их фотография с другого ракурса.
На ней видно, что второй справа куб также имеет два конденсатора из разных материалов. Посмотрим на Ailsa Bay:
Здесь не наблюдается задвоенных конденсаторов, но видно, но есть кубы, работающие с оборудованием из нержавейки.
Итак, возвращаясь к сути вопроса — использование меди, при прочих равных, меняет ароматическое восприятие дистиллята следующим образом:
Производители виски не хотят плохих ароматов в своём дистилляте, вот и используют медь.
2. Этерификация
Идём далее. Этерификация – процесс образования эфиров при взаимодействии спиртов и кислот. Наличие большего количества эфиров насыщают и расширяют органолептические характеристики виски. Проводились исследования, которые показали, что контакт с медью значительно увеличивает количество эфиров в дистилляте.
Вот таблица результатов экспериментов на оборудовании из стекла, в ходе которых при одной выгонке контакт с медью отсутствовал, а при другой выгонке присутствовал. После замерялось количество эфиров в дистилляте.
Второй столбец показывает содержание эфиров в граммах на 100 литров алкоголя в дистилляте, произведённом без контакта с медью, третий столбец – при контакте с медью, последний столбец – процент роста содержания.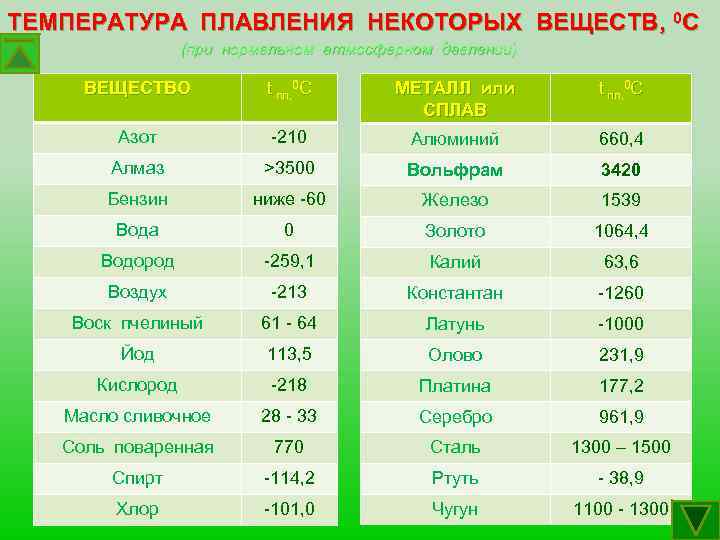
Как мы видим, количество эфиров от контакта с медью увеличилось от 1,5 раз до 3,6 раз. Для справки посмотрим, какие ароматы несут некоторые из этих эфиров:
Винокуры хотят больше фруктовых ароматов в виски, вот и используют медное оборудование.
3. Альдегидность
Ну и, наконец, альдегиды, органические соединения, которые являются нежелательными для употребления и, по большей части, обладают негативно воспринимаемыми резкими ароматами, придают дистилляту колкость. Образуются во время брожения в результате взаимодействия дрожжей, аминокислот и углеводов. Образование альдегидов во время брожения в своё время было прослежено японским учёным Масакадзу Окада:
В браге много уксусного альдегида, есть пропионовый, кротоновый, может быть и формальдегид.
Несмотря на то, что конкретных исследований по количеству альдегидов в дистиллятах в зависимости от наличия или отсутствия контакта с медью найти не удалось, в разных источниках можно встретить замечания, что медь способствует окислению альдегидов, чем снижает их количество в продукте.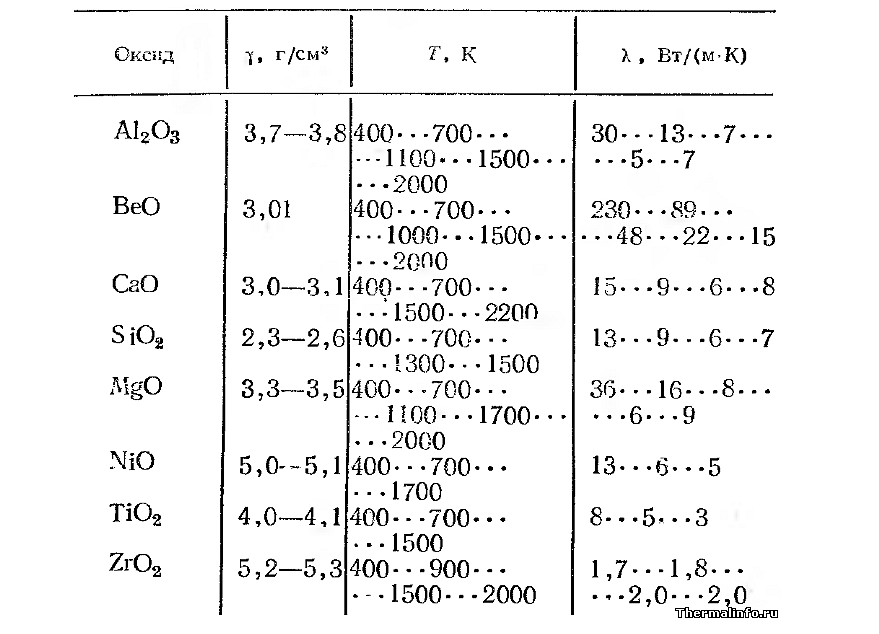
Дистиллеры не желают резких запахов и колкости в виски, поэтому предпочитают медь.
Glendalough Distillery, Ирландия
Итак, подведём итоги. Работа на медном оборудовании:
- сокращает количество сернистых соединений в дистилляте, уменьшая количество нежелательных запахов;
- увеличивает количество эфиров в продукте, увеличивая объём приятных ароматов;
- способствует уменьшению альдегидов, сокращая резкость ароматов и колкость продукта.
Поэтому винокуры любят медь. Люблю её и я, особенно тёплую. Спасибо ей за виски!
Алексей Неаронов
Медные колонны на Slane Distillery, Ирландия
Список использованной литературы
- Barry Harriston, Olivier Fagnen, Frances Jack, James Brosnan, The Impact of Copper in Different Parts of Malt Whisky Pot Stills on New Make Spirit Composition and Aroma, Scotch Whisky Research Institute, Edinburgh, 2011
- Maik Werner, Doris Rauhut, Philippe Cottereau, Yeasts and Natural Production of Sulphites, Internet Journal of Enology and Viticulture, 12/3, 2009
- Masakazu Yamada, On the Origin of Aldehydes in Fermentation Products, Journal of the Agricultural Chemical Society of Japan, 1928
- T.
 Yang, The impact Of Whisky Blend Matrices On The Sensory Perception Of Peaty Flavours, International Centre for Brewing and Distilling, Heriot-Watt University, Edinburgh, September 2014
Yang, The impact Of Whisky Blend Matrices On The Sensory Perception Of Peaty Flavours, International Centre for Brewing and Distilling, Heriot-Watt University, Edinburgh, September 2014
Сварка меди и медных сплавов
Сварка меди и ее сплавов
Свариваемость меди. Медь сваривается плохо из-за ее высокой теплопроводностью и повышенной склонности к образованию трещин при сварке.
Теплопроводность меди при комнатной температуре в шесть раз больше теплопроводности технического железа, поэтому сварки меди и ее сплавов должна производиться с увеличенной погонной тепловой энергией, а во многих случаях с предварительным и сопутствующим подогревом основного металла.
При переходе из твердого состояния в жидкое медь выделяет большое количество теплоты (скрытая теплота плавления), поэтому сварочная ванна поддерживается в жидком состоянии более длительное время, чем при сварке стали. Повышенная водопровиднисть меди затрудняет ее сварки в вертикальном, горизонтальном и особенно в потолочном положениях.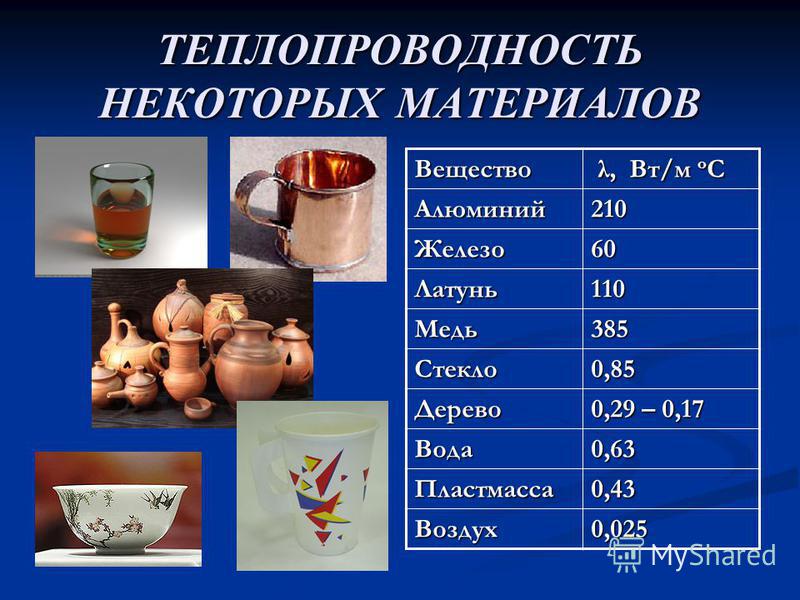
Водород в присутствии кислорода делает негативное воздействие на свойства меди. Водород проникает в медь при повышенных температурах сварки, реагирует с кислородом оксида меди (Сu2О + 2Н Н2О + 2Сu), образует водяной пар, стремясь расшириться, приводит к появлению мелких трещин. Это явление при сварке меди называют «водородной болезнью». Если сваривать медь покрытыми медными электродами без подогрева свариваемого, (с быстрым охлаждением), то возникают горячие трещины.
Однако при сварке с подогревом, создает условия медленного охлаждения, водяной пар в большинстве случаев к затвердевания металла выходит наружу; небольшая часть водяного пара остается между слоем сварочного шлака и поверхностью металла шва. В результате этого поверхность металла шва после удаления еще горячего шлака становится неровной с мелкими углублениями, что можно избежать при очень медленном охлаждении шва и шлака.
Чем больше содержится кислорода в меди, сваривается, тем значительнее оказывается «водородная болезнь».
Примеси в меди мышьяка, свинца, сурьмы, висмута и серы затрудняют сварки. Они практически не растворяются в меди, не образуют с ней легкоплавкие химические соединения, что, находясь в свободном состоянии, располагаются по границам зерен и ослабляют межатомные связи. В результате под действием усадочной растягивающей силы, в процессе охлаждения сварного соединения образуются горячие трещины. Поэтому содержание каждой из вредных примесей (кислорода, висмута, свинца в меди и в сварочных материалах) не должно быть более 0,03%, а для особо ответственных сварных изделий — 0,01%.
Коэффициент линейного расширения меди больше коэффициента линейного расширения железа, в связи с чем сварочные деформации при сварке конструкций из меди и ее сплавов не более, чем при сварке сталей.
Основные виды сварки меди плавлением: дуговая покрытыми электродами; дуговая порошковой проволокой, дуговая в газе, автоматическая дуговая под флюсом, плазменная сварка, газовая сварка и др..
Сварка меди покрытыми металлическими электродами дает удовлетворительное качество в случаях, если медь сваривается, содержит кислорода не более 0,01%. При содержании в меди кислорода в количествах более 0,03% сварные соединения имеют низкие механические свойства.
При содержании в меди кислорода в количествах более 0,03% сварные соединения имеют низкие механические свойства.
Для сварки меди применяют покрытые электроды марок К-100 (завод «Комсомолец»), ОМЗ-1 (опытный Московский завод) и др.. Состав электрода марки К-100 следующий: стержень из металла марки М1, покрытие — плавиковый шпат 12,5%, полевой шпат-15%, ферромарганец Мn1, Мn2 — 47,5%, кремнистая медь (73 — 75% меди , 23 — 25% кремния и другой примеси) — 25%.
Сварка ведут в нижнем положении постоянным током обратной полярности. При сварке листов толщиной более 6 мм требуется предварительный подогрев основного металла до 300 — 400 ° С.
Газовая сварка медных листов толщиной до 10 мм выполняется пламенем мощностью 150 дм3 ацетилена /ч на 1 мм толщины металла. Листы
большей толщины сваривают пламенем из расчета 200 дм 3 на 1 мм толщины металла. Сварка лучше делать одновременно двумя горелками с двух сторон восстановительным пламенем, для того чтобы не допускать образования в сварочной ванне оксидов меди. Сварки меди на вуглевоживаючим пламенем не допускаются, так как при этом образуются поры и трещины в шве вследствие образования СО2 и Н2О по реакциям: С + Сn2О-+ С2 + 2Сn; Н2 + Сn2ОН2О + 2Сn.
Сварки меди на вуглевоживаючим пламенем не допускаются, так как при этом образуются поры и трещины в шве вследствие образования СО2 и Н2О по реакциям: С + Сn2О-+ С2 + 2Сn; Н2 + Сn2ОН2О + 2Сn.
Шов заполняется за один слой. Многослойное газовая сварка вызывает перегрев металла и трещины в швах. Во избежание перегрева меди, сварки следует вести с высокими скоростями нагрева и охлаждения сварных соединений.
Металл толщиной до 2 мм сваривают встык без присадочного материала, при толщине 3 мм и более применяют скос кромок с углом обработки 90 ° и притуплением 1,5 — 2 мм. Толстые медные листы сваривают встык с разделкой кромок в вертикальном положении одновременно с двух сторон двумя горелками. Присадочный проволокой служит чистая медь или медь с содержанием раскислителей: фосфора — до 0,2% и кремния — до 0,15 — 0,30%. Проволока подбирают диаметрами от 1,5 до 8 мм в зависимости от толщины листов, свариваемых; проволока диаметром 8 мм употребляется для листов толщиной 15 мм и более.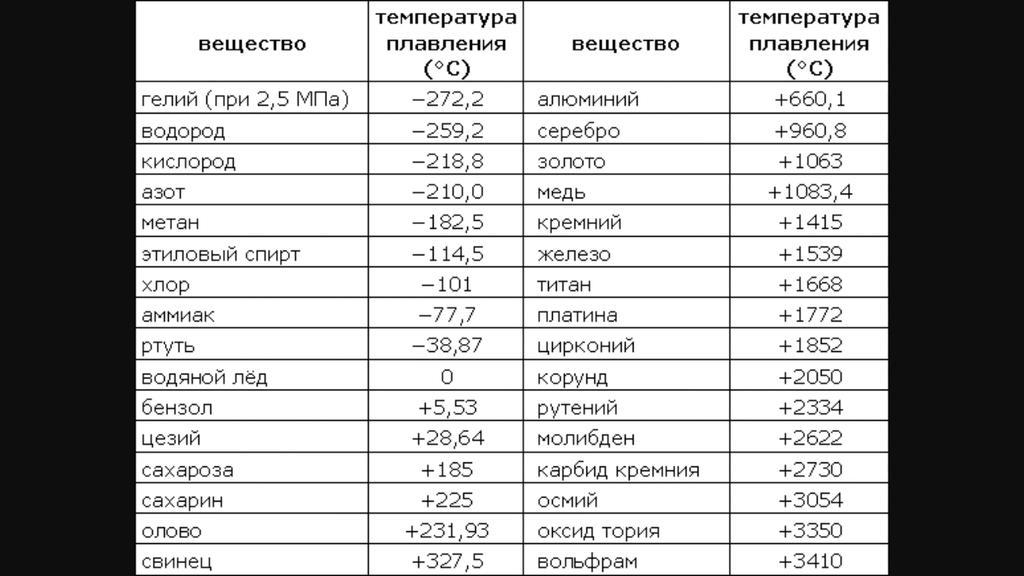
Газовая сварка меди выполняется с флюсами, состоящие в основном из бури.
Высокое качество сварного соединения получают, применяя газофлюсового сварки, при которой порошкообразный флюс засасывается ацетиленом и подается непосредственно в пламя горелки от специальной установки КГФ-2-66.
Использование проковки металла шва (лучше околошовной металла) еще более улучшает механические свойства сварных соединений.
Сварка латуни. Латунь представляет собой сплав меди с цинком, температура плавления латуни 800-1000 С.
При дуговой сварке из латуни интенсивно испаряется цинк; расплавленный металл поглощает водород не успевает выделиться при затвердевании жидкого металла в сварочной ванне, в результате чего в шве образуются газовые поры. Водород попадает в сварочную ванну из покрытия, флюса или воздуха.
Сварка латуней покрытыми электродами находит ограниченное применение, в основном для исправления брака литья. Это объясняется сильным испарением цинка по сравнению прежде всего с газовой сваркой или дуговой под флюсом, или дуговой в защитном газе.
Для дуговой сварки латуни применяют электроды с покрытием вида ЗТ. Состав электрода следующий: стержень с кремниемарганцевои бронзы Бр КМЦ 3-1, содержащий 3% кремния и 1% марганца, покрытие с 17,5% марганцевой руды, 13% плавикового шпата, 16% серебристого графита, 32% ферросилиция 75%-ного , 2,5% алюминия в порошке. Сварка ведется постоянным током при обратной полярности короткой дугой с целью снижения выгорания цинка. От вытекания металла из сварочной ванны стык защищают прокаленной асбестовой подкладкой с обратной стороны стыка. При толщине листов до 4 мм разделки кромок такая же, как и для стали. После сварки шов проковывают, а затем обжигают при 600-650 ° С для выравнивания химического состава и придания металлу мелкозернистой структуры.
Сварка латуни можно выполнять угольным электродом на постоянном токе прямой полярности с применением флюса.
C111 / CW114A / Сернистая медь
C111 / CW114C представляет собой сернистую медь свободной обработки с классом обрабатываемости примерно 80% (латунь свободной обработки = 100%). Добавление серы к меди создает сульфид меди Cu2S в микроструктуре, который действует как стружколом и формирует основу свободной механической обработки.
Добавление серы к меди создает сульфид меди Cu2S в микроструктуре, который действует как стружколом и формирует основу свободной механической обработки.
Свободные режущие свойства сернистой меди в сочетании с высокими показателями электропроводности и теплопроводности (обычно присущими только более чистой меди) позволяют использовать ее в самых разных областях. C111/CW114C также можно обрабатывать на гораздо более высоких скоростях с меньшим износом инструмента, что дает механикам и конструкторам более экономичный продукт.
Сернистая медь раскисляется во время производства путем добавления фосфора, в результате чего материал не подвержен водородному охрупчиванию. Другими преимуществами C111/CW114C являются высокая коррозионная стойкость, очень хорошая формуемость и возможность легкого соединения пайкой.
Химический состав
Медь | Рем |
Сера | 0,2–0,7% |
Фосфор | 0,003-0,012% |
Всего показов | 0,1% макс. |
Связанные характеристики
С111 | КВ114К |
CuSP | С14700 |
Основные характеристики
- Отличная электропроводность
- Свободная обрабатываемость
- Отсутствие водородного охрупчивания
- Очень хорошая теплопроводность
- Высокая коррозионная стойкость
Типичные физические свойства
Точка плавления | 1079°С |
Плотность | 8,94 г/см³ |
Удельная теплоемкость | 385 Дж/кг °К |
Теплопроводность | 347 Вт/м°К |
Коэффициент теплового расширения (20-200°C) | 17 x 10 -6 на °C |
Электропроводность | 93% МАКО |
Удельное электрическое сопротивление | 0,0181 мкм·м |
Модуль упругости | 12500 кг/мм² |
Характеристики изготовления
Диапазон температур горячей обработки | 750-870°С |
Возможность горячего формования | Хорошо |
Способность к холодной штамповке | Хорошо |
Холодное восстановление между отжигами | 70% макс. |
Класс обрабатываемости (свободная обработка латуни = 100) | 80 |
Методы соединения
Пайка | Отлично |
Пайка | Хорошо |
Кислородно-ацетиленовая сварка | Не рекомендуется |
Дуговая сварка в среде защитных газов | Не рекомендуется |
Сварка сопротивлением: Точечная и шовная Стыковая сварка | Не рекомендуется Ярмарка |
Типичное применение:
Сернистая медь C111/CW114C традиционно используется для электрических компонентов, для которых требуются высокие значения проводимости в сочетании со свободными свойствами механической обработки, в том числе; клеммы трансформаторов и автоматических выключателей, электрические контакты и соединители, зажимы, кабельные вводы и крепеж.
Эта техническая информация предоставляется компанией Holme Dodsworth Metals бесплатно, и пользователь может использовать такую информацию по своему усмотрению и на свой риск. Для получения более подробных технических рекомендаций по выбору отпуска, изготовлению, соединению, обработке, физическим и механическим характеристикам, пожалуйста, свяжитесь с нами, так как объем не позволяет перечислить все характеристики материала.
Сравнение элементов периодической таблицы | Сравните медь и серу
Сравните медь и серу
Сравните медь и серу на основе их свойств, атрибутов и фактов из периодической таблицы. Сравните элементы по более чем 90 свойствам. Все элементы подобных категорий обнаруживают много сходств и различий в своих химических, атомных, физических свойствах и использовании. Эти сходства и различия следует знать, изучая элементы таблицы Менделеева. Вы можете изучить подробное сравнение между медью и серой с самой надежной информацией об их свойствах, атрибутах, фактах, использовании и т. д. Вы можете сравнить медь и серу по более чем 90 такие свойства, как электроотрицательность, степень окисления, атомные оболочки, орбитальная структура, электросродство, физические состояния, электрическая проводимость и многое другое.
д. Вы можете сравнить медь и серу по более чем 90 такие свойства, как электроотрицательность, степень окисления, атомные оболочки, орбитальная структура, электросродство, физические состояния, электрическая проводимость и многое другое.
29 Cu Copper
Swap Sulfur vs Copper
Periodic Table Element Comparison
16 S Sulfur
Facts
| Name | Copper | Sulfur | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Atomic Number | 29 | 16 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Атомный символ | Cu | S | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Atomic Weight | 63.546 | 32.065 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Phase at STP | Solid | Solid | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Color | Copper | Yellow | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Metallic Classification | Переходный металл | Другой неметалл | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Группа Периодической таблицы | Группа 11 | Группа 16 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Название группы | Семейство меди | Семейство кислорода | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Период в периодической таблице | ПЕРИОН 4 | ПЕРИОД 3 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| БЛОК В ПЕРИОНАЛЬНОЙ ТЕРИЧЕСКОЙ ДЕЙСТВИЯ | 6. | [Ne] 3s2 3p4 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Структура электронной оболочки (электронов на оболочку) | 2, 8, 18, 1 | 2, 8, 6 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 1357.77 K | 388.36 K | |
| Boiling Point | 3200 K | 717.87 K |
| CAS Number | CAS7440-50-8 | CAS7704-34-9 |
| Neighborhood Elements | Соседние элементы меди | Соседние элементы серы |
История
| История | Элемент Медь был открыт Ближним Востоком в 9 году000 г. до н.э. Медь получила свое название от английского слова (лат. cuprum). | Элемент Сера был открыт китайцами/индейцами за год до 2000 г. до н.э. Сера получила свое название от латинского слова sulphur, «огонь и сера». |
| Discovery | Middle East (9000 BCE) | Chinese/Indians (Before 2000 BCE) |
| Isolated | Anatolia (6000 BCE) | () |
Presence: Abundance in Nature и вокруг нас 9-7 %)
| Abundance in Universe | 60 / 1 | 500000 / 20000 |
| Abundance in Sun | 700 / 10 | 400000 / 10000 |
| Abundance in Meteorites | 110000 / 31000 | 41000000 / 22000000 |
| Abundance in Earth’s Crust | 68000 / 22000 | 420000 / 270000 |
| Abundance in Oceans | 3 / 0. 29 29 | 928000 / 179000 |
| Abundance in Humans | 1000 / 99 | 2000000 / 3 |
Crystal Structure and Atomic Structure
| Atomic Volume | 7.124 cm3/mol | 15.53 cm3 /MOL |
| Атомный радиус | 145 PM | 88 PM |
| Ковалентный радиус | 138 PM | 102 PM |
| 140 pm | 180 pm | |
| Atomic Spectrum | ||
| Lattice Constant | 361.49, 361.49, 361.49 pm | 1043.7, 1284.5, 2436.9 pm |
| Lattice Angle | π/ 2, π/2, π/2 | π/2, π/2, π/2 |
| Space Group Name | Fm_ 3m | Fddd |
| Space Group Number | 225 | 70 |
| Crystal Structure | Face Centered Cubic | Face Centered Orthorhombic |
Atomic and Orbital Properties
| Atomic Number | 29 | 16 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Number of Electrons (with no заряд) | 29 | 16 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Число протонов | 29 | 16 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Массовое число 6,03360018 | 32. 065 065 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Number of Neutrons | 35 | 16 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Shell structure (Electrons per energy level) | 2, 8, 18, 1 | 2, 8, 6 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Electron Configuration | [AR] 3D10 4S1 | [NE] 3S2 3P4 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| VALENCE ELECTRONS | 3D10 4S1 | 3S2 3P4 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| . 2 . . . . . . . . . . . . . . . . . | ||
| Символ атомного термина (квантовые номера) | 2S1/2 | 3P2 |
| Структура раковины | ||
| Известные изотопы | 52cu, 53cu, 54cu, 55cu, 56cu, 57cu, 58cu, 59cu, 60cu, 61cu, 62cu, 63cu, 64cu, 65cu, 66cu, 68cu, 68cu, 68cu, 68cu, 68cu, 68cu, 68cu, 68cu, 68cu, 68cu, 68cu, 68cu, 68cu, 68cu, 68cu, 63cu, 63cu, 68cu, 63cu, 63cu, 63cu, 63cu, 63cu, 63cu, 63cu, 63cu, 68cu, 63cu, 63cu, 63cu, 63cu, 63cu, 63cu, 63cu. Cu, 70Cu, 71Cu, 72Cu, 73Cu, 74Cu, 75Cu, 76Cu, 77Cu, 78Cu, 79Cu, 80Cu Cu, 70Cu, 71Cu, 72Cu, 73Cu, 74Cu, 75Cu, 76Cu, 77Cu, 78Cu, 79Cu, 80Cu | 26S, 27S, 28S, 29S, 30S, 31S, 32S, 33S, 35S, 38S,3 33 , 39S, 40S, 41S, 42S, 43S, 44S, 45S, 46S, 47S, 48S, 49S |
| Стабильные изотопы | Naturally Cocdursing Stable Osotables: 63CU, 65CU 9003 | |
| Нейтронное сечение | 3,78 | 0,52 |
| Neutron Mass Absorption | 0.0021 | 0.00055 |
Chemical Properties: Ionization Energies and electron affinity
| Valence or Valency | 2 | 6 |
| Electronegativity | 1.9 Pauling Scale | 2.58 Шкала Полинга |
| Сродство к электрону | 118,4 кДж/моль | 200 кДж/моль |
| Энергия ионизации | 1st: 745. 2nd: 1957.9 kJ/mol 3rd: 3555 kJ/mol 4th: 5536 kJ/mol 5th: 7700 kJ/mol 6th: 9900 kJ/mol 7th: 134400 кДж/моль 8th: 16000 кДж/моль 9 -й: 19200 кДж/моль 10th: 22400 кДж/моль 11th: 25600 кДж/моль 12th: 35600 кДж/моль 13. : 38700 кДж/моль 14-я: 42000 кДж/моль 15-я: 46700 кДж/моль 16-я: 50200 кДж/моль 17th: 53700 kJ/mol 18th: 61100 kJ/mol 19th: 64702 kJ/mol 20th: 163700 kJ/mol 21st: 174100 kJ/mol 22nd: 184900 kJ/mol 23rd: 198800 kJ/mol 24th: 210500 kJ/mol 25th: 222700 kJ/mol 26th: 239100 kJ/mol 27th: 249660 kJ/mol 28th: 1067358 kJ/mol 29th: 1116105 кДж/моль | 1-й: 999,6 кДж/моль 2-й: 2252 кДж/моль 3rd: 3357 kJ/mol 4th: 4556 kJ/mol 5th: 7004.3 kJ/mol 6th: 8495. 7th: 27107 kJ/mol 8th: 31719 kJ/mol 9th: 36621 кДж/моль 10th: 43177 кДж/моль 11th: 48710 кДж/моль 12th: 54460 кДж/моль 13th: 62930 кДж/моль 14th: 68216 KJ/MOL 15th 15th: 3 -е. 311048 кДж/моль 16-й: 337138 кДж/моль |
Физические свойства
| Density | 8.92 g/cm3 | 1.96 g/cm3 |
| Molar Volume | 7.124 cm3/mol | 15.53 cm3/mol |
Elastic Properties | ||
| Young Modulus | 130 | — |
| Shear Modulus | 48 GPa | — |
| Bulk Modulus | 140 GPa | 7.7 GPa |
| Poisson Ratio | 0.34 | — |
Hardness — Tests to Measure of Hardness of Element | ||
| Mohs Hardness | 3 MPa | 2 MPa |
| Vickers Hardness | 369 MPa | — |
| Твердость по Бринеллю | 874 МПа | — |
Электрические свойства | ||
500 S/m | 1e-15 S/m | |
| Resistivity | 1. 7e-8 m Ω 7e-8 m Ω | 1000000000000000 m Ω |
| Superconducting Point | — | — |
Heat and Conduction Properties | ||
| Thermal Conductivity | 400 W/(m K) | 0.205 W/(m K) |
| Thermal Expansion | 0.0000165 /K | — |
Magnetic Properties | ||
| Magnetic Type | Diamagnetic | Diamagnetic |
| Curie Point | — | — |
| Mass Magnetic Susceptibility | -1.08e-9 m3/kg | — 6.2e-9 м3/кг |
| Молярная магнитная восприимчивость | -6.86e-11 м3/моль | -1.99e-10 м3/моль |
| Объемная магнитная восприимчивость | -0.0000122 | |
Optical Properties | ||
| Refractive Index | — | 1. 001111 001111 |
Acoustic Properties | ||
| Speed of Sound | 3570 m/s | — |
Тепловые свойства — Энтальпии и термодинамика
| Температура плавления | 1357,77 K | 388.36 K |
| Boiling Point | 3200 K | 717.87 K |
| Critical Temperature | — | 1314 K |
| Superconducting Point | — | — |
Enthalpies | ||
| Теплота плавления | 13,1 кДж/моль | 1,73 кДж/моль |
| Теплота парообразования | 300 кДж/моль | |
| Heat of Combustion | — | — |
Regulatory and Health — Health and Safety Parameters and Guidelines
| CAS Number | CAS7440-50-8 | CAS7704-34- |
| RTECS Номер | RTECSGL5325000 | {RTECSWS4250000, N/A, N/A, N/A, N/A, N/A} |
| DOT HAZE0023 | ||
| DOT Numbers | 3089 | — |
| EU Number | — | — |
| NFPA Fire Rating | 1 | {N/A, N/A, N/A, N/ A, N/A, N/A} |
| Опасности NFPA | — | N/A, N/A, N/A, N/A, N/A, N/A |
| NFPA Health Рейтинг | 1 | — |
| Рейтинг реактивности NFPA | 0 | — |
| AutoIgnition Point | — | — |
| Flashpoint | — | — |
Compare With Other Elements
Compare Copper with allGroup 11 elements Copper vs RoentgeniumCopper vs SilverCopper vs Gold Compare Copper with allPeriod 4 elements Copper vs GermaniumCopper vs NickelCopper vs BromineCopper vs ScandiumCopper vs ArsenicCopper vs CobaltCopper vs CalciumCopper vs ChromiumCopper vs SeleniumCopper vs KryptonCopper vs VanadiumCopper vs ZincCopper vs PotassiumCopper vs TitaniumCopper vs ManganeseCopper против IronCopper против Gallium Compare Copper with allTransition Metal elements Copper vs NickelCopper vs RutheniumCopper vs RhodiumCopper vs ZirconiumCopper vs RoentgeniumCopper vs DarmstadtiumCopper vs DubniumCopper vs SeaborgiumCopper vs CadmiumCopper vs TungstenCopper vs ScandiumCopper vs TantalumCopper vs SilverCopper vs RheniumCopper vs NiobiumCopper vs CobaltCopper vs MolybdenumCopper vs MercuryCopper Медь против хрома, медь, иттрий, медь, иридий, медь, хассий, медь, ванадий, медь, цинк, медь, технеций, медь, платина, медь, мейтнерий, медь, коперниций, медь, титан, медь, марганец, медь, железо, медь, медь, палладий, медь, гафний, медь, осмий, медь, золото, медь, Резерфорд. |

 5 kJ/mol
5 kJ/mol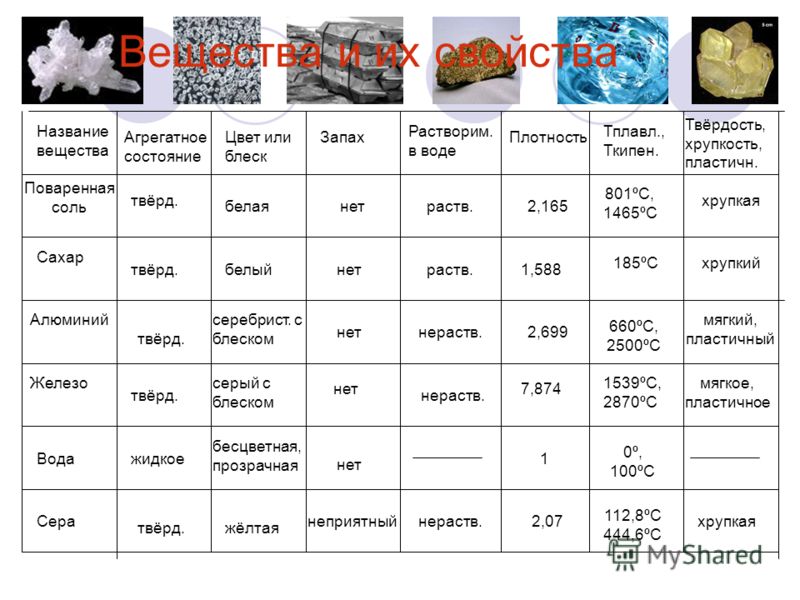 8 kJ/mol
8 kJ/mol