Какая у меди температура плавления: Температура плавления меди – при какой температуре плавится медь
Содержание
Медь в Севастополе — характеристики, расшифровка
- Медно-никелевый сплав (22)
- Медь (13)
- Сплав меди жаропрочный (19)
- Сплав медно-фосфористый (2)
| Цвет: золотисто-розовый пластичный металл | Теплопроводность: 55,5-58 МСм/м |
| Удельный вес меди: 8,93 г/cм3 | Плотность меди: 8,93х103 кг/м3 |
| Удельная теплоемкость меди: 0,094 кал/град | Температура плавления меди: 1083 °C |
| Удельная теплота плавления меди: 42 кал/г | Температура кипения меди: 2600 °C |
| Коэффициент линейного расширения меди: (при 20 °C) — 16,7 *106(1/град) | Удельное сопротивление меди (при 20 °C): 0,0167 Ом*мм2/м |
Получение меди: В зависимости от добавок к меди получают сплавы с различными свойствами (высокопрочные, антифрикционные, химически стойкие и др. ). Широкое применение для изготовления полуфабрикатов и фасонного литья получили сплавы меди с цинком, оловом, алюминием, бериллием, свинцом, никелем и марганцем.
). Широкое применение для изготовления полуфабрикатов и фасонного литья получили сплавы меди с цинком, оловом, алюминием, бериллием, свинцом, никелем и марганцем.
Плавка меди может производиться во всех плавильных печах, применяемых для приготовления медных сплавов.
Независимо от типа плавильной печи плавка меди ведется под слоем древесного угля. Печи перед загрузкой шихты нагревают до температуры 900—1000° С. На дно плавильной печи засыпают хорошо прокаленный древесный уголь в количестве, достаточном, чтобы покрыть поверхность металла после расплавления, затем загружают медь, отходы и засыпают сверху древесным углем. Процесс плавления должен вестись интенсивно.
После расплавления медь нагревают до заданной температуры и проводят раскисление в два приема: предварительное и окончательное.
Первое осуществляется непосредственно в плавильных печах, а второе — в ковшах перед разливкой расплава.
Предварительное раскисление меди производят фосфористой медью, а окончательное раскисление рекомендуется производить оловом или цинком. Остатки олова и цинка в меди менее вредно влияют на ее свойства, чем остатки фосфора, алюминия и других раскислителей.
Остатки олова и цинка в меди менее вредно влияют на ее свойства, чем остатки фосфора, алюминия и других раскислителей.
После окончательного раскисления медь быстро разливают по изложницам.
Медноникелевые сплавы (копель, константан, мельхиор, нейзильбер) преимущественно плавят в электрических индукционных печах без магнитопровода с основной футеровкой и очень редко плавят в топливных печах. Плавку ведут под слоем флюса, состоящего из плавикового шпата, битого стекла и извести. Древесный уголь может применяться только при плавке медноникелевых сплавов с низким содержанием никеля. Порядок ведения плавки следующий: в расплавленную и раскисленную (фосфористой медью) медь после удаления шлака вводят крупные отходы сплава и чистый никель (при температуре 1450—1500°С), а в последнюю очередь загружают мелкие отходы, стружку и т. п. Марганец вводят в. чистом виде, в виде лигатуры медь — марганец или в виде ферромарганца. Окончательным раскислителем служит магний, который добавляют в количестве 0,05—0,1% от веса шихты. Температура литья 1300—1350° С. Шихтовые материалы медноникелевых сплавов не должны содержать углерод и серу, так как эти примеси являются вредными для этих сплавов.
Температура литья 1300—1350° С. Шихтовые материалы медноникелевых сплавов не должны содержать углерод и серу, так как эти примеси являются вредными для этих сплавов.
| Краткие обозначения: | ||||
| σв | — временное сопротивление разрыву (предел прочности при растяжении), МПа | ε | — относительная осадка при появлении первой трещины, % | |
| σ0,05 | — предел упругости, МПа | Jк | — предел прочности при кручении, максимальное касательное напряжение, МПа | |
| σ0,2 | — предел текучести условный, МПа | σизг | — предел прочности при изгибе, МПа | |
| δ5,δ4,δ10 | — относительное удлинение после разрыва, % | σ-1 | — предел выносливости при испытании на изгиб с симметричным циклом нагружения, МПа | |
| σсж0,05 и σсж | — предел текучести при сжатии, МПа | J-1 | — предел выносливости при испытание на кручение с симметричным циклом нагружения, МПа | |
| ν | — относительный сдвиг, % | n | — количество циклов нагружения | |
| sв | — предел кратковременной прочности, МПа | R и ρ | — удельное электросопротивление, Ом·м | |
| ψ | — относительное сужение, % | E | — модуль упругости нормальный, ГПа | |
| KCU и KCV | — ударная вязкость, определенная на образце с концентраторами соответственно вида U и V, Дж/см2 | T | — температура, при которой получены свойства, Град | |
| sT | — предел пропорциональности (предел текучести для остаточной деформации), МПа | l и λ | — коэффициент теплопроводности (теплоемкость материала), Вт/(м·°С) | |
| HB | — твердость по Бринеллю | C | — удельная теплоемкость материала (диапазон 20o — T ), [Дж/(кг·град)] | |
| HV | — твердость по Виккерсу | pn и r | — плотность кг/м3 | |
| HRCэ | — твердость по Роквеллу, шкала С | а | — коэффициент температурного (линейного) расширения (диапазон 20o — T ), 1/°С | |
| HRB | — твердость по Роквеллу, шкала В | σtТ | — предел длительной прочности, МПа | |
| HSD | — твердость по Шору | G | — модуль упругости при сдвиге кручением, ГПа | |
Температура плавления меди
Историки предполагают, что первобытные люди находили медь в виде самородков, порой достигающих значительных размеров. Свое название на латинском языке медь (Cuprum) получила от острова Кипр, где ее добывали древние греки. Благодаря тому, что температура плавления меди не слишком высока и составляет 1083 °С, самородки или руду, содержащую медь, можно было плавить на костре. Это обеспечивало получение меди и позволяло использовать ее для изготовления оружия и предметов быта.
Свое название на латинском языке медь (Cuprum) получила от острова Кипр, где ее добывали древние греки. Благодаря тому, что температура плавления меди не слишком высока и составляет 1083 °С, самородки или руду, содержащую медь, можно было плавить на костре. Это обеспечивало получение меди и позволяло использовать ее для изготовления оружия и предметов быта.
Несмотря на то, что медь широко применялась людьми еще с древних времен, по распространению в земной коре она занимает 23 место среди других элементов. Чаще всего она в природе встречается в виде соединений, входящих в состав сульфидных руд. Наиболее распространенные из них – медный блеск и медный колчедан. Существует несколько технологий получения меди из руды, причем по каждой из них процесс происходит в несколько этапов.
Припой для пайки меди, алюминия, латуни, стали, нержавейки….
Когда необходимо надежно скрепить между собой различные твердые соединения, то чаще всего для этого…
Как уже отмечалось, невысокая температура плавления меди позволяла успешно ее обрабатывать еще на самом начальном этапе развития цивилизации. И надо отдать должное древним металлургам, ими были найдены варианты получения и использования не только чистой меди, но и ее сплавов. Плавление – это переход металла из твердого состояния в жидкое. Для этого использовали нагрев, и низкая температура плавления меди позволяла успешно проводить подобную операцию.
И надо отдать должное древним металлургам, ими были найдены варианты получения и использования не только чистой меди, но и ее сплавов. Плавление – это переход металла из твердого состояния в жидкое. Для этого использовали нагрев, и низкая температура плавления меди позволяла успешно проводить подобную операцию.
Затем в жидкую медь добавляли олово или производили его восстановление из касситерита (руды, содержащей олово) на поверхности меди. В итоге получали бронзу, по прочности превосходящую Cuprum и применяемую для изготовления оружия. Однако сейчас хотелось бы остановиться более подробно на операции плавления, позволяющей получить достаточно чистый материал из руды.
Латунь — это сплав меди с… Состав латуни
Это сплав, похожий на золото, но намного его дешевле. Известный еще в Древнем Риме, но повторно…
Температура плавления у каждого металла своя и зависит от наличия примесей в составе исходного материала. Так, медь, температура плавления которой составляет 1083 °С, после добавления олова образует бронзу, которая плавится при температуре 930-1140°С в зависимости от содержания олова. Латунь же, сплав меди и цинка, имеет температуру плавления 900-1050°С.
Латунь же, сплав меди и цинка, имеет температуру плавления 900-1050°С.
В процессе нагрева металла происходит разрушение кристаллической решетки. Первоначально, по мере нагрева, температура возрастает, а затем, начиная с некоторого значения, остается постоянной, хотя нагрев и продолжается. В этот момент и происходит плавление. Так продолжается в течение всего времени, пока весь металл не расплавится, и только потом температура начнет повышаться. Это справедливо для всех металлов, температура плавления меди также не изменяется.
При охлаждении картина обратная: сначала температура снижается до начала затвердевания металла, потом держится постоянной и после полного отвердения металла начинает опять понижаться. Такое поведение металла, если его изобразить на графике, называется фазовой диаграммой, показывающей, в каком состоянии находится вещество при конкретной температуре. Для ученых фазовая диаграмма является одним из инструментов в изучении поведения металлов при плавлении.
Если продолжить нагрев расплавленного металла, то при некоторой температуре начинается процесс, похожий на кипение.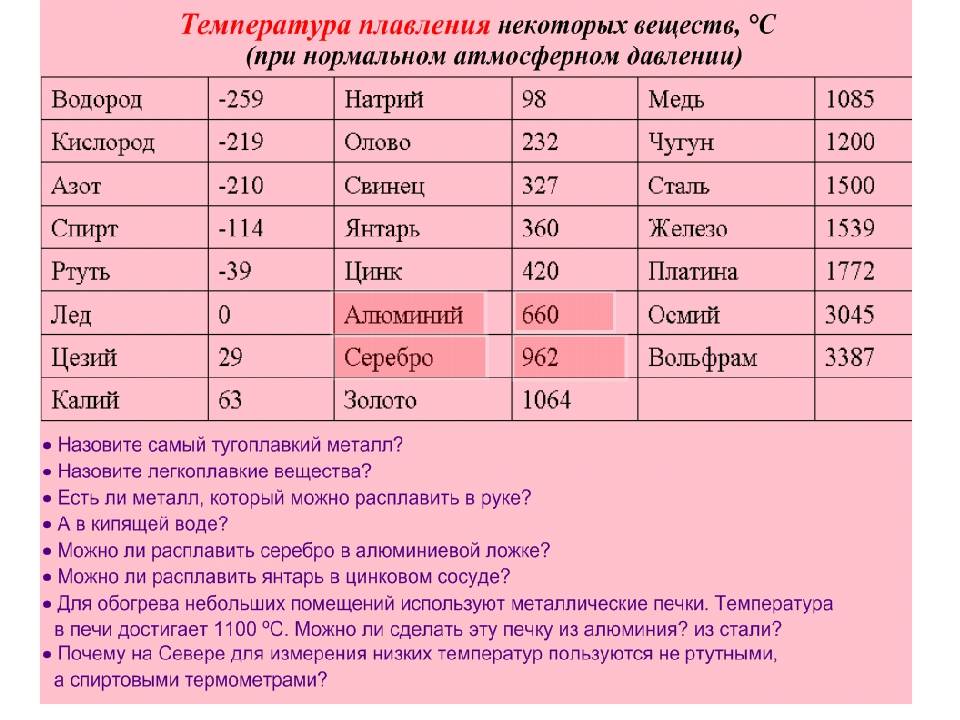 Так, температура кипения меди составляет 2560 °С. Это название процесс получил за внешнее сходство с кипением жидкости, когда из нее начинают выделяться пузырьки газа. То же самое происходит и с металлом, например, при достаточно высокой температуре из жидкого железа начинает выходить углерод, образующийся в ходе его окисления.
Так, температура кипения меди составляет 2560 °С. Это название процесс получил за внешнее сходство с кипением жидкости, когда из нее начинают выделяться пузырьки газа. То же самое происходит и с металлом, например, при достаточно высокой температуре из жидкого железа начинает выходить углерод, образующийся в ходе его окисления.
В статье рассмотрен процесс плавления металлов, описано понятие температуры плавления, ее поведение в процессе проведения плавки. Объясняется, какое влияние низкая температура плавления меди оказала на развитие цивилизации и металлургии.
Химические элементы периодической таблицы, отсортированные по температуре плавления
- Главная
- Периодическая таблица
- Химические элементы, перечисленные по температуре плавления
Элементы периодической таблицы, отсортированные по температуре плавления
click для имени любого элемента для дальнейших химических свойств, данных об окружающей среде или воздействии на здоровье.
Этот список содержит 118 химических элементов.
| Химические элементы периодической таблицы, отсортированные по: | Температура плавления | Название химического элемента | Символ | |
| — Название по алфавиту | -272 | Гелий | Не | 2 |
| — Атомный номер | -259 | Водород | H | 1 |
| — Символ | -249 | 900 13 Неон | Ne | 10 |
| — Атомная масса | -220 | Фтор | F | 9 |
| — Электроотрицательность | -218 900 25 | Кислород | O | 8 |
| — Плотность | -210 | Азот | N | 7 |
| — Температура плавления | -189 | Аргон | Ar | 18 |
| — Температура кипения | -157 | Криптон 90 014 | Кр | 36 |
| — Радиус Вандервальса | -112 | Ксенон | Xe 90 025 | 54 |
| — Год открытия | -101 | Хлор | Cl | 17 |
| — Фамилия изобретателя | -71 | Радон | 900 13 Р-н | 86 |
| — Элементы земной коры | -39 | Ртуть | Hg | 80 |
| — Элементы в организме человека | -7 | Бром | Br | 35 |
| — Коваленц радиус | 27 | Франций | 90 013 Пт | 87 |
| — Энергия ионизации | 29 | Цезий | Cs | 55 9002 5 |
Для студентов и преподавателей химии: Таблица справа упорядочена по температуре плавления. Химический элемент с самой низкой температурой плавления — гелий, а элемент с самой высокой температурой плавления — углерод. Для температуры плавления используется единица Цельсия (C). Щелкните здесь: чтобы перевести градусы Цельсия в градусы Фаренгейта или Кельвина. Обратите внимание, что элементы не показывают своего естественного отношения друг к другу, как в периодической системе. Там вы можете найти металлы, полупроводники, неметаллы, инертный благородный газ (ы), галогены, лантаноиды, актиноиды (редкоземельные элементы) и переходные металлы. | 30 | Галлий | Ga | 31 |
| 39 | Рубидий | 37 | ||
| 44 | Фосфор | P | 15 | |
| 64 | Калий | К | 19 | |
| 98 | Натрий | Na | 11 | |
| 113 | Сера | S | 1 6 | |
| 114 | Йод | I | 53 | |
| 157 | Индий | In | 49 | |
| 180 | Литий | Li 900 25 | 3 | |
| 217 | Селен | Se | 34 | |
| 232 9002 5 | Олово | Sn | 50 | |
| 254 | Полоний | Po | ||
| 271 | Висмут | Би | 83 | |
| Астатин | Ат | 85 | ||
| 303 | Таллий | Тл | 81 | |
| 321 | Кадмий | Cd | 48 | |
| 3 27 | Свинец | Pb | 82 | |
| 420 | Цинк | Цинк | 30 | |
| 449 | Теллур | Te | 52 | |
| 630 | Сурьма | Sb | 51 | |
| 639 | Магний | Mg | 12 | |
| 640 | Нептуний | Np | 93 | |
| 640 | Плутоний | Pu | 94 | |
| 660 | 900 13 Алюминий | Al | 13 | |
| 700 | Радий | Ra | ||
| 725 | Барий | Ba | 56 | |
| 769 | Стронций | Sr | 38 | |
| 795 | Церий | 58 | ||
816. 8 8 | Мышьяк | Ас | 33 | |
| 8 22 | Европий | Eu | 63 | |
| 824 | Иттербий 90 014 | Ыб | 70 | |
| 827 | Нобелий | № | 102 9002 5 | |
| 839 | Кальций | Ca | 20 | |
| 860 | Эйнштейний 9001 4 | Es | 99 | |
| 900 | Калифорния | Cf 900 14 | 98 | |
| 920 | Лантан | Ла | 57 | |
| 935 9002 5 | Празеодим | Pr | 59 | |
| 937 | Германий | Ge 90 014 | 32 | |
| 962 | Серебристый | Серебряный | 47 | |
| 986 | Берклиум | Bk | 97 | |
| 994 | Америций 9001 4 | Ам | 95 | |
| 1010 | Неодим | Nd | 60 | |
| 1050 | Актиний | Ac | 89 | |
| 1064 | Au | 79 | ||
| 1072 | Самарий | Sm | 62 | |
| 1083 | Медь | Медь | 29 | |
| 1100 | Прометий | Пм | 61 | |
| 1132 | Уран | 92 | ||
| 1245 | Марганец | Mn | 25 | 1278 | Бериллий | Be | 4 |
| 1311 | Гадолиний | 64 | ||
| 1340 | Кюриум | См | 96 | |
| 1360 | Тербий | Тб | 65 | |
| 1410 | Si | 14 | ||
| 1412 | Диспрозий | Dy | 66 | |
| 1453 | Никель | Ni | 28 | |
| 1470 | Гольмий | Ho | 67 | |
| 1495 | 90 013 Кобальт | Co | 27 | |
| 1522 | Эрбий | Er 9 0025 | 68 | |
| 1523 | Иттрий | Y | 39 | |
| 1527 | Фермиум | Fm | 100 | |
| 1535 | Железо | Fe | 26 | |
| 1539 | Скандий | Sc | 21 | |
| 1545 | Тулий | Tm | 69 | |
| 1552 | Палладий | Pd | 46 | |
| 1568 | Pro тактиний | Па | 91 | |
| 1627 | Лоренсиум | Lr | 103 | |
| 1656 | Лютеций | Lu | 71 900 25 | |
| 1660 | Титан | Ti | 22 | |
| 1750 | 900 13 Торий | Th | 90 | |
| 1772 | Платина | Pt | 78 | |
| 1852 | Цирконий | Цирконий | 40 900 25 | |
| 1857 | Хром | Cr | 24 | |
| 1890 | 9 0013 Ванадий | V | 23 | |
| 1966 | Родий | Rh | 45 | |
| 2150 | Гафний | Hf | 72 9002 5 | |
| 2200 | Технеций | Tc | 43 | |
| 2250 | Рутений | Ru | 44 | |
| 2300 | Бор | B 90 025 | 5 | |
| 2410 | Иридий | Ir | 77 | |
| 2468 | Ниобий | Nb | 41 | |
| 2617 | 9 0013 Молибден | Мо | 42 | |
| 2996 | Тантал | Та | ||
| 3045 | Осмий | Ос | 76 | |
| 3180 | Рений | Re | 75 | |
| 3410 | Тунг Стен | W | 74 | |
| 3500 | Карбон | C | ||
| Менделевий | Md | 101 | ||
| Резерфордиум | Рф | 104 | ||
| Дубниум | Дб 9 0014 | 105 | ||
| Сиборгиум | Sg | 106 | ||
| 9106 7 | Борий | Bh | 107 | |
| Хассиум | 108 | |||
| Мейтнерий | Mt | 109 | ||
| Дармштадтиум | Ds | 110 | ||
| Рентгений 9002 5 | Rg | 111 | ||
| Coprnicium | Cn | |||
| Нигоний | Nh | 113 | ||
| Флеровиум | Fl | 114 | ||
| Московиум | Mc 9002 5 | 115 | ||
| Ливермориум | Lv | 116 | ||
| Теннессин | Ц | 117 | ||
| Оганесон | Ог 9 0014 | 118 |
Щелкните здесь: схематический обзор периодической таблицы элементов в виде диаграммы
Пожалуйста, сообщайте о любой случайной ошибке в приведенной выше статистике по химическим элементам
Справочник по точкам плавления элементов – Ангстрем Сайенсиз
| Символы | Точка плавления | Имя | # | ||
|---|---|---|---|---|---|
| 0,95 К | -272,05 °С | -458 °F | Гелий | Он | 2 |
| 14,025 К | -258,975 °С | -434 °F | Водород | Х | 1 |
| 24,553 К | -248,447 °С | -415,205 °F | Неон | Не | 10 |
| 50,35 К | -222,65 °С | -368,77 °F | Кислород | О | 8 |
| 53,48 К | -219,52 °С | -363,14 °F | Фтор | Ф | 9 |
| 63,14 К | -209,86 °С | -345,75 °F | Азот | Н | 7 |
| 83,81 К | -189,19 °С | -308,54 °F | Аргон | Ар | 18 |
| 115,78 К | -157,22 °С | -251 °F | Криптон | Кр | 36 |
| 161,3 К | -111,7 °С | -169,1 °F | Ксенон | Хе | 54 |
| 172,16 К | -100,84 °С | -149,51 °F | Хлор | Кл | 17 |
| 202 К | -71 °С | -96 °F | Радон | Рн | 86 |
| 234,28 К | -38,72 °С | -37,7 °F | Меркурий | рт. ст. ст. | 80 |
| 265,9 К | -7,1 °С | 19,2 °F | Бром | Бр | 35 |
| 300 К | 27 °С | 81 °F | Франций | Пт | 87 |
| 301,55 К | 28,55 °С | 83,39 °F | Цезий | цезий | 55 |
| 302,9 К | 29,9 °С | 85,8 °F | Галлий | Га | 31 |
| 312,64 К | 39,64 °С | 103,35 °F | Рубидий | 37 | |
| 317,3 К | 44,3 °С | 111,7 °F | Фосфор | Р | 15 |
| 336,35 К | 63,35 °С | 146,03 °F | Калий | К | 19 |
| 371 К | 98 °С | 208 °F | Натрий | Нет | 11 |
| 386,7 К | 113,5 °С | 236,3 °F | Йод | я | 53 |
| 388,36 К | 115,36 °С | 239,65 °F | Сера | С | 16 |
| 429,76 К | 156,76 °С | 314,17 °F | Индий | В | 49 |
| 453,7 К | 180,7 °С | 357,3 °F | Литий | Ли | 3 |
| 494 К | 221 °С | 430 °F | Селен | Se | 34 |
| 505,06 К | 232,06 °С | 449,71 °F | Олово | Сн | 50 |
| 527 К | 254 °С | 489 °F | Полоний | ПО | 84 |
| 544,52 К | 271,52 °С | 520,74 °F | Висмут | Би | 83 |
| 575 К | 302 °С | 576 °F | Астатин | В | 85 |
| 577 К | 304 °С | 579°F | Таллий | Тл | 81 |
| 594,18 К | 321,18 °С | 610,12 °F | Кадмий | CD | 48 |
| 600,6 К | 327,6 °С | 621,7 °F | Свинец | Пб | 82 |
| 692,73 К | 419,73 °С | 787,51 °F | Цинк | Цин | 30 |
| 722,65 К | 449,65 °С | 841,37 °F | Теллур | Те | 52 |
| 903,9 К | 630,9 °С | 1167,6 °F | Сурьма | Сб | 51 |
| 913 К | 640 °С | 1184 °F | Плутоний | Пу | 94 |
| 913 К | 640 °С | 1184 °F | Нептуний | Нп | 93 |
| 922 К | 649 °С | 1200 °F | Магний | мг | 12 |
| 933,25 К | 660,25 °С | 1220,45 °F | Алюминий | Ал | 13 |
| 973 К | 700 °С | 1292 °F | Радий | Ра | 88 |
| 1002 К | 729 °С | 1344 °F | Барий | Ба | 56 |
| 1042 К | 769 °С | 1416 °F | Стронций | Старший | 38 |
| 1071 К | 798 °С | 1468 °F | Церий | Се | 58 |
| 1081 К | 808 °С | 1486 °F | Мышьяк | Как | 33 |
| 1095 К | 822 °С | 1512 °F | Европий | ЕС | 63 |
| 1097 К | 824 °С | 1515 °F | Иттербий | Ыб | 70 |
| 1112 К | 839 °С | 1542 °F | Кальций | Са | 20 |
| 1133 К | 860 °С | 1580 °F | Эйнштейний | Эс | 99 |
| 1173 К | 900 °С | 1652 °F | Калифорния | См.
|

