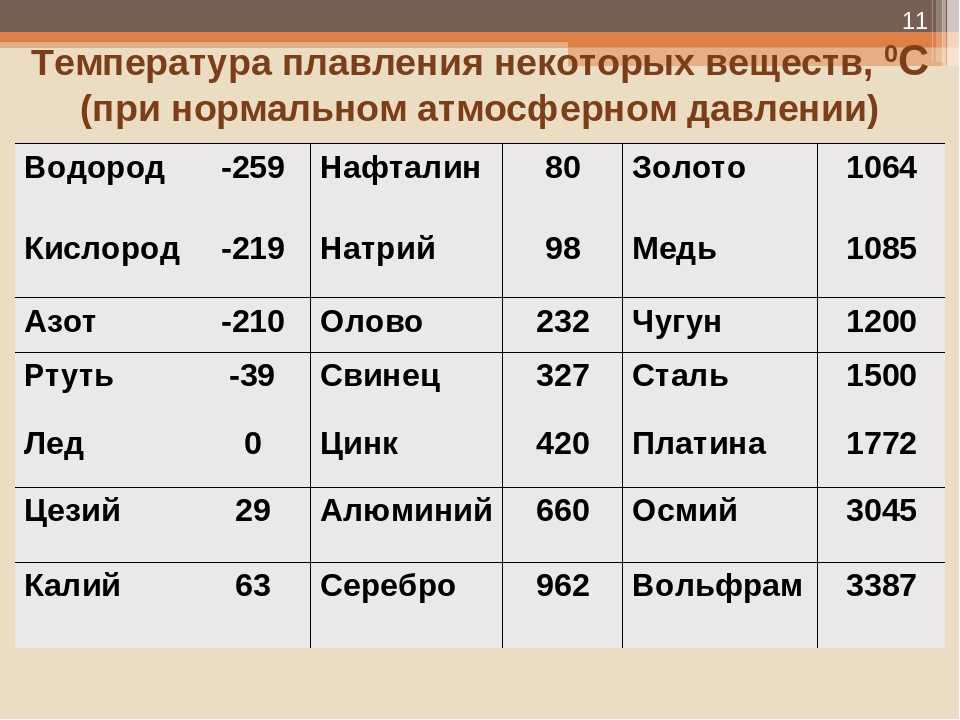
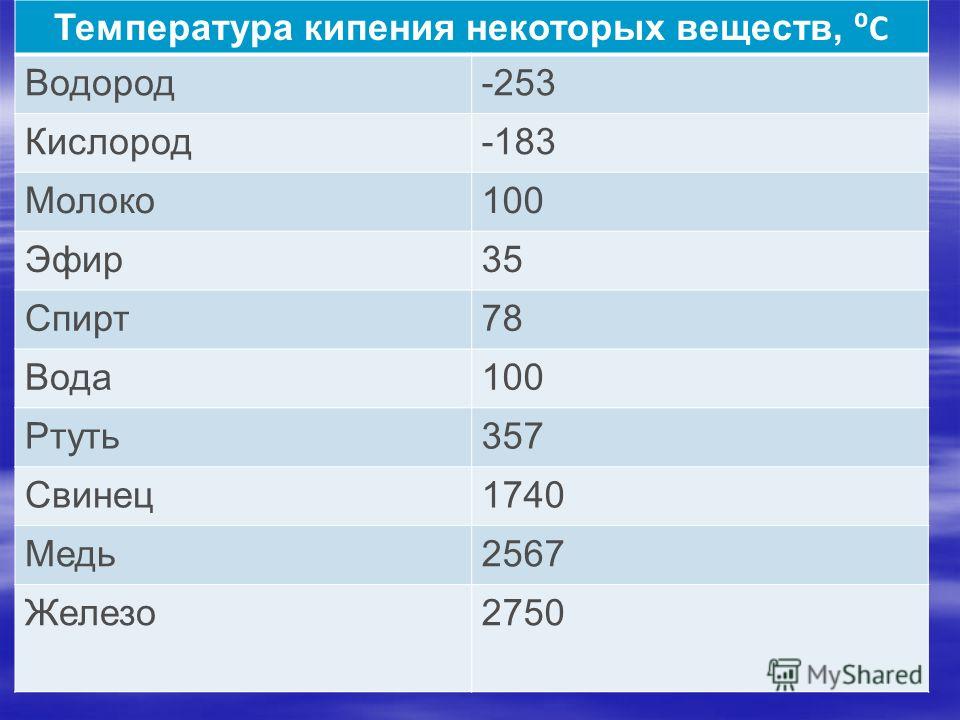
Какова температура кипения и плавления меди: Температура плавления меди – при какой температуре плавится медь
Содержание
Температура плавления меди и ее сплавов, график, характеристики
Медные изделия отличаются хорошей прочностью, пластичностью, высокой электропроводностью, устойчивостью к коррозии и химически активным веществам. Для изготовления объектов используется медная руда, которая на заводах обогащается и переплавляется в однородные бруски, прутья или слитки. Чтобы изготовить какое-либо медное изделие, материал помещают в термостойкую форму, доводят до температуры плавления, а потом прекращают нагрев, что приводит к застыванию вещества. Но какая температура плавления меди? Можно ли расплавить медные заготовки в домашних условиях — или для этого требуются специальные печи? О каких правилах техники безопасности нужно знать?
Содержание
- 1 Общие сведения
- 2 Температура плавления меди
- 3 Плавление сплавов на основе меди
- 4 Как расплавить медь в домашних условиях?
- 4.1 Оборудование и правила техники безопасности
- 4.2 Алгоритм расплавления медных изделий
- 5 Заключение
Общие сведения
Температурой плавления называют температуру, при которой твердое вещество переходит в жидкость. Медь расплавляется при температуре 1083 градусов, поэтому этот металл относят к категории тугоплавких. При снижении этой температуры металл может вновь принять твердую форму. Плавят медь на заводах, хотя эту процедуру можно провести в домашних условиях. На химическом уровне расплавление возникает за счет деструкции кристаллической решетки, которая формирует твердую структуру вещества. Атомы меди в кристаллической решетке всегда находятся в непрерывном движении.
Медь расплавляется при температуре 1083 градусов, поэтому этот металл относят к категории тугоплавких. При снижении этой температуры металл может вновь принять твердую форму. Плавят медь на заводах, хотя эту процедуру можно провести в домашних условиях. На химическом уровне расплавление возникает за счет деструкции кристаллической решетки, которая формирует твердую структуру вещества. Атомы меди в кристаллической решетке всегда находятся в непрерывном движении.
Однако их взаимное притяжение и отталкивание происходит сбалансировано, поэтому атомы сохраняют исходное положение в течение длительного времени. В случае повышения температуры атомы меди получают дополнительную энергию, что заставляет двигаться их более интенсивно. При небольшом повышении дополнительная энергия «гасится» за счет сбалансированного движения атомов в решетке. Однако при достижении определенной температуры нагрева количество энергии становится избыточным, а кристаллическая решетка начинает разрушаться.
В этот момент и происходит расплавление вещества. Взаимное притяжение атомов частично сохраняется, поэтому вещество принимает жидкую форму. Однако в случае дальнейшего нагрева энергия атомов усиливается еще сильнее, что может привести к окончательному разрыву связи атомов друг с другом. Эту точку перехода называют испарением (жидкость трансформируется в пар). В случае снижения температуры медного пара может переходить обратно в жидкость, а потом — в твердое состояние.
Взаимное притяжение атомов частично сохраняется, поэтому вещество принимает жидкую форму. Однако в случае дальнейшего нагрева энергия атомов усиливается еще сильнее, что может привести к окончательному разрыву связи атомов друг с другом. Эту точку перехода называют испарением (жидкость трансформируется в пар). В случае снижения температуры медного пара может переходить обратно в жидкость, а потом — в твердое состояние.
Температура плавления меди
При нормальных условиях температура плавления меди составляет 1083 градусов по шкале Цельсия. А во время нагрева происходит ряд превращений на молекулярном уровне, что приводит к изменению свойств вещества. Чтобы разобраться во всех этих изменениях, нужно рассмотреть основные этапы нагрева и расплавления медного слитка. Примерный график плавления меди выглядит так:
- В нормальном состоянии при температуре от 0 до 100 градусов внутри меди образуется прочная кристаллическая решетка, которая обеспечивает материалу большую устойчивость, упругость, химическую инертность.
 Решетка является достаточно прочной, однако в случае сильной деформации может происходить пространственное изменение положения атомов в решетке. Этим объясняется ковкость и пластичность медных изделий, которые могут сгибаться и деформироваться (скажем, при кузнечной обработке или в случае пресса).
Решетка является достаточно прочной, однако в случае сильной деформации может происходить пространственное изменение положения атомов в решетке. Этим объясняется ковкость и пластичность медных изделий, которые могут сгибаться и деформироваться (скажем, при кузнечной обработке или в случае пресса). - В нормальном состоянии при температуре от 0 до 100 градусов на поверхности медного изделия также образуется тонкая оксидная пленка. Наличие такой пленки является большим плюсом для изделия, поскольку она выполняет множество важных функций — минимизирует контакт с внешними веществами, защищает материал от коррозии, немного увеличивает прочность. В случае охлаждения материала ниже температуры 0 градусов сама медь сохраняет все свои физические свойства. Однако оксидная пленка при охлаждении становится менее упругой и плотной, изделие становится менее твердым (хотя с практической точки зрения это снижение прочности практически незаметно).
- При нагреве материала выше температуры 100 градусов происходит постепенная деструкция оксидной пленки на поверхности металла.
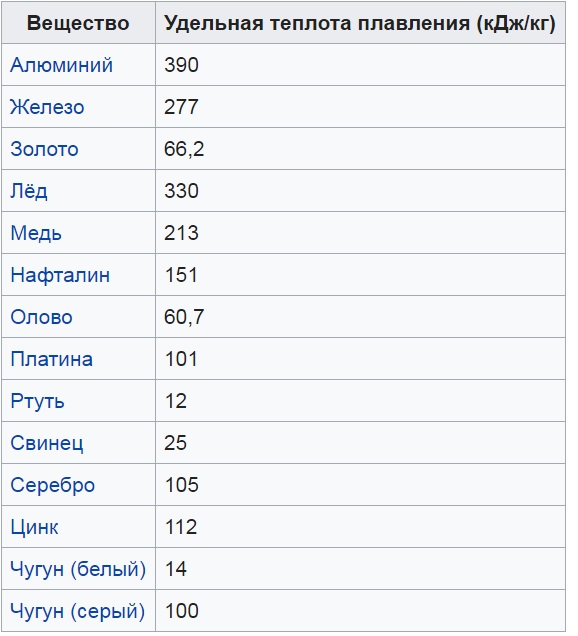 Это повышает химическую активность материала, что делает его восприимчивым к воздействию веществ во внешней среде. Одновременно с этим при нагреве происходит насыщение энергией атомов меди, что делает материал более пластичным. По этой причине ковку медных изделий выполняют именно после нагрева, поскольку без нагрева для изменения формы изделия понадобится большое количество физических усилий (это может быть мускульная сила кузнеца, расходы электроэнергии для запуска электрического пресса и так далее).
Это повышает химическую активность материала, что делает его восприимчивым к воздействию веществ во внешней среде. Одновременно с этим при нагреве происходит насыщение энергией атомов меди, что делает материал более пластичным. По этой причине ковку медных изделий выполняют именно после нагрева, поскольку без нагрева для изменения формы изделия понадобится большое количество физических усилий (это может быть мускульная сила кузнеца, расходы электроэнергии для запуска электрического пресса и так далее). - При достижении температуры 1083 градусов кристаллическая медная решетка начинается постепенно разрушаться, что превращает твердую медь в жидкую. На физическом уровне происходит следующее — из-за избытка энергии атомы начинают двигаться в кристаллической решетке более интенсивно и хаотично, что приводит к частому столкновению атомов между собой. В конечном счете это разрушает решетку, хотя за счет взаимного столкновения и притяжения атомы не разлетаются в разные стороны. На физическом уровне такая структура материала соответствует жидкости (то есть такому состоянию вещества, при котором атомы находятся в относительно свободном движении, но не разлетаются в разные стороны подобно газу).
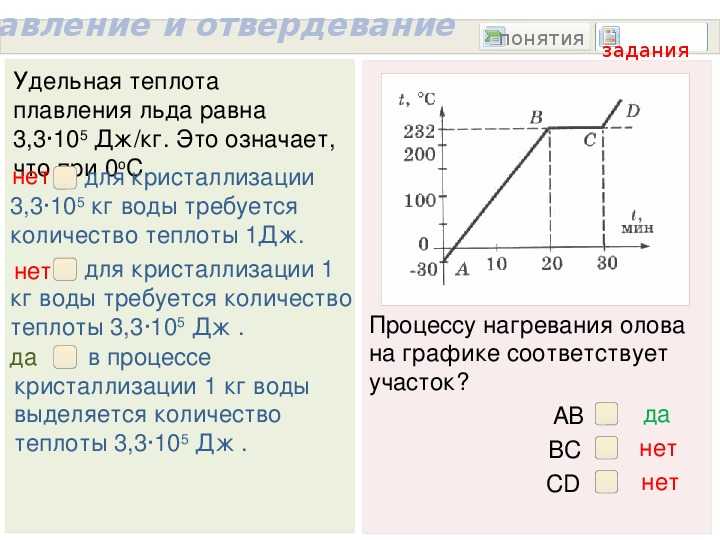
- При остывании медной жидкости ниже температуры 1083 градусов происходит постепенная кристаллизация вещества. Медь вновь обретает твердую форму (чем ниже температура, тем интенсивней происходит затвердение вещества). Однако при необходимости жидкую медь можно и дальше нагревать (на химическом уровне будет происходить дальнейшее насыщение атомов энергией). При достижении температуры 2595 градусов по Цельсию жидкость начнет закипать, а медь начнет принимать газообразную форму. На практике длительное удержание вещества в газообразной форме проблематично — при контакте с атмосферным воздухом вещество будет быстро остывать, обратно превращаясь в жидкость. Чтобы обойти это ограничение, используются разные технологии. Оптимальная — нагрев вещества в тугоплавкой камере с поддержанием стабильной температуры выше критической точки (то есть выше температуры 2595 градусов). В таком случае температура среды будет высокой, а остывание вещества происходить не будет.
Чтобы расплавить/испарить медное изделие с помощью высокоточного нагревательного прибора, нагревать рекомендуется до чуть более высокой температуры.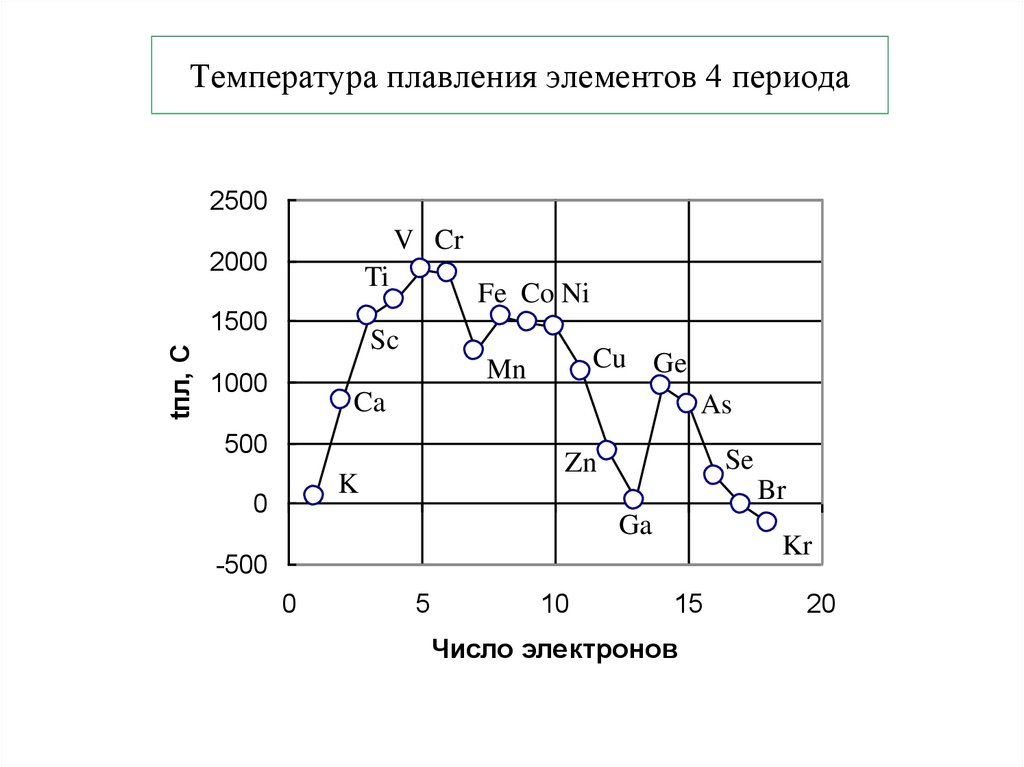 Скажем, в случае расплавления нагревать изделие следует до температуры 1100-1200 градусов (а не 1083 градусов). С практической точки зрения объясняется это просто — нагрев вещества происходит неравномерно, поэтому некоторые фрагменты медного изделия будут долго держать свою форму, тогда как другие — быстро расплавятся. К тому же вещество будет постоянно остывать, что может привести к кристаллизации отдельных фрагментов расплава.
Скажем, в случае расплавления нагревать изделие следует до температуры 1100-1200 градусов (а не 1083 градусов). С практической точки зрения объясняется это просто — нагрев вещества происходит неравномерно, поэтому некоторые фрагменты медного изделия будут долго держать свою форму, тогда как другие — быстро расплавятся. К тому же вещество будет постоянно остывать, что может привести к кристаллизации отдельных фрагментов расплава.
Плавление сплавов на основе меди
На практике медь используют не только в качестве чистого вещества, но и в виде различных сплавов. Примеры таких сплавов — бронза, латунь, мельхиор и другие. Так как сплавы являются многокомпонентными веществами, то их плавление происходит по другому принципу. Рассмотрим примерный алгоритм плавления медных сплавов на примере латуни:
- При температуре до 100 градусов Цельсия кристаллическая решетка является устойчивой и однородной. В случае удара происходит деформация материала. На поверхности материала имеется тонкая оксидная пленка, которая защищает изделие от воздействия воды, атмосферного воздуха, химически активных веществ.

- При нагреве латуни до 100 градусов внешняя пленка постепенно плавится, что делает вещество менее прочным. Также из-за повреждения защитной пленки увеличивается химическая активность материала (то есть он начинает более активно вступать в реакцию с водой, воздухом, химическими веществами). Кристаллическая решетка устойчива к небольшому нагреву, поэтому материал сохраняет свою форму.
- Температура 880 градусов — это точка солидуса. При достижении этой температуры начинается расплавление самых легкоплавких элементов, входящих в состав сплава. Это приводит к частичному переходу твердого вещества в жидкость. На химическом уровне при достижении точки солидуса происходит частичное разрушение кристаллической решетки вещества, однако у более тугоплавких фракций решетка сохраняется.
- Температура 950 градусов — это точка ликвидуса. При достижении этой отметки плавятся самые тугоплавкие фракции, которые сохраняют свою твердость при более низких температурах. В результате на химическом уровне материал полностью становится жидким, поскольку полностью разрушается кристаллическая решетка у всех компонентов, входящих в состав латуни.

Как расплавить медь в домашних условиях?
Обычно медь и сплавы на ее основе плавят в специальных печах, где происходит не только расплавление материала, но и формовка новых деталей. Однако при желании медные изделия можно расплавить и в домашних условиях. Температура плавления меди в домашних условиях будет стандартной — 1083 градусов. Опытные металлурги рекомендуют нагревать вещество с небольшим запасом, чтобы минимизировать теплопотери и не допустить повторной кристаллизации вещества при его охлаждении. Во время домашнего расплавления необходимо соблюдать правила техники безопасности. Ниже мы рассмотрим эти правила, а потом узнаем, как именно нужно проводить домашнюю расплавку медных изделий.
Оборудование и правила техники безопасности
Для расплавления Вам понадобится купить или собрать специальное оборудование. В качестве исходного вещества подойдет чистая медь в слитках или брусках. Также для переплавки можно использовать различные детали и домашнюю утварь, содержащие большое количество меди. Это могут быть декоративные изделия, запчасти авто, очищенные провода и другие. Перед переплавкой проверьте удельное содержание меди (обычно ставится штамп с нужной информацией). Для нагрева объектов понадобится муфельная печь с регулятором температуры.
Это могут быть декоративные изделия, запчасти авто, очищенные провода и другие. Перед переплавкой проверьте удельное содержание меди (обычно ставится штамп с нужной информацией). Для нагрева объектов понадобится муфельная печь с регулятором температуры.
Для расплавления слитков или изделий понадобится не только печь, но и посуда-тигель, в которую будет помещаться медь. При выборе тигля отдайте свое предпочтение посуде, выполненной из тугоплавкой керамики или огнеупорной глины. Эти материалы не трескаются и не деформируются при большой нагреве. Из керамики или огнеупорной глины Вам также нужно выполнить форму, в которую будет заливаться расплавленная медь. Помимо этого Вам понадобится и ряд вспомогательных элементов — металлургические щипцы и крюк для работы с тиглем, древесный уголь (если Вы используете обычную печь), бытовой пылесос для удаления мусора с металлургической площадки и так далее.
Также стоит не забывать о правилах техники безопасности:
- Все работы рекомендуется проводить на улице либо в хорошо проветриваемом большом помещении с нормальным уровнем влажности воздуха.
 Это может быть гараж, пристройка к дому, мастерские.
Это может быть гараж, пристройка к дому, мастерские. - Для металлургических работ человеку понадобится купить защитную одежду, которая будет защищать его тело от маленьких капель расплавленной меди и термического воздействия высоких температур. Защитная одежда должна покрывать не только туловище, но и руки, голову и ноги.
- В случае утечки металла из активной зоны нужно выключить печь, чтобы остановить процедуру переплавки. «Сбежавший» металл необходимо потушить, однако учтите — вода для этих целей не подходит. В случае тушения раскаленного металла водой жидкость может начать распадаться на молекулы кислорода и водорода, что может спровоцировать взрыв (молекулярный водород чрезвычайно взрывоопасен). Для тушения расплавленного металла следует использовать асбестовое одеяло либо сухую кальцинированную соду или хлорид натрия.
Алгоритм расплавления медных изделий
Переплавку медных изделий следует делать так:
- Возьмите медные изделия или слитки и поместите в тигель.
 Тигель с расходными материалами поместите в печь. Начните постепенно нагревать материал: сперва выставите температуру 100 градусов, потом — 200 и так далее. Доведите температуру до 1090-1150 градусов (медь плавится при температуре 1083 градусов, однако нужно брать температуру с небольшим запасом).
Тигель с расходными материалами поместите в печь. Начните постепенно нагревать материал: сперва выставите температуру 100 градусов, потом — 200 и так далее. Доведите температуру до 1090-1150 градусов (медь плавится при температуре 1083 градусов, однако нужно брать температуру с небольшим запасом). - Когда материал расплавится, достаньте его из печи с помощью металлургических щипцов. На поверхности смеси вы увидите остатки оксидной пленки. С помощью крюка ее нужно сдвинуть к одной из стенок тигля, чтобы она не попала в форму. После удаления пленки аккуратно перелейте расплавленную медь в форму (переливать жидкость нужно тонкой струей, чтобы не допустить утечку или распрыскивания металла).
- Выключите муфельную печь, накройте форму огнеупорной крышкой и дождитесь полного остывания формы вместе с расплавленным металлом. При желании Вы можете поставить форму обратно в печь, чтобы минимизировать контакт металла с атмосферным воздухом (однако перед помещением формы убедитесь, что печь выключена).
 После полного остывания и затвердения металла достаньте переплавленную запчасть из формы.При необходимости выполните финальную полировку или шлифовку.
После полного остывания и затвердения металла достаньте переплавленную запчасть из формы.При необходимости выполните финальную полировку или шлифовку.
Заключение
Твердая медь переходит в жидкое состояние при температуре 1083 градуса по Цельсию. Расплавление представляет собой сложный химический процесс, при котором разрушается твердая кристаллическая решетка вещества, что приводит к изменению его формы. Для повышения температуры меди нужно выполнить ее нагрев. На заводах и фабриках для этого используют специальные камеры и печи. Выполнить нагрев вещества можно в домашних условиях — для этого нужно собрать или приобрести мощную печь, которая может нагревать вещества до температуры выше 1100 градусов. Нагревать медь нужно с запасом, что связано с теплопотерями и особенностями процедуры нагрева.
Для переплавки меди в домашних условиях помимо печи нужно подготовить дополнительное оборудование — тигель, металлургические щипцы, крюк, керамическую форму и так далее. Переплавка выполняется просто — с помощью печи медь нагревается до 1083 градусов, а потом она переливается в форму для застывания. Расплавление медных сплавов отличается от расплавления чистой меди. Сплавы характеризуются «плавающей» температурой плавления. Например, латунь плавится при температуре от 880 до 950 градусов в зависимости от концентрации легирующих элементов. Металлурги рекомендуют плавить латуниевый сплав при температуре 950 градусов (точка ликвидуса).
Переплавка выполняется просто — с помощью печи медь нагревается до 1083 градусов, а потом она переливается в форму для застывания. Расплавление медных сплавов отличается от расплавления чистой меди. Сплавы характеризуются «плавающей» температурой плавления. Например, латунь плавится при температуре от 880 до 950 градусов в зависимости от концентрации легирующих элементов. Металлурги рекомендуют плавить латуниевый сплав при температуре 950 градусов (точка ликвидуса).
Используемая литература и источники:
- Лидин Р. А., Молочко В. А., Андреева Л. Л. Химические свойства неорганических веществ. — «Химия», 2000.
- Максимов М. М., Горнунг М. Б. Очерк о первой меди. — М.: Недра, 1976.
- Электротехнический справочник. Т. 1. / Составитель И. И. Алиев. — М. : ИП РадиоСофт, 2006.
- Статья на Википедии
таблица по возрастанию в градусах, самая высокая температура плавления
Plazmen.ru » Сварка
Автор Валерий Шилков На чтение 6 мин Просмотров 19. 5к.
5к.
Металлы и сплавы — это незаменимая основа для литейного и ювелирного производства, ковки и многих других сфер. Что бы ни делал человек из металла (какой бы это ни был процесс), для правильной работы ему нужно знать, при какой температуре плавится тот или иной металл. Мы подробно рассмотрим процесс плавления, его отличие от кипения, а также сравним температуры в таблицах.
Содержание
Таблица температур плавления
Узнать какая нужна температура для плавления металлов, поможет таблица по возрастанию температурных показателей.
| Элемент или соединение | Необходимый температурный режим |
|---|---|
| Литий | +18°С |
| Калий | +63,6°С |
| Индий | +156,6°С |
| Олово | +232°С |
| Таллий | +304°С |
| Кадмий | +321°С |
| Свинец | +327°С |
| Цинк | +420°С |
Таблица плавления среднеплавких металлов и сплавов.
| Элемент либо сплав | Температурный режим |
|---|---|
| Магний | +650°С |
| Алюминий | +660°С |
| Барий | +727°С |
| Серебро | +960°С |
| Золото | +1063°С |
| Марганец | +1246°С |
| Медь | +1083°С |
| Никель | +1455°С |
| Кобальт | +1495°С |
| Железо | +1539°С |
| Дюрали | +650°С |
| Латуни | +950…1050°С |
| Чугун | +1100…1300°С |
| Углеродистые стали | +1300…1500°С |
| Нихром | +1400°С |
Таблица плавления тугоплавких металлов и сплавов.
| Наименование элемента | Температурный режим |
|---|---|
| Титан | +1680°С |
| Платина | +1769,3°С |
| Хром | +1907°С |
| Цирконий | +1855°С |
| Ванадий | +1910°С |
| Иридий | +2447°С |
| Молибден | +2623°С |
| Тантал | +3017°С |
| Вольфрам | +3420°С |
Что такое температура плавления
Каждый металл имеет неповторимые свойства, и в этот список входит температура плавления. При плавке металл уходит из одного состояния в другое, а именно из твёрдого превращается в жидкое. Чтобы сплавить металл, нужно приблизить к нему тепло и нагреть до необходимой температуры – этот процесс и называется температурой плавления. В момент, когда температура доходит до нужной отметки, он ещё может пребывать в твёрдом состоянии. Если продолжать воздействие – металл или сплав начнет плавиться.
При плавке металл уходит из одного состояния в другое, а именно из твёрдого превращается в жидкое. Чтобы сплавить металл, нужно приблизить к нему тепло и нагреть до необходимой температуры – этот процесс и называется температурой плавления. В момент, когда температура доходит до нужной отметки, он ещё может пребывать в твёрдом состоянии. Если продолжать воздействие – металл или сплав начнет плавиться.
Плавление и кипение – это не одно и то же. Точкой перехода вещества из твердого состояния в жидкое, зачастую называют температуру плавления металла. В расплавленном состоянии у молекул нет определенного расположения, но притяжение сдерживает их рядом, в жидком виде кристаллическое тело оставляет объем, но форма теряется.
При кипении объем теряется, молекулы между собой очень слабо взаимодействуют, движутся хаотично в разных направлениях, совершают отрыв от поверхности. Температура кипения – это процесс, при котором давление металлического пара приравнивается к давлению внешней среды.
Для того, чтобы упростить разницу между критическими точками нагрева мы подготовили для вас простую таблицу:
| Свойство | Температура плавки | Температура кипения |
|---|---|---|
| Физическое состояние | Сплав переходит в расплав, разрушается кристаллическая структура, проходит зернистость | Переходит в состояние газа, некоторые молекулы могут улетать за пределы расплава |
| Фазовый переход | Равновесие между твердым состоянием и жидким | Равновесие давления между парами металла и воздухом |
| Влияние внешнего давления | Нет изменений | Изменения есть, температура уменьшается при разряжении |
При какой температуре плавится
Металлические элементы, какими бы они ни были — плавятся почти один в один. Этот процесс происходит при нагреве. Оно может быть, как внешнее, так и внутреннее. Первое проходит в печи, а для второго используют резистивный нагрев, пропуская электричество либо индукционный нагрев. Воздействие выходит практически схожее. При нагреве, увеличивается амплитуда колебаний молекул. Образуются структурные дефекты решётки, которые сопровождаются обрывом межатомных связей. Под процессом разрушения решётки и скоплением подобных дефектов и подразумевается плавление.
Воздействие выходит практически схожее. При нагреве, увеличивается амплитуда колебаний молекул. Образуются структурные дефекты решётки, которые сопровождаются обрывом межатомных связей. Под процессом разрушения решётки и скоплением подобных дефектов и подразумевается плавление.
У разных веществ разные температуры плавления. Теоретически, металлы делят на:
- Легкоплавкие – достаточно температуры до 600 градусов Цельсия, для получения жидкого вещества.
- Среднеплавкие – необходима температура от 600 до 1600 ⁰С.
- Тугоплавкие – это металлы, для плавления которых требуется температура выше 1600 ⁰С.
Плавление железа
Температура плавления железа достаточно высока. Для технически чистого элемента требуется температура +1539 °C. В этом веществе имеется примесь — сера, а извлечь ее допустимо лишь в жидком виде.
Без примесей чистый материал можно получить при электролизе солей металла.
Плавление чугуна
Чугун – это лучший металл для плавки. Высокий показатель жидкотекучести и низкий показатель усадки дают возможность эффективнее пользоваться им при литье. Далее рассмотрим показатели температуры кипения чугуна в градусах Цельсия:
Высокий показатель жидкотекучести и низкий показатель усадки дают возможность эффективнее пользоваться им при литье. Далее рассмотрим показатели температуры кипения чугуна в градусах Цельсия:
- Серый — температурный режим может достигать отметки 1260 градусов. При заливке в формы температура может подниматься до 1400.
- Белый — температура достигает отметки 1350 градусов. В формы заливается при показателе 1450.
Важно! Показатели плавления такого металла, как чугун – на 400 градусов ниже, по сравнению со сталью. Это значительно снижает затраты энергии при обработке.
Плавление стали
Плавления стали при температуре 1400 °C
Сталь — это сплав железа с примесью углерода. Её главная польза — прочность, поскольку это вещество способно на протяжении длительного времени сохранять свой объем и форму. Связано это с тем, что частицы находятся в положении равновесия. Таким образом силы притяжения и отталкивания между частицами равны.
Справка! Сталь плавится при 1400 °C.
Плавление алюминия и меди
Температура плавления алюминия равна 660 градусам, это означает то, что расплавить его можно в домашних условиях.
Чистой меди – 1083 градусов, а для медных сплавов составляет от 930 до 1140 градусов.
От чего зависит температура плавления
Для разных веществ температура, при которой полностью перестраивается структура до жидкого состояния – разная. Если взять во внимание металлы и сплавы, то стоит подметить такие моменты:
- В чистом виде не часто можно встретить металлы. Температура напрямую зависит от его состава. В качестве примера укажем олово, к которому могут добавлять другие вещества (например, серебро). Примеси позволяют делать материал более либо менее устойчивым к нагреву.
- Бывают сплавы, которые благодаря своему химическому составу могут переходить в жидкое состояние при температуре свыше ста пятидесяти градусов. Также бывают сплавы, которые могут «держаться» при нагреве до трех тысяч градусов и выше.
 С учетом того, что при изменении кристаллической решетки меняются физические и механические качества, а условия эксплуатации могут определяться температурой нагрева. Стоит отметить, что точка плавления металла — важное свойство вещества. Пример этому – авиационное оборудование.
С учетом того, что при изменении кристаллической решетки меняются физические и механические качества, а условия эксплуатации могут определяться температурой нагрева. Стоит отметить, что точка плавления металла — важное свойство вещества. Пример этому – авиационное оборудование.
Термообработка, в большинстве случаев, почти не изменяет устойчивость к нагреву. Единственно верным способом увеличения устойчивости к нагреванию можно назвать внесение изменений в химический состав, для этого и проводят легирование стали.
У какого металла самая высокая температура плавления
Вольфрам – самый тугоплавкий металл, 3422 °C (6170 °F).
Твердый, тугоплавкий, достаточно тяжелый материал светло-серого цвета, который имеет металлический блеск. Механической обработке поддается с трудом. При комнатной температуре достаточно хрупок и ломается. Ломкость металла связана с загрязнением примесями углерода и кислорода.
Примечание! Технически, чистый металл при температуре выше 400 °C становится очень пластичным.
Демонстрирует химическую инертность, неохотно вступает в реакции с другими элементами. В природе встречается в виде таких сложных минералов, как: гюбнерит, шеелит, ферберит и вольфрамит.
Вольфрам можно получить из руды, благодаря сложным химическим переработкам, в качестве порошка. Используя прессование и спекание, из него создают детали обычной формы и бруски.
Вольфрам — крайне стойкий элемент к любым температурным воздействиям. По этой причине размягчить вольфрам не могли более сотни лет. Не существовало такой печи, которая смогла бы нагреться до нескольких тысяч градусов по Цельсию. Ученым удалось доказать, что это самый тугоплавкий металл. Хотя бытует мнение, что сиборгий, по некоторым теоретическим данным, имеет большую тугоплавкость, но это лишь предположение, поскольку он является радиоактивным элементом и у него небольшой срок существования.
Оцените автора
Температура плавления меди и ее сплавов, график, характеристики. Как расплавить в домашних условиях
Нахождение в природе
Самородная медь
Промышленное значение имеют халькопирит CuFeS2, также известный как медный колчедан, халькозин Cu2S и борнит Cu5FeS4.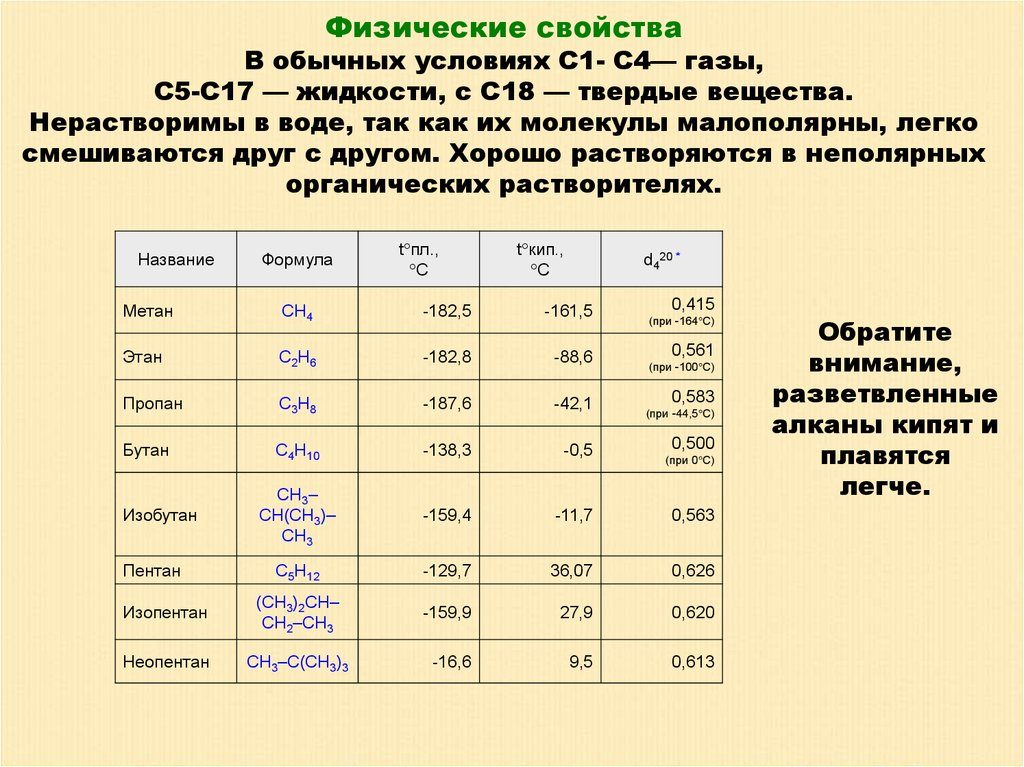 Вместе с ними встречаются и другие минералы меди: ковеллин CuS, куприт Cu2O, азурит Cu3(CO3)2(OH)2, малахит Cu2CO3(OH)2. Иногда медь встречается в самородном виде. Самый большой самородок был найден в Северной Америке, а его вес составлял 420 тонн [2]. Сульфиды меди образуются в основном в среднетемпературных гидротермальных жилах. Также нередко встречаются месторождения меди в осадочных породах — медистые песчаники и сланцы. Наиболее известные из месторождений такого типа — Удокан в Читинской области, Джезказган в Казахстане, меденосный пояс Центральной Африки и Мансфельд в Германии.
Вместе с ними встречаются и другие минералы меди: ковеллин CuS, куприт Cu2O, азурит Cu3(CO3)2(OH)2, малахит Cu2CO3(OH)2. Иногда медь встречается в самородном виде. Самый большой самородок был найден в Северной Америке, а его вес составлял 420 тонн [2]. Сульфиды меди образуются в основном в среднетемпературных гидротермальных жилах. Также нередко встречаются месторождения меди в осадочных породах — медистые песчаники и сланцы. Наиболее известные из месторождений такого типа — Удокан в Читинской области, Джезказган в Казахстане, меденосный пояс Центральной Африки и Мансфельд в Германии.
Большая часть медной руды добывается открытым способом. Содержание меди в руде составляет от 0,4 до 1,0 %.
Купрум: характеристика элемента
Научное наименование меди Cuprum (Купрум) происходит от названия греческого острова Кипр, где медь начали добывать ещё в середине третьего тысячелетия до нашей эры. В периодической таблице Менделеева химический элемент медь имеет 29 атомный (порядковый) номер, находится в 11 группе четвёртого периода. Принадлежит к пластичным переходным металлам. В чистом виде имеет характерный золотисто-розовый цвет. Чистую медь легко окислить, поэтому в естественных условиях она всегда образует на своей поверхности тонкую оксидную плёнку, которая придаёт ей красноватый оттенок.
Принадлежит к пластичным переходным металлам. В чистом виде имеет характерный золотисто-розовый цвет. Чистую медь легко окислить, поэтому в естественных условиях она всегда образует на своей поверхности тонкую оксидную плёнку, которая придаёт ей красноватый оттенок.
Физические свойства
Это второй металл после серебра по уровню электропроводности, что делает её крайне востребованной в современной электронике. Второе ценное качество — высокая теплопроводность, это позволяет её широко применять во всевозможных теплообменниках и в холодильной аппаратуре.
- Температура плавления 1083 градуса.
- Температура кипения 2567 градусов.
- Удельное сопротивление при 20 градусах составляет 1,68·10 -3 Ом·м.
- Плотность 8,92 г/см.
Нахождение в природе
В природе встречается в самородном виде и в виде соединений.
Самые крупные месторождения самородной меди находятся в США в районе озера Верхнего. Именно в этом районе был найден самый крупный медный самородок весом 3560 килограмм. А также много самородной меди встречается в рудных горах Германии.
А также много самородной меди встречается в рудных горах Германии.
В России и на постсоветском пространстве добыча меди происходит путём извлечения из сульфидной руды. Её можно добыть, извлекая из медного колчедана или халькопирита CuFeS2. Наиболее известны такие месторождения, как Удокан в Забайкалье и Джезказган в Казахстане.
Сульфиты меди чаще всего образуются в так называемых среднетемпературных гидротермальных жилах. Могут образовываться и в осадочных породах в виде медистых песчаников и сланцев.
Как правило, медная руда всегда добывается открытым способом. Процентное содержание чистой меди в руде составляет от 0,2 до 1,0 процента в зависимости от месторождения.
Медные сплавы
Являются самыми первыми металлическими сплавами, получение которых человечество освоило ещё на самой заре своего развития. При какой температуре плавится медь, зависит от того, в каком сплаве она находится. В настоящее время наиболее известны и востребованы такие сплавы, как:
- Латунь.
 Сплав с добавление цинка, содержание которого может доходить до 40%. Цинк повышает пластичность и прочность металла. Температура, при которой латунь плавится, составляет 880 — 950 градусов.
Сплав с добавление цинка, содержание которого может доходить до 40%. Цинк повышает пластичность и прочность металла. Температура, при которой латунь плавится, составляет 880 — 950 градусов. - Бронза. Сплав с оловом, с добавлением некоторых других компонентов, таких как кремний, бериллий, свинец. Получать бронзу из меди человек научился ещё в самом начале бронзового века. Бронза не утратила своей актуальности даже с наступлением века железа, например, ещё в начале 20 века стволы пушек изготавливали из так называемой орудийной бронзы. Температура, при которой бронза начинает плавиться, составляет 930 — 1140 градусов.
- Мельхиор. Кроме меди, содержит в своём составе 5−30% никеля. Никель увеличивает прочность медного сплава и повышает его электрическое сопротивление. Кроме того, сильно повышается коррозионная стойкость. Температура плавления — 1170 градусов. По своим внешним характеристикам мельхиор очень похож на серебро, раньше его называли белой медью. Но он обладает более высокой механической прочностью, чем обычное серебро.

- Дюраль, или дюралюминий. Основную массу сплава составляет алюминий 93%, на медь приходится 5%, оставшиеся 2% занимают марганец, железо и магний. Название происходит от названия немецкого города Дюрен, где в 1906 году был впервые получен этот высокопрочный сплав алюминия. Одной из его особенностей является тот факт, что его прочностные характеристики с течением времени имеют тенденцию к увеличению. Поэтому он не теряет своей прочности после нескольких лет эксплуатации, как другие металлы. В настоящее время этот сплав является основой самолётостроения.
- Ювелирные сплавы. Сплавы меди с золотом. Тем самым увеличивается устойчивость драгметалла к механическим воздействиям и истиранию.
Физические свойства
Медь — золотисто-розовый пластичный металл, на воздухе быстро покрывается оксидной плёнкой, которая придаёт ей характерный интенсивный желтовато-красный оттенок. Медь обладает высокой тепло- и электропроводностью (занимает второе место по электропроводности после серебра).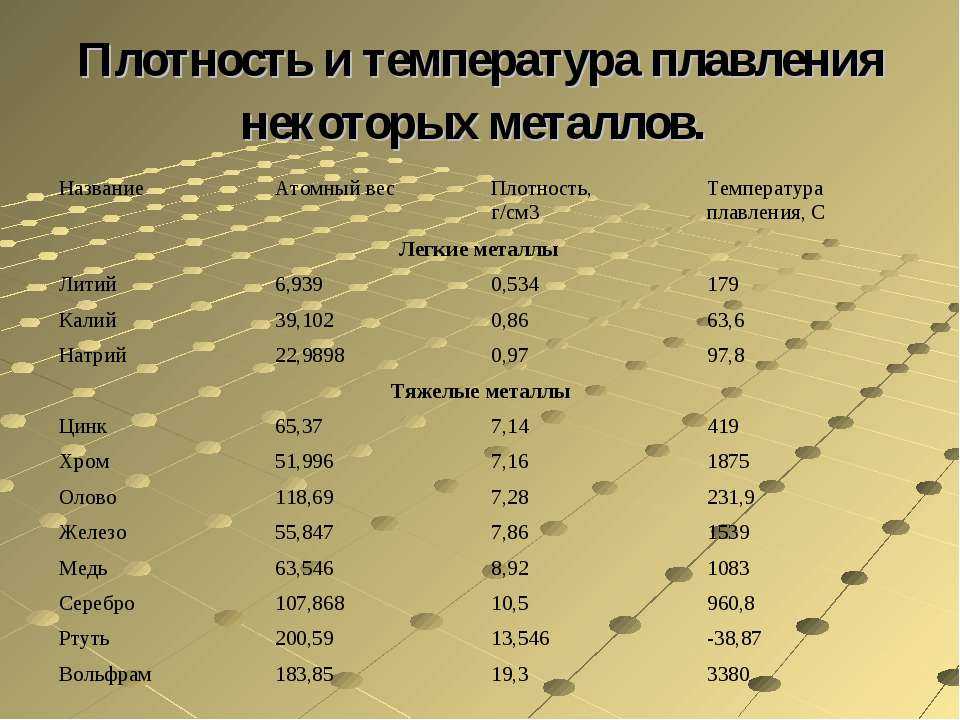 Имеет два стабильных изотопа — 63Cu и 65Cu, и несколько радиоактивных изотопов. Самый долгоживущий из них, 64Cu, имеет период полураспада 12,7 ч и два варианта распада с различными продуктами.
Имеет два стабильных изотопа — 63Cu и 65Cu, и несколько радиоактивных изотопов. Самый долгоживущий из них, 64Cu, имеет период полураспада 12,7 ч и два варианта распада с различными продуктами.
Существует ряд сплавов меди: латунь — сплав меди с цинком, бронза — сплав меди с оловом, мельхиор — сплав меди и никеля, и некоторые другие.
Сплавы меди
Сплавы, повышающие прочность и другие свойства меди, получают введением в нее добавок, таких, как цинк, олово, кремний, свинец, алюминий, марганец, никель. На сплавы идет более 30% меди.
Латуни — сплавы меди с цинком ( меди от 60 до 90% и цинка от 40 до 10%) — прочнее меди и менее подвержены окислению. При присадке к латуни кремния и свинца повышаются ее антифрикционные качества, при присадке олова, алюминия, марганца и никеля возрастает антикоррозийная стойкость. Листы, литые изделия используются в машиностроении, особенно в химическом, в оптике и приборостроении, в производстве сеток для целлюлознобумажной промышленности.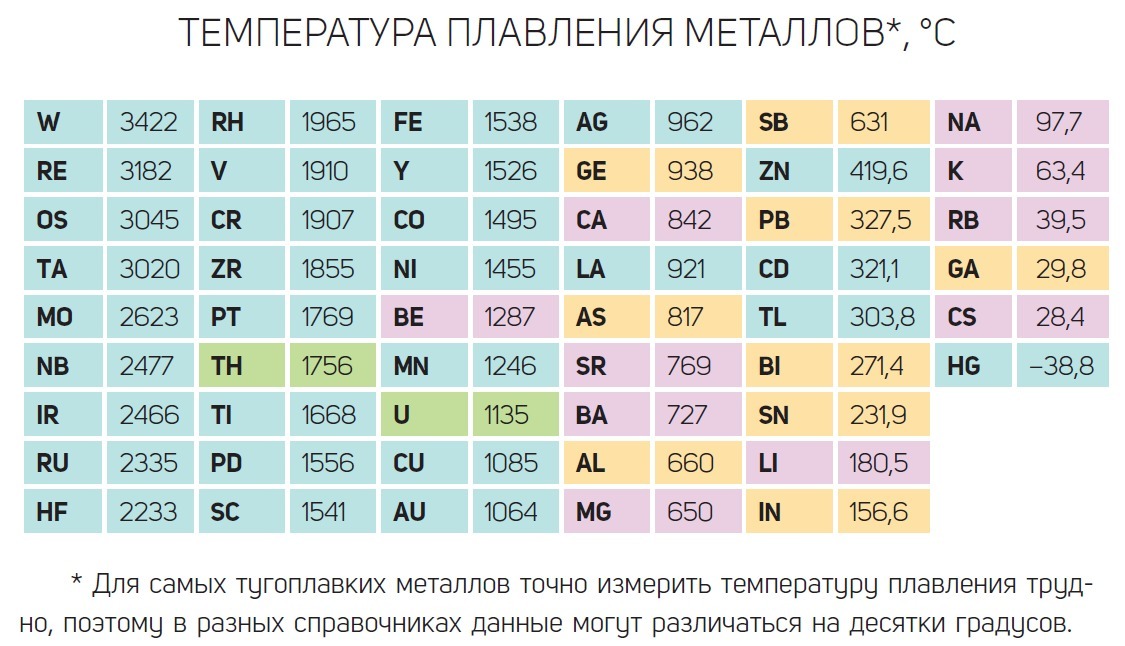
Бронзы. Раньше бронзами называли сплавы меди (80-94%) и олова (20-6%). В настоящее время производят безоловянные бронзы, именуемые по главному вслед за медью компоненту.
- Алюминиевые бронзы содержат 5-11% алюминия, обладают высокими механическими свойствами в сочетании с антикоррозийной стойкостью.
- Свинцовые бронзы, содержащие 25-33% свинца, используют главным образом для изготовления подшипников, работающих при высоких давлениях и больших скоростях скольжения.
- Кремниевые бронзы, содержащие 4-5% кремния, применяют как дешевые заменители оловянных бронз.
- Бериллиевые бронзы, содержащие 1,8-2,3% бериллия, отличаются твердостью после закалки и высокой упругостью. Их применяют для изготовления пружин и пружинящих изделий.
- Кадмиевые бронзы — сплавы меди с небольшим количества кадмия (до1%) — используют при производстве троллейных проводов, для изготовления арматуры водопроводных и газовых линий и в машиностроении.
Припои — сплавы цветных металлов, применяемые при пайке для получения монолитного паяного шва. Среди твердых припоев известен медносеребряный сплав (44,5-45,5% Ag; 29-31% Cu; остальное — цинк).
Среди твердых припоев известен медносеребряный сплав (44,5-45,5% Ag; 29-31% Cu; остальное — цинк).
Бронза
Бронза
Цветной металл для изготовки изделий разных типов начали использовать с древних времен. Данный факт подтверждается найденными материалами при археологических раскопках. Состав бронзы изначально был богат оловом.
Промышленностью выпускается различное количество разновидностей бронзы. Опытный мастер способен по цвету металла определить его предназначение. Однако не каждому под силу определить точную марку бронзы, для этого используется маркировка. Способы производства бронзы подразделяются на литейные, когда происходит плавление и отлив и деформируемые.
Состав металла зависит от предназначения к использованию. Основным показателем является наличие бериллия. Повышенная концентрация элемента в сплаве, подвергнутая процедуре закаливания, может соперничать с высокопрочными сталями. Наличие в составе олова отнимает у металла гибкость и пластичность.
Производство бронзовых сплавов изменилось с древних времен фактически внедрением современного оборудования. Технология с использованием в качестве флюса в виде древесного угля используется до сих пор. Последовательность получения бронзы:
- печь разогревается для требуемой температуры, после этого в нее устанавливается тигель;
- после плавки металл может окислится, во избежание этого добавляют флюс в качестве древесного угля;
- кислотным катализатором служит фосфорная медь, добавление происходит после полного прогрева сплава.
Плавка бронзы
Старинные изделия из бронзы подвержены естественным процессам – патинирование. Зеленоватый цвет с белым оттенком проявляется из-за образования пленки, обволакивающей изделие. Искусственные методы патинирования включают в себя методы с использованием серы и параллельным нагреванием до определенной температуры.
Латунь
Латунь
Сплав на основе меди с добавлением цинка называется латунь.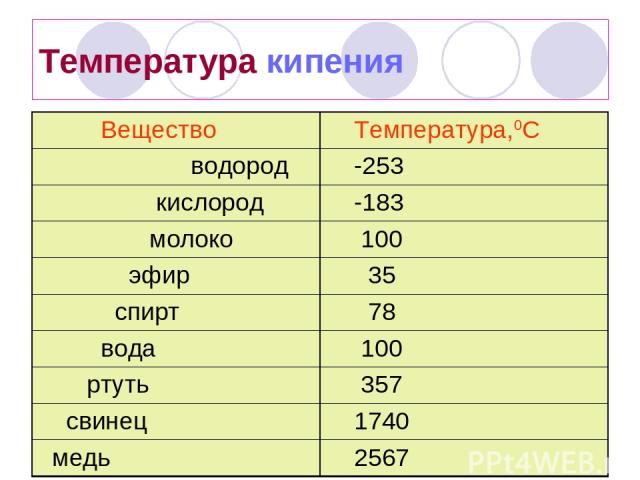 В некоторых ситуациях добавляется олово в меньших пропорциях. Джеймс Эмерсон в 1781 году решил запатентовать комбинацию. Содержание цинка в сплаве может варьироваться от 5 до 45%. Латуни различают в зависимости от предназначения и спецификации:
В некоторых ситуациях добавляется олово в меньших пропорциях. Джеймс Эмерсон в 1781 году решил запатентовать комбинацию. Содержание цинка в сплаве может варьироваться от 5 до 45%. Латуни различают в зависимости от предназначения и спецификации:
- простые, состоящие из двух компонентов – меди и цинка. Маркировка таких сплавов обозначается буквой «Л», напрямую значащая содержание меди в сплаве в процентах;
- многокомпонентные латуни – содержат множество других металлов в зависимости от назначения к использованию. Такие сплавы повышают эксплуатационные свойства изделий, обозначаются также буквой «Л», но с прибавлением цифр.
Физические свойства латуни относительно высокие, коррозийная стойкость на среднем уровне. Большинство сплавов не критично к пониженным температурам, возможно эксплуатировать металл в различных условиях. Технологии получения латуни взаимодействует с процессами медной и цинковой промышленности, обработке вторичного сырья. Эффективным способом плавки является использование электропечи индукционного типа с магнитным отводом и регулировкой температуры.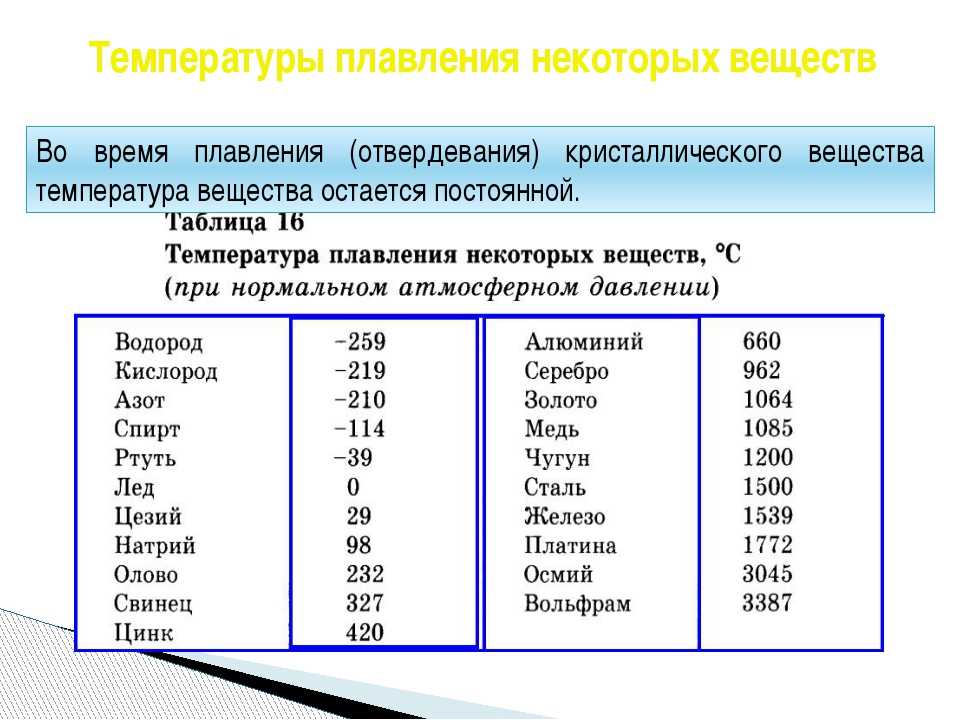 После получения однородной массы, она разливается в формы и подвергается процессам деформации.
После получения однородной массы, она разливается в формы и подвергается процессам деформации.
Плавка латуни
Применение материала в различных отраслях, повышает на него спрос с каждым годом. Сплав применяется в суд строительстве и производстве боеприпасов, различных втулок, переходников, болтов, гаек и сантехнических материалов.
Что такое температура плавления
Каждый металл имеет неповторимые свойства, и в этот список входит температура плавления. При плавке металл уходит из одного состояния в другое, а именно из твёрдого превращается в жидкое. Чтобы сплавить металл, нужно приблизить к нему тепло и нагреть до необходимой температуры – этот процесс и называется температурой плавления. В момент, когда температура доходит до нужной отметки, он ещё может пребывать в твёрдом состоянии. Если продолжать воздействие – металл или сплав начнет плавиться.
Плавление и кипение – это не одно и то же. Точкой перехода вещества из твердого состояния в жидкое, зачастую называют температуру плавления металла.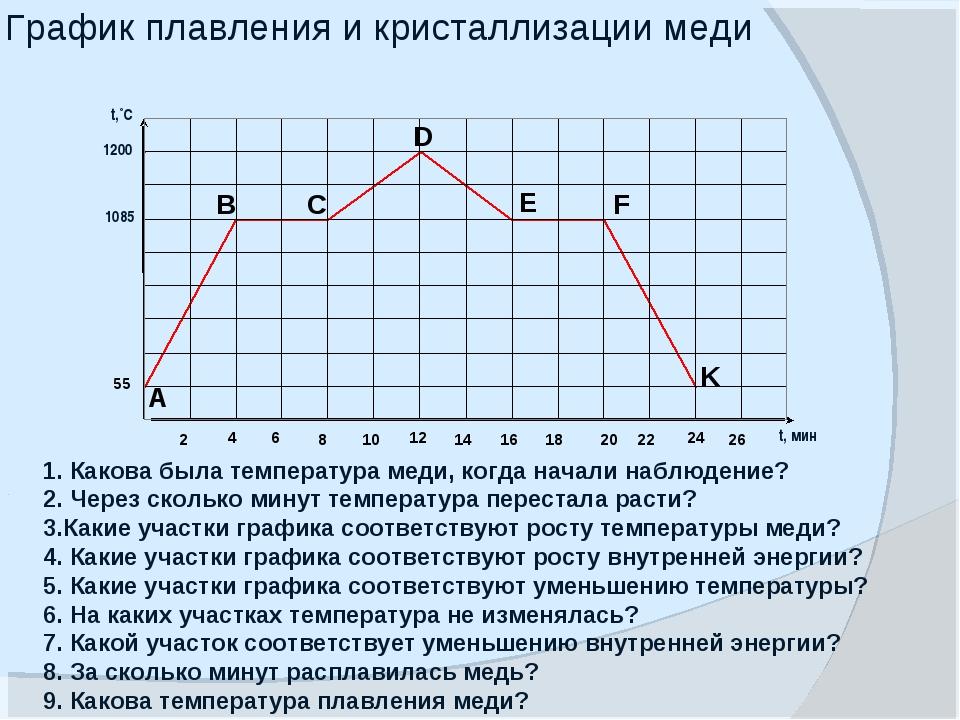 В расплавленном состоянии у молекул нет определенного расположения, но притяжение сдерживает их рядом, в жидком виде кристаллическое тело оставляет объем, но форма теряется.
В расплавленном состоянии у молекул нет определенного расположения, но притяжение сдерживает их рядом, в жидком виде кристаллическое тело оставляет объем, но форма теряется.
При кипении объем теряется, молекулы между собой очень слабо взаимодействуют, движутся хаотично в разных направлениях, совершают отрыв от поверхности. Температура кипения – это процесс, при котором давление металлического пара приравнивается к давлению внешней среды.
Для того, чтобы упростить разницу между критическими точками нагрева мы подготовили для вас простую таблицу:
| Свойство | Температура плавки | Температура кипения |
| Физическое состояние | Сплав переходит в расплав, разрушается кристаллическая структура, проходит зернистость | Переходит в состояние газа, некоторые молекулы могут улетать за пределы расплава |
| Фазовый переход | Равновесие между твердым состоянием и жидким | Равновесие давления между парами металла и воздухом |
| Влияние внешнего давления | Нет изменений | Изменения есть, температура уменьшается при разряжении |
Соединения меди
Оксид меди (I) Cu2O3 и закись меди (I) Cu2O, как и другие соединения меди (I) менее устойчивы, чем соединения меди (II).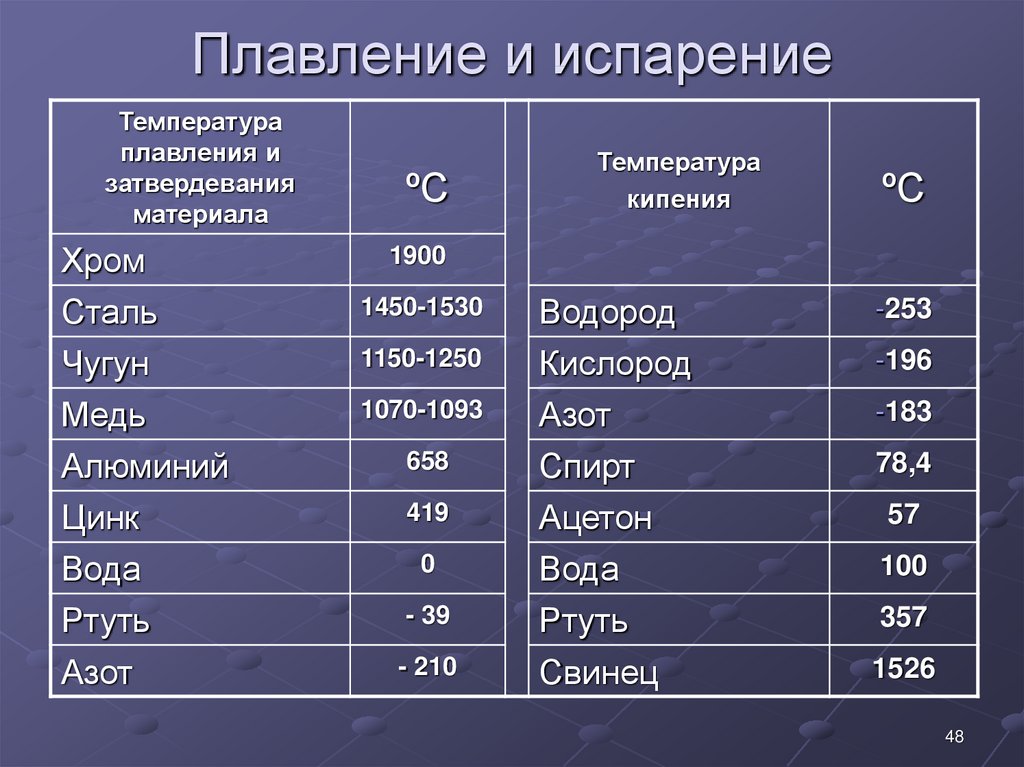 Оксид меди (I), или закись меди Cu2O в природе встречается в виде минерала куприта. Кроме того, она может быть получена в виде осадка красного оксида меди (I) в результате нагревания раствора соли меди (II) и щелочи в присутствии сильного восстановителя.
Оксид меди (I), или закись меди Cu2O в природе встречается в виде минерала куприта. Кроме того, она может быть получена в виде осадка красного оксида меди (I) в результате нагревания раствора соли меди (II) и щелочи в присутствии сильного восстановителя.
Оксид меди (II), или окись меди, CuO — черное вещество, встречающееся в природе (например в виде минерала тенерита). Его получают прокаливанием гидроксокарбоната меди (II) (CuOH)2CO3 или нитрата меди (II) Cu(NO2)2. Оксид меди (II) хороший осислитель.
Гидроксид меди (II) Cu(OH)2 осаждается из растворов солей меди (II) при действии щелочей в виде голубой студенистой массы. Уже при слабом нагревании даже под водой он разлагается, превращаясь в черный оксид меди (II). Гидроксид меди (II) — очень слабое основание. Поэтому растворы солей меди (II) в большинстве случаев имеют кислую реакцию, а со слабыми кислотами медь образует основные соли.
Сульфат меди (II) CuSO4 в безводном состоянии представляет собой белый порошок, который при поглощении воды синеет.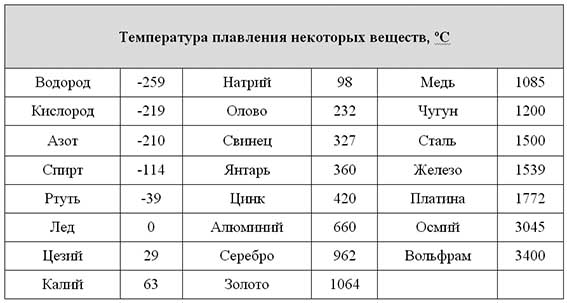 Поэтому он применяется для обнаружения следов влаги в органических жидкостях. Водный раствор сульфата меди имеет характерный сине-голубой цвет. Эта окраска свойственна гидратированным ионам [Cu(h3O)4]2+, поэтому такую же окраску имеют все разбавленные растворы солей меди (II), если только они не содердат каких-либо окрашенных анионов. Из водных растворов сульфат меди кристаллизуется с пятью молекулами воды, образуя прозрачные синие кристаллы медного купороса. Медный купорос применяется для электролитического покрытия металлов медью, для приготовления минеральных красок, а также в качестве исходного вещества при получении других соединений меди. В сельском хозяйстве разбавленный раствор медного купороса применяется для опрыскивания растений и протравливания зерна перед посевом, чтобы уничтожить споры вредных грибков.
Поэтому он применяется для обнаружения следов влаги в органических жидкостях. Водный раствор сульфата меди имеет характерный сине-голубой цвет. Эта окраска свойственна гидратированным ионам [Cu(h3O)4]2+, поэтому такую же окраску имеют все разбавленные растворы солей меди (II), если только они не содердат каких-либо окрашенных анионов. Из водных растворов сульфат меди кристаллизуется с пятью молекулами воды, образуя прозрачные синие кристаллы медного купороса. Медный купорос применяется для электролитического покрытия металлов медью, для приготовления минеральных красок, а также в качестве исходного вещества при получении других соединений меди. В сельском хозяйстве разбавленный раствор медного купороса применяется для опрыскивания растений и протравливания зерна перед посевом, чтобы уничтожить споры вредных грибков.
Хлорид меди (II) CuCl2. 2h3O. Образует темно-зеленые кристаллы, легко растворимые в воде. Очень концентрированные растворы хлорида меди (II) имеют зеленый цвет, разбавленные — сине-голубой. Применяется для получения хлорида меди (II), для приготовления синих и зеленых минеральных красок, а также в пиротехнике.
Применяется для получения хлорида меди (II), для приготовления синих и зеленых минеральных красок, а также в пиротехнике.
Ацетат меди (II) Cu (Ch4COO)2.h3O. Получается обработкой металлической меди или оксида меди (II) уксусной кислотой. Обычно представляет собой смесь основных солей различного состава и цвета (зеленого и сине-зеленого). Под названием ярь-медянка применяется для приготовления масляной краски.
Комплексные соединения меди образуются в результате соединения двухзарядных ионов меди с молекулами аммиака. Из солей меди получают разноообразные минеральные краски. Все соли меди ядовиты. Поэтому, чтобы избежать образования медных солей, медную посуду покрывают изнутри слоем олова (лудят).
Соединения
Медный купорос
В соединениях медь бывает двух степеней окисления: менее стабильную степень Cu+ и намного более стабильную Cu2+, которая даёт соли синего и сине-зелёного цвета. В необычных условиях можно получить соединения со степенью окисления +3 и даже +5.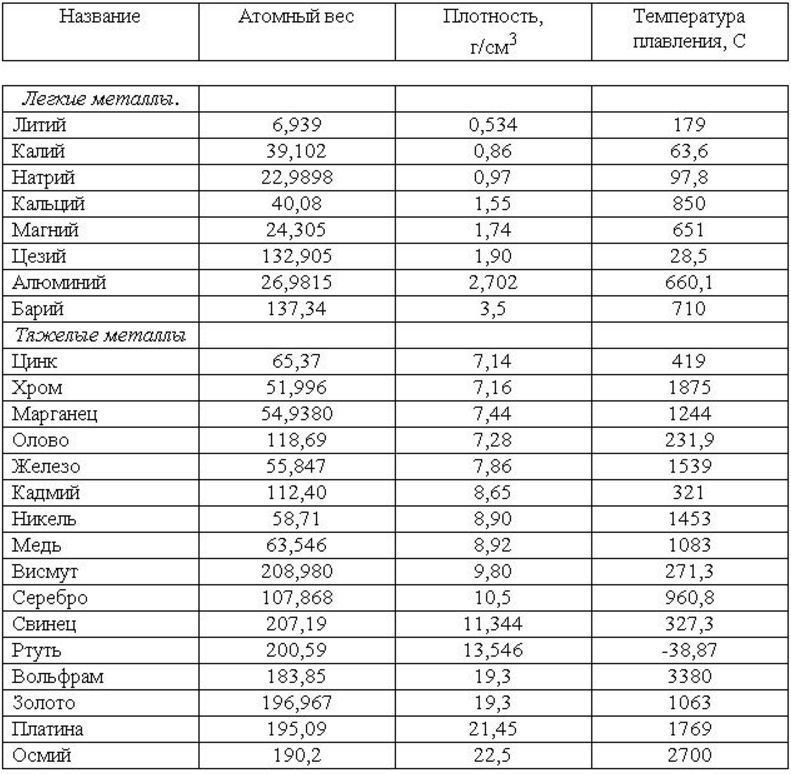 Последняя встречается в солях купраборанового аниона Cu(B11h21)23-, полученных в 1994 году.
Последняя встречается в солях купраборанового аниона Cu(B11h21)23-, полученных в 1994 году.
Карбонат меди(II) имеет зелёную окраску, что является причиной позеленения элементов зданий, памятников и изделий из меди. Сульфат меди(II) при гидратации даёт синие кристаллы медного купороса CuSO4∙5h3O, используется как фунгицид. Также существует нестабильный сульфат меди(I) Существует два стабильных оксида меди — оксид меди(I) Cu2O и оксид меди(II) CuO. Оксиды меди используются для получения оксида иттрия бария меди (YBa2Cu3O7-δ), который является основой для получения сверхпроводников. Хлорид меди(I) — бесцветные кристаллы (в массе белый порошок) плотностью 4,11 г/см³. В сухом состоянии устойчив. В присутствии влаги легко окисляется кислородом воздуха, приобретая сине-зелёную окраску. Может быть синтезирован восстановлением хлорида меди(II) сульфитом натрия в водном растворе.
От чего зависит температура плавления
Для разных веществ температура, при которой полностью перестраивается структура до жидкого состояния – разная.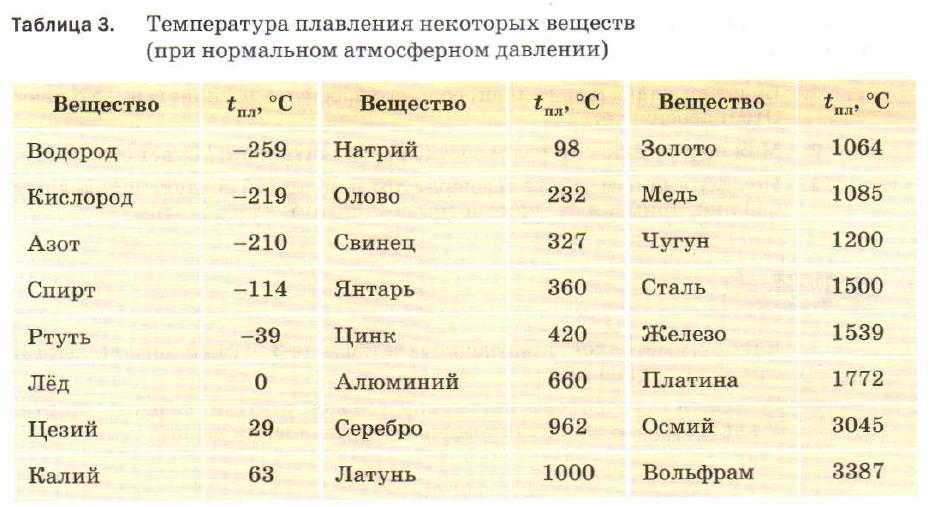 Если взять во внимание металлы и сплавы, то стоит подметить такие моменты:
Если взять во внимание металлы и сплавы, то стоит подметить такие моменты:
- В чистом виде не часто можно встретить металлы. Температура напрямую зависит от его состава. В качестве примера укажем олово, к которому могут добавлять другие вещества (например, серебро). Примеси позволяют делать материал более либо менее устойчивым к нагреву.
- Бывают сплавы, которые благодаря своему химическому составу могут переходить в жидкое состояние при температуре свыше ста пятидесяти градусов. Также бывают сплавы, которые могут «держаться» при нагреве до трех тысяч градусов и выше. С учетом того, что при изменении кристаллической решетки меняются физические и механические качества, а условия эксплуатации могут определяться температурой нагрева. Стоит отметить, что точка плавления металла — важное свойство вещества. Пример этому – авиационное оборудование.
Термообработка, в большинстве случаев, почти не изменяет устойчивость к нагреву. Единственно верным способом увеличения устойчивости к нагреванию можно назвать внесение изменений в химический состав, для этого и проводят легирование стали.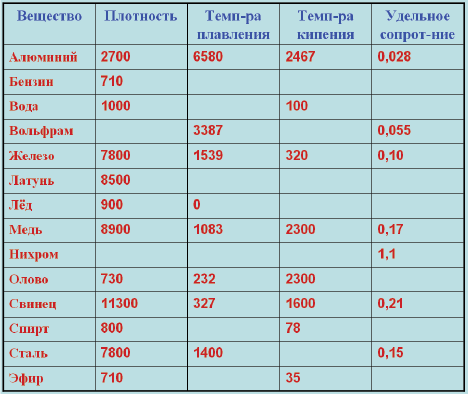
Способы получения меди
В природе медь существует в соединениях и в виде самородков. Соединения представлены оксидами, гидрокарбонатами, сернистыми и углекислыми комплексами, а также сульфидными рудами. Самые распространённые руды — это медный колчедан и медный блеск. Содержание меди в них составляет 1-2%. 90% первичной меди добывают пирометаллургическим способом и 10% гидрометаллургическим.
1. Пирометаллургический способ включает в себя такие процессы: обогащение и обжиг, плавка на штейн, продувка в конвертере, электролитическое рафинирование. Обогащают медные руды методом флотации и окислительного обжига. Сущность метода флотации заключается в следующем: частицы меди, взвешенные в водной среде, прилипают к поверхности пузырьков воздуха и поднимаются на поверхность. Метод позволяет получить медный порошкообразный концентрат, который содержит 10-35% меди.
Окислительному обжигу подлежат медные руды и концентраты со значительным содержанием серы. При нагреве в присутствии кислорода происходит окисление сульфидов, и количество серы снижается почти в два раза. Обжигу подвергаются бедные концентраты, в которых содержится 8-25% меди. Богатые концентраты, содержащие 25-35% меди, плавят, не прибегая к обжигу.
При нагреве в присутствии кислорода происходит окисление сульфидов, и количество серы снижается почти в два раза. Обжигу подвергаются бедные концентраты, в которых содержится 8-25% меди. Богатые концентраты, содержащие 25-35% меди, плавят, не прибегая к обжигу.
Следующий этап пирометаллургического способа получения меди – это плавка на штейн. Если в качестве сырья используется кусковая медная руда с большим количеством серы, то плавку проводят в шахтных печах. А для порошкообразного флотационного концентрата применяют отражательные печи. Плавка происходит при температуре 1450 °С.
В горизонтальных конвертерах с боковым дутьём медный штейн продувается сжатым воздухом для того, чтобы произошли процессы окисления сульфидов и феррума. Далее образовавшиеся окислы переводят в шлак, а серу в оксид. В конвертере образуется черновая медь, которая содержит 98,4-99,4% меди, железо, серу, а также незначительное количество никеля, олова, серебра и золота.
Черновая медь подлежит огневому, а далее электролитическому рафинированию. Примеси удаляют с газами и переводят в шлак. В результате огневого рафинирования образуется медь с чистотой до 99,5%. А после электролитического рафинирования чистота составляет 99,95%.
Примеси удаляют с газами и переводят в шлак. В результате огневого рафинирования образуется медь с чистотой до 99,5%. А после электролитического рафинирования чистота составляет 99,95%.
2. Гидрометаллургический способ заключается в выщелачивании меди слабым раствором серной кислоты, а затем выделении металлической меди непосредственно из раствора. Такой способ применяется для переработки бедных руд и не допускает попутного извлечения драгоценных металлов вместе с медью.
При какой температуре плавится
Металлические элементы, какими бы они ни были — плавятся почти один в один. Этот процесс происходит при нагреве. Оно может быть, как внешнее, так и внутреннее. Первое проходит в печи, а для второго используют резистивный нагрев, пропуская электричество либо индукционный нагрев. Воздействие выходит практически схожее. При нагреве, увеличивается амплитуда колебаний молекул. Образуются структурные дефекты решётки, которые сопровождаются обрывом межатомных связей.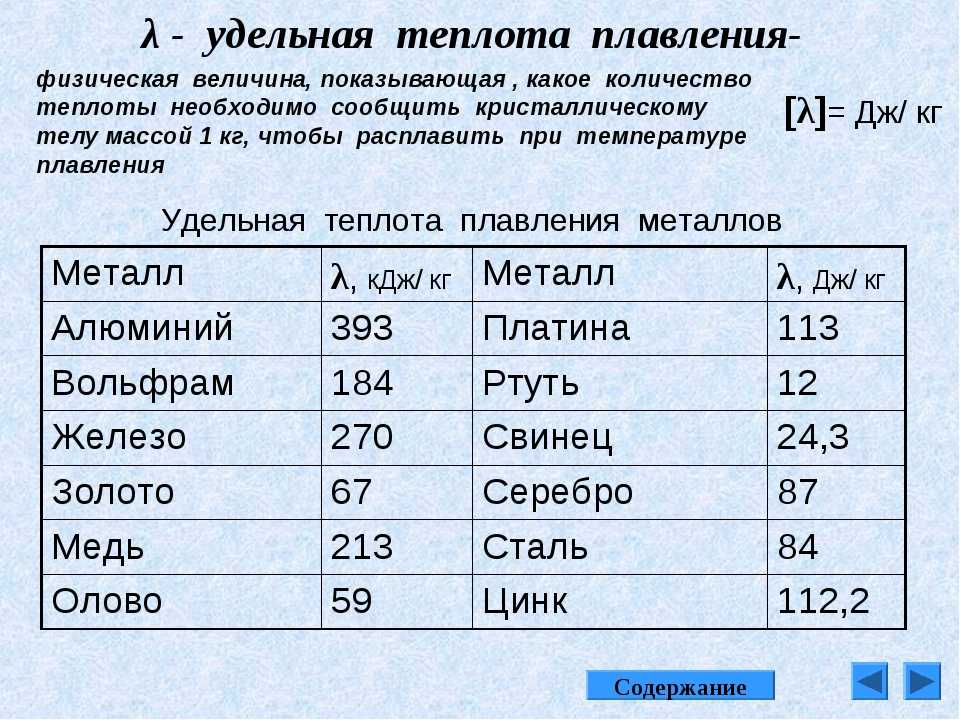 Под процессом разрушения решётки и скоплением подобных дефектов и подразумевается плавление.
Под процессом разрушения решётки и скоплением подобных дефектов и подразумевается плавление.
У разных веществ разные температуры плавления. Теоретически, металлы делят на:
- Легкоплавкие – достаточно температуры до 600 градусов Цельсия, для получения жидкого вещества.
- Среднеплавкие – необходима температура от 600 до 1600 ⁰С.
- Тугоплавкие – это металлы, для плавления которых требуется температура выше 1600 ⁰С.
Плавление железа
Температура плавления железа достаточно высока. Для технически чистого элемента требуется температура +1539 °C. В этом веществе имеется примесь — сера, а извлечь ее допустимо лишь в жидком виде.
Без примесей чистый материал можно получить при электролизе солей металла.
Плавление чугуна
Чугун – это лучший металл для плавки. Высокий показатель жидкотекучести и низкий показатель усадки дают возможность эффективнее пользоваться им при литье. Далее рассмотрим показатели температуры кипения чугуна в градусах Цельсия:
- Серый — температурный режим может достигать отметки 1260 градусов.
 При заливке в формы температура может подниматься до 1400.
При заливке в формы температура может подниматься до 1400. - Белый — температура достигает отметки 1350 градусов. В формы заливается при показателе 1450.
Плавление стали
Сталь — это сплав железа с примесью углерода. Её главная польза — прочность, поскольку это вещество способно на протяжении длительного времени сохранять свой объем и форму. Связано это с тем, что частицы находятся в положении равновесия. Таким образом силы притяжения и отталкивания между частицами равны.
Плавление алюминия и меди
Температура плавления алюминия равна 660 градусам, это означает то, что расплавить его можно в домашних условиях.
Чистой меди – 1083 градусов, а для медных сплавов составляет от 930 до 1140 градусов.
Методы добычи
Медь добывают открытым и закрытым способом. Первый актуален, если руда находится в толще до 500 метров. Для более глубоких залежей строят специальные подземные шахты. Чистую медь получают в основном пирометаллургическим способом, реже – гидрометаллургическим.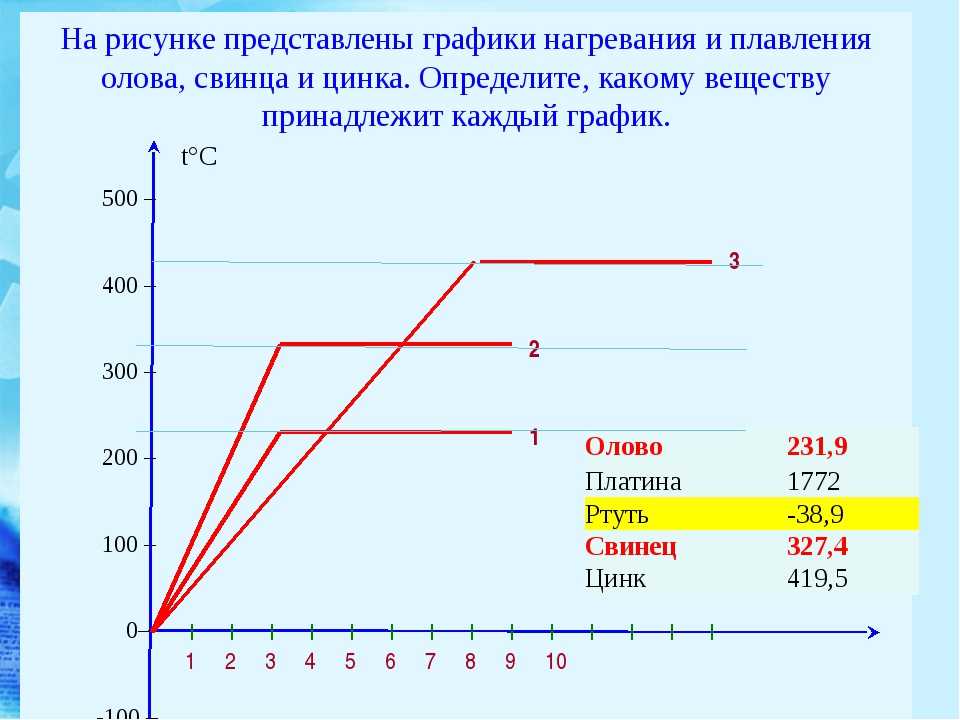
Пирометаллургическая методика условно подразделяется на два этапа, и в качестве исходного сырья использует халькопирит (медный купорос). Первая стадия – флотация или окислительный обжиг. Целью этой технологии является обогащение медной руды, в которой повышена концентрация серы. В процессе обработки, сера удаляется до 1%, другие содержащиеся в руде металлы переводятся в оксидные соединения.
Химические формулы процесса:
- ZnS + 1.5O2 = ZnO + SO2 + Q – реакция протекает при температуре, превышающей +800 градусов;
- ZnS + 2O2 = ZnSO2 + Q – оптимальная температура варьируется в пределах +600/+700 градусов.
После этого, обогащённая руда плавится в шахтных печах при температуре + 14 500 градусов, преобразуясь в сплав, состоящий из сульфидов железа и меди (штейн). Чтобы повысить качество, проводится конвертерный обдув без подачи топлива. Содержание меди в таком сплаве составляет примерно 91%. Вторая стадия – рафинирование, после чего медная составляющая увеличивается до 99.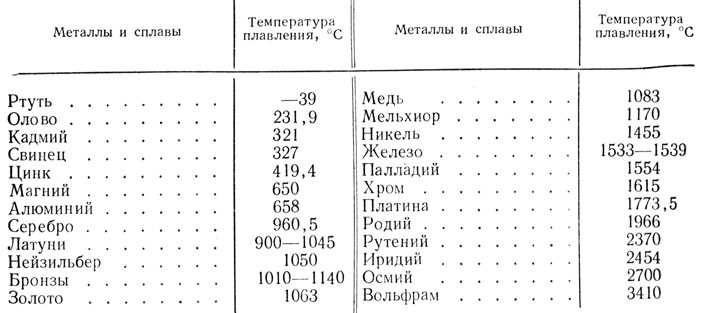 9%.
9%.
Гидрометаллургический способ основывается на выщелачивании. Для этого руду дробят на небольшие куски, и заливают растворителями:
- Nh5OH;
- h3SO4;
- Fe (SO4).
В результате получается раствор, в котором выделяется медь и другие металлы. Формулы процесса:
- CuO+h3SO4>CuSO4+h3O – выщелачивание серной кислотой;
- CuSO4+2Fe2SO4>4FeSO4+2CuSO+S – применение сульфата железа;
- Cu2S + 2 Fe2 (SО4)3>2 СuSO4 + 4 FeSO4 + S – выщелачивание сернокислым железом.
Полученный раствор проходит последующую обработку для извлечения металла. Например, может использоваться методика цементации: CuSО4 + Fe>FeSО4 + Cu. Здесь в состав добавляются куски железа, заменяющие медную составляющую в сернокислых солях.
Применение меди
Благодаря ценным качествам медь и медные сплавы используются в электротехнической и электромашиностроительной отрасли, в радиоэлектронике и приборостроении. Существуют сплавы меди с такими металлами, как цинк, олово, алюминий, никель, титан, серебро, золото. Реже применяются сплавы с неметаллами: фосфором, серой, кислородом. Выделяют две группы медных сплавов: латуни (сплавы с цинком) и бронзы (сплавы с другими элементами).
Реже применяются сплавы с неметаллами: фосфором, серой, кислородом. Выделяют две группы медных сплавов: латуни (сплавы с цинком) и бронзы (сплавы с другими элементами).
Медь обладает высокой экологичностью, что допускает её использование в строительстве жилых домов. К примеру, медная кровля за счёт антикоррозионных свойств, может прослужить больше ста лет без специального ухода и покраски.
Медь в сплавах с золотом используется в ювелирном деле. Такой сплав увеличивает прочность изделия, повышает стойкость к деформированию и истиранию.
Для соединений меди характерна высокая биологическая активность. В растениях медь принимает участие в синтезе хлорофилла. Поэтому её можно увидеть в составе минеральных удобрений. Недостаток меди в организме человека может вызвать ухудшение состава крови. Она есть в составе многих продуктов питания. К примеру, этот металл содержится в молоке. Однако важно помнить, что избыток соединений меди может вызвать отравление. Именно поэтому нельзя готовить пищу в медной посуде.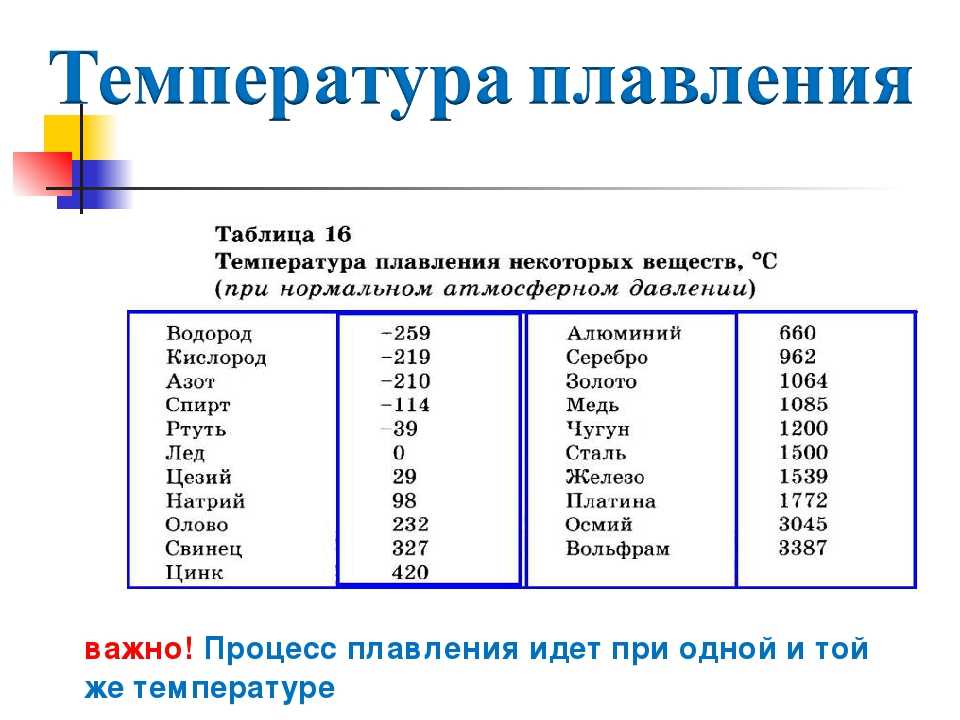 Во время кипячения в пищу может попасть большое количество меди. Если же посуда внутри покрыта слоем олова, то опасности отравления нет.
Во время кипячения в пищу может попасть большое количество меди. Если же посуда внутри покрыта слоем олова, то опасности отравления нет.
В медицине медь используют, как антисептическое и вяжущее средство. Она является компонентом глазных капель от конъюнктивита и растворов от ожогов.
Температура плавления меди
При нормальных условиях температура плавления меди составляет 1083 градусов по шкале Цельсия. А во время нагрева происходит ряд превращений на молекулярном уровне, что приводит к изменению свойств вещества. Чтобы разобраться во всех этих изменениях, нужно рассмотреть основные этапы нагрева и расплавления медного слитка. Примерный график плавления меди выглядит так:
- В нормальном состоянии при температуре от 0 до 100 градусов внутри меди образуется прочная кристаллическая решетка, которая обеспечивает материалу большую устойчивость, упругость, химическую инертность. Решетка является достаточно прочной, однако в случае сильной деформации может происходить пространственное изменение положения атомов в решетке.
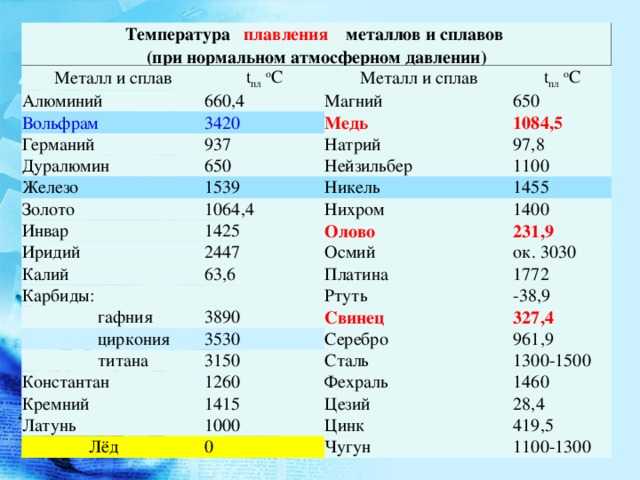 Этим объясняется ковкость и пластичность медных изделий, которые могут сгибаться и деформироваться (скажем, при кузнечной обработке или в случае пресса).
Этим объясняется ковкость и пластичность медных изделий, которые могут сгибаться и деформироваться (скажем, при кузнечной обработке или в случае пресса). - В нормальном состоянии при температуре от 0 до 100 градусов на поверхности медного изделия также образуется тонкая оксидная пленка. Наличие такой пленки является большим плюсом для изделия, поскольку она выполняет множество важных функций — минимизирует контакт с внешними веществами, защищает материал от коррозии, немного увеличивает прочность. В случае охлаждения материала ниже температуры 0 градусов сама медь сохраняет все свои физические свойства. Однако оксидная пленка при охлаждении становится менее упругой и плотной, изделие становится менее твердым (хотя с практической точки зрения это снижение прочности практически незаметно).
- При нагреве материала выше температуры 100 градусов происходит постепенная деструкция оксидной пленки на поверхности металла. Это повышает химическую активность материала, что делает его восприимчивым к воздействию веществ во внешней среде.
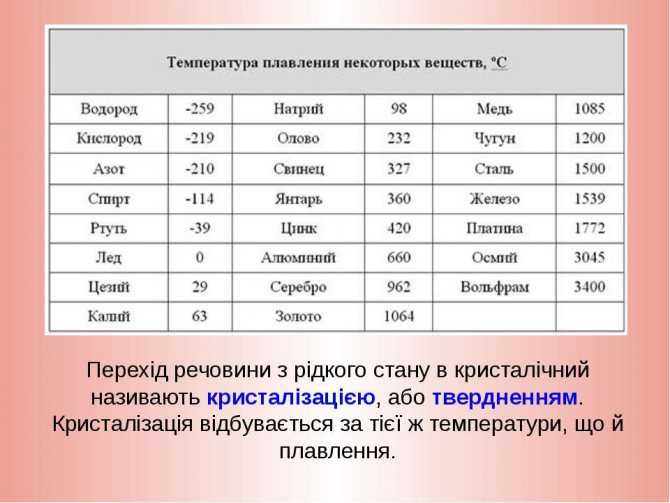 Одновременно с этим при нагреве происходит насыщение энергией атомов меди, что делает материал более пластичным. По этой причине ковку медных изделий выполняют именно после нагрева, поскольку без нагрева для изменения формы изделия понадобится большое количество физических усилий (это может быть мускульная сила кузнеца, расходы электроэнергии для запуска электрического пресса и так далее).
Одновременно с этим при нагреве происходит насыщение энергией атомов меди, что делает материал более пластичным. По этой причине ковку медных изделий выполняют именно после нагрева, поскольку без нагрева для изменения формы изделия понадобится большое количество физических усилий (это может быть мускульная сила кузнеца, расходы электроэнергии для запуска электрического пресса и так далее). - При достижении температуры 1083 градусов кристаллическая медная решетка начинается постепенно разрушаться, что превращает твердую медь в жидкую. На физическом уровне происходит следующее — из-за избытка энергии атомы начинают двигаться в кристаллической решетке более интенсивно и хаотично, что приводит к частому столкновению атомов между собой. В конечном счете это разрушает решетку, хотя за счет взаимного столкновения и притяжения атомы не разлетаются в разные стороны. На физическом уровне такая структура материала соответствует жидкости (то есть такому состоянию вещества, при котором атомы находятся в относительно свободном движении, но не разлетаются в разные стороны подобно газу).
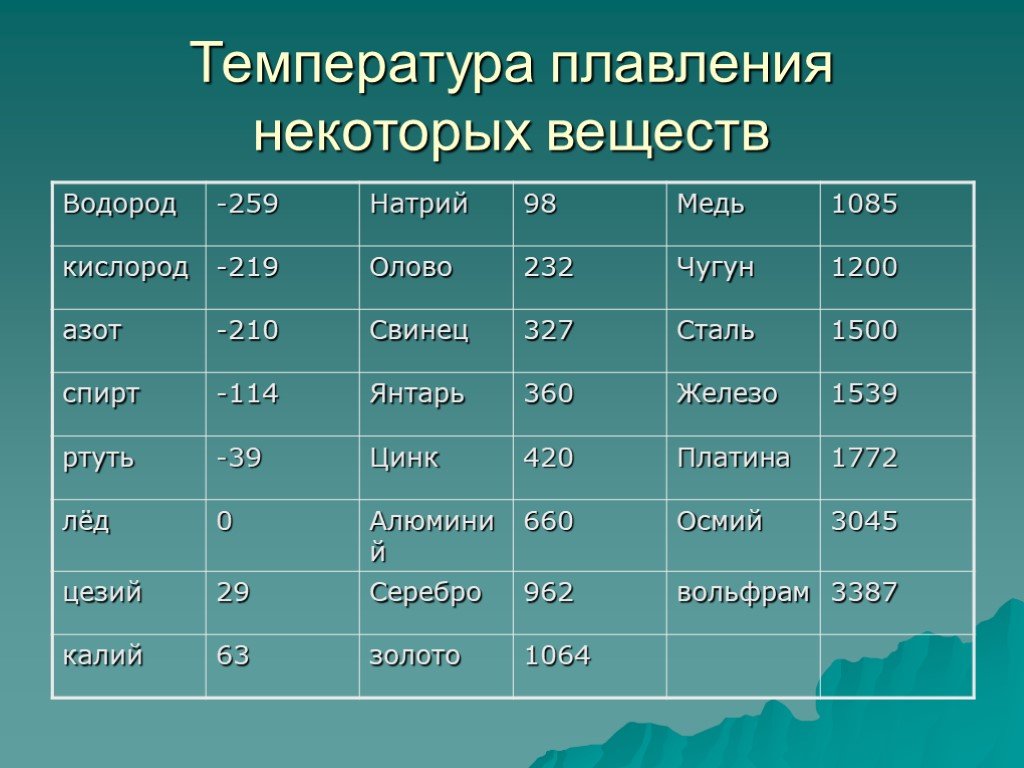
- При остывании медной жидкости ниже температуры 1083 градусов происходит постепенная кристаллизация вещества. Медь вновь обретает твердую форму (чем ниже температура, тем интенсивней происходит затвердение вещества). Однако при необходимости жидкую медь можно и дальше нагревать (на химическом уровне будет происходить дальнейшее насыщение атомов энергией). При достижении температуры 2595 градусов по Цельсию жидкость начнет закипать, а медь начнет принимать газообразную форму. На практике длительное удержание вещества в газообразной форме проблематично — при контакте с атмосферным воздухом вещество будет быстро остывать, обратно превращаясь в жидкость. Чтобы обойти это ограничение, используются разные технологии. Оптимальная — нагрев вещества в тугоплавкой камере с поддержанием стабильной температуры выше критической точки (то есть выше температуры 2595 градусов). В таком случае температура среды будет высокой, а остывание вещества происходить не будет.
Чтобы расплавить/испарить медное изделие с помощью высокоточного нагревательного прибора, нагревать рекомендуется до чуть более высокой температуры.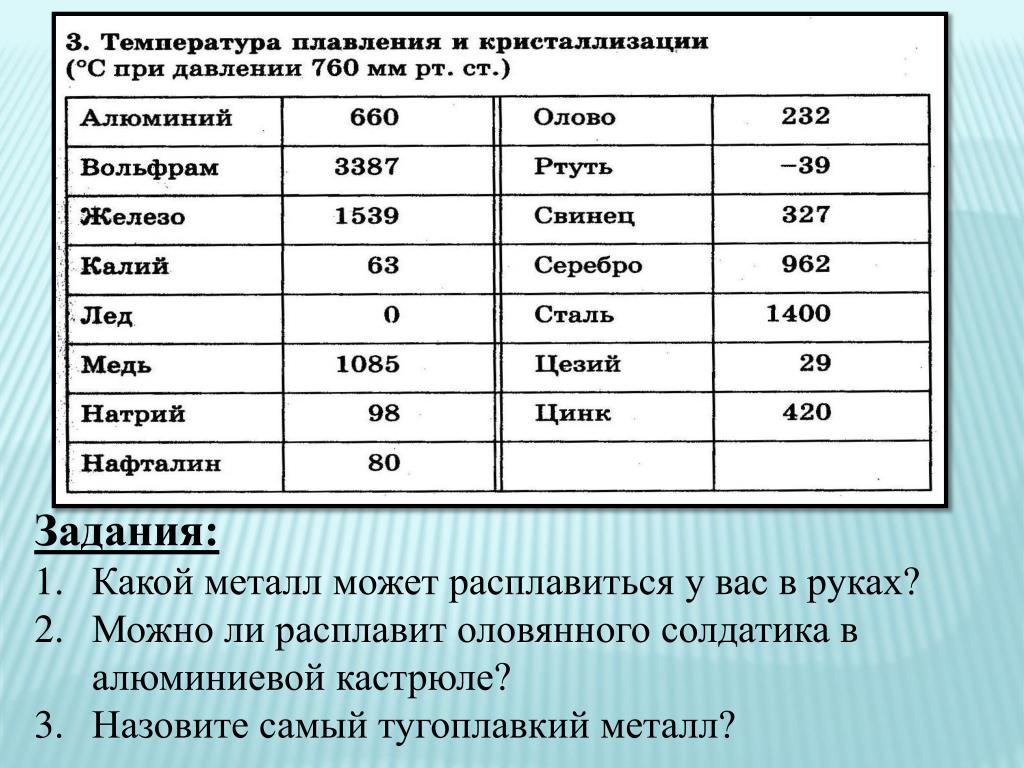 Скажем, в случае расплавления нагревать изделие следует до температуры 1100-1200 градусов (а не 1083 градусов). С практической точки зрения объясняется это просто — нагрев вещества происходит неравномерно, поэтому некоторые фрагменты медного изделия будут долго держать свою форму, тогда как другие — быстро расплавятся. К тому же вещество будет постоянно остывать, что может привести к кристаллизации отдельных фрагментов расплава.
Скажем, в случае расплавления нагревать изделие следует до температуры 1100-1200 градусов (а не 1083 градусов). С практической точки зрения объясняется это просто — нагрев вещества происходит неравномерно, поэтому некоторые фрагменты медного изделия будут долго держать свою форму, тогда как другие — быстро расплавятся. К тому же вещество будет постоянно остывать, что может привести к кристаллизации отдельных фрагментов расплава.
Температура плавления меди по вертикали отложите температуру
Начертите график плавления меди. По вертикали отложите температуру (1 клетка — 40 °С), а по горизонтали — время (1 клетка — 10 мин). Начальная температура меди равна 1000 °С, время нагревания до температуры плавления 20 мин, время перехода меди в жидкое состояние 30 мин. Желательно ответ фото.
Ответы и объяснения 1
Вот, если я все правильно понял
Знаете ответ? Поделитесь им!
Как написать хороший ответ?
Чтобы добавить хороший ответ необходимо:
- Отвечать достоверно на те вопросы, на которые знаете правильный ответ;
- Писать подробно, чтобы ответ был исчерпывающий и не побуждал на дополнительные вопросы к нему;
- Писать без грамматических, орфографических и пунктуационных ошибок.

- Копировать ответы со сторонних ресурсов. Хорошо ценятся уникальные и личные объяснения;
- Отвечать не по сути: «Подумай сам(а)», «Легкотня», «Не знаю» и так далее;
- Использовать мат — это неуважительно по отношению к пользователям;
- Писать в ВЕРХНЕМ РЕГИСТРЕ.
Есть сомнения?
Не нашли подходящего ответа на вопрос или ответ отсутствует? Воспользуйтесь поиском по сайту, чтобы найти все ответы на похожие вопросы в разделе Физика.
Трудности с домашними заданиями? Не стесняйтесь попросить о помощи — смело задавайте вопросы!
Физика — область естествознания: естественная наука о простейших и вместе с тем наиболее общих законах природы, о материи, её структуре и движении.
Источник
Плавление сплавов на основе меди
На практике медь используют не только в качестве чистого вещества, но и в виде различных сплавов. Примеры таких сплавов — бронза, латунь, мельхиор и другие. Так как сплавы являются многокомпонентными веществами, то их плавление происходит по другому принципу.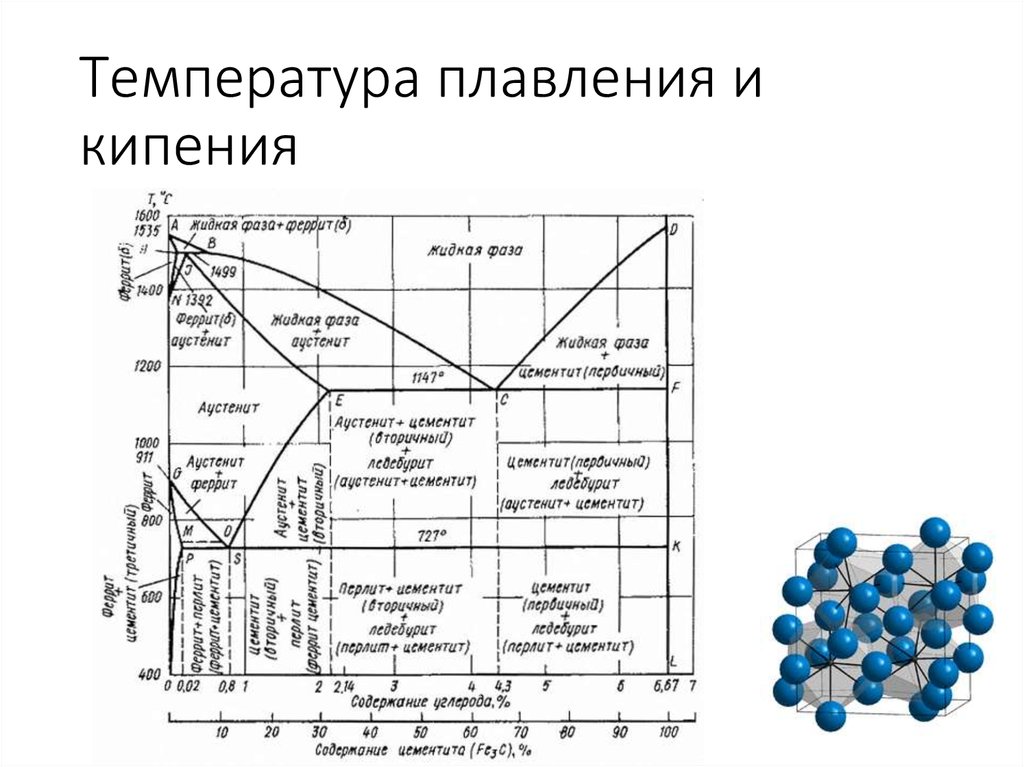 Рассмотрим примерный алгоритм плавления медных сплавов на примере латуни:
Рассмотрим примерный алгоритм плавления медных сплавов на примере латуни:
- При температуре до 100 градусов Цельсия кристаллическая решетка является устойчивой и однородной. В случае удара происходит деформация материала. На поверхности материала имеется тонкая оксидная пленка, которая защищает изделие от воздействия воды, атмосферного воздуха, химически активных веществ.
- При нагреве латуни до 100 градусов внешняя пленка постепенно плавится, что делает вещество менее прочным. Также из-за повреждения защитной пленки увеличивается химическая активность материала (то есть он начинает более активно вступать в реакцию с водой, воздухом, химическими веществами). Кристаллическая решетка устойчива к небольшому нагреву, поэтому материал сохраняет свою форму.
- Температура 880 градусов — это точка солидуса. При достижении этой температуры начинается расплавление самых легкоплавких элементов, входящих в состав сплава. Это приводит к частичному переходу твердого вещества в жидкость.
 На химическом уровне при достижении точки солидуса происходит частичное разрушение кристаллической решетки вещества, однако у более тугоплавких фракций решетка сохраняется.
На химическом уровне при достижении точки солидуса происходит частичное разрушение кристаллической решетки вещества, однако у более тугоплавких фракций решетка сохраняется. - Температура 950 градусов — это точка ликвидуса. При достижении этой отметки плавятся самые тугоплавкие фракции, которые сохраняют свою твердость при более низких температурах. В результате на химическом уровне материал полностью становится жидким, поскольку полностью разрушается кристаллическая решетка у всех компонентов, входящих в состав латуни.
График температуры плавления металла в зависимости от давления
Таблица температур плавления
Узнать какая нужна температура для плавления металлов, поможет таблица по возрастанию температурных показателей.
| Элемент или соединение | Необходимый температурный режим |
| Литий | +18°С |
| Калий | +63,6°С |
| Индий | +156,6°С |
| Олово | +232°С |
| Таллий | +304°С |
| Кадмий | +321°С |
| Свинец | +327°С |
| Цинк | +420°С |
Таблица плавления среднеплавких металлов и сплавов.
| Элемент либо сплав | Температурный режим |
| Магний | +650°С |
| Алюминий | +660°С |
| Барий | +727°С |
| Серебро | +960°С |
| Золото | +1063°С |
| Марганец | +1246°С |
| Медь | +1083°С |
| Никель | +1455°С |
| Кобальт | +1495°С |
| Железо | +1539°С |
| Дюрали | +650°С |
| Латуни | +950…1050°С |
| Чугун | +1100…1300°С |
| Углеродистые стали | +1300…1500°С |
| Нихром | +1400°С |
Таблица плавления тугоплавких металлов и сплавов.
| Наименование элемента | Температурный режим |
| Титан | +1680°С |
| Платина | +1769,3°С |
| Хром | +1907°С |
| Цирконий | +1855°С |
| Ванадий | +1910°С |
| Иридий | +2447°С |
| Молибден | +2623°С |
| Тантал | +3017°С |
| Вольфрам | +3420°С |
Как расплавить медь в домашних условиях?
Обычно медь и сплавы на ее основе плавят в специальных печах, где происходит не только расплавление материала, но и формовка новых деталей.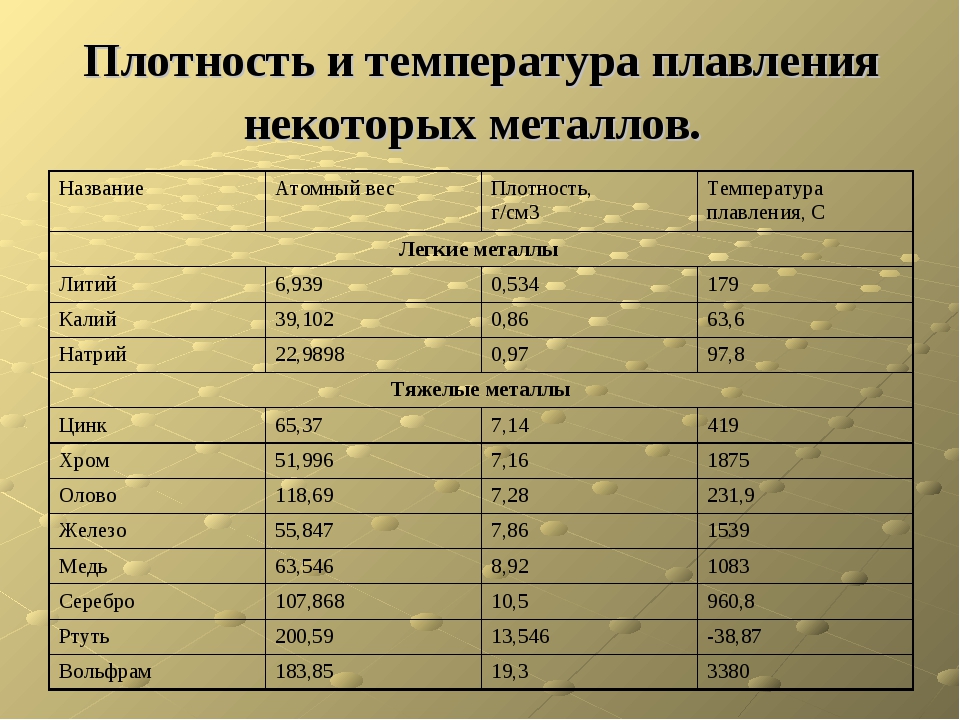 Однако при желании медные изделия можно расплавить и в домашних условиях. Температура плавления меди в домашних условиях будет стандартной — 1083 градусов. Опытные металлурги рекомендуют нагревать вещество с небольшим запасом, чтобы минимизировать теплопотери и не допустить повторной кристаллизации вещества при его охлаждении. Во время домашнего расплавления необходимо соблюдать правила техники безопасности. Ниже мы рассмотрим эти правила, а потом узнаем, как именно нужно проводить домашнюю расплавку медных изделий.
Однако при желании медные изделия можно расплавить и в домашних условиях. Температура плавления меди в домашних условиях будет стандартной — 1083 градусов. Опытные металлурги рекомендуют нагревать вещество с небольшим запасом, чтобы минимизировать теплопотери и не допустить повторной кристаллизации вещества при его охлаждении. Во время домашнего расплавления необходимо соблюдать правила техники безопасности. Ниже мы рассмотрим эти правила, а потом узнаем, как именно нужно проводить домашнюю расплавку медных изделий.
Муфельная печь
Лабораторный муфель – самое удобное устройство для расплавления металла.
Несколько советов, как расплавить медный сплав в лабораторных условиях:
- у муфельной печи есть ручка температурного регулятора, ее нужно поставить на отметку, незначительно превышающую температуру расплавления сплава;
- графитовый или керамический тигель перед загрузкой шихты хорошо прогревают;
- после отливки с горячего тигля проволочным крюком снимают окалину.
Литье в муфеле прогревается равномерно, плавильщик изолирован от летучих вредных компонентов, Через огнеупорное стекло дверцы удобно наблюдать за ходом расплавления меди.
Газовая горелка
Плавка меди в небольших объемах осуществляется ручной газовой горелкой. Мощность портативного устройства большого значения не имеет. Горелку располагают под тиглем, в котором будут плавить медный лом, направляют пламя на донце, языки должны охватывать его полностью. Процесс трудоемкий, длительный. Для защиты от кислорода цветной лом присыпают угольной крошкой.
Горн
Плавят медь в домашних условиях, используя тигельную печь или горн. Он представляет собой ограниченное пространство, куда на подставке помещается тигель. Снизу поджигаются угли или подводится горелка. Необходимо организовать воздухоподдув, чтобы повысить температуру горения топлива. Для ускорения процесса расплавления сверху горн прикрывают плотной крышкой. Хорошо раскаленный древесный уголь разогревают, засыпают в тигель с ломом.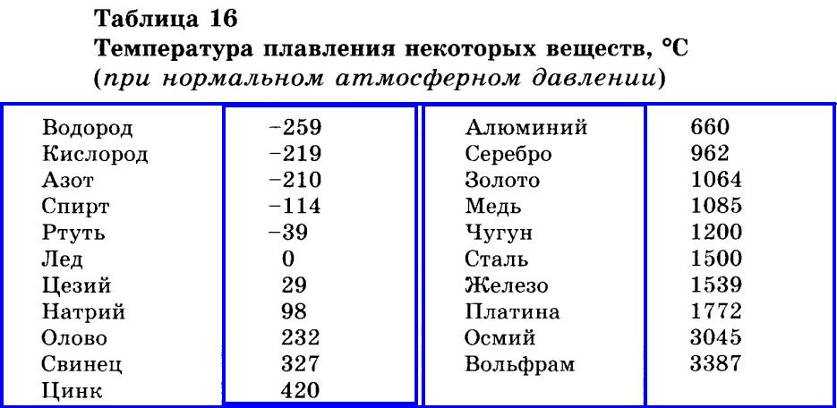 Метод используют специалисты, часто занимающиеся литьем в небольших объемах.
Метод используют специалисты, часто занимающиеся литьем в небольших объемах.
Паяльная лампа
Сплав с цинком, оловом плавится при невысокой температуре. В качестве источника энергии для расплавления используют обычную паяльную лампу, ее располагают вертикально под тиглем так, чтобы пламя охватывало поверхность дна и нижнюю часть боковой стенки. Для снижения объема окалины лом присыпают древесным углем. Процесс окисления при расплавлении под слоем угольной крошки будет протекать не так интенсивно.
Микроволновая печь
Плавить медь в домашних условиях можно в микроволновке, из нее достают поворотный механизм. Под размер тигля делают огнеупорный контейнер с крышкой из шамотного кирпича. Сначала в течение 15 минут на максимальном режиме нагревают керамический тигель, он разогревается до желтоватого свечения. Затем в него засыпают подготовленный лом, снова убирают шамотный контейнер в печь, плавить медный лом необходимо 20-30 минут на максимальном режиме, создается температура порядка +1200°С.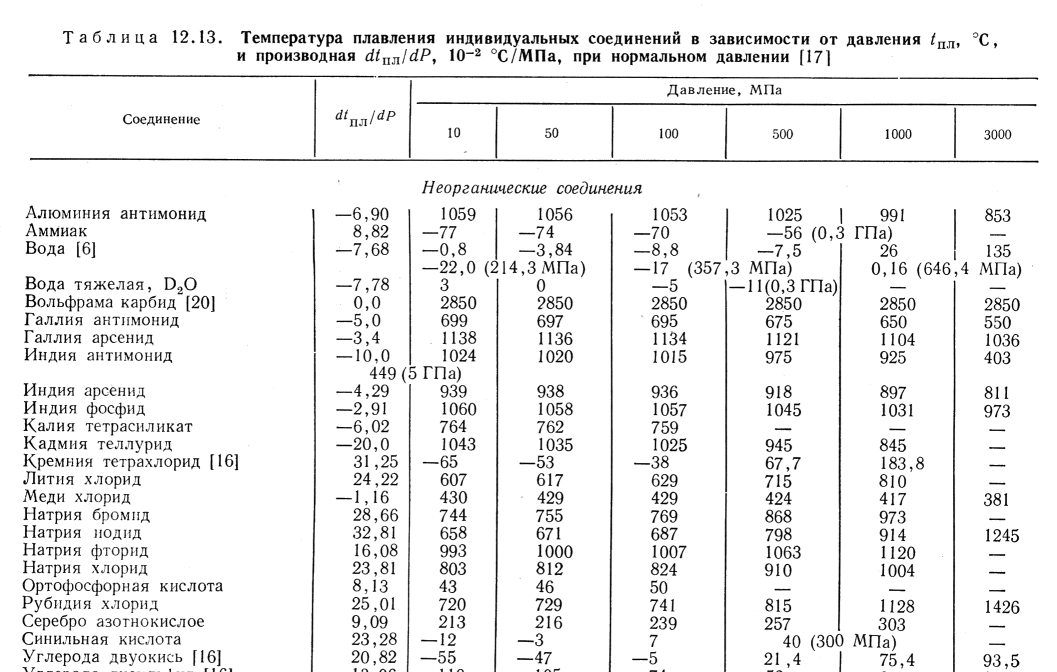 Затем сплав выливают в заранее подготовленную изложницу или форму.
Затем сплав выливают в заранее подготовленную изложницу или форму.
Для изготовления мелких деталей лучше выбирать многокомпонентные сплавы: латуни, бронзы, они не такие текучие, их проще плавить, не нужны слишком высокие температуры. Когда плавят медь в домашних условиях, соблюдают технику безопасности, предусматривают противопожарные меры.
- Главная
- Технологии
График плавления меди
Расплавление любого металла заключается в том, что под воздействием высоких температур разрушается кристаллическая решётка и металл переходит из твёрдого состояния в жидкое. Можно выделить некоторые закономерности, свойственные любому металлу в процессе расплавления:
- Во время нагревания температура внутри металла повышается, но кристаллическая решётка не подвергается разрушению. Металл сохраняет своё твёрдое состояние.
- При достижении температуры плавления, для меди это 1083 градуса, температура внутри металла перестаёт повышаться, несмотря на то что общий нагрев и передача тепла продолжаются.

- После того как вся масса метала переходит в расплавленное состояние, температура внутри металла снова начинает резко повышаться.
В случае процесса охлаждения расплавленного металла происходит всё то же самое, но в обратной последовательности. Сначала происходит резкое снижение температуры внутри металла, затем на значении 1080 градусов падение температуры прекращается до тех пор, пока вся масса метала не перейдёт в твёрдое состояние. После этого температура снова начинает резко падать, пока не сравняется с температурой окружающего воздуха и кристаллизация не завершится окончательно.
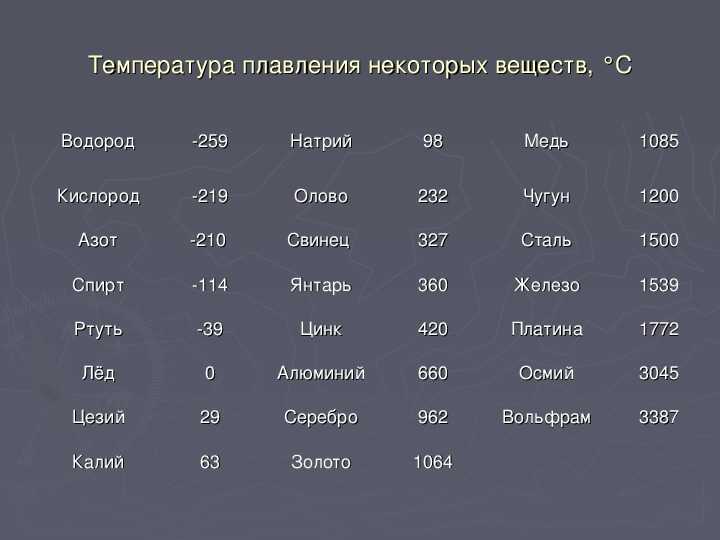
Температура кипения
Медь начинает активно выделять углерод в виде пузырьков газа при температуре 2560 градусов. Внешне это очень напоминает кипение воды. На самом деле это процесс активного окисления меди, в результате которого металл теряет практически все свои уникальные свойства. Детали, отлитые из кипящей меди, имеют в своей структуре большое количество пор, которые будут уменьшать механическую прочность материала и ухудшать его декоративные свойства. Потому в процессе плавки необходимо внимательно следить за температурой и не допускать закипания меди.
Потому в процессе плавки необходимо внимательно следить за температурой и не допускать закипания меди.
Графики плавления и отвердевания
График плавления и отвердевания тела показывает нам все этапы процесса. Из него мы можем извлечь информацию о температуре плавления тела, например, о том, как долго это тело потребовалось нагревать, чтобы достичь той или иной температуры. Для понимания того, как строятся подобные графики, рассмотрим некоторые примеры.
На рисунке представлен график плавления и отвердевания железа.
В начальный момент времени, температура была равна 1200 оС, и пока она не достигла 1539 оС, плавление не началось. Молекулы сохраняли свой порядок, что характерно для твёрдого тела. По достижении температуры плавления, порядок нарушается, поскольку тело переходит в жидкое состояние. Его температура какое-то время остаётся постоянной, о чем свидетельствует горизонтальный участок графика. После того, как железо полностью расплавилось, температура снова начала увеличиваться. Порядок полностью нарушился, поскольку этот участок графика соответствует периоду, когда железо было полностью жидким. Достигнув отметки 1880 оС, железо перестали нагревать, и температура начала падать. Достигнув температуры кристаллизации, железо начало твердеть. Это заняло какое-то время, в течение которого температура вновь не менялась, начал восстанавливаться порядок. После этого, температура стала ниже температуры отвердевания, и железо вновь стало полностью твёрдым, а порядок молекул восстановился. Этому соответствует последний участок графика.
Порядок полностью нарушился, поскольку этот участок графика соответствует периоду, когда железо было полностью жидким. Достигнув отметки 1880 оС, железо перестали нагревать, и температура начала падать. Достигнув температуры кристаллизации, железо начало твердеть. Это заняло какое-то время, в течение которого температура вновь не менялась, начал восстанавливаться порядок. После этого, температура стала ниже температуры отвердевания, и железо вновь стало полностью твёрдым, а порядок молекул восстановился. Этому соответствует последний участок графика.
Упаржнения.
1.
Построить график плавления олова. Температура плавления составляет 232 оС, а начальная температура 200 оС. За 5 мин олово достигнет температуры плавления, и ещё 5 мин будет плавиться. 2,5 мин занимает нагревание олова от температуры плавления до 250 оС, и столько же займет охлаждение до 232 оС.
Итак, возьмём 20 оС за одну клетку по вертикали и 2,5 мин за одну клетку по горизонтали. Тогда первая точка будет иметь координаты 0 минут и 200 градусов, а вторая — 5 минут и 232 градуса. Соединим эти две точки. В этой точке начинается плавление длительностью 5 минут. Температура не меняется, поэтому координаты третьей точки будет 10 минут и 232 градуса. После этого, олово нагревается до 250 градусов за 2,5 минуты, поэтому координаты четвёртой точки будут 12,5 минут и 250 градусов. Это точка является пиком графика, поскольку в этот момент олово достигло наивысшей температуры. Дальше график симметричен, поэтому абсолютно аналогичным способом достраиваем и вторую часть графика.
Соединим эти две точки. В этой точке начинается плавление длительностью 5 минут. Температура не меняется, поэтому координаты третьей точки будет 10 минут и 232 градуса. После этого, олово нагревается до 250 градусов за 2,5 минуты, поэтому координаты четвёртой точки будут 12,5 минут и 250 градусов. Это точка является пиком графика, поскольку в этот момент олово достигло наивысшей температуры. Дальше график симметричен, поэтому абсолютно аналогичным способом достраиваем и вторую часть графика.
Для построения этого графика мы использовали некую начальную информацию о теле. Значит, из готового графика можно извлечь информацию.
2.
На рисунке представлен график плавления и отвердевания для какого-то вещества.
И нам надо найти ответы на вопросы:
— Какой самой высокой температуры достигло вещество?
Итак, смотрим на график. Вертикальная ось соответствует температуре, следовательно, наивысшая температура соответствует пику графика. Это 1250 оС.
— Какова температура плавления данного вещества?
Температуре плавления соответствуют горизонтальные участки графика, поскольку температура остаётся неизменной во время плавления или кристаллизации. На графике видно, что горизонтальные участки соответствуют температуре 1000 оС, поэтому, это и есть температура плавления.
— Сколько времени заняло плавление, и сколько времени заняла кристаллизация?
На графике мы видим, что по горизонтальной оси, соответствующей времени между отметкой 0 и отметкой 40 — две клетки. Длина горизонтальных отрезков тоже составляет две клетки. Поэтому, и плавление, и кристаллизация заняли по 40 минут.
— Какова скорость нагревания данного вещества в твердом состоянии, и какова скорость нагревания в жидком состоянии?
По вертикальной оси расстояние между отметкой 1000 и отметкой 1250 — одна клетка. Следовательно, расстояние в две клетки соответствует пятистам градусам. Тогда, в начальный момент времени, температура составляла 500 градусов. Мы видим на графике, что температура достигла температуры плавления за 40 минут. Поэтому, скорость нагревания в твердом состоянии равна 500 оС за 40 минут, т.е. 12,5 оС/мин.
Мы видим на графике, что температура достигла температуры плавления за 40 минут. Поэтому, скорость нагревания в твердом состоянии равна 500 оС за 40 минут, т.е. 12,5 оС/мин.
На графике видно, что вещество в жидком состоянии нагрелось от 1000 оС до 1250 оС. По горизонтальной оси, длина этого процесса соответствует одной клетке, а, значит, двадцати минутам, т.к. 40 минут — это две клетки. Значит, скорость нагревания в жидком состоянии равна 250 оС за 20 минут, т.е. 12,5 оС/мин.
Следует помнить о том, что нагревание вещества в твердом состоянии на самом деле может происходить не с той же скоростью, что и нагревание вещества в жидком состоянии. Да и зависимость скорости нагревания или остывания от температуры может быть нелинейной. Несмотря на это, даже из такого графика можно извлечь, некоторую информацию.
Данный график предполагает достаточно сложные математические операции для подробного анализа, с которыми мы познакомимся намного позже. Однако, у нас достаточно знаний, чтобы ответить на следующие вопросы:
— Какая максимальная температура была достигнута данным веществом?
Опять же, обращаемся к самой высокой точке.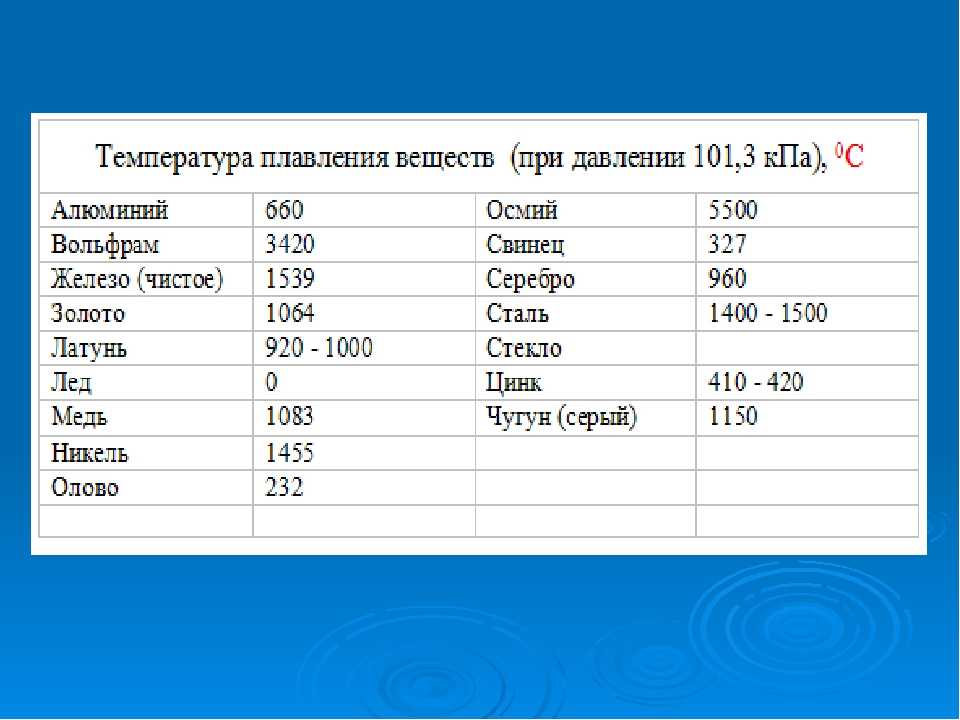 Она соответствует 450 оС.
Она соответствует 450 оС.
Держалась ли в какой-нибудь момент времени постоянная температура свыше 315 оС?
Постоянной температуре будет соответствовать горизонтальный участок графика. На данном графике, такой участок только один. Исходя из того, что отметка 450 оС находится на расстоянии 3 клетки от нулевой отметки по оси температуры, одна клетка соответствует 150 оС, а 2 клетки — 300 оС. Мы видим, что наш горизонтальный участок находится ниже отметки оС градусов, следовательно, температура выше 315 оС не держалась.
— Определите, нагревалось тело или остывало в первые 12 минут?
Одна клетка по горизонтальной оси соответствует 20 минутам. Мы видим, что на промежутке, более длительном, чем 12 минут, температура увеличивалась с течением времени. Следовательно, тело нагревалось.
Определите среднюю скорость нагревания в период с 40 до 100 минут.
Итак, отмечаем на графике интервал от 40 до 100 минут. Мы видим, что в этот период температура менялась по какому-то сложному закону.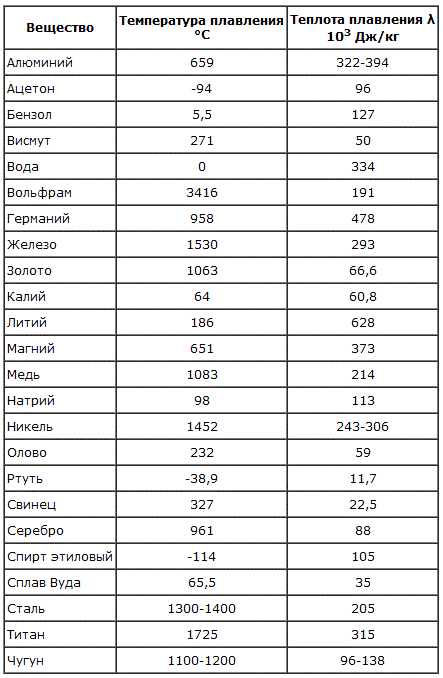 Однако, мы знаем, что бы ни происходило в этот период, температура возросла от 150 оС до 450 оС за 60 минут. Поэтому, в среднем, тело нагревалось со скоростью 300 оС в час или 5 оС в минуту.
Однако, мы знаем, что бы ни происходило в этот период, температура возросла от 150 оС до 450 оС за 60 минут. Поэтому, в среднем, тело нагревалось со скоростью 300 оС в час или 5 оС в минуту.
При построении графиков помните, что очень важно соблюдать масштабирование, т.е. равные интервалы, относящиеся к одной и той же величине, обозначать равным количеством клеток.
Медь — Температура плавления — Температура кипения
Автор
Медь — Температура плавления и кипения
Температура плавления меди 1084,61°2 9000.
Температура кипения меди 2927°C .
Обратите внимание, что эти точки связаны со стандартным атмосферным давлением.
Температура кипения – насыщение
В термодинамике насыщение определяет состояние, при котором смесь пара и жидкости может существовать вместе при данной температуре и давлении.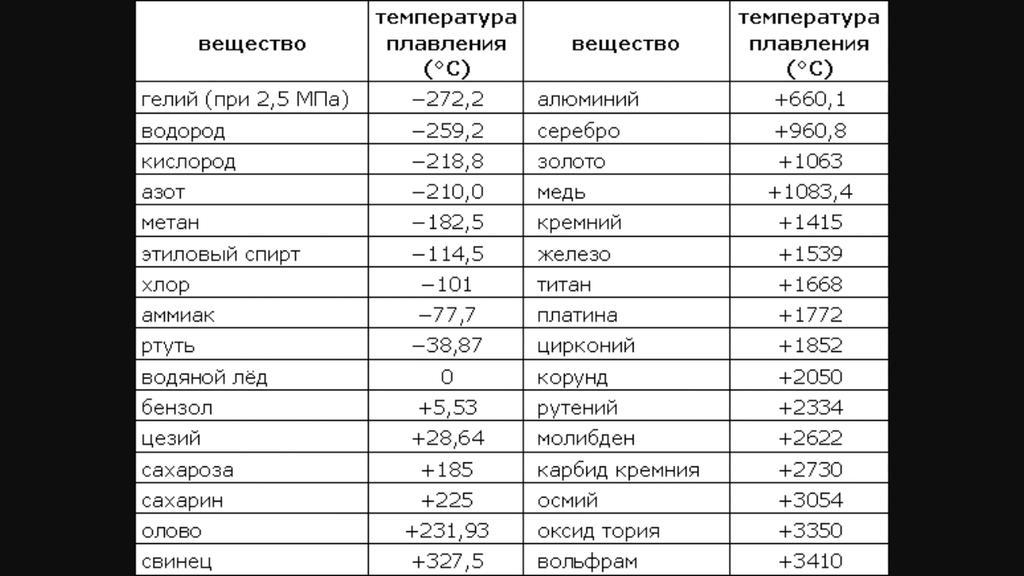 Температура, при которой начинает происходить испарение (кипение) при данном давлении, называется температурой насыщения или точкой кипения . Давление, при котором начинается испарение (кипение) при данной температуре, называется давлением насыщения. Когда ее рассматривают как температуру обратного перехода из пара в жидкость, ее называют точкой конденсации.
Температура, при которой начинает происходить испарение (кипение) при данном давлении, называется температурой насыщения или точкой кипения . Давление, при котором начинается испарение (кипение) при данной температуре, называется давлением насыщения. Когда ее рассматривают как температуру обратного перехода из пара в жидкость, ее называют точкой конденсации.
Точка плавления
В термодинамике точка плавления определяет состояние, при котором твердое тело и жидкость могут существовать в равновесии. Добавление тепла превратит твердое вещество в жидкость без изменения температуры. Температура плавления вещества зависит от давления и обычно указывается при стандартном давлении. Когда ее рассматривают как температуру обратного перехода от жидкого к твердому, ее называют точкой замерзания или точкой кристаллизации.
Первая теория, объясняющая механизм плавления в объеме, была предложена Линдеманном, который использовал колебание атомов в кристалле для объяснения плавления.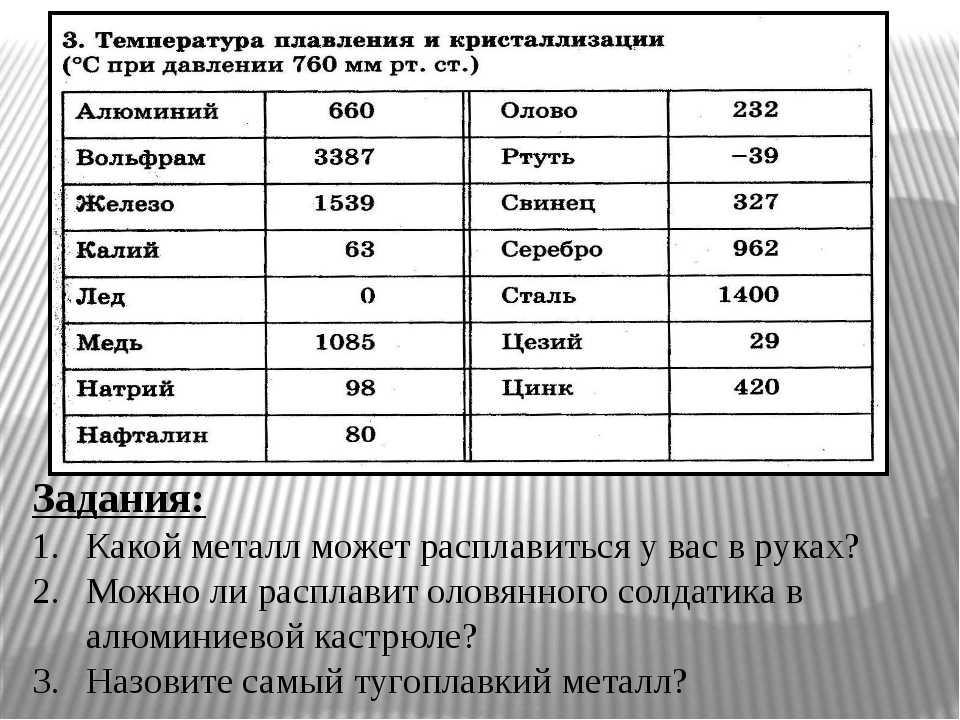 Твердые тела похожи на жидкости тем, что оба находятся в конденсированном состоянии, а частицы находятся гораздо ближе друг к другу, чем частицы газа. Атомы в твердом теле тесно связаны друг с другом либо в правильной геометрической решетке (кристаллические твердые тела, которые включают металлы и обычный лед), либо в неправильной (аморфное твердое тело, такое как обычное оконное стекло), и обычно имеют низкую энергию. движение отдельных атомов , ионов или молекул в твердом теле ограничено колебательным движением вокруг фиксированной точки. Когда твердое тело нагревается, его частицы вибрируют быстрее , поскольку твердое тело поглощает кинетическую энергию. В какой-то момент амплитуда колебаний становится настолько большой, что атомы начинают вторгаться в пространство своих ближайших соседей и возмущать их, и начинается процесс плавления. Точка плавления – это температура, при которой разрушающие вибрации частиц твердого тела преодолевают силы притяжения, действующие внутри твердого тела.
Твердые тела похожи на жидкости тем, что оба находятся в конденсированном состоянии, а частицы находятся гораздо ближе друг к другу, чем частицы газа. Атомы в твердом теле тесно связаны друг с другом либо в правильной геометрической решетке (кристаллические твердые тела, которые включают металлы и обычный лед), либо в неправильной (аморфное твердое тело, такое как обычное оконное стекло), и обычно имеют низкую энергию. движение отдельных атомов , ионов или молекул в твердом теле ограничено колебательным движением вокруг фиксированной точки. Когда твердое тело нагревается, его частицы вибрируют быстрее , поскольку твердое тело поглощает кинетическую энергию. В какой-то момент амплитуда колебаний становится настолько большой, что атомы начинают вторгаться в пространство своих ближайших соседей и возмущать их, и начинается процесс плавления. Точка плавления – это температура, при которой разрушающие вибрации частиц твердого тела преодолевают силы притяжения, действующие внутри твердого тела.
Copper – Properties
| Element | Copper | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Atomic Number | 29 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Symbol | Cu | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Element Category | Transition Metal | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Фаза при STP | Твердое тело | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Атомная масса [а.е.м.] | 63,546 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Плотность при STP [г/см3] | 8,92 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Electron Configuration | [Ar] 3d10 4s1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Possible Oxidation States | +1,2 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Electron Affinity [kJ/mol] | 118.4 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Electronegativity [Pauling scale] | 1.9 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 1st Ionization Energy [eV] | 7.7264 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Year of Discovery | unknown | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Discoverer | unknown | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Thermal properties | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Melting Point [Celsius scale] | 1084.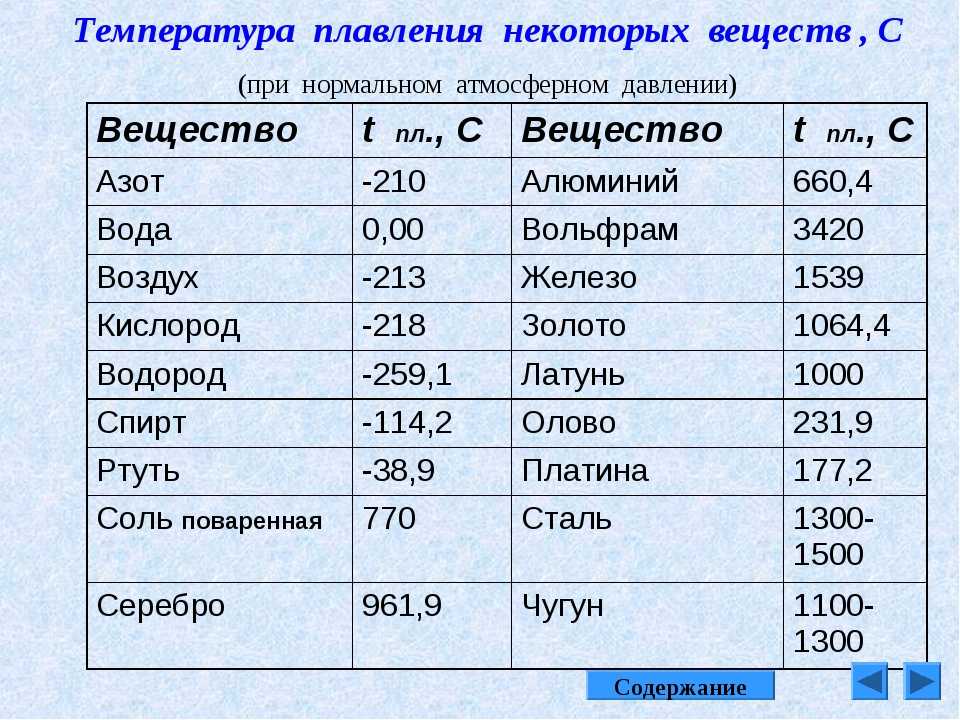 62 62 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Boiling Point [Celsius scale] | 2927 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Thermal Conductivity [W/m K] | 401 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Специфическое тепло [J/G K] | 0,38 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Тепла слияния [KJ/MOL] | 13,05 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ОТРЕЙТА ВАПОРИЗИВА0189
– сообщите об этом объявлении Температура плавления металлов | OnlineMetals.
Температура плавления металлов | OnlineMetals.com® Сэкономьте до 60% на Выберите лист/плиту из углеродистой стали Сегодня!
Один из наиболее часто задаваемых вопросов касается температуры плавления металлов. В зависимости от проекта или конечного использования температура плавления может иметь огромное влияние на результат. Если вы пытаетесь расплавить металл или подвергаете металл воздействию высоких температур, вам нужно знать температуру плавления конкретного материала, который вы используете. Температура плавления сплавов железа и температура плавления стали возникают при более высоких температурах, около 2200-2500 градусов по Фаренгейту (°F) / 1205-1370 градусов по Цельсию (°C). Температура плавления медных сплавов (включая бронзу, чистую медь и латунь) ниже, чем у железа, и колеблется в пределах 1675-1981°F / 913-1082°C.
Стандартные металлы с температурой плавления В этой таблице температур плавления указаны наиболее распространенные металлы, используемые в производстве, в порядке их температур плавления, и они чаще используются из-за таких факторов, как прочность и коррозионная стойкость. Алюминий Латунь, желтая 1660-1710 905-932 Бронза Brass, Red 1810-1880 990-1025 Copper Cast Iron 2060-2200 1127-1204 Carbon Steel 2500-2800 1371-1593 Nickel Кованое железо 2700-2900 1482-1593 Нержавеющая сталь Титан Ниже приведена более подробная таблица металлов, содержащая температуры плавления в градусах Фаренгейта и Цельсия. Мы не возим все эти металлы, но предоставляем их в качестве справочной информации. Какой металл имеет самую низкую температуру плавления? При более низких предельных значениях точки плавления находится ртуть (и алюминиевые сплавы для более часто используемых металлов). У ртути самая низкая температура плавления составляет -38 ° F / -39 ° C, в то время как алюминиевые сплавы плавятся при 865–1240 ° F / 463–671 ° C. Какой металл имеет самую высокую температуру плавления?К верхнему пределу экстремальных температур плавления относится вольфрам (и титан для более часто используемых металлов). Вольфрам имеет самую высокую температуру плавления при чрезвычайно высокой температуре 6,150 ° F / 3,39.9 °C, а титан плавится при 3040 °F / 1670 °C. Guide to Melting Points VideoShop the ProductsMercury Phosphorus Selenium Babbitt Bismuth Cadmium Magnesium Alloys 660-1200 349-649 Алюминиевые сплавы 865-1240 463-671 Алюминиевая бронза 1190-1215 600-655 Magnesium Aluminium Beryllium Copper 1587-1750 865-955 Manganese Bronze 1590-1630 865-890 Silver, Sterling Admiralty Brass 1650-1720 900-940 Латунь, желтый 1660-1710 905-932 Бронз Серебро, чистый Латунь, красный 1810-1880 990-1025 1810-1880 990-1025 0002 Copper Iron, Cast 2060-2200 1127-1204 Iron, Ductile Manganese Beryllium Monel 2370-2460 1300-1350 Hastelloy 2410-2460 1320-1350 Сталь, углерод 2500-2800 1371-1540 Inconel 2540-2600 1390-1425 25440-2600 3995 0-1425 Silicon Nickel Iron, Wrought 2700-2900 1482-1593 Cobalt Steel, Stainless Palladium Titanium Thorium Platinum Chromium Rhodium Ниобий (Колумбий) Молибден Тантал Рений Вольфрам Какова температура плавления меди? | Металлургия | Свойства металлов и неметалловКакова температура плавления меди? 1085 градусов Цельсия – это температура плавления меди. Температура плавления меди – это температура, при которой металл переходит из твердого состояния в жидкое. При этой температуре молекулы металла находятся в постоянном движении, вибрируя и сталкиваясь друг с другом. Энергии этих столкновений достаточно, чтобы преодолеть силы, удерживающие молекулы на месте, и они начинают свободно двигаться. Температура плавления меди 1084 градуса по Цельсию. Можно ли плавить медь дома? Да, вы можете плавить медь в домашних условиях в небольших количествах, но вам необходимо принять некоторые меры предосторожности, чтобы сделать это безопасно. Во-первых, вам понадобится печь, способная достигать высоких температур, необходимых для плавления меди. Во-вторых, вам нужно убедиться, что помещение, где вы работаете, хорошо проветривается, так как пары расплавленной меди могут быть токсичными. Но делать это не рекомендуется, так как это может привести к опасным ситуациям и пожару. Не пытайтесь расплавить медь из-за пожара или несчастного случая. Во избежание несчастных случаев никогда не пытайтесь плавить какие-либо металлы на кухне без вентиляции или защиты. Почему температура плавления меди такая высокая? Высокая температура плавления меди обусловлена прочной металлической связью внутри металла. Атомы меди удерживаются вместе металлическими связями, которые намного прочнее ионных или ковалентных связей в других материалах. Эта прочная связь придает меди высокую температуру плавления, а также высокую электрическую и теплопроводность. Высокая твердость меди также влияет на ее температуру плавления. Медь так же тверда, как сталь, и потребуется значительное количество энергии, чтобы разрушить металлические связи, удерживающие ее вместе. Температура плавления или кипения меди? Температура кипения меди выше, чем ее температура плавления. Температура кипения меди 2590 градусов Цельсия, что выше его температуры плавления в 1084 градуса Цельсия. Это связано с тем, что медь обладает высокой удельной теплоемкостью, что затрудняет ее охлаждение. Таким образом, медь необходимо нагревать до тех пор, пока ее молекулы не начнут свободно двигаться при этой температуре, чтобы она достигла жидкого состояния. Это один из самых плотных металлов в мире. Медные кольца вредны для вас? Медные кольца носить тебе не вредно. Это нетоксичный элемент. Медь является природным элементом. Единственным недостатком медных колец на пальцах может быть аллергия. Медь содержит некоторое количество никеля в следовых количествах, а у некоторых людей никель может вызывать аллергические реакции. Медь считается относительно безопасным металлом при использовании в ювелирных изделиях, хотя у некоторых людей может быть аллергия на него. Некоторые люди считают, что медные кольца могут оказывать негативное воздействие на организм, например, вызывать боль в суставах или нарушать работу организма. Тем не менее, нет никаких научных доказательств в поддержку этих утверждений. Что делает бура при плавке меди? Бура останавливает окисление меди. Чем выше температура, тем лучше работает. Вы можете использовать буру для меди для различных целей, но если вы плавите медь как метод сохранения тепла, вы можете использовать ее в сочетании с другим методом нагрева вашего объекта. Если вы пытаетесь снизить температуру плавления меди, чтобы предотвратить повреждение от контакта с водой или кислородом, то бура не сработает. Стоит ли зачищать медный провод на металлолом? Разбирать стоит, так как цена высока и это не очень дорогое вложение. Также, если вы делаете это в маленькой комнате или с другими людьми, они будут вдыхать пыль. Если рядом с вашим районом много торговцев медью и ломом, лучше продать их, а не грабить. Не стоит зачищать медные провода на металлолом. Можно ли плавить медь в пропановой горниле? Вы можете плавить медь в кузнице пропана. Процесс относительно прост и требует лишь нескольких инструментов и материалов. Во-первых, вам понадобится пропановая кузница. Их можно приобрести в Интернете или в большинстве хозяйственных магазинов. Вам также понадобится термостойкий контейнер для плавки меди. Хорошим вариантом для этого является тигель. Чтобы расплавить медь, просто поместите слиток в горн и включите огонь. Как только медь расплавится, вы можете залить ее в тигель. Дайте ему остыть, прежде чем обращаться с ним. Однако при работе с металлом вы будете подвергаться воздействию высоких температур. Газ пропан также легко воспламеняется и может воспламеняться при высоких температурах, что делает его чрезвычайно опасным. Можно ли плавить медь и алюминий вместе? Одновременно можно плавить медь и алюминий. Температура плавления алюминия 660 градусов Цельсия, а температура плавления меди 1084 градуса Цельсия. Два металла имеют разные температуры плавления, причем медь имеет более высокую температуру плавления, чем алюминий. Это означает, что если вы попытаетесь расплавить их вместе, сначала расплавится алюминий, а затем начнет плавиться медь. Проблема в том, что алюминий при плавлении начнет окисляться, и это загрязнит медь. Во избежание ожогов при работе с расплавленными металлами следует надевать перчатки. Вы также должны убедиться, что помещение, где вы работаете, хорошо проветривается, так как пары металлов могут быть вредными. Однако делать это не рекомендуется, так как это может привести к опасным ситуациям и пожару. Сколько стоит медь? Стоимость меди около 3$. Стоимость меди определяется рыночной ценой на металл. Эта цена определяется множеством факторов, в том числе доступностью металла, глобальными экономическими условиями и себестоимостью производства. Медь используется в самых разных областях, от электропроводки до сантехники, поэтому спрос на этот металл может сильно колебаться. В результате цена на медь также может колебаться, что делает ее волатильной инвестицией. Медь мягкая или твердая? Медь — мягкий металл, ковкий и пластичный. Он также является хорошим проводником тепла и электричества. Медь часто используется в электропроводке и сантехнике. Медь – твердый мягкий металл. Это ковкий металл, и его можно формовать в горячем состоянии. Его также можно вытянуть в проволоку. При воздействии элементов медь окисляется и образует на своей поверхности зеленый слой оксида меди. Как удалить примеси из меди? Для удаления примесей из меди контактируют с расплавом меди вещество, содержащее карбид кремния. Однако это изменит чистоту меди. Примеси связываются с карбидом кремния и медью, оседая на дно. Примеси в меди можно восстановить и использовать повторно, но это приведет к несколько более низкой чистоте металла. Можно ли плавить медь в стальном тигле? Медь можно плавить в стальном тигле. Этот тигель содержит сталь, карбид кремния и никель. Он разработан, чтобы выдерживать высокие температуры, предотвращая плавление сосуда и обеспечивая отсутствие загрязнений на меди. Однако, несмотря на то, что вы можете использовать стальные тигли для плавки меди, их следует использовать только при более низких температурах. Тигель вступит в реакцию с медью, если вы нагреете ее слишком сильно и повредите тигель. Тигель используется для нагрева металлов и плавления их, когда они находятся в твердом состоянии, чтобы их можно было перелить в другой контейнер, когда они станут жидкими. Сталь является хорошей альтернативой использованию керамики. Он не портится при таких же высоких температурах, как керамика, что позволяет плавить металлы, не беспокоясь о разрушении тигля. Какой процент олова добавляют в медь для образования бронзы? 12-процентное олово добавляется к меди для образования бронзы. Сплав нагревают до точки плавления обоих материалов, а затем они смешиваются. Тем не менее, бронза была открыта, когда выяснилось, что добавление большего количества олова облегчает форму металла и повышает его коррозионную стойкость. Бронза в настоящее время используется в тех случаях, когда требуется твердость или коррозионная стойкость, например, в электрооборудовании или оборудовании. При какой температуре кипит медь? Медь кипит при 2560 градусов по Фаренгейту. | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||

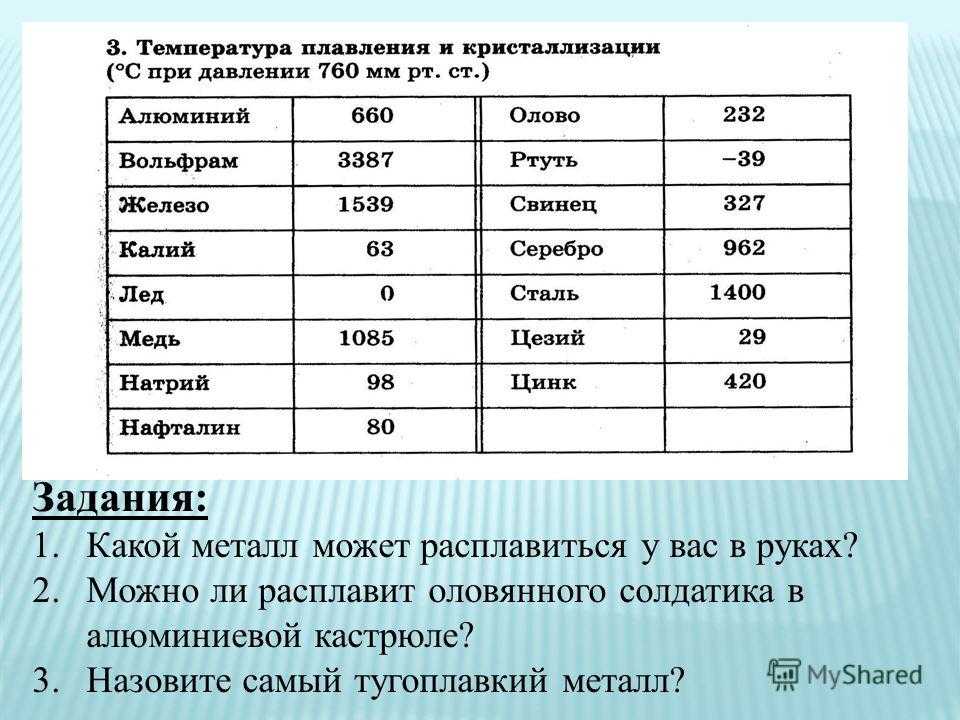
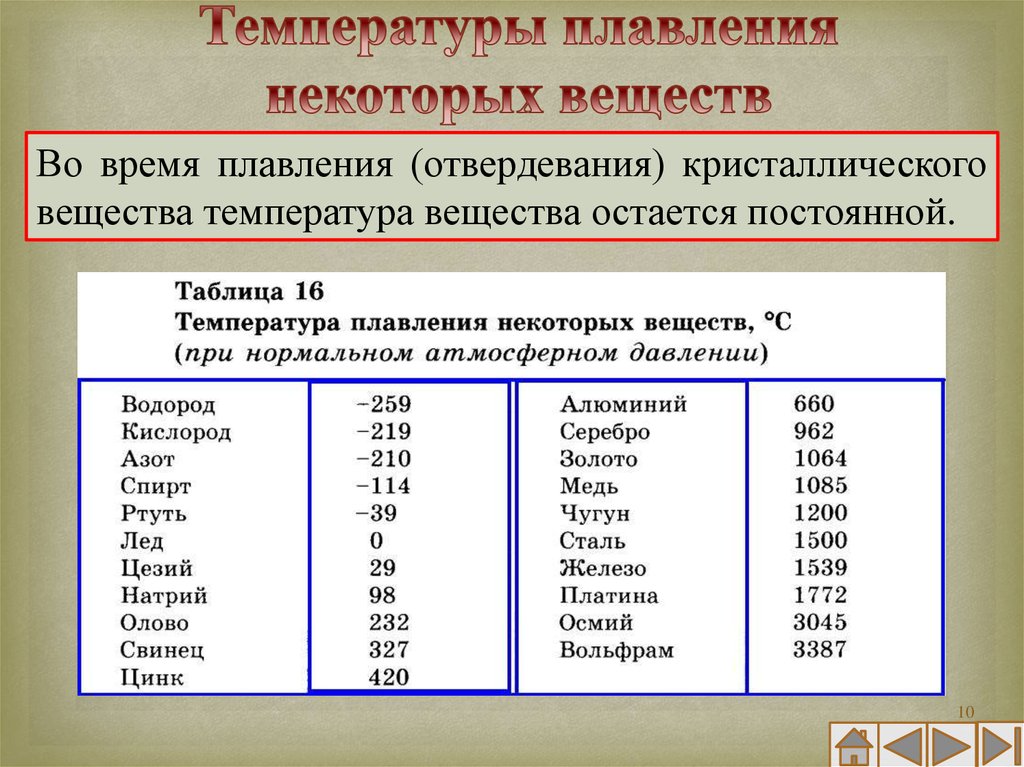
 com®
com®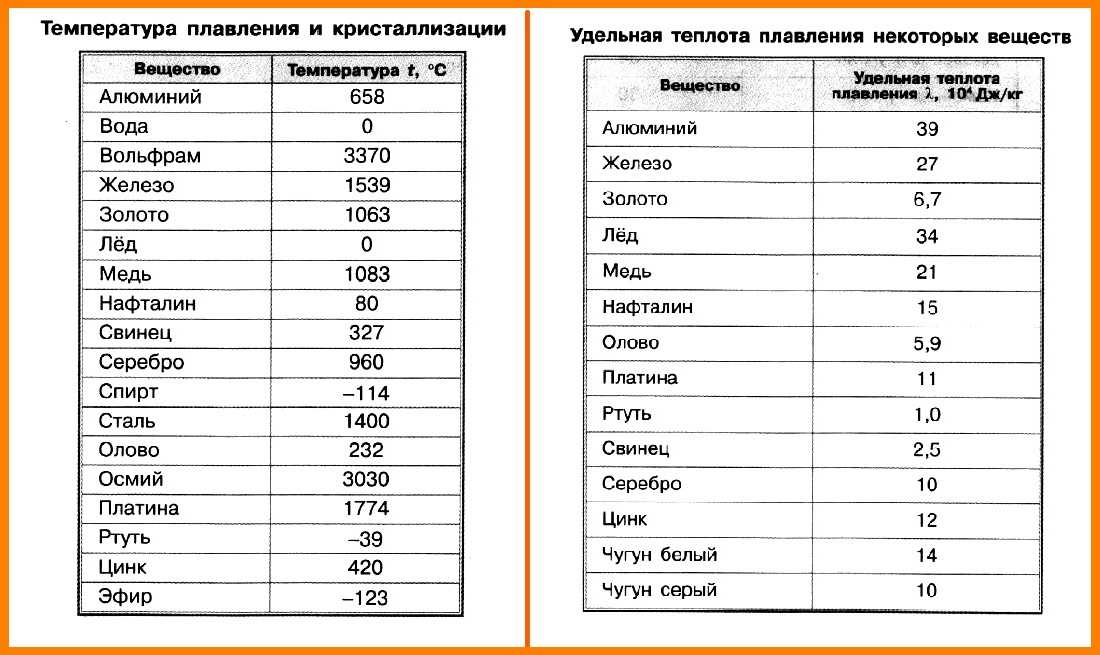 Металлы, легированные алюминием, и температура плавления алюминия имеют более низкий температурный диапазон, чем медные сплавы. Чистый алюминий плавится при температуре около 1218 ° F / 659 ° C, но сплавление с другими элементами может повысить ее. В приведенной ниже таблице указаны наиболее распространенные металлы, представленные в нашем каталоге, такие как температура плавления нержавеющей стали и точка плавления титана!
Металлы, легированные алюминием, и температура плавления алюминия имеют более низкий температурный диапазон, чем медные сплавы. Чистый алюминий плавится при температуре около 1218 ° F / 659 ° C, но сплавление с другими элементами может повысить ее. В приведенной ниже таблице указаны наиболее распространенные металлы, представленные в нашем каталоге, такие как температура плавления нержавеющей стали и точка плавления титана! Просканируйте ниже, чтобы узнать температуры плавления популярных металлов, которые вы можете приобрести в Online Metals сегодня.
Просканируйте ниже, чтобы узнать температуры плавления популярных металлов, которые вы можете приобрести в Online Metals сегодня.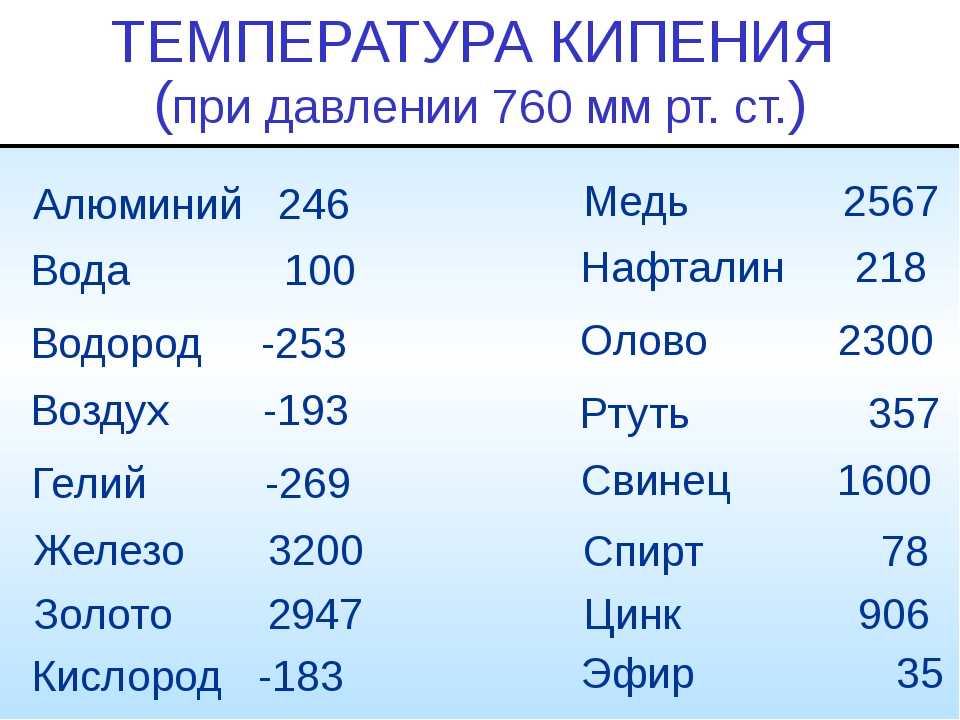
 Если его температура поднимается выше 1085 градусов по Цельсию, он готовит и становится жидкостью. Его температура плавления не меняется при нагревании в печи или на огне.
Если его температура поднимается выше 1085 градусов по Цельсию, он готовит и становится жидкостью. Его температура плавления не меняется при нагревании в печи или на огне. Наконец, вам нужно будет использовать соответствующее защитное снаряжение, такое как перчатки и маска для лица, чтобы защитить себя от жары и паров.
Наконец, вам нужно будет использовать соответствующее защитное снаряжение, такое как перчатки и маска для лица, чтобы защитить себя от жары и паров.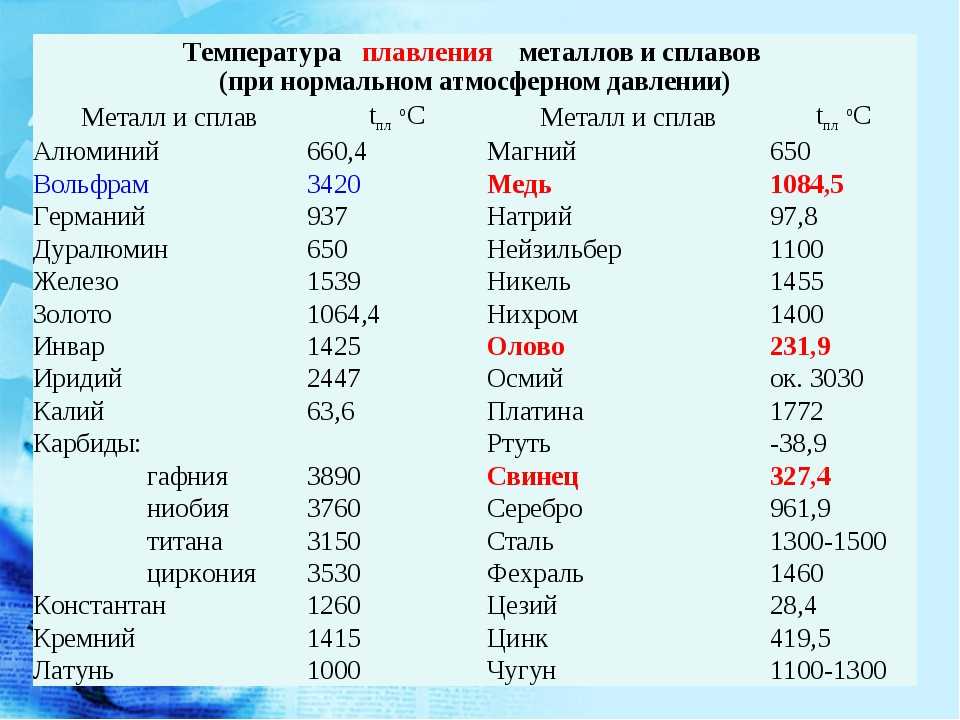
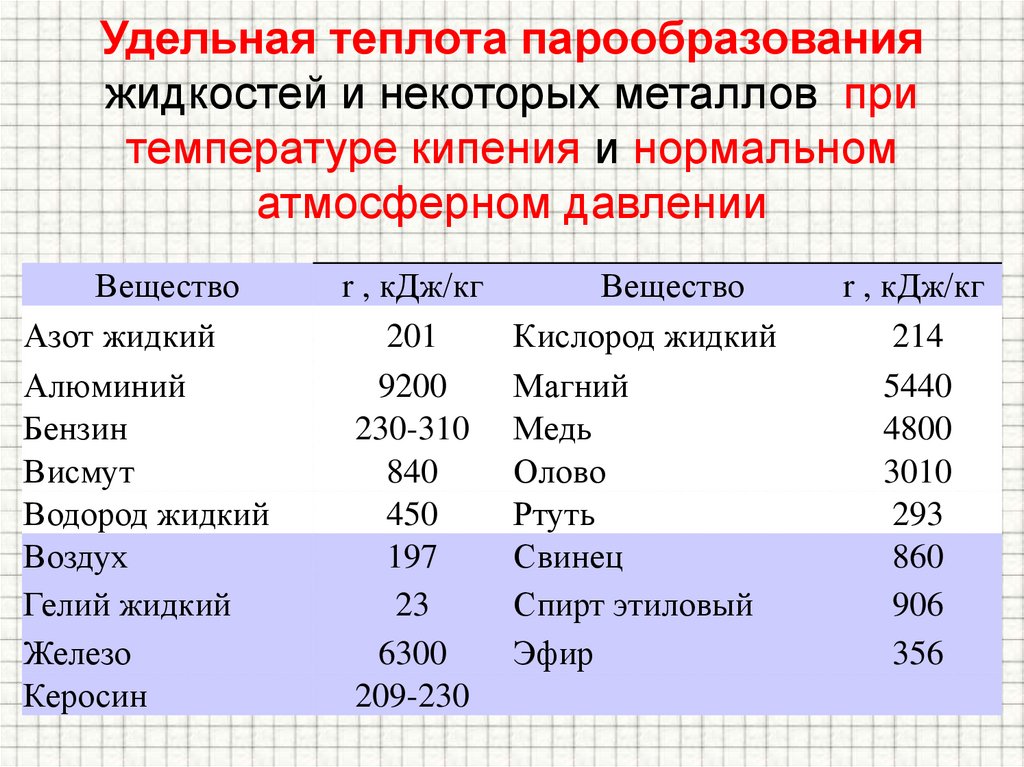 Если у вас возникло какое-либо раздражение или другая неблагоприятная реакция после ношения медного кольца, лучше снять его и обратиться к врачу.
Если у вас возникло какое-либо раздражение или другая неблагоприятная реакция после ношения медного кольца, лучше снять его и обратиться к врачу.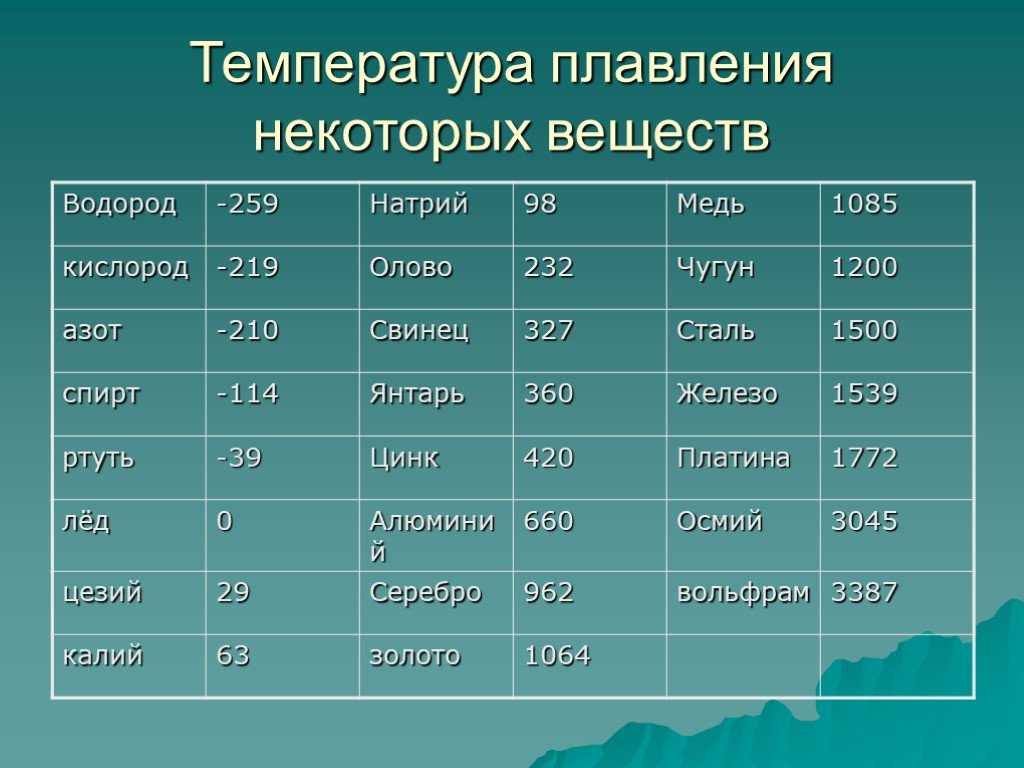 Тем не менее, это не рекомендуется, потому что во время соскабливания вы также будете подвергать кожу воздействию частиц меди.
Тем не менее, это не рекомендуется, потому что во время соскабливания вы также будете подвергать кожу воздействию частиц меди.

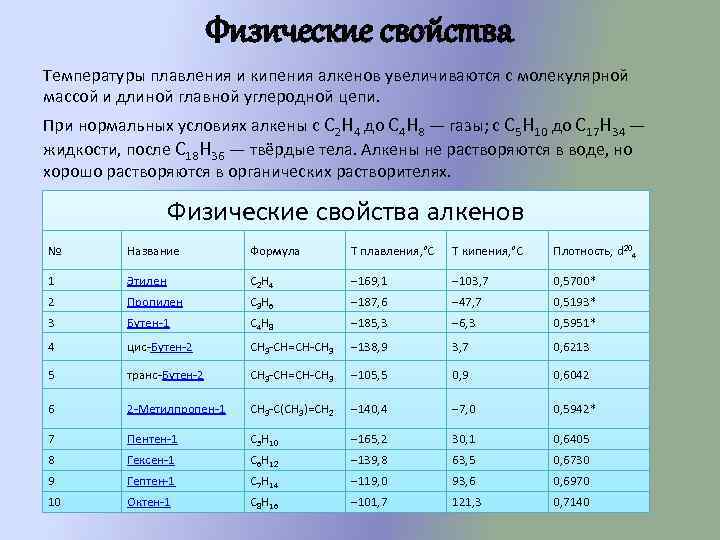 Этот слой мягкий и легко удаляется, но не влияет на твердость основного материала.
Этот слой мягкий и легко удаляется, но не влияет на твердость основного материала.