Катодная поляризация это: Катодная поляризация | это… Что такое Катодная поляризация?
Содержание
Катодная и анодная поляризация в химических процессах коррозии
12 декабря 2012
Катодная поляризация вызывается причинами, аналогичными анодной. Концентрационная катодная поляризация — это снижение потенциала катода чаще всего в связи с недостатком в приэлектродном пространстве того вещества, которое должно восстанавливаться. Если это катионы и если диффузия, за счет которой катионы попадают в приэлектродное пространство,— процесс менее эффективный, чем их разряд на электроде, то катионы просто не успевают в достаточных количествах подойти к катоду из глубины раствора, Тогда некоторые из уже разрядившихся катионов возвращаются обратно, туда, где их мало, унося с металла свой положительный заряд и тем уменьшая его положительный потенциал. Коррозия весьма опасное явление, так как ослабляет металлоконструкции из-за их ржавления, однако существуют марки стали, которые мало подверженны коррозии, так и обычные конструкционные стали, например сталь 45, сталь 20 и другие, которые необходимо защищать от коррозии покраской, электрохимическим покрытием и другими способами.
Катодное перенапряжение — это снижение потенциала катода за счет того, что энергетический барьер существует не только при «уходе из дома» (начале движения), но и при «возвращении домой».
Таким образом, благодаря процессам поляризации электрохимическая коррозия имеет некоторую склонность к самозатуханию.
Но существует ряд явлений, препятствующих поляризации. Прежде чем перейти к рассмотрению этих явлений, с точки зрения защиты от коррозии чрезвычайно вредных, кратко остановимся на понятии лимитирующей стадии процессов. С первого взгляда кажется очевидным, что лимитирующая стадия — это самая медленная стадия процесса. В буквальном переводе «лимитирующая» означает «ограничивающая» — процесс не может идти со скоростью большей, чем скорости этой стадии. Но вот пример. В ведре, наполненном водой, пробили две дырки — большую и маленькую. Ясно, что через маленькую дырку утечка будет меньше, а через большую — больше. Общая же скорость истечения воды будет равна сумме скоростей истечения через оба отверстия.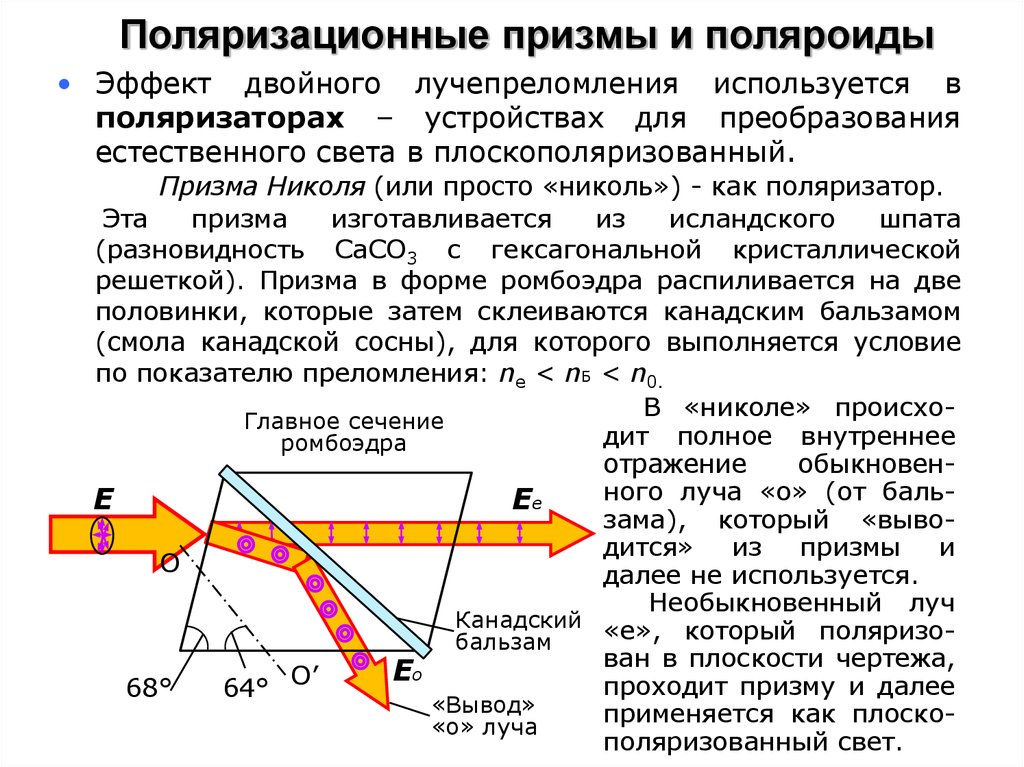 Медленная стадия есть, а общая скорость процесса превышает ее в несколько раз! Но парадокс этот в действительности кажущийся. Дело в том, Что понятие лимитирующей стадии применимо только к процессам, протекающим последовательно, а наше истечение воды из дырявого ведра — это пример параллельного процесса.
Медленная стадия есть, а общая скорость процесса превышает ее в несколько раз! Но парадокс этот в действительности кажущийся. Дело в том, Что понятие лимитирующей стадии применимо только к процессам, протекающим последовательно, а наше истечение воды из дырявого ведра — это пример параллельного процесса.
А вот пример последовательного процесса — перемещение пассажиров с московской станции метро «Павелецкая-радиальная» на станцию «Павелецкая-кольцевая» с помощью эскалатора. Если пропускная способность эскалатора, скажем, четыре человека в секунду, то как бы много ни приносил голубой экспресс пассажиров на станцию «Павелецкая-радиальная», на станции «Павелецкая-кольцевая» они будут появляться не чаще, чем четыре счастливчика в секунду. А если на радиальной станет совсем невмоготу, то наверх пустят еще одну лестницу, и число счастливчиков удвоится, а количество оторванных пуговиц несколько уменьшится. Этот пример показывает, что для увеличения скорости последовательных процессов нужно найти «узкое место», самую медленную стадию, и интенсифицировать ее.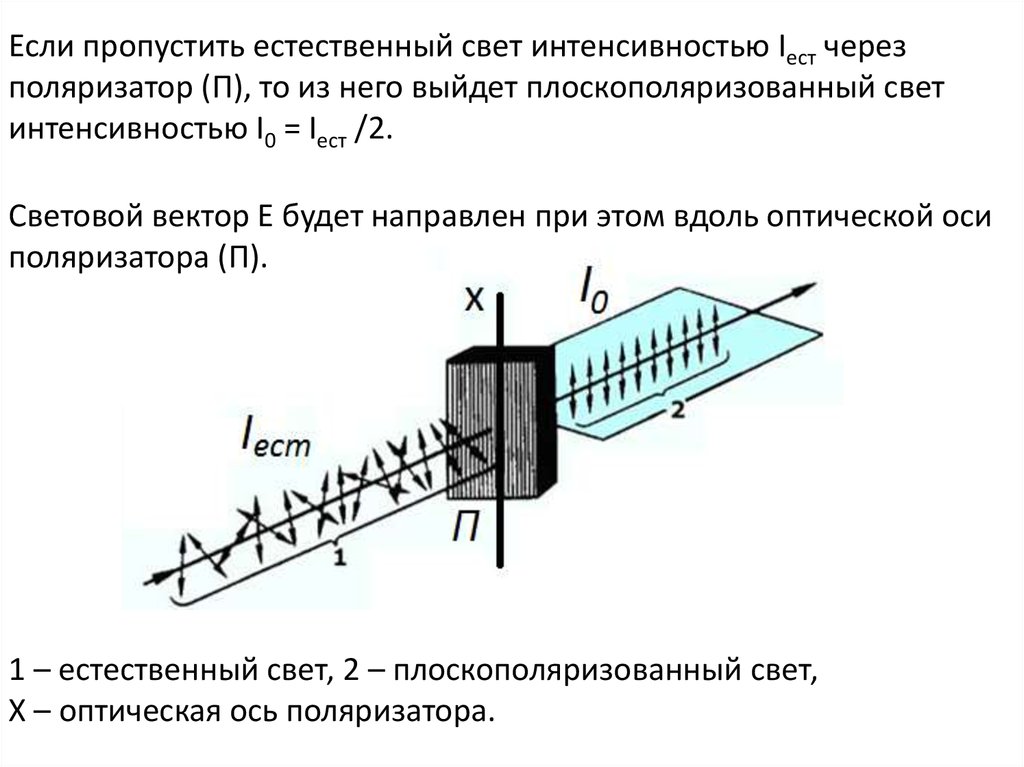
Теперь вернемся к электрохимической коррозии. Этот процесс протекает через ряд последовательных стадий: анодное растворение металла, приводящее к появлению избытка электронов на аноде, перемещение этих электронов к катоду, где они восстанавливают катионы, приходящие из раствора электролита, и пополнение убыли катионов за счет анодных процессов.
Все «узловые точки» — анод, катод и раствор электролита — связаны друг с другом не более чем одной стрелкой. Это означает, что в данном процессе нет параллельных путей, и он относится к последовательным. Каждая из стрелочек на этом рисунке показывает перемещение заряженных частиц и аналогична эскалатору, рассмотренному в примере с пересадкой пассажиров в Московском метрополитене.
Поляризация и деполяризация при коррозии
Поляризацией называется изменение потенциалов электродов при протекании электрического тока, а также процессы, приводящие к уменьшению скорости коррозии за счет изменения потенциалов, а, следовательно, и снижению коррозионного тока. Когда цепь между катодом и анодом разомкнута (до момента времени τ1, рисунок 1), катод и анод имеют значения потенциалов φк0 и φa0 соответственно — это равновесные или стационарные потенциалы. После замыкания цепи (после τ1) между анодом и катодом начинает протекать электрический ток и потенциалы катода и анода изменяются до значений φк итφa. Разность потенциалов при этом изменяется от Е0 до Е. Смещения потенциалов анода и катода составляют ΔЕa и ΔЕk — анодная и катодная поляризация. В результате поляризации скорость коррозии падает, потенциал анода становится менее отрицательным, а потенциал катода менее положительным, разность потенциалов падает и ток коррозии уменьшается.
Когда цепь между катодом и анодом разомкнута (до момента времени τ1, рисунок 1), катод и анод имеют значения потенциалов φк0 и φa0 соответственно — это равновесные или стационарные потенциалы. После замыкания цепи (после τ1) между анодом и катодом начинает протекать электрический ток и потенциалы катода и анода изменяются до значений φк итφa. Разность потенциалов при этом изменяется от Е0 до Е. Смещения потенциалов анода и катода составляют ΔЕa и ΔЕk — анодная и катодная поляризация. В результате поляризации скорость коррозии падает, потенциал анода становится менее отрицательным, а потенциал катода менее положительным, разность потенциалов падает и ток коррозии уменьшается.
Рисунок 1 — схема изменения потенциалов катода и анода после замыкания цепи
Причиной поляризации является торможение (маленькая скорость) одной или нескольких составляющих процесса электрохимической коррозии. В результате скорость накопления отрицательных зарядов на аноде или положительных на катоде становится меньше скорости перехода электронов от анода к катоду и потенциалы анода и катода изменяются. Поскольку скорость всего процесса определяется скоростью самой медленной (лимитирующей) стадией, то в результате поляризации скорость коррозии в целом замедляется. Анодная поляризации (торможение анодного процесса) может быть вызвана медленным выходом ионов металла в раствор (лимитирует химическая реакция), образованием на поверхности металла защитной оксидной пленки или медленным отводом ионов металла от поверхности, что затрудняет выход следующих (лимитирует диффузия). Катодная поляризации (торможение катодного процесса) может быть вызвана маленькой скоростью окисления катионов или молекул раствора на поверхности металла (лимитирует химическая реакция) или медленным подводом кат ионов или молекул раст вора к поверхности катода и отводом продукгов восстановления от катода в раствор (лимитирует диффузия).
В результате скорость накопления отрицательных зарядов на аноде или положительных на катоде становится меньше скорости перехода электронов от анода к катоду и потенциалы анода и катода изменяются. Поскольку скорость всего процесса определяется скоростью самой медленной (лимитирующей) стадией, то в результате поляризации скорость коррозии в целом замедляется. Анодная поляризации (торможение анодного процесса) может быть вызвана медленным выходом ионов металла в раствор (лимитирует химическая реакция), образованием на поверхности металла защитной оксидной пленки или медленным отводом ионов металла от поверхности, что затрудняет выход следующих (лимитирует диффузия). Катодная поляризации (торможение катодного процесса) может быть вызвана маленькой скоростью окисления катионов или молекул раствора на поверхности металла (лимитирует химическая реакция) или медленным подводом кат ионов или молекул раст вора к поверхности катода и отводом продукгов восстановления от катода в раствор (лимитирует диффузия).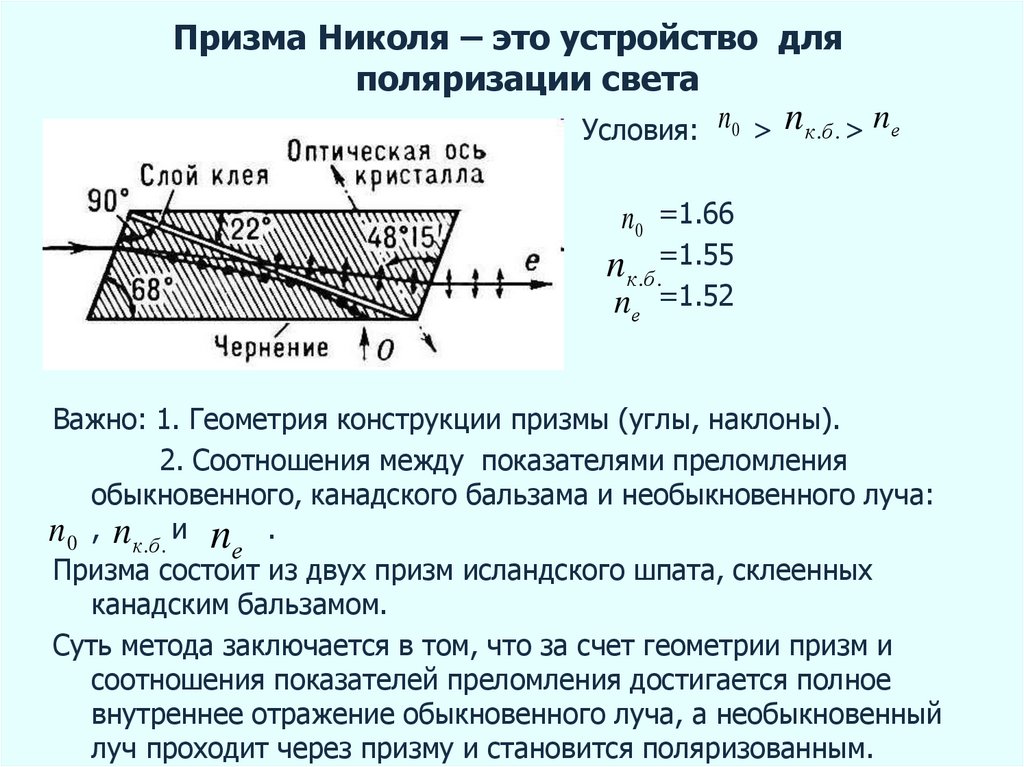
Деполяризацией называются явления, способствующие увеличению скорости коррозионных процессов и соответственно уменьшению поляризации электродов. Вещесгва, уменьшающие поляризацию называются деполяризаторами. Наиболее распространенными катодными деполяризаторами являются водород и кислород — основные окислители в растворах. Коррозия с участием ионов водорода возможна в случае, когда равновесный потенциал металла отрицательнее равновесного потенциала водородного электрода в данных условиях. Деполяризующее действие будет оказывать увеличение содержания в растворе водорода. Коррозия с участием молекул кислорода — наиболее распространенный случай. Деполяризующее действие будет оказывать увеличение содержания в растворе кислорода. Деполяризующее действие будут также оказывать растворение защитной оксидной пленки и все факторы, облегчающие доступ окислителей к поверхности металла, например, перемешивание.
На нашем сайте Вы можете заказать решениe заданий по всем разделам материаловедения. |
AMPP Store — 96314 ВЛИЯНИЕ КАТОДНОЙ ПОЛЯРИЗАЦИИ НА ПРОЧНОСТЬ СВЯЗИ ПРЕДВАРИТЕЛЬНО НАПРЯЖЕННЫХ НАТЯЖЕНИЙ В БЕТОНЕ
Дом
/
Материалы конференции
/
Материалы конференции NACE
/
- 96314 ВЛИЯНИЕ КАТОДНОЙ ПОЛЯРИЗАЦИИ НА ПРОЧНОСТЬ СВЯЗИ ПРЕДВАРИТЕЛЬНО НАПРЯЖЕННЫХ НАТЯЖЕНИЙ В БЕТОНЕ
Доступно для скачивания
Номер продукта:
51300-96314-СГ
ISBN:
96314 1996 КП
Автор:
Эммануэль Жубер, Уильям Х. Хартт
Хартт
Цена участника:
$0.00
Цена для нечленов:
20 долларов США
Цена:
20 долларов США
Возможность потери связи для предварительно натянутой арматуры в бетоне в
Реакция на катодную защиту может ограничить применимость этой методологии контроля коррозии к этому классу материалов. Чтобы исследовать возможное возникновение и значение такой потери сцепления, ряд предварительно напряженных бетонных балок был катодно поляризован с использованием плотности тока в диапазоне 50-5000…
Возможность потери связи для предварительно натянутой арматуры в бетоне в
Реакция на катодную защиту может ограничить применимость этой методологии контроля коррозии к этому классу материалов. Чтобы исследовать возможное возникновение и значение такой потери сцепления, ряд предварительно напряженных бетонных балок был катодно поляризован с использованием плотности тока в диапазоне 50-5000.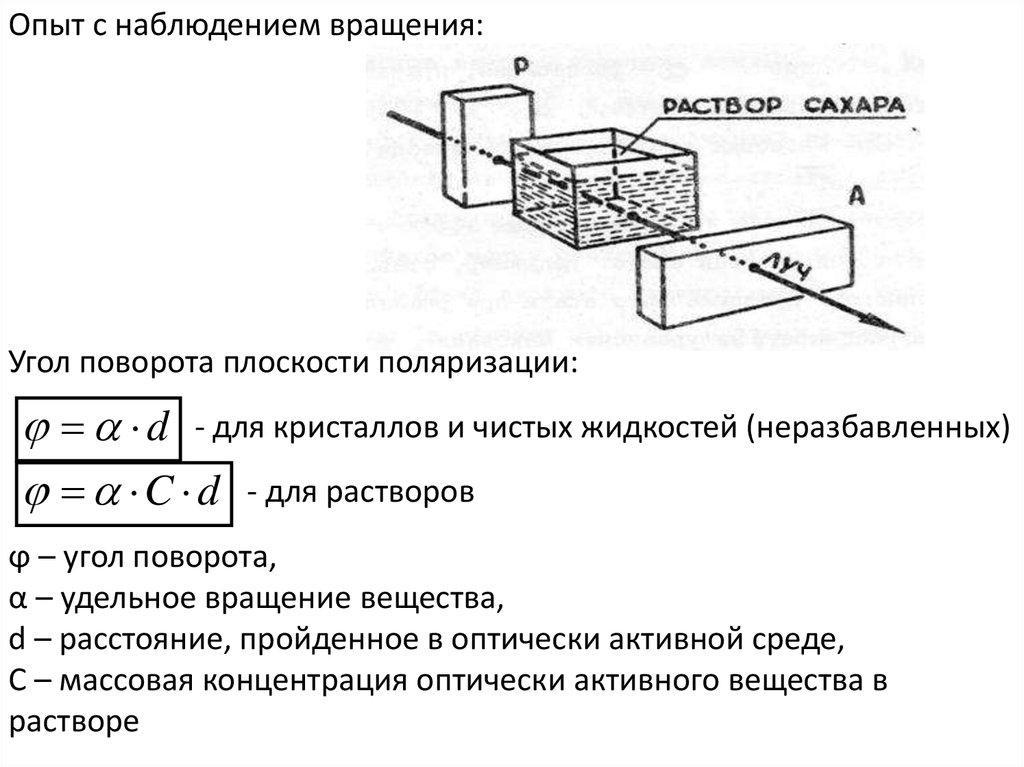 ..
..
СКИДКИ — Чем больше вы покупаете, тем больше экономите
20 долларов США
20 долларов США
Ярлыки товаров
Материалы конференции 1996 г. (446)
- ,
Материалы конференции (10919)
- ,
Загружаемый (7812)
Также приобретен
Доступно для скачивания
Номер продукта:
51300-96315-СГ
ISBN:
96315 1996 КП
Автор:
Станислас Кишовски, Уильям Х. Хартт
Хартт
20 долларов США
Доступно для скачивания
Номер продукта:
51300-96308-СГ
ISBN:
96308 1996 КП
Автор:
Бернард С. Ковино-младший, Софи Дж. Буллард, Гордон Р. Холкомб, Стивен Д. Крамер, Гален Э. Макгилл, Cu
20 долларов США
Доступно для скачивания
Номер продукта:
51300-96316-СГ
ISBN:
96316 1996 КП
Автор:
Джек Беннетт, Клем Фирлотт
20 долларов США
Характеристики катодной поляризации углеродистой стали в почвах Альберты | КОРРОЗИЯ NACE
Пропустить пункт назначения навигации
Цитировать
- Посмотреть эту цитату
- Добавить в менеджер цитирования
Делиться
- Твиттер
- MailTo
Поиск по сайту
Цитата
Делорм, Джеффри. «Катодные поляризационные характеристики углеродистой стали в почвах Альберты». Доклад, представленный на КОРРОЗИИ 2020, физическое мероприятие отменено, июнь 2020 г.
«Катодные поляризационные характеристики углеродистой стали в почвах Альберты». Доклад, представленный на КОРРОЗИИ 2020, физическое мероприятие отменено, июнь 2020 г.
Скачать файл цитирования:
- Рис (Зотеро)
- Менеджер ссылок
- EasyBib
- Подставки для книг
- Менделей
- Бумаги
- КонецПримечание
- РефВоркс
- Бибтекс
Расширенный поиск
Поведение катодной поляризации было исследовано для образцов из углеродистой стали UNS K02600 в тридцати (30) образцах почвы, отобранных в центральной и южной части провинции Альберта, Канада. Исследовалась поляризация купонов в зависимости от плотности тока и свойств грунта. Поляризационные данные были собраны для пассивно аэрируемых образцов при плотностях приложенного катодного тока до 20 мА/м 9 .0157 2 . Были собраны дополнительные данные о типе почвы, электропроводности, склонности к удержанию влаги, окислительно-восстановительном потенциале и рН. Приложения включают проектирование CP и численное моделирование, а также разработку планов мониторинга конструкций из углеродистой стали в почве.
Приложения включают проектирование CP и численное моделирование, а также разработку планов мониторинга конструкций из углеродистой стали в почве.
ВВЕДЕНИЕ
Расчет требуемой пропускной способности системы или характеристик поляризации требует знания поведения поляризации. В этой работе исследуется поляризационное поведение образцов UNS K02600 (мягкая углеродистая сталь) с изменением засыпки для определения ожидаемой поляризации в зависимости от плотности тока. Результаты этого исследования применяются для оценки расчетных токов для оголенных конструкций, численного моделирования поляризации трубопровода и интерпретации купонов для мониторинга эффективности систем катодной защиты трубопроводов при наличии изменений в составе грунта. Образцы почвы были взяты на участках в центральной и южной части Альберты, Канада, и обычно брались с глубины примерно 2 м (6 футов). Общий тип встречаемой почвы был суглинистый с неоднородным размером частиц.
ЭКСПЕРИМЕНТАЛЬНАЯ МЕТОДИКА
Общая процедура оценки поляризационных характеристик заключалась в упаковке образцов грунта в пористые керамические чашки с купонами и продавливании различных уровней тока катодной защиты через общий электролит.
