Коррозия электрохимическая и химическая: Химическая коррозия
Содержание
Общие представления о коррозии металлов
Общие представления о коррозии металлов.
Под коррозией понимают разрушение металла вследствие его химического и электрохимического взаимодействия с окружающей средой.
В терминах окислительно-восстановительных реакций сущность этого взаимодействия сводится к окислению металла и восстановлению окислителя среды.
Me — ne = Men+ окисление (ионизация) металла
Ox + ne = Red восстановление окислителя среды
Коротко можем записать:
коррозия = окисление металла + восстановление окислителя.
Окислитель- “Ox” всегда принимает электроны. Поэтому в качестве окислителя среды может выступать любое вещество, способное принимать на себя электроны от атомов металла.
Ox- окислитель среды= захватчик электронов
Red-восстановитель среды= поставщик электронов
Примеры коррозии металлов в различных средах:
Атмосферная коррозия- окисление железа кислородом воздуха
4Fe + 3O2 = 2Fe2O3 окислитель-кислород
В этой реакции железо поставляет электроны, а кислород их захватывает
4Fe — 12e = 4Fe3+ окисление железа
3O2 + 12e = 6O2- восстановление кислорода
Коррозия железа в водных средах, содержащих ионы водорода
2Fe + 6H+ = 2Fe3+ + 3H2 окислитель-ионы водорода
В этой реакции железо также отдает электроны, а принимают их ионы водорода
2Fe — 6e = 2Fe3+ окисление железа
6H+ + 6e = 3H2 восстановление ионов водорода
Коррозия наносит огромный ущерб почти всем отраслям народного хозяйства, при этом основные убытки определяются даже не потерей металла, а порчей дорогостоящих металлических изделий, конструкций, машин и аппаратов, что в первую очередь связано с утратой функциональных возможностей их отдельных узлов. Достаточно упомянуть разрывы нефте- и газопроводов, а также разрывы труб городского водоснабжения. Коррозия металлической арматуры железобетонных конструкций приводит к потере их прочности и разрушению промышленных и жилых зданий.
Достаточно упомянуть разрывы нефте- и газопроводов, а также разрывы труб городского водоснабжения. Коррозия металлической арматуры железобетонных конструкций приводит к потере их прочности и разрушению промышленных и жилых зданий.
О масштабах коррозии черных металлов можно судить хотя бы по тому, что примерно каждая шестая домна в мире работает на восполнение коррозионных потерь.
Классификация различных видов коррозии.
По механизму действия коррозия делится на химическую и электрохимическую
Химическая коррозия — взаимодействие металла с окружающей средой, при котором окисление металла и восстановление окислителя коррозионной среды происходит в одном акте без перехода заряженных частиц через границу металл-окислительная среда.
Химическая коррозия = окисление металла + восстановление окислителя без перехода заряженных частиц через границу металл-коррозионная среда.
Скорость химической коррозии не зависит от потенциала металла.
Примером химической коррозии может служить окисление железа кислородом воздуха
4Fe + 3O2 = 2Fe2O3
Образующаяся при этом оксидная пленка на металле может предохранять его от дальнейшего окисления, если температура окисления невысока. При высоких температурах химического окисления любое железное изделие превращается в окалину. Химический вид коррозии может также иметь место и в растворах неэлектролитов.
Электрохимическая коррозия — взаимодействие металла с окружающей средой, при котором окисление металла и восстановление окислителя коррозионной среды происходит в результате протекания нескольких элементарных актов, сопровождающихся переходом заряженных частиц через границу металл-окислительная среда.
Электрохимическая коррозия = окисление металла + восстановление окислителя с переходом заряженных частиц через границу металл-коррозионная среда.
Скорость электрохимической коррозии зависит от потенциала металла.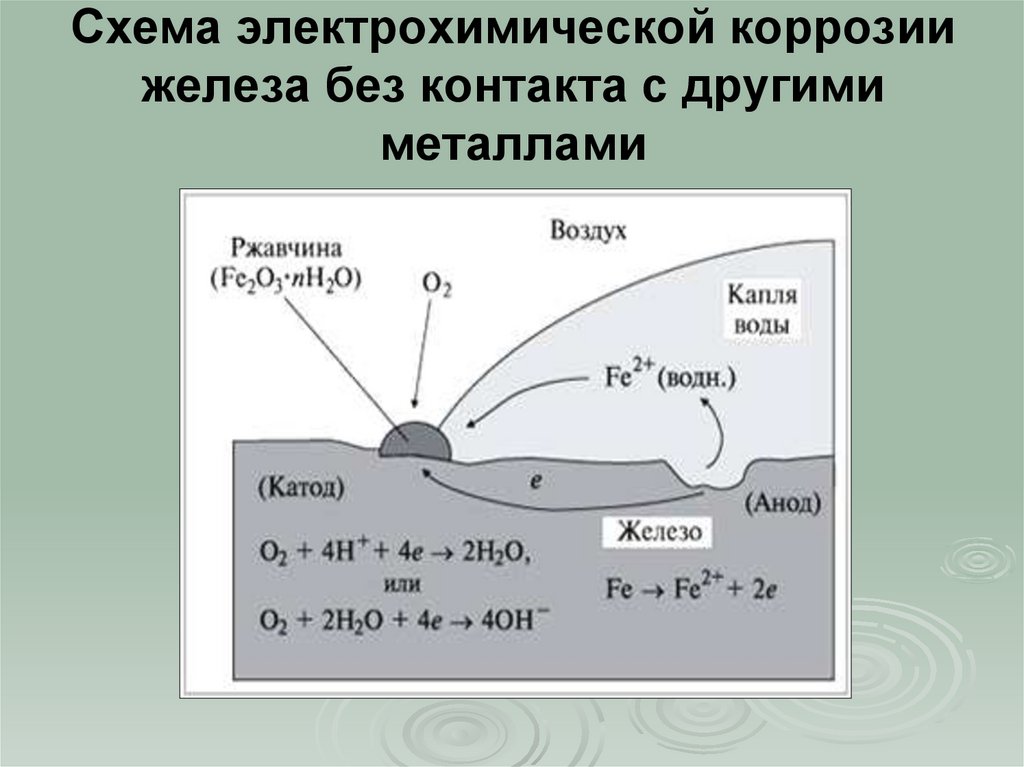
Примером может служить растворение цинка в кислоте
Zn + 2H+ = Zn2++ Н2
Еще со школы мы привыкли рассматривать эту реакцию, как химическую. На самом деле эта реакция протекает через две сопряженные электрохимические реакции:
реакцию окисления атома цинка
Zn = Zn2+ + 2e
и реакцию восстановления ионов водорода
2H+ + 2е= Zn2++ Н2
Если сложить эти две реакции, то получим суммарную реакцию
Zn + 2H+ = Zn2+ + Н2
При этом заряженная частица- ион цинка переходит через границу металл-раствор в объем раствора, а пара электронов остается в металле, заряжая его отрицательно по схеме
Ионы водорода подходят к отрицательно заряженной поверхности металла, а электроны из металла переходит через границу раздела металл-раствор на ионы водорода, в результате образуется молекула водорода
По характеру коррозионной среды различают следующие типы коррозии
Другими словами — коррозия в небе, на суше и на море.
Газовая коррозия — химическая коррозия металлов в газах при высоких температурах (например, в камере сгорания реактивных двигателей).
Атмосферная коррозия— коррозия в атмосфере воздуха (при наличии конденсированной пленки влаги и атмосферных осадков).
Электролитная коррозия— коррозия в речной и морской воде, а также в растворах солей, кислот, щелочей.
Грунтовая коррозия-коррозия металлических изделий при контакте с грунтом-почвенным электролитом.
По условиям эксплуатации различают следующие типы электрохимической коррозии
Щелевая коррозия-электрохимическая коррозия в щелях и зазорах
между двумя металлами, куда попадает электролит.
Контактная коррозия-электрохимическая коррозия любых двух контак-
тирующих металлов, погруженных в электролит. Она проявляется в усиле-
нии коррозии одних металлов при их контакте с другими металлами.
Коррозионное растрескивание-коррозия металла при одновременном
воздействии коррозионной среды и внешних или внутренних механических
напряжений растяжения с образованием транскристаллитных или межкрис-
таллитных трещин.
Коррозионная усталость— понижение предела усталости металла при
одновременном воздействии циклических растягивающих напряжений и кор-
розионной среды.
Коррозия при трении — разрушение металла, вызываемое одновременным
воздействием коррозионной среды и трения.
Формы коррозионных разрушений.
По форме коррозионных разрушений коррозия делится на виды
Для всех металлических изделий, испытывающих механическую нагрузку,наиболее опасными являются локальные виды коррозии. Это демонстрирует график зависимости потерь прочности детали из дуралимина от коррозионных потерь веса при различных видах коррозионного разрушения.
При коррозии металла на его поверхности одновременно протекают две независимые электрохимические реакции
Me — ne = Men+ окисление (ионизация) металла
Ox + ne = Red восстановление окислителя среды
В стационарном состоянии все электроны, которые выделяются в результа-
те ионизации металла должны потребляться в сопряженном процессе восс-
тановления окислителя.
Если в качестве окислителя при коррозии металла выступают ионы
водорода, то такая коррозия называется коррозией с водородной деполя-
ризацией.
В этом случае при одном и том же стационарном потенциале одновременно протекают процессы растворения металла и восстановления ионов водорода
Me = Men+ + ne
2H+ + 2e = H2
Если в качестве окислителя при коррозии металла выступают молекулы растворенного кислорода, то такая коррозия называется коррозией с кислородной деполяризацией. В этом случае при одном и том же стационарном потенциале одновременно протекают процессы растворения металла
и восстановления молекул кислорода. Эти процессы для щелочных растворов имеют вид
Me = Men+ + ne
16 Тематика семинарских занятий — лекция, которая пользуется популярностью у тех, кто читал эту лекцию.
O2 + 2H2O + 4e = 4OH—
В кислых растворах восстановление кислорода протекает по схеме
О2 + 4H+ + 4e = 2H2O восстановление кислорода
В нейтральных средах для активных металлов, вытесняющих водород
из воды, в качестве восстановителя могут выступать сами молекулы воды
2H2O + 2e =H2 + 2OH—
Химическая и электрохимическая коррозия металлов.
 Условия, при которых происходит коррозия, меры защиты металлов и сплавов от коррозии. / Ответы на экзамен по химии / Готовые сочинения на экзамен
Условия, при которых происходит коррозия, меры защиты металлов и сплавов от коррозии. / Ответы на экзамен по химии / Готовые сочинения на экзамен
Химическая и электрохимическая коррозия металлов. Условия, при которых происходит коррозия, меры защиты металлов и сплавов от коррозии.
/ Ответы на экзамен по химии / Готовые сочинения на экзаменПоступим.ру — сообщество школьников, выпускников и абитуриентов, егэ 2021, ответы на экзамены, мобильные шпаргалки, готовые сочинения, егэ, экзаменационные сочинения, темы сочинений, форум, коллективный блог
|
Последние публикации в коллективном блоге:
Посещаемые разделы форума: Последние обсуждаемые темы на форуме:
|
|
|
Химическая коррозия — Концепция — Химическое видео от Brightstorm
Химическая коррозия возникает в результате окисления металла. Это процесс возвращения металлов в их естественное состояние, которое является рудой. Большинство металлов образуют тонкое оксидное покрытие, которое защищает внутренние атомы. Защитное покрытие часто наносится для защиты металла от кислорода и влаги.
Это процесс возвращения металлов в их естественное состояние, которое является рудой. Большинство металлов образуют тонкое оксидное покрытие, которое защищает внутренние атомы. Защитное покрытие часто наносится для защиты металла от кислорода и влаги.
коррозия
В этом разделе давайте продолжим и обсудим коррозию, которая относится к более широкому разделу электрохимии. Поэтому всякий раз, когда вы слышите слова «электрохимия», вы должны немедленно задуматься об окислительно-восстановительных реакциях и вспомнить, откуда исходит поток электронов. поэтому помните, что окисление — это потеря электронов, а восстановление — это приобретение электронов, и что они происходят вместе в паре, и поэтому у вас будет один вид, который окисляет, и один вид, который восстанавливается.
Итак, коррозия, в основном, связана с окислением металла, что опять-таки знакомо нам, и поэтому мы знаем, что это обмен электронами. Таким образом, металл окисляется восстановителем. Итак, процесс возвращения металлов в их естественное состояние, то есть в руду, происходит при коррозии. Таким образом, он превращается из красивого, блестящего и красивого в довольно ржавый и отвратительный. Так что очевидно, что в естественном рудном состоянии он не так привлекателен, как в блестящем металлическом состоянии.
Таким образом, он превращается из красивого, блестящего и красивого в довольно ржавый и отвратительный. Так что очевидно, что в естественном рудном состоянии он не так привлекателен, как в блестящем металлическом состоянии.
Итак, поскольку мы знаем, что большинство металлов реагируют в окружающей среде с кислородом, как нам избежать коррозии или замедлить ее? Таким образом, большинство металлов образуют тонкое оксидное покрытие, которое защищает внутренние атомы от коррозии. Таким образом, вы можете получить некоторую начальную коррозию снаружи, а затем в какой-то момент они образуют эту оксидную пленку, которая замедляет процесс коррозии. Например, алюминий является популярным. Алюминий в изобилии присутствует в окружающей среде, поэтому он легко теряет электроны и должен легко окисляться кислородом. И все же алюминий используется для создания множества крупных конструкций, таких как самолеты и тому подобное. Таким образом, он образует слой оксида алюминия Al2O3, который предотвращает его дальнейшую коррозию. И другие подобные металлы делают то же самое. Никель и хром и на самом деле немало других.
И другие подобные металлы делают то же самое. Никель и хром и на самом деле немало других.
Итак, как я уже сказал, защитное покрытие часто образуется металлами само по себе, или его можно наносить для защиты металла от кислорода и влаги. Вы также можете использовать процесс, называемый легированием металлов. И один из наиболее распространенных процессов, который используется в нашей среде для защиты некоторых металлов, называется катодной защитой, и он работает для стальных резервуаров и труб, которые закопаны под землю, и поэтому вы в основном используете другой металл, который обеспечивает электроны легче, чем сталь или железо. В этом случае мы могли бы сказать, магний, и он связан с проводом и с трубопроводом, который нужно защитить. Таким образом, в основном, поскольку магний будет давать электроны легче, чем железо, он будет окисляться первым и, следовательно, защищать железо. Таким образом, в основном, он предотвращает окисление до определенного времени. Очевидно, что в какой-то момент магний закончится, и провода придется заменить.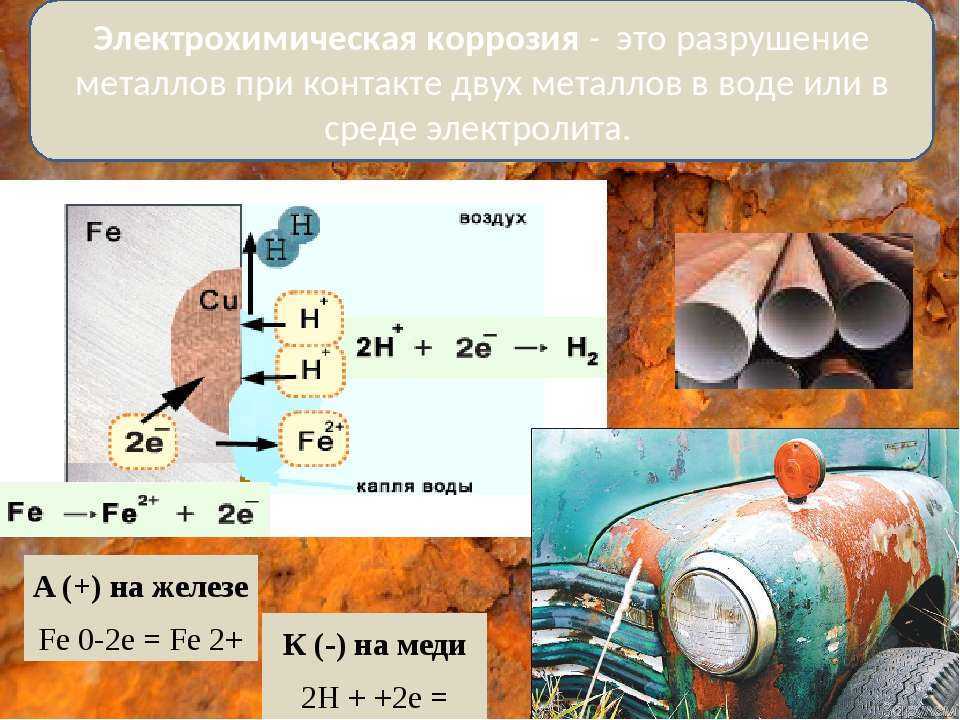
Это коррозия.
Типы коррозии — ZfP — TUM Wiki
Анжелика Ретт, зимний семестр 2018/19
Введение
«Коррозия – это необратимая межфазная реакция материала (металла, керамики, полимера) с окружающей средой, которая приводит к износу материала или при растворении в материале компонента окружающей среды. Часто, но не обязательно, коррозия приводит к последствиям, наносящим ущерб использованию рассматриваемого материала». [1]
Коррозия возникает на границе между материалом и окружающей средой. Материал необратимо растворяется. Часто этот процесс приводит к потере стабильности и других важных свойств, и материал становится непригодным для дальнейшего использования. В гражданском строительстве очень опасна коррозия железобетонных элементов. Для обнаружения коррозии в этих компонентах можно использовать различные методы неразрушающего контроля.
Физические принципы
Электрохимическая коррозия
Электрохимическая коррозия представляет собой сумму нескольких химических реакций, называемых окислением и восстановлением. Сочетание этих двух процессов называется окислительно-восстановительной реакцией. Это происходит там, где металлические материалы встречаются с электролитами. Электролиты могут проводить заряды, примерами являются вода, кислоты, основания и атмосфера. [2] Место, где происходит окисление, называется анодом. Металл окисляется и становится положительно заряженным ионом. Максимальное количество электронов, которое может высвободить атом, равно количеству его валентных электронов. Многие ионы металлов могут находиться в различных заряженных состояниях, поэтому для одного атома металла возможны разные реакции. В примере железа два возможных окисления 9-
Сочетание этих двух процессов называется окислительно-восстановительной реакцией. Это происходит там, где металлические материалы встречаются с электролитами. Электролиты могут проводить заряды, примерами являются вода, кислоты, основания и атмосфера. [2] Место, где происходит окисление, называется анодом. Металл окисляется и становится положительно заряженным ионом. Максимальное количество электронов, которое может высвободить атом, равно количеству его валентных электронов. Многие ионы металлов могут находиться в различных заряженных состояниях, поэтому для одного атома металла возможны разные реакции. В примере железа два возможных окисления 9-
Окислительно-восстановительная реакция не может привести к накоплению заряда, все освободившиеся электроны должны быть поглощены реакциями восстановления. [2]
Стандартная серия ЭДС
Различные возможные реакции для одного атома не равновероятны, что изображается стандартным рядом электродвижущей силы (рядом ЭДС). Различные реакции восстановления перечислены для разных материалов в зависимости от вероятности их протекания. Благородные материалы становятся все более инертными, тогда как менее благородные материалы становятся все более активными и, следовательно, находятся дальше в конце списка. 9- \rightleftharpoons Li
Различные реакции восстановления перечислены для разных материалов в зависимости от вероятности их протекания. Благородные материалы становятся все более инертными, тогда как менее благородные материалы становятся все более активными и, следовательно, находятся дальше в конце списка. 9- \rightleftharpoons Li
Химическая коррозия
Химическая коррозия происходит без электролитов, часто при высоких температурах. Должен иметь место прямой перенос электрона между партнерами по реакции. Следовательно, окисление и восстановление происходят в одном и том же месте. Свойства продуктов реакции могут влиять на скорость протекания коррозионных процессов. Например, гидрофильные продукты вызывают электрохимическую коррозию. [3] Химическая коррозия во многих случаях представляет собой реакцию между металлом и кислородом, в результате которой образуется оксид металла, например [5]
2Mg + O_2 \rightarrow 2MgO
Типы коррозии
Коррозия может происходить как равномерно распределенной по открытой поверхности, так и локально. Если разрушение материала происходит равномерно, то процесс называется равномерной коррозией. Если затронуты только определенные области, это называется локализованной коррозией. Наиболее известным случаем равномерной коррозии является ржавление стали, подвергающейся воздействию атмосферы. Эффект можно уменьшить, покрыв открытые участки менее реактивными материалами. [6] Разрывы таких покрытий приводят к локальной коррозии на открытых участках. [7]
Если разрушение материала происходит равномерно, то процесс называется равномерной коррозией. Если затронуты только определенные области, это называется локализованной коррозией. Наиболее известным случаем равномерной коррозии является ржавление стали, подвергающейся воздействию атмосферы. Эффект можно уменьшить, покрыв открытые участки менее реактивными материалами. [6] Разрывы таких покрытий приводят к локальной коррозии на открытых участках. [7]
Далее будут описаны формы локальной коррозии.
Гальваническая коррозия
Если два различных металлических материала соединяются вместе в присутствии электролита и соединяются электрически, образуется элемент коррозии. Более благородный металл действует как катод, а менее благородный — как анод и, следовательно, подвергается коррозии. Освобожденные от окисления электроны распространяются к катоду, где реагируют с ионами, циркулирующими в электролите. Создается замкнутая цепь, которая используется для измерения потенциального поля. Этот процесс изображен на рис. 1. [2] [5]
Этот процесс изображен на рис. 1. [2] [5]
Гальваническая коррозия также может использоваться для предотвращения коррозии. Компонент, который нуждается в защите, электрически соединен с менее благородным металлом, который будет действовать как анод в этом созданном таким образом коррозионном элементе и предотвратит коррозию компонента. Менее благородный металл называется жертвенным анодом. [2]
| Рисунок 1: Гальваническая коррозия. Только менее благородный материал подвергается коррозии, благородная часть защищена. Штриховая линия указывает исходный объем анода |
Селективное выщелачивание
Также известно как: Селективная коррозия, Селективное травление
Селективное выщелачивание возникает в сплавах, когда корродирует только один компонент сплава (изображено на рис. 2). Согласно ряду ЭДС, корродирует менее благородный компонент. Иногда поражается только поверхностный слой, а структурных повреждений не происходит. Но есть известные случаи, такие как графитизация чугуна или децинкификация латуни, когда затрагивается весь компонент и остается только пористая основа, что делает компонент менее стабильным. [2] [6]
Иногда поражается только поверхностный слой, а структурных повреждений не происходит. Но есть известные случаи, такие как графитизация чугуна или децинкификация латуни, когда затрагивается весь компонент и остается только пористая основа, что делает компонент менее стабильным. [2] [6]
| Рисунок 2: Селективная коррозия в Alloy, где только компонент A затронут коррозион и растворяется (указывается на селективный в серых) 9009. 9009. |
Точечная коррозия
Точечная коррозия — это форма локальной коррозии, которая часто вызывается трещинами или отверстиями в защитном покрытии. Питтинговая коррозия распространяется под поверхностью, что очень затрудняет ее обнаружение, поэтому эффект дефекта очень опасен, поскольку небольшой дефект приводит к значительной потере стабильности. Пример точечной коррозии показан на рис. 3. [7]
Рисунок 3: Коррозия ямки.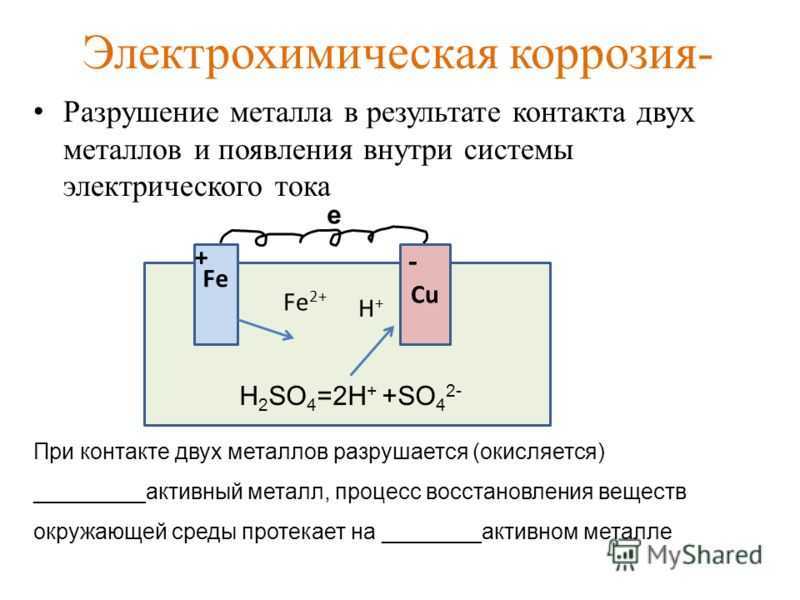 щели из-за разницы в концентрации кислорода. Концентрация внутри щели меньше, чем снаружи, что делает щель анодной частью реакции. Это называется концентрационной ячейкой. Электроны, освобожденные в результате окисления, распространяются по материалу в соседние области, где происходит восстановление, и эти электроны связываются. Положительно заряженные ионы металлов реагируют с другими ионами, содержащимися в воздухе. Щели могут быть небольшими дефектами на поверхности, но часто они возникают из-за особенностей конструкции, например, в болтовых или заклепочных соединениях (как показано на рис. 4). [2] [5] . Также известен как: коррозия под напряжением щели из-за разницы в концентрации кислорода. Концентрация внутри щели меньше, чем снаружи, что делает щель анодной частью реакции. Это называется концентрационной ячейкой. Электроны, освобожденные в результате окисления, распространяются по материалу в соседние области, где происходит восстановление, и эти электроны связываются. Положительно заряженные ионы металлов реагируют с другими ионами, содержащимися в воздухе. Щели могут быть небольшими дефектами на поверхности, но часто они возникают из-за особенностей конструкции, например, в болтовых или заклепочных соединениях (как показано на рис. 4). [2] [5] . Также известен как: коррозия под напряжением Коррозионное растрескивание под напряжением (SCC) происходит только для некоторых металлов или сплавов в коррозионной среде, если присутствуют статические растягивающие напряжения. Напряжения могут быть вызваны внешними нагрузками или внутренними напряженными состояниями. После образования на поверхности первых микротрещин, часто из-за механических нагрузок или питтинга, начинается распространение трещин перпендикулярно напряжениям. Коррозия Усталость Как показано на диаграммах Вёлера, если нагрузки применяются периодически, материалы будут страдать от усталостного повреждения после определенного количества циклов нагрузки. Межкристаллитная коррозия Межкристаллитная коррозия возникает у некоторых сплавов с элементами хрома после термической обработки и сварки. Высокие температуры способствуют образованию карбида хрома. Водородное охрупчиваниеТакже известно как: водородное растрескивание, водородное растрескивание под напряжением Водородное охрупчивание описывает явление, при котором пластичные металлы могут подвергаться хрупкому разрушению при диффузии атомарного водорода через кристаллическую решетку. Это может произойти только в том случае, если применяется растяжение ((Механические напряжения|напряжения]] и материал находится в коррозионной среде, что делает явление очень похожим на коррозионное растрескивание под напряжением. Разница в том, что водородное охрупчивание может иметь место даже при наличии отсутствие существующих трещин. Атомарный водород, образующийся в результате восстановительных процессов, диффундирует через поверхность к участкам с дефектами и затем будет реагировать различными способами. Если два атома водорода соединятся вместе, они могут образовать молекулу водорода. Эта молекула будет примерно в 600 раз больше, чем два отдельных атома и, следовательно, давление внутри металла резко увеличится. Эрозия Коррозия и кавитация КоррозияКоррозия может возникнуть в результате эрозии или кавитации, которые разрушают защитные слои. Поэтому ее называют соответственно эрозионной или кавитационной коррозией. Эрозия – это механическое истирание поверхностных слоев из-за движения жидкости, которое показано на рис. 6. Это обычно можно обнаружить в трубах на изгибах, где жидкость резко меняет свое направление или поток становится турбулентным. В зависимости от материала покрытия вихретоковый контроль может использоваться для определения остаточной толщины покрытия. Кавитация — это лопание пузырьков газа, которые образуются в быстро движущихся жидкостях из-за разницы давлений.
|

 1 / Автор: Miriada
1 / Автор: Miriada Условия, при которых происходит коррозия, меры защиты металлов и сплавов от коррозии.
Условия, при которых происходит коррозия, меры защиты металлов и сплавов от коррозии.
 В зависимости от металла трещины растут либо внутрикристаллитно (по границам зерен), либо транскристаллитно (поперек зерен). Это показано на рис. 5. Распространение трещин представляет собой комбинацию процессов коррозии и растрескивания из-за приложенных напряжений. Как только размер трещины достигает критического предела, приложенные напряжения приводят к разрушению компонента. Опасность SCC заключается в величине напряжений, необходимых для возникновения и распространения. Они намного ниже критических напряжений самого компонента. Эта форма коррозии не дает никаких видимых продуктов коррозии и поэтому часто ошибочно принимается за хрупкое разрушение, но материалы, подверженные SCC, в основном пластичны. [2] [5] [6]
В зависимости от металла трещины растут либо внутрикристаллитно (по границам зерен), либо транскристаллитно (поперек зерен). Это показано на рис. 5. Распространение трещин представляет собой комбинацию процессов коррозии и растрескивания из-за приложенных напряжений. Как только размер трещины достигает критического предела, приложенные напряжения приводят к разрушению компонента. Опасность SCC заключается в величине напряжений, необходимых для возникновения и распространения. Они намного ниже критических напряжений самого компонента. Эта форма коррозии не дает никаких видимых продуктов коррозии и поэтому часто ошибочно принимается за хрупкое разрушение, но материалы, подверженные SCC, в основном пластичны. [2] [5] [6] 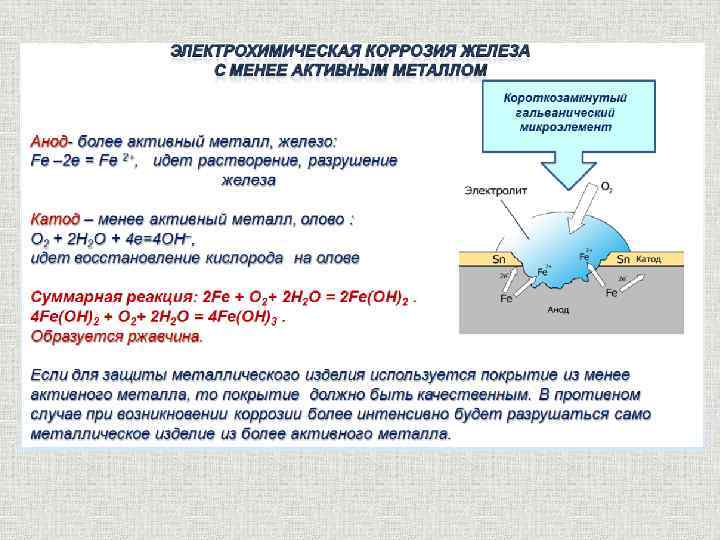 Будут образовываться трещины — в основном транскристаллитные — и компонент может разрушиться, даже если приложенные нагрузки не достигнут прочности на растяжение указанного материала. Коррозионная среда снизит количество циклов до отказа за счет сокращения времени до появления первых трещин. Скорость распространения этих трещин ускоряется из-за коррозионного воздействия. Этот процесс называется коррозионной усталостью и, в отличие от SCC, не зависит от типа материала. [6] [8]
Будут образовываться трещины — в основном транскристаллитные — и компонент может разрушиться, даже если приложенные нагрузки не достигнут прочности на растяжение указанного материала. Коррозионная среда снизит количество циклов до отказа за счет сокращения времени до появления первых трещин. Скорость распространения этих трещин ускоряется из-за коррозионного воздействия. Этот процесс называется коррозионной усталостью и, в отличие от SCC, не зависит от типа материала. [6] [8]  [2][8]
[2][8] 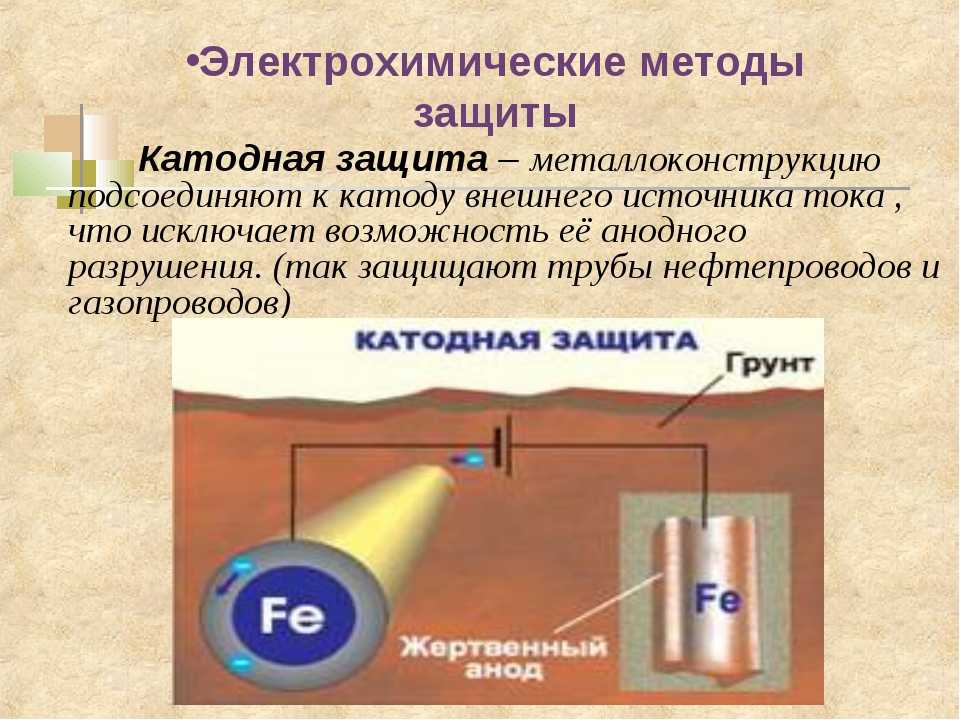 Это приведет к образованию в основном межкристаллитных трещин. Атомы водорода также могут реагировать с углеродом внутри металла и образовывать молекулы метана, которые будут собираться в пузыри. Эти пузыри приводят к потеря прочности и образование трещин [2] [5] [6] [8]
Это приведет к образованию в основном межкристаллитных трещин. Атомы водорода также могут реагировать с углеродом внутри металла и образовывать молекулы метана, которые будут собираться в пузыри. Эти пузыри приводят к потеря прочности и образование трещин [2] [5] [6] [8]  Когда эти пузырьки лопаются, на поверхность действуют высокие локальные силы, и защитные слои могут быть повреждены. [2] [8]
Когда эти пузырьки лопаются, на поверхность действуют высокие локальные силы, и защитные слои могут быть повреждены. [2] [8]  Другие менее реактивные горячие газы
Другие менее реактивные горячие газы