Коррозия химическая и электрохимическая: Химическая коррозия
Содержание
Виды коррозии, защита и хранение металлических изделий
Несоблюдение правил хранения может привести к порче продукции. Гарантия производителя на изделия из оцинкованной стали предоставляется только в том случае, если соблюдены все условия транспортировки, хранения и монтажа изделий.
Основой оцинкованных изделий служит стальной лист, на котором под внешним воздействием атмосферы возможно возникновение коррозии. Чтобы этого избежать тонколистый стальной прокат обработан несколькими защитными слоями: цинковым и несколькими полимерными покрытиями, которые препятствуют прямому контакту стали с внешней средой.
Если оцинкованная сталь подвергается воздействию влаги (дождь, роса, конденсат) в среде, где не хватает кислорода, то вода быстро реагирует с цинком и постепенно разъедает покрытие. Наиболее распространённые условия, в которых появляется белая ржавчина, — изделия хранятся в заводской упаковке и/или плотно прижатыми друг к другу.
Физико-химические процессы разрушения металла
Коррозия — это самопроизвольно протекающий процесс разрушения металла, вследствие химического или электрохимического взаимодействия металла с окружающей средой.
Различают химическую и электрохимическую коррозию.
Химическая коррозия — коррозия металла в газовой и жидкостной среде, не проводящей ток. Коррозия этого вида состоит в окислении металла в результате непосредственного его химического взаимодействия с окружающей средой. В таких средах, как воздух, продукты сгорания каменного угля и других видов топлива (нефть, бензин, керосин, смазочные масла) обычно развивается химическая коррозия.
Но наличие даже небольших количеств влаги в указанных веществах может в большей или меньшей степени сообщить коррозии электрохимический характер. Химическая коррозия в чистом виде — достаточно специфическое явление, преобладающее в средах, достаточно закрытых для окружающего природного воздействия. Большое практическое значение имеет электрохимическая коррозия.
Большое практическое значение имеет электрохимическая коррозия.
Электрохимическая коррозия
Электрохимическая коррозия имеет характер анодного окисления металла, которое может протекать по двум различным механизмам:
– гальванокоррозия — окисление металла, являющегося анодом самопроизвольно возникающей гальванической цепи;
– электрокоррозия — окисление металла, являющегося анодом своеобразной электролизной системы, самопроизвольно возникающей под влиянием тока от внешнего источника.
Гальванокоррозия
При гальванокоррозии основная масса металла обычно играет роль анода. В качестве материала катода могут служить самые разнообразные вещества, но обязательно являющиеся электронными проводниками. Сюда относятся более электронофильные металлы, чем анод. Например, по отношению к железному аноду такими металлами являются Sn, Pb, Cu, Hg, Ag и т.п. Роль катодов может выполнять и ряд электропроводящих неметаллических материалов, среди которых назовём ржавчину, зёрна графита, угля, цементита (карбида железа Fe3C), шлаковые включения в металл и т.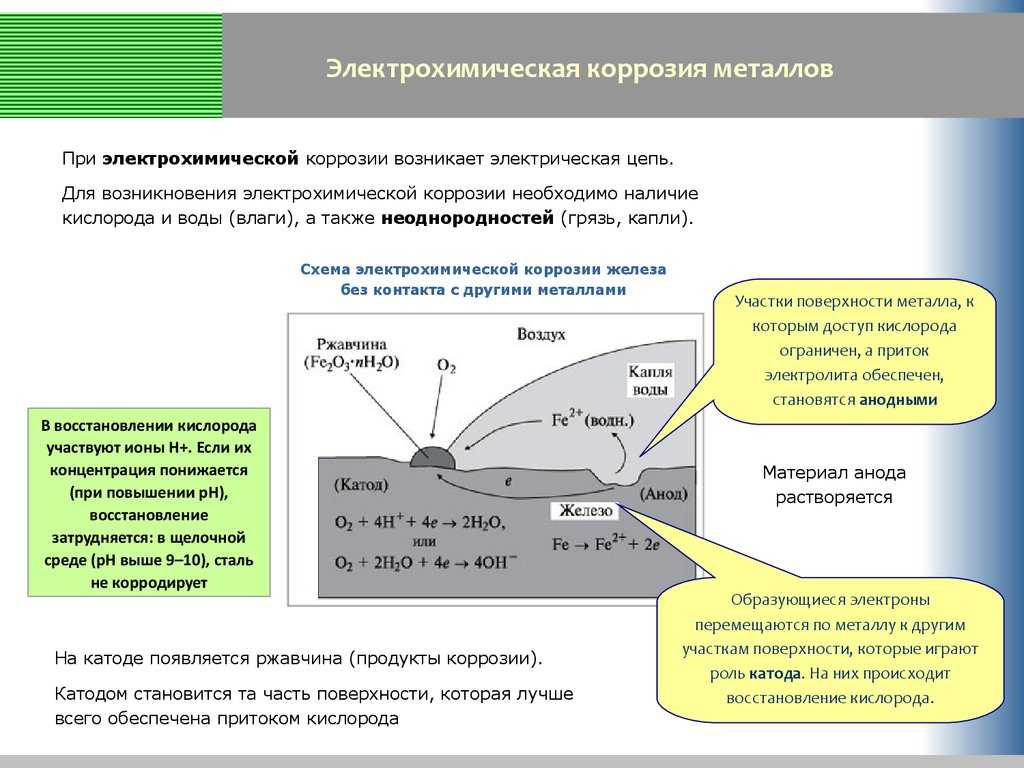 д.
д.
Процессы, протекающие при гальванокоррозии, рассмотрим на двух примерах, представляющих практический интерес: коррозию железа в контакте: а) с цинком и б) с оловом во влажном воздухе.
а) Коррозионный процесс в гальванопаре Zn/Fe. Цинк, как сравнительно более химически активный металл, подвергается анодному окислению и переходит в состояние ионов.
Реакция на аноде**: 2Zn – 4e- → 2Zn** (окисление).
Реакция на катоде: 2h3O + O2 + 4e- → 4OH’ (восстановление).
Вторичная реакция: 2Zn** + 4OH’ → 2Zn(OH)2.
В процессе работы коррозионной гальванопары Zn/Fe окисляется, разрушается цинк. За счёт электронов последнего железо предохраняется от коррозии.
б) Коррозионный процесс в гальванопаре Sn/Fe. В данном случае железо более химически активный металл, чем олово. Катодом гальванопары будет олово, а анодом — железо.
Реакция на аноде**: 2Fe – 4e- → 2Fe** (окисление).
Реакция на катоде: 2h3O + O2 + 4e- → 4OH’ (восстановление).
Они приводят к образованию бурой ржавчины.
Таким образом, в процессе работы рассматриваемой гальванопары окисляется и разрушается железо, а олово остается без изменения.
На практике подобные явления встречаются при коррозии оцинкованного и луженого железа. В случае нанесения на железо менее химически активного металла (Sn, Cu, Ni, Cr, Ag, Au), для придания поверхности декоративных и других полезных свойств, защита железа происходит путем его изоляции от внешней среды. При повреждении внешнего защитного слоя начинают протекать описанные реакции и железо ржавеет.
Коррозионные элементы могут возникать во всех случаях, когда в присутствии электролита соприкасаются металлы, различающиеся между собой электродными потенциалами.
Особо нужно отметить влияние температуры. Повышение температуры ускоряет физические и химические процессы. В водной среде это особенно заметно при температуре около 60°С. При температуре около 70°С в гальванопаре Zn/Fe может произойти изменение потенциала цинка, в результате чего цинковое покрытие становится катодам, а железо анодом. Отмечают, что изменению полярности цинка способствуют низкое содержание в воде кислорода и высокое бикарбонатов. В таких условиях коррозировать будет железо.
В водной среде это особенно заметно при температуре около 60°С. При температуре около 70°С в гальванопаре Zn/Fe может произойти изменение потенциала цинка, в результате чего цинковое покрытие становится катодам, а железо анодом. Отмечают, что изменению полярности цинка способствуют низкое содержание в воде кислорода и высокое бикарбонатов. В таких условиях коррозировать будет железо.
Электрокоррозия
К электрокоррозии относятся случаи электрохимической коррозии металлов, протекающие под влиянием электрического тока от внешнего источника. Здесь в основе явления, как уже отмечалось, лежит самопроизвольно возникающий процесс электролиза. В качестве примера рассмотрим электрокоррозию под влиянием так называемых блуждающих токов.
Металлические листы с полимерным покрытием, сложенные в пачку, представляют собой электрический конденсатор, где металлическая основа листа представляет собой обкладки конденсатора, а полимерное покрытие — диэлектрический слой между обкладками. В следствие неравномерности нагрева листов, воздействия внешних источников энергии и других факторов окружающей среды между различными листами пачки могут возникать разности электрического потенциала.
В следствие неравномерности нагрева листов, воздействия внешних источников энергии и других факторов окружающей среды между различными листами пачки могут возникать разности электрического потенциала.
В воде любого типа в большем или меньшем количестве содержатся растворенные соли, коллоидные и взвешенные вещества, живые микроорганизмы, в воду попадают частицы пыли и дыма. Поэтому при изучении поведения цинка и цинковых покрытий в водных средах воду следует рассматривать как коррозионный электролит. Если торцевую часть листов с разностью электрических потенциалов поместить в раствор соли, которым могут являться атмосферные осадки и конденсат, то возникает естественный процесс электролиза. На одном из листов, на его торцевой части, будет происходить анодное окисление металла, т.е. его коррозия.
Состав электролита, в особенности величина его рН, существенно влияет на скорость коррозии. Так, повышение концентрации Н’-ионов (кислая среда), как правило, резко убыстряет разрушение металла.
Повышение концентрации ОН’-ионов (щелочная среда) в электролите замедляет коррозию таких металлов, как Fe, Mg в следствии образования гидроокисных защитных плёнок.
У металлов Al, Zn, Pb повышение щелочности среды на разрушение этих металлов действует убыстряющим образом т.к. гидроокиси этих металлов растворимы в щелочах. Описанная особенность этих металлов является причиной такого явления как белая ржавчина.
Белая ржавчина на цинковом покрытии
Цинк — сравнительно реактивный металл, он активно реагирует с кислотами и щелочами. Лучше всего он проявляет свои антикоррозионные свойства в рН нейтральной среде. Долговечность цинкового покрытия зависит от формирования оксидно-карбонатной пленки. После окончательного формирования оксидно-карбонатной пленки уровень коррозии цинковых покрытий становится очень низким — не более двух микрон в год в нейтральной среде.
Химические реакции, требуемые для формирования этой плёнки, занимают некоторое время (от нескольких недель до нескольких месяцев):
1. Фаза окисления 2Zn + O2 = 2ZnO
Фаза окисления 2Zn + O2 = 2ZnO
2. Фаза гидратации 2Zn = 2h3O + O2 = 2Zn(OH)2
3. Карбонизации 5Zn(OH)2 = 2CO2 + 2ZnCO3.3Zn(OH)2 + 2h3O
На последнем этапе окончательно формируется трудно растворимый основной карбонат цинка, который обеспечивает надежную антикоррозионную защиту цинковому слою при негативном воздействии влаги. В условиях относительно сухой среды протекают все три реакции, и на поверхности оцинкованного изделия формируется оксидно-карбонатная плёнка, будучи почти непроницаемой для кислорода и влаги, резко ограничивает дальнейший процесс взаимодействия цинка с кислородом.
Иное происходит, если изделие свежеоцинкованное или на нём присутствуют места без сформированного плёночного покрытия (в частности, срезы профилированной продукции) хранится в условиях, когда на него воздействует дождь, роса, конденсат, а подвод углекислого газа и кислорода, способствующего образованию плотной оксидно-карбонатной пленки затруднен.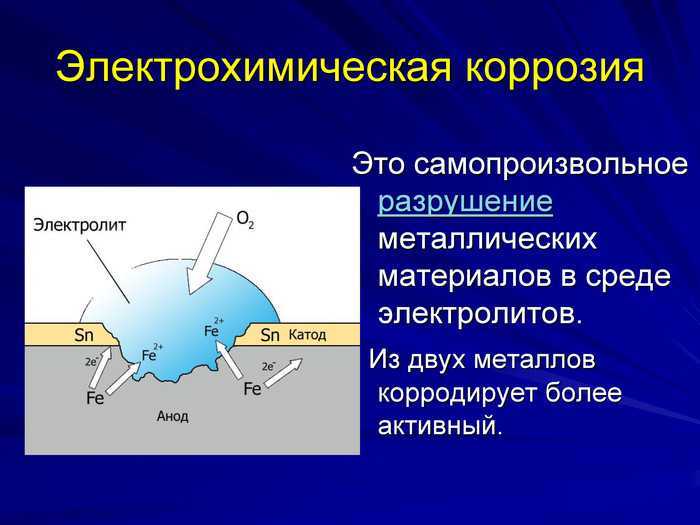 В этом случает происходят только фазы окисления и гидратации. В результате получаются гидроксид и оксид цинка — вещества в виде белого порошка, обладающие низкой адгезионной способностью к поверхности, легко пропускающие кислород к цинку, допускающие его последующее окисление и развитие процессов образования белой ржавчины.
В этом случает происходят только фазы окисления и гидратации. В результате получаются гидроксид и оксид цинка — вещества в виде белого порошка, обладающие низкой адгезионной способностью к поверхности, легко пропускающие кислород к цинку, допускающие его последующее окисление и развитие процессов образования белой ржавчины.
Еще одним случаем, представляющим опасность образования белой ржавчины, являются участки соприкасающихся между собой поверхностей оцинкованных изделий с уже окончательно сформировавшейся оксидно-карбонатной плёнкой. В этих местах задерживается дождевая влага (или конденсируется влага из воздуха при нахождении изделий на воздухе при температуре ниже точки росы), а испаряется она в последнюю очередь. Во всех природных водах присутствует углекислота, которая может находиться в воде в виде растворенного газа СО2 и недиссоциированных молекул Н2СО3 или ионов НСО3- и СО3в2-. Углекислота и присутствующие в воде нитраты, сульфаты, хлориды без доступа кислорода разрушают образующуюся на поверхности цинка оксидно-карбонатную пленку и тем самым усиливают коррозию, приводящую к образованию белой ржавчины.
При очень длительном хранении (от полугода) оцинкованных изделий с полимерным покрытием в неблагоприятных условиях, оксид и гидроксид цинка — вещества в виде белого порошка может выделяться и на поверхности полимерного покрытия (в особенности на обратной стороне листа, который как правило покрыт только грунтовым полимерным слоем).
В благоприятных (для белой ржавчины) условиях разъедание цинка может происходить при уровнях коррозии в 20–50 раз больших, чем обычно предполагается.
Условия хранения и эксплуатации
Из всего вышеизложенного можно сделать следующие выводы.
Цинковое покрытие стальных изделий хорошо работает как защитный слой в нейтральной сухой или влажной воздушной среде и при кратковременном воздействии воды со свободным доступом кислорода. При таких условиях работает эффект гальванопары Zn/Fe — эффект оксидно-карбонатной пленки. Такие условия соответствуют нормальным условиям эксплуатации изделий.
В случае долговременного нахождения стальных оцинкованных изделий, сложенных в пачку, в водной среде при ограниченном доступе кислорода и повышенной температуре (более 70°С), начинают протекать реакции, при которых защитные эффекты перестают работать. Происходит активное разрушение защитного слоя. Как правило, такие негативные условия складываются при неправильном хранении изделий. При нарушении условий хранения риск поражения коррозией значительно выше, чем при неправильной эксплуатации или монтаже.
Правила хранения оцинкованных изделий:
• Изделия хранятся в заводской упаковке НЕ более 1 (одной) недели с даты поставки. Пачки в заводской упаковке укладываются на ровное место на бруски с шагом 0,5 м.
• При необходимости хранения профилированной продукции более 1 (одной) недели ее размещают под навесами или в крытых неотапливаемых, сухих помещениях без прямого воздействия солнечных лучей и осадков (в соответствии с ГОСТ 7566).
Изделия следует распаковать (снять заводскую упаковку), расположить на ровной поверхности и переложить каждый лист одинаковыми рейками (штабель высотой до 70 см).
• Хранение на открытом воздухе допускается только на период монтажных работ. Изделия должны быть расположены под небольшим наклоном в 3° так, чтобы между ними обеспечивались свободная циркуляция воздуха и слив воды.
• Максимальный срок хранения во всех вышеперечисленных условиях не должен превышать 2 (двух) месяцев с даты поставки.
Используемая литература:
- «Общая химия» учебники и учебные пособия для высших сельскохозяйственных учебных заведений. А.Г. Кульман. Издательство «Колос» 1968.
- «Курс общей химии» учебник для студентов вузов. Коровин Н.В., Масленникова Г.Н., Гуськова Л.Г. и др. под ред. Коровина Н.В. Высш. школа 1981.
- «Защита от коррозии, старения и биоповреждений машин, оборудовани и сооружений» Справочник в 2т.
 Т1. Под ред. Герасименко А.А. М. Машиностроение. 1987.
Т1. Под ред. Герасименко А.А. М. Машиностроение. 1987. - «Основы учения о коррозии и защите металлов» Дж. Скалли. Перевод с английского проф. А.В. Шрейдера. Издательство «Мир», Москва 1978.
- СТБ 1527-2005 «Профили металлические холодногнутые для наружной облицовки фасадов зданий и комплектующие изделия к ним».
- СТБ 1382-2003 «Профили металлические холодногнутые для кровель и комплектующие изделия к ним».
- ГОСТ 7566-2018 «Металлопродукция. Правила приемки, маркировка, упаковка, транспортирование и хранение».
Страница не найдена — Инженерная практика
Свежий выпуск: №
06-07/2022
Популярное в этом месяце
Результаты работы с механизированным фондом скважин ПАО «ЛУКОЙЛ» за 2021 год
РЕНЕВ Дмитрий Юрьевич, ПАО «ЛУКОЙЛ»
Анализ промысловых данных и динамическое моделирование механизированной добычи малодебитными скважинами
ЮЩЕНКО Тарас Сергеевич, ООО «Газпромнефть – Технологические партнерства»ДЕМИН Евгений Викторович, ООО «Газпромнефть НТЦ»
Публикации автора на сайте журнала «Инженерная практика»
БЕЛОВ Петр Васильевич, ООО «Лайтор»
Автономный актив. Отдельные элементы и перспективы развития
Отдельные элементы и перспективы развития
КУЗЬМИН Максим Игоревич, ООО «Газпромнефть НТЦ»ГРЕХОВ Иван Викторович, ООО «Газпромнефть НТЦ»ГЕРАСИМОВ Ростислав Владимирович, ООО «Газпромнефть НТЦ»
Повышение эффективности добычи трудноизвлекаемых запасов скважинами малого диаметра
КУПАЕВ Илья Денисович, ТПП «РИТЭК-Самара-Нафта»МЕДВЕДЕВ Алексей Сергеевич, АО «РИТЭК»
Ближайшие совещания
Отраслевая техническая Конференция
Эксплуатация осложненного фонда (ОФ) скважин ‘2022. Эффективные технологии для работы с ОФ в российских нефтегазовых Компаний. Новые вызовы. Технологическая независимость.
Эффективные технологии для работы с ОФ в российских нефтегазовых Компаний. Новые вызовы. Технологическая независимость.
22-24 ноября 2022 года, г. г. Сургут
Ближайшие тренинги
Тренинг-курс
Ловильный сервис на нефтяных и газовых скважинах
14-18 ноября 2022 г., г. Пермь
Большие проблемы в исследованиях электрохимической коррозии
Коррозия – это процесс деградации или разрушения материала в результате химической реакции между материалом и окружающей средой. Это незаменимая область исследований в области материаловедения и инженерии, поскольку коррозионная стойкость характеризует стабильность или долговечность материала, что является одним из наиболее важных характеристик материала при применении.
Это незаменимая область исследований в области материаловедения и инженерии, поскольку коррозионная стойкость характеризует стабильность или долговечность материала, что является одним из наиболее важных характеристик материала при применении.
По сравнению с другими материалами металлы относительно активны и, вероятно, подвержены коррозии. Таким образом, исследования коррозии в основном касаются механизма повреждения и поведения различных металлов, включая черные и цветные, монокристаллы или нанокристаллы, литые или кованые, а также конструкционные или функциональные сплавы. Он естественным образом разросся в разные ветви на основе сплава (Шрейр и др., 19).94), таких как коррозия стали, коррозия алюминиевых сплавов, коррозия никелевых сплавов и т. д. Состав и микроструктура всегда являются наиболее решающими факторами в определении коррозионной стойкости сплава. В этом аспекте критическим вопросом, который необходимо решить, является то, как на процесс коррозии влияют фазовый состав матрицы, сегрегированный легирующий элемент, структура решетки, кристаллический дефект, ориентация кристаллов, размер зерна, состав вторичной фазы, распределение интерметаллических частиц, пористость, микроструктура. плотность трещин, уровень примесей и состояние поверхности.
плотность трещин, уровень примесей и состояние поверхности.
Другим важным аспектом исследования коррозии является сложное влияние факторов окружающей среды на коррозию. Чувствительность коррозионного поведения к факторам окружающей среды привела к различной степени и формам повреждения металлов в различных условиях эксплуатации (Cramer and Covino, 2006). В зависимости от среды, которой подвергаются металлы, коррозию можно легко разделить на различные типы, такие как водная или неводная коррозия, коррозия окружающей среды или высокотемпературная коррозия, кислотная или щелочная коррозия и т. д. В естественной среде атмосферная коррозия, морская вода коррозия и подземная коррозия обычно по-разному воздействуют на металлы. Различные проблемы с коррозией, связанные с условиями обслуживания, также часто возникают в химической, нефтегазовой, трубопроводной, гражданской, автомобильной, аэрокосмической, военной, ядерной и медицинской отраслях. Поскольку большинство факторов окружающей среды, таких как температура, давление, химический состав, концентрация компонентов, значение pH, электрическая или теплопроводность, вязкость и т. д., могут прямо или косвенно взаимодействовать и постоянно или непостоянно влиять на процесс коррозии, прогнозирование долгосрочных коррозионное поведение довольно сложно. Выявление ключевого влияющего фактора и понимание его влияния на кинетику коррозии должно быть предметом исследования в этом аспекте.
д., могут прямо или косвенно взаимодействовать и постоянно или непостоянно влиять на процесс коррозии, прогнозирование долгосрочных коррозионное поведение довольно сложно. Выявление ключевого влияющего фактора и понимание его влияния на кинетику коррозии должно быть предметом исследования в этом аспекте.
В основе исследований коррозии лежит изучение механизма реакции материала с окружающей средой. Именно фундаментальное понимание подробных реакционных процессов, процедур и стадий, а также факторов, влияющих на них, лежит в основе науки о коррозии. Большинство проблем с коррозией в окружающей среде можно отнести к электрохимическим реакциям (Kaesche, 2003), поскольку влага и водная жидкость широко распространены в естественной среде, а электрохимическая реакция обычно протекает быстрее, чем реакции окисления-восстановления в условиях окружающей среды. Коррозионное разрушение, вызванное напряжением, во многих случаях является результатом сложных взаимодействий между напряжением и электрохимическими реакциями; напряжение резко облегчает электрохимический процесс, а последнее резко усиливает повреждающее действие первого.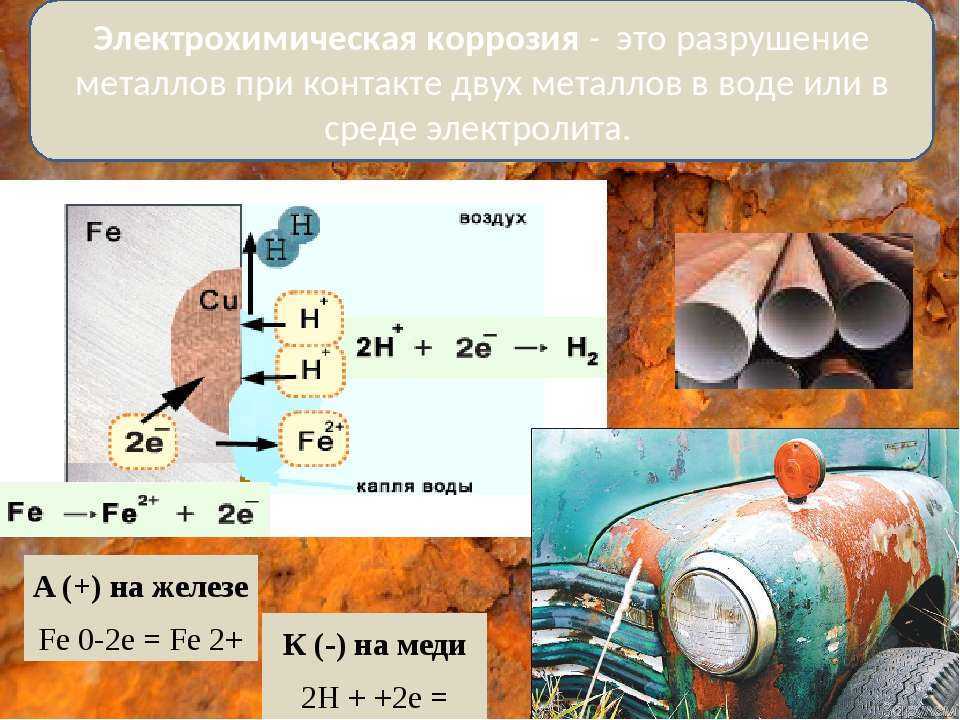 Даже при высоких температурах коррозию расплавленной соли также можно описать как электрохимический процесс. Таким образом, электрохимия является одним из наиболее актуальных предметов исследования коррозии (Mansfeld and Bertocci, 2005). Чтобы получить представление об основной области науки о коррозии, следует уделить первоочередное внимание изучению подробных электрохимических механизмов и созданию моделей интерфейса металл-электролит.
Даже при высоких температурах коррозию расплавленной соли также можно описать как электрохимический процесс. Таким образом, электрохимия является одним из наиболее актуальных предметов исследования коррозии (Mansfeld and Bertocci, 2005). Чтобы получить представление об основной области науки о коррозии, следует уделить первоочередное внимание изучению подробных электрохимических механизмов и созданию моделей интерфейса металл-электролит.
Изучив основные аспекты и суть науки о коррозии, никогда не следует забывать, что конечной целью исследований коррозии является минимизация коррозионного повреждения. В связи с этим большой интерес представляют все методы, способные препятствовать реакции металла с окружающей средой и эффективно замедлять коррозионный процесс. Фактически, катодная защита (Baeckmann et al., 1997), покрытие (Swaraj, 1996), обработка/модификация поверхности (Biestek and Weber, 1976) и ингибитор (Braford, 19).93) методы, которые замедляют коррозию с помощью различных механизмов, имеют долгую историю успешного уменьшения коррозионного повреждения на практике. Они создали важное продолжение науки о коррозии, которая более или менее пересекается с наукой о поверхностях и покрытиях, технологиями и инженерией. Хотя технологические инновации являются центральной темой в этой области, очень желательны научные прорывы. Инновации в предотвращении коррозии часто появляются, когда новые идеи, методы и результаты других дисциплин внедряются в эту прикладную область исследований коррозии.
Они создали важное продолжение науки о коррозии, которая более или менее пересекается с наукой о поверхностях и покрытиях, технологиями и инженерией. Хотя технологические инновации являются центральной темой в этой области, очень желательны научные прорывы. Инновации в предотвращении коррозии часто появляются, когда новые идеи, методы и результаты других дисциплин внедряются в эту прикладную область исследований коррозии.
Из приведенного выше краткого введения можно выделить следующие основные характеристики, которые практически отличают исследования коррозии от других дисциплин материаловедения и инженерии:
(1) Коррозия возникает в сложной системе, на которую одновременно воздействуют факторы окружающей среды и металлургические параметры. . Эти взаимодействующие факторы чрезвычайно усложняют коррозионную систему. Таким образом, невозможно четко определить ключевой влияющий фактор и этап, определяющий скорость, которые управляют фундаментальной кинетикой процесса коррозии. Следовательно, многие коррозионные явления не поддаются теоретическому объяснению. Исследования коррозии в некоторых случаях должны опираться на значительный объем эмпирических знаний.
Следовательно, многие коррозионные явления не поддаются теоретическому объяснению. Исследования коррозии в некоторых случаях должны опираться на значительный объем эмпирических знаний.
(2) Коррозия — процесс, чувствительный ко времени. Поскольку большинство факторов окружающей среды могут заметно меняться со временем, коррозионные характеристики металла могут быть невероятно разными на разных стадиях. Даже в коррозионной системе с постоянными факторами внешней среды и строго контролируемыми начальными и граничными условиями состояние корродирующей поверхности может меняться во времени за счет растворения металла или отложения продуктов коррозии. Следовательно, различные параметры окружающей среды в сочетании со сложным влиянием факторов окружающей среды делают теоретическое предсказание коррозии чрезвычайно трудным.
(3) Отсутствуют методы с высоким разрешением in situ для выявления механизма коррозии. Из-за зависимости коррозии от условий окружающей среды измерения ex situ могут не дать существенной информации о процессе коррозии или могут исказить эту информацию.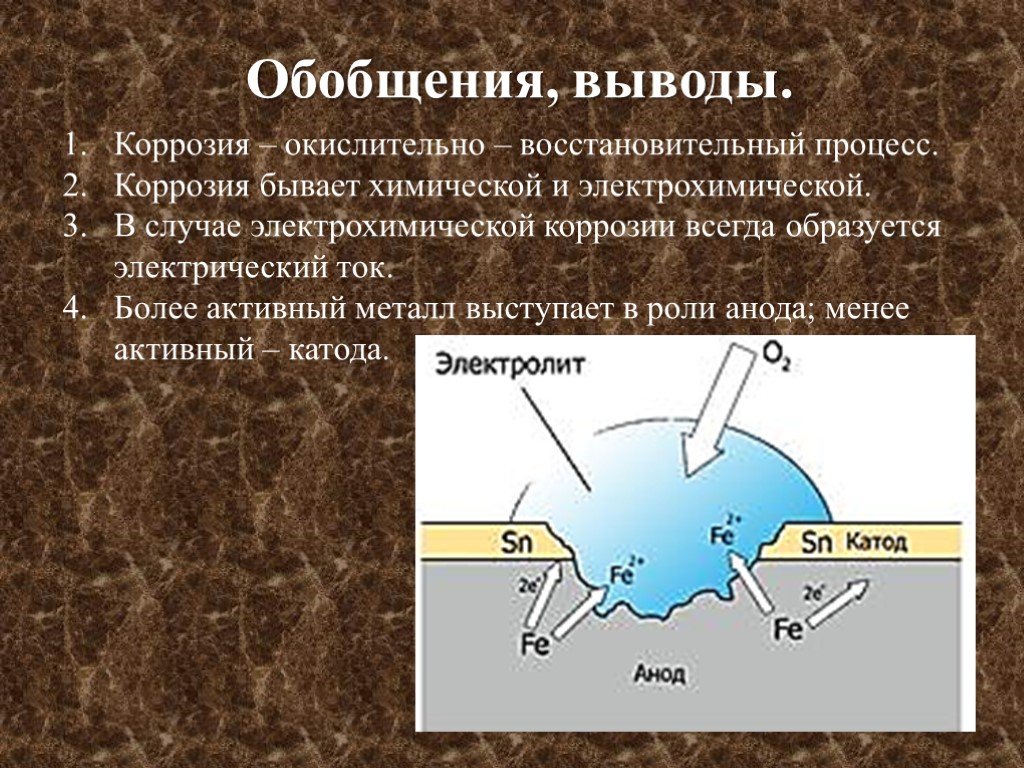 В настоящее время большинство передовых инструментов, обычно используемых для характеристики микроструктуры и состава поверхности металла на наноуровне, должны работать в высоком вакууме, или требуют тщательной предварительной обработки/подготовки образца, или требуют добавления некоторых вспомогательных частиц для провоцируют дополнительные реакции в коррозионной системе. Они не могут производить настоящие in situ возникает из-за ненарушенной корродирующей поверхности в агрессивных средах. Ожидается, что некоторые новые появляющиеся методы с высоким разрешением in situ , например, специально разработанная электролитная ячейка, которую можно установить в SEM или TEM, станут доступными для большинства исследователей коррозии при изучении микроструктуры и состава корродирующей поверхности в жидкие среды.
В настоящее время большинство передовых инструментов, обычно используемых для характеристики микроструктуры и состава поверхности металла на наноуровне, должны работать в высоком вакууме, или требуют тщательной предварительной обработки/подготовки образца, или требуют добавления некоторых вспомогательных частиц для провоцируют дополнительные реакции в коррозионной системе. Они не могут производить настоящие in situ возникает из-за ненарушенной корродирующей поверхности в агрессивных средах. Ожидается, что некоторые новые появляющиеся методы с высоким разрешением in situ , например, специально разработанная электролитная ячейка, которую можно установить в SEM или TEM, станут доступными для большинства исследователей коррозии при изучении микроструктуры и состава корродирующей поверхности в жидкие среды.
Помимо этих основных характеристик исследования коррозии и вытекающих из этого трудностей, существует множество сложных вопросов, требующих решения, некоторые из которых стали серьезными препятствиями, критически препятствующими дальнейшему развитию науки о коррозии. Успешное решение этих критических проблем может значительно продвинуть эту область. Например, следующие темы особенно сложны и могут заинтересовать исследователей, занимающихся коррозионной наукой.
Успешное решение этих критических проблем может значительно продвинуть эту область. Например, следующие темы особенно сложны и могут заинтересовать исследователей, занимающихся коррозионной наукой.
(1) Коррозия метастабильных металлов: в то время как наука о материалах распространяется на нанотехнологии и метастабильные микроструктуры, такие как аморфные и нанокристаллические сплавы, современные принципы коррозии, основанные на традиционных кристаллических металлах, начинают сталкиваться с новыми проблемами. Понимание реакции коррозии на поверхности, состоящей из чрезвычайно высокой плотности дефектов, является новой областью в науке о коррозии. Чтобы расширить и углубить знания о коррозии и обеспечить практическое применение инновационных материалов, в первую очередь необходимо решить задачу разработки новых теорий коррозии для высокоактивированной металлической поверхности.
(2) Коррозия и защита передовых технических металлов: по мере роста спроса на материалы с некоторыми весьма желаемыми свойствами несколько сплавов, которые изначально считались непригодными для некоторых применений, теперь попадают в короткий список кандидатов. Например, сплавы Mg изначально были слишком активны, чтобы быть популярными конструкционными материалами, но теперь высокое соотношение прочности и веса делает их привлекательными в автомобильной промышленности в качестве материалов-кандидатов для автомобилей следующего поколения. Эти типы материалов обычно имеют коррозионное поведение, отличное от традиционных сплавов, и существующие знания и технологии защиты от коррозии и защиты не могут быть непосредственно применены к ним. Важно и сложно продолжать дальнейшее развитие существующих принципов и методов коррозии для покрытия этих передовых технических сплавов.
Например, сплавы Mg изначально были слишком активны, чтобы быть популярными конструкционными материалами, но теперь высокое соотношение прочности и веса делает их привлекательными в автомобильной промышленности в качестве материалов-кандидатов для автомобилей следующего поколения. Эти типы материалов обычно имеют коррозионное поведение, отличное от традиционных сплавов, и существующие знания и технологии защиты от коррозии и защиты не могут быть непосредственно применены к ним. Важно и сложно продолжать дальнейшее развитие существующих принципов и методов коррозии для покрытия этих передовых технических сплавов.
(3) Подробный механизм влияния наноструктуры на коррозию: коррозионная стойкость сплава в основном определяется его поверхностными «слабыми местами». Эти активные центры на поверхности фактически представляют собой кристаллические дефекты, такие как дислокации, двойники, границы зерен, границы раздела фаз, сегрегированные легирующие элементы, осажденные интерметаллиды или примесные включения. Понимание деталей коррозионной реакции в этих местах, очевидно, является неизбежным шагом в решении центральной проблемы науки о коррозии. К сожалению, эти дефекты обычно находятся в наномасштабе. Выявить механизм микрокоррозии в этих дефектных участках до получения 9 высокого разрешения — большая проблема.0019 in situ экспериментальных методов освоены учеными-коррозионистами.
Понимание деталей коррозионной реакции в этих местах, очевидно, является неизбежным шагом в решении центральной проблемы науки о коррозии. К сожалению, эти дефекты обычно находятся в наномасштабе. Выявить механизм микрокоррозии в этих дефектных участках до получения 9 высокого разрешения — большая проблема.0019 in situ экспериментальных методов освоены учеными-коррозионистами.
(4) Механизм коррозии и технология предотвращения коррозии в экстремальных условиях: к экстремальным условиям относятся чрезвычайно сильные помехи электрических и магнитных полей, облучения, давления, температуры и т. д. Коррозионные повреждения в этих суровых условиях обнаружены в ядерной, аэрокосмической , газовая / нефтяная и химическая промышленность. Однако до того, как исследователи получат in situ , специально разработанные для этих экстремальных условий, их понимание этого вида коррозии не может быть таким всеобъемлющим, как понимание коррозии окружающей среды. Кроме того, из-за суровых условий эксплуатации и ограниченности промышленных методов эксплуатации в этих отраслях отчаянно не хватает экономически эффективных мер по предотвращению коррозии. Поскольку этот вид коррозии может в конечном итоге угрожать общественной безопасности, ученый-коррозионист обязан принять вызов, чтобы улучшить понимание коррозии в экстремальных условиях и разработать более эффективные методы предотвращения.
Поскольку этот вид коррозии может в конечном итоге угрожать общественной безопасности, ученый-коррозионист обязан принять вызов, чтобы улучшить понимание коррозии в экстремальных условиях и разработать более эффективные методы предотвращения.
(5) Понимание, мониторинг и моделирование коррозии in vivo : человеческое тело представляет собой сложную самоподдерживающуюся коррозионную систему. Коррозия in vivo представляет собой процесс биодеградации, происходящий в очень хорошо контролируемой окружающей среде. Измерения коррозии на месте или мониторинг в режиме реального времени без нарушения физиологических реакций внутри человеческого тела затруднены. Сложное влияние физиологических реакций и компонентов жидкости организма на коррозию является еще одним препятствием для понимания in vivo механизм коррозии. Также маловероятно точное моделирование реальной среды in vivo путем имитации жидкости организма и физиологических реакций в лаборатории. Поэтому исследование механизма биодеградации и процесса коррозии in vivo в лаборатории останется сложной задачей в исследованиях коррозии.
Поэтому исследование механизма биодеградации и процесса коррозии in vivo в лаборатории останется сложной задачей в исследованиях коррозии.
(6) Прогнозирование коррозии в реальных условиях: в естественной среде условия спонтанной коррозии не контролируются. Более того, существует множество изменений факторов окружающей среды, которые могут влиять на коррозию, что в значительной степени усложняет коррозионный процесс. Хуже того, неизбежная жизненная деятельность в реальном мире также может влиять на процесс коррозии, что делает поведение коррозии почти непредсказуемым. Например, микробио/бактерии, колонизирующие канализационные системы, образование биопленки на морской инфраструктуре, загрязнение воздуха автомобильными выхлопами и загрязнение почвы/подземных вод бытовыми отходами могут неожиданно ускорить коррозию открытых объектов. . Непредвиденная коррозия инфраструктуры под землей, в бетоне или в воде при определенных обстоятельствах может привести к катастрофе. Чтобы снизить риск, прогнозирование коррозионных характеристик в естественных условиях считается большой проблемой в исследованиях коррозии. В этом аспекте создание долгосрочной базы данных о коррозии является важной задачей, а компьютерное моделирование может стать подходом, который может привести к прорыву в прогнозировании коррозии.
В этом аспекте создание долгосрочной базы данных о коррозии является важной задачей, а компьютерное моделирование может стать подходом, который может привести к прорыву в прогнозировании коррозии.
(7) Механизм перехода состояния поверхности: начало пассивации, возникновение питтинга и разрушение поверхностной пленки являются примерами перехода состояния поверхности. Таких поверхностных изменений на практике гораздо больше. Переход от исходной поверхности к новому стационарному состоянию является переходным процессом. Новое состояние обычно зависит от начальных условий поверхности, которые в конечном итоге могут повлиять на общее коррозионное повреждение. Например, разрыв первоначально сформированной пленки может в значительной степени повлиять на характер роста пленки на более поздней стадии; распределение точечной коррозии на поверхности металла на ранней стадии будет влиять на конечную морфологию коррозии; исходная чистота поверхности стали иногда может определять пассивность стали. Очень интересно узнать, как, когда и где внезапно начинается переход. Предсказать появление перехода на металлической поверхности сложно, но это сложная цель, которую необходимо решить при исследовании коррозии.
Очень интересно узнать, как, когда и где внезапно начинается переход. Предсказать появление перехода на металлической поверхности сложно, но это сложная цель, которую необходимо решить при исследовании коррозии.
(8) Разработка антикоррозионных функциональных покрытий: покрытия могут полностью изменить свойства поверхности металла, что открывает множество новых областей применения металлов. Улучшенная коррозионная стойкость или защитная способность традиционно являются важным требованием для разработки покрытий в технике предотвращения коррозии. Вообще говоря, коррозионная стойкость покрытия зависит от стабильности материала покрытия, целостности и толщины слоя покрытия и адгезии покрытия к металлам. Это также зависит от того, как покрытие реагирует на температуру, нагрузку и истирание в процессе эксплуатации. Антикоррозионное покрытие обычно представляет собой компромисс многих требований. Если новое покрытие может быть электро- или теплоизолирующим или проводящим, противоскользящим или самовыделяющим смазку, супергидрофобным или гидрофильным, избирательно адсорбирующим и поглощающим определенные виды и т. д., оно найдет гораздо более широкое применение. себя, а также значительно расширить применение металлических компонентов/деталей в промышленности. Однако у такого покрытия будет слишком много противоречивых требований, чтобы идти на компромисс. Его изобретение и разработка не только сложны, но и интересны.
д., оно найдет гораздо более широкое применение. себя, а также значительно расширить применение металлических компонентов/деталей в промышленности. Однако у такого покрытия будет слишком много противоречивых требований, чтобы идти на компромисс. Его изобретение и разработка не только сложны, но и интересны.
Таким образом, коррозия как процесс разрушения материала, вызванный реакцией материала с окружающей его средой, интенсивно и всесторонне исследовалась. Много достижений было сделано в отношении состава сплава и влияния микроструктуры, влияния факторов окружающей среды, механизма коррозии и методов защиты. Однако подробный механизм коррозии in situ под влиянием множества различных факторов не был всесторонне раскрыт из-за отсутствия 9 высокого разрешения.0019 in situ методов. В настоящее время самая большая трудность в исследованиях коррозии состоит в том, чтобы получить глубокое понимание процесса разложения in situ на коррозионной поверхности, скрытой коррозионной средой. Вокруг этого есть по крайней мере восемь больших проблем на передовых рубежах исследований коррозии. Оспаривание этих актуальных тем может привести к прорыву в области науки о коррозии.
Вокруг этого есть по крайней мере восемь больших проблем на передовых рубежах исследований коррозии. Оспаривание этих актуальных тем может привести к прорыву в области науки о коррозии.
Бекманн В., Швенк В. и Принц В. (1997). Справочник по катодной защите от коррозии , 3-е изд. Хьюстон, Техас: Издательство Gulf Professional.
Бистек Т. и Вебер Дж. (1976). Электролитические и химические конверсионные покрытия . Редхилл: Portcullis Press Limited.
Брафорд, С.А. (1993). Защита от коррозии . Лондон: Ван Рейнхольд.
Крамер, С. Д., и Ковино, Б. С. младший (редакторы) (2006). Справочник по ASM, том 13C: Коррозия: окружающая среда и промышленность . Парк материалов, Огайо: ASTM International.
Каеше, Х. (2003). Коррозия металлов, физико-химические основы и актуальные проблемы . Берлин: Спрингер.
Мансфельд Ф. и Берточчи У. (ред.) (2005 г.). Коррозионные испытания и стандарты , 2-е изд. Западный Коншохокен, Пенсильвания: ASTM International.
Shreir, L.L., Jarman, A.A., and Burstein, G.T. (eds) (1994). Коррозия-Том 1: Реакции металла/окружающей среды . Бостон, Массачусетс: Баттерворт Хайнеманн.
Сварадж, П. (1996). Поверхностные покрытия: наука и технология , 2-е изд. Чичестер: Джон Вили и сыновья.
Коррозия: электрохимическая | Машиностроение
Коррозия окружает нас повсюду, в нашей повседневной жизни, тихо работает и идет своим чередом. Коррозия — это ухудшение свойств материала из-за реакции с окружающей средой. NACE определяет коррозию как «разрушение вещества (обычно металла) или его свойств из-за реакции с окружающей средой». и другие материалы также подвержены коррозии.
Последствия коррозии можно увидеть повсюду: на наших домах, на детских площадках, на наших автомобилях, зданиях и мостах. Если его не остановить, это может привести к серьезным авариям, таким как обрушение моста I-35W в Миннеаполисе 1 августа 2007 г., в результате которого 13 человек погибли и 145 получили ранения 2 , или рейс Aloha 243, у которого в середине полета произошла взрывная декомпрессия, оторвавшая часть. фюзеляжа, в результате чего один член экипажа погиб и 65 пассажиров и членов экипажа получили ранения 3 .
фюзеляжа, в результате чего один член экипажа погиб и 65 пассажиров и членов экипажа получили ранения 3 .
Коррозия также имеет финансовые последствия. В США коррозия вызывает ежегодные убытки в размере 47,9 млрд долларов в коммунальном хозяйстве, 29,7 млрд долларов в транспортной отрасли, 22,6 млрд долларов в инфраструктуре, 20,1 млрд долларов в государственных структурах и 17,6 млрд долларов в производстве и обрабатывающей промышленности 4 . Это составляет 275,7 млрд долларов в год из-за коррозии, при этом самые большие затраты приходятся на системы питьевой воды и канализации на 36 млрд долларов и увеличиваются 5 .
Исследования коррозии показали нам, что существует два основных механизма коррозии: электрохимическое и химическое окисление. Оба этих типа имеют множество форм и разветвлений, некоторые из них более выражены, чем другие, но механизм, с помощью которого они разлагают вещество или материал, всегда можно проследить до одного из этих двух типов. В этой части статьи мы рассмотрим механизм электрохимической коррозии и ее наиболее распространенные формы.
В этой части статьи мы рассмотрим механизм электрохимической коррозии и ее наиболее распространенные формы.
Электрохимическая коррозия
Электрохимическая коррозия — это процесс, посредством которого металл возвращается в состояние окисления с наименьшей энергией. Чтобы правильно понять электрохимическую коррозию, нужно понять, как находят руды и превращают их в металл.
Необработанные руды берутся из природы, где некоторые из них существуют в химическом соединении с другими элементами в термодинамически стабильном состоянии. Например, железо встречается вместе с оксидами, гидратами и сульфидами. Чтобы извлечь или очистить железо, энергия (тепло) нагнетается в руду, чтобы превратить ее в металл. Это приводит к тому, что железная руда восстанавливается и становится термодинамически нестабильной. Фундаментальные законы термодинамики диктуют, что нестабильная система в конечном итоге возвращается к своей стабильной форме, равновесию.
Однако некоторые металлы уже встречаются в природе в металлической форме, например, золото, и поэтому уже стабильны в металлической форме, поэтому золото не подвергается коррозии. Это не означает, что только те металлы, которые встречаются в природе в чистом металлическом виде, являются единственными, которые не подвергаются коррозии, есть руды, которые при окислении дают металл, который не подвергается коррозии, разница в том, что количество энергия (тепло), необходимая для окисления руды, в этом случае минимальна.
Это не означает, что только те металлы, которые встречаются в природе в чистом металлическом виде, являются единственными, которые не подвергаются коррозии, есть руды, которые при окислении дают металл, который не подвергается коррозии, разница в том, что количество энергия (тепло), необходимая для окисления руды, в этом случае минимальна.
Нестабильные металлы становятся стабильными в течение многих лет в результате электрохимической коррозии, если их не защитить. Для возникновения электрохимической коррозии необходимо наличие коррозионной ячейки. Коррозионная ячейка представляет собой комбинацию четырех элементов: анода, катода, электролита и металлического пути, соединяющего анод и катод. Без любого из этих четырех элементов коррозии не будет, все элементы должны присутствовать. Современные исследования показали, что кислород может сильно влиять на коррозию, и эксперты часто считают его очень важным элементом, утверждая, что в некоторых формах коррозии кислород является последним завершающим этапом для достижения истинного состояния с самой низкой энергией.
- На аноде происходит фактическая потеря металла. Ионизируясь в электролите, ионы высвобождают электроны в ходе сложной серии химических реакций с образованием оксида железа (Fe2O3) и кислорода. Оксид железа — это то, что мы обычно называем ржавчиной.
- Катод является чрезвычайно важным элементом коррозионной ячейки, поскольку он определяет скорость коррозии. Электроны с анода перемещаются к катоду и задерживаются там. Чем больше электронов может разместить катод, тем быстрее будет корродировать анод. Это основная взаимосвязь между анодом и катодом в коррозионной ячейке.
- Электролит также является важным элементом коррозионной ячейки, поскольку это раствор, который окружает анод и катод. Электролит также влияет на скорость коррозии, поскольку проводимость электролита либо позволяет электронам свободно перемещаться от анода к катоду, либо ограничивает их поток, тем самым снижая скорость коррозии.
- Металлический путь — это то, что некоторые могут назвать внутренней цепью, поскольку она обеспечивается металлом, в котором находятся анод и катод.
 Металлический путь замыкает цепь коррозии.
Металлический путь замыкает цепь коррозии.
Кислород считается важным фактором коррозии, поскольку без кислорода коррозия замедляется и в конечном итоге останавливается. Кислород отвечает за реакцию с ионами водорода, которые высвобождаются на катоде из-за аккомодации электронов. При недостатке кислорода ионы водорода накапливаются на катоде и препятствуют аккомодации электронов, останавливая процесс коррозии. Это явление называется поляризацией 6 .
Хотя электрохимическая коррозия относится к механизму коррозии, она может проявляться во многих формах. Наиболее распространены гальваническая, точечная и щелевая коррозия.
Гальваническая коррозия
Гальваническая коррозия возникает, когда два разных металла погружаются в раствор и соединяются металлическим путем. Примером может служить железный корабль с алюминиевыми винтами. Электролит — это море, а металлическая дорожка — это настоящая конструкция корабля. Анод и катод определяются из гальванического ряда. В таблице 1 показана упрощенная гальваническая серия.
В таблице 1 показана упрощенная гальваническая серия.
Из таблицы 1 видно, что на железном корабле алюминиевые гребные винты будут наиболее активным металлом или анодом и, следовательно, будут подвергаться коррозии. Следует отметить, что чем дальше друг от друга находятся два металла в гальваническом ряду, тем выше будет скорость коррозии.
В этом конкретном случае также стоит обратить внимание на размер анода и размер катода. Чем больше катод, тем больше электронов он может принять от анода, заставляя его ионизироваться с большей скоростью, что приводит к гораздо более быстрой коррозии. Эта зависимость между ними является линейной, чем больше разница в размерах между катодом и анодом, тем быстрее будет корродировать анод. Это применимо только в том случае, если катод больше анода. Если анод больше катода, скорость коррозии замедляется. Следовательно, отношение теперь обратное.
Точечная коррозия
Точечная коррозия – это форма коррозии, которая часто связана с соотношением размеров между анодом и катодом, описанным выше. Наиболее распространенной причиной питтинга является неоднородность металлов. Иногда металлы непостоянны по своему содержанию, в них могут входить горшечные металлы или другие крупинки легкокорродирующих металлов. Если в металле есть включения такого рода, которые являются более анодными, чем остальной металл, эти примеси корродируют быстрее и вызывают язвы. Обратное также возможно, примеси могут быть катодными по отношению к остальной части металла, это вызовет ямки в окружающей примеси области.
Наиболее распространенной причиной питтинга является неоднородность металлов. Иногда металлы непостоянны по своему содержанию, в них могут входить горшечные металлы или другие крупинки легкокорродирующих металлов. Если в металле есть включения такого рода, которые являются более анодными, чем остальной металл, эти примеси корродируют быстрее и вызывают язвы. Обратное также возможно, примеси могут быть катодными по отношению к остальной части металла, это вызовет ямки в окружающей примеси области.
Неоднородность — не единственная причина точечной коррозии. Защитные покрытия могут сломаться и обнажить часть подложки, которую они должны были защищать. Это приводит к тому, что остальная часть металла с покрытием действует как катод, а небольшая несплошность становится анодом. В соответствии с соотношением размеров между анодом и катодом скорость коррозии на этом маленьком аноде будет высокой, что приведет к образованию язв.
Щелевая коррозия
Это особая форма коррозии, которая возникает в очень маленьких трещинах на металлах. Щелевая коррозия — очень интересная форма, потому что в какой-то момент она включает один из двух основных механизмов: электрохимический и химический. Щелевая коррозия часто локализуется в местах застоя электролита. К таким местам часто относятся соединения внахлест, под прокладками и под изоляцией. В этих местах щелевая коррозия обычно начинается как электрохимическая коррозия с попаданием в щель электролита. Из-за небольшого размера щели кислород, необходимый для поддержания электрохимической коррозии, вскоре истощается, и электролит становится кислым. Это происходит за счет гидролиза ионов металлов, вызванного электрохимической коррозией 9.0105 7 . В этот момент тип или механизм коррозии представляет собой химическую атаку.
Щелевая коррозия — очень интересная форма, потому что в какой-то момент она включает один из двух основных механизмов: электрохимический и химический. Щелевая коррозия часто локализуется в местах застоя электролита. К таким местам часто относятся соединения внахлест, под прокладками и под изоляцией. В этих местах щелевая коррозия обычно начинается как электрохимическая коррозия с попаданием в щель электролита. Из-за небольшого размера щели кислород, необходимый для поддержания электрохимической коррозии, вскоре истощается, и электролит становится кислым. Это происходит за счет гидролиза ионов металлов, вызванного электрохимической коррозией 9.0105 7 . В этот момент тип или механизм коррозии представляет собой химическую атаку.
Хотя создание коррозионной ячейки может показаться трудным процессом, это происходит легче, чем можно было подумать. Электрохимическая коррозия может произойти везде, она может взаимодействовать не с одним металлом, а также проникать внутрь бетона и разъедать арматурные стержни. Вся наша инфраструктура подвержена коррозии. Многие другие формы коррозии можно наблюдать в промышленных условиях, однако, как уже объяснялось, все эти формы восходят к электрохимическим. Эти другие формы могут включать нитевидную, атмосферную и прокатную коррозию.
Вся наша инфраструктура подвержена коррозии. Многие другие формы коррозии можно наблюдать в промышленных условиях, однако, как уже объяснялось, все эти формы восходят к электрохимическим. Эти другие формы могут включать нитевидную, атмосферную и прокатную коррозию.
Электрохимическая коррозия является наиболее распространенным механизмом в современной промышленности, и ее последствия можно измерить с точки зрения экономики, здоровья, безопасности и даже культуры. Этот механизм коррозии может существовать внутри наших тел, в кардиостимуляторах, он может привести к падению мостов, разрыву газопроводов и даже к ржавчине культурных сооружений, таких как статуя Свободы, если о них не заботиться должным образом. Электрохимическая коррозия — это сила, с которой необходимо считаться в современном мире, и ее необходимо решать как таковую. В следующем выпуске мы рассмотрим механизм химического окисления и его наиболее распространенные формы.
См. также Коррозия: химическое окисление
1 VanDelinder, L. S. изд. Основы коррозии — введение, глава 1, объем и язык коррозии. Национальная ассоциация инженеров по коррозии, стр. 14, 1984
S. изд. Основы коррозии — введение, глава 1, объем и язык коррозии. Национальная ассоциация инженеров по коррозии, стр. 14, 1984
2 Фроммер, Фредерик и Лоуи, Джоан. «Дефекты конструкции моста могут быть не такими редкими, как предполагалось» USA Today. 25 декабря 2010 г.
3 Кристофф, Сьюзан. «Усталостный отказ самолета Aloha Flight 243: как циклическая нагрузка и коррозия вызвали отказ во время полета», Suite 101. 27 декабря 2010 г.
4 Томпсон, Нил. «Стоимость коррозии: в США 276 миллиардов долларов в год». Стоимость коррозии. 28 декабря 2010 г.
5 Томпсон, Нил. «Стоимость коррозии: в США 276 миллиардов долларов в год». Стоимость коррозии. 28 декабря 2010 г.
6 Мангер, Чарльз. Предотвращение коррозии с помощью защитных покрытий, Глава 1, Коррозионная ячейка. Национальная ассоциация инженеров по коррозии, стр. 21, 1984
7 Томпсон, Нил. «Хронология расщелины». Коррозия-Доктора.
