Питтинг коррозия: Питтинг – суть процесса, методы борьбы с питтинговой коррозией стали
Содержание
Питтинговая коррозия — что это? Распространение, особенности и методы защиты
Виды коррозии достаточно обширны и разнообразны, у каждого свои причины и последствия. Одним из распространенных проявлений коррозии является питтинговая коррозия или, как ее еще называют, точечная коррозия.
Коррозийному разрушению подвергаются практически все металлы, какие-то более восприимчивы, а какие-то нет. Сегодня в мире существуют технологии, которые помогают замедлить процессы разрушения, происходящие с элементами, но не избавить от них полностью.
Питтинговая коррозия – это непредсказуемый и наиболее опасный вид процессов коррозийного разрушения.
Особенности питтинговой коррозии
Внешнее проявление точечной коррозии – это точечные язвы буро-рыжего цвета.
Отличительными чертами данного вида разрушения является то, что она возникает и распространяется в верхних слоях элемента, поражает участки ранее полученных дефектов, также питтинг обычно распространяется в слоях верхнего антикоррозийного покрытия.
Точечной коррозии металла подвергаются в большей степени пассивные металлы, к которым относится: медь, сурьма, ртуть, платина, также часто питтинг наблюдается на алюминии, никеле, цинке. Поэтому все изделия из данных материалов подвержены такому виду разрушения (микросхемы, агрегаты, сплавы этих металлов и др.).
Факторы, влияющие на образование питтинга на поверхности металлических материалов:
- Перепады температур или постоянное действие повышенных температур.
- Плохо обработанная поверхность (шероховатости, потертости, рыхлости и т.д.).
- Действие кислотных сред.
- Действие веществ с примесями соли.
Классификация точечных повреждений
По размеру бывают:
- Микропиттинги величиной до 0,1 мм;
- Обычные размером до 1 мм;
- Язвенный питтинг имеет размеры более 1 мм.
Также различают открытые, закрытые и поверхностные точечные язвы.
В открытом виде ржавые пятна хорошо просматриваются на поверхности материала, достаточно человеческого зрения. Если язвенных образований слишком много, то в процессе своего распространения они сливаются в одну сплошную диффузную составляющую. Закрытый вид питтинга самый опасный, так как его невозможно рассмотреть с внешней стороны, так как они увеличиваются не наружу, а вглубь материала изделия. Такие язвы могут быть найдены только с использование специальных просвечивающих приборов.
Если язвенных образований слишком много, то в процессе своего распространения они сливаются в одну сплошную диффузную составляющую. Закрытый вид питтинга самый опасный, так как его невозможно рассмотреть с внешней стороны, так как они увеличиваются не наружу, а вглубь материала изделия. Такие язвы могут быть найдены только с использование специальных просвечивающих приборов.
Поверхностный питтинг встречается наиболее редко, разрушение происходит не вглубь или наружу элемента, а вширь, что способствует образованию не просто точек, а выбоин на поверхности элемента.
Питтинговая коррозия — причины образования
Интенсивное образование ржавчины происходит при контакте металлического изделия с солеными растворами и различными химически агрессивными средами.
Нужно понимать, что питтинговая коррозия это точечные язвы там, где происходило нарушение технологий производства, механические повреждения, приводящие к микроскопическим дефектам. Если сплав был произведен с нарушением технологии, то в нем могут быть инородные включения, поры, которые нарушают работу изделия.
Если сплав был произведен с нарушением технологии, то в нем могут быть инородные включения, поры, которые нарушают работу изделия.
Важной причиной появления питтингов можно назвать среду, в которой эксплуатируется материал. При частых динамических воздействиях, нарушается структурная целостность зерен металла, что приводит, к внутренним разрушениям и распространению коррозийных процессов.
Проявление точечных язв
Чтобы более полно понимать, что такое питтинговая коррозия, необходимо разобрать процесс ее появления и развития:
- Начальная стадия или зарождение – отмечалось выше, что питтинги образуются в местах ранее полученных дефектов в виде трещин, сколов, рыхлостей от удара и т.п. Также на поверхности металла существует естественная защитная пленка, от воздействия факторов окружающей среды, она может истончаться или пропадать вовсе, что содействует более быстрому процессу разрушения.
- Процесс роста – рост происходит вследствие электрохимических реакций и полного растворения защитной оксидной пленки.

- С момента зарождения коррозия в определенном месте развивается очень быстро, но со временем ее распространение замедляется и все больше углубляется внутрь материала элемента для полного разрушения металлической решетки.
Имеются случаи, когда питтинг не развивается, а наоборот происходит его замедление – процесс репассивации. Но это может произойти только на ранних этапах развития ржавчины.
Формы питтингового повреждения
Если рассматривать питтинг более тщательно, то можно обратить внимание, что одни точки имеют правильную округлую форму, другие могут быть: многогранниками, объединенными многогранниками, пирамидальные, призматические. В некоторых многогранников наблюдается блестящее дно язвы.
Форма питинговой коррозии металлов будет напрямую зависеть от формы частиц кристаллической решетки, так как продукты разрушения повреждают именно кристаллическую решетку материала, и образуются пустоты.
По форме точечных язв на изделии, можно понять, из какого именно металла оно сделано.
Методы защиты металлов и сплавов от коррозии
Защита металлов и сплавов от питтинговой коррозии:
- Электрохимическая защита. Этот вид защиты часто применяется вместе с применением ингибиторов.
- Так как наиболее подвержены питтинговым образованиям пассивные сплавы, то наилучшим решением будет минимизировать их величину в составе сплавов или совсем заменить на другой, более устойчивый к разрушению материал.
Существуют вещества, введение которых в сплав, повышает его антикоррозийную стойкость (например, кремний и хром).
- Применение ингибиторов, которые в замкнутой системе подавляют или задерживают развитие разрушающих процессов, вследствие химических и физико-химических воздействий (вещества на сульфатной основе, щелочи, нитраты).
- Нанесения защитного антикоррозийного покрытия на предварительно очищенную и подготовленную поверхность элемента.

Важно понимать, что представленные методы борьбы с точечной коррозией металла возможны только на производстве или на начальном этапе создания сплава для конструкции или детали.
Таким образом, наличие питтингов не ставит крест на работоспособности конструкции, если они были замечены вовремя. Стоит всегда тщательно следить за состоянием изделий, включенных в работ, во время проводить технические обследования и не скупиться на качественную антикоррозийную защиту для металлов.
Питтинг покрытия и его опасности
Питтинговая точечная коррозия: что это и какую опасность в себе несет
Люди часто заявляют, что каждый металл можно защитить при помощи особого оксидного покрытия, которое будет затруднить появление коррозии.
Но есть и особый вид ржавчины, которая называется питтинговой коррозией, которая затрагивает металлы с защитными покрытиями. В большинстве случаев такая коррозия будет затрагивать лишь верхний оксидный металлический слой, а вглубь будет проникать достаточно медленно.
Но как же появляется такая ржавчина? Правда ли то, что есть коррозия нержавеющей стали? Далее вы найдете ответы на все вопросы.
Содержание:
- 1 Что такое питтинг
- 2 Подробности
- 2.1 Причины появления
- 2.2 Этапы появления точечной коррозии
- 2.3 Классификация
- 2.4 Защита объектов из металла
- 3 Заключение
Что такое питтинг
Итак, питтинг является разновидностью коррозии, при которой на металлической поверхности будут появляться так называемые питтинги. Такая коррозия будет затрагивать медные, железные, алюминиевые сплавы, а также те, что на основе хрома и прочие. Коррозия питтингового типа возможна даже на нержавейке.
Питтинг обычно будет затрагивать разные металлические конструкции, которые будут контактировать с соленой водой (как правило, это разные участки около берега). Это связано с тем, что для вступления в силу реакции требуется избыток ионов-активаторов, которые станут вытеснять кислород из защитной оксидной пленки – а такие вещества в большом количестве выделяются именно в воде. Также обращайте внимание, что вначале питтинг обычно начинает затрагивать верхние слои оксидной пленки, но из-за усиливающегося распространения ржавчины он может начать захватывать металл полностью. Такая коррозия появляется обычно при комбинации сразу двух факторов.
Также обращайте внимание, что вначале питтинг обычно начинает затрагивать верхние слои оксидной пленки, но из-за усиливающегося распространения ржавчины он может начать захватывать металл полностью. Такая коррозия появляется обычно при комбинации сразу двух факторов.
Подробности
Причины появления
Предлагаем рассмотреть основные причины питтинговой точечной коррозии.
- Деформация механического характера
Это может быть царапина, вмятина, растрескивание в области удара, а также другое. Этот фактор будет ключевым, потому что на большинстве металлических сплавов на поверхность есть весьма тонкий, но все-таки слой защиты, который способствует предотвращению коррозии.
Естественно, что при повреждении такого слоя металл будет становиться незащищенным перед ржавчиной.
- Структурная неоднородность
Такой фактор тоже является крайне важным, потому что неоднородности часто будут создавать небольшие по размеру очаги, где спустя время начнет появляться ржавчина. Неопытные инженеры могут подумать, что такой фактор будет опасным лишь для металла и стали низкого качества, но это вовсе не так. Действительно, сплавы низкого качества будут иметь неоднородную структуру и ржавеют намного чаще, но еще структурная неоднородность может появиться и у деталей, которые обработаны, на которые забыли нанести покрытие с защитой. Простой пример – во время сверления отверстия будет нарушена целостность внешней пленки против коррозии – это будет привлекать внимание к появлению повреждений.
- Высокая степень шероховатости
Если поверхность объекта из металла является весьма шероховатой, то в подобном случае на ней вряд ли будет удерживаться особое антикоррозийное покрытие. По этой причине появление на подобной поверхности коррозии, но это лишь вопрос времени. Еще обращайте внимание на то, что тут будет действовать одно правило – чем больше шероховатость поверхности металла, тем скорее она станет покрываться коррозией. Гладкий однородный металл будет обладать прекрасной устойчивостью к ржавчине.
По этой причине появление на подобной поверхности коррозии, но это лишь вопрос времени. Еще обращайте внимание на то, что тут будет действовать одно правило – чем больше шероховатость поверхности металла, тем скорее она станет покрываться коррозией. Гладкий однородный металл будет обладать прекрасной устойчивостью к ржавчине.
- Агрессивная среда
Не поверите, но может случиться даже точечная коррозия нержавеющей стали, если будет контакт с агрессивными средами (кислоты, воды с огромным содержанием солей, щелочей и прочего). Агрессивные среды тоже могут повредить внешний антикоррозийный слой, а это спустя время может привести к появлению питтинга. Также обратите внимание, что различные вещества будут влиять на металл разными способами – если морская вода при не долгосрочном контакте не будет наносить какие-либо повреждения, а вот при контакте с сильными кислотами могут появиться сильные повреждения. По этой причине следует соблюдать правила хранения и обработку металла.
Этапы появления точечной коррозии
Основной опасностью такой коррозии будет быстрое распространение. Все дело заключается в том, что по мере появления ржавчины будет разрушаться защитный внешний слой, и поэтому такую коррозию не удастся локализовать на определенном участке. Даже самые малые по размеру фрагменты растут и увеличиваются в размере, а при отсутствии своевременной обработки коррозия очень быстро станет целиком захватывать металл, что сделает его бесполезным и в какой-то мере опасным (к примеру, когда идет речь о навесной конструкции из металла).
Такая коррозия по металлу станет распространяться в несколько этапов:
- Точечная ржавчина начинает появляться в местах, где повреждено антикоррозийное покрытие (трещины, царапины, вмятины и прочее), а еще при неоднородной металлической структуре. Еще одной локализацией будет обработанный металл, на который по каким-то причинам не успели нанести защитное покрытие.
- На химическом уровне это будет происходить так – ионы-активаторы под воздействием электрохимической силы станут вытеснять кислород из оксидной пленки, которой покрыт лист металла или изделие.
 Это приведет к постепенному разрушению внешнего покрытия металла с появлением характерных язв и пятен рыжевато-коричневого цвета.
Это приведет к постепенному разрушению внешнего покрытия металла с появлением характерных язв и пятен рыжевато-коричневого цвета. - По мере того, как будет разрушаться оксидная пленка, ржавчина станет захватывать новые участки поверхности объекта из металла, то это может привести к ухудшению свойств физического характера (теряется твердость/плотность/прочность и прочее). Реакция окисления будет идти по электрохимическому сценарию благодаря вытеснению кислорода из пленки оксида.
- После всецелого уничтожения оксидной пленки питтинг начнет проникать внутрь металлического сплава – и тогда наступит диффузный этап. Скорость протекания такого процесса будет достаточно низкой, а полное ржавление может занимать огромное количество времени.
Стоит обратить внимание на то, что иногда будет происходить пассивация металла самопроизвольного типа, что приведет к замедлению появления ржавчины. На практике такой сценарий встречается весьма редко, хотя подобные случаи можно встретить на практике. Стоит обратить внимание на то, что в случае перехода точечной коррозии на диффузный этап пассивация не будет возможна по физическим причинам.
Стоит обратить внимание на то, что в случае перехода точечной коррозии на диффузный этап пассивация не будет возможна по физическим причинам.
Классификация
Есть несколько видов питтинга:
- Поверхностный. При подобном сценарии ржавчина начнет затрагивать исключительно верхнюю металлическую поверхность. Еще она будет распространяться в виде небольших и тоненьких линий с диаметром от 0.1 до 0.3 см. Поверхностная ржавчина на первоначальном этапе обычно будет захватывать углы, но спустя время она начнет распространяться в горизонтальном направлении по всей поверхности элемента из металла.
- Открытый. При подобном сценарии коррозии начнет появляться в виде частых больших точек, причем их диаметр будет составлять от 0.2 до 0.5 см. На поверхности сперва будут появляться несколько точек, которые размещено далеко друг от друга. Спустя время количество точек будет прямопропорционально расти, и они станут захватывать всю поверхность объекта из металла.

- Закрытый. При подобном сценарии питтинг будет захватывать сначала внутреннюю поверхность пленки из металла, а также распространение коррозии обычно идет виде недлинных линий или больших окружностей со средним диаметром (от 0.5 до 1.5 см). Такой сценарий будет встречаться крайне редко, и является самым опасным, а также губительным в связи со сложностью своевременного обнаружения. Подобная коррозия будет проявляться лишь на позднем этапе роста коррозии, когда металл спасти невозможно.
А теперь немного о том, как защитить объекты.
Защита объектов из металла
Главным методом защиты нержавейки и металла от коррозии питтингового типа будет пассивация. Для обработки обычно применяют особый раствор на основании лимонной и азотной кислоты. При необходимости кислотный раствор может усиливаться разными вспомогательными добавками. Определенные инженеры добавляют в раствор калия ферроцианид при концентрации 2.5%. Целью пассивации будет замедление коррозии до полного прекращения появления новой ржавчины.
Такой кислотный раствор будет играть роль новой защитной пленки, которая будет образовываться на поверхности во время процесса.
Кроме этого можно использовать и другие вспомогательные защитные меры:
- Заделка дефектов и трещин. Одной из основных причин появления коррозии будет нарушение целостности оксидной пленки из-за внешних дефектов. Если такие повреждения заделать вовремя, то ржавчина не успеет появиться.
- Удаление шероховатостей и неровностей. Ржавчина крайне часто появляется на неровной поверхности, а зачистка поверхности металла будет надежно защищать элемент.
- Нанесение хромированного покрытия. Определенные виды стали можно защитить при помощи нанесения дополнительного покрытия на хромовой основе, а еще такой элемент будет препятствовать появлению ржавчины.
Надеемся, теперь вам станет проще защищать металлические элементы.
Заключение
Питтинг – это особая форма ржавчины, которая способа захватывать оксидный защитный слой металла.
В большинстве случаев ржавчины будет распространяться в виде длинных полос и небольших по размеру точек. На позднем этапе могут появляться большие неровные пятна и длинные язвы-полосы.
Главными причинами появления питтинга станут механические дефекты, повреждения химического типа, наличие неровностей и прочее. В зависимости от типа ржавчины будут отличать несколько видов питтинга – закрытый, открытый и поверхностный. Основным способом защиты металла будет пассивация, а еще своевременная обработка локальных дефектов.
О новейших методах изучения процессов питтинговой коррозии
Библиографическое описание:
Замалетдинов, И. И. О новейших методах изучения процессов питтинговой коррозии / И. И. Замалетдинов, Е. А. Колобова. — Текст : непосредственный // Техника. Технологии. Инженерия. — 2017. — № 1 (3). — С. 36-45. — URL: https://moluch.ru/th/8/archive/46/1655/ (дата обращения: 02.10.2022).
И. О новейших методах изучения процессов питтинговой коррозии / И. И. Замалетдинов, Е. А. Колобова. — Текст : непосредственный // Техника. Технологии. Инженерия. — 2017. — № 1 (3). — С. 36-45. — URL: https://moluch.ru/th/8/archive/46/1655/ (дата обращения: 02.10.2022).
There are summarizes of current methods for studying pitting (PC), including a method of using neural networks, 3D method for studying the morphology during the growth of pitting, finite element method, ellipsometry method, and others. Get useful information to deepen our understanding of the mechanism and kinetics of growth of pitting corrosion.
Keywords: Pitting corrosion, neural networks, velocity of pitting’s growth
Питтинговая коррозия является опасным видом локального поражения металлов и сплавов, которая, помимо перфорации стенок оболочкового оборудования химических производств, может инициировать процессы коррозионного растрескивания и коррозионной усталости. Поэтому интерес к изучению ПК возрастает в связи с развитием металловедения, с необходимостью создания устойчивых к локальным видам коррозии металлов и сплавов. Прежде чем перейти к новейшим исследованиям в области ПК вкратце охарактеризуем условия возникновения ПК и теоретические представления о ПК, которые базируются на работах научных школ Я. М. Колотыркина [1], И. Л. Розенфельда [2], Н. Д. Томашова [3] и др.
Поэтому интерес к изучению ПК возрастает в связи с развитием металловедения, с необходимостью создания устойчивых к локальным видам коррозии металлов и сплавов. Прежде чем перейти к новейшим исследованиям в области ПК вкратце охарактеризуем условия возникновения ПК и теоретические представления о ПК, которые базируются на работах научных школ Я. М. Колотыркина [1], И. Л. Розенфельда [2], Н. Д. Томашова [3] и др.
Питтинговая коррозия характерна для пассивирующихся металлов в средах, содержащих в первую очередь галиды (Cl—, Br—, I—) металлов. При достижении критического потенциала питтингообразования на активных центрах поверхности металла адсорбируются агрессивные анионы и при достижении критической концентрации Скр вызывают растворение в виде соли. Схематически процесс можно представить в виде следующих последовательных стадий [4]:
Пассивацию металла вызывают молекулы воды, которые к атому металла обращены кислородным концом. Ионы хлора вытесняют молекулы воды с поверхности и образуют с металлом интермедиаты (комплексы), переходящие в раствор. Далее следует быстрая стадия гидролиза с высвобождением хлор-ионов, вступающих в новое поверхностное взаимодействие с атомами металла. Таким образом формируется циклический или автокаталитический путь реакции питтингообразования [4].
Ионы хлора вытесняют молекулы воды с поверхности и образуют с металлом интермедиаты (комплексы), переходящие в раствор. Далее следует быстрая стадия гидролиза с высвобождением хлор-ионов, вступающих в новое поверхностное взаимодействие с атомами металла. Таким образом формируется циклический или автокаталитический путь реакции питтингообразования [4].
В работе [5] изучали ПК на аэрокосмических сплавах (Al-5,6 Zn-2,5 Mg-1,6 Cu) путем использования искусственных нейронных сетей для моделирования процесса. При этом были использованы оптическая профилометрия и функции Вейбулла для характеристики распределения по глубинам и диаметрам питтингов. Авторы использовали временные эмпирические зависимости скорости роста питтингов, полученные ранее исследователями [6,7]:
,(1)
где t — время, d — глубина или диаметр питтинга, К и b — константы, где b принимает значения от 0,3 до 0,5 [6]. Далее применили трехпараметровую Вейбуловскую функцию распределения для определения популяции питтингов по глубине и диаметру:
(2)
где d — глубина питтинга или эквивалентный ей диаметр, α— Вейбуловский параметр формы питтинга, β — параметр масштаба. γ — параметр сдвига (локализации). Методом практической профилометрии установлено, что параметром сдвига можно пренебречь, поэтому выражение (2) авторы [5] упростили:
γ — параметр сдвига (локализации). Методом практической профилометрии установлено, что параметром сдвига можно пренебречь, поэтому выражение (2) авторы [5] упростили:
,(3)
где параметры уравнения такие же, что и в уравнении (2). Вейбуловские параметры глубины и диаметра (обозначенные как αгл, βгл, αдиам, βдиам) были использованы в создании искусственных нейронных сети (ИНС). Входами во все НС были показатели температуры, рН, [Cl—], время экспозиции, в то время как выходами были максимальная глубина питтингов, максимальный диаметр питтинга, αгл, βгл, αдиам, βдиам. Каждый параметр, (т. е. температура, глубина питтинга и т. д.) был нормализован между значениями 0 и 1 перед подачей в ИНС. Поскольку температура и величина рН равномерно распределены по их весам, они были нормализованы в соответствии с линейными правилами. Например, температура была нормализована в соответствии с уравнением
Например, температура была нормализована в соответствии с уравнением
,(4)
где Тнорм— нормализованная температура, Ti — температура i -ого опыта, Tmin,, Tmax— минимальная и максимальная температура соответственно. Аналогичной нормализации была подвергнута величина рН, а концентрация хлорида, время, глубина и диаметр питтинга были нормализованы по логарифмической зависимости:
.(5)
Нейроносетевое моделирование проводилось с помощью программного обеспечения JMP8. Программное обеспечение позволило выбрать определенный процент данных вначале для тренинга ИНС (67 % было использовано для определения βгл и 90 % для остальных).
Рис. 1. Нейроносетевая структура для всех конечных параметров (вид параметра, α; параметр шкалы, β; максимальная глубина питтинга или диаметр dmax. Число нод (Нn) в промежуточном слое варьируется для каждого параметра. Входные параметры: температура, рН, концентрация Cl—, время, ориентация (продольная и поперечная) зерен после прокатки, смещение. Выходные параметры α, β или dмакс.
Входные параметры: температура, рН, концентрация Cl—, время, ориентация (продольная и поперечная) зерен после прокатки, смещение. Выходные параметры α, β или dмакс.
3D — изображение [5], полученное оптической профилометрией представлено на рис. 2.
Рис. 2. Слева: Очерченные круговые контуры групп питтингов для съемки на оптическом профилометре сплава алюминия АА 7075 (время испытаний 720 часов при температуре 60оС в растворе 0,6 М хлорида, рН = 6. Справа: 3D изображение образца после испытания
Каждый питтинг был зафиксирован программой в виде круга, пронумерован, расположение и размеры глубин и диаметров были записаны.
В табл. 1 приведено определенное пользователем число узлов (в скрытом слое), использованное для каждой ИНС.
В циклических условиях возникают напряжения, вызывающие рост трещин из глубоких питтингов. Поэтому измеренная действительная максимальная глубина питтингов была сопоставлена с результатами расчета ИНС. Результаты представлены на рис. 3.
Результаты представлены на рис. 3.
Таблица 1
Число нод искусственной нейронной сети при употреблении входящих параметров
Параметр | Число нод |
αглубина питтинга | 10 |
βглубина питтинга | 10 |
αдиаметр питтинга | 10 |
βдиаметр питтинга | 9 |
Максимальная глубина | 11 |
Максимальный диаметр | 12 |
Видно, что данные обучения/проверки ИНС со средним квадратичным отклонением R2 = 0,71 хорошо согласуются с результатами опытов со средним квадратичным отклонением R2 = 0,90. При анализе результатов использования ИНС было установлено, что на максимальную глубину питтингов оказывало влияние время испытаний, температура и рН раствора, а концентрация хлорида и ориентация тонкой структуры после прокатки сплава не оказывало существенного влияния. Незначительное влияние концентрации хлорида объяснено достаточным количеством хлорида для роста питтингов, влияние хлорида возможно возникнет в опытах при более низких концентрациях.
При анализе результатов использования ИНС было установлено, что на максимальную глубину питтингов оказывало влияние время испытаний, температура и рН раствора, а концентрация хлорида и ориентация тонкой структуры после прокатки сплава не оказывало существенного влияния. Незначительное влияние концентрации хлорида объяснено достаточным количеством хлорида для роста питтингов, влияние хлорида возможно возникнет в опытах при более низких концентрациях.
Рис. 3. Действительные максимальные глубины питтингов и рассчитанные ИНС максимальные глубины ложатся на одну прямую [5]
Временные уравнения роста питтингов были получены обученной ИНС: кинетика t1/4 была характерна для щелочных сред и для повышенных температур, а кинетика t1/2 была свойственна для кислых сред и для пониженных температур, однако для многих промежуточных значений рН и температур кинетика была t1/3. Показатель степени от 0,3 до 0,5 для большинства сред соответствовал литературным данным [6,7]. Кроме того, выявленные закономерности кинетики роста питтингов в литературе и результаты предсказаний нейронной сети по величинам степени b делают ей доверие, несмотря на интерполяционный ее характер.
Кроме того, выявленные закономерности кинетики роста питтингов в литературе и результаты предсказаний нейронной сети по величинам степени b делают ей доверие, несмотря на интерполяционный ее характер.
В работе [8] проводились анализы электрохимического шума с использованием временной и частотной зависимостей и статистических параметров потенциала и значений тока, полученные на нержавеющей стали AISI 316 в процессе питтинговой коррозии в деаэрированном 0,5 М растворе NaCl и в процессе коррозионного растрескивания под напряжением в кипящем подкисленном растворе NaCl. Визуальные наблюдения и статистические анализы значений спектрального оценивания тока и потенциала, использующего метод максимальной энтропии, дали полезную информацию на установление различия между этими коррозионными процессами и на влияние напряжения на усиление питтинговой коррозии. Результаты хорошо согласовывались с оптическими микроскопическими наблюдениями.
Исследователи [9] изучали трехмерную питтинговую коррозию, инициированную на включениях MnS стали А537 при циклических нагрузках. При этом использовали софокусный сканирующий лазерный микроскоп с элементным анализом. Ими установлено, что при циклических механических нагрузках питтинги растут анизотропно, т. е. скорости растворения стенок питтинга и дна различаются. Существенно более высокая скорость роста была обнаружена в перпендикулярном направлении оси нагрузок. Конечный элементный анализ указывает на то, что локальная продольная нагрузка играет важную роль на рост питтинга. Кинетика роста питтинга вширь доминировала в продольном направлении. Слияние питтингов в дальнейшем увеличивает скорость роста питтингов, как и предсказывалось методом конечного анализа.
При этом использовали софокусный сканирующий лазерный микроскоп с элементным анализом. Ими установлено, что при циклических механических нагрузках питтинги растут анизотропно, т. е. скорости растворения стенок питтинга и дна различаются. Существенно более высокая скорость роста была обнаружена в перпендикулярном направлении оси нагрузок. Конечный элементный анализ указывает на то, что локальная продольная нагрузка играет важную роль на рост питтинга. Кинетика роста питтинга вширь доминировала в продольном направлении. Слияние питтингов в дальнейшем увеличивает скорость роста питтингов, как и предсказывалось методом конечного анализа.
Объектом исследования [9] служила горячекатаная плита из стали А537, которая используется для изготовления нефтяной платформы. Химический состав стали, масс. %: 0,13 С; 1,48 Mn; 0,46 Si; 0,012 P; 0,005 S; 0,04 Cr; 0,19 Ni; 0,05 V; 0,17 Cu; 0,016 Mo, остальное железо. Матрица стали состоит из ферритно-перлитной структуры, полученной при прокатке и коротких поперечных перемещениях, включающей в большом количестве включения MnS в феррите. Статистика измерений показала, что размеры включений MnS в длину составила 27,1 ± 16,4 мкм, в ширину — 2,3 ±0,8 мкм с объемной фракцией 0,24 ± 0,11 % [9].
Статистика измерений показала, что размеры включений MnS в длину составила 27,1 ± 16,4 мкм, в ширину — 2,3 ±0,8 мкм с объемной фракцией 0,24 ± 0,11 % [9].
Испытания на растяжение проводили на универсальной испытательной машине (Shimadzu, модели AG-100KNG) при номинальной скорости деформации 4,2∙10–4 с-1 при комнатной температуре на трех прямоугольных стандартных образцах по направлению прокатки оси нагрузки. Во время испытаний на растяжение деформация записывалась тензометром. Механические свойства были следующие: предел текучести 303±3 МПа, прочность на растяжение 513±1 МПа, относительное удлинение 33±1 %, модуль Юнга (Е) 206±5 ГПа [9].
Образцы гантельной формы с калибровочными размерами длиной и шириной соответственно 15 и 6 мм, и толщиной 6 мм были использованы для тестов на усталостную коррозию. Осевая нагрузка была вдоль направления прокатки. Все образцы были отполированы сначала наждачной бумагой с зернами карбида кремния, затем алмазной пастой на полировочной машине. Коррозионные усталостные испытания проводили на установке Shimadzu, модели ENF-EAS с генератором синусоидальных колебаний с частотой 1 Гц с отношением напряжений 0 при комнатной температуре 20–25 оС. Серия усталостных испытаний проводилась при различных количествах циклов (1×104, 4×104, 7×104, 1×105, 2×105) при напряжении 140 МПа. Было установлено, что коррозионная усталость до разрушения составляла примерно 1×106 циклов. Не было коррозионных трещин в питтингах вплоть до 2×105 циклов, как установлено растровой электронной микроскопией. Поэтому это количество циклов являлось идеальным для исследования влияния циклических напряжений на рост питтингов [9]. Схема установки испытаний на коррозионную усталость представлена на рис. 4.
Коррозионные усталостные испытания проводили на установке Shimadzu, модели ENF-EAS с генератором синусоидальных колебаний с частотой 1 Гц с отношением напряжений 0 при комнатной температуре 20–25 оС. Серия усталостных испытаний проводилась при различных количествах циклов (1×104, 4×104, 7×104, 1×105, 2×105) при напряжении 140 МПа. Было установлено, что коррозионная усталость до разрушения составляла примерно 1×106 циклов. Не было коррозионных трещин в питтингах вплоть до 2×105 циклов, как установлено растровой электронной микроскопией. Поэтому это количество циклов являлось идеальным для исследования влияния циклических напряжений на рост питтингов [9]. Схема установки испытаний на коррозионную усталость представлена на рис. 4.
Из резервуара раствор 3,5 % NaCl со скоростью 20 мл/мин центробежным насосом нагнетался через нижний штуцер в сосуд с образцом, при этом жидкость контактировала с площадкой 1 см2 (остальная поверхность изолировалась силиконовым клеем) узкой части испытуемого образца. Через верхний штуцер жидкость самотеком поступала обратно в резервуар.
Через верхний штуцер жидкость самотеком поступала обратно в резервуар.
После коррозионных испытаний продукты коррозии удаляли раствором этилендиаминотетрауксусной кислотой (готовили 200 мл 1,5 % -ный раствор). Раствор не растворял матрицу и включения MnS.
Морфологию питтингов изучали в продольно-поперечном направлении конфокальным сканирующим лазерным микроскопом (OLYMPUS LEXT OLS3000). Тестировалось более 40 окрестностей вокруг включений MnS. На рис. 5 представлена картина поверхности, на которой форма питтингов была нерегулярной. Поэтому 3D — измерения (длина, ширина и глубина) обсчитывалась программным обеспечением, установленном на OLYMPUS LEXT OLS3000. В случае слияния питтингов их рассматривали как один питтинг.
Рис. 4. Схема установки для испытаний на коррозионную усталость
Установлено, что из всех направлений рост в глубину оказался наименьшим после 200 кс испытаний без циклических нагрузок. В условиях циклических нагрузок рост питтинга ускоряется как в ширину, так и в глубину, но со значительным ускорением в ширину. Имеется незначительный рост скорости в длину для циклически напряженных образцов после 100 кс. Явление, по-видимому, связано со слиянием питтингов.
Имеется незначительный рост скорости в длину для циклически напряженных образцов после 100 кс. Явление, по-видимому, связано со слиянием питтингов.
Рис. 5. (а) Поверхность до коррозионных испытаний; (б) питтинги, инициированные после испытаний в растворе 3,5 % NaCl без приложения напряжений
Рис. 5. (с) Питтинги, инициированные после циклических напряжений; (d) 3D — питтинги, снятые софокусным сканирующим микроскопом, обратная картинка с Z фактором 1,5
Кинетику роста питтинга в 3D направлении можно представить в виде уравнения [9]:
, (6)
где f(t) представляет ширину, длину и глубину питтингов, a, b, n экспериментальные константы. Константа a представляет инициативный размер питтинга, возникший на включении MnS. Результаты расчетов кинетических параметров [9] представлены в табл.2.
Таблица 2
Сравнение кинетических данных 3D размеров питтингов, полученных без циклических нагрузок ис ними.
3D размер | Амплитуда напряжений, МПа | α, мкм | b, мкм∙с—n | n | R2 |
Ширина | 0 | 3.6±2,7 | 0,20 | 0,32±0,14 | 0,981 |
140 | 7,5±0,2 | 1,3∙10–5 | 1,15±0,05 | 0,998 | |
Длина | 0 | 20,4±4,9 | 0,84 | 0,28±0,11 | 0,993 |
140 | 31±1,4 | 3,9∙10–3 | 0,72±0,10 | 0,991 | |
Глубина | 0 | 3,4±0,26 | 2,0∙10–4 | 0,76±0,23 | 0,948 |
140 | 4,3±0,8 | 1,7∙10–3 | 0. | 0,963 |
Показано, что константа “a” для ширины питтинга была больше, чем усредненный размер включения (т. е. 2,3 мкм). Это объяснено авторами [9] наличием трещины между включением MnS и матрицей (рис. 5(a)). Относительно большие различия, которые найдены для рассчитанной «оригинальной длины» подтверждают, что оригинальная длина питтингов варьируется на различных образцах.
Рассчитанная экспонента n роста питтинга в ширину увеличивалась от 0,32 до 1,15, когда была приложена циклическая нагрузка. Можно сделать сравнение данных табл. 2 и уравнения (6) скорости роста питтинга для образцов, испытанных без напряжений и с напряжением. Например, для после испытаний продолжительностью 200 кс скорости роста в ширину были 16 и 93 пм/с соответственно без нагрузки и с нагрузкой. Результаты свидетельствуют, что скорость роста в ширину может значительно ускоряться при воздействии циклических нагрузок.
В общем, циклические нагрузки усиливают скорость роста питтингов. Питтинги, инициированные на включениях MnS, продемонстрировали анизотропное поведение роста. Скорости роста питтингов в ширину и глубину после воздействия циклических нагрузок были выше, чем скорость роста в длину. Чтобы понять этот феномен рассчитывали методом анализа конечных элементов напряжения вокруг питтингов и их распределение.
Питтинги, инициированные на включениях MnS, продемонстрировали анизотропное поведение роста. Скорости роста питтингов в ширину и глубину после воздействия циклических нагрузок были выше, чем скорость роста в длину. Чтобы понять этот феномен рассчитывали методом анализа конечных элементов напряжения вокруг питтингов и их распределение.
Локальные напряжения и распределение напряжений одиночного полуэллипсоидного питтинга были промоделированы методом конечных элементов. Выбраны граничные условия, при которых движение левой стороны модели питтинга фиксировалось вдоль направления х, в то время как движения вдоль направлений y и z были свободными, как показано на рис. 6а. Одноосное растягивающее напряжение 280 МПа (нагрузка от 0 до 280 МПа колебаний с синусоидной волной) была приложена к правой стороне модели. Направление нагрузки было параллельно длинной оси полуэллипсоидного питтинга (направление х на рис. 6а). В соответствии со статистическими результатами типичные длина, ширина и глубина питтингов были 45, 15 и 7,5 мкм соответственно. 3D усредненные напряжения отдельного полуэллипсоидного питтинга показано на рис. 6.
3D усредненные напряжения отдельного полуэллипсоидного питтинга показано на рис. 6.
Авторы [10] для изучения процессов ПК сталей 304 и 904L применили метод электрохимической высокочастотной модуляции (ЭВЧМ). Метод заключается в наложении к анодному процессу ПК сигналов возмущения, состоящих из синусоидальных колебаний. Поясняющая схема приведена на рис.7. На корродирующую поверхность подается потенциал, который вырабатывает соответствующий ток (величина тока есть функция потенциала). На нижнем снимке потенциал возмущения состоит из двух синусоидальных волн, наложенных методом ЭВЧМ. В ответ будут получены дополнительные и более высокие частоты, являющиеся нелинейными из-за явлений, протекающие при питтингообразовании. Производится математический анализ токовых сигналов по соответствующим уравнениям для расчета тока коррозии тафелевых наклонов.
Рис. 6. 3D зоны напряжений вокруг единичного полуэллиптического питтинга (длиной 45 мкм, шириной 15 мкм и глубиной 7,5 мкм). Направление деформации показано стрелками. Зона концентраций согласованных напряжений направлена по оси х. Цветовая гамма с цифрами напряжений приведена слева от рисунка
Направление деформации показано стрелками. Зона концентраций согласованных напряжений направлена по оси х. Цветовая гамма с цифрами напряжений приведена слева от рисунка
Соответствующая математическая модель разрабатывалась, чтобы изучить реакцию на возмущение при потенциалах ниже и выше потенциодинамического потенциала питтингообразования. Ставилась цель быстрого нахождения области нелинейного изменения тока с потенциалом. Ток как функция потенциала может определяться по уравнению (7).
, (7)
где icorr — ток коррозии, К2 и К3— параметры, ассоциируемые с ПК, bc — катодный тафелевский наклон. Здесь Е, Еcorr, Epit — cоответствующие приложенный потенциал, потенциал коррозии и потенциал питтингообразования. Параметры К2 и К3 ассоциируются с ПК и их значения выбираются по уравнению (7) для представления стремительного роста тока с потенциалом, происходящего при инициировании питтинга.
В ЭВЧМ технике авторы [10] применяли возмущающий сигнал потенциала, состоящий из двух синусоидальных волн, как показано ниже
,(8)
где Uo — амплитуда потенциала возмущения, f1 и f2— частоты возмущения в Гц и Едс — потенциал двойного слоя. Подстановка уравнения (8) в уравнение (7) дает ток во временной области, который может быть затем преобразован в частотной области. Для определения теоретических значений факторов причин ниже потенциала питтингообразования и вблизи потенциала ПО, были выбраны параметры, приведенные в таблице 3.
Рис. 7. Верхняя часть временной домен тока как функции потенциала; нижняя часть — частотный домен
Таблица 3
Коррозионные параметры, показывающие свои соответствующие входные значения для симуляции цели
Параметр | Характеристика | Входные значения |
icor | Ток коррозии | 1 мкА |
Epit | Потенциал питтингообразования | 0,4 В |
К2 | Питтинговый параметр | 1 мкА |
К3 | Нелинейный параметр | 92 мВ-1 |
U0 | Амплитуда потенциала | 10 мВ |
bc | Катодный тафелевский наклон | 120 мВ на декаду |
Ecorr | Потенциал коррозии | 0 В |
f1 | Первая частота | 2 Гц |
f2 | Вторая частота | 5 Гц |
Edl | Потенциал двойного слоя | -0,3, -0,2…. |
Рис. 8. Поляризационная кривая. Различные нелинейные изменения тока в области роста питтингов и в пассивной области. Потенциал коррозии равен 0 В, а потенциал питтингобразования равен 0,4 В
Видно, что токовые компоненты в области питтинговой коррозии существенно выше, чем токи в пассивной области.
Принимая во внимание данные, полученные с помощью современных методов изучения питтинговой коррозии, можно сделать соответствующие выводы:
- Метод нейронносетевого моделирования позволил выяснить наиболее влиятельные на рост глубины питтингов во время циклических нагрузок входные параметры. Для изучения процесса также использовался метод оптической профилометрии
- В ходе исследования [9] установлен анизотропный характер роста питтингов при циклических механических нагрузках. В период приложения нагрузки, экспонента n роста питтингов в ширину возрастала более чем в 2 раза, что свидетельствует о воздействии циклической нагрузки на скорость роста в ширину
- При приложении одноосного растягивающего напряжения к полу-эллипсообразному питтингу, напряжения, возникающие перпендикулярно оси растяжения, превышают значение приложенной нагрузки, увеличивая скорость роста ПК в ширину и глубину
- Метод электрохимической высокочастотной модуляции позволяет отследить инициирование роста питтинга, в связи со стремительным ростом силы тока и потенциала в этот период.

Литература:
- Колотыркин Я. М. Металл и коррозия. М.: Металлургия, 1985. — 88 с.
- Розенфельд И. Л. Ингибиторы коррозии. Монография. — М.: Химия, 1977. — 352 с.: ил.
- Томашов Н. Д. Коррозия металлов с кислородной деполяризацией. Учебник: — М., Л.: Издательство АН СССР, 1947. — 250 с.
- Розенфельд И. Л. Ускоренные методы коррозионных испытаний металлов (теория и практика)/ И. Л. Розенфельд, К. А. Жигалова. М.: Металлургия, 1966. — 348с.
- Modeling the environmental dependence of pit growth using neural network approaches/ M. K. Cavanaugh, R. G. Buchheit, N. Birbilis//Corrosion Science, Vol.52 (2010), p.3070–3077.
- Pitting corrosion of aluminium/ Z. Szklarska-Smialowska// Corrosion Science, Vol. 41 (1999), p.1743–1767.
- A simplified method for estimating corrosion cavity growth rates/ G Engelhardt, M Urquidi-Macdonald, DD Macdonald// Corrosion Science,Vol.39 (1997), p.419–441.

- Assessment of stress corrosion crack initiation and propagation in AISI type 316 stainless steel by electrochemical noise technique/ T. Anita, M. G. Pujar, H. Shaikh, R. K. Dayal, H. S. Khatak// Corrosion Science, Vol.48, Issue 9, September 2006, p.2689–2710.
- Anisotropic 3D growth of corrosion pits initiated at MnS inclusions for A537 steel during corrosion fatigue/ Jin Ma, Bo Zhang, Jianqiu Wang, Guozhen Wang, En-Hou Han, Wei Ke //Corrosion Science, Vol.52 (2010), p.2867–2877.
- Evolution of current transients and morphology of metastable and stable pitting on stainless steel near the critical pitting temperature/ M. H. Moayed, R. C. Newman// Corrosion Science, Vol.48, Issue 4, April 2006, p.1004–1018.
Основные термины (генерируются автоматически): скорость роста, глубина, параметр, потенциал, ширина, LEXT, OLYMPUS, коррозионная усталость, максимальная глубина, нагрузка.
Точечная (питтинговая) коррозия
Питтинговая коррозия — один из опасных видов локального кор- розионного разрушения, характерного для условий, когда пассивное состоя- ние поверхности металла или сплава может частично нарушаться. При этом коррозии подвергаются весьма ограниченные участки металла, а вся осталь- ная поверхность находится в устойчивом пассивном состоянии, что приво- дит к появлению точечных язв или глубоких питтингов. Обычно такой кор- розии подвергаются легкопассивирующиеся металлы и сплавы: хромистые и хромоникелевые стали, алюминий и его сплавы, никель, титан и др.
При этом коррозии подвергаются весьма ограниченные участки металла, а вся осталь- ная поверхность находится в устойчивом пассивном состоянии, что приво- дит к появлению точечных язв или глубоких питтингов. Обычно такой кор- розии подвергаются легкопассивирующиеся металлы и сплавы: хромистые и хромоникелевые стали, алюминий и его сплавы, никель, титан и др.
Питтинговая коррозия возникает в растворах, содержащих окислители (например кислород) и одновременно активирующие анионы (Cl-, Br-, I-), например, в растворах хлорного железа, в морской воде, в смесях азотной и соляной кислот и др.
Основное условие образования питтинга — смещение электро- химического потенциала, за счет наличия окислителей в растворе, положи- тельнее некоторого критического значения, так называемого потенциала питтингообразования, при этом поверхность питтинга является анодом и разрушается с высокой скоростью вследствие контакта с остальной поверх- ностью, находящейся в пассивном состоянии и представляющей собой, благодаря относительно большой площади, почти неполяризуемый катод.
При развитии питтинговой коррозии следует различать три стадии: возникновение, развитие питтинга и репассивация. Возникновение питтинга связано с нарушением пассивного состояния на отдельных участках по- верхности металлов и сплавов в результате воздействия анионов- активаторов. На этих участках происходит ускоренное разрушение оксидных пленок, что вызывает местное активирование. Нарушение пассивного со- стояния на отдельных участках приводит к увеличению скорости коррозии. Такими участками могут быть неметаллические включения (например сульфиды), границы зерен, участки с пониженной концентрацией хрома в твердом растворе, которые могут образовываться при термообработке, и др.
Возникновение точечной коррозии металлов и сплавов в сильной сте- пени зависит от природы анионов и их концентрации. Наиболее сильными анионами-активаторами являются Cl-, Br-. Такие анионы, как OH-, CrO42-,
|
NO3 , SO4 , ClO3 затрудняют возникновение точечной коррозии нержа- веющей стали в растворе хлорида натрия.
На возникновение точечной коррозии оказывают влияние состав спла- ва, природа металла, состояние поверхности и т. д. Например, с повышением содержания никеля и хрома сопротивление сталей точечной коррозии по- вышается.
Термическая обработка повышает склонность сталей к точечной кор- розии. Так, например, отпуск нержавеющих хромоникелевых сталей вызыва- ет склонность к межкристаллитной коррозии и понижает сопротивление ста- ли к точечной коррозии.
Рост питтинга связан с работой коррозионного гальванического эле- мента, в котором анодом является питтинг, а катодом — остальная поверх- ность металла, находящаяся в пассивном состоянии. Эффективной работе такого коррозионного элемента благоприятствует достаточное количество деполяризаторов, а также нахождение питтингов в активном состоянии, че- му способствует понижение рН раствора. Скорость коррозии в питтингах различна. В большинстве из них процесс коррозии с течением времени за- медляется, в части питтингов коррозия прекращается совсем, и лишь в не- большой части она развивается вглубь металла. Явление прекращения роста питтингов называется репассивацией.
Явление прекращения роста питтингов называется репассивацией.
Для защиты от точечной коррозии используют электрохимические ме- тоды, ингибиторы и легирование металла. Так, легирование сталей хромом, кремнием, молибденом повышает их стойкость к точечной коррозии.
Контактная коррозия
Контактной коррозией называется электрохимическая коррозия, вы- званная контактом металлов, имеющих разные стационарные потенциалы в данном электролите. При этом возникает коррозионный гальванический элемент, работа которого влияет на скорость коррозии контактирующих металлов. Работа коррозионного элемента определяется сопротивлением анодного и катодного процессов и омическим сопротивлением. С увеличени- ем разности между стационарными потенциалами катода и анода, уменьше- нием омического сопротивления и сопротивления катодного и анодного процессов контактная коррозия возрастает. Как правило, коррозия металла, имеющего более отрицательный потенциал (анод) увеличивается, а скорость
коррозии металла с более положительным потенциалом (катод) снижается по сравнению со скоростью в отсутствие контакта.
На контактную коррозию металлов большое влияние оказывают пло- щади катодов и анодов, состав среды, перемешивание нейтрального раствора и др.
С увеличением площади катода при постоянной площади анода ско- рость контактной коррозии растет. Если скорость коррозии контролируется скоростью диффузии, например диффузией кислорода при коррозии с ки- слородной деполяризацией, то с увеличением площади катода скорость кон- тактной коррозии повышается. При перемешивании нейтрального раствора растет диффузия кислорода к поверхности катода, следовательно, увеличи- вается контактная коррозия.
Контактная коррозия может проявляться и в атмосферных условиях. При этом максимальная скорость коррозии наблюдается на участках, непо- средственно прилегающих к месту контакта. По мере удаления от места контакта плотность тока коррозионного элемента падает и, следовательно, скорость контактной коррозии снижается.
Для защиты от контактной коррозии в основном применяются сле- дующие методы:
— подбор контактируемых металлов и сплавов с минимальной разни- цей потенциалов;
— изоляция металлов в местах контакта;
— введение в закрытые системы ингибиторов, снижающих коррозию контактируемых металлов.
Щелевая коррозия
Щелевой коррозией называется усиление коррозии в щелях и зазорах между металлами, прокладочными материалами и металлом, в морских ус- ловиях (между слоем микроорганизмов и обшивкой корабля). Наиболее чув- ствительны к щелевой коррозии пассивирующиеся металлы (нержавеющие стали, алюминиевые сплавы, титан и др.).
Механизм щелевой коррозии состоит в следующем. С течением време- ни из-за затруднения доступа окислителя и расходования его в процессе кор- розии в щели снижается концентрация окислителя и, тем самым, снижается скорость катодного процесса. Происходит уменьшение катодного тока, при
этом потенциал катода смещается в отрицательную сторону, что приводит к переходу поверхности металла щели в активное состояние и скорость его растворения увеличивается. Появление в растворе продуктов коррозии и их гидролиз приводят к подкислению раствора. Дальнейшее протекание корро- зионного процесса при ограниченной скорости подвода свежего электролита способствует понижению рН, что облегчает анодный процесс растворения металла и создает возможность протекания коррозии с водородной деполя- ризацией.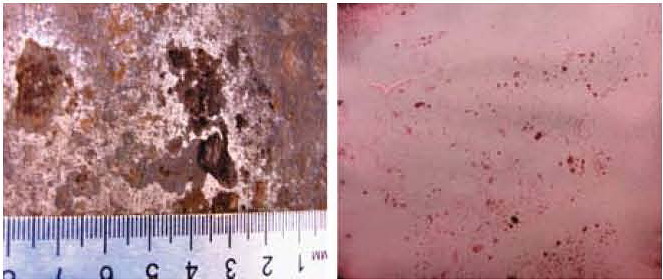 Это приводит к увеличению коррозионного тока, процесс подкис- ления раствора в щели ускоряется, и металл в щели при смещении потенциа- ла в отрицательную сторону становится анодом по отношению к металлу от- крытой поверхности. Это обычно наблюдается в практических случаях ще- левой коррозии.
Это приводит к увеличению коррозионного тока, процесс подкис- ления раствора в щели ускоряется, и металл в щели при смещении потенциа- ла в отрицательную сторону становится анодом по отношению к металлу от- крытой поверхности. Это обычно наблюдается в практических случаях ще- левой коррозии.
В зависимости от вида контроля электрохимической коррозии за- труднение доступа кислорода может вызывать увеличение или уменьшение скорости коррозии металла в зазоре. Если скорость коррозии контролируется анодным процессом, то торможение доступа кислорода вызывает увеличение скорости коррозии металла в зазоре. Если же скорость коррозии контроли- руется катодным процессом, затруднение доступа кислорода вызывает уменьшение скорости коррозии металла в зазоре.
Особенно чувствительны к щелевой коррозии металлы и сплавы, пас- сивное состояние которых связано с наличием в электролите растворенного кислорода и других пассиваторов. Затруднение доступа этих веществ в зазор приводит к снижению их концентрации ниже критического значения, в ре- зультате чего металл переходит из пассивного в активное состояние и проис- ходит щелевая коррозия.
Нержавеющие стали в условиях, когда в зазоре, вследствие зат- руднения доступа окислителя, они находятся в активном состоянии, подвер- гаются интенсивной щелевой коррозии. Снижение рН раствора до 3,5 — 4,0 способствует усилению щелевой коррозии.
ХИМИЧЕСКАЯ КОРРОЗИЯ
Многие металлические конструкции подвергаются коррозионному разрушению при воздействии на них сухих газов (воздуха, продуктов горе- ния топлива при высоких температурах и др.), а также жидких неэлектроли- тов (нефть, бензин, жидкая сера, бром и др.). В этом случае протекает гете- рогенная химическая реакция газообразной или жидкой среды с металлом, при которой окисление металла и восстановление окислительного компонен- та коррозионной среды протекают в одном акте. Это химическая коррозия.
Наиболее распространенным видом химической коррозии является га- зовая коррозия – это коррозия металлов в газах при высоких температурах. Газовая коррозия имеет место при высокотемпературной обработке металлов (ковка, штамповка, прокатка, термообработка и др. ), при эксплуатации мно- гих металлических изделий (газовые турбины, химические аппараты, двига- тели внутреннего сгорания и др.).
), при эксплуатации мно- гих металлических изделий (газовые турбины, химические аппараты, двига- тели внутреннего сгорания и др.).
Эксплуатируемые при высоких температурах металлические изделия должны сохранять высокие механические свойства: длительную прочность и сопротивление текучести (жаропрочность), а также сопротивляться коррози- онному воздействию (жаростойкость).
Газовая коррозия
Термодинамическая возможность протекания процесса газовой корро- зии может быть определена путем сопоставления упругости диссоциации ок- сида металла при данных условиях и парциального давления кислорода в га- зовой фазе.
Химическая реакция окисления металла
Me + 1/2O2 = MeO (7.1)
будет находиться в равновесии, если упругость диссоциации оксида ( PMeO ) и
парциальное давление кислорода в газовой фазе ( P ) равны. Если P > P ,
O2 O2
MeO
то будет протекать реакция окисления металла, если же
PMeO > PO , то реакция
протекает в обратном направлении, т. е. в сторону восстановления данного оксида до чистого металла и кислорода (табл. 7.1).
е. в сторону восстановления данного оксида до чистого металла и кислорода (табл. 7.1).
Таблица 7.1
|
Т, К | Упругость диссоциации оксидов, атм. | |||
| 2Cu2O =
4Cu + O2 | 2NiO =
2Ni + O2 | 2ZnO =
2Zn + O2 | 2FeO =
2Fe + O2 | |
| 0,5610-30 | 1,810-46 | 1,310-68 | - | |
| 3,710-16 | 1,710-26 | 2,410-40 | 9,110-30 | |
| 1,510-11 | 8,410-20 | 7,110-21 | 2,010-22 | |
| 2,010-8 | 2,610-15 | 1,510-21 | 1,610-13 | |
| 3,610-6 | 4,410-12 | 6,710-18 | 7,910-16 |
Данные табл. 7.1 показывают, что упругость диссоциации оксидов воз- растает с повышением температуры, т.е. сродство металла с кислородом па- дает. При Т = 2000 К медь становится неокисляемым металлом. Для осталь- ных металлов, даже при высоких температурах, протекание реакции окисле- ния термодинамически вероятно. Однако если резко снизить парциальное давление кислорода в газовой фазе, то для Fe, Zn, Ni станет термодинамиче- ски вероятным не процесс окисления, а процесс восстановления из оксидов, что и используется при выплавке металлов из руд. При этом температурная зависимость реальной скорости окисления металлов совершенно иная, чем для термодинамической вероятности процесса окисления: с повышением температуры скорость окисления металлов растет.
7.1 показывают, что упругость диссоциации оксидов воз- растает с повышением температуры, т.е. сродство металла с кислородом па- дает. При Т = 2000 К медь становится неокисляемым металлом. Для осталь- ных металлов, даже при высоких температурах, протекание реакции окисле- ния термодинамически вероятно. Однако если резко снизить парциальное давление кислорода в газовой фазе, то для Fe, Zn, Ni станет термодинамиче- ски вероятным не процесс окисления, а процесс восстановления из оксидов, что и используется при выплавке металлов из руд. При этом температурная зависимость реальной скорости окисления металлов совершенно иная, чем для термодинамической вероятности процесса окисления: с повышением температуры скорость окисления металлов растет.
При газовой коррозии происходит непосредственное взаимодействие атомов металла и кислорода с образованием пленки оксида данного металла. Молекулы кислорода, достигшие поверхности металла, адсорбируются на ней. Различают два типа адсорбции:
— физическую, осуществляемую за счет Ван-дер-Ваальсовых сил;
— химическую, или хемосорбцию, осуществляемую за счет сил хими- ческого взаимодействия.
Обычно кислород хемосорбируется на поверхности металла с высоким тепловым эффектом, близким к тепловому эффекту образования оксида. По- этому адсорбцию кислорода можно рассматривать как химическое взаимо- действие, приводящее к образованию зародышей новой фазы – оксида ме- талла. Следовательно, адсорбция кислорода является начальной стадией окисления металла.
Процесс окисления протекает следующим образом. Вначале на чистой поверхности металла происходит физическая адсорбция кислорода, которая приводит к ослаблению связей между атомами в молекуле кислорода. Моле-
кулы диссоциируют, и атомы кислорода оттягивают электроны от атомов металла. Наступает стадия химической адсорбции, когда смещение электро- нов к кислороду с образованием О2-равносильно образованию зародышей оксида. Таким образом, при взаимодействии кислорода с металлом образует- ся оксидная пленка.
Образование оксида может происходить на поверхности металла, на поверхности или внутри оксидной пленки. Первый случай имеет место, если превалирует скорость диффузии кислорода, второй – если превалирует ско- рость диффузии ионов металла. В большинстве случаев скорости диффузии ионов (или атомов) кислорода и ионов металла соизмеримы и зона роста ок- сидной пленки находится внутри.
Первый случай имеет место, если превалирует скорость диффузии кислорода, второй – если превалирует ско- рость диффузии ионов металла. В большинстве случаев скорости диффузии ионов (или атомов) кислорода и ионов металла соизмеримы и зона роста ок- сидной пленки находится внутри.
В соответствии с ионно-электронной теорией окисления Вагнера, в ок- сидной пленке протекает встречная диффузия ионов металла и кислорода. При этом поверхность металла является анодом и на ней протекает реакция ионизации атомов металла. Положительные ионы металла и освободившиеся электроны перемещаются в пленке раздельно (рис. 7.1).
Рис. 7.1 Схема процесса химического окисления металла
Электроны перемещаются со значительно большей скоростью, диффу- зия ионов металла протекает по дефектным местам кристаллической решет- ки или по ее междоузлиям. На скорость перемещения электронов и ионов оказывают влияние удельная электропроводность оксидной пленки и разме- ры ионов металла, атомов и ионов кислорода. В табл. 7.2 приведены данные по размерам атомов и ионов некоторых элементов.
В табл. 7.2 приведены данные по размерам атомов и ионов некоторых элементов.
Таблица 7.2
| Символ | Al | Al3+ | Ni | Ni2+ | Fe | Fe2+ | O | O2- |
| Диаметр, нм | 0,143 | 0,050 | 0,125 | 0,078 | 0,126 | 0,075 | 0,060 | 0,140 |
Адсорбировавшиеся из газовой фазы молекулы кислорода диссоции- руют на внешней поверхности оксида. Атомы кислорода диффундируют внутрь оксидной пленки, где, принимая электроны, превращаются в ионы О2-. Ионы кислорода продолжают диффундировать вглубь навстречу ионам металла. Таким образом, внешняя поверхность пленки, на которой кислород принимает электроны, является катодом. Следовательно, встречная диффу- зия ионов металла и кислорода протекает в электрическом поле.
Скорость газовой коррозии принято выражать через скорость роста ок- сидной пленки
Uок = dy/dtτ, (7.2)
где Uок – скорость газовой коррозии; y – толщина оксидной пленки; τt – вре- мя окисления металла.
В одних случаях пленки могут расти до заметных толщин, в других они будут чрезвычайно тонкими, порядка нескольких молекулярных слоев.
Одним из основных условий, определяющих способность образован- ного первичного слоя оксида тормозить дальнейшее окисление металла, яв- ляется сплошность получаемой пленки.
Если объем получаемого оксида Voк меньше объема металла VMe , то образуется несплошная пористая пленка, обладающая низкими защитными свойствами. Наоборот, если объём пленки больше объема окислившегося металла (Voк/VMe>1), то можно ожидать образования сплошных пленок, об- ладающих способностью защищать металл от коррозии.
В зависимости от характера образующихся пленок возможны раз- личные закономерности роста оксидных пленок.
Линейный закон роста пленок. Для металлов, образующих несплош- ные пленки, скорость роста пленки остается постоянной во времени:
dy = k × C,
dt (7.3)
где у – толщина пленки; t — время окисления; к – постоянная величина, С – концентрация окислителя на поверхности металла, независимая от времени из-за большой легкости адсорбции.
После интегрирования y = kt + A, (7.4)
где А — постоянная интегрирования.
Следовательно, толщина пленки, или величина химической коррозии, пропорциональна времени окисления. Константа интегрирования А опреде- ляет толщину пленки в начальный момент окисления (t = 0). Если принять, что окисление начинается на чистой металлической поверхности, то А = 0.
Линейный закон роста оксидных пленок наблюдается на щелочных и щелочноземельных металлах, имеющих отношение (Voк/VMe)<1 (рис. 7.2).
7.2).
Рис. 7.2 Окисление чистого магния в атмосфере кислорода при различных температурах
При определенных условиях (достаточно высокая температура) этому закону подчиняются также металлы, образующие летучие, легко возгоняю- щиеся оксиды. Скорость коррозии таких металлов, в основном, определяет- ся скоростью сублимации их оксидов. К ним относятся осмий, молибден, ру- тений, иридий, ванадий, вольфрам и сплавы, содержащие достаточное коли- чество этих элементов.
Параболический закон роста пленок. Для металлов, у которых (Voк/VMe)>1, процесс коррозии будет тормозиться диффузией кислорода че- рез сплошную пленку и все больше замедляться по мере ее роста.
Рассмотрим не начальный момент окисления, а такое состояние, когда на металле уже имеется некоторая сплошная пленка толщиной y . Тогда можно записать:
dn = Kd
P dc dt ,
dy
(7. 5)
5)
где dn — масса диффундирующего вещества, г; Kd — коэффициент диффузии, см2/c, Р — поперечное сечение, cм2; dc/dy — градиент концентрации кислорода, г/см3; dt — время диффузии, c.
Если считать режим диффузии стационарным, то dc/dy можно заме- нить отношением (С0 — С1)/y,
где С0 — концентрация кислорода на внешней поверхности пленки; С1 — кон- центрация кислорода на границе пленки с металлом.
При этом C1 » 0 , так как при имеющейся толщине пленки у весь ки- слород, проникающий через пленку, сразу же вступает в реакцию. Тогда скорость диффузии на единицу поверхности металла равна
U = dn = K C0 ,
d P d y
(7.6)
Если скорость роста пленки Uок равна скорости диффузии кислорода,
то Uок
= Kd
C0 , т. е. скорость окисления пропорциональна концентрации ки-
y
слорода и обратно пропорциональна толщине пленки
U ок
=dy dt
C0
= Kd ,
y
(7. 7)
7)
ydy =Kd C0dt. (7.8)
Интегрируя выражение (9.8), получаем:
y 2 = Kt + A,
(7.9)
где К — константа, учитывающая коэффициент диффузии и концентрацию кислорода, зависящая от температуры; A — постоянная интегрирования, кото- рая характеризует толщину пленки в начальный момент (ее можно принять равной нулю).
Исходя из уравнения (7.5), можно заключить, что в данном случае окисление металлов протекает по параболической кривой. Скорость роста
dy =
пленки
tgj
dt
(7.10)
представляет собой тангенс угла наклона касательной, проходящей через данную точку (рис. 7.3).
Рис. 7.3 Параболические кривые окисления железа на воздухе при повышенных температурах
По параболическому закону наблюдается окисление для ряда тех- нически важных металлов, таких, как железо, кобальт, никель, медь, а также марганец, бериллий, цирконий, титан.
Логарифмический закон роста пленок. Для некоторых металлов рост пленки во времени происходит медленнее, чем это следует из закона стацио- нарной диффузии, т.е. параболического закона окисления металлов. Наблю- дается логарифмическая зависимость скорости окисления
y = ln(Kt ).
(7.11)
Экспериментально логарифмический закон роста пленок установлен при окислении алюминия и цинка в интервале температур 225-280°С, железа до 375°С, никеля до 650°С (рис.7.4).
Рис. 7.4 Окисление железа во времени: а – логарифмические кривые; б – кривые окисления в полулогарифмических координатах
Линейный ход кривых в полулогарифмических координатах доказы- вает существование логарифмической зависимости окисления. Наличие та- кого закона окисления у алюминия, цинка, хрома, кремния, объясняют уп- лотнением внешних слоев пленки с увеличением толщины ее, в связи с чем уменьшается скорость диффузии кислорода во времени.
Приведенные законы роста окисных пленок справедливы для опре- деленных условий. На практике для одного и того же металла, в зависимости от температуры окисления, времени, состава атмосферы, могут иметь место все случаи окисления.
Влияние различных факторов на газовую коррозию
Скорость газовой коррозии в значительной степени меняется в зависи- мости от внутренних и внешних факторов.
К внутренним факторам относятся природа металла, состав сплава, его структура, обработка поверхности, наличие напряжений. Состав сплава влияет на скорость газовой коррозии сталей. Значительное повышение ус- тойчивости к газовой коррозии происходит при легировании сталей хромом, алюминием, кремнием, что связано с образованием на поверхности оксид- ных пленок с высокими защитными свойствами. Высокой жаростойкостью обладают сплавы никеля с хромом – нихромы, содержащие 80% никеля и 20% хрома. Углерод не вызывает заметных изменений в скорости коррозии.
Структура сплава в незначительной степени влияет на скорость газо- вой коррозии. При переходе стали из ферритной структуры в аустенитную наблюдается некоторое замедление окисления при повышении температуры.
Наиболее жаростойкой является сталь с аустенитной структурой. Хро- моникелевые стали с двухфазной аустенитно-ферритной структурой менее устойчивы к окислению. С увеличением содержания ферритной составляю- щей скорость окисления стали повышается. Так, например, хромоникелевая аустенитная сталь 12Х18Н9Т имеет более высокую жаростойкость, чем двухфазная сталь Х18Н5Т с более высоким содержанием хрома. Это связано с тем, что на двухфазных сталях образуются менее совершенные пленки, чем на однофазных.
Характер обработки поверхности металла влияет на скорость газовой коррозии лишь в начальной стадии окисления: гладкие поверхности имеют несколько меньшую скорость газовой коррозии.
К внешним факторам относятся температура, состав газовой среды, скорость движения газа, условия нагревания и т. д.
д.
С повышением температуры скорость окисления металлов значительно возрастает. Это связано с увеличением константы скорости реакции и коэф- фициента диффузии кислорода.
Металлы при высоких температурах могут взаимодействовать с кисло- родом, парами воды, оксидом углерода (IV), оксидом серы (IV) по реакциям:
2Me + O2 = 2MeO;
Me + CO2 = MeO + CO; Me + h3O = MeO + h3; 3Me + SO2 = 2MeO + MeS.
Защитные свойства образующихся пленок различны, что влияет на скорость окисления металлов в указанных средах. Так, при температуре 900°С скорость окисления железа возрастает в ряду Н2О ®→ СО2 →® О2 →® SO2.
Значительное увеличение скорости окисления металлов наблюдается при повышении концентрации кислорода в атмосфере инертных газов, со- держащих небольшие примеси кислорода. При переходе же от атмосферы воздуха к атмосфере чистого кислорода не наблюдается увеличения скорости коррозии пропорционально увеличению парциального давления кислорода.
Скорость движения газа заметно влияет на скорость коррозии в на- чальной стадии окисления. Однако при очень больших скоростях движения газовой среды возникает опасность эрозионного разрушения оксидных пле- нок, что может сильно увеличить скорость коррозии.
Наличие резких колебаний температуры в процессе нагревания может привести к разрушению защитных оксидных пленок. Коэффициент термиче- ского расширения оксида, как правило, значительно ниже, чем для чистого
металла. Вследствие этого резкие колебания температуры способствуют воз- никновению добавочных внутренних напряжений и механическому разру- шению оксидной защитной пленки.
Живите по правилу: МАЛО ЛИ ЧТО НА СВЕТЕ СУЩЕСТВУЕТ? Я неслучайно подчеркиваю, что место в голове ограничено, а информации вокруг много, и что ваше право…
Что способствует осуществлению желаний? Стопроцентная, непоколебимая уверенность в своем…
Что делает отдел по эксплуатации и сопровождению ИС? Отвечает за сохранность данных (расписания копирования, копирование и пр. )…
)…
ЧТО ТАКОЕ УВЕРЕННОЕ ПОВЕДЕНИЕ В МЕЖЛИЧНОСТНЫХ ОТНОШЕНИЯХ? Исторически существует три основных модели различий, существующих между…
Не нашли то, что искали? Воспользуйтесь поиском гугл на сайте:
Сравнение точечной и щелевой коррозии: Выявление различий | Информационный ресурс
Коррозия — повреждение технических материалов в результате химического взаимодействия с окружающей средой — представляет собой необычайно затратную проблему. Неконтролируемая коррозия систем трубок — главная причина ежегодных миллиардных убытков в сфере шельфовой добычи. Коррозию можно предотвратить, если знать, на что обратить внимание, и своевременно принять упреждающие меры для снижения рисков возникновения коррозии.
Почти все металлы в нашем мире подвержены коррозии при определенных условиях. Существуют способы предотвращения коррозии в нефтегазовой отрасли, в особенности при шельфовой добыче. Однако они требуют фундаментальных знаний различных видов коррозии и понимания причин ее возниковения. Понимание того, где искать коррозию, помогает свести к минимуму риски ее возникновения на буровых платформах и нефтеперерабатывающих заводах, а также существенно экономит время и деньги.
Понимание того, где искать коррозию, помогает свести к минимуму риски ее возникновения на буровых платформах и нефтеперерабатывающих заводах, а также существенно экономит время и деньги.
Хотите найти подходящие материалы для шельфовой добычи? Руководство Swagelok по подбору материалов поможет принять меры для предотвращения коррозии.
ПРОСМОТРЕТЬ РУКОВОДСТВО ПО ПОДБОРУ МАТЕРИАЛОВ
Возникновение коррозии
Коррозия возникает при окислении атомов металла под воздействием жидкости или газа, что ведет к потере материала на его поверхности. Такая потеря материала приводит к уменьшению толщины стенок компонентов из углеродистой и низколегированных сталей, которые подвержены общей коррозии, что повышает вероятность механических повреждений.
Системы металлических трубок чаще всего используются в аналитических и технологических системах, гидравлических трубопроводах, а также в системах управления и бытовых системах. Многие специализированные металлы, используемые в нефтегазовой отрасли, представляют собой нержавеющую сталь с содержанием хрома более 10 %. Это способствует формированию оксидного слоя, защищающего металл от коррозии. Тем не менее при разрушении этого слоя под воздействием окружающей среды возникает коррозия нержавеющей стали.
Это способствует формированию оксидного слоя, защищающего металл от коррозии. Тем не менее при разрушении этого слоя под воздействием окружающей среды возникает коррозия нержавеющей стали.
Практически все металлы подвержены коррозии при определенных условиях. К примеру, ржавление является обычным явлением, сопутствующим коррозии углеродистой стали, в результате которого происходит разрушение железа и образование оксида железа. Однако существует и множество других видов коррозии. Каждый вид коррозии представляет опасность, которую необходимо оценить при выборе наиболее подходящего материала для вашей области применения.
Выявление распространенных видов коррозии
Существует множество различных видов коррозии, которые могут нанести серьезный урон нефтегазовым установкам. Многие виды коррозии возникают только при определенном химическом составе металла и условиях эксплуатации. Далее мы рассмотрим две формы местной коррозии нержавеющей стали: точечную и щелевую.
Точечная коррозия
Точечная коррозия возникает при разрушении защитного оксидного слоя на поверхности нержавеющей стали, в результате чего находящиеся под ним атомы чистого металла могут начать терять электроны путем окисления в коррозионном водном растворе. Эта электрохимическая реакция вызывает образование небольших точечных выемок, или «питтингов».
Эта электрохимическая реакция вызывает образование небольших точечных выемок, или «питтингов».
Как правило, питтинги можно обнаружить при тщательном визуальном осмотре, однако они могут распространяться глубоко, полностью пронизывая стенку трубки. Точечная коррозия также может способствовать образованию трещин в компонентах, находящихся под механической нагрузкой. В средах с повышенной концентрацией хлора, в том числе вызванной испарением из капель соленой воды, вероятность точечной коррозии выше, особенно при высоких температурах.
Во время осмотра металлических трубок на предмет точечной коррозии ищите красновато-коричневые отложения оксида железа и точечные выемки на поверхности металла.
Щелевая коррозия
Как и точечная коррозия, щелевая коррозия начинается с разрушения защитной оксидной пленки нержавеющей стали с дальнейшим образованием неглубоких выемок. Однако щелевая коррозия, как следует из названия, возникает не на виду, а в щелях.
В обычной жидкостной или газовой системе щели имеются между трубками и их опорами или хомутами, между соседними линиями трубопроводов, а также под слоем грязи и отложений, которые могут скапливаться на поверхностях. Избежать образования щелей в трубопроводных конструкциях практически невозможно, а узкие щели представляют собой большую опасность нарушения целостности нержавеющей стали. Щелевая коррозия возникает в результате диффузии морской воды в щель, что приводит к образованию агрессивной химической среды, в которой вызывающие коррозию ионы растворяются и не могут быстро диффундировать из щели. В такой ситуации коррозия может быстро распространиться по всей поверхности внутри щели.
Избежать образования щелей в трубопроводных конструкциях практически невозможно, а узкие щели представляют собой большую опасность нарушения целостности нержавеющей стали. Щелевая коррозия возникает в результате диффузии морской воды в щель, что приводит к образованию агрессивной химической среды, в которой вызывающие коррозию ионы растворяются и не могут быстро диффундировать из щели. В такой ситуации коррозия может быстро распространиться по всей поверхности внутри щели.
Щелевую коррозию можно увидеть только после снятия хомута с установленной трубки. Важно помнить, что щелевая коррозия может возникать при более низких температурах, чем точечная коррозия, поскольку под геометрической щелью (например, под трубным хомутом) легче образуется «питтинг».
Предотвращение коррозии
Зачастую коррозию можно свести к минимуму благодаря обучению персонала, предоставив ему базовые знания о материалах.
Подбор материалов. Прежде всего уделите внимание подбору материалов для трубок, опор и хомутов. Трубки из нержавеющей стали 316 подходят во многих случаях при условии, что их содержат в чистоте, а температура не слишком высока. В теплом климате, особенно в местах, где быстро образуются отложения солей, и в ситуациях, когда ржавчина со строительных балок и пола из углеродистой стали скапливается на поверхностях нержавеющей стали, коррозия трубок из нержавеющей стали 316 наблюдается чаще.
Трубки из нержавеющей стали 316 подходят во многих случаях при условии, что их содержат в чистоте, а температура не слишком высока. В теплом климате, особенно в местах, где быстро образуются отложения солей, и в ситуациях, когда ржавчина со строительных балок и пола из углеродистой стали скапливается на поверхностях нержавеющей стали, коррозия трубок из нержавеющей стали 316 наблюдается чаще.
В таких случаях лучше использовать трубки из супераустенитной (например, 6Mo или 6HN) или супердуплексной (например, 2507) нержавеющей стали, которые имеют гораздо более высокую стойкость к коррозии. Повышенный предел прочности на разрыв и предел текучести супердуплексной нержавеющей стали также упрощает создание систем с более высоким максимально допустимым рабочим давлением (МДРД). Во избежание дорогостоящих ошибок обратитесь в региональный авторизованный центр продаж и сервисного обслуживания Swagelok, где вам помогут подобрать подходящие продукты и материалы для вашей области применения.
Расположение и конструкция. Для предотвращения щелевой коррозии требуется тщательное проектирование системы для сведения к минимуму числа мест, в которых может возникнуть коррозия. Один из способов уменьшения количества щелей в системе трубок — избегать размещения трубок вплотную к стенам или друг к другу. При выявлении щелевой коррозии трубок из нержавеющей стали 316 можно заменить их трубками из более устойчивого к коррозии материала и смонтировать их при помощи недорогих трубных обжимных фитингов из нержавеющей стали 316. Компания Swagelok предлагает несколько сочетаний трубных обжимных фитингов из нержавеющей стали 316 с трубками из различных коррозионностойких сплавов.
Курс обучения — материаловедение и коррозия
Помимо этих простых мер рекомендованный подход к предотвращению коррозии включает в себя углубленное обучение и внедрение эффективной программы регулярного контроля коррозии. Компания Swagelok предлагает курс обучения материаловедению, который поможет инженерам, техническим специалистам и другим сотрудникам, участвующим в процессе подбора материалов, выбрать подходящие коррозионностойкие сплавы для жидкостных и газовых систем. Получение базового представления о коррозии — как она выглядит, где и по каким причинам возникает — теми, кто работает с трубными системами каждый день, может предотвратить разрушение материалов и дорогостоящий ремонт. Обратитесь в региональный центр продаж и сервисного обслуживания Swagelok и узнайте, как курс обучения материаловедению может помочь вашей организации в борьбе с коррозией.
Получение базового представления о коррозии — как она выглядит, где и по каким причинам возникает — теми, кто работает с трубными системами каждый день, может предотвратить разрушение материалов и дорогостоящий ремонт. Обратитесь в региональный центр продаж и сервисного обслуживания Swagelok и узнайте, как курс обучения материаловедению может помочь вашей организации в борьбе с коррозией.
ПОДРОБНЕЕ О КУРСЕ ОБУЧЕНИЯ МАТЕРИАЛОВЕДЕНИЮ SWAGELOK
Моделирование питтинговой коррозии в COMSOL Multiphysics®
Когда капля воды попадает на металлическую поверхность, это может привести к возникновению коррозии. При определённых условиях и достаточно длительном времени коррозионного воздействия на металлической поверхности образуется маленькое углубление. Со временем электрохимические условия в таком углублении меняются, вследствие чего нижняя часть поверхности приобретает анодную поляризацию, а удалённая от неё часть — катодную. В результате этого интенсивность коррозии в донной части углубления возрастает, что приводит к увеличению размеров углубления и образованию так называемого питтинга.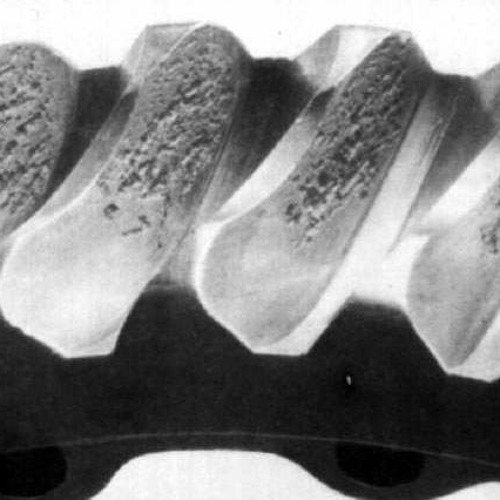 Моделирование питтинговой коррозии позволяет проанализировать развитие питтингов, возникающих в различных материалах и конструкциях при определённых условиях. В этой статье мы рассмотрим, как построить модель питтинговой коррозии.
Моделирование питтинговой коррозии позволяет проанализировать развитие питтингов, возникающих в различных материалах и конструкциях при определённых условиях. В этой статье мы рассмотрим, как построить модель питтинговой коррозии.
Коррозионные процессы. Краткое введение
Гальваническая коррозия возникает при наличии электрического контакта между двумя металлами, атомы которых имеют разные значения энергии сродства к электрону. Если два таких металла поместить в электролит, то на их поверхности образуется двойной электрический слой. Потенциал двойного электрического слоя для этих двух металлов будет разным. Таким образом, электроны передаются от металла с меньшим электрохимическим потенциалом к металлу с более высоким потенциалом, как показано на рис. 1.
На поверхности благородных металлов (с высоким электрохимическим потенциалом) электроны участвуют в реакции восстановления (катодная реакция). Металлы с меньшим потенциалом отдают электроны и в результате этой анодной реакции растворяются.
Рисунок 1. Схематическое описание гальванической коррозии.
Если позволить электрохимическому процессу, схема которого показана на рис. 1, осуществляться в течение некоторого времени, то металл с меньшим потенциалом (в данном случае это железо) будет растворяться вблизи поверхности контакта с другим металлом (см. рис. 2), потенциал которого выше.
Рисунок 2. В результате гальванической коррозии железо растворяется вблизи области контакта с медью.
Теперь рассмотрим каплю воды на поверхности металла (см. рис. 3). На микроскопическом уровне металл может состоять из разных фаз с отличающимся сродством к электрону. Это означает, что, например, в кристаллитах будут идти катодные реакции, а в межкристаллитных областях — анодные.
Рисунок 3. Схема микроструктуры металлической поверхности: показаны кристаллиты и межкристаллитные области.
Согласно схеме, показанной на рис. 2, на той поверхности, где растворяется железо, образуется гидроксид железа. Гидроксид железа — один из компонентов ржавчины. Но если электрохимический процесс идёт по схеме, представленной на рис. 3, тогда ржавчина может появляться на всей поверхности металла, поскольку межкристаллитные области распределены очень равномерно. Такую коррозию обычно называют генерализованной.
Гидроксид железа — один из компонентов ржавчины. Но если электрохимический процесс идёт по схеме, представленной на рис. 3, тогда ржавчина может появляться на всей поверхности металла, поскольку межкристаллитные области распределены очень равномерно. Такую коррозию обычно называют генерализованной.
Теперь обратимся к рис. 4, на котором показана схема дальнейшего развития генерализованной коррозии, описанной на рис. 3. В центре капли диффузия кислорода к зернам кристаллита занимает больше времени, чем по краям капли, где диффузионный пробег намного короче. На поверхности металла, расположенной под центром капли, концентрация кислорода понижена, что в свою очередь уменьшает электрохимический потенциал в этой части поверхности по отношению к областям по периметру капли. Таким образом, когда потенциал оказывается меньше потенциала пассивации железа, защитный оксидный слой теряет устойчивость. В итоге, кристаллиты, расположенные в центральной части, из-за снижения концентрации кислорода станут анодами. В результате растворения железа в центральной части капли на поверхности металла появляется углубление. Кроме того, ионы железа вступают в реакцию с водой с образованием протонов, из-за чего в углублении снижается водородный показатель pH. Уменьшение pH повышает кислотность среды и, таким образом, ещё сильнее ускоряет коррозию. Описанный процесс получил название эксперимента Эванса с каплей (Evans drop experiment)[1] в честь учёного, который первым объяснил и воспроизвёл этот процесс.
В результате растворения железа в центральной части капли на поверхности металла появляется углубление. Кроме того, ионы железа вступают в реакцию с водой с образованием протонов, из-за чего в углублении снижается водородный показатель pH. Уменьшение pH повышает кислотность среды и, таким образом, ещё сильнее ускоряет коррозию. Описанный процесс получил название эксперимента Эванса с каплей (Evans drop experiment)[1] в честь учёного, который первым объяснил и воспроизвёл этот процесс.
Рисунок 4. Эксперимент Эванса с каплей. Образование углубления приводит к снижению водородного показателя, что дополнительно ускоряет анодную реакцию.
Образование углубления может происходить и по другому сценарию. Например, механическое воздействие или наличие примесей на поверхности металла могут ослабить оксидную плёнку, которая в некоторой степени защищает поверхность железа от дальнейшей коррозии. Нержавеющая сталь тоже имеет защитную оксидную плёнку, которая может быть повреждена вследствие механического или химического воздействия. —
—
Концентрацию гидроксильных ионов можно исключить при условии равновесия автопротолиза воды. Концентрацию одного из других ионов, а именно протона, можно исключить, приняв условие электронейтральности. Оба допущения в COMSOL Multiphysics® учитываются автоматически при использовании интерфейса Tertiary Current Distribution, Nernst-Planck с выбранной опцией Water-based with electroneutrality. Отметим, что при расчёте плотности тока электролита в уравнение баланса токов включены уравнения переноса для всех ионов. Ещё одной зависимой переменной является электрический потенциал электролита.
Предположим, что в результате электроосаждения внутри углубления образовался пористый слой, поэтому будем рассматривать углубление как пористую структуру, поры которой заполнены электролитом. Это разумное предположение, поскольку из того металла, на месте которого образовалось углубление, с высокой вероятностью сформируется пористое отложение. Задачу будем решать в двумерной осесимметричной постановке, как показано на рис. 5.
5.
Рисунок 5. Геометрическая модель расчётной области.
Реакция растворения металла моделируется на всей границе, обозначенной на рис. 5 как «Fe electrode surface». Будем считать, что скорость анодной реакции пропорциональна концентрации протонов. Такая зависимость характерна для условий повышенной кислотности в присутствии хлорида [2]. Чтобы связать перемещение границы расчётной области с интенсивностью растворения железа, воспользуемся методом подвижной сетки.
Как мы уже отмечали, реакция восстановления кислорода не моделируется. Мы заменяем моделирование этого процесса на граничное условие постоянного электрического потенциала электролита вдали от углубления на горизонтальной границе, которая обозначена как «Bulk electrolyte boundary». Также на этой границе мы зададим концентрацию ионов натрия, хлорида и железа.
Будем считать, что в области, занятой электролитом, в том числе в углублении, идут реакции автопротолиза воды и образования гидроксида железа. Отметим, что гидроксид расходуется в реакции образования Fe(OH)2(s), поэтому, как уже упоминалось выше (см. рис. 4), водородный показатель уменьшается.
Отметим, что гидроксид расходуется в реакции образования Fe(OH)2(s), поэтому, как уже упоминалось выше (см. рис. 4), водородный показатель уменьшается.
Начальные значения концентраций и электрического потенциала электролита рассчитываются с помощью решения стационарной задачи для исходной геометрической модели. То есть для получения начальных значений задача решается для неизменяемой геометрической модели с указанными выше граничными условиями с помощью стационарного решателя. В результате получается некоторое распределение концентраций и электрического потенциала электролита для t = 0. Это решение является начальным условием для нестационарной задачи.
Результаты
Использование стационарного решения в качестве начальных условий является разумным подходом, поскольку изменение состава и электрического потенциала электролита сначала, то есть в течение первых суток, происходит довольно медленно.
На рис. 6 показано, как увеличится углубление по истечении 30 дней. Для области внутри углубления характерен большой градиент потенциала электролита. В углублении потенциал электролита изменяется от 0,43 мВ до 16,5 мВ, тогда как за пределами углубления потенциал изменяется от 0 мВ до 0,43 мВ в течение 30 дней. Отметим, что интенсивность процессов переноса в углублении ниже, поскольку эта область представляет собой пористую среду с более низкими по сравнению с электролитом снаружи эффективными свойствами переноса. Качественно такое же распределение потенциала наблюдается в течение всего моделируемого периода времени, при этом донная часть углубления увеличивается в размерах быстрее, чем устье. По этой причине проходное сечение для переноса заряда в устье углубления сужается, что приводит к большим градиентам потенциала электролита. В результате мы действительно наблюдаем коррозию на плоской поверхности. Через 30 дней поверхность сместится примерно на 0,35 мкм, а смещение донной части углубления составит 1,45 мкм.
Для области внутри углубления характерен большой градиент потенциала электролита. В углублении потенциал электролита изменяется от 0,43 мВ до 16,5 мВ, тогда как за пределами углубления потенциал изменяется от 0 мВ до 0,43 мВ в течение 30 дней. Отметим, что интенсивность процессов переноса в углублении ниже, поскольку эта область представляет собой пористую среду с более низкими по сравнению с электролитом снаружи эффективными свойствами переноса. Качественно такое же распределение потенциала наблюдается в течение всего моделируемого периода времени, при этом донная часть углубления увеличивается в размерах быстрее, чем устье. По этой причине проходное сечение для переноса заряда в устье углубления сужается, что приводит к большим градиентам потенциала электролита. В результате мы действительно наблюдаем коррозию на плоской поверхности. Через 30 дней поверхность сместится примерно на 0,35 мкм, а смещение донной части углубления составит 1,45 мкм.
Рисунок 6. Размеры донной части углубления увеличиваются быстрее, чем размеры устья. Это приводит к большему градиенту потенциала электролита вблизи устья.
Это приводит к большему градиенту потенциала электролита вблизи устья.
Изменение водородного показателя в процессе коррозии показано на рис. 7. Значение водородного показателя в донной части через сутки равно 9,48, а через 30 суток — 9,14. Может показаться, что это незначительное изменение, однако оно соответствует увеличению концентрации протонов в 2,2 раза. Константа скорости коррозионного процесса пропорциональна концентрации протонов, а значит и скорость коррозии тоже возрастает.
Рисунок 7. Водородный показатель в углублении в различные моменты времени.
На рис. 8 приведены значения скорости коррозии в мкм/сут для четырех моментов времени, показанных выше. Максимальная скорость коррозии в донной части углубления через 30 дней в 2,3 раза выше по сравнению со скоростью коррозии через 1 день. Соответственно, концентрация протонов через 30 дней в 2,2 раза выше, чем через 1 день.
Рисунок 8. Скорость коррозии на поверхности металла в разные моменты времени.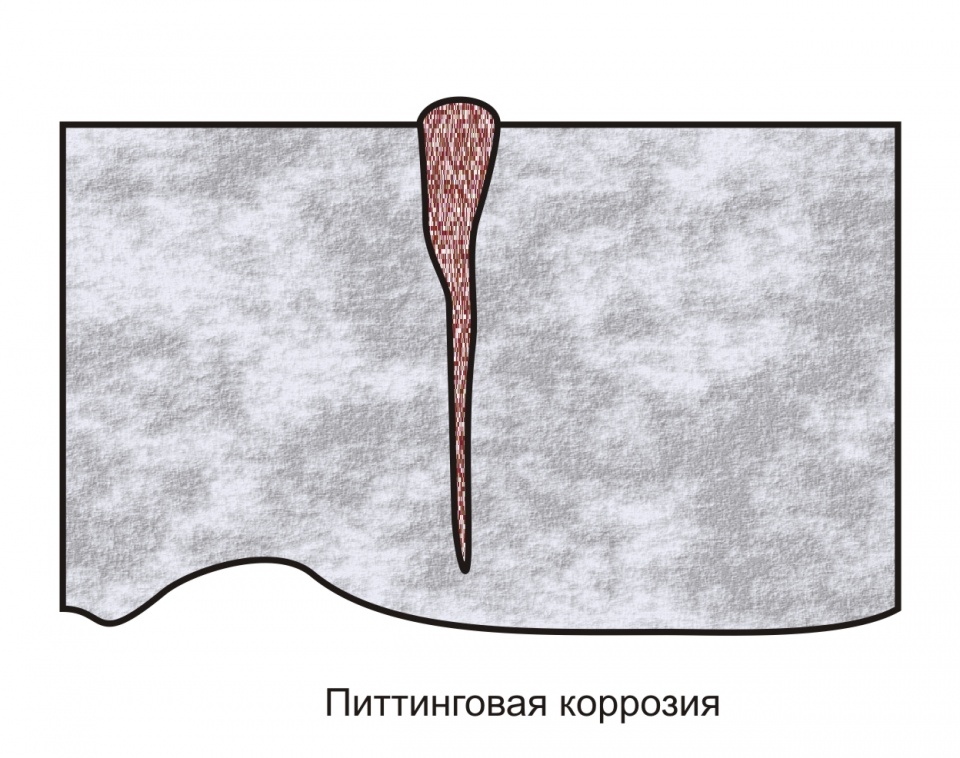
Распределение концентрации ионов натрия обратно распределению концентрации ионов железа. Причина — условие электронейтральности. По мере того, как ионы железа попадают в электролит, ионы натрия выталкиваются из углубления. В отличие от ионов натрия, ионы хлорида, наоборот, движутся в углубление, вследствие условия электронейтральности (не показаны).
Рисунок 9. Концентрация ионов натрия в различные моменты времени.
Расчётная модель демонстрирует эффект «порочного круга» питтинговой коррозии. Интенсивность процесса растёт с течением времени, пока углубление не станет достаточно глубоким. Тогда омические потери и продукты коррозии ограничивают скорость реакции.
Заключение
Расчётную модель можно усложнить, если добавить учёт материального баланса осажденных продуктов коррозии. Плотность продуктов реакции меньше, чем плотность железа, поэтому они образуются в углублении, но затем вытесняются из него. Этот процесс можно смоделировать, если пористость сделать зависимой переменной и учесть конвективный перенос оксидов.
Ещё одно направление усложнения модели — введение в неё полной геометрической модели капли, что позволит учесть диффузию и восстановление кислорода.
Кроме того, модель можно дополнить более подробным описанием химическим процессов. Например, можно учесть образование различных ионов железа, описать дополнительные окислительно-восстановительные реакции, а также включить в модель больше различных оксидов и гидроксидов железа, образующихся на поверхности металла. Тем не менее, мы можем поэкспериментировать и с исходной моделью, которая сама по себе уже является достаточно комплексной, несмотря на относительную простоту её построения.
Дальнейшие шаги
Узнайте о функциональных возможностях модуля «Коррозия», кликнув по кнопке:
Описание модуля
Источники
- U.R. Evans, “Corrosion and Oxidation of Metals”, Amolds, p. 118., 1960.
- H.C. Kuo and K. Nobe, “Electrodissolution Kinetics of Iron in Chloride Solutions”, J. of Electrochem.
 Soc, vol. 125, no.6, 1978.
Soc, vol. 125, no.6, 1978.
Что такое точечная коррозия? Как обнаружить и лечить питтинговую коррозию?
Точечная коррозия поражает металлы и сплавы, такие как сталь, железо, алюминий и другие. Обычно он ограничивается определенными областями. Он быстро проникает и атакует, и его трудно обнаружить. Чаще всего это происходит, когда слой пассивного покрытия физически поврежден или подвергся химическому воздействию. Это создает слабое место, где вода или коррозионные растворы воздействуют на подложку.
Соседние материалы часто остаются незатронутыми. Если ее не остановить, точечная коррозия может быть разрушительной для кровельных систем или любой металлической конструкции. Она возникает быстро и ее легко не заметить, поэтому многие считают ее самой опасной формой коррозии.
Точечная коррозия Объяснение
Точечная коррозия представляет собой полость, отверстие или ямку, которые образуются на небольшой площади или в точке. Ямки или отверстия закрыты небольшим количеством продуктов коррозии (ржавчины) на поверхности. Когда катодная реакция на большой площади (покрытие) поддерживает анодную реакцию на небольшой площади (открытый металл), образуется ямка, полость или маленькое отверстие. Окисление происходит в металле даже при отсутствии подачи кислорода.
Когда катодная реакция на большой площади (покрытие) поддерживает анодную реакцию на небольшой площади (открытый металл), образуется ямка, полость или маленькое отверстие. Окисление происходит в металле даже при отсутствии подачи кислорода.
Высокое потребление электронов большим катодом переносится на маленький анод, что приводит к интенсивной точечной коррозии. Это будет незаметно и произойдет быстро с очень вредными последствиями. На поверхности видно только небольшое пятно ржавчины, в то время как повреждение происходит глубоко в металлической конструкции внизу.
Диаграмма точечной коррозии, показывающая, как ржавчина образуется в небольшой анодной области из-за большого потребления электронов большой катодной площадью, образующей ямку внизу.
Что вызывает точечную коррозию?
Точечная коррозия возникает, когда катод (поврежденное покрытие) большой, а анод (открытый металл) маленький. Обычно поверхностный защитный слой или пленка становится катодом, когда он повреждается и трескается. Затем обнажается небольшой участок металла, который становится анодом.
Затем обнажается небольшой участок металла, который становится анодом.
Питтинг проявляется сильно, если раствор на поверхности металла содержит ионы хлорида, гипохлорита или бромида. Другими вредными растворами являются те, которые содержат фториды и йодиды. Также известно, что сульфиды и вода усиливают процесс питтинговой коррозии.
Наиболее распространенными причинами точечной коррозии являются;
- Трещины в защитном покрытии
- Царапины, потертости и мелкие сколы
- Неравномерное напряжение
- Дефект металлической подложки
- Турбулентный поток жидкости
- Неоднородное защитное покрытие
- Химическое воздействие на защитное покрытие
Металлы, склонные к точечной коррозии;
- Stainless steel
- Chromium
- Passive iron
- Mercury
- Cobalt
- Aluminum
- Copper
- Associated alloys
Another example of pitting corrosion occurs when a metal is poorly maintained and exposed to water droplets and dust частицы. Область под каплей недостаточно насыщена кислородом, в то время как окружающие области хорошо насыщены кислородом. Это приводит к дифференциальной аэрационной коррозии, когда окружающие области являются катодными, а небольшая область под каплями и частицами пыли становится анодной. Электроны проходят через металл и встречают воду и кислород. Ионы образуются и распадаются вместе, образуя ржавчину. По мере образования ржавчины в металле появляются ямки, трещины и щели.
Область под каплей недостаточно насыщена кислородом, в то время как окружающие области хорошо насыщены кислородом. Это приводит к дифференциальной аэрационной коррозии, когда окружающие области являются катодными, а небольшая область под каплями и частицами пыли становится анодной. Электроны проходят через металл и встречают воду и кислород. Ионы образуются и распадаются вместе, образуя ржавчину. По мере образования ржавчины в металле появляются ямки, трещины и щели.
Типы точечной коррозии
Точечная коррозия может проявляться в различных формах. Форма ямки во многом зависит от затронутого материала и направления зерна в этом материале. Чаще всего страдают пассивные металлы и сплавы, в том числе нержавеющая сталь и алюминий. Однако почти любой металл или материал, подверженный коррозии, может быть затронут.
Желобковая точечная коррозия
Желобовые углубления имеют тенденцию быть полусферическими, чашеобразными или неправильной формы. Точечная коррозия возникает, когда пассивная пленка (защитный слой) разрушается, а металлическая стенка разрушается, образуя узкие и глубокие бороздки. Их плоские стенки обнажают кристаллическую структуру металла. Они могут быстро перфорировать толщину материала, например, кровельного листа, фермы или элемента водосточного желоба.
Их плоские стенки обнажают кристаллическую структуру металла. Они могут быстро перфорировать толщину материала, например, кровельного листа, фермы или элемента водосточного желоба.
Диаграмма поперечного сечения точечной коррозии с вертикальной коррозией зерна.
Диаграмма поперечного сечения узкой и глубокой точечной коррозии.
Диаграмма сечения эллиптической точечной коррозии.
Неглубокая, широкая желобчатая диаграмма поперечного сечения точечной коррозии.
Боковая питтинговая коррозия
Боковые ямки покрыты полупроницаемой пленкой продуктов коррозии (ржавчины) и появляются в виде горизонтальных зерен, подрезов и подповерхностных форм. Боковая точечная коррозия может очень быстро проникнуть в металл. Это очень трудно обнаружить, потому что поверхность металла выглядит нетронутой и свободной от коррозии. При наличии лишь нескольких небольших пятен ржавчины может показаться, что повреждение очень незначительное.
Диаграмма сечения поперечного сечения точечной коррозии при горизонтальном воздействии зерен.
Диаграмма поперечного сечения подповерхностной боковой точечной коррозии.
Подрезание боковой точечной коррозии Диаграмма поперечного сечения.
Как проверить на питтинговую коррозию?
Визуальный осмотр корродированной металлической поверхности является первым и основным используемым методом. Подсчитайте количество ямок через окуляр микроскопа на определенной площади поверхности, например, 20 см 2 , чтобы определить приблизительный размер и распределение ямок. Количество ям не обязательно является самым важным фактором для рассмотрения. Глубина ямы, безусловно, самая большая опасность. Одна узкая глубокая яма может быть более опасной, чем множество мелких ям. Металлографический поперечный разрез для измерения глубины ямок покажет интенсивность атаки.
Звуковые испытания — это когда ультразвуковые импульсы звуковой энергии передаются через контактную жидкость на масляной или водной основе на поверхность металла. Волны генерируются и отражают эхо, которые преобразуются в электрические сигналы. Эти сигналы можно интерпретировать, чтобы показать расположение ямок, щелей и дефектов в металле. Этот тест обладает хорошей чувствительностью и дает мгновенную информацию о глубине, ширине и расположении ямок и дефектов.
Волны генерируются и отражают эхо, которые преобразуются в электрические сигналы. Эти сигналы можно интерпретировать, чтобы показать расположение ямок, щелей и дефектов в металле. Этот тест обладает хорошей чувствительностью и дает мгновенную информацию о глубине, ширине и расположении ямок и дефектов.
Электромагнитные испытания используются для обнаружения дефектов или неоднородностей в структуре электропроводящих материалов, таких как сталь и железо. Материалы с дефектами будут создавать магнитное поле, отличное от поля эталонного материала без дефектов.
Электрохимические испытания для измерения точечной коррозии в любом металле, такие как циклическая поляризация и потенциостатические испытания, также возможны. Это краткосрочные электрохимические тесты, дающие мгновенные результаты.
Другим вариантом является испытание погружением или метод снижения веса. Эти тесты требуют больше времени для выполнения. Они включают удаление образца металла и погружение в раствор. Через несколько дней его можно снять, чтобы рассчитать скорость коррозии. Вы можете наблюдать за ямками и их глубиной под микроскопом и производить необходимые расчеты.
Они включают удаление образца металла и погружение в раствор. Через несколько дней его можно снять, чтобы рассчитать скорость коррозии. Вы можете наблюдать за ямками и их глубиной под микроскопом и производить необходимые расчеты.
Существует несколько стандартов, которые содержат рекомендации по электрохимическим испытаниям на точечную коррозию нержавеющих сталей, и наиболее популярными из них являются:
- Испытание на циклическую поляризацию по ASTM G61
- Испытание на электрохимическую точечную коррозию по ASTM G150
Как лечить точечную коррозию?
Рекомендуется использовать рекомендуемые процедуры очистки, чтобы полностью обнажить ямки и удалить продукты коррозии. Избегайте использования растворов, которые чрезмерно воздействуют на основной металл. Желательно во время чистки периодически прощупывать ямки остроконечным инструментом. Это позволит вам определить степень любого подреза или подповерхностной коррозии. Энергичная очистка ямы проволочной щеткой значительно расширит отверстия. Удаление продуктов коррозии и подрезов металла поможет вам оценить степень повреждения.
Удаление продуктов коррозии и подрезов металла поможет вам оценить степень повреждения.
Когда металлический материал будет чистым и свободным от мусора, проведите окончательную проверку повреждений. Если вы довольны тем, что коррозия была обнаружена вовремя, вы можете приступить к нанесению базового грунтовочного покрытия, а затем еще одного или двух верхних слоев. Если повреждение серьезное, а компонент слишком слабый, его необходимо заменить.
Цинк-фосфатное грунтовочное покрытие является одним из наиболее популярных методов покрытия для защиты от точечной коррозии. Специально разработанные грунтовки, такие как фосфат цинка, улучшают коррозионную стойкость.
Металлизация распылением цинка — это метод, который очень эффективен против коррозии. Он имеет гладкую поверхность, которая эстетически привлекательна и популярна. Он не обеспечивает такую же защиту, как горячее цинкование, но поскольку это холодный процесс, нет риска деформации металла. Металлизация распылением цинка идеально подходит для использования на декоративных металлических предметах, таких как художественные выставки, металлические перила и заборы.
Металлизация распылением цинка идеально подходит для использования на декоративных металлических предметах, таких как художественные выставки, металлические перила и заборы.
Химическое покрытие использует электростатический или сжатый воздух для нанесения порошка специального состава на стальную поверхность. Затем он плавится, образуя гладкую защитную пленку. Обработанная таким образом сталь не только защищена от коррозии и УФ-повреждений, но и обладает высокой устойчивостью к отслаиванию, царапанью и растрескиванию.
Горячее погружение — это метод покрытия цинком, который можно использовать для стали всех форм и размеров. Он включает погружение стали в ванну с расплавленным цинком при температуре до 450°C. Сталь, оцинкованная таким образом, является особенно популярным подходом для применения в трубах, поскольку она хорошо защищена от коррозии, а также от экстремальных погодных условий.
Как предотвратить и защитить от точечной коррозии?
Факторы окружающей среды, вызывающие точечную коррозию, должны быть по возможности сведены к минимуму. Влажность, температура, содержание хлоридов и кислот pH, а также уровень солей должны контролироваться и сводиться к минимуму.
Влажность, температура, содержание хлоридов и кислот pH, а также уровень солей должны контролироваться и сводиться к минимуму.
Для катодной защиты металл, подверженный риску, должен быть покрыт химически активным металлом, который легче подвергается коррозии. Это может быть гальванизированное цинковое покрытие или подобное. Реакционноспособный металл будет действовать как анод и сначала подвергаться коррозии, предотвращая образование точечной коррозии на подложке.
Для защиты от химического воздействия лучше подходят устойчивые к коррозии металлы, такие как сплавы. Сплавы, содержащие титан, азот, хром и молибден, очень эффективны в средах с высоким содержанием ионов хлора.
Питтинговую коррозию можно контролировать с помощью:
- Использование покрытия, предотвращающего точечную коррозию на металлических поверхностях
- Использование более устойчивых к коррозии материалов
- Обеспечение регулярного смывания жидкостей, контактирующих с материалом защита
- Предотвращение застойных зон
- Использование ингибитора / контроль химического состава жидкости
- Поддержание защитной пленки материала
Подробнее
Точечная коррозия – Википедия
Изучение и оценка точечной коррозии
Различные типы точечной коррозии
Взрыв канализации Гвадалахары из-за точечной коррозии
Точечная коррозия по сравнению с щелевой коррозией является чрезвычайно дорогостоящей проблемой.
 Повреждение трубных систем из-за неконтролируемой коррозии является основной причиной потери прибыли для морских и прибрежных приложений, ежегодно обходясь в миллиарды долларов. Коррозию можно предотвратить, если компании знают, на что обращать внимание, и принимают упреждающие меры для снижения рисков коррозии, пока не стало слишком поздно.
Повреждение трубных систем из-за неконтролируемой коррозии является основной причиной потери прибыли для морских и прибрежных приложений, ежегодно обходясь в миллиарды долларов. Коррозию можно предотвратить, если компании знают, на что обращать внимание, и принимают упреждающие меры для снижения рисков коррозии, пока не стало слишком поздно.
Почти каждый металл, используемый в нашем мире, подвергается коррозии при определенных обстоятельствах. Существуют меры, которые можно предпринять для предотвращения коррозии в нефтегазовой отрасли, особенно на шельфе. Эти шаги требуют фундаментального понимания различных типов коррозии и их причин. Знание того, где искать коррозию, может свести к минимуму риски на нефтяных вышках и нефтеперерабатывающих заводах, существенно сэкономив время и деньги.
Заинтересованы в поиске подходящих материалов для морской и прибрежной среды? Примите меры для борьбы с коррозией с помощью Руководства по выбору материалов Swagelok.
ПОСМОТРЕТЬ РУКОВОДСТВО ПО ВЫБОРУ МАТЕРИАЛОВ
Как возникает коррозия
Коррозия возникает, когда атом металла окисляется жидкостью, что приводит к потере материала на поверхности металла. Возникающие в результате потери материала уменьшают толщину стенок деталей из углеродистых и низколегированных сталей, подверженных общей коррозии, что делает их склонными к механическим повреждениям.
Возникающие в результате потери материала уменьшают толщину стенок деталей из углеродистых и низколегированных сталей, подверженных общей коррозии, что делает их склонными к механическим повреждениям.
Системы металлических труб чаще всего используются для аналитических и технологических контрольно-измерительных приборов, гидравлических линий, а также в системах управления и инженерных сетях. Многие инженерные металлы, используемые в нефтегазовой промышленности, изготавливаются из нержавеющей стали, которая содержит более 10% хрома. Последний способствует образованию оксидного слоя, защищающего металлы от коррозии. Однако коррозия нержавеющей стали возникает, когда условия окружающей среды вызывают разрушение этого слоя.
Почти каждый металл подвергается коррозии при определенных обстоятельствах. Например, ржавчина является часто встречающимся побочным продуктом коррозии углеродистой стали в результате коррозии железа и образования оксида железа. Однако существует много других типов коррозии. Каждый тип представляет собой уникальную угрозу, которую необходимо учитывать при выборе оптимального материала для вашего приложения.
Каждый тип представляет собой уникальную угрозу, которую необходимо учитывать при выборе оптимального материала для вашего приложения.
Определение распространенных типов коррозии
Существует множество типов коррозии, которые могут нанести ущерб нефтегазовым установкам. Многие виды коррозии зависят от химического состава металла и условий эксплуатации. Пока вы читаете дальше, мы сосредоточимся на двух формах локальной коррозии нержавеющей стали: точечной и щелевой коррозии.
Точечная коррозия
Точечная коррозия возникает, когда разрушается защитный оксидный слой на поверхности нержавеющей стали, что приводит к потере электронов металлом под ним в результате окисления в присутствии агрессивного водного раствора. Эта электрохимическая реакция инициирует образование небольших полостей или «ямок».
Хотя эти ямки обычно обнаруживаются при тщательном визуальном осмотре, они могут расти достаточно глубоко, чтобы полностью пробить стенку трубы.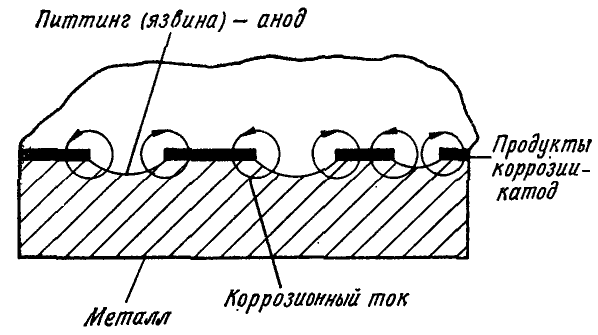 Питтинговая коррозия также может способствовать возникновению трещин в компонентах, подвергающихся растяжению. Окружающая среда с более высокой концентрацией хлоридов, в том числе созданная в результате испарения осажденных капель соленой воды, подвержена точечной коррозии, особенно при высоких температурах.
Питтинговая коррозия также может способствовать возникновению трещин в компонентах, подвергающихся растяжению. Окружающая среда с более высокой концентрацией хлоридов, в том числе созданная в результате испарения осажденных капель соленой воды, подвержена точечной коррозии, особенно при высоких температурах.
При осмотре металлических труб на предмет точечной коррозии ищите красновато-коричневые отложения оксида железа, а также потенциальные ямки, которые могли образоваться на поверхности металла.
Щелевая коррозия
Подобно точечной коррозии, щелевая коррозия начинается с разрушения защитной оксидной пленки нержавеющей стали и продолжается с образованием мелких язв. Однако щелевая коррозия, как следует из названия, происходит не на виду, а в щелях.
В типичной жидкостной системе существуют щели между трубками и трубными опорами или зажимами, между соседними участками труб, а также под грязью и отложениями, которые могут скапливаться на поверхностях. Трещин практически невозможно избежать в трубных установках, а узкие щели представляют собой одну из самых больших опасностей для целостности нержавеющей стали. Щелевая коррозия возникает, когда морская вода диффундирует в щель, что приводит к химически агрессивной среде, в которой ионы, вызывающие коррозию, не могут легко диффундировать из щели. В таком случае вся поверхность внутри щели может подвергаться быстрой коррозии.
Щелевая коррозия возникает, когда морская вода диффундирует в щель, что приводит к химически агрессивной среде, в которой ионы, вызывающие коррозию, не могут легко диффундировать из щели. В таком случае вся поверхность внутри щели может подвергаться быстрой коррозии.
Щелевую коррозию можно наблюдать только визуально, когда с установленной трубки снят хомут. Важно помнить, что щелевая коррозия может возникать при более низких температурах, чем точечная коррозия, потому что требуется меньше усилий для создания «ямки» под геометрической щелью (например, трубным хомутом).
Как предотвратить коррозию
Во многих случаях коррозию можно свести к минимуму путем обучения персонала базовым знаниям о материалах:
Выбор материала: во-первых, рассмотрите выбор материалов для применения в трубках, от самой трубки до трубных опор и зажимов. Трубки из нержавеющей стали типа 316 хорошо работают во многих установках, если они содержатся в чистоте и температура не слишком высока.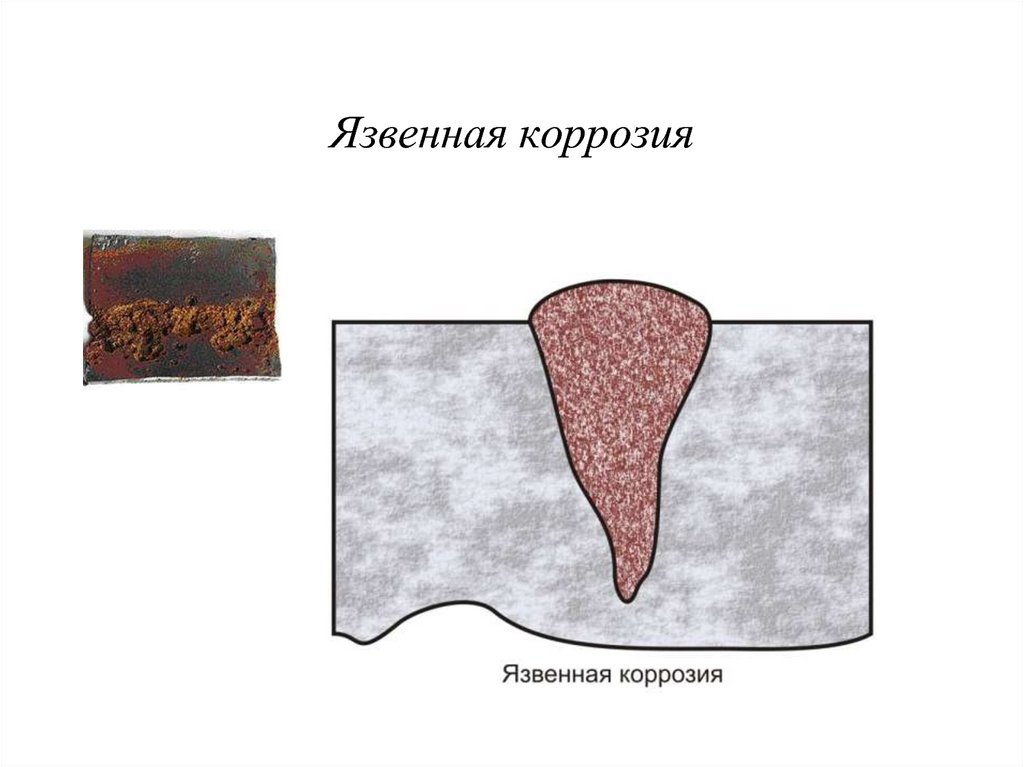 В более теплом климате, особенно в местах, где легко образуются солевые отложения, и в установках, где ржавчина от конструкционных балок и полов из углеродистой стали накапливается на поверхностях из нержавеющей стали, коррозия труб из нержавеющей стали типа 316 наблюдается легче.
В более теплом климате, особенно в местах, где легко образуются солевые отложения, и в установках, где ржавчина от конструкционных балок и полов из углеродистой стали накапливается на поверхностях из нержавеющей стали, коррозия труб из нержавеющей стали типа 316 наблюдается легче.
В этих случаях трубы из супераустенитной (например, 6Mo или 6HN) или супердуплексной (например, 2507) нержавеющей стали обеспечивают гораздо лучшую коррозионную стойкость. Более высокая текучесть и прочность на растяжение супердуплексной нержавеющей стали также упрощают создание систем, которые должны быть рассчитаны на более высокое максимально допустимое рабочее давление (МДРД). Чтобы избежать дорогостоящих ошибок и определить, какой материал подходит для вашего применения, свяжитесь с местным уполномоченным Центр продаж и обслуживания Swagelok для получения рекомендаций по выбору подходящих продуктов и материалов.
Размещение и проектирование: Для предотвращения коррозии необходимы тщательные методы работы системы, чтобы свести к минимуму количество мест, где может возникнуть щелевая коррозия. Один из способов уменьшить щели в трубной системе — избегать размещения трубок непосредственно у стен или друг против друга. При обнаружении щелевой коррозии трубок из нержавеющей стали типа 316 можно заменить трубки типа 316 на более устойчивые к коррозии, которые можно установить с помощью экономичных трубных фитингов типа 316. Компания Swagelok предлагает несколько специально разработанных комбинаций трубных обжимных фитингов из нержавеющей стали типа 316 с трубками из различных коррозионностойких сплавов.
Один из способов уменьшить щели в трубной системе — избегать размещения трубок непосредственно у стен или друг против друга. При обнаружении щелевой коррозии трубок из нержавеющей стали типа 316 можно заменить трубки типа 316 на более устойчивые к коррозии, которые можно установить с помощью экономичных трубных фитингов типа 316. Компания Swagelok предлагает несколько специально разработанных комбинаций трубных обжимных фитингов из нержавеющей стали типа 316 с трубками из различных коррозионностойких сплавов.
Коррозия и обучение материаловедению
Помимо этих простых мер, лучший подход к предотвращению коррозии включает углубленное обучение и внедрение регулярной и надежной программы мониторинга коррозии. Компания Swagelok предлагает курсы по материаловедению, чтобы научить инженеров, технических специалистов и всех, кто участвует в процессе выбора материалов, правильно выбирать коррозионно-стойкие сплавы для жидкостных систем. Базовое понимание коррозии — как она выглядит, где возникает и по каким причинам — среди тех, кто каждый день работает с трубными системами, может предотвратить выход материала из строя и дорогостоящий ремонт. Обратитесь в местный центр продаж и обслуживания Swagelok, чтобы узнать, как программа обучения материаловедению может помочь вашей организации бороться с коррозией.
Обратитесь в местный центр продаж и обслуживания Swagelok, чтобы узнать, как программа обучения материаловедению может помочь вашей организации бороться с коррозией.
УЗНАТЬ БОЛЬШЕ О SWAGELOK МАТЕРИАЛОВЕДЧЕСКИЙ ТРЕНИНГ
Как определить и устранить точечную коррозию
Коррозия — враг металлов всех видов. Этот разрушительный процесс заставляет металлические материалы постепенно ржаветь и разрушаться; и часто он атакует исподтишка, незаметный, пока не будет нанесен ущерб.
Коррозию еще труднее обнаружить и предотвратить, так как она проявляется во многих формах. Одним из них является точечная коррозия, считающаяся одной из самых коварных и разрушительных форм коррозии. Питтинговая коррозия может деформировать металлические поверхности, а также поставить под угрозу их стабильность.
В этом руководстве мы дадим краткий обзор точечной коррозии, что она делает и что ее вызывает. Мы также рассмотрим, как определить и устранить точечную коррозию. Читайте дальше, чтобы узнать больше об этой уникальной форме коррозии и о том, как предотвратить разрушение металлических труб и других компонентов.
Что такое точечная коррозия?
Точечная коррозия, более известная как точечная коррозия, представляет собой тип локальной коррозии, поражающей алюминий, железо, сталь и другие металлические материалы. Для него характерны покрытые ржавчиной полости или ямки, которые он оставляет на поверхности материала. Если ее не остановить, точечная коррозия может навсегда повредить материал и истончить металл, что приведет к разрушительной потере структурной целостности.
Что вызывает точечную коррозию?
Точечная коррозия чаще всего возникает из-за депассивации небольшого участка. Эта небольшая область становится анодом, а окружающая область становится катодом. Это приводит к локальной коррозии.
Но что в первую очередь вызывает депассивацию? Небольшие дефекты, такие как трещины, сколы и царапины! Небольшие царапины на поверхности металла могут показаться не слишком опасными, но эти незначительные потертости могут повредить защитное покрытие металла и свести на нет его пассивность. К наиболее частым причинам точечной коррозии относятся:
К наиболее частым причинам точечной коррозии относятся:
- Трещины
- Царапины
- Чипсы
- Неравномерное напряжение
- Дефектная металлическая подложка
- Воздействие турбулентной жидкости
- Неоднородное защитное покрытие
- Химические атаки
Итак, если ваш металл каким-либо образом поврежден или подвергся воздействию неспокойной воды, внимательно следите за точечной коррозией. Другой потенциальной причиной питтинга является дифференциальная аэрация. Когда металл, за которым плохо ухаживают, подвергается воздействию воды или частиц пыли, небольшая площадь становится бескислородной. Это вызывает разницу в аэрации между ним и окружающей территорией. Происходит реакция, и на поверхности металла образуются ржавые ямки.
Как распознать точечную коррозию
Многие считают точечную коррозию одной из самых опасных форм коррозии из-за сложности ее прогнозирования, обнаружения и предотвращения. Вы можете подумать: «Подождите, поскольку он создает ямки на поверхности металла, разве его не должно быть легко обнаружить?» К сожалению, ямы, которые он создает, невероятно малы. Большинство из них невидимы (или почти невидимы) для человеческого глаза. Они также обычно покрыты слоем коррозии, из-за чего их еще труднее обнаружить.
Вы можете подумать: «Подождите, поскольку он создает ямки на поверхности металла, разве его не должно быть легко обнаружить?» К сожалению, ямы, которые он создает, невероятно малы. Большинство из них невидимы (или почти невидимы) для человеческого глаза. Они также обычно покрыты слоем коррозии, из-за чего их еще труднее обнаружить.
Хотя обнаружить точечную коррозию невооруженным глазом практически невозможно, существует надежных способов проверить ее. Тестирование может предотвратить разрушение точечной коррозии, поэтому мы рекомендуем часто тестировать восприимчивые материалы. Общие методы проверки на точечную коррозию включают:
Визуальный осмотр
С помощью микроскопа профессионал подсчитает количество язв в данной области. Это помогает им определить их размер и распределение, а также интенсивность.
Акустические испытания
Во время акустических испытаний ультразвуковая энергия передается на металл через связующее вещество. Эти ультразвуковые импульсы отражаются от металла и преобразуются в электрические сигналы. Эти сигналы покажут расположение ямок и других дефектов в металле.
Эти сигналы покажут расположение ямок и других дефектов в металле.
Электромагнитные испытания
Этот метод испытаний используется для обнаружения неровностей на поверхности проводящих металлов, таких как сталь и железо.
Электрохимические испытания
Электрохимические испытания — еще один способ проверить скорость коррозии металлов. Во время испытания на рабочий электрод из металла подается электрический ток для создания измеряемых сигналов.
Испытание на погружение
Кусок металла погружают в раствор. Остается постоять несколько дней. После удаления измеряют скорость коррозии, а язвы исследуют под микроскопом для дальнейшего определения масштаба и интенсивности.
Какие материалы подвергаются наибольшему риску?
Материалы, содержащие ионы бромида, хлорида или гипохлорита, наиболее подвержены точечной коррозии. Материалы, подвергшиеся воздействию растворов, содержащих фториды или йодиты (например, вода или сульфиды), также подвергаются повышенному риску. Некоторые металлы, склонные к точечной коррозии:
Некоторые металлы, склонные к точечной коррозии:
- Хром
- Нержавеющая сталь
- Меркурий
- Кобальт
- Алюминий
- Медь
Предотвращение щелевой коррозии
В дополнение к знанию того, как определить и устранить точечную коррозию, вы, вероятно, в первую очередь захотите узнать, как предотвратить точечную коррозию. Есть несколько способов минимизировать риск питтинга.
Использование коррозионно-стойких материалов является одной из первых профилактических мер. Сплавы, содержащие титан, азот, хром и молибден, хорошо сопротивляются точечной коррозии. Другим эффективным методом профилактики является катодная защита, которая предотвращает коррозию, превращая металлическую поверхность в электрохимическую ячейку. В идеале вы должны покрыть материал более активным металлом. Этот коррозионно-активный металл будет действовать как анод и подвергаться коррозии вместо исходного металла, предотвращая точечную коррозию.
Еще одним из наиболее эффективных способов предотвращения точечной коррозии является контроль факторов окружающей среды (влажность, температура, содержание хлоридов, кислот pH и уровень солей) в меру своих возможностей. Другие методы предотвращения точечной коррозии включают использование и уход за защитным покрытием и контроль воздействия жидкости и пыли.
Можно ли удалить точечную коррозию?
Возможно, вам будет приятно узнать, что, в отличие от большинства форм коррозии, точечная коррозия поддается устранению. Предполагая, что металл все еще структурно прочный, вы можете удалить коррозию с помощью мягкой кислоты. Если вы хотите удалить настоящую точечную коррозию, вам нужно отшлифовать, соскрести или подвергнуть пескоструйной очистке металл. Вы также можете удалить питтинг механическим способом.
Когда коррозия и точечная коррозия исчезнут, вы можете загрунтовать металл, используя один из следующих методов покрытия:
- Цинк-фосфатное грунтование
- Металлизация цинковым напылением
- Химическое покрытие
- Горячее погружение
Ищете способы предотвратить точечную коррозию? Специалисты Dreym Engineering могут помочь! Мы предлагаем тест на коррозионную активность почвы для измерения коррозионной активности почвы, в которой закопаны ваши металлические компоненты. Мы также разрабатываем и устанавливаем системы катодной защиты, чтобы еще больше снизить риск точечной коррозии. Свяжитесь с нами сегодня, чтобы узнать больше о наших услугах по предотвращению коррозии или запланировать консультацию.
Мы также разрабатываем и устанавливаем системы катодной защиты, чтобы еще больше снизить риск точечной коррозии. Свяжитесь с нами сегодня, чтобы узнать больше о наших услугах по предотвращению коррозии или запланировать консультацию.
404 — СТРАНИЦА НЕ НАЙДЕНА
Почему я вижу эту страницу?
404 означает, что файл не найден. Если вы уже загрузили файл, имя может быть написано с ошибкой или файл находится в другой папке.
Другие возможные причины
Вы можете получить ошибку 404 для изображений, поскольку у вас включена защита от горячих ссылок, а домен отсутствует в списке авторизованных доменов.
Если вы перейдете по временному URL-адресу (http://ip/~username/) и получите эту ошибку, возможно, проблема связана с набором правил, хранящимся в файле .htaccess. Вы можете попробовать переименовать этот файл в .htaccess-backup и обновить сайт, чтобы посмотреть, решит ли это проблему.
Также возможно, что вы непреднамеренно удалили корневую папку документа или ваша учетная запись должна быть создана заново. В любом случае, пожалуйста, немедленно свяжитесь с вашим веб-хостингом.
В любом случае, пожалуйста, немедленно свяжитесь с вашим веб-хостингом.
Вы используете WordPress? См. Раздел об ошибках 404 после перехода по ссылке в WordPress.
Как найти правильное написание и папку
Отсутствующие или поврежденные файлы
Когда вы получаете ошибку 404, обязательно проверьте URL-адрес, который вы пытаетесь использовать в своем браузере. Это сообщает серверу, какой ресурс он должен использовать попытка запроса.
http://example.com/example/Example/help.html
В этом примере файл должен находиться в папке public_html/example/Example/
Обратите внимание, что CaSe важен в этом примере. На платформах с учетом регистра e xample и E xample не совпадают.
Для дополнительных доменов файл должен находиться в папке public_html/addondomain.com/example/Example/, а имена чувствительны к регистру.
Разбитое изображение
Если на вашем сайте отсутствует изображение, вы можете увидеть на своей странице поле с красным размером X , где отсутствует изображение. Щелкните правой кнопкой мыши на X и выберите «Свойства». Свойства сообщат вам путь и имя файла, который не может быть найден.
Щелкните правой кнопкой мыши на X и выберите «Свойства». Свойства сообщат вам путь и имя файла, который не может быть найден.
Это зависит от браузера, если вы не видите на своей странице поле с красным X , попробуйте щелкнуть правой кнопкой мыши на странице, затем выберите «Просмотр информации о странице» и перейдите на вкладку «Мультимедиа».
http://example.com/cgi-sys/images/banner.PNG
В этом примере файл изображения должен находиться в папке public_html/cgi-sys/images/
Обратите внимание, что в этом примере важен CaSe . На платформах с учетом регистра символов PNG и png не совпадают.
Ошибки 404 после перехода по ссылкам WordPress
При работе с WordPress ошибки 404 Page Not Found часто могут возникать при активации новой темы или изменении правил перезаписи в файле .htaccess.
Когда вы сталкиваетесь с ошибкой 404 в WordPress, у вас есть два варианта ее исправления.
Вариант 1. Исправьте постоянные ссылки
- Войдите в WordPress.
- В меню навигации слева в WordPress нажмите Настройки > Постоянные ссылки (Обратите внимание на текущую настройку. Если вы используете пользовательскую структуру, скопируйте или сохраните ее где-нибудь.)
- Выберите По умолчанию .
- Нажмите Сохранить настройки .
- Верните настройки к предыдущей конфигурации (до того, как вы выбрали «По умолчанию»). Верните пользовательскую структуру, если она у вас была.
- Нажмите Сохранить настройки .
Во многих случаях это сбросит постоянные ссылки и устранит проблему. Если это не сработает, вам может потребоваться отредактировать файл .htaccess напрямую.
Вариант 2. Измените файл .htaccess
Добавьте следующий фрагмент кода 9index.php$ — [L]
RewriteCond %{REQUEST_FILENAME} !-f
RewriteCond %{REQUEST_FILENAME} !-d
RewriteRule .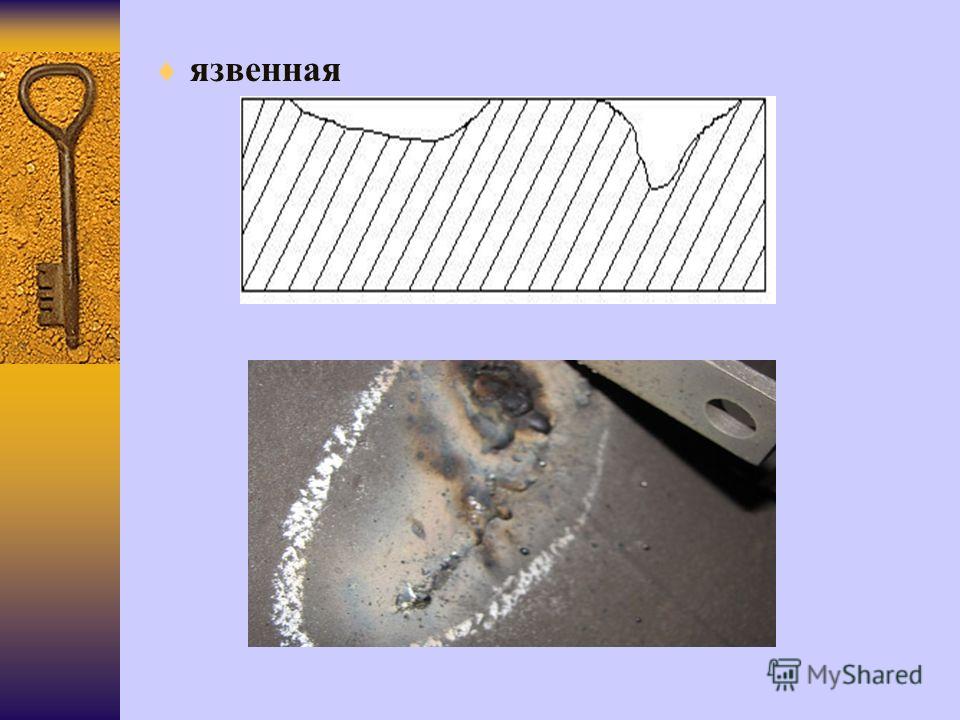 /index.php [L]
/index.php [L]
# Конец WordPress
Если ваш блог показывает неправильное доменное имя в ссылках, перенаправляет на другой сайт или отсутствуют изображения и стиль, все это обычно связано с одной и той же проблемой: в вашем блоге WordPress настроено неправильное доменное имя.
Как изменить файл .htaccess
Файл .htaccess содержит директивы (инструкции), которые сообщают серверу, как вести себя в определенных сценариях, и напрямую влияют на работу вашего веб-сайта.
Перенаправление и перезапись URL-адресов — это две очень распространенные директивы, которые можно найти в файле .htaccess, и многие скрипты, такие как WordPress, Drupal, Joomla и Magento, добавляют директивы в .htaccess, чтобы эти скрипты могли работать.
Возможно, вам потребуется отредактировать файл .htaccess в какой-то момент по разным причинам. В этом разделе рассказывается, как редактировать файл в cPanel, но не о том, что нужно изменить. статьи и ресурсы для этой информации. )
)
Существует множество способов редактирования файла .htaccess
- Отредактируйте файл на своем компьютере и загрузите его на сервер через FTP
- Использовать режим редактирования программы FTP
- Использовать SSH и текстовый редактор
- Используйте файловый менеджер в cPanel
Самый простой способ отредактировать файл .htaccess для большинства людей — через диспетчер файлов в cPanel.
Как редактировать файлы .htaccess в файловом менеджере cPanel
Прежде чем что-либо делать, рекомендуется сделать резервную копию вашего веб-сайта, чтобы вы могли вернуться к предыдущей версии, если что-то пойдет не так.
Откройте файловый менеджер
- Войдите в cPanel.
- В разделе «Файлы» щелкните значок «Диспетчер файлов ».
- Установите флажок для Корень документа для и выберите доменное имя, к которому вы хотите получить доступ, в раскрывающемся меню.

- Убедитесь, что установлен флажок Показать скрытые файлы (dotfiles) «.
- Нажмите Перейти . Файловый менеджер откроется в новой вкладке или окне.
- Найдите файл .htaccess в списке файлов. Возможно, вам придется прокрутить, чтобы найти его.
Для редактирования файла .htaccess
- Щелкните правой кнопкой мыши файл .htaccess и выберите Редактировать код в меню. Кроме того, вы можете щелкнуть значок файла .htaccess, а затем 9Значок 0089 Code Editor вверху страницы.
- Может появиться диалоговое окно с вопросом о кодировании. Просто нажмите Изменить , чтобы продолжить. Редактор откроется в новом окне.
- При необходимости отредактируйте файл.
- Нажмите Сохранить изменения в правом верхнем углу, когда закончите. Изменения будут сохранены.
- Протестируйте свой веб-сайт, чтобы убедиться, что ваши изменения были успешно сохранены.
 Если нет, исправьте ошибку или вернитесь к предыдущей версии, пока ваш сайт снова не заработает.
Если нет, исправьте ошибку или вернитесь к предыдущей версии, пока ваш сайт снова не заработает. - После завершения нажмите Закрыть , чтобы закрыть окно диспетчера файлов.
Прямое наблюдение развития точечной коррозии на поверхностях углеродистой стали в масштабах от нано до микромасштабов
Реферат
Вызванная Cl − коррозия металлов и сплавов имеет отношение к широкому спектру инженерных материалов, конструкций и системы. Из-за проблем с изучением точечной коррозии количественным и статистически значимым образом ее кинетика остается плохо изученной. Здесь путем прямых наблюдений от нано- до микромасштаба с использованием вертикальной сканирующей интерферометрии (VSI) мы изучаем временную эволюцию точечной коррозии на углеродистой стали AISI 1045 на больших площадях поверхности в Cl 9.0091--свободные и Cl —-обогащенные растворы. Особое внимание уделяется изучению зарождения и роста ямок и связанного с этим образования шероховатых областей на стальных поверхностях. При статистическом анализе сотен отдельных ямок количественно выделяют три стадии питтинговой коррозии: индукцию, распространение и насыщение. Путем количественной оценки кинетики этих процессов мы контекстуализируем наше текущее понимание электрохимической коррозии в рамках, учитывающих эволюцию пространственной динамики и морфологии. В присутствии Cl − , коррозия сильно ускоряется из-за множества автокаталитических факторов, включая дестабилизацию защитной поверхностной оксидной пленки и сохранение агрессивной микросреды внутри ямок, оба из которых способствуют дальнейшему зарождению и росту ямок. Эти результаты дают новое представление о прогнозировании и моделировании процессов коррозии стали в водной среде со средним значением pH.
При статистическом анализе сотен отдельных ямок количественно выделяют три стадии питтинговой коррозии: индукцию, распространение и насыщение. Путем количественной оценки кинетики этих процессов мы контекстуализируем наше текущее понимание электрохимической коррозии в рамках, учитывающих эволюцию пространственной динамики и морфологии. В присутствии Cl − , коррозия сильно ускоряется из-за множества автокаталитических факторов, включая дестабилизацию защитной поверхностной оксидной пленки и сохранение агрессивной микросреды внутри ямок, оба из которых способствуют дальнейшему зарождению и росту ямок. Эти результаты дают новое представление о прогнозировании и моделировании процессов коррозии стали в водной среде со средним значением pH.
Введение
Точечная коррозия представляет собой повреждающую форму локальной коррозии металлов, которая является предметом исследований в течение нескольких десятилетий 1,2 . Несмотря на то, что на образование ямок расходуется относительно небольшое количество (масса) материала, роль ямок в качестве мест дефектов для зарождения трещин и продолжающейся коррозии может быть значительной 3,4 . Кроме того, хорошо известно, что ионы галогенидов, такие как хлорид (Cl — ), ускоряют точечную коррозию сплавов, таких как сталь 5,6,7 . Было предложено множество механизмов для объяснения возникновения питтинговой коррозии в присутствии Cl — , которая включает разрушение поверхностной пленки окисления/пассивации в результате процессов, включающих: проникновение Cl − видов через пленку, а также адсорбция ионов и локальное истончение, что в конечном итоге приводит к разрушению пленки 2,8 .
Кроме того, хорошо известно, что ионы галогенидов, такие как хлорид (Cl — ), ускоряют точечную коррозию сплавов, таких как сталь 5,6,7 . Было предложено множество механизмов для объяснения возникновения питтинговой коррозии в присутствии Cl — , которая включает разрушение поверхностной пленки окисления/пассивации в результате процессов, включающих: проникновение Cl − видов через пленку, а также адсорбция ионов и локальное истончение, что в конечном итоге приводит к разрушению пленки 2,8 .
Однако возникновение и развитие точечной коррозии трудно количественно изучить по ряду причин. Во-первых, небольшой размер ямок затрудняет их обнаружение, особенно на ранних стадиях питтинга, когда ямки имеют диаметр ≤20 мкм и глубину всего несколько десятков нанометров 9,10,11 . Во-вторых, ямки могут быть скрыты продуктами коррозии, которые могут образовываться (одновременно с ямками) на металлических поверхностях 11,12,13 . В то время как электрохимические исследования могут быть применены для изучения точечной коррозии – эти подходы оценивают только объемное («среднее») поведение – без возможности разрешения микромасштабных особенностей 2,14,15,16 . Совсем недавно электрохимическая сканирующая туннельная микроскопия (ECSTM) использовалась для изучения удаления оксидного слоя и возникновения питтинговой коррозии на металлических поверхностях 17,18 , тогда как атомно-силовая микроскопия (АСМ) 19 использовалась для наблюдения за морфологией одиночных ямок. . Эти методы позволили получить ценную информацию о росте ямок, не прибегая к каким-либо предположениям относительно активной площади питтинговых участков или относительно текущей плотности одиночных ямок 9.0091 8 . Однако ECSTM может исследовать только небольшое поле зрения (FOV) порядка нескольких квадратных микрон, тогда как AFM не может отображать острые и глубокие ямки (> 10 мкм) из-за его ограниченного вертикального диапазона.
В то время как электрохимические исследования могут быть применены для изучения точечной коррозии – эти подходы оценивают только объемное («среднее») поведение – без возможности разрешения микромасштабных особенностей 2,14,15,16 . Совсем недавно электрохимическая сканирующая туннельная микроскопия (ECSTM) использовалась для изучения удаления оксидного слоя и возникновения питтинговой коррозии на металлических поверхностях 17,18 , тогда как атомно-силовая микроскопия (АСМ) 19 использовалась для наблюдения за морфологией одиночных ямок. . Эти методы позволили получить ценную информацию о росте ямок, не прибегая к каким-либо предположениям относительно активной площади питтинговых участков или относительно текущей плотности одиночных ямок 9.0091 8 . Однако ECSTM может исследовать только небольшое поле зрения (FOV) порядка нескольких квадратных микрон, тогда как AFM не может отображать острые и глубокие ямки (> 10 мкм) из-за его ограниченного вертикального диапазона. Совсем недавно аппарат электрохимических поверхностных сил (EC-SFA) использовался для устранения очагов коррозии в замкнутых пространствах in situ и в присутствии ионов Cl — и приложенного потенциала, хотя и с ограничениями по характеру геометрии. можно проверить 20 .
Совсем недавно аппарат электрохимических поверхностных сил (EC-SFA) использовался для устранения очагов коррозии в замкнутых пространствах in situ и в присутствии ионов Cl — и приложенного потенциала, хотя и с ограничениями по характеру геометрии. можно проверить 20 .
Чтобы преодолеть эти ограничения, интерферометрия с вертикальным сканированием (VSI) впервые используется для изучения возникновения и развития точечной коррозии. Вкратце, VSI использует интерференцию света с короткими длинами когерентности для оценки топографии поверхности. Таким образом, достигается вертикальный диапазон до нескольких миллиметров, который может быть отобран с субнанометровым вертикальным разрешением и субмикронным латеральным разрешением. Это позволяет обнаруживать ямки от их зарождения до зрелости. Кроме того, для получения статистически достоверных данных несколько изображений могут быть объединены в мозаику для создания составных изображений, представляющих выборочные области площадью до десятков квадратных миллиметров. Эти возможности позволяют наблюдать за зарождением и распространением ямок с непревзойденным разрешением на репрезентативных участках поверхности, охватывающих тысячи отдельных ямок. Таким образом, это исследование однозначно проливает свет на новые представления о кинетике и механизмах точечной коррозии в (среднеуглеродистых) углеродистых сталях. Хотя электрохимические свойства этого материала в присутствии различных реакционных растворов хорошо изучены 21,22,23 , эволюция топографии их поверхностей гораздо меньше отслеживалась и количественно анализировалась. Чтобы продемонстрировать этот новый подход к исследованию точечной коррозии, сталь AISI 1045 была подвергнута воздействию деионизированной (DI) воды и растворов, содержащих Cl — , чтобы получить количественное представление об эволюции морфологии поверхности по мере развития коррозии и выяснить влияние водного раствора Cl — вида по усилению коррозионной активности.
Эти возможности позволяют наблюдать за зарождением и распространением ямок с непревзойденным разрешением на репрезентативных участках поверхности, охватывающих тысячи отдельных ямок. Таким образом, это исследование однозначно проливает свет на новые представления о кинетике и механизмах точечной коррозии в (среднеуглеродистых) углеродистых сталях. Хотя электрохимические свойства этого материала в присутствии различных реакционных растворов хорошо изучены 21,22,23 , эволюция топографии их поверхностей гораздо меньше отслеживалась и количественно анализировалась. Чтобы продемонстрировать этот новый подход к исследованию точечной коррозии, сталь AISI 1045 была подвергнута воздействию деионизированной (DI) воды и растворов, содержащих Cl — , чтобы получить количественное представление об эволюции морфологии поверхности по мере развития коррозии и выяснить влияние водного раствора Cl — вида по усилению коррозионной активности.
Результаты и обсуждение
Гетерогенная коррозия поверхностей из стали AISI 1045
Тщательное изучение данных трехмерной топографии, полученных с помощью VSI, выявило крайне неоднородное, то есть гетерогенное, развитие коррозии как в деионизированной (DI) воде, так и в 100 мМ растворах NaCl. Деградация поверхности происходила за счет зарождения, накопления и роста коррозионных язв. Для количественного изучения неоднородности коррозии разность высот реагирующих поверхностей рассчитывалась попиксельно относительно непрореагировавшей t 0 поверхность, через каждое временное поле зрения. Затем частотное распределение перепадов высоты отслеживалось во времени, как показано на рис. 1. Следует отметить, что отрицательные и положительные перепады высот указывают либо на чистое удаление, либо на чистое отложение материала на поверхность соответственно. По мере развития коррозии становятся очевидными отчетливые изменения в этих распределениях. Как и следовало ожидать, при t 0 распределение характеризовалось острым пиком с центром на 0 мкм. Этот «пик» сохранялся даже в более поздние времена, указывая на то, что большая часть поверхности имеет в основном однородную, неизменную топографию по всему полю зрения и что только локализованные области на поверхности (т.
Деградация поверхности происходила за счет зарождения, накопления и роста коррозионных язв. Для количественного изучения неоднородности коррозии разность высот реагирующих поверхностей рассчитывалась попиксельно относительно непрореагировавшей t 0 поверхность, через каждое временное поле зрения. Затем частотное распределение перепадов высоты отслеживалось во времени, как показано на рис. 1. Следует отметить, что отрицательные и положительные перепады высот указывают либо на чистое удаление, либо на чистое отложение материала на поверхность соответственно. По мере развития коррозии становятся очевидными отчетливые изменения в этих распределениях. Как и следовало ожидать, при t 0 распределение характеризовалось острым пиком с центром на 0 мкм. Этот «пик» сохранялся даже в более поздние времена, указывая на то, что большая часть поверхности имеет в основном однородную, неизменную топографию по всему полю зрения и что только локализованные области на поверхности (т. е. охватывающие менее 1% всех пикселей) демонстрируют существенные изменения. которые характерны для образования ямок 8 .
е. охватывающие менее 1% всех пикселей) демонстрируют существенные изменения. которые характерны для образования ямок 8 .
Рисунок 1
Типичные частотные диаграммы, показывающие распределение разности высот в разных местах пикселей для стали AISI 1045, реагирующей с: (a) деионизированной водой и (b) 100 мМ раствором NaCl. Разница высот рассчитывается путем вычитания высот в заданном (x , y) местоположении в соответствующие моменты времени, указанные в легенде, из высоты t = 0 h. Таким образом, отрицательные перепады высоты указывают на потерю массы (например, образование ямок и шероховатость поверхности), а положительные перепады высот указывают на отложение продуктов коррозии. (c) и (d) представляют собой распределения в диапазоне высот от -5 до 5 мкм, показывающие более подробно соответствующие распределения высот в (a) и (b) .
Изображение в полный размер
Эволюция высоты поверхности в деионизированной воде и в 100 мМ растворах NaCl различна, как показано на рис. 1. В деионизированной воде коррозия связана в первую очередь с углублением локализованных «низкочастотного хвоста», показанного на рис. 1 (а). Наибольшее измеренное отступание поверхности, которое затронуло примерно 0,001% всех пикселей или, что эквивалентно, 0,001% площади поверхности, составило около 10 мкм после примерно 10,2 ч реакции (рис. 1а). С другой стороны, в присутствии 100 мМ NaCl широко распространенное скопление локализованных ямок глубиной до 5 мкм привело к развитию вторичного пика с центром на Δ ч ≈ -2 мкм всего через 0,33 ч контакта с раствором. Со временем этот вторичный пик стал неотличим от начального пика, предполагая, что в целом происходило быстрое зарождение и рост ямок до тех пор, пока вся стальная поверхность не была обширно покрыта ямками, как показано ниже. Красные стрелки на (рис. 1b, d) указывают на смещение положения основного пика, предполагая, что коррозия привела к общему отступлению поверхности порядка 0,7 мкм примерно через 3,7 ч в присутствии NaCl.
1. В деионизированной воде коррозия связана в первую очередь с углублением локализованных «низкочастотного хвоста», показанного на рис. 1 (а). Наибольшее измеренное отступание поверхности, которое затронуло примерно 0,001% всех пикселей или, что эквивалентно, 0,001% площади поверхности, составило около 10 мкм после примерно 10,2 ч реакции (рис. 1а). С другой стороны, в присутствии 100 мМ NaCl широко распространенное скопление локализованных ямок глубиной до 5 мкм привело к развитию вторичного пика с центром на Δ ч ≈ -2 мкм всего через 0,33 ч контакта с раствором. Со временем этот вторичный пик стал неотличим от начального пика, предполагая, что в целом происходило быстрое зарождение и рост ямок до тех пор, пока вся стальная поверхность не была обширно покрыта ямками, как показано ниже. Красные стрелки на (рис. 1b, d) указывают на смещение положения основного пика, предполагая, что коррозия привела к общему отступлению поверхности порядка 0,7 мкм примерно через 3,7 ч в присутствии NaCl. В свою очередь, среднее уменьшение высоты поверхности, которое можно связать с величиной потери массы, существенно больше в присутствии водного Cl − , чем в деионизированной воде.
В свою очередь, среднее уменьшение высоты поверхности, которое можно связать с величиной потери массы, существенно больше в присутствии водного Cl − , чем в деионизированной воде.
Процесс коррозии сопровождается образованием продуктов коррозии. В деионизированной воде одновременно с точечной коррозией наблюдалось в целом однородное увеличение высоты примерно на 3 мкм примерно на 0,1% площади изображения, что указывает на образование и рост поверхностного слоя продуктов коррозии. Анализы, проведенные с использованием µ-рамановской спектроскопии и энергодисперсионной рентгеновской спектроскопии (SEM-EDS), идентифицировали эти продукты коррозии как состоящие из лепидокрокита (γ-FeOOH), гетита (α-FeOOH) и оксидов железа гематита (Fe 2 O 3 ) и магнетит (Fe 3 O 4 ) 24,25 . С другой стороны, при воздействии 100 мМ NaCl частотное распределение изменения высоты поверхности имеет длинный хвост, означающий увеличение высоты до> 20 мкм после 3,7 ч воздействия раствора (рис. 1b). Это указывает на существенное образование продуктов коррозии на стали AISI 1045, реагирующей с растворами, содержащими Cl − , что согласуется с предыдущими наблюдениями 26 . Действительно, данные о составе, полученные с помощью µ-рамановской спектроскопии, указывают на присутствие лепидокрокита и акагенита (β-FeOOH) на стали AISI 1045, подвергнутой воздействию как 10 мМ, так и 100 мМ NaCl после 24 часов контакта с раствором (см. рис. S1), что соответствует предыдущие отчеты 27,28,29 . Следует отметить, что наблюдаемое увеличение высоты в присутствии Cl — также локализовано, и только на небольшой части поверхности (0,02% площади) наблюдается увеличение от 10 до 20 мкм. Конкретные особенности поверхности, связанные с этими частотными распределениями, дополнительно обсуждаются ниже.
1b). Это указывает на существенное образование продуктов коррозии на стали AISI 1045, реагирующей с растворами, содержащими Cl − , что согласуется с предыдущими наблюдениями 26 . Действительно, данные о составе, полученные с помощью µ-рамановской спектроскопии, указывают на присутствие лепидокрокита и акагенита (β-FeOOH) на стали AISI 1045, подвергнутой воздействию как 10 мМ, так и 100 мМ NaCl после 24 часов контакта с раствором (см. рис. S1), что соответствует предыдущие отчеты 27,28,29 . Следует отметить, что наблюдаемое увеличение высоты в присутствии Cl — также локализовано, и только на небольшой части поверхности (0,02% площади) наблюдается увеличение от 10 до 20 мкм. Конкретные особенности поверхности, связанные с этими частотными распределениями, дополнительно обсуждаются ниже.
Крайне локализованный характер коррозионных реакций показан на рисунках 2–3, которые представляют собой большие поля зрения 1000 мкм × 1000 мкм. Для ясности данные топографии поверхности представлены вместе с соответствующей картой градиента, что помогает идентифицировать особенности высокого склона, такие как участки питтинга. В целом, как в деионизированной воде, так и в 100 мМ растворе NaCl ямки зарождались по мере огрубления поверхности. В то время как образование ямок и огрубение поверхности протекали сходным образом как в деионизированной воде, так и в растворах NaCl, ожидаемо, что в последнем случае протекание реакций сильно ускоряется. В деионизированной воде начальный период примерно до 1,7 ч характеризуется отсутствием значительных изменений в морфологии поверхности, как показано на рис. 2(а). После этого момента зарождение ямок сопровождается значительным огрублением поверхности вблизи участков питтинга (например, см. рис. 2b, c, f, g). Этот начальный период зародышеобразования представляет собой время, необходимое для установления критического локального кислого pH, вызывающего питтинг 9.0091 30 . Такое зарождение ямок провоцируется током пассивного растворения, вызывающим локальные нестабильности в микроструктуре поверхности сплава 30 . Примечательно, что по мере развития коррозии новые ямки образуются преимущественно в пределах изначально шероховатой/дестабилизированной области (например, см.
В целом, как в деионизированной воде, так и в 100 мМ растворе NaCl ямки зарождались по мере огрубления поверхности. В то время как образование ямок и огрубение поверхности протекали сходным образом как в деионизированной воде, так и в растворах NaCl, ожидаемо, что в последнем случае протекание реакций сильно ускоряется. В деионизированной воде начальный период примерно до 1,7 ч характеризуется отсутствием значительных изменений в морфологии поверхности, как показано на рис. 2(а). После этого момента зарождение ямок сопровождается значительным огрублением поверхности вблизи участков питтинга (например, см. рис. 2b, c, f, g). Этот начальный период зародышеобразования представляет собой время, необходимое для установления критического локального кислого pH, вызывающего питтинг 9.0091 30 . Такое зарождение ямок провоцируется током пассивного растворения, вызывающим локальные нестабильности в микроструктуре поверхности сплава 30 . Примечательно, что по мере развития коррозии новые ямки образуются преимущественно в пределах изначально шероховатой/дестабилизированной области (например, см.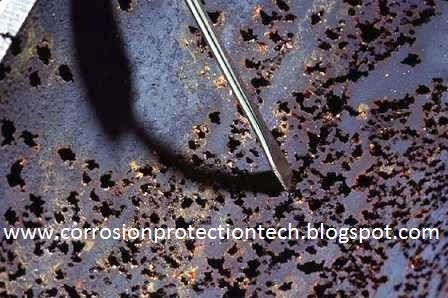 рис. 2d,h), которые напоминают «круглый бассейн»; из-за локального подкисления в результате потребления кислорода внутри карьеров в этих зонах 31,32 . Постулируется, что образование этих круглых бассейнов глубиной от 100 до 200 нм по отношению к некорродированной поверхности происходит из-за (эффективного) 1/r 2 Масштабирование плотности тока коррозии, которая распространяется от геометрического центра круглого резервуара(ов) к нешероховатым (некорродированным) местам на стальной поверхности. Эти процессы зарождения ямок, шероховатости и образования ямок вокруг участков ямок, а также роста и разрастания ямок со временем привели к тому, что стальная поверхность демонстрировала явное обесцвечивание, характерное для «ржавчины».
рис. 2d,h), которые напоминают «круглый бассейн»; из-за локального подкисления в результате потребления кислорода внутри карьеров в этих зонах 31,32 . Постулируется, что образование этих круглых бассейнов глубиной от 100 до 200 нм по отношению к некорродированной поверхности происходит из-за (эффективного) 1/r 2 Масштабирование плотности тока коррозии, которая распространяется от геометрического центра круглого резервуара(ов) к нешероховатым (некорродированным) местам на стальной поверхности. Эти процессы зарождения ямок, шероховатости и образования ямок вокруг участков ямок, а также роста и разрастания ямок со временем привели к тому, что стальная поверхность демонстрировала явное обесцвечивание, характерное для «ржавчины».
Рисунок 2
Репрезентативные иллюстрации изменения высоты стальной поверхности после воздействия деионизированной воды после: (а) 1,7 ч, (б) 2,2 з, (в) 2,7 з, (г) 3,7 з. Соответствующие карты градиента показаны в: (e) до (h) соответственно. Места питтинга не проявлялись до t = 1,7 ч, как показано в (a) и (e) . По истечении этого времени ямки зарождаются, как показано на (b , f) , а затем продолжают расти с одновременным огрублением поверхности (c , d , g , h) 906:30 . Новые ямки образовались вокруг первоначально стабилизированных ямок, которые часто изолированы, как видно из (c) и (g) . Рис. 3 0,7 ч, (г) 3,7 ч. Соответствующие карты градиента показаны в (e) до (h) соответственно. Окончание «периода покоя» знаменуется развитием круглых бассейнов вокруг первоначально образовавшейся изолированной ямы 9.0632 (б , ф) . Вначале в этих бассейнах наблюдается значительное зарождение и рост ямок, после чего образование ямок происходит почти равномерно по всей поверхности (d , h) .
Соответствующие карты градиента показаны в: (e) до (h) соответственно. Места питтинга не проявлялись до t = 1,7 ч, как показано в (a) и (e) . По истечении этого времени ямки зарождаются, как показано на (b , f) , а затем продолжают расти с одновременным огрублением поверхности (c , d , g , h) 906:30 . Новые ямки образовались вокруг первоначально стабилизированных ямок, которые часто изолированы, как видно из (c) и (g) . Рис. 3 0,7 ч, (г) 3,7 ч. Соответствующие карты градиента показаны в (e) до (h) соответственно. Окончание «периода покоя» знаменуется развитием круглых бассейнов вокруг первоначально образовавшейся изолированной ямы 9.0632 (б , ф) . Вначале в этих бассейнах наблюдается значительное зарождение и рост ямок, после чего образование ямок происходит почти равномерно по всей поверхности (d , h) .
Изображение в полный размер
Коррозия – хотя и ускоренная, но имеет сходную динамику – в стали, подвергшейся воздействию 100 мМ раствора NaCl, как показано на рис. 3. Ожидаемо, что коррозия протекает намного быстрее в присутствии водного раствора Cl − со значительным сокращение времени до зарождения ямки, образования впадины и роста ямки (и впадины) (рис. S2). Например, в течение 0,2 часа воздействия вокруг первоначально образовавшихся изолированных ямок (см. рис. 3b) наблюдаются отчетливые круглые бассейны глубиной порядка 100-200 нм (см. рис. 3b), аналогичные тем, которые образовались в деионизированной воде, как описано выше. Внутри этих бассейнов зарождаются новые ямки (рис. 3б, е), и, кроме того, ямки наблюдаются за пределами районов бассейнов после более длительных периодов Cl 9.0091 − экспозиция (рис. 3в,ж). Этот характер обширных поверхностных изъязвлений не наблюдался в деионизированной воде даже после > 10 часов воздействия.
3. Ожидаемо, что коррозия протекает намного быстрее в присутствии водного раствора Cl − со значительным сокращение времени до зарождения ямки, образования впадины и роста ямки (и впадины) (рис. S2). Например, в течение 0,2 часа воздействия вокруг первоначально образовавшихся изолированных ямок (см. рис. 3b) наблюдаются отчетливые круглые бассейны глубиной порядка 100-200 нм (см. рис. 3b), аналогичные тем, которые образовались в деионизированной воде, как описано выше. Внутри этих бассейнов зарождаются новые ямки (рис. 3б, е), и, кроме того, ямки наблюдаются за пределами районов бассейнов после более длительных периодов Cl 9.0091 − экспозиция (рис. 3в,ж). Этот характер обширных поверхностных изъязвлений не наблюдался в деионизированной воде даже после > 10 часов воздействия.
Прямое наблюдение за различными стадиями зарождения и роста ямок
Эволюцию питтинга оценивали путем количественного определения параметров питтинга, включая: (i) плотность питтинга (т. ямки, те, которые могли быть скрыты из-за отложения продуктов коррозии внутри/над ними, а также вновь образовавшиеся и растущие ямки (рис. 4), (ii) средняя глубина и радиус ямок, присутствующих в FOV (рис. 5a,b ) и (iii) среднее соотношение сторон ямки (т. е. отношение глубины ямки к ее эффективному круглому радиальному отверстию, рис. 5c).
ямки, те, которые могли быть скрыты из-за отложения продуктов коррозии внутри/над ними, а также вновь образовавшиеся и растущие ямки (рис. 4), (ii) средняя глубина и радиус ямок, присутствующих в FOV (рис. 5a,b ) и (iii) среднее соотношение сторон ямки (т. е. отношение глубины ямки к ее эффективному круглому радиальному отверстию, рис. 5c).
Рисунок 4
Плотность питтинга на стальных поверхностях, реагирующих с: (a) DI водой и (b) 100 мМ раствором NaCl в зависимости от времени. Соответствующие кривые наилучшего соответствия, полученные путем подбора модифицированного уравнения Аврами второго порядка, показаны пунктирными линиями. Заштрихованные области указывают периоды индукции, распространения и насыщения питтинговой коррозии.
Полноразмерное изображение
Рис. 5
Эволюция геометрии ямки после воздействия: (а) ДИ вода и (б) 100 мМ раствор NaCl. На первичном и вторичная ось и соответственно. (c) Средние отношения размеров ямок (т. е. AR = глубина ямки/радиус ямки, или D/R, безразмерные) также приведены для деионизированной воды и 100 мМ растворов NaCl. Заштрихованные области указывают периоды индукции, распространения и насыщения. Пунктирная и сплошная линии на (c) указывают на окончание периодов индукции и распространения, соответственно, как в деионизированной воде, так и в 100 мМ NaCl.
(c) Средние отношения размеров ямок (т. е. AR = глубина ямки/радиус ямки, или D/R, безразмерные) также приведены для деионизированной воды и 100 мМ растворов NaCl. Заштрихованные области указывают периоды индукции, распространения и насыщения. Пунктирная и сплошная линии на (c) указывают на окончание периодов индукции и распространения, соответственно, как в деионизированной воде, так и в 100 мМ NaCl.
Изображение в полный размер
Анализ параметров питтинга позволяет выявить три различных этапа коррозии: (1) период индукции , когда питтинг зарождается, но поверхность претерпевает незначительные топографические изменения, (2) период распространения , который характеризуется быстрое увеличение плотности ямок и (3) период насыщения , когда скорость образования ямок показывает асимптотическое плато (см. рис. 4) 9{2}})\), где N и t — плотность и время питтинга, а a и b — подгоночные параметры соответственно (таблица 1). Максимальная скорость увеличения (площадной) плотности очагов питтинга, r max
Максимальная скорость увеличения (площадной) плотности очагов питтинга, r max
, можно записать как: \(\,{r}_{max}=\sqrt{\frac{2a}{e}}b\). Следует отметить, что эта функциональная форма удачно описывает сигмоидальный характер эволюции плотности питтингов во времени, а не является атрибуцией специфических механистических особенностей. Времена, обозначающие окончание периодов индукции и распространения, т инд
и т опора
соответственно, получаются путем определения седловых точек из третьей производной уравнения 2D-Аврами (см. рис. 4 и таблицу 1).
Таблица 1 Параметры наилучшего соответствия модифицированного уравнения Аврами второго порядка, подогнанного к данным о плотности питтингов, показанным на рис. 4.
Полноразмерная таблица
Периоды индукции, распространения и насыщения, определенные Эволюция плотности ямок также очерчивает эволюцию геометрии ямок, как показано на рис. 5. Например, начало индукционного периода в деионизированной воде характеризуется стабильными средними глубиной и радиусом ямок и, следовательно, соотношением сторон (рис. 5а). , в). Позже, во время периодов распространения и насыщения, глубина ямок постоянно увеличивалась, в то время как радиус ямок оставался почти постоянным, что свидетельствует об углублении существующих ямок без зарождения новых. Наблюдался заметный контраст со 100 мМ раствором NaCl. При этом средняя глубина ямки неуклонно увеличивалась как в периоды индукции, так и в периоды насыщения (рис. 5б). С другой стороны, средний радиус ямок перешел от изначально стабильного (индукционного) к постепенному уменьшению в процессе распространения из-за постоянного появления новых и более мелких ямок (например, см. рис. 5b), достигая стабильного значения только в режиме насыщения. . Действительно, период распространения характеризуется быстрым зарождением небольших и неглубоких ямок, что приводит к почти постоянной средней глубине ямок, несмотря на углубление существующих ямок, хотя это также может указывать на частичное заполнение существующих ямок из-за осаждения продуктов коррозии.
5. Например, начало индукционного периода в деионизированной воде характеризуется стабильными средними глубиной и радиусом ямок и, следовательно, соотношением сторон (рис. 5а). , в). Позже, во время периодов распространения и насыщения, глубина ямок постоянно увеличивалась, в то время как радиус ямок оставался почти постоянным, что свидетельствует об углублении существующих ямок без зарождения новых. Наблюдался заметный контраст со 100 мМ раствором NaCl. При этом средняя глубина ямки неуклонно увеличивалась как в периоды индукции, так и в периоды насыщения (рис. 5б). С другой стороны, средний радиус ямок перешел от изначально стабильного (индукционного) к постепенному уменьшению в процессе распространения из-за постоянного появления новых и более мелких ямок (например, см. рис. 5b), достигая стабильного значения только в режиме насыщения. . Действительно, период распространения характеризуется быстрым зарождением небольших и неглубоких ямок, что приводит к почти постоянной средней глубине ямок, несмотря на углубление существующих ямок, хотя это также может указывать на частичное заполнение существующих ямок из-за осаждения продуктов коррозии. внутри них. В дополнение к параметрам питтинга, среднеквадратическая шероховатость (RMS) поверхности областей без питтинга также увеличивалась со временем (см. рис. S3). Таким образом, в отличие от плотности питтинга (см. рис. 4), окончательный период насыщения не наблюдался ни для глубины питтинга, ни для шероховатости поверхности, что указывает на сохранение коррозионных реакций, как показано на рис. 5 и рис. S3.
внутри них. В дополнение к параметрам питтинга, среднеквадратическая шероховатость (RMS) поверхности областей без питтинга также увеличивалась со временем (см. рис. S3). Таким образом, в отличие от плотности питтинга (см. рис. 4), окончательный период насыщения не наблюдался ни для глубины питтинга, ни для шероховатости поверхности, что указывает на сохранение коррозионных реакций, как показано на рис. 5 и рис. S3.
Топографические проявления электрохимически индуцированной точечной коррозии
Измерения на больших полях зрения с разрешением на уровне наноразмеров позволили осуществлять мониторинг и статистический анализ процесса коррозии. Из приведенного выше обсуждения становится ясно, что коррозия стали AISI 1045 очень неоднородна (рис. 2 и 3) и протекает в несколько этапов. Хотя ожидается, что сталь 1045 не будет пассивировать при погружении либо в деионизированную воду, либо в 100 мМ растворы NaCl (pH 5,8), согласно диаграммам Пурбе (т. особенность пассивация к коррозии) 37,38 , зарождение ямок и связанное с этим увеличение шероховатости поверхности постепенно развиваются в течение начального периода погружения; т. е. в период индукции, когда скорость эволюции топографии (и, следовательно, реакции) исчезающе мала.
е. в период индукции, когда скорость эволюции топографии (и, следовательно, реакции) исчезающе мала.
Считается, что индукционный период является результатом наличия оксидной пленки, которая образуется после воздействия воздуха на сталь и предположительно состоит из оксидов железа толщиной ≤20 нм 2,39,40 . Важно подчеркнуть, что индукционные ямки не только способствуют разрушению этого оксидного слоя, но и катализируют коррозию вблизи них, что приводит к образованию шероховатых неглубоких впадин, среднеквадратическая шероховатость которых примерно в 10 раз выше, чем их некорродированная среда. (рис. 2c и 3b). Ожидается, что из-за их значительной глубины (> 100 нм) эти бассейны будут полностью активированы, поскольку отступ поверхности в этих зонах намного больше, чем типичная толщина оксидных слоев (т. е. пассивированных или нет), которые образуются на стальных поверхностях. повышается при воздействии воздуха или щелочных растворов 41,42,43 . Таким образом, образование этих бассейнов четко указывает на увеличение локальной коррозионной активности, которая возникает в результате подкисления, вызванного потреблением кислорода во время точечной коррозии. Быстрое потребление кислорода внутри ямок и его сравнительно медленное восполнение за счет диффузии приводит к локальным различиям потенциала и pH, т. е. от дна ямки до периметра отверстия ямки 44,45 , что приводит к устойчивому вертикальному распространению коррозионные язвы, а также образование впадин за счет бокового расширения устья язв. Ожидается, что непреднамеренный гидролиз ионов трехвалентного железа и образование гидроксиоксидов (рис. S4) приведет к дальнейшему подкислению и расширению устья ямы 9.0091 46,47 . Кроме того, недавно выявленная концентрация электрического поля вблизи устья ямы также способствует формированию круглой впадины – за счет электрически стимулированного растворения вблизи устья ямы 20 . Напротив, область за пределами этих бассейнов демонстрирует ограниченную точечную коррозию, особенно в случае деионизированной воды, и при малых временах воздействия даже в присутствии ионов Cl —.
Быстрое потребление кислорода внутри ямок и его сравнительно медленное восполнение за счет диффузии приводит к локальным различиям потенциала и pH, т. е. от дна ямки до периметра отверстия ямки 44,45 , что приводит к устойчивому вертикальному распространению коррозионные язвы, а также образование впадин за счет бокового расширения устья язв. Ожидается, что непреднамеренный гидролиз ионов трехвалентного железа и образование гидроксиоксидов (рис. S4) приведет к дальнейшему подкислению и расширению устья ямы 9.0091 46,47 . Кроме того, недавно выявленная концентрация электрического поля вблизи устья ямы также способствует формированию круглой впадины – за счет электрически стимулированного растворения вблизи устья ямы 20 . Напротив, область за пределами этих бассейнов демонстрирует ограниченную точечную коррозию, особенно в случае деионизированной воды, и при малых временах воздействия даже в присутствии ионов Cl —.
Ионы Cl − значительно ускоряют коррозию стали 6,7,48 , что проявляется в следующем: (а) усиленная и ускоренная тенденция к развитию шероховатых впадин, (б) зарождение ямок внутри, а также за пределами областей впадин при более длительном времени экспозиции, и, в) агрессивная автокаталитическая питтинговая коррозия.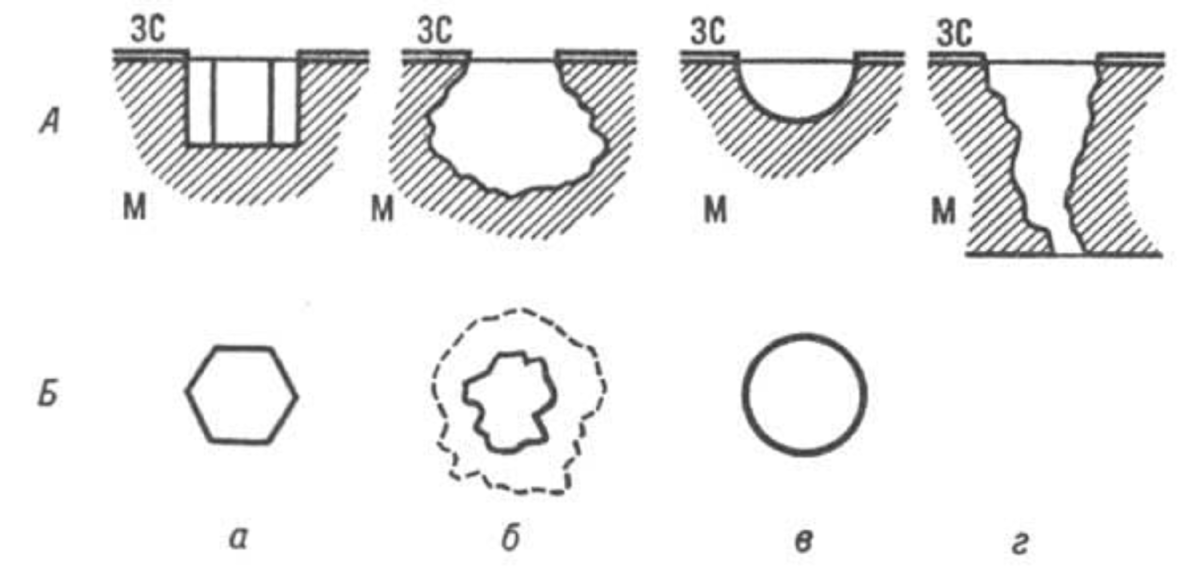 Эти наблюдения могут быть подтверждены анализом кривых плотности ямок, показанных на рис. 4 (таблица 1). На основании результатов подгонки экспоненциальной функции роста было обнаружено, что индукционный период гораздо менее заметен, а скорость распространения плотности ямок примерно в 4 раза выше в присутствии 100 мМ NaCl по сравнению с деионизированной водой. Многочисленные исследования показали, что точечная коррозия металлов, несущих пленку окисления/пассивации, в присутствии Cl − происходит посредством механизмов, включающих проникновение через пленку 49 и (Cl − ) ионную адсорбцию 1,6 . Таким образом, локализованное окислительное растворение либо оксидной пленки, либо нижележащей стали, что приводит к образованию ямок и впадин, ускоряется, когда присутствуют ионы Cl — 7 . Во-первых, ожидается, что повышенная адсорбция Cl — в локализованных доменах вызовет локальное растворение и истончение за счет образования ионных точечных дефектов и областей с высокой локальной плотностью тока.
Эти наблюдения могут быть подтверждены анализом кривых плотности ямок, показанных на рис. 4 (таблица 1). На основании результатов подгонки экспоненциальной функции роста было обнаружено, что индукционный период гораздо менее заметен, а скорость распространения плотности ямок примерно в 4 раза выше в присутствии 100 мМ NaCl по сравнению с деионизированной водой. Многочисленные исследования показали, что точечная коррозия металлов, несущих пленку окисления/пассивации, в присутствии Cl − происходит посредством механизмов, включающих проникновение через пленку 49 и (Cl − ) ионную адсорбцию 1,6 . Таким образом, локализованное окислительное растворение либо оксидной пленки, либо нижележащей стали, что приводит к образованию ямок и впадин, ускоряется, когда присутствуют ионы Cl — 7 . Во-первых, ожидается, что повышенная адсорбция Cl — в локализованных доменах вызовет локальное растворение и истончение за счет образования ионных точечных дефектов и областей с высокой локальной плотностью тока. Это согласуется с укороченным индукционным периодом, который наблюдается, когда Cl 9Вводится 0091 – ионов по сравнению с деионизированной водой. С другой стороны, проникновение Cl — в образующуюся на воздухе оксидную пленку приведет к образованию загрязненной пленки с более высокой ионной проводимостью, чем исходная пленка. Наблюдение за образованием ямок за пределами локально активированных областей бассейнов подтверждает гипотезу о том, что проникновение ионов Cl — является релевантным, но вторичным механизмом возникновения питтинга. Это основано на наблюдении, что изначально плотность ям за пределами бассейнов намного ниже, чем внутри регионов бассейнов. Следует отметить, что равномерно распределенная точечная коррозия возникала только в более поздние периоды времени, что согласуется с начальным периодом минимальной коррозии в этих областях. Отсюда следует «характерное время», которое связано с проникновением в образовавшийся на воздухе оксидный слой Cl − видов на критическую глубину в зависимости от толщины и состава локального раствора и твердого вещества (защитной пленки).
Это согласуется с укороченным индукционным периодом, который наблюдается, когда Cl 9Вводится 0091 – ионов по сравнению с деионизированной водой. С другой стороны, проникновение Cl — в образующуюся на воздухе оксидную пленку приведет к образованию загрязненной пленки с более высокой ионной проводимостью, чем исходная пленка. Наблюдение за образованием ямок за пределами локально активированных областей бассейнов подтверждает гипотезу о том, что проникновение ионов Cl — является релевантным, но вторичным механизмом возникновения питтинга. Это основано на наблюдении, что изначально плотность ям за пределами бассейнов намного ниже, чем внутри регионов бассейнов. Следует отметить, что равномерно распределенная точечная коррозия возникала только в более поздние периоды времени, что согласуется с начальным периодом минимальной коррозии в этих областях. Отсюда следует «характерное время», которое связано с проникновением в образовавшийся на воздухе оксидный слой Cl − видов на критическую глубину в зависимости от толщины и состава локального раствора и твердого вещества (защитной пленки).
Происхождение индукционных колодцев заслуживает дальнейшего рассмотрения. Например, предполагается возникновение индукционных ямок в местах дефектов, например, в стали AISI 1045, на границах между ферритом и цементитом или в местах внедрения частиц вторичной фазы, слабо пассивированных или термодинамически неустойчивых (т. по отношению к объемному сплаву) 1,7,8 и, следовательно, могут служить местами зародышеобразования для образования ямок. Действительно, наш анализ SEM-EDS показывает, что индукционные ямки, сформированные на поверхностях из стали AISI 1045, обычно имеют высокие концентрации серы и марганца, содержание которых обычно уменьшается по мере роста ямок (например, см. рис. 6). Это наблюдение подтверждает идею о том, что язвы могут возникать, хотя и не исключительно, в результате растворения включений сульфида марганца (MnS), которые образуются в стали во время ее обработки 22,50 . Эти включения, демонстрирующие высокое химическое сродство к кислороду и воде, могут быстро растворяться, оставляя после себя ямки, диаметр которых может достигать более 20 мкм 51 . Еще более проблематичным является то, что ионы галогенидов/Cl —, как известно, предпочтительно адсорбируются в таких местах включения 52 .
Еще более проблематичным является то, что ионы галогенидов/Cl —, как известно, предпочтительно адсорбируются в таких местах включения 52 .
Рисунок 6
СЭМ-микрофотографии репрезентативной индукционной ямки на стали AISI 1045, реагирующей со 100 мМ NaCl для: (a) 0,1 h и (b) 906:30 3,3 ч, показывающее радиальное расширение со временем. В (a) области образцов, помеченные от 1 до 4, имеют следующие содержания Mn и S: 0,1%, 2,3%, 22,1% и 17,3% и 0,1%, 0,2%, 0,1% и 0% соответственно. по данным SEM-EDS (в массовых %). При более длительном времени реакции в (b) области образцов, помеченные от 5 до 9, имеют следующие содержания Mn и S: 2,2 %, 5,0 %, 2,8 %, 2,8 % и 1,3 %, а также 0,1 %, 0,1 %, 0,01 %. %, 0,2 % и 0,0 % соответственно (в массовых %). Относительно высокие концентрации Mn и S согласуются с наличием включения MnS в этом месте питтинга. 9{+}\). Локальное закисление в микроокружении возникает из-за высвобождения протонов из-за химических, электрохимических и геометрических градиентов внутри и вокруг ямок 49 . Формирование бассейновых областей и появление различных стадий питтинга вытекают из кинетики этого процесса подкисления. В целом микросреда внутри ямы характеризуется низким pH и высокой концентрацией ионов, особенно Cl − (если они присутствуют), что также может способствовать образованию солевых пленок 53 внутри карьеров 8,54,55,56,57,58 . Как показано на рис. 4 и 5, углубление ямок происходит даже после достижения насыщения по плотности ямок, что свидетельствует о высокоагрессивной микросреде приповерхностной области, что приводит к углублению всей поверхности. Это согласуется с профилями изменения высоты поверхности, представленными на рис. 1, показывающими продолжающееся накопление продуктов коррозии на стадии насыщения.
Формирование бассейновых областей и появление различных стадий питтинга вытекают из кинетики этого процесса подкисления. В целом микросреда внутри ямы характеризуется низким pH и высокой концентрацией ионов, особенно Cl − (если они присутствуют), что также может способствовать образованию солевых пленок 53 внутри карьеров 8,54,55,56,57,58 . Как показано на рис. 4 и 5, углубление ямок происходит даже после достижения насыщения по плотности ямок, что свидетельствует о высокоагрессивной микросреде приповерхностной области, что приводит к углублению всей поверхности. Это согласуется с профилями изменения высоты поверхности, представленными на рис. 1, показывающими продолжающееся накопление продуктов коррозии на стадии насыщения.
Выводы
В совокупности прямые наблюдения за точечной коррозией – от нано- до микромасштабов – в деионизированной воде и Cl 9Растворы, содержащие растворы 0091–, показывают, что ионы Cl – усиливают коррозию, способствуя разрушению образующихся на воздухе оксидных пленок, которые должны присутствовать на стальных поверхностях, и способствуя поддержанию агрессивной микросреды точечной коррозии. Поясняется, что точечная коррозия является преобладающей формой коррозии в углеродистой стали AISI 1045 и имеет основополагающее значение для начала и развития такой деградации. Следует отметить, что, хотя в настоящем исследовании изучается поведение коррозии непассивированной поверхности, наблюдения могут быть связаны с пассивированными поверхностями, испытывающими локальные транспассивные условия. Например, можно предположить, что аналогичные изменения поверхности могут происходить в углеродистых сталях, подвергающихся щелевой коррозии, или во время гальванической связи с катодным материалом, хотя сама сталь в массе находится в пассивированном состоянии. Важно отметить, что измеренные статистические скорости поверхностной регрессии (реакции) полезны для оценки долгосрочных скоростей коррозии, которые могут быть получены с помощью электрохимического анализа, такого как поляризация Тафеля. Важным результатом этой работы является то, что она предлагает количественную, прямую и недвусмысленную основу для корреляции эволюции морфологии поверхности реагирующих поверхностей с известными электрохимическими процессами, такими как коррозия, путем тщательного изучения эволюции таких вредных реакций во времени.
Поясняется, что точечная коррозия является преобладающей формой коррозии в углеродистой стали AISI 1045 и имеет основополагающее значение для начала и развития такой деградации. Следует отметить, что, хотя в настоящем исследовании изучается поведение коррозии непассивированной поверхности, наблюдения могут быть связаны с пассивированными поверхностями, испытывающими локальные транспассивные условия. Например, можно предположить, что аналогичные изменения поверхности могут происходить в углеродистых сталях, подвергающихся щелевой коррозии, или во время гальванической связи с катодным материалом, хотя сама сталь в массе находится в пассивированном состоянии. Важно отметить, что измеренные статистические скорости поверхностной регрессии (реакции) полезны для оценки долгосрочных скоростей коррозии, которые могут быть получены с помощью электрохимического анализа, такого как поляризация Тафеля. Важным результатом этой работы является то, что она предлагает количественную, прямую и недвусмысленную основу для корреляции эволюции морфологии поверхности реагирующих поверхностей с известными электрохимическими процессами, такими как коррозия, путем тщательного изучения эволюции таких вредных реакций во времени.
Методы
Материалы и подготовка образцов
Коммерчески доступную сталь AISI 1045 разрезали на прямоугольные образцы размерами 1,7 см × 0,8 см ×1,7 см (длина × ширина × высота) с помощью низкоскоростной алмазной пилы. вафельный нож (Buehler, IsoMet 1000). Эта среднеуглеродистая сталь имеет номинальный состав в % по массе: C (0,4–0,5%), P (0–0,04%), Mn (0,6–0,9%), S (0–0,05%), Si (0,2–0,04%). 0,3%) и Fe (98,2–98,9%). Политетрафторэтилен (ПТФЭ), который, как известно, инертен в агрессивных растворах 59,60,61 , использовали в качестве эталонного материала для визуализации VSI, как указано ниже. Кроме того, ПТФЭ является гидрофобным – поэтому он противостоит отложению продуктов коррозии на своих поверхностях. Купоны из ПТФЭ были разрезаны и помещены рядом со стальным образцом в эпоксидную «шайбу» (см. рис. 7a) для облегчения обращения. После отверждения смолы в течение не менее 10 часов при температуре окружающей среды затвердевшую шайбу постепенно полировали с использованием наждачной бумаги с зернистостью 400, 600, 800 и 1200 и алмазных паст с размером частиц 6, 3, 1, ¼ мкм. Полированный образец очищали ультразвуком в этаноле в течение 2 минут, а затем сушили в потоке газообразного азота сверхвысокой чистоты (UHP).
Полированный образец очищали ультразвуком в этаноле в течение 2 минут, а затем сушили в потоке газообразного азота сверхвысокой чистоты (UHP).
Рисунок 7
( a ) Изображение полированной эпоксидной «шайбы», в которую были залиты ПТФЭ и сталь AISI 1045, и, (b) Репрезентативное изображение VSI эталона (ПТФЭ) и стальные образцы, заделанные рядом друг с другом.
Полноразмерное изображение
Вертикальная сканирующая интерферометрия (VSI)
Эволюцию морфологии стальной поверхности в процессе коррозии отслеживали с помощью вертикального сканирующего интерферометра (NewView 8200, Zygo Corporation). Чтобы получить изображение больших областей коррозии, был использован объектив Мирау с 5-кратным увеличением (числовая апертура, N.A. = 0,13), который обеспечивает поперечное разрешение (т. е. размер пикселя) 1,63 мкм в x и y направлений. Номинальное вертикальное разрешение порядка 2 нм. При такой конфигурации поле зрения каждого изображения VSI составляет 1,7 мм × 1,7 мм и может быть расширено за счет слияния («мозаики») нескольких изображений, отображаемых вдоль сетки (например, сетка, состоящая из изображений A × B, состоит из изображений A. B). изображения, сделанные последовательно). Были исследованы плиточные участки, состоящие из стальной и эталонной поверхностей и имеющие номинальные размеры порядка 5,7 мм × 3,0 мм (см. рис. 7b). Наблюдаемая площадь поверхности стали составляет около 10,7 мм 9 .0091 2 и состоит из 4,03 × 10 6 пикселей. Такая большая площадь позволяет одновременно наблюдать за сотнями очагов коррозии.
B). изображения, сделанные последовательно). Были исследованы плиточные участки, состоящие из стальной и эталонной поверхностей и имеющие номинальные размеры порядка 5,7 мм × 3,0 мм (см. рис. 7b). Наблюдаемая площадь поверхности стали составляет около 10,7 мм 9 .0091 2 и состоит из 4,03 × 10 6 пикселей. Такая большая площадь позволяет одновременно наблюдать за сотнями очагов коррозии.
Для инициирования коррозии полированный образец погружали в 70 мл либо: ( i ) 18 МОм·см деионизированной (DI) воды, либо ( ii ) 100 мМ раствора NaCl, приготовленного путем добавления ACS NaCl реактивной чистоты до 18 МОм·см деионизированной воды. Измеренный рН деионизированной воды и раствора, содержащего Cl — , составлял около 5,6–5,8, а температура реакции составляла 25 ± 3 °C. Коррозионный раствор (70 мл) контактировал с поверхностью с номинальной площадью 17 мм × 8 мм, в результате чего отношение поверхности (твердое тело) к объему (жидкость) составило 0,002 мм9. 0091 −1 (S/V) 62 . Образец периодически извлекали из раствора и сушили потоком газообразного азота перед определением топографии поверхности. Коррозионную активность периодически оценивали в течение 10 часов в деионизированной воде и 3,5 часа в 100 мМ растворе NaCl, в это время стальная поверхность была почти полностью покрыта (видимыми) продуктами коррозии («ржавчиной»).
0091 −1 (S/V) 62 . Образец периодически извлекали из раствора и сушили потоком газообразного азота перед определением топографии поверхности. Коррозионную активность периодически оценивали в течение 10 часов в деионизированной воде и 3,5 часа в 100 мМ растворе NaCl, в это время стальная поверхность была почти полностью покрыта (видимыми) продуктами коррозии («ржавчиной»).
Данные топографии поверхности (т. е. в виде трехмерных (3D) изображений), полученные с помощью VSI, были обработаны и проанализированы с использованием MATLAB©. Анализ проводился с использованием специально разработанных сценариев, которые выполняли следующие операции: (1) выравнивались 3D-изображения заданной (визуализируемой) области, полученные в разное время реакции; (2) выявлены очаги коррозии; и (3) была охарактеризована геометрия (т.е. радиус, глубина и соотношение сторон) участков, все в зависимости от времени контакта с реакционным раствором. Если заданное местоположение пикселя не содержало данных о высоте, такие данные извлекались путем интерполяции из 4 -я функция порядка подогнана под известные соседние (местные топографические) данные. Для совмещения 3D-изображений эталон ПТФЭ был отмечен острым инструментом (рис. S4). Затем область произвольного размера, охватывающая метку , была вырезана из 3D-изображения, а затем преобразована в 2D-изображение в градациях серого. Затем это 2D-изображение было совмещено с изображением, полученным в точке 90 598 t 90 599 = 0, с использованием алгоритма регистрации изображения, который допускал перемещение и жесткое вращение только в пределах 90 598 x-y 90 599самолет. Алгоритм регистрации изображения создал матрицу 2D-преобразования, которая затем была применена ко всему 3D-изображению. Выравнивание трехмерной топографии поверхности с использованием контрольной метки позволило точно идентифицировать переходные и вновь образованные элементы на стальной поверхности по мере развития коррозии. Помимо поперечного выравнивания, 3D-изображения также были выровнены по вертикали (по координате z ) путем сопоставления средних высот эквивалентных областей на эталоне из ПТФЭ на t = 0 и в более поздние моменты времени (см.
Для совмещения 3D-изображений эталон ПТФЭ был отмечен острым инструментом (рис. S4). Затем область произвольного размера, охватывающая метку , была вырезана из 3D-изображения, а затем преобразована в 2D-изображение в градациях серого. Затем это 2D-изображение было совмещено с изображением, полученным в точке 90 598 t 90 599 = 0, с использованием алгоритма регистрации изображения, который допускал перемещение и жесткое вращение только в пределах 90 598 x-y 90 599самолет. Алгоритм регистрации изображения создал матрицу 2D-преобразования, которая затем была применена ко всему 3D-изображению. Выравнивание трехмерной топографии поверхности с использованием контрольной метки позволило точно идентифицировать переходные и вновь образованные элементы на стальной поверхности по мере развития коррозии. Помимо поперечного выравнивания, 3D-изображения также были выровнены по вертикали (по координате z ) путем сопоставления средних высот эквивалентных областей на эталоне из ПТФЭ на t = 0 и в более поздние моменты времени (см. {2}}\), где z — высота каждого пикселя) по сравнению с пороговым значением. Порог для идентификации ямок на основе градиента был выбран на основе распределения градиентов на каждом изображении (например, см. рис. 8b). Типичное значение такого порога составляет 1%, т. е. если максимальное распределение частоты градиента в изображении VSI составляет F , то пиксели с величиной градиента ниже 0,01 F считаются участками без ямок, тогда как пиксели с величиной градиента больше, чем при 0,01 F идентифицируются как ямки (рис. 8б).
{2}}\), где z — высота каждого пикселя) по сравнению с пороговым значением. Порог для идентификации ямок на основе градиента был выбран на основе распределения градиентов на каждом изображении (например, см. рис. 8b). Типичное значение такого порога составляет 1%, т. е. если максимальное распределение частоты градиента в изображении VSI составляет F , то пиксели с величиной градиента ниже 0,01 F считаются участками без ямок, тогда как пиксели с величиной градиента больше, чем при 0,01 F идентифицируются как ямки (рис. 8б).
Рисунок 8
( a ) Иллюстрация роста ямок на стали AISI 1045 в 100 мМ NaCl. Снизу вверх на диаграмме показано изменение глубины после 0 мин, 5 мин, 10 мин и 15 мин воздействия раствора. Через 15 мин глубина питтинга составила около 2 мкм, а (б) Методика выявления участков питтинга на поверхности образца. Как правило, ямки отличаются от шероховатости образца с помощью порогового значения градиента, показанного пунктирной синей линией.
Полноразмерное изображение
Известно, что ямки можно также идентифицировать на основе абсолютного изменения высоты по отношению к исходной поверхности. Однако такие методы неэффективны для различения локализованного уменьшения высоты (т. е. образования ямок) от равномерного отступления поверхности (т. е. равномерного растворения). Напротив, использование метода на основе локального градиента позволяет идентифицировать ямы исключительно на основе их геометрических характеристик и градиента их ближайшего окружения. Однако, поскольку в методе градиента используется идея о том, что стенки ямы должны иметь высокий уклон, он имеет тенденцию игнорировать область на дне ямы, которая часто имеет низкий уклон. Таким образом, чтобы убедиться, что яма была идентифицирована полностью, был реализован алгоритм выпуклой оболочки (рис. S5). Во-первых, все соседние пиксели, изначально идентифицированные как принадлежащие ямкам (например, пиксели на стенках ямок), были сгруппированы 63 . Затем вокруг каждой группы пикселей была нарисована двумерная выпуклая оболочка на основе их координат x и y , чтобы указать область, которая является потенциальным местом питтинга. На основе перекрытий в областях, принадлежащих различным потенциальным участкам питтинга, группировка точек была итеративно обновлена. Затем была нарисована новая выпуклая оболочка вокруг точек, принадлежащих двум перекрывающимся областям, таким образом объединяя области в одну яму. Этот процесс выполнялся итеративно, пока количество питов не сходилось к стабильному значению. Каждой яме был присвоен уникальный идентификатор для дальнейшего анализа.
Затем вокруг каждой группы пикселей была нарисована двумерная выпуклая оболочка на основе их координат x и y , чтобы указать область, которая является потенциальным местом питтинга. На основе перекрытий в областях, принадлежащих различным потенциальным участкам питтинга, группировка точек была итеративно обновлена. Затем была нарисована новая выпуклая оболочка вокруг точек, принадлежащих двум перекрывающимся областям, таким образом объединяя области в одну яму. Этот процесс выполнялся итеративно, пока количество питов не сходилось к стабильному значению. Каждой яме был присвоен уникальный идентификатор для дальнейшего анализа.
Характеристика геометрии ямок, быстротечности и эволюции поверхности
После выявления участков ямок был проведен анализ для характеристики зарождения и роста ямок. Чтобы установить базовую поверхность, используемую для коррекции наклона и кривизны, сначала к трехмерному изображению был подогнан полином 4-го порядка , исключая все выявленные ямки, чтобы зафиксировать кривизну поверхности (рис. {2}} {n}} \), где n — количество точек данных, а dz — расстояние до базовой линии. Глубина каждой ямки определялась как расстояние между самой нижней точкой ямки и базовой поверхностью (рис. S6). С другой стороны, радиус ямки был рассчитан по измеренной площади ямки, предполагая, что ямки можно описать окружностью. Путем анализа перекрывающихся ямок (т. е. одних и тех же ямок) на разнесенных во времени топографиях поверхности можно изучить процесс зарождения и роста каждой ямки. Это позволяет количественно определить плотность ямок в зависимости от времени и оценить скорость роста ямок, при этом имея возможность отличить существующие от новых ямок в каждый временной интервал.
{2}} {n}} \), где n — количество точек данных, а dz — расстояние до базовой линии. Глубина каждой ямки определялась как расстояние между самой нижней точкой ямки и базовой поверхностью (рис. S6). С другой стороны, радиус ямки был рассчитан по измеренной площади ямки, предполагая, что ямки можно описать окружностью. Путем анализа перекрывающихся ямок (т. е. одних и тех же ямок) на разнесенных во времени топографиях поверхности можно изучить процесс зарождения и роста каждой ямки. Это позволяет количественно определить плотность ямок в зависимости от времени и оценить скорость роста ямок, при этом имея возможность отличить существующие от новых ямок в каждый временной интервал.
Доступность данных
Сценарии анализа и наборы данных, созданные во время и/или проанализированные в ходе исследования названия, доступны у соответствующего автора по обоснованному запросу.
Ссылки
- «>
Колотыркин Дж. М. Питтинговая коррозия металлов. КОРРОЗИЯ 19 , 261–268 т (1963 г.).
Артикул
КАСGoogle ученый
Штрехблов, Х.-Х. Зарождение и репассивация очагов коррозии при питтинге железа и никеля. Матер. Коррос. 27 , 792–799 (1976).
Артикул
КАСGoogle ученый
Линдли, Т. С., Макинтайр, П. и Трант, П. Дж. Зарождение усталостной трещины в очагах коррозии. Мет. Технол. 9 , 135–142 (1982).
Артикул
Google ученый
Рохлин С.И., Ким Дж.-Ю., Надь Х. и Зоофан Б. Влияние точечной коррозии на возникновение усталостных трещин и усталостную долговечность. англ. Фракт. мех. 62 , 425–444 (1999).
Артикул
Google ученый
- «>
Писториус, П. К. и Бурштейн, Г. Т. Рост коррозионных язв на нержавеющей стали в растворе хлорида, содержащем разбавленный сульфат. Коррос. науч. 33 , 1885–1897 (1992).
Артикул
КАСGoogle ученый
Хоар, Т. П. и Джейкоб, В. Р. Разрушение пассивности нержавеющей стали ионами галогенидов. Природа 216 , 1299–1301 (1967).
ОБЪЯВЛЕНИЕ
Статья
КАСGoogle ученый
Маркус П., Морис В. и Штреблов Х.-Х. Локализованная коррозия (точечная коррозия): модель нарушения пассивации, включающая роль наноструктуры оксидного слоя. Коррос. науч. 50 , 2698–2704 (2008).
Артикул
КАСGoogle ученый
Франкель, Г. С. Точечная коррозия металлов. Обзор критических факторов. Дж. Электрохим.
 соц. 145 , 2186–2198 (1998).
соц. 145 , 2186–2198 (1998).Артикул
КАСGoogle ученый
Уильямс Д. Э., Мохиуддин Т. Ф. и Чжу Ю. Ю. Выяснение механизма запуска точечной коррозии нержавеющих сталей с использованием сканирующей электрохимической и фотоэлектрохимической микроскопии с субмикронным разрешением. Дж. Электрохим. соц. 145 , 2664–2672 (1998).
Артикул
КАСGoogle ученый
Пикеринг, Х. В. и Франкенталь, Р. П. О механизме локальной коррозии железа и нержавеющей стали I. Электрохимические исследования. Дж. Электрохим. соц. 119 , 1297–1304 (1972).
Артикул
КАСGoogle ученый
Франкель, Г. С., Стокерт, Л., Хункелер, Ф. и Боэни, Х. Метастабильная точечная коррозия нержавеющей стали. КОРРОЗИЯ 43 , 429–436 (1987).

Артикул
КАСGoogle ученый
Laycock, N.J., White, S.P., Noh, J.S., Wilson, P.T. & Newman, R.C. Перфорированные крышки для посадочных ям. Дж. Электрохим. соц. 145 , 1101–1108 (1998).
Артикул
КАСGoogle ученый
Эрнст П., Лейкок Н. Дж., Моайед М. Х. и Ньюман Р. К. Механизм формирования кружевного покрова в ямках. Коррос. науч. 39 , 1133–1136 (1997).
Артикул
КАСGoogle ученый
Штрехблов, Х.-Х. Нарушение пассивности и локальная коррозия: теоретические концепции и фундаментальные экспериментальные результаты. Матер. Коррос. 35 , 437–448 (1984).
Артикул
КАСGoogle ученый
Исаакс, Х.
 С. Локальное разрушение и ремонт пассивных поверхностей во время точечной коррозии. Коррос. науч. 29 , 313–323 (1989).
С. Локальное разрушение и ремонт пассивных поверхностей во время точечной коррозии. Коррос. науч. 29 , 313–323 (1989).Артикул
КАСGoogle ученый
Солтис, Дж. Разрушение пассивации, зарождение и распространение питов в металлических материалах – Обзор. Коррос. науч. 90 , 5–22 (2015).
Артикул
КАСGoogle ученый
Кунце Дж., Морис В., Кляйн Л.Х., Штреблов Х.-Х. & Marcus, P. Исследование in situ STM влияния хлоридов на начальные стадии анодного окисления Cu(111) в щелочных растворах. Electrochimica Acta 48 , 1157–1167 (2003).
Артикул
КАСGoogle ученый
Массуд, Т., Морис, В., Кляйн, Л. Х. и Маркус, П. Наноморфология и атомная структура пассивных пленок на нержавеющей стали.
 Дж. Электрохим. соц. 160 , C232–C238 (2013).
Дж. Электрохим. соц. 160 , C232–C238 (2013).Артикул
КАСGoogle ученый
Массуд, Т., Морис, В., Кляйн, Л. Х., Сейе, А. и Маркус, П. Наноструктура и локальные свойства оксидных слоев, выращенных на нержавеющей стали в моделируемой среде реактора с водой под давлением. Коррос. науч. 84 , 198–203 (2014).
Артикул
КАСGoogle ученый
Мерола, К. и др. . In situ Нано- и микроскопическое изображение и механизм роста электрохимического растворения (например, коррозии) ограниченной металлической поверхности. Проц. Натл. акад. науч. 114 , 9541–9546 (2017).
Артикул
пабмед
ПабМед Центральный
КАСGoogle ученый
Бобина М., Келленбергер А., Милле Дж.-П.
 , Мунтян С. и Василчин Н. Коррозионная стойкость углеродистой стали в растворах слабых кислот в присутствии l-гистидина в качестве ингибитора коррозии . Коррос. науч. 69 , 389–395 (2013).
, Мунтян С. и Василчин Н. Коррозионная стойкость углеродистой стали в растворах слабых кислот в присутствии l-гистидина в качестве ингибитора коррозии . Коррос. науч. 69 , 389–395 (2013).Артикул
КАСGoogle ученый
Кадоваки М. и др. . Микроэлектрохимические наблюдения в режиме реального времени за очень ранней стадией питтинга на феррито-перлитной стали в растворах хлоридов. Дж. Электрохим. соц. 164 , C261–C268 (2017).
Артикул
КАСGoogle ученый
Кадоваки М. и др. . Сопротивление точечной коррозии мартенсита стали AISI 1045 и полезная роль внедренного углерода. Дж. Электрохим. соц. 164 , C962–C972 (2017).
Артикул
КАСGoogle ученый
Nie, X., Li, X.
 , Du, C., Huang, Y. & Du, H. Характеристика продуктов коррозии, образующихся на поверхности углеродистой стали, с помощью рамановской спектроскопии. J. Raman Spectrosc. 40 , 76–79 (2009).
, Du, C., Huang, Y. & Du, H. Характеристика продуктов коррозии, образующихся на поверхности углеродистой стали, с помощью рамановской спектроскопии. J. Raman Spectrosc. 40 , 76–79 (2009).ОБЪЯВЛЕНИЕ
Статья
КАСGoogle ученый
Двиведи, Д., Лепкова, К. и Беккер, Т. Коррозия углеродистой стали: обзор основных свойств поверхности и методов определения. RSC Adv. 7 , 4580–4610 (2017).
Артикул
КАСGoogle ученый
Ван, М. Ф., Ли, X. Г., Ду, Н., Хуанг, Ю. З. и Корсунский, А. Прямые доказательства начальной точечной коррозии. Электрохим. коммун. 10 , 1000–1004 (2008 г.).
Артикул
КАСGoogle ученый
Асами, К. и Кикучи, М. Глубокое распространение ржавчины на простой углеродистой стали и атмосферостойких сталях, подвергавшихся воздействию прибрежно-промышленной атмосферы в течение 17 лет.
 Коррос. науч. 45 , 2671–2688 (2003).
Коррос. науч. 45 , 2671–2688 (2003).Артикул
КАСGoogle ученый
Rémazeilles, C. & Refait, P. Об образовании β-FeOOH (акаганеита) в хлоридсодержащих средах. Коррос. науч. 49 , 844–857 (2007).
Артикул
КАСGoogle ученый
Ли, С. и Хихара, Л. Х. Микро-рамановское спектроскопическое исследование морской атмосферной коррозии углеродистой стали: влияние акаганеита. Дж. Электрохим. соц. 162 , C495–C502 (2015).
Артикул
КАСGoogle ученый
Williams, D. E., Westcott, C. & Fleischmann, M. Стохастические модели точечной коррозии нержавеющих сталей II. Измерение и интерпретация данных при постоянном потенциале. Дж. Электрохим. соц. 132 , 1804–1811 (1985).
Артикул
КАСGoogle ученый
- «>
Батлер Г., Стреттон П. и Бейнон Дж. Г. Инициирование и рост питтингов на высокочистом железе и его сплавах с хромом и медью в растворах нейтральных хлоридов. руб. Коррос. J. 7 , 168–173 (1972).
Артикул
КАСGoogle ученый
Панова, А. А., Пантано, П. и Уолт, Д. Р. In Situ Флуоресцентная визуализация локализованной коррозии с помощью pH-чувствительного волокна для визуализации. Анал. хим. 69 , 1635–1641 (1997).
Артикул
пабмед
КАСGoogle ученый
Бурштейн Г. Т., Писториус П. К. и Маттин С. П. Зарождение и рост очагов коррозии на нержавеющей стали. Коррос. науч. 35 , 57–62 (1993).
Артикул
КАСGoogle ученый
Бурштейн, Г. Т., Лю, К., Соуто, Р. М. и Вайнс, С.
 П. Происхождение точечной коррозии. Коррос. англ. науч. Технол. 39 , 25–30 (2004).
П. Происхождение точечной коррозии. Коррос. англ. науч. Технол. 39 , 25–30 (2004).Артикул
КАСGoogle ученый
Punckt, C. и др. . Внезапное начало точечной коррозии на нержавеющей стали как критическое явление. Наука 305 , 1133–1136 (2004).
ОБЪЯВЛЕНИЕ
Статья
пабмед
КАСGoogle ученый
Аврами М. Кинетика фазового перехода. II Соотношения трансформации и времени для случайного распределения ядер. J. Chem. физ. 8 , 212–224 (1940).
ОБЪЯВЛЕНИЕ
Статья
КАСGoogle ученый
Мисава, Т. Термодинамическое рассмотрение системы Fe-h3O при 25 °C. Коррос. науч. 13 , 659–676 (1973).
Артикул
КАСGoogle ученый
«>Бардвелл, Дж. А., Макдугалл, Б. и Спроул, Г. И. Использование ВИМС для исследования индукционной стадии питтинга железа. Дж. Электрохим. соц. 136 , 1331–1336 (1989).
Артикул
КАСGoogle ученый
Карно, А. и др. . Механизмы коррозии сталебетонных форм в контакте с агентом для извлечения из формы изучены методами EIS и XPS. Коррос. науч. 45 , 2513–2524 (2003).
Артикул
КАСGoogle ученый
Эйххорн, К.-Й. & Forker, W. Свойства оксидных и водяных пленок, образующихся при атмосферном воздействии железа и низколегированных сталей.
 Коррос. науч. 28 , 745–758 (1988).
Коррос. науч. 28 , 745–758 (1988).Артикул
КАСGoogle ученый
Граат, П. и Сомерс, М. Одновременное определение состава и толщины тонких пленок оксида железа из спектров XPS Fe 2p. Заяв. Серф. науч. 100–101 , 36–40 (1996).
Артикул
ОБЪЯВЛЕНИЯGoogle ученый
Годс П., Исгор О. Б., Браун Дж. Р., Бенсебаа Ф. и Кингстон. Исследование профиля глубины XPS пассивной оксидной пленки углеродистой стали в насыщенном растворе гидроксида кальция и влияние хлорида на свойства пленки. Заявл. Серф. науч. 257 , 4669–4677 (2011).
ОБЪЯВЛЕНИЕ
Статья
КАСGoogle ученый
Энгельхардт Г., Уркиди-Макдональд М. и Макдональд Д. Д. Упрощенный метод оценки скорости роста коррозионной полости.
 Коррос. науч. 39 , 419–441 (1997).
Коррос. науч. 39 , 419–441 (1997).Артикул
КАСGoogle ученый
Engelhardt, G. & Macdonald, D.D. Детерминистический прогноз распределения глубины карьера. Коррозия 54 , 469–479 (1998).
Артикул
КАСGoogle ученый
Тернбулл, А. Состав раствора и электродный потенциал в ямках, щелях и трещинах. Коррос. науч. 23 , 833–870 (1983).
Артикул
КАСGoogle ученый
Рефе, П. и Генен, Ж.-М. Механизмы окисления гидроксихлорида железа β-Fe2(OH)3Cl в водном растворе: образование акаганеита vs гетита. Коррос. науч. 39 , 539–553 (1997).
Артикул
КАСGoogle ученый
Boehni, H.
 Нарушение пассивности и локальные коррозионные процессы. Ленгмюр 3 , 924–930 (1987).
Нарушение пассивности и локальные коррозионные процессы. Ленгмюр 3 , 924–930 (1987).Артикул
КАСGoogle ученый
Хоар, Т.П., Мирс, Д.К. и Ротвелл, Г.П. Взаимосвязь между анодной пассивностью, осветлением и питтингом. Коррос. науч. 5 , 279–289 (1965).
Артикул
КАСGoogle ученый
Руднев В., Лавлесс Д. и Кук Р. Л. Справочник по индукционному нагреву , Второе издание . (CRC Press, 2017).
Пайк, С. Х., Уайт, Х. С. и Алкир, Р. С. Сканирующая электрохимическая микроскопия. Обнаружение растворенных соединений серы из включений в нержавеющей стали. Дж. Электрохим. соц. 147 , 4120–4124 (2000).
Артикул
КАСGoogle ученый
Лин, Б.
 , Ху, Р., Е, С., Ли, Ю. и Лин, С. Исследование возникновения точечной коррозии в углеродистой стали в хлоридсодержащих средах с использованием сканирующих электрохимических зондов. Electrochimica Acta 55 , 6542–6545 (2010).
, Ху, Р., Е, С., Ли, Ю. и Лин, С. Исследование возникновения точечной коррозии в углеродистой стали в хлоридсодержащих средах с использованием сканирующих электрохимических зондов. Electrochimica Acta 55 , 6542–6545 (2010).Артикул
КАСGoogle ученый
Бек, Т. Р. и Алкир, Р. К. Возникновение солевых пленок во время образования и роста очагов коррозии. Дж. Электрохим. соц. 126 , 1662–1666 (1979).
Артикул
КАСGoogle ученый
Галвеле, Дж. Транспортные процессы при нарушении пассивности — II. Полный гидролиз ионов металлов. Коррос. науч. 21 , 551–579 (1981).
Артикул
КАСGoogle ученый
Исаакс Х.С. и Киссель Г. Подготовка поверхности и распространение ямок в нержавеющих сталях.
 Дж. Электрохим. соц. 119 , 1628–1632 (1972).
Дж. Электрохим. соц. 119 , 1628–1632 (1972).Артикул
КАСGoogle ученый
Исаакс Х.С. Поведение резистивных слоев при локальной коррозии нержавеющей стали. Дж. Электрохим. соц. 120 , 1456–1462 (1973).
Артикул
КАСGoogle ученый
Шайнер, С. и Хельмих, К. Стабильная точечная коррозия нержавеющей стали как процесс растворения, контролируемый диффузией, с острой подвижной границей электрода. Коррос. науч. 49 , 319–346 (2007).
Артикул
КАСGoogle ученый
Scheiner, S. & Hellmich, C. Модель конечного объема для управляемой диффузией и активацией точечной коррозии нержавеющей стали. Вычисл. Методы Прил. мех. англ. 198 , 2898–2910 (2009).
ОБЪЯВЛЕНИЕ
Статья
МАТЕМАТИКАGoogle ученый
«>Чаудхури, Р. Г. и Париа, С. Динамические краевые углы на поверхности ПТФЭ водным раствором поверхностно-активного вещества в отсутствие и в присутствии электролитов. J. Коллоидный интерфейс Sci. 337 , 555–562 (2009).
ОБЪЯВЛЕНИЕ
Статья
пабмед
КАСGoogle ученый
Миллер Дж. Д., Верамасунени С., Дрелич Дж., Яламанчили М. Р. и Ямаути Г. Влияние шероховатости, определенное с помощью атомно-силовой микроскопии, на смачивающие свойства тонких пленок ПТФЭ. Полим. англ. науч. 36 , 1849–1855 (1996).
Артикул
КАСGoogle ученый
«>Барбер, С. Б., Добкин, Д. П. и Хухданпаа, Х. Алгоритм Quickhull для выпуклых оболочек. Программное обеспечение ACM Trans Math 22 , 469–483 (1996).
MathSciNet
Статья
МАТЕМАТИКАGoogle ученый
Кесаван, С., Можи, Т. А. и Уайлд, Б. Е. Техническое примечание: Диаграммы потенциального pH для Fe-Cl 9Система 0091 − -h3O при температуре от 25 до 150°C. КОРРОЗИЯ 45 , 213–215 (1989).
Артикул
КАС
Google ученый
Sperati, C.A. & Starkweather, H.W. Фторсодержащие полимеры. II. Политетрафторэтилен. В Fortschritte Der Hochpolymeren-Forschung 465–495, https://doi.org/10.1007/BFb0050504 (Springer, Berlin, Heidelberg, 1961).
Пигнателли, И. и др. . Механизм растворения-осаждения лежит в основе ползучести бетона во влажной среде. J. Chem. физ. 145 , 054701 (2016).
ОБЪЯВЛЕНИЕ
Статья
пабмед
КАС
Google ученый
Скачать ссылки
Благодарности
Авторы признательны за финансовую поддержку этого исследования, предоставленную: Национальным научным фондом (CAREER Award: 1253269, CMMI: 1401533), Yara Industrial Nitrates, программой Университета ядерной энергии Министерства энергетики США. (DE-NE0008398) и Министерством транспорта США через Федеральное управление автомобильных дорог (DTFH61-13-H-00011). Содержание данной статьи отражает взгляды и мнения авторов, которые несут ответственность за точность представленных данных. Эти исследования проводились в Лаборатории химии строительных материалов (ЛЦ 2 ) и Центр молекулярного приборостроения (MIC) в Калифорнийском университете в Лос-Анджелесе. Таким образом, авторы с благодарностью признают поддержку, которая сделала эти лаборатории и их операции возможными.
Содержание данной статьи отражает взгляды и мнения авторов, которые несут ответственность за точность представленных данных. Эти исследования проводились в Лаборатории химии строительных материалов (ЛЦ 2 ) и Центр молекулярного приборостроения (MIC) в Калифорнийском университете в Лос-Анджелесе. Таким образом, авторы с благодарностью признают поддержку, которая сделала эти лаборатории и их операции возможными.
Информация об авторе
Примечания автора
Пэн Го и Эрика Каллагон Ла Планте внесли равный вклад в эту работу.
Авторы и аффилированные лица
Лаборатория химии строительных материалов (LC2), Департамент гражданского и экологического проектирования, Калифорнийский университет, Лос-Анджелес, Калифорния, , США
Пэн Го, Эрика Каллагон Ла Плант, Бу Ван, Синь Чен и Гаурав Сант
Факультет материаловедения и инженерии, Калифорнийский университет, Лос-Анджелес, Калифорния, , США
Магдалена Балонис & Gaurav Sant
Факультет биоинженерии Калифорнийского университета, Лос-Анджелес, Калифорния, , США
Магдалена Балонис
Лаборатория физики аморфных и неорганических тел (PARISlab), Департамент гражданского строительства и окружающей среды Инженерия, Калифорнийский университет, Лос-Анджелес, Калифорния, , США
Mathieu Bauchy
Калифорнийский институт Nanosystems, Калифорнийский университет, Лос -Анджелес, Калифорния, , США
Gaurav Sant
Авторы
- Erika Callagon La Plante
Просмотр публикаций автора
Вы также можете искать этого автора в
PubMed Google Академия - Бу Ван
Посмотреть публикации автора
Вы также можете искать этого автора в
PubMed Google Scholar - Xin Chen
Просмотр публикаций автора
Вы также можете искать этого автора в
PubMed Google Scholar - Magdalena Balonis
Просмотр публикаций автора
Вы также можете искать этого автора в
PubMed Google Scholar - Матье Боши
Просмотр публикаций автора
Вы также можете искать этого автора в
PubMed Google Scholar - Gaurav Sant
Просмотр публикаций автора
Вы также можете искать этого автора в
PubMed Google Scholar
. также можете искать этого автора в
также можете искать этого автора в
PubMed Google Scholar
Contributions
G. S., E.C.L. и Х.К. написал рукопись. П.Г. и Б.В. провел эксперименты и проанализировал данные. Все авторы внесли свой вклад в обсуждение результатов, внесли свой вклад в рукопись и одобрили окончательную версию.
S., E.C.L. и Х.К. написал рукопись. П.Г. и Б.В. провел эксперименты и проанализировал данные. Все авторы внесли свой вклад в обсуждение результатов, внесли свой вклад в рукопись и одобрили окончательную версию.
Автор, ответственный за переписку
Переписка с
Гаурав Сант.
Заявление об этике
Конкурирующие интересы
Авторы не заявляют об отсутствии конкурирующих интересов.
Дополнительная информация
Примечание издателя: Springer Nature остается нейтральной в отношении юрисдикционных претензий в опубликованных картах и институциональной принадлежности.
Электронный дополнительный материал
Дополнительная информация
Права и разрешения
Открытый доступ Эта статья находится под лицензией Creative Commons Attribution 4.0 International License, которая разрешает использование, совместное использование, адаптацию, распространение и воспроизведение на любом носителе или в любом формате, при условии, что вы укажете соответствующую ссылку на первоначальный автор(ы) и источник, предоставьте ссылку на лицензию Creative Commons и укажите, были ли внесены изменения. Изображения или другие сторонние материалы в этой статье включены в лицензию Creative Commons для статьи, если иное не указано в кредитной строке материала. Если материал не включен в лицензию Creative Commons статьи, а ваше предполагаемое использование не разрешено законом или выходит за рамки разрешенного использования, вам необходимо получить разрешение непосредственно от правообладателя. Чтобы просмотреть копию этой лицензии, посетите http://creativecommons.org/licenses/by/4.0/.
Изображения или другие сторонние материалы в этой статье включены в лицензию Creative Commons для статьи, если иное не указано в кредитной строке материала. Если материал не включен в лицензию Creative Commons статьи, а ваше предполагаемое использование не разрешено законом или выходит за рамки разрешенного использования, вам необходимо получить разрешение непосредственно от правообладателя. Чтобы просмотреть копию этой лицензии, посетите http://creativecommons.org/licenses/by/4.0/.
Перепечатка и разрешения
Об этой статье
Эта статья цитируется
Исследование кинетики коррозии стали трубопровода методом вертикальной сканирующей интерферометрии с рамановской спектроскопией
- Янис Хойер
- Андреас Люттге
npj Деградация материалов (2018)
Ингибирование коррозии стали нитратом кальция в средах жидкостей заканчивания, обогащенных галогенидами
- Шици Донг
- Эрика Каллагон Ла Планте
- Гаурав Сант
npj Деградация материалов (2018)
Комментарии
Отправляя комментарий, вы соглашаетесь соблюдать наши Условия и Правила сообщества. Если вы обнаружите что-то оскорбительное или не соответствующее нашим условиям или правилам, отметьте это как неприемлемое.
Если вы обнаружите что-то оскорбительное или не соответствующее нашим условиям или правилам, отметьте это как неприемлемое.
Питтинговая коррозия – Конструкционная целостность Материалы Услуги
Точечная коррозия – это локализованное коррозионное воздействие, включающее растворение металлической поверхности трубы на небольшом и четко определенном участке. Питтинговая коррозия может возникнуть в любом компоненте, контактирующем с водой в условиях застойного насыщения кислородом. Точечная коррозия в трубках экономайзера обычно является результатом неправильной практики отключения, которая допускает контакт со стоячей водой с высоким содержанием кислорода. Точечная коррозия также может возникать в трубах с водяными стенками в результате кислотного воздействия в результате неудовлетворительной химической очистки или кислотного загрязнения.
Ямки, связанные с условиями низкого pH, как правило, многочисленны и расположены довольно близко друг к другу. Ямки, как правило, имеют глубокие стенки по сравнению с длиной дефекта. Разрушение поверхности пассивного металла инициирует процесс точечной коррозии в условиях застоя кислорода. Возникает большая разность потенциалов между небольшой площадью инициированной активной ямки (анод) и пассивной областью вокруг ямки (катод). Яма будет расти в присутствии концентрированной соли или кислых веществ. Соль иона металла (M+A-) соединяется с водой и образует гидроксид металла и соответствующую свободную кислоту (например, соляную кислоту, когда присутствует хлорид). Кислородное восстановление на катоде подавляет коррозию вокруг краев ямки, но внутри ямки скорость атаки увеличивается, поскольку локальная среда внутри ямки становится более кислой. В том случае, если поверхности вдоль стенок ямки не репассивированы, скорость роста ямки будет продолжать увеличиваться, поскольку реакция больше не определяется средой объемной жидкости. Питтинг часто встречается в застойных условиях, которые позволяют инициировать и концентрировать место, позволяя атаке продолжаться.
Разрушение поверхности пассивного металла инициирует процесс точечной коррозии в условиях застоя кислорода. Возникает большая разность потенциалов между небольшой площадью инициированной активной ямки (анод) и пассивной областью вокруг ямки (катод). Яма будет расти в присутствии концентрированной соли или кислых веществ. Соль иона металла (M+A-) соединяется с водой и образует гидроксид металла и соответствующую свободную кислоту (например, соляную кислоту, когда присутствует хлорид). Кислородное восстановление на катоде подавляет коррозию вокруг краев ямки, но внутри ямки скорость атаки увеличивается, поскольку локальная среда внутри ямки становится более кислой. В том случае, если поверхности вдоль стенок ямки не репассивированы, скорость роста ямки будет продолжать увеличиваться, поскольку реакция больше не определяется средой объемной жидкости. Питтинг часто встречается в застойных условиях, которые позволяют инициировать и концентрировать место, позволяя атаке продолжаться.
Наиболее распространенная причина точечной коррозии в трубопроводах, соприкасающихся с паром, возникает из-за богатого кислородом застойного конденсата, образующегося во время останова. Принудительное охлаждение и/или неправильный слив и вентиляция узлов могут привести к избыточной влажности. Граница между жидкостью и воздухом является областью наибольшей восприимчивости. Точечная коррозия также может быть ускорена, если условия допускают отложение солей, таких как сульфат натрия, которые смешиваются с влагой во время останова. Унос летучих веществ зависит от давления в барабане, в то время как механический перенос может увеличиться при работе с высоким уровнем в барабане или отверстиями в сепараторах барабана. Точечная коррозия из-за воздействия сульфата натрия может возникать в секциях подогревателя обычных блоков и блоков-утилизаторов-утилизаторов, поскольку сульфат менее растворим и откладывается на внутренних поверхностях. Во время остановов образующаяся влага имеет более кислую реакцию.
Принудительное охлаждение и/или неправильный слив и вентиляция узлов могут привести к избыточной влажности. Граница между жидкостью и воздухом является областью наибольшей восприимчивости. Точечная коррозия также может быть ускорена, если условия допускают отложение солей, таких как сульфат натрия, которые смешиваются с влагой во время останова. Унос летучих веществ зависит от давления в барабане, в то время как механический перенос может увеличиться при работе с высоким уровнем в барабане или отверстиями в сепараторах барабана. Точечная коррозия из-за воздействия сульфата натрия может возникать в секциях подогревателя обычных блоков и блоков-утилизаторов-утилизаторов, поскольку сульфат менее растворим и откладывается на внутренних поверхностях. Во время остановов образующаяся влага имеет более кислую реакцию.
В обычных агрегатах точечная коррозия возникает в местах, где конденсат может образовываться и оставаться в жидком состоянии во время останова, если узлы не вентилируются должным образом, не осушаются или не промываются воздухом или инертным газом. Эти области включают горизонтальные трубы экономайзера и в нижней части наклонных изгибов или в нижних точках провисающих горизонтальных труб в трубах, контактирующих с паром.
Эти области включают горизонтальные трубы экономайзера и в нижней части наклонных изгибов или в нижних точках провисающих горизонтальных труб в трубах, контактирующих с паром.
В котлах-утилизаторах повреждения возникают на поверхностях любого компонента, который намеренно поддерживается во влажном состоянии в периоды простоя или на котором задерживается вода из-за неполного слива или конденсации во время периодов простоя.
Разрушение вследствие неправильной химической очистки обычно усиливается в зонах термического влияния сварки или в местах, где отложения могли остаться после очистки.
Ямки часто бывают небольшого размера и могут быть заполнены продуктами коррозии или оксидами, поэтому определение серьезности питтинговой коррозии при визуальном осмотре может быть затруднено.
Повреждение затронутых поверхностей имеет тенденцию быть глубоким по сравнению с шириной ямки, так что соотношение сторон является отличительной чертой.
Основной фактор, который способствует точечной коррозии в трубах котлов, связан с неправильными методами остановки, которые допускают образование и сохранение стоячей, насыщенной кислородом воды без защитной среды. Подтверждение наличия стоячей воды включает: а) анализ продуктов коррозии внутри и вокруг приямка; б) отбор проб труб на пораженных участках для определения наличия локальной коррозии; и c) оценка процедур останова для проверки наличия условий, способствующих застою воды. Унос сульфата натрия и его отложение в подогревателе может привести к образованию кислых растворов во время незащищенного останова и вызвать точечную коррозию. Точно так же летучая зола может втягиваться в трубы подогревателя под вакуумом и образовывать кислую среду.
Подтверждение наличия стоячей воды включает: а) анализ продуктов коррозии внутри и вокруг приямка; б) отбор проб труб на пораженных участках для определения наличия локальной коррозии; и c) оценка процедур останова для проверки наличия условий, способствующих застою воды. Унос сульфата натрия и его отложение в подогревателе может привести к образованию кислых растворов во время незащищенного останова и вызвать точечную коррозию. Точно так же летучая зола может втягиваться в трубы подогревателя под вакуумом и образовывать кислую среду.
Визуальный осмотр (волоконная оптика) и волноводное исследование могут использоваться для определения поврежденных зон и областей с сильными отложениями, особенно в котлах-утилизаторах. Ультразвуковой контроль можно использовать для определения степени потерь или утончения металла на трубах без внешних ребер.
Точечная коррозия чаще всего устраняется путем замены в натуральной форме на пораженных участках после их выявления. Сварка подушечками не считается приемлемым долгосрочным ремонтом. Цикл питтинга может начаться снова, если не будут приняты надлежащие методы простоя. Эти действия должны сопровождаться анализом и оптимизацией химического цикла агрегата (как питательной воды, так и котловой воды).
Цикл питтинга может начаться снова, если не будут приняты надлежащие методы простоя. Эти действия должны сопровождаться анализом и оптимизацией химического цикла агрегата (как питательной воды, так и котловой воды).
- Услуги неразрушающего контроля/инспекции для определения географии повреждений с использованием методов скрининга первого уровня, включая визуальный осмотр (волоконная оптика) и волноводный контроль, в сочетании с более подробными оценками второго уровня с ультразвуковым контролем (УЗК) для обычных котлов и котлов-утилизаторов не -оребренная трубка.
- Предоставить рекомендации относительно подходящих мест отбора проб труб для обычных и котлов-утилизаторов, а также провести металлографический анализ для определения степени точечной коррозии.
- Провести оценку первого уровня для выявления тепловых переходных процессов и определения мест, где в паровых трубопроводах образуется конденсат, который плохо дренируется.
- Предоставить руководство по проведению испытаний на унос пара для выявления присутствия сульфата натрия.


 68±0,19
68±0,19 .0,6
.0,6