Температура плавления латунь: Как расплавить латунь в домашних условиях: плавление латуни дома
Содержание
Температура испарения меди
Главная » Разное » Температура испарения меди
Температура плавления меди – при какой температуре плавится медь
Благодаря тому, что температура плавления меди достаточно невысокая, этот металл стал одним из первых, которые древние люди начали использовать для изготовления различных инструментов, посуды, украшений и оружия. Самородки меди или медную руду можно было расплавить на костре, что, собственно, и делали наши далекие предки.
Этап плавления меди
Несмотря на активное применение человечеством с древних времен, медь не является самым распространенным природным металлом. В этом отношении она значительно уступает остальным элементам и занимает в их ряду только 23-е место.
Как плавили медь наши предки
Благодаря невысокой температуре плавления меди, составляющей 1083 градуса Цельсия, наши далекие предки не только успешно получали из руды чистый металл, но и изготавливали различные сплавы на его основе. Чтобы получить такие сплавы, медь нагревали и доводили до жидкого расплавленного состояния. Затем в такой расплав просто добавляли олово или выполняли его восстановление на поверхности расплавленной меди, для чего использовалась оловосодержащая руда (касситерит). По такой технологии получали бронзу – сплав, обладающий высокой прочностью, который использовали для изготовления оружия.
Затем в такой расплав просто добавляли олово или выполняли его восстановление на поверхности расплавленной меди, для чего использовалась оловосодержащая руда (касситерит). По такой технологии получали бронзу – сплав, обладающий высокой прочностью, который использовали для изготовления оружия.
Какие процессы происходят при плавлении меди
Что характерно, температуры плавления меди и сплавов, полученных на ее основе, отличаются. При добавлении в медь олова, имеющего меньшую температуру плавления, получают бронзу с температурой плавления 930–1140 градусов Цельсия. А сплав меди с цинком (латунь) плавится при 900–10500 Цельсия.
Во всех металлах в процессе плавления происходят одинаковые процессы. При получении достаточного количества теплоты при нагревании кристаллическая решетка металла начинает разрушаться. В тот момент, когда он переходит в расплавленное состояние, его температура не повышается, хотя процесс передачи ему теплоты при помощи нагрева не прекращается. Температура металла начинает вновь повышаться только тогда, когда он весь перейдет в расплавленное состояние.
Диаграмма состояния системы хром-медь
При охлаждении происходит противоположный процесс: сначала температура резко снижается, затем на некоторое время останавливается на постоянной отметке. После того, как весь металл перейдет в твердую фазу, температура снова начинает снижаться до полного его остывания.
Как плавление, так и обратная кристаллизация меди, связаны с параметром удельной теплоты. Данный параметр характеризует удельное количество теплоты, которая требуется для того, чтобы перевести металл из твердого состояния в жидкое. При кристаллизации металла такой параметр характеризует количество теплоты, которое он отдает при остывании.
Более подробно узнать о плавлении меди помогает фазовая диаграмма, показывающая зависимость состояния металла от температуры. Такие диаграммы, которые можно составить для любых металлов, помогают изучать их свойства, определять температуры, при которых они кардинально меняют свои свойства и текущее состояние.
Кроме температуры плавления, у меди есть и температура кипения, при которой расплавленный металл начинает выделять пузырьки, наполненные газом.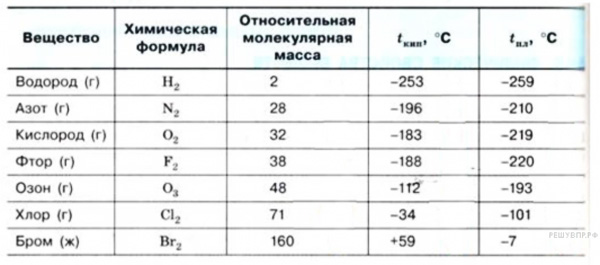 На самом деле никакого кипения меди не происходит, просто этот процесс внешне очень его напоминает. Довести до такого состояния ее можно, если нагреть до температуры 2560 градусов.
На самом деле никакого кипения меди не происходит, просто этот процесс внешне очень его напоминает. Довести до такого состояния ее можно, если нагреть до температуры 2560 градусов.
Как понятно из всего вышесказанного, именно невысокую температуру плавления меди можно назвать одной из основных причин того, что сегодня мы можем использовать этот металл, обладающий многими уникальными характеристиками.
Температура кипения и плавления металлов, температура плавления стали
Температура кипения и плавления металлов
В таблице представлена температура плавления металлов tпл, их температура кипения tк при атмосферном давлении, плотность металлов ρ при 25°С и теплопроводность λ при 27°С.
Температура плавления металлов, а также их плотность и теплопроводность приведены в таблице для следующих металлов: актиний Ac, серебро Ag, алюминий Al, золото Au, барий Ba, берилий Be, висмут Bi, кальций Ca, кадмий Cd, кобальт Co, хром Cr, цезий Cs, медь Cu, железо Fe, галлий Ga, гафний Hf, ртуть Hg, индий In, иридий Ir, калий K, литий Li, магний Mg, марганец Mn, молибден Mo, натрий Na, ниобий Nb, никель Ni, нептуний Np, осмий Os, протактиний Pa, свинец Pb, палладий Pd, полоний Po, платина Pt, плутоний Pu, радий Ra, рубидий Pb, рений Re, родий Rh, рутений Ru, сурьма Sb, олово Sn, стронций Sr, тантал Ta, технеций Tc, торий Th, титан Ti, таллий Tl, уран U, ванадий V, вольфрам W, цинк Zn, цирконий Zr.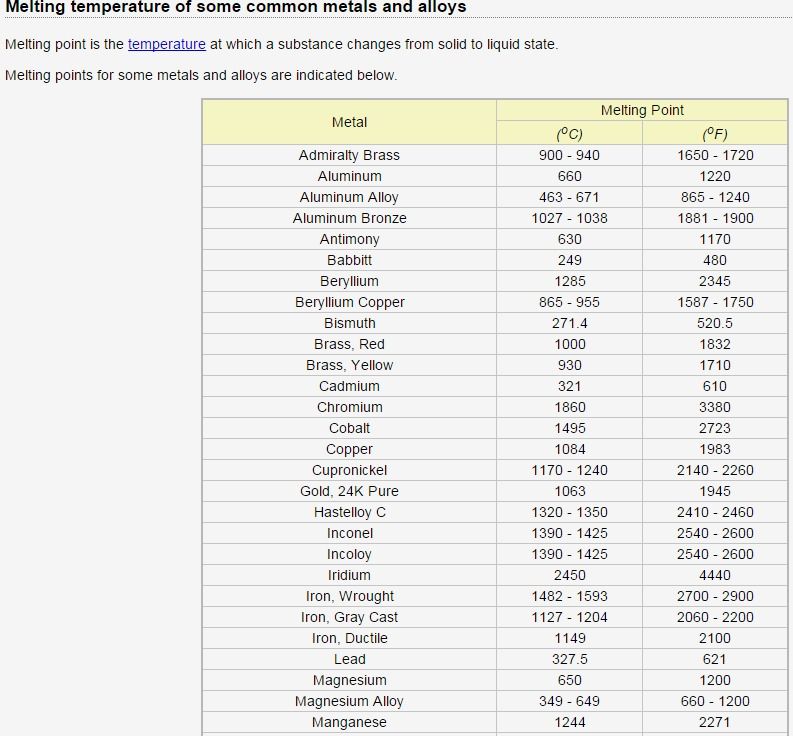
По данным таблицы видно, что температура плавления металлов изменяется в широком диапазоне (от -38,83°С у ртути до 3422°С у вольфрама). Низкой положительной температурой плавления обладают такие металлы, как литий (18,05°С), цезий (28,44°С), рубидий (39,3°С) и другие щелочные металлы.
Наиболее тугоплавкими являются следующие металлы: гафний, иридий, молибден, ниобий, осмий, рений, рутений, тантал, технеций, вольфрам. Температура плавления этих металлов выше 2000°С.
Приведем примеры температуры плавления металлов, широко применяемых в промышленности и в быту:
- температура плавления алюминия 660,32 °С;
- температура плавления меди 1084,62 °С;
- температура плавления свинца 327,46 °С;
- температура плавления золота 1064,18 °С;
- температура плавления олова 231,93 °С;
- температура плавления серебра 961,78 °С;
- температура плавления ртути -38,83°С.
Максимальной температурой кипения из металлов, представленных в таблице, обладает рений Re — она составляет 5596°С. Также высокими температурами кипения обладают металлы, относящиеся к группе с высокой температурой плавления.
Также высокими температурами кипения обладают металлы, относящиеся к группе с высокой температурой плавления.
Плотность металлов в таблице находится в диапазоне от 0,534 до 22,59 г/см3, то есть самым легким металлом является литий, а самым тяжелым металлом осмий. Следует отметить, что осмий имеет плотность большую, чем плотность урана и даже плутония при комнатной температуре.
Теплопроводность металлов в таблице изменяется от 6,3 до 427 Вт/(м·град), таким образом хуже всего проводит тепло такой металл, как нептуний, а лучшим теплопроводящим металлом является серебро.
Температура плавления стали
Представлена таблица значений температуры плавления стали распространенных марок. Рассмотрены стали для отливок, конструкционные, жаропрочные, углеродистые и другие классы сталей.
Температура плавления стали находится в диапазоне от 1350 до 1535°С. Стали в таблице расположены в порядке возрастания их температуры плавления.
| Сталь | tпл, °С | Сталь | tпл, °С |
|---|---|---|---|
| Стали для отливок Х28Л и Х34Л | 1350 | Коррозионно-стойкая жаропрочная 12Х18Н9Т | 1425 |
| Сталь конструкционная 12Х18Н10Т | 1400 | Жаропрочная высоколегированная 20Х23Н13 | 1440 |
| Жаропрочная высоколегированная 20Х20Н14С2 | 1400 | Жаропрочная высоколегированная 40Х10С2М | 1480 |
| Жаропрочная высоколегированная 20Х25Н20С2 | 1400 | Сталь коррозионно-стойкая Х25С3Н (ЭИ261) | 1480 |
| Сталь конструкционная 12Х18Н10 | 1410 | Жаропрочная высоколегированная 40Х9С2 (ЭСХ8) | 1480 |
| Коррозионно-стойкая жаропрочная 12Х18Н9 | 1410 | Коррозионно-стойкие обыкновенные 95Х18…15Х28 | 1500 |
| Сталь жаропрочная Х20Н35 | 1410 | Коррозионно-стойкая жаропрочная 15Х25Т (ЭИ439) | 1500 |
| Жаропрочная высоколегированная 20Х23Н18 (ЭИ417) | 1415 | Углеродистые стали | 1535 |
Источники:
- Волков А.
 И., Жарский И. М. Большой химический справочник. — М: Советская школа, 2005. — 608 с.
И., Жарский И. М. Большой химический справочник. — М: Советская школа, 2005. — 608 с. - Казанцев Е. И. Промышленные печи. Справочное руководство для расчетов и проектирования.
-
Физические величины. Справочник. А. П. Бабичев, Н. А. Бабушкина, А. М. Братковский и др.; Под ред. И. С. Григорьева, Е. З. Мейлихова. — М.: Энергоатомиздат, 1991. — 1232 с.
Тепловые и термодинамические свойства меди
Рассмотрим тепловые и термодинамические свойства меди.
Температура плавления 1083°С, температура кипения 2573°С, характеристическая температура ΘD 345 К, удельная теплота плавления 239 кДж/кг, удельная теплота испарения 4790 кДж/кг. Удельная теплоемкость меди при 293 К при постоянном давлении Ср= 384,2 Дж/(кг*K), а жидкой (при температуре плавления) 495 Дж/(кг*К). Удельная электронная теплоемкость Срэл = [0,688 мДж/(моль*К2)] *Т. Теплопроводность λ при 293 К равна 397 Вт/(м*К), при температуре 1356 К 165,8 Вт/(м*К).
Зависимость теплопроводности λ, от температуры (чистота 99,999 %):
|
Т, К
|
λ, Вт/(м*К)
|
Т, К
|
λ, Вт/(м*К)
|
Т, К
|
λ, Вт/(м*К)
|
|
2
5
20
50
|
523,5
1487,0
2518,0
1189,5
|
100
150
200
250
|
481,3
428,4
413
406,0
|
300
350
400
|
401,2
397,2
393,7
|
Теплопроводность меди заметно не изменяется под влиянием висмута, свинца, серы, селена, сильно понижается под влиянием незначительных количеств мышьяка, алюминия, снижается под влиянием сурьмы. Температурный коэффициент линейного расширения при 293 К α = 16,7*10-6К-1.
Температурный коэффициент линейного расширения при 293 К α = 16,7*10-6К-1.
Изменение α в зависимости от температуры (чистота 99,999%):
|
Т, К
|
α*106 К-1
|
Т, К
|
α*106 К-1
|
Т, К
|
α*106 К-1
|
|
5
|
0,0024
|
20
|
0,23
|
400
|
17,58
|
|
7
|
0,01062
|
40
|
2,28.
|
600
|
18,92
|
|
10
|
0,0294
|
60
|
5,40
|
800
|
20,09
|
|
13
|
0,06322
|
100
|
10,33
|
1000
|
22,1
|
|
15
|
0,9634
|
200
|
15,18
|
1200
|
24,5
|
|
|
|
|
|
1300
|
27,0
|
Температурный коэффициент объемного расширения при 293 К β = 49,2*10-6 К-1, в диапазоне 293-1356 К: β= (45,0+0,016 Т)*10-6К-1, где β Д коэффициент объемного расширения, К-1; Т Д температура, К.
Молярная энтропия s° в зависимости от температуры:
|
Т, К
|
298
|
500
|
1000
|
1500
|
2000
|
2500
|
3000
|
|
s°, Дж/(моль*К)
|
33,39
|
44,8
|
65,28
|
87,19
|
96,20
|
103,24
|
215,53
|
Поверхностное натяжение при 1083 °С σ =1351 мН/м. Поверхностная энергия v =1115 мДж/м2, для грани (100) v =1060, а для (111) v = 926 мДж/м3. Энергия дефекта упаковки 67 МДж/м2. Давление пара р в зависимости от температуры:
|
Т, К
|
Р, Па
|
Т, К
|
Р, Па
|
|
700
800
900
|
31,066*10-15
38,514*10-12
97,804*10-10
|
1000
1100
|
82,22*10-8
30,968*10-6
|
Давление пара при температуре плавления Р =50,47 мПа. Энергия активации самодиффузии в интервале 1135Д1330 К Е= 205 КДж/моль.
Энергия активации самодиффузии в интервале 1135Д1330 К Е= 205 КДж/моль.
Параметры взаимной диффузии (предэкспоненциальный множитель Do и энергия активации Е) некоторых элементов в меди:
|
Диффундирующий элемент
|
T, К
|
Образующаяся фаза
|
D0, м2/с
|
Е, кДж/моль
|
|
Н
|
—
|
Твердый раствор
|
5,6*10-8
|
38,52
|
|
Be
|
—
|
Твердый раствор
|
2,32*10-8
|
117,23
|
|
Si
|
—
|
Твердый раствор
|
3,7*10-6
|
167,47
|
|
S
|
1403Д1673
|
Жидкая фаза
|
3,44*10-7
|
28,85
|
|
S
|
1073Д1273
|
Твердый раствор
|
8,24*10-5
|
196,78
|
|
Мп
|
973Д1348
|
Твердый раствор
|
5*10-5
|
192,59
|
|
Fe
|
973Д1343
|
Твердый раствор
|
1,4*10-4
|
216,88
|
|
Co
|
973Д1348
|
Твердый раствор
|
1,93*10-4
|
226,51
|
|
Ni
|
973Д1348
|
Твердый раствор
|
2,7*10-4
|
236,55
|
|
Zn
|
878Д1323
|
Твердый раствор
|
3,4*10-5
|
190,92
|
|
Ge
|
952Д1288
|
Твердый раствор
|
3,97*10-5
|
187,5
|
|
As
|
1083Д1328
|
Твердый раствор
|
2*10-5
|
176,6
|
|
Rh
|
1023Д1328
|
Твердый раствор
|
3,3*10-4
|
242,5
|
|
Pd
|
1080Д1328
|
Твердый раствор
|
1,71*10-4
|
227
|
|
Ag
|
973Д1173
|
Твердый раствор
|
1,3*10-6
|
161,6
|
|
Cd
|
998Д1223
|
Твердый раствор
|
9,35*10-5
|
191,34
|
|
In
|
1023Д1343
|
Твердый раствор
|
1,3*10-4
|
193
|
|
Sn
|
973Д1189
|
Твердый раствор
|
1,0*10-4
|
190,5
|
|
Sb
|
873Д1273
|
Твердый раствор
|
3,4*10-5
|
175,85
|
|
Au
|
—
|
Твердый раствор
|
1*10-5
|
187,99
|
|
Tl
|
1058Д1269
|
Твердый раствор
|
7,1*10-5
|
181,29
|
Таблица температуры плавления (tпл) металлов и сплавов при нормальном атмосферном давлении
| Металл или сплав | tпл. С С |
|---|---|
| Алюминий | 660,4 |
| Вольфрам | 3420 |
| Германий | 937 |
| Дуралюмин | ~650 |
| Железо | 1539 |
| Золото | 1064?4 |
| Инвар | 1425 |
| Иридий | 2447 |
| Калий | 63,6 |
| Карбиды гафния | 3890 |
| ниобия | 3760 |
| титана | 3150 |
| циркония | 3530 |
| Константин | ~1260 |
| Кремний | 1415 |
| Латунь | ~1000 |
| Легкоплавкий сплав | 60,5 |
| Магний | 650 |
| Медь | 1084,5 |
| Натрий | 97,8 |
| Нейзильбер | ~1100 |
| Никель | 1455 |
| Нихром | ~1400 |
| Олово | 231,9 |
| Осмий | 3030 |
| Платина | 17772 |
| Ртуть | — 38,9 |
| Свинец | 327,4 |
| Серебро | 961,9 |
| Сталь | 1300-1500 |
| Фехраль | ~1460 |
| Цезий | 28,4 |
| Цинк | 419,5 |
| Чугун | 1100-1300 |
Вернуться в раздел аналитики
Запись опубликована автором admin в рубрике Полезные материалы. Добавьте в закладки постоянную ссылку.
Добавьте в закладки постоянную ссылку.
Медные сплавы — Температура плавления
Для медных сплавов, обладающих температурой плавления до 1000° и выше, применяются исключительно машины с холодной камерой давления, работающие по принципу прессования. [c.413]
Тугоплавкие (твердые) припои применяются, когда необходимо иметь прочный спай, выдерживающий высокую температуру. Применяются медно-цинковые тугоплавкие припои ПМЦ-36, ПМЦ-48 и ПМЦ-54. Указанные цифры в обозначении припоя указывают на содержание в нем меди, остальное — цинк и небольшое количество примесей железа (0,1%) и свинца (0,5%). Температура полного расплавления указанных припоев соответственно 825, 865 и 880° С, твердость припоев ПМЦ-48 и ПМЦ-54 составляет НВ 130 и 90, предел прочности при растяжении 21 и 25 кгс/мм (210—250 МПа). Чем больше в сплаве меди, тем припой прочнее, но более тугоплавок чем больше цинка, тем припой менее прочен и более хрупок, но более легкоплавок. Припой ПМЦ-36 применяется для пайки латуни Л-62, ПМЦ-42 — для пайки деталей из медных сплавов с температурой плавления выше 900—920° С, когда паяное соединение не подвергается ударным нагрузкам, вибрации и изгибу. Припой ПМЦ-54 применяют для пайки деталей из меди, бронзы и стали, не испытывающих ударных нагрузок и изгиба. В случае, когда паяное соединение должно обладать высокой прочностью и хорошей сопротивляемостью ударным и изгибающим нагрузкам, в качестве припоев применяются латуни Л-62 и Л-68. Припои медно-цинковые поставляются в форме зерен.
[c.298]
Припой ПМЦ-36 применяется для пайки латуни Л-62, ПМЦ-42 — для пайки деталей из медных сплавов с температурой плавления выше 900—920° С, когда паяное соединение не подвергается ударным нагрузкам, вибрации и изгибу. Припой ПМЦ-54 применяют для пайки деталей из меди, бронзы и стали, не испытывающих ударных нагрузок и изгиба. В случае, когда паяное соединение должно обладать высокой прочностью и хорошей сопротивляемостью ударным и изгибающим нагрузкам, в качестве припоев применяются латуни Л-62 и Л-68. Припои медно-цинковые поставляются в форме зерен.
[c.298]
Применение индукционного нагрева обычно экономически оправдано при пайке среднеплавкими припоями (медь, латунь, ферромарганец, медно-серебряные сплавы) с температурой плавления 400—1200 °С. [c.219]
Припои. Различают легкоплавкие (мягкие) припои (оловянносвинцовые, висмутовые и кадмиевые) с температурой плавления до 300° С и тугоплавкие (твердые) припои (серебряные, медно-цинковые) с температурой плавления свыше 500° С.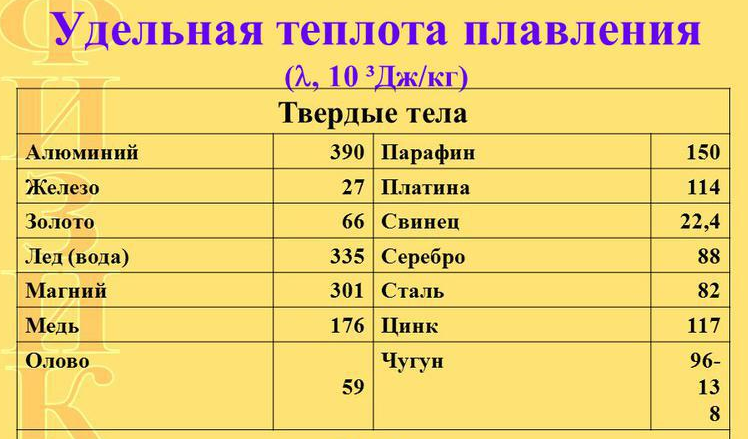 Мягкими припоями паяют медь, медные славы, луженую сталь, луженый никель и др. Наиболее распространенными мягкими припоями являются сплавы олова и свинца (с содержанием олова от 90 до 18%) — ПОС и сплавы олова, свинца и кадмия — ПОСК, или висмута — ПОСВ. Они отличаются малой твердостью и сравнительно низкими механическими
[c.407]
Мягкими припоями паяют медь, медные славы, луженую сталь, луженый никель и др. Наиболее распространенными мягкими припоями являются сплавы олова и свинца (с содержанием олова от 90 до 18%) — ПОС и сплавы олова, свинца и кадмия — ПОСК, или висмута — ПОСВ. Они отличаются малой твердостью и сравнительно низкими механическими
[c.407]
В случае пропитки медью железных или стальных прессовок составляющая основу железная матрица (или скелет) нагревается, находясь в контакте с медным сплавом, до температуры, несколько превышающей температуру плавления меди, обычно лежащей в диапазоне 1095-1150 °С. Под действием капиллярных сил расплавленный медный сплав проникает в сообщающиеся друг с другом поры и в идеальном случае заполняет весь объем пор. [c.87]
Сплавы на медной основе. При получении медных сплавов широко применяют лигатуры в виде двойных сплавов Си — Мп Си—N1 Си—81 Си—А1 Си—Р и др. Лигатурами называются сплавы металлов, температура плавления которых ниже температуры плавления тугоплавкого компонента, входящего в состав сплава. [c.222]
[c.222]
Твердый припой представляет собой тугоплавкий сплав с температурой плавления от 600 до 900° С. В табл. 35 приведен состав наиболее часто применяемых медно-цинковых и серебряных твердых припоев. [c.285]
Для пайки конструкционных сталей и сплавов чаще всего используют припои с температурой плавления до 1050 °С, для меди и медных сплавов — до температуры 800 °С. [c.456]
Железо с медью образует раствор, в котором предельная растворимость железа в меди при температуре плавления последней составляет около 3% (рис. 215). Но только при содержании в меди 10—15% железа можно получить сплав с температурой плавления 1330—1370 °С, близкой к температуре плавления чугунов. В этом случае обеспечивается смешиваемость составляющих самого расплава с чугуном. Однако после затвердевания наплавка представляет собой мягкую медную основу с различными по форме и величине вкраплениями очень твердой стальной составляющей. Эти включения и затрудняют механическую обработку металла. Частично диффундируя в основной металл, медь проявляет себя как графитизатор, поэтому на участке 1 околошовной зоны отбел проявляется слабо.
[c.363]
Эти включения и затрудняют механическую обработку металла. Частично диффундируя в основной металл, медь проявляет себя как графитизатор, поэтому на участке 1 околошовной зоны отбел проявляется слабо.
[c.363]
Медно-цинковые припои представляют собой двойные сплавы меди и цинка в разных соотношениях. От химического состава сплава зависит температура плавления его. Механические свойства медно-цинковых припоев также зависят от процентного содержания в них меди. [c.29]
В атмосфере углекислоты медь неустойчива. Хлор, бром и йод при температурах ниже точек плавления их соединений с медью разрушают ее, а с повышением температуры скорость коррозии сильно возрастает. Медь можно применять в газообразных НС1 и lo при температурах ниже 225 и 260° С соответственно. Азот не действует на медь п ее сплавы, а окислы азота разрушают медные сплавы. Аммиак также вызывает окисление меди и ее сплавов. В условиях диссоциации аммиака наблюдается водородная коррозия меди.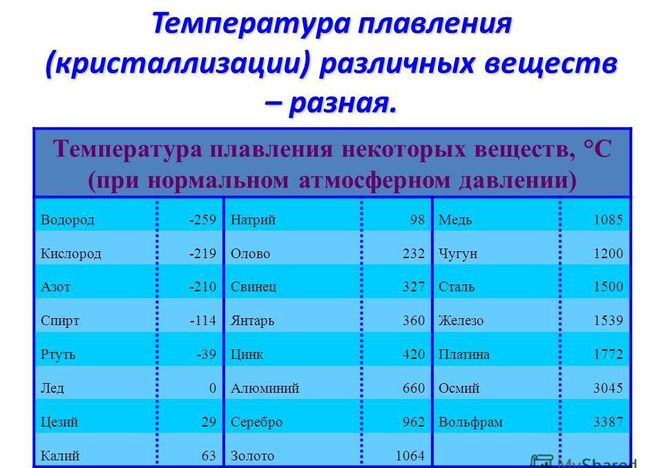 [c.255]
[c.255]
Для выплавки тугоплавких металлов (титана, хрома, циркония, ниобия, молибдена, вольфрама и рения) традиционные огнеупорные материалы (динас, магнезит, шамот, хромомагнезит) непригодны, так как они обладают недостаточной огнеупорностью (1300 — 1600°С), а температура плавления титанового сплава составляет более 2000°С. Поэтому все тугоплавкие технически чистые металлы выплавляют в специальных медных водоохлаждаемых тиглях-кристаллизаторах. [c.302]
Газовая сварка реализуется за счет оплавления газовым пламенем частей соединяемых деталей и прутка присадочного металла, она используется для соединения деталей из металлов и сплавов с различными температурами плавления при небольшой толщине (до 30 мм), а также для сварки неметаллических деталей. Для ее реализации не требуется источника электроэнергии. Широкое распространение имеет электродуговая сварка, при которой оплавленный (за счет электрической дуги) металл соединяемых элементов вместе с металлом электрода образует прочный шов. Для защиты от окисления шва электрод обмазывают защитным покрытием часто сварку производят под слоем флюса или в защитной среде инертных газов (аргона, гелия). Электродуговой сваркой на сварочных автоматах, полуавтоматах, а также вручную соединяют детали из конструкционных сталей, чугуна, алюминиевых, медных и титановых сплавов. Последние сваривают в среде аргона или гелия.
[c.469]
Для защиты от окисления шва электрод обмазывают защитным покрытием часто сварку производят под слоем флюса или в защитной среде инертных газов (аргона, гелия). Электродуговой сваркой на сварочных автоматах, полуавтоматах, а также вручную соединяют детали из конструкционных сталей, чугуна, алюминиевых, медных и титановых сплавов. Последние сваривают в среде аргона или гелия.
[c.469]
Возможна пайка друг с другом хорошо пригнанных деталей из сплава без внесения припоя при нагреве их выше температуры плавления меди (или медно-никелевого расплава) за счет капиллярного втягивания расплава в зазор. При этом детали не теряют своих размеров. [c.113]
Для стальных деталей припоем обычно служит чистая электролитическая медь (марки М1 и М2). Она весьма жидкотекуча в восстановительной атмосфере, даёт прочное, чистое соединение, не требует флюса, за исключением некоторых плохо смачиваемых сортов стали. Применение флюсов вообще удорожает процесс пайки и требует последующей очистки. Флюсы требуются при содержании в стали более 1—2о/о хрома, марганца, кремния, ванадия и алюминия, образующих окисные плёнки, не восстанавливаемые газовой атмосферой и ухудшающие смачивание. Никель, наоборот, усиливает смачивание и является желательным элементом в сталях для пайки. Иногда в качестве припоя используется латунь, которая обычно требует применения флюса для уменьшения окисления цинка и растворения образовавшейся окиси. В процессе пайки латунь может повышать температуру плавления вследствие испарения части цинка. С флюсом латунь растекается почти так же хорошо, как и чистая медь. Для меди и медных сплавов, не-
[c.448]
Флюсы требуются при содержании в стали более 1—2о/о хрома, марганца, кремния, ванадия и алюминия, образующих окисные плёнки, не восстанавливаемые газовой атмосферой и ухудшающие смачивание. Никель, наоборот, усиливает смачивание и является желательным элементом в сталях для пайки. Иногда в качестве припоя используется латунь, которая обычно требует применения флюса для уменьшения окисления цинка и растворения образовавшейся окиси. В процессе пайки латунь может повышать температуру плавления вследствие испарения части цинка. С флюсом латунь растекается почти так же хорошо, как и чистая медь. Для меди и медных сплавов, не-
[c.448]
Машинное масло — Теплоемкость 39 Медные сплавы — Температура плавления 71 Медный блеск 371 Медный колчедан 371 Медь 371 [c.718]
Газовую сварку чугуна цветными сплавами без подогрева детали в сочетании с дуговой сваркой широко применяют в ремонтном производстве для сварки трещин на обрабатываемых поверхностях корпусных деталей. Присадочным материалом для газовой сварки является латунь, которая более соответствует требованиям сварки по сравнению с другими цветными сплавами на медной основе. Температура плавления латуни ниже температуры плавления чугуна (880—950 °С), поэтому ее можно применить для сварки, не доводя чугун до плавления и не вызывая в нем особенных структурных изменений и внутренних напряжений.
[c.111]
Присадочным материалом для газовой сварки является латунь, которая более соответствует требованиям сварки по сравнению с другими цветными сплавами на медной основе. Температура плавления латуни ниже температуры плавления чугуна (880—950 °С), поэтому ее можно применить для сварки, не доводя чугун до плавления и не вызывая в нем особенных структурных изменений и внутренних напряжений.
[c.111]
Медно-никелевые электроды (монель МНЧ-2) состоят из 27—30 % меди и 66—68 % никеля [14]. Монель имеет температуру плавления 1260—1340 °С, что соответствует температуре плавления чугуна, и благодаря никелю хорошо сплавляется с чугуном. Однако этот сплав дает значительную усадку, что приводит к появлению высоких внутренних напряжений, способствующих образованию трещин. Поэтому монель наплавляют короткими валиками длиной 40—50 мм и сразу же после этого проковывают шов молотком. Прочность сварного соединения в этом случае не превышает 100 МПа.
[c. 117]
117]
Сплавы изготовляли в индукционной печи в вакууме путем нагрева S в толстостенных танталовых тиглях с последующим сбрасыванием в водоохлаждаемый медный приемник. Температуру плавления сплавов измеряли капельным методом. Часть диаграммы состояния системы показывает наличие в системе эвтектического равновесия Ж (pS ) + + (Та) при 1519 °С с эвтектической точкой при 3,2% (ат.) Та. Растворимость Та в жидком S можно описать уравнением lg(N) = А/Т + В, где Л — атомная доля Та в жидком S Г- температура (К) А — В = [c.261]
Пока мы знаем лишь один способ выращивания частиц второй фазы в теле металла — распад твердого раствора при старении. Известные на сегодня стареющие медные сплавы (в основном разные типы бронз) вполне могут использоваться для наших целей при температурах не выше 400—500 °С. При более высоких температурах их прочность резко падает. Однако для ряда отраслей промышленности нужны сплавы, сохраняющие свои свойства до 1000—1050 °С, т. е.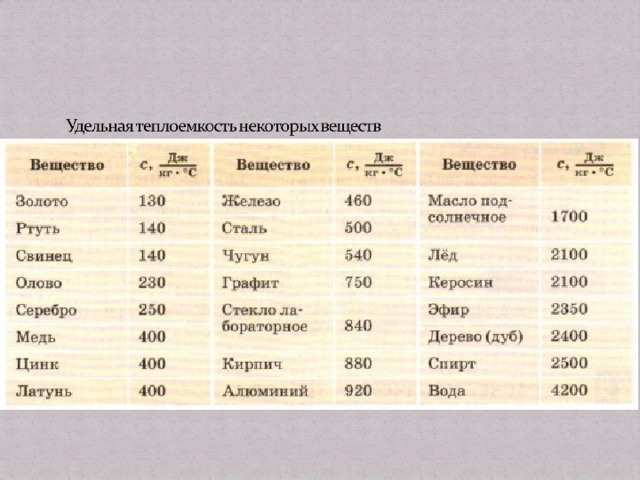 почти до температуры плавления меди. Поисками путей их изготовления мы сейчас и займемся.
[c.239]
почти до температуры плавления меди. Поисками путей их изготовления мы сейчас и займемся.
[c.239]
На фотографии (рис. 141), снятой через электронный микроскоп, прекрасно видны оксидные частицы, вкрапленные в медную матрицу. Строго говоря, матрица не чисто медная в ней содержатся и кислород (концентрации Со), и остаточный (не выведенный в оксид) алюминий. Однако из-за низкого порога реакции окисления алюминия его содержанием в меди можно безбоязненно пренебречь. По крайней мере, при рабочих температурах сопротивление этого твердого раствора почти такое же, как и чистой меди. Зато прочность сплава из-за присутствия оксидных частиц станет намного выше. Причем оксид алюминия — вещество тугоплавкое и в меди почти не растворяется. А поэтому упрочняющий эффект сохраняется вплоть до температуры плавления металла. [c.243]
Твердые припои имеют температуру плавления 850—900° С и представляют собой сплавы меди с цинком твердость и прочность паяного ими шва — повышенные.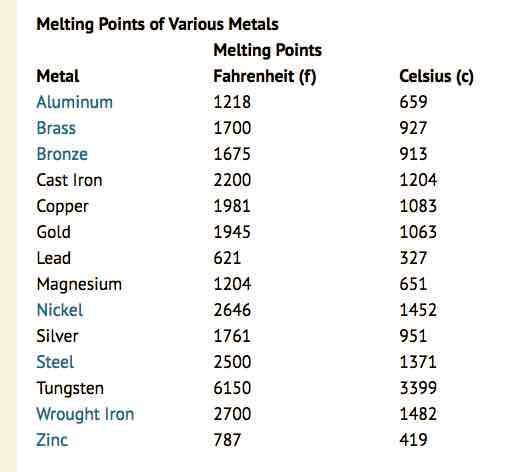 Серебряные припои состоят из серебра и меди температура плавления их 740—830° С они имеют ще большую прочность. Пайка ими медных проводов почти не меняет их электропроводность. И здесь прочность спая обеспечивается образованием твердого раствора между припоем и соединяемым металлом.
[c.462]
Серебряные припои состоят из серебра и меди температура плавления их 740—830° С они имеют ще большую прочность. Пайка ими медных проводов почти не меняет их электропроводность. И здесь прочность спая обеспечивается образованием твердого раствора между припоем и соединяемым металлом.
[c.462]
Спекание. Для спекания порошковых сплавов применяют электропечи с металлическим сопротивлением, с угольными сопротивлениями в виде труб и высокочастотные. Спекание производится в защитной атмосфере. Для спекания медных сплавов, железа и фрикционных материалов применяют защитные атмосферы, получаемые при частич ом сжигании газа. При спекании вольфрама, молибдена, твердых сплавов, магнитных и электротехнических материалов применяют водород. Температура спекания составляет примерно температуры плавления металла, например для меди 800—850° С, для железа — [c.479]
Сурьма находит применение в качестве легирующего компонента сплавов на свинцовой, оловянной и медной основе (баббитов, припоев, сплавов для литья под давлением и т.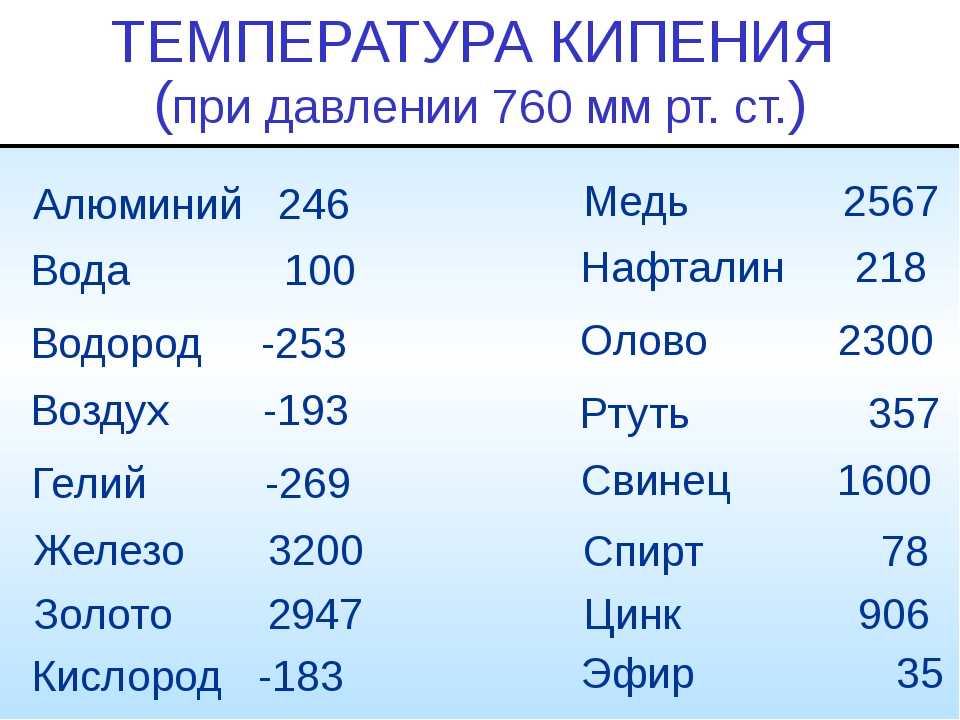 д.). Температура плавления сурьмы 630 °С плотность при 20 °С 6700 кг/м , при температуре плавления 6550 кг/м .
[c.144]
д.). Температура плавления сурьмы 630 °С плотность при 20 °С 6700 кг/м , при температуре плавления 6550 кг/м .
[c.144]
При температуре прессования медных сплавов 350—650 °С используют щелочно-фосфатные стекла с температурой плавления 350—400 °С [167] при 800—1000 °С — боросиликатные двух- и многокомпонентные стекла. [c.223]
К твердым припоям относят такие, температура плавления которых 600-1083 °С, а прочность спая высокая (ог =400-500 МПа). К этим припоям относят чистую медь и сплавы меди с цинком и серебром. Наиболее часто применяют медно-цинковые припои марок ПМЦ-42, ПМЦ-47, ПМЦ-52, которые содержат соответственно 42, 47 и 52 % меди и застывают в интервале температур 890-830 С. [c.347]
Пропитка пучков вольфрамовых волокон жидкими двойными медными сплавами осуществлялась в условиях, идентичных используемым ранее для композиций с матрицей из чистой меди. Содержание легирующего элемента каждого двойного медного сплава было ограничено количеством, которое позволило обеспечить температуру плавления, равную 1150° С или ния е, чтобы произвести пропитку при 1200° С. Сравнивалось влияние легирующих элементов на свойства композиций, упрочненных волокнами вольфрама, и системы, образованной взаимно нерастворимыми компонентами (в случае матрицы из чистой меди). В качестве легирующих элементов изучались алюминий, хром, кобальт, ниобий, никель и титан.
[c.240]
Сравнивалось влияние легирующих элементов на свойства композиций, упрочненных волокнами вольфрама, и системы, образованной взаимно нерастворимыми компонентами (в случае матрицы из чистой меди). В качестве легирующих элементов изучались алюминий, хром, кобальт, ниобий, никель и титан.
[c.240]
Марки оловянно-свинцовых припоев состоят из букв и цифр. Марка припоя, например, ПОС-90 означает П — припой О — олово С — свинец цифра 90 указывает, что в этом припое 90% (по весу) олова, остальное — свинец. Припой ПОСС-4-6 содержит олова— 4%, сурьмы — 6%, остальное — свинец. Твердые припои представляют собой тугоплавкие сплавы с температурой плавления от 700° С и выше. Они используются в тех случаях, когда необходимо получить высокую прочность соединения. В качестве твердых припоев наиболее часто применяют медно-цинковые и серебряные сплавы (табл. 22). [c.106]
Медно-цинковые Л68 ЛОК59-1-0,3 68 Си 32 2п 59 Си 39,7 2п 1 8п 0,3 81 940 905 Для пайки заготовок из углеродистой, легированной сталей и сплавов, имеющих температуру плавления выше 1000 С
[c. 279]
279]
При литье под давлением можно, как мы видели выше, получать отливки из сплавов, имеющих температуру плавления, не выше точки плавления медных сплавов. Производство литья поддавлением из черных сплавов в производственных масштабах пока еще не освоено. Кроме того, при литье поддавлением формы в большинстве случаев имеют линию разъема, что ограничивает область применения этого способа. [c.265]
Припои представляют собой сплавы цветных металлов сложного состава. Все припои по температуре плавления подразделяют на особо легкоплавкие (температура плавления с 145 °С), легкоплавкие (температура плавления 145с 450 °С), среднеилавкие (температура плавления 450 температура плавления >1050 °С). К особолегкоплавким и легкоплавким припоям относятся оловянно-свинцовые, на основе висмута, индия, кадмия, цинка, олова, свинца. К среднеплавким и высокоплавким припоям относятся медные, медно-цинковые, медно-никелевые, с благородными металлами (серебром, золотом, платиной). Припои изготовляют в виде прутков, проволок, листов, полос, спиралей, дисков, колец, зерен и т. д., укладываемых в место соединения.
[c.240]
Припои изготовляют в виде прутков, проволок, листов, полос, спиралей, дисков, колец, зерен и т. д., укладываемых в место соединения.
[c.240]
Серебро. Среди металлов серебро — наиболее низкоомный проводник величина р = 0,016 ом Температурный коэффициент сопротивления TKR = 3,6 10 /1 град. Температура плавления серебра 960° С. Серебро отличается небольшой твердостью оно является высокопластичным металлом, легко претерпевающим упругие деформации. Его окисление на воздухе при нормальной температуре протекает весьма медленно, поэтому его используют для покрытий проводников в высокочастотных элементах. При высоких частотах сопротивление посеребренного проводника может быть в десятки раз ниже, чем медного. При повышенных температурах (свыше 200° С) серебро на воздухе начинает окисляться. Если в воздухе присутствуют сернистые соединения, то на поверхности образуется слой сернистого серебра AgjS с высоким удельным сопротивлением. Для защиты серебряного покрытия от окисления и воздействия сернистых соединений в некоторых случаях, на него наносят слой лака или весьма тонкий слой (толщиной доли микрона) палладия. Из серебра выполняют электроды слюдяных и керамических конденсаторов проводниковые элементы схем, провода высокочастотных катушек и т. п. Серебро является компонентом различных сплавов и контактных материалов.
[c.274]
Из серебра выполняют электроды слюдяных и керамических конденсаторов проводниковые элементы схем, провода высокочастотных катушек и т. п. Серебро является компонентом различных сплавов и контактных материалов.
[c.274]
Возможно, что избирательный переход частиц меди в режиме трения, представленном на рис. 18, происходит отчасти благодаря образованию трибоплазмы в локальных точках в период приработки пар трения медный сплав — сталь, когда имеет место взаимодействие отдельных микровыступов контактных поверхностей. По-видимому, ИП в какой-то степени обусловлен субмикроплаз-менным напылением в местах фактического касания трущихся поверхностей продуктов возбуждения, в основном меди, так как температура плавления и прочность меди значительно меньше температуры плавления и прочности стали, и в плазме преобладают атомы и ионы меди наряду с другими более легкоплавкими, чем сталь, продуктами износа. Это предположение объясняет и многие другие экспериментальные данные. Например, почему ИП имеет место при трении пар никель—сталь, серебро—сталь, сталь—сталь (при наличии в смазке частиц меди) и проявляется только в местах фактического касания поверхностей. [c.43]
[c.43]
Литий — серебристо-белый очень мягкий металл, легко окисляющийся на воздухе. По ГОСТ 8774—75 устанавливаются три марки лития ЛЭ-1 (содержание чистого лития не менее 99,5%), Л9-2(98,8%) и ЛЭ-3 (98,0%). Применяется в машиностроении для дегазации и раскисления стали, чугуна, бронз и латуни, в баббитах — вместо олова для повышения температуры плавления и апти-фрикгцгонных свойств. Повышает качество алюминиевых, магниевых, медных, свинцовых и других сплавов, улучшает их антикоррозионные и литейные свойства и т. д., образует твердые припои для пайки без флюсов. Поставляетс.ч в виде чушек массой до 2,5 кг и хранится в плотно закрытых (запаянных) банках из белой жести (по 12—20 чушек — до 50 кг), залитых смесью трансформаторного масла (50%) и парафина (50%) с надписью Осторожно, от воды загорается . [c.170]
Никель и богатые никелем снлавы принадлежат к числу тугоплавких металлов. Данные о температурах плавления и разливки никеля и его сплавов приведены в табл. 183. Плавку ведут в отапливаемых мазутом или газом тиглях, индукционных печах типа Аякс и в высокочастотных электропечах. Особенно хорошие результаты даёт плавка в высокочастотных электропечах, снабжённых вакуумной установкой, последняя предотвращает поглощение газов жидким металлом. Ввиду высокой температуры плавления медно-нике-левых сплавов графитовые тигли непригодны, так как их материал разъедается расплавленным металлом, причём образуются карбиды
[c.193]
183. Плавку ведут в отапливаемых мазутом или газом тиглях, индукционных печах типа Аякс и в высокочастотных электропечах. Особенно хорошие результаты даёт плавка в высокочастотных электропечах, снабжённых вакуумной установкой, последняя предотвращает поглощение газов жидким металлом. Ввиду высокой температуры плавления медно-нике-левых сплавов графитовые тигли непригодны, так как их материал разъедается расплавленным металлом, причём образуются карбиды
[c.193]
Термодинамическая активность компонентов сплава характеризует концентрахщю свободных ионов, способных вступить во взаимодействие с кислородом. Она зависит от концентращ1и компонентов сплава и выражается формулой а — где с — концентрация компонента в сплаве у — коэффициент активности [ 16]. Термодинамическая активность является одной из важных предпосылок для образования в окааине окислов легирующих элементов. Наиболее пригодны в качестве основы никель и железо медные сплавы имеют относительно низкую температуру плавления. В гл. IV будут рассмотрены экспериментальные данные по исследованию наиболее распространенных сплавов для нагревателей.
[c.16]
В гл. IV будут рассмотрены экспериментальные данные по исследованию наиболее распространенных сплавов для нагревателей.
[c.16]
Фосфор является интенсивным рас-кислителем медных сплавов и упроч-нителем как по растворному типу, так и вследствие образования химических соединений. Фосфор снижает температуру плавления и улучшает практическую жид котеку честь. [c.199]
Некоторые критические температуры меди и ее сплавов — температуры плавления, отжига, рекристаллизации, сильного роста и пережога — приведены в табл. 3. Медные сплавы склонны к пережогу в интервале температур 800—900 °С. В медиых сплавах пережогу способствуют примеси висмута, в никелевых сплава — серы, т. е. приводящие к горячеломкости вследствие образования. чегкоплавких эвтектик с основой сплава. Для предотвращейия пережога медиых сплавов процесс пайки следует вести на 100 С ниже температуры их солидуса [12, 17]. [c.40]
ICSC 0303 — НАФТЕНАТ МЕДИ
ICSC 0303 — НАФТЕНАТ МЕДИ
| НАФТЕНАТ МЕДИ | ICSC: 0303 (Апрель 2006) |
| CAS #: 1338-02-9 |
| EINECS #: 215-657-0 |
| ОСОБЫЕ ОПАСНОСТИ | ПРОФИЛАКТИЧЕСКИЕ МЕРЫ | ТУШЕНИЕ ПОЖАРА | |
|---|---|---|---|
| ПОЖАР И ВЗРЫВ | Воспламеняющееся. При пожаре выделяет раздражающие или токсичные пары (или газы). При пожаре выделяет раздражающие или токсичные пары (или газы). | НЕ использовать открытый огонь, НЕ допускать образование искр, НЕ КУРИТЬ. | Использовать порошок, пену, двуокись углерода. В случае пожара: охлаждать бочки и т.д. распыляя воду. |
| СИМПТОМЫ | ПРОФИЛАКТИЧЕСКИЕ МЕРЫ | ПЕРВАЯ ПОМОЩЬ | |
|---|---|---|---|
| Вдыхание | См. примечания. | Применять вентиляцию. | Свежий воздух, покой. |
| Кожа | Покраснение. Шершавая кожа. | Защитные перчатки. | Снять загрязненную одежду. Ополоснуть и затем промыть кожу водой с мылом. |
| Глаза | Покраснение. | Использовать средства защиты глаз. | Промыть большим количеством воды в течение нескольких минут (снять контактные линзы, если это возможно сделать без затруднений). |
| Проглатывание | Не принимать пищу, напитки и не курить во время работы. Мыть руки перед едой. | Прополоскать рот. Дать выпить один или два стакана воды. Обратиться за медицинской помощью . | |
| ЛИКВИДАЦИЯ УТЕЧЕК | КЛАССИФИКАЦИЯ И МАРКИРОВКА |
|---|---|
| Индивидуальная защита: костюм химической защиты и респиратор с фильтром для органических газов и паров, подходящий для концентрации вещества в воздухе. НЕ допускать попадания этого химического вещества в окружающую среду. Как можно быстрее собрать пролитую жидкость в емкости с крышками. Тщательно собрать оставшееся. |
Согласно критериям СГС ООН
ОСТОРОЖНО
Горючая жидкость и пар Транспортировка |
| ХРАНЕНИЕ | |
Обеспечить огнестойкость. Отдельно от пищевых продуктов и кормов. Хранить в местах не имеющих сливов или доступа к канализации Отдельно от пищевых продуктов и кормов. Хранить в местах не имеющих сливов или доступа к канализации | |
| УПАКОВКА | |
| Не перевозить с продуктами питания и кормами для животных. |
Исходная информация на английском языке подготовлена группой международных экспертов, работающих от имени МОТ и ВОЗ при финансовой поддержке Европейского Союза. |
| НАФТЕНАТ МЕДИ | ICSC: 0303 |
| ФИЗИЧЕСКИЕ И ХИМИЧЕСКИЕ СВОЙСТВА | |
|---|---|
|
Агрегатное Состояние; Внешний Вид
Физические опасности
Химические опасности
|
|
| ВОЗДЕЙСТВИЕ НА ОРГАНИЗМ И ЭФФЕКТЫ ОТ ВОЗДЕЙСТВИЯ | |
|---|---|
|
Пути воздействия
Эффекты от кратковременного воздействия
|
Риск вдыхания
Эффекты от длительного или повторяющегося воздействия
|
| Предельно-допустимые концентрации |
|---|
| ОКРУЖАЮЩАЯ СРЕДА |
|---|
Это вещество попадает в окружающую среду при нормальном использовании. Однако следует проявлять большую осторожность, чтобы избежать какого-либо дополнительного высвобождения, например, при ненадлежащем удалении. Однако следует проявлять большую осторожность, чтобы избежать какого-либо дополнительного высвобождения, например, при ненадлежащем удалении. |
| ПРИМЕЧАНИЯ |
|---|
| Растворители-носители, используемые в коммерческих формуляциях, могут изменять физические и токсикологические свойства. Technical products contain between 1 and 12 % of copper. |
| ДОПОЛНИТЕЛЬНАЯ ИНФОРМАЦИЯ |
|---|
|
Классификация ЕС Символ: Xn, N; R: 10-22-50/53; S: (2)-60-61; Примечание: A |
| (ru) | Ни МОТ, ни ВОЗ, ни Европейский Союз не несут ответственности за качество и точность перевода или за возможное использование данной информации. © Версия на русском языке, 2018 |
Вольфрам | Plansee
Хорош во всех отношениях. Свойства вольфрама
Свойства вольфрама
Вольфрам относится к группе тугоплавких металлов, то есть металлов, температура плавления которых выше, чем у платины (1772 °C). В тугоплавких металлах энергия связи между отдельными атомами особенно высока. Такие металлы отличаются высокой температурой плавления и одновременно низким давлением пара, хорошей жаропрочностью, а в случае вольфрамо-медных композитов — еще и высоким модулем упругости. Для них также характерны низкий коэффициент теплового расширения и относительно высокая плотность.
Вольфрам имеет самую высокую температуру плавления среди всех металлов, а также чрезвычайно высокий модуль упругости. В целом его свойства аналогичны молибдену. Оба металла относятся к одной группе в периодической системе химических элементов. Однако некоторые свойства вольфрама более ярко выражены по сравнению с молибденом. Благодаря превосходным термическим свойствам вольфрам легко выдерживает самые высокие температуры.
Чтобы придать выпускаемому вольфраму и его сплавам нужные свойства, мы используем разные виды и количества легирующих элементов и соответствующим образом настраиваем технологический процесс.
Мы используем преимущественно легированные вольфрамовые материалы. Например, в WVM и WК65 добавляется небольшое количество калия. Калий положительно влияет на механические свойства материала, особенно при высоких температурах. Добавлением La2O3 можно не только улучшить обрабатываемость сплава, но и, что особенно важно, снизить работу выхода электронов, что позволит использовать вольфрам для изготовления катодов.
Рений мы добавляем, чтобы повысить пластичность вольфрама. Медь же улучшает электропроводность материала. Благодаря хорошей обрабатываемости наши тяжелые сплавы подходят также для производства изделий сложной геометрии. Они могут использоваться, например, в качестве материала для экранирующих пластин или амортизирующих и абсорбирующих компонентов.
Медь Температура плавления и физико-химические свойства
Медь (от латинского cuprum ) — очень популярный химический элемент, относящийся к группе переходных металлов. Его добывали в древности на Кипре, отсюда и его латинское название. Проверим, какими свойствами обладает медь и при какой температуре она плавится.
Его добывали в древности на Кипре, отсюда и его латинское название. Проверим, какими свойствами обладает медь и при какой температуре она плавится.
Свойства меди
Медь
славится отличной электропроводностью (59,6⋅10 6 См/м) и теплопроводностью.Он имеет плотность 8,96 г/см³ и легко поддается обработке, как в холодном, так и в горячем виде (при температуре 650–800 °С). Интересен тот факт, что медь является одним из четырех металлов с естественным цветом, отличным от серого или серебряного (например, осмий голубоватый, а желтоватый становится золотым и цезием). В нормальных условиях чистая медь окрашивается в оранжево-красный цвет, но темнеет из-за окисления на открытом воздухе. Медь, как и алюминий, может быть успешно переработана, как и алюминий.
Температура плавления меди
Медь плавится при 1084,62°С . Температура кипения, в свою очередь, составляет 2562 °С.
Интересно, что медь является третьим наиболее извлекаемым металлом после железа и алюминия по объему. По глобальным оценкам, используется до 80% когда-либо добытой меди. Неудивительно, поскольку, по данным « The World Copper Factbook », переработка в 2002–2008 годах обеспечивала почти 35% потребляемой меди.Еще одним интересным фактом является то, что медь в небольших количествах попадает в питьевую воду из медной сантехники, а в теплой воде ее больше.
По глобальным оценкам, используется до 80% когда-либо добытой меди. Неудивительно, поскольку, по данным « The World Copper Factbook », переработка в 2002–2008 годах обеспечивала почти 35% потребляемой меди.Еще одним интересным фактом является то, что медь в небольших количествах попадает в питьевую воду из медной сантехники, а в теплой воде ее больше.
Можно ли плавить медь в домашних условиях? Теоретически можно, но это достаточно сложная задача с точки зрения подготовки позиции. Во-первых, проблема может заключаться в генерации достаточно высокой температуры — более тысячи градусов по Цельсию. Как правило, пропан-кислородная горелка и подходящий сосуд, напр.глиняный тигель. Также эффективно построить самодельную коксовую печь с солидным дутьем.
Кшиштоф Камзол
Главный редактор Joblife.pl
.
Основы физики: тепло, термодинамика
Внутренняя энергия пленки, часть 1 и 2 (начало прибл. 37 мин 30 с), температура
37 мин 30 с), температура
Температурное расширение кузова пленка
Определение удельной теплоемкости воды. фильм
Пример расчета удельной теплоемкости (введение в баланс) фильм
Тест 2017 для обучения ответ
Теоретические вопросы к тесту:
- Дайте определение первому закону термодинамики. Сохраните шаблон.
- Введите определение теплоты и запишите формулу.
- Введите определение удельной теплоемкости и напишите формулу
- Объясните, что такое тепловой баланс.
- Введите определение теплоты плавления и запишите формулу.
- Введите формулу для перевода температуры из градусов Кельвина в градусы Цельсия и наоборот.
- Введите определения теплоты парообразования и запишите формулу.
Примеры задач (аналогичные), которые могут возникнуть при испытании:
- Какая температура установится в сосуде, если бросить 1 кг меди при температуре 200 0 С в 10 литров воды при температуре из 70 0 С? Удельная теплоемкость воды 4200 Дж/кг 0 С.
 Удельная теплоемкость меди 380 Дж/кг 0 С.
Удельная теплоемкость меди 380 Дж/кг 0 С. - Керосин в баке был нагрет до 5 0 С, потреблено 21000 Дж тепла. Сколько керосина было в баке? cN = 2100 Дж/кг 0 С.
- Преобразование из абсолютной шкалы температуры 33 К в градусы 0 С и из шкалы Цельсия температуры -60 0 С в градусы К.
- Какая температура установится в сосуде, если в 20 литров воды при 30 0 С бросить 800 г меди при 100 0 С? Удельная теплоемкость воды 4200 Дж/кг 0 С.Удельная теплоемкость меди 380 Дж/кг 0 С. (4 балла)
- Кусок железа массой 1 кг и температурой 100 0 С остыл до температуры 10 0 С. Рассчитайте энергию (тепло), выделившуюся в окружающую среду. cFe = 450 Дж/кг 0 С. (3 балла)
- Преобразование абсолютной температуры 45 К в градусы 0 С и температуры по шкале Цельсия -250 0 С в градусы К.
.
Температура плавления некоторых металлов, их сплавов и сталей в градусах Цельсия.
Температура плавления некоторых металлов и их сплавов и сталей в градусах Цельсия.
| Металл | Температура плавления |
|---|---|
| Латунь (Cu-69%, Zn 30%, Sn-1%) | 900 — 940 |
| Алюминий | 660 |
| Алюминиевые сплавы | 463 — 671 |
| Алюминиевая бронза | 600 — 655 |
| Сурьма | 630 |
| Берилл | 1285 |
| Медный берилл | 865 — 955 |
| Висмут | 271.4 |
| Латунь | 1000 — 930 |
| Кадмий | 321 |
| Серый чугун | 1175 — 1290 |
| Хром | 1860 |
| Кобальт | 1495 |
| Медь | 1084 |
| Мельхиор | 1170 — 1240 |
| Золото, 24К | 1063 |
| Хастеллой С | 1320 — 1350 |
| Инконель | 1390 — 1425 |
| Инколой | 1390 — 1425 |
| Иридий — Иридий | 2450 |
| Кованое железо | 1482 — 1593 |
| Чугун, серый чугун | 1127 — 1204 |
| Ковкий чугун | 1149 |
| Свинец | 327,5 |
| Магний | 650 |
| Магниевые сплавы | 349 — 649 |
| Марганец | 1244 |
| Марганцево-коричневый | 865 — 890 |
| Меркурий | |
| Молибден | 2620 |
| Монель | 1300 — 1350 |
| Никель | 1453 |
| Ниобий (колумбий) | 2470 |
| Осм | 3025 |
| Палладий | 1555 |
| Люминофор | 44 |
| Платина | 1770 |
| Плутон | 640 |
| Калий | 63.3 |
| Красная латунь | 990 — 1025 |
| Рен | 3186 |
| Стержень | 1965 |
| Рутений | 2482 |
| Селен | 217 |
| Кремний | 1411 |
| Серебро, Монета | 879 |
| Чистое серебро | 961 |
| Серебро 92,5% + надбавка | 893 |
| Натрий | 97.83 |
| Углеродистая сталь | 1425 — 1540 |
| Нержавеющая сталь | 1510 |
| Тантал | 2980 |
| Трек | 1750 |
| Олово | 232 |
| Титан | 1670 |
| Вольфрам | 3400 |
| Уран | 1132 |
| Ванадий | 1900 |
| Желтая латунь | 905 — 932 |
| Цинк | 419. 5 5 |
| Циркон | 1854 |
.
Точка плавления меди / Paulturner-Mitchell.com
Историки предполагают, что первобытные люди находили медь в виде самородков, иногда достигавших значительных размеров. Латинское название меди (Cuprum) происходит от острова Кипр, где ее добывали древние греки. Благодаря тому, что температура плавления меди не очень высока и составляет 1083°С, медные самородки или руды можно переплавлять на костре. Это обеспечило производство меди и позволило использовать ее в изготовлении оружия и предметов быта.
Несмотря на то, что медь с древних времен широко использовалась людьми, распространяясь по земной коре, среди других элементов они занимают 23-е место. Чаще всего встречается в природе в виде соединений, входящих в состав сульфидных руд. Наиболее распространенными из них являются медный блеск и медный колчедан. Существует несколько технологий получения меди из руды, и каждая из них имеет несколько стадий.
Как уже было сказано, низкотемпературная плавка меди позволяла эффективно ее перерабатывать еще в самом начале развития цивилизации.И надо отдать должное древней металлургии, их возможностям получать и использовать не только чистую медь, но и ее сплавы. Плавление – это переход металла из твердого состояния в жидкое. Для этого использовали нагрев, а низкая температура плавления меди позволяла успешно проводить такую операцию.
Затем в жидкую медь добавляли олово или олово, извлекая его из касситерита (оловосодержащей руды) на поверхности меди. В результате они получили бронзу, более прочную, чем купрум, и использовали ее для изготовления оружия.Теперь, однако, я хотел бы более подробно остановиться на операции плавки, позволяющей получить из руды достаточно чистый материал.
Температура плавления каждого металла своя и зависит от наличия примесей в исходном материале. Так, медь, имеющая температуру плавления 1083°С, при добавлении олова образует бронзу, которая в зависимости от содержания олова плавится при 930-1140°С.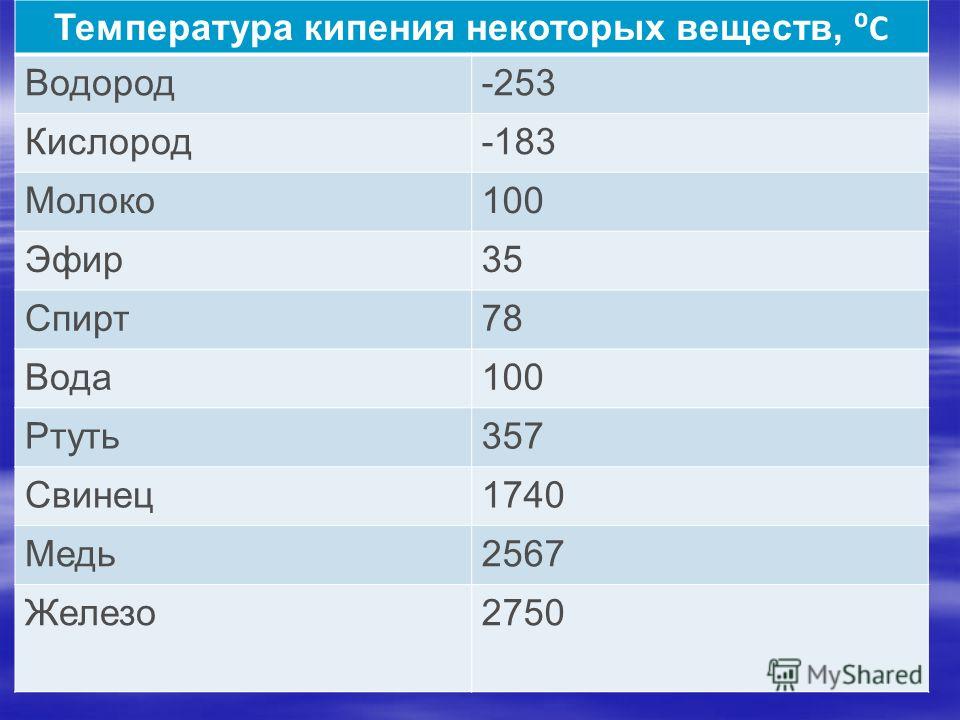 Латунь, сплав меди и цинка, имеет температуру плавления 900-1050°С.
Латунь, сплав меди и цинка, имеет температуру плавления 900-1050°С.
В процессе нагрева металл разрушается в кристаллической решетке. Вначале по мере нагревания температура повышается, а затем, начиная с некоторого значения, остается постоянной, хотя нагрев продолжается. В этот момент он тает. Это продолжается до тех пор, пока весь металл не растворится, и только тогда температура начнет повышаться. Это касается всех металлов, температура плавления меди также не меняется.
После охлаждения картина обратная: сначала температура снижается до начала затвердевания металла, затем остается постоянной и после полного отверждения металла снова начинает снижаться.Такое поведение металла, если его нанести на график, называется фазовой диаграммой, показывающей состояние, в котором находится вещество при определенной температуре. Для ученых фазовая диаграмма является одним из инструментов изучения поведения металлов при плавлении.
Если продолжать нагревать расплавленный металл, то при определенной температуре начинается процесс, аналогичный кипению. Так, температура кипения меди составляет 2560 °С. Название процесс получил из-за внешнего сходства с кипением жидкостей, когда начинают выделяться пузырьки газа.То же самое происходит и с металлом, например, при достаточно высокой температуре расплавленного железа начинает улетучиваться образовавшийся при окислении углерод.
Так, температура кипения меди составляет 2560 °С. Название процесс получил из-за внешнего сходства с кипением жидкостей, когда начинают выделяться пузырьки газа.То же самое происходит и с металлом, например, при достаточно высокой температуре расплавленного железа начинает улетучиваться образовавшийся при окислении углерод.
В статье рассматривается процесс плавления металлов, дается понятие температуры плавления и ее поведение при плавлении. Объяснил, насколько низкой была температура плавления меди для развития цивилизации и металлургии.
.
Физические свойства металлов. Температура плавления и плотность металлов и сплавов
Температура плавления металлов, которая колеблется от низшей (-39°С для ртути) до высшей (3400°С для вольфрама), а также плотность твердых металлов при 20°С и плотность жидких металлов при температуры плавления приведены в таблице плавки цветных металлов .
Таблица 1. Выплавка цветных металлов
Атомный вес | Температура плавления t и , °С | Плотность ρ , г/см3 | ||
устойчивый при 20°С | редко в т и | |||
Алюминий | ||||
Вольфрам | ||||
Марганец | ||||
молибден | ||||
Циркон | ||||
Сварка и плавка цветных металлов
Сварка меди . Температура плавления металлической Cu почти в шесть раз выше температуры плавления стали, медь интенсивно поглощает и растворяет различные газы, образуя с кислородом оксиды. Оксид меди II с медью образует эвтектику, температура плавления которой (1064 °С) ниже, чем у меди (1083 °С). Когда жидкая медь затвердевает, эвтектика располагается по границам зерен, что делает медь хрупкой и склонной к растрескиванию. Поэтому основной задачей при сварке меди является защита ее от окисления и активное раскисление сварочной ванны.
Температура плавления металлической Cu почти в шесть раз выше температуры плавления стали, медь интенсивно поглощает и растворяет различные газы, образуя с кислородом оксиды. Оксид меди II с медью образует эвтектику, температура плавления которой (1064 °С) ниже, чем у меди (1083 °С). Когда жидкая медь затвердевает, эвтектика располагается по границам зерен, что делает медь хрупкой и склонной к растрескиванию. Поэтому основной задачей при сварке меди является защита ее от окисления и активное раскисление сварочной ванны.
Наиболее распространена газовая сварка меди кислородно-ацетиленовым пламенем с использованием горелок в 1,5…2 раза мощнее стальной сварочной горелки. Связующее — медные стержни, содержащие фосфор и кремний. Если толщина изделий больше 5…6 мм, их сначала нагревают до температуры 250…300°С. Сварочные флюсы представляют собой обожженную буру или смесь 70 % буры и 30 % борной кислоты. Повышают механические свойства и улучшают структуру наплавленного металла, медь после сварки проковывают при температуре ок. 200…300°С. Затем его повторно нагревают до 500-550°С и охлаждают в воде. Медь также сваривают электродугой с электродами, в токе защитных газов, под слоем флюса, на конденсаторных машинах методом трения.
200…300°С. Затем его повторно нагревают до 500-550°С и охлаждают в воде. Медь также сваривают электродугой с электродами, в токе защитных газов, под слоем флюса, на конденсаторных машинах методом трения.
сварка латуни . Латунь представляет собой сплав меди и цинка (до 50%). Основным загрязнением в этом случае является испарение цинка, в результате чего шов теряет свои свойства, в нем появляются поры.Латунь, как и медь, в основном сваривают ацетиленовым окислительным пламенем, которое образует на поверхности ванны пленку тугоплавкого оксида цинка, ограничивающую дальнейшее прогорание и испарение цинка. Флюсы используются так же, как и для сварки меди. Они образуют на поверхности ванны шлаки, которые связывают оксиды цинка и затрудняют выход паров из сварочной ванны. Латунь также сваривают в защитных газах и на контактных машинах.
бронзовая сварка .В большинстве случаев бронза является литейным материалом, поэтому сварка
применяется при устранении дефектов или при ремонте. Наиболее часто используется сварка металлическим электродом. Связующее изготавливается из стержней того же состава, что и основной металл, а флюсы или покрытие электродов представляют собой соединения хлоридов и фторидов калия и натрия.
Наиболее часто используется сварка металлическим электродом. Связующее изготавливается из стержней того же состава, что и основной металл, а флюсы или покрытие электродов представляют собой соединения хлоридов и фторидов калия и натрия.
. Основными факторами, препятствующими сварке алюминия, являются его низкая температура плавления (658°С), высокая теплопроводность (примерно в 3 раза выше теплопроводности стали), образование тугоплавких оксидов алюминия, имеющих температуру плавления 2050°С. С, т.е. технология плавки цветных металлов , , такие как медь или бронза, не подходят для плавки алюминия.Кроме того, эти оксиды плохо реагируют как с кислотными, так и с основными флюсами и поэтому плохо удаляются из сварного шва.
Самый распространенный факел для газовой сварки алюминия с ацетиленом. В последние годы получили широкое распространение также сварка под флюсом и автоматическая дуговая сварка металлическими электродами в среде аргона. Для всех способов сварки, за исключением аргонодуговой, применяют флюсы или электродные покрытия, в состав которых входят соединения фтора и хлора, лития, калия, натрия и других элементов. Проволока или стержни того же состава, что и основной металл, используются в качестве связующего для всех способов сварки.
Проволока или стержни того же состава, что и основной металл, используются в качестве связующего для всех способов сварки.
Алюминий хорошо сваривается электронным лучом в вакууме, на контактных машинах, электрошлаковым и другими способами.
Сварка алюминиевых сплавов . Алюминиевые сплавы с магнием и цинком свариваются без особых осложнений
, так же как и алюминий. Исключение составляет дюралюминий – алюминиево-медные сплавы.Эти сплавы термически упрочняются после закалки и последующего старения. При температуре плавления цветных металлов выше 350°С в них происходит снижение прочности, не восстанавливаемое термической обработкой. Поэтому при сварке дюралюминия в околошовной зоне прочность падает на 40…50 %. Если дюраль сваривают в защитных газах, то такое снижение можно восстановить термической обработкой до 80…90 % по отношению к прочности основного металла.
Сварка магниевых сплавов . При газовой сварке обязательно применяют фторидные флюсы, которые в отличие от хлоридных флюсов не вызывают коррозии сварных соединений.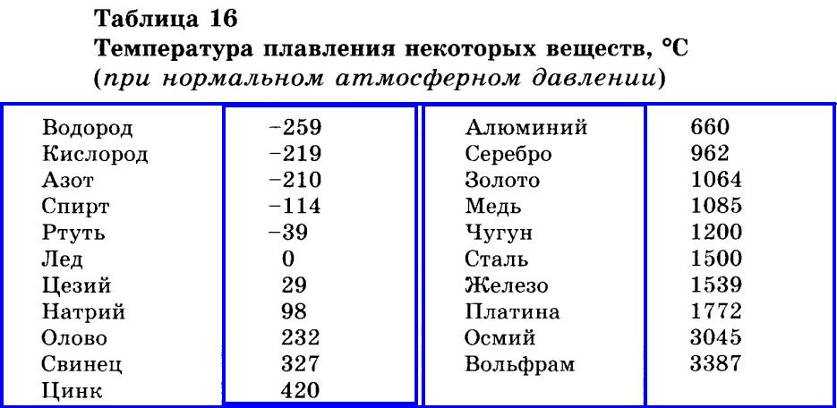 Дуговая сварка магниевых сплавов металлическими электродами из-за низкого качества сварных швов до сих пор не применялась. При сварке магниевых сплавов наблюдается значительное увеличение зерна на участках, близких к шву, и сильное развитие столбчатых кристаллов в шве.Поэтому предел прочности сварных соединений составляет 55…60 % предела прочности основного металла.
Дуговая сварка магниевых сплавов металлическими электродами из-за низкого качества сварных швов до сих пор не применялась. При сварке магниевых сплавов наблюдается значительное увеличение зерна на участках, близких к шву, и сильное развитие столбчатых кристаллов в шве.Поэтому предел прочности сварных соединений составляет 55…60 % предела прочности основного металла.
Таблица 2. Физические свойства промышленных цветных металлов
Недвижимость | М м и высокий | |||||||||||
Атомный номер | ||||||||||||
Атомный вес | ||||||||||||
при температуре 20°С, кг/м² 3 | ||||||||||||
Температура плавления, °С | ||||||||||||
Температура кипения, °С | ||||||||||||
Атомный диаметр, нм | ||||||||||||
Скрытая теплота плавления, кДж/кг | ||||||||||||
Скрытая теплота парообразования | ||||||||||||
Удельная теплоемкость при температуре 20°С, Дж/(кг . | ||||||||||||
Удельная теплопроводность, 20°С, Вт/(м — °С) | ||||||||||||
Коэффициент линейного расширения при температуре 25°С, 10 6 — ° З — 1 | ||||||||||||
Удельное электрическое сопротивление при температуре 20°С, мкОм — м | ||||||||||||
Модуль нормальной упругости, ГПа | ||||||||||||
Модуль сдвига, ГПа | ||||||||||||
Плавильный тигель
Неотъемлемой частью производства металла и металлических изделий является их использование в процессе производства тиглей для производства, плавки и переплава черных и цветных металлов. Тигли являются составной частью металлургического оборудования для литья различных металлов, сплавов и тому подобного.
Тигли являются составной частью металлургического оборудования для литья различных металлов, сплавов и тому подобного.
Керамический тигель для плавки цветных металлов используется для плавки металлов (медь, бронза) с древних времен.
После кристаллизации убедитесь, что вещество достаточно чистое. Наиболее простым и эффективным методом выявления и определения меры чистоты вещества является определение его температуры плавления ( Т пл). Температура плавления – это диапазон температур, при котором твердое вещество становится жидким.Все чистые химические вещества имеют узкий температурный диапазон перехода из твердого состояния в жидкое. Этот диапазон температур для чистых веществ составляет максимум 1-2 o C. Использование температуры плавления в качестве меры чистоты вещества основано на том, что наличие примесей (1) снижает температуру плавления и ( 2) расширяет диапазон температур плавления. Например, чистый образец бензойной кислоты плавится в интервале 120-122°С, а слабозагрязненный образец плавится при 114-119°С.
Использование температуры плавления для идентификации, конечно, сопряжено с большой неопределенностью, поскольку существует несколько миллионов органических соединений, и многие из них неизбежно совпадают с их точками плавления. Однако, во-первых, Т мкл вещества, полученного в синтезе, почти всегда отличается от Т мкл исходных соединений. Во-вторых, можно использовать технику «задания температуры плавления смешанного образца». Если Т пл смеси равных количеств испытуемого вещества и известного образца не отличаются от Т пл последнего, то оба образца представляют собой одно и то же вещество.
МЕТОД ОПРЕДЕЛЕНИЯ ТЕМПЕРАТУРЫ ПЛАВЛЕНИЯ . Тщательно растереть испытуемое вещество в мелкий порошок. Капилляр заполняют веществом (высотой 3-5 мм; капилляр должен быть тонкостенным, запаянным с одной стороны, внутренним диаметром 0,8-1 мм и высотой 3-4 см). Для этого осторожно вдавливают открытый конец капилляра в порошок вещества и периодически постукивают его запаянным концом о поверхность стола 5-10 раз. Для полного вытеснения порошка к запаянному концу капилляра его насыпают в вертикальную стеклянную трубку (длиной 30-40 см и диаметром 0,5-1 см) на твердой поверхности.Вставьте капилляр в металлический патрон, прикрепленный к наконечнику термометра (рис. 3.5), и поместите термометр с патроном в прибор для определения температуры плавления.
Для полного вытеснения порошка к запаянному концу капилляра его насыпают в вертикальную стеклянную трубку (длиной 30-40 см и диаметром 0,5-1 см) на твердой поверхности.Вставьте капилляр в металлический патрон, прикрепленный к наконечнику термометра (рис. 3.5), и поместите термометр с патроном в прибор для определения температуры плавления.
В приборе термометр с капиллярами нагревается электрической катушкой, напряжение на которую подается через трансформатор, а скорость нагрева зависит от приложенного напряжения. Сначала аппарат нагревают со скоростью 4-6°С в минуту и на 10°С, а затем ожидаемый Т пл нагревают со скоростью 1-2°С в минуту.За температуру плавления принимают расстояние от размягчения кристаллов (смачивания вещества) до полного их плавления.
Полученные данные заносятся в лабораторный журнал.
Перегонка
Дистилляция является важным и широко используемым методом очистки органических жидкостей и разделения жидких смесей. Этот метод включает кипячение и испарение жидкости, а затем конденсацию паров в дистиллят. Разделение двух жидкостей, имеющих разность температур кипения 50-70°С и более, можно осуществить простой перегонкой.Если разница меньше, необходимо применять фракционную перегонку в более сложном аппарате. Некоторые жидкости с высокой температурой кипения разлагаются при перегонке. Однако при падении давления температура кипения падает, что позволяет перегонять высококипящие жидкости без разложения в вакууме.
Этот метод включает кипячение и испарение жидкости, а затем конденсацию паров в дистиллят. Разделение двух жидкостей, имеющих разность температур кипения 50-70°С и более, можно осуществить простой перегонкой.Если разница меньше, необходимо применять фракционную перегонку в более сложном аппарате. Некоторые жидкости с высокой температурой кипения разлагаются при перегонке. Однако при падении давления температура кипения падает, что позволяет перегонять высококипящие жидкости без разложения в вакууме.
При котором кристаллическая решетка металла разрушается и переходит из твердого состояния в жидкое.
Температура плавления металлов — показатель температуры нагретого металла, при которой начинается процесс (плавление).Сам процесс противоположен кристаллизации и неразрывно с ней связан. Расплавить металл? Он должен быть нагрет внешним источником, нагрет до точки плавления, а затем продолжать обеспечивать тепло для преодоления энергии фазового перехода. Дело в том, что значение температуры плавления металлов само по себе указывает на температуру, при которой материал будет находиться в фазовом равновесии на границе жидкость-твердое тело. При этой температуре чистый металл может находиться как в твердом, так и в жидком состоянии одновременно.Для осуществления процесса плавления необходимо перегреть металл немного выше равновесной температуры, чтобы обеспечить положительный термодинамический потенциал. Усильте процесс.
При этой температуре чистый металл может находиться как в твердом, так и в жидком состоянии одновременно.Для осуществления процесса плавления необходимо перегреть металл немного выше равновесной температуры, чтобы обеспечить положительный термодинамический потенциал. Усильте процесс.
Температура плавления металлов постоянна только для чистых веществ. Наличие примесей будет смещать равновесный потенциал в ту или иную сторону. Это связано с тем, что металл с примесями образует другую кристаллическую решетку, и силы взаимодействия атомов в них будут отличаться от таковых в чистых материалах.В зависимости от температуры плавления металлы делят на легкоплавкие (до 600°С, например галлий, ртуть), среднеплавкие (600-1600°С, медь, алюминий) и тугоплавкие (>1600°С, вольфрам, молибден).
В современном мире чистые металлы редко используются из-за их ограниченных физических свойств. В промышленности давно и плотно используются различные сочетания металлов — сплавов, разновидностей и свойств которых гораздо больше. Температура плавления металлов, из которых состоят различные сплавы, также будет отличаться от точки плавления их сплава.Различные концентрации веществ определяют порядок их плавления или кристаллизации. Однако существуют равновесные концентрации, при которых металлы, входящие в состав сплава, затвердевают или плавятся одновременно, т. е. ведут себя как однородный материал. Такие сплавы называются эвтектическими.
Температура плавления металлов, из которых состоят различные сплавы, также будет отличаться от точки плавления их сплава.Различные концентрации веществ определяют порядок их плавления или кристаллизации. Однако существуют равновесные концентрации, при которых металлы, входящие в состав сплава, затвердевают или плавятся одновременно, т. е. ведут себя как однородный материал. Такие сплавы называются эвтектическими.
Знание температуры плавления очень важно при работе с металлом, это значение необходимо как на производстве, для расчета параметров сплава, так и при эксплуатации металлических изделий, когда изменяется температура фазового перехода материала, из которого изготовлено изделие делается решает.ограничения в его использовании. Для удобства эти данные сведены в единую плавку металлов — суммарный результат физических характеристик различных металлов. Аналогичные таблицы есть и для сплавов. Температура плавления металлов также зависит от давления, поэтому данные в таблице приведены для конкретного значения давления (обычно это нормальные условия, когда давление составляет 101,325 кПа). Чем выше давление, тем выше температура плавления, и наоборот.
Чем выше давление, тем выше температура плавления, и наоборот.
Одним из основных направлений в металлургической промышленности является литье металлов и их сплавов в связи с дешевизной и относительной простотой процесса.Вы можете отливать формы любого контура различных размеров, от маленьких до больших; подходит как для массового производства, так и для индивидуального производства.
Литье является одним из древнейших направлений металлообработки и берет свое начало примерно в бронзовом веке: 7-3 тысячелетия до н.э. мне. С тех пор было открыто много материалов, что привело к технологическому прогрессу и повышению требований в литейной промышленности.
В настоящее время существует множество направлений и видов литья, отличающихся технологическим процессом.Одно остается неизменным – физическое свойство металлов переходить из твердого состояния в жидкое, и важно знать, при какой температуре начинают плавиться разные виды металлов и их сплавов.
процесс плавки металла
Этот процесс относится к переходу вещества из твердого состояния в жидкое. После достижения температуры плавления металл может быть как твердым, так и жидким, дальнейший рост приведет к полному жидкостному переходу материала.
После достижения температуры плавления металл может быть как твердым, так и жидким, дальнейший рост приведет к полному жидкостному переходу материала.
То же самое происходит и при затвердевании — как только будет достигнута точка плавления, вещество начнет переходить из жидкого состояния в твердое, а температура не изменится до полной кристаллизации.
При этом следует помнить, что это правило распространяется только на голое железо. Сплавы не имеют четкого температурного предела и совершают переходы состояний в определенном диапазоне:
- Солидус — Температурная линия, при которой наиболее легкоплавкий компонент сплава начинает плавиться.
- Ликвидус – это конечная температура плавления всех компонентов, ниже которой начинают появляться первые кристаллы сплава.
Точка плавления таких веществ не может быть точно измерена, точка перехода состояния указывает числовой диапазон.
В зависимости от температуры, при которой начинается плавление металлов, их принято делить на:
- Плавкий до 600°С.
 К ним относятся цинк, свинец и другие.
К ним относятся цинк, свинец и другие. - Среднеплавкий, до 1600°С.Наиболее распространены сплавы и металлы, такие как золото, серебро, медь, железо, алюминий.
- Огнеупорный материал, температура выше 1600°С. Титан, молибден, вольфрам, хром.
Существует также точка кипения — точка, при которой расплавленный металл начинает выделяться газом. Он очень теплый, обычно в 2 раза выше температуры плавления.
Влияние давления
Температура плавления и равная ему температура замерзания зависят от давления, которое увеличивается с ростом давления.Это связано с тем, что при увеличении давления атомы сближаются друг с другом и должны быть отодвинуты, чтобы разрушить кристаллическую решетку. Для высокого кровяного давления требуется больше энергии теплового движения, и соответствующая температура плавления увеличивается.
Существуют исключения, когда температура, необходимая для сжижения, снижается с увеличением давления. К таким веществам относятся лед, висмут, германий и сурьма.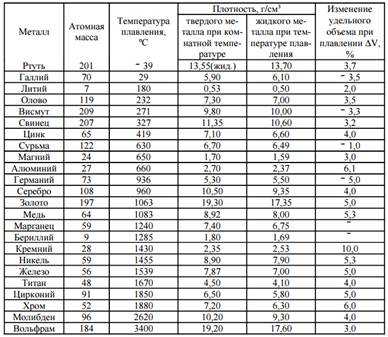
Таблица температуры плавления
Для всех, кто работает в сталелитейной промышленности, будь то сварщик, литейщик, сталевар или ювелир, важно знать, при каких температурах плавятся материалы, с которыми они работают.В таблице ниже приведены температуры плавления наиболее распространенных веществ.
Таблица температур плавления металлов и сплавов
| Имя | Т.пл, °С |
|---|---|
| Алюминий | 660,4 |
| Медь | 1084,5 |
| Олово | 231,9 |
| Цинк | 419,5 |
| Вольфрам | 3420 |
| Никель | 1455 |
| Серебро | 960 |
| Золото | 1064,4 |
| Платина | 1768 |
| Титан | 1668 |
| Дюралюминий | 650 |
| Углеродистая сталь | 11:00-15:00 |
| 11:10-14:00 | |
| Железо | 1539 |
| Меркурий | -38.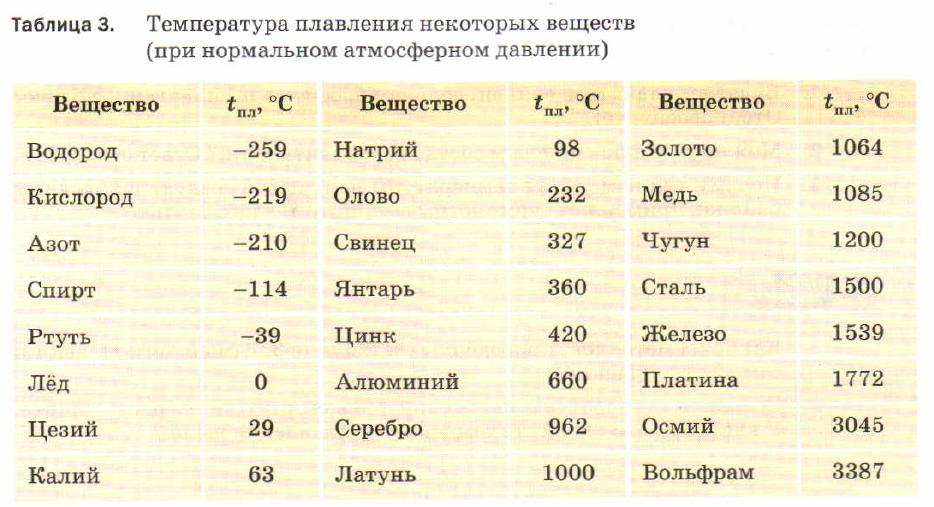 9 9 |
| Мельхиор | 1170 |
| Циркон | 3530 |
| Кремний | 1414 |
| Нихром | 1400 |
| Висмут | 271,4 |
| немецкий | 938,2 |
| банка | 13:00-15:00 |
| Коричневый | 930-1140 |
| Кобальт | 1494 |
| Калий | 63 |
| Натрий | 93,8 |
| Латунь | 1000 |
| Магний | 650 |
| Марганец | 1246 |
| Хром | 2130 |
| молибден | 2890 |
| Свинец | 327,4 |
| Берилл | 1287 |
| , чтобы выиграть | 3150 |
| Фехраль | 1460 |
| Сурьма | 630,6 |
| Карбид титана | 3150 |
| карбид циркония | 3530 |
| Гал | 29,76 |
Помимо плавильного стола есть много других вспомогательных материалов. Например, ответ на вопрос, какова температура кипения железа, дан в таблице кипящих веществ. Помимо кипения, металлы обладают рядом других физических свойств, таких как прочность.
Например, ответ на вопрос, какова температура кипения железа, дан в таблице кипящих веществ. Помимо кипения, металлы обладают рядом других физических свойств, таких как прочность.
Помимо возможности перехода из твердого состояния в жидкое, одним из важных свойств материала является его прочность — возможность твердого сопротивления растрескиванию и необратимым изменениям формы. Основным показателем прочности считается сопротивление, возникающее в результате разрушения предварительно отожженной заготовки.Понятие прочности не применимо к ртути, поскольку она находится в жидком состоянии. Прочность определяют в МПа — МегаПаскалях.
Группы прочности металла следующие:
- Хрупкий. Их сопротивление не превышает 50 МПа. К ним относятся олово, свинец, мягкие щелочные металлы
- Стабильный, 50-500 МПа. Медь, алюминий, железо, титан. Материалы этой группы являются основой многих конструкционных сплавов.
- Высокая прочность, свыше 500 МПа. Например, молибден и .
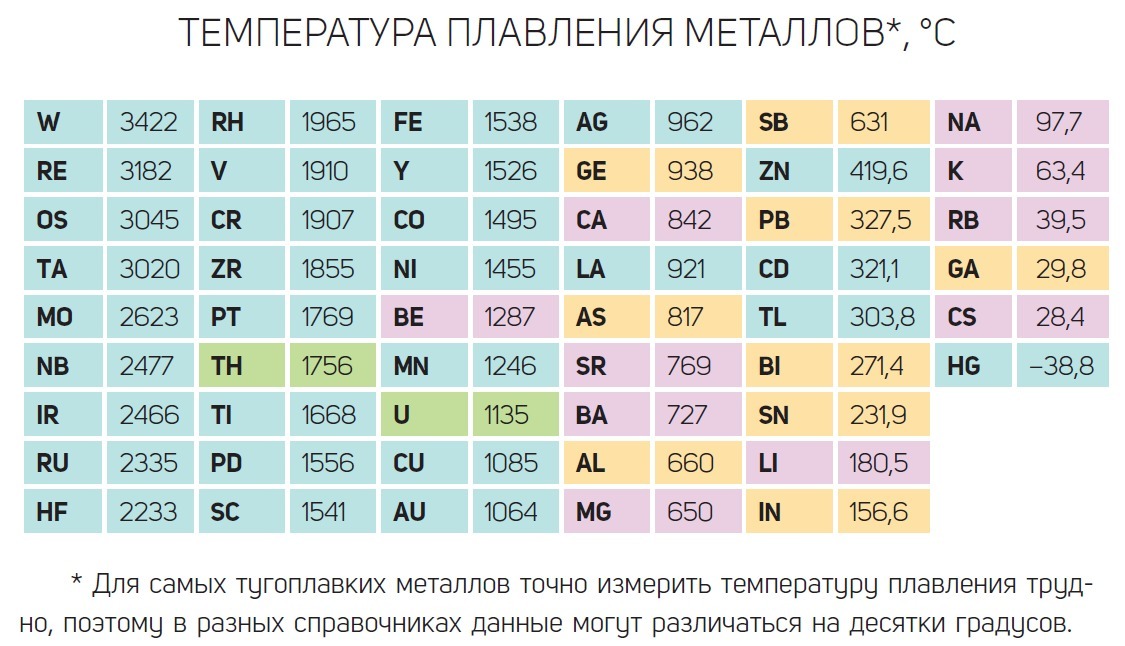
Таблица прочности металла
Самые распространенные ноги в повседневной жизни
Как видно из таблицы, температуры плавления элементов значительно различаются, даже для материалов, распространенных в быту.
Ну и минимальная температура.У ртути температура плавления -38,9°С, так что она уже жидкая при комнатной температуре. Этим и объясняется тот факт, что бытовые термометры имеют более низкий показатель -39 градусов Цельсия: ниже этого показателя ртуть становится твердой.
Наиболее часто используемые в бытовом применении припои содержат значительный процент олова, имеющего температуру плавления 231,9°С, поэтому большинство припоев плавится при рабочей температуре паяльника 250-400°С.
Кроме того, существуют легкоплавкие припои с более низкой температурой плавления, до 30°С, и применяются, когда опасен перегрев припаиваемых материалов. Для этих целей применяют припой с висмутом, а плавление этих материалов находится в пределах 29,7 — 120°С.
Температура плавления высокоуглеродистых материалов колеблется от 1100 до 1500°С в зависимости от легирующих элементов.
Температуры плавления металлов и их сплавов лежат в очень широком диапазоне температур, от очень низких температур (ртутный) до нескольких тысяч градусов. Знание этих показателей, как и других физических свойств, очень важно для людей, работающих в металлургической промышленности. Например, знание температуры плавления золота и других металлов пригодится ювелирам, литейщикам и сталелитейщикам.
Каждый металл и сплав имеет свой уникальный набор физических и химических свойств, не последним из которых является температура плавления.Сам процесс означает переход тела из одного физического состояния в другое, в данном случае из кристаллического твердого состояния в жидкое. Чтобы расплавить металл, необходимо приложить к нему тепло, пока не будет достигнута температура плавления. Благодаря ему он еще может оставаться твердым, но при дальнейшем воздействии и повышении температуры металл начинает плавиться. Если температуру понизить, то есть отвести некоторое количество тепла, элемент затвердеет.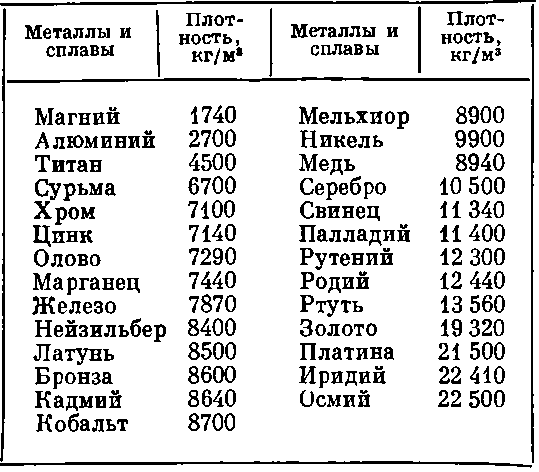
Самая высокая температура плавления среди металлов принадлежит вольфраму : она составляет 3422 °С, самая низкая — у ртути: элемент плавится при — 39 °С.Как правило, точное значение для сплавов определить не удается: оно может существенно варьироваться в зависимости от процентного содержания компонентов. Обычно они записываются в виде диапазона чисел.
Как это происходит?
Все металлы плавятся примерно одинаково — при внешнем или внутреннем нагреве. Первый проходит в термической печи, второй при переходе — нагрев электрическим сопротивлением или индукционный нагрев в высокочастотном электромагнитном поле.Оба варианта воздействуют на металл схожим образом.
С повышением температуры амплитуда тепловых колебаний молекул также увеличивается, появляются дефекты структурной сетки, которые выражаются в росте дислокаций, скачках атомов и других нарушениях. Это сопровождается разрывом межатомных связей и требует определенного количества энергии.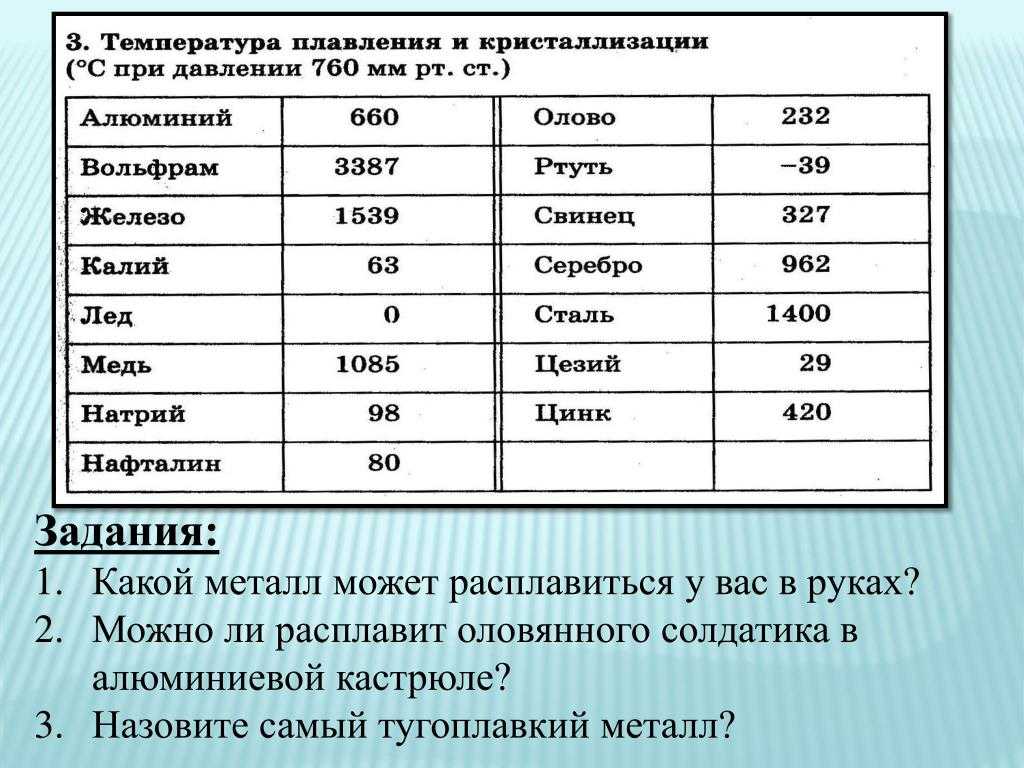 При этом на поверхности тела образуется квазижидкий слой. Период разрушения сети и накопления дефектов называется плавлением.
При этом на поверхности тела образуется квазижидкий слой. Период разрушения сети и накопления дефектов называется плавлением.
В зависимости от температуры плавления металлы делятся на:
В зависимости от температуры плавления выбирают и плавильный аппарат. Чем выше оценка, тем сильнее она должна быть. Вы можете проверить температуру необходимого элемента в таблице.
Другим важным значением является температура кипения. Это значение, при котором жидкость начинает кипеть, оно соответствует температуре насыщенного пара, образующегося над плоской поверхностью кипящей жидкости. Обычно она почти в два раза выше температуры плавления.
Оба значения обычно указываются при нормальном давлении. Между собой прямо пропорциональны .
- Давление увеличивается — количество расплава увеличивается.
- Давление падает — количество плавления уменьшается.
Таблица металлов и легкоплавких сплавов (до 600°С)
Таблица среднеплавких металлов и сплавов (от 600°С до 1600°С)
.
Латунный припой температура плавления
Указанные припои идеально подходят для паяного сочленения латунных заготовок с большим содержанием меди.
В качестве связующего вещества довольно часто используется и чистая латунь, но при работе с ней важно обеспечить нужную температуру плавления, которая не должна превышать тот же параметр для обрабатываемых деталей.
При необходимости получения посредством пайки надёжного соединения повышенной прочности рекомендуется выбирать тугоплавкие (так называемые «твердые») составы, обладающие повышенной температурой плавления.
Для правильного выбора типа латунного припоя, подходящего для конкретных условий спайки, следует воспользоваться той же таблицей, приведенной выше.
Прочность пайки зависит, в первую очередь, от правильного подбора припоя и флюса и, во вторую очередь, от тщательности подготовки спаиваемых деталей.
Это значит, что их поверхности должны быть очищены от окислов, которые мешают проникать припою в спаиваемые детали (диффундировать).
При пайке надо всегда помнить, что температура плавления припоя должна быть ниже максимальной рабочей температуры флюса.
Там, где в тексте эта температура не приводится, дается разъяснение, какими припоями можно паять с данной маркой флюса.
Многие новички задают вопрос, чем паять бронзу и латунь. Интерес обусловлен тем, что пайка сопряжена с некоторыми сложностями. В ходе термического воздействия происходит активное испарение из сплава цинка, в результате чего образуется плотная пленка из цинковых и медных оксидов. Разрушить ее достаточно затруднительно. Как утверждают специалисты, не справится с этой задачей и канифоль.
Как утверждают специалисты, не справится с этой задачей и канифоль.
Мастеру придется воспользоваться специальными флюсами. Если применять оловянно-свинцовый припой, то существует риск, что место соединения будет с низкой механической прочностью. В отличие от медной спайки в данном случае показатель прочности будет в полтора раза ниже. Причина тому – испаряющийся цинк. Выбор способа пайки бронзовых деталей будет зависеть от ее состава. Бронзу с высоким содержанием олова и никеля следует паять с применением оловянно-свинцовых припоев. Бронзу, содержащую алюминий и бериллий, лучше соединять специальными припоями и флюсами.
Припои
Основные свойства, которыми должен обладать припой, можно сформулировать так:
- температура его плавления должна быть ниже температуры плавления спаиваемых металлов;
- он должен хорошо смачивать спаиваемый металл;
- припой должен быть относительно прочным;
- при пайке не должны образовываться пары (металл — припой), отрицательные в электрохимическом отношении, в противном случае паяный шов быстро разрушится;
- металлы, входящие в состав припоя, должны быть недефицитными и недорогими.

Припои по своим физическим свойствам делятся на две группы:
- легкоплавкие припои (их еще называют мягкими припоями) с температурой плавления до 500°
- и тугоплавкие (твердые) с температурой плавления выше 500°.
Наиболее широко распространены легкоплавкие припои на основе сплава олово-свинец
Таблица 1 Припои на основе олово-свинец
| Марки припоя | Температура плавления о С | Применение |
| Олово | 232 | Для лужения |
| ПОС 90 | 220 | То же |
| ПОС 61 | 185 | Для пайки меди и стали |
| ПОС 50 | 210 | Для пайки меди, латуни, никеля, серебра и т.д. |
| ПОС 40 | 235 | То же |
| ПОС 30 | 256 | — |
| ПОС 18 | 277 | Для пайки свинца, цинка, луженной жести |
| ПОС 4-6 | 265 | Для пайки меди и стали |
Примечание
Все припои содержат небольшой процент примеси сурьмы.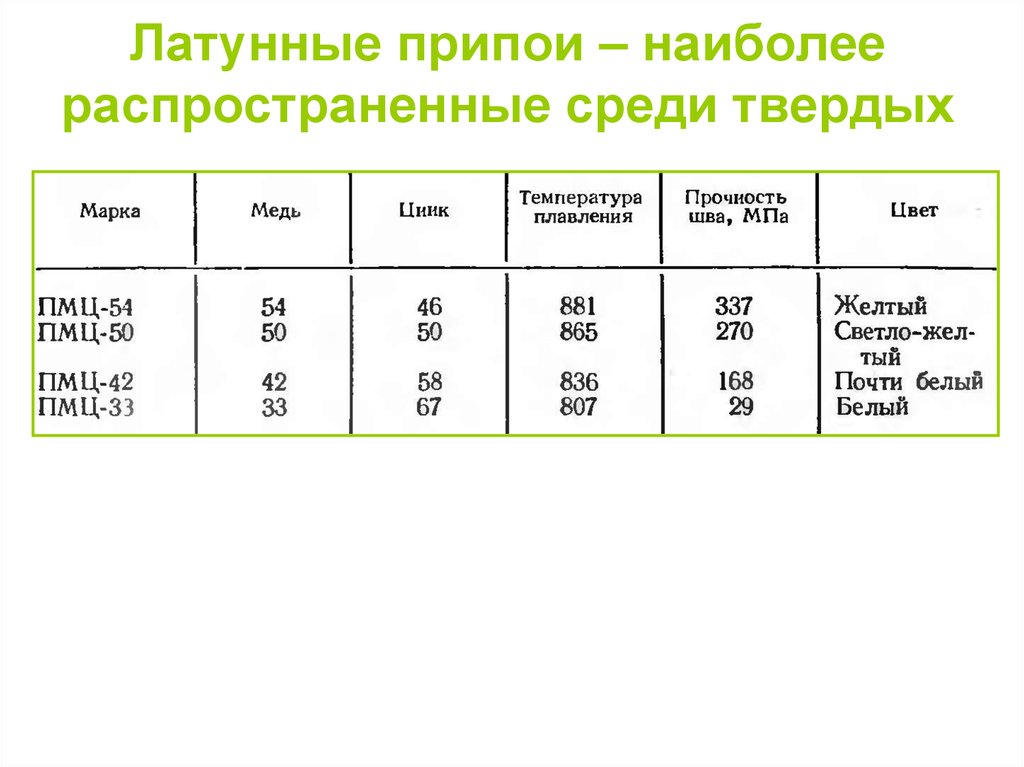 Последний припой содержит 5 – 6% сурьмы. В (табл. 1) приведены припои на основе сплава олово-свинец, для сравнения сюда включено олово. Цифра в марке припоя говорит о количестве (в %) олова в данном припое, остальное – свинец.
Последний припой содержит 5 – 6% сурьмы. В (табл. 1) приведены припои на основе сплава олово-свинец, для сравнения сюда включено олово. Цифра в марке припоя говорит о количестве (в %) олова в данном припое, остальное – свинец.
Из тугоплавких применяются припои на основе меди и серебра
Кроме припоев для пайки стальных и никельсодержащих сплавов пользуются иногда медью марок МО, Ml, M2, МЗ и М4.
Употребляется медь в виде:
Температура пайки медью лежит в пределах 1150—1200°.
Латуни (сплавы медь-цинк) и специальные медно-цинковые припои хороши тем, что температура их плавления несколько ниже, чем у меди. Соединения, спаянные латунью, более прочны, чем спаянные медью. В (табл. 2) приведены три широко распространенных медно-цинковых припоя и некоторые марки латуней, применяемых в качестве припоев.
Таблица 2 Медно-цинковые и латунные припои
| Марки припоя (латуни) | Температура плавления, о С | Применение |
| ПМЦ 36 | 825 | Для пайки латуни марки Л 62 |
| ПМЦ 48 | 865 | Для пайки медных сплавов |
| ПМЦ 54 | 880 | для пайки меди и сплавов из стали |
| Л 62 | 905 | Для пайки меди и стали |
| Л 68 | 938 | То же |
Медно-фосфорные припои отличаются относительно низкой температурой плавления и хорошей затекаемостью в расплавленном состоянии. Наличие в припоях фосфора при пайке меди и ее сплавов позволяет иногда обходиться без флюса, так как фосфор обладает флюсующими свойствами.
Наличие в припоях фосфора при пайке меди и ее сплавов позволяет иногда обходиться без флюса, так как фосфор обладает флюсующими свойствами.
При пайке медно-фосфорными припоями латуни Л62, нейзильбера * , алюминиевой бронзы и медно-никелевых сплавов необходимо применять борсодержащие флюсы. По ГОСТу пайка стали медно-фосфорными припоями не допускается из-за хрупкости паяного шва. Однако при отсутствии медно-цинковых или серебряных припоев можно применять и медно-фосфорные.
К основным медно-фосфорным припоям относятся так называемые фосфористые меди марок МФ-1, МФ-2, МФ-3.
- Температура плавления первых двух – 750°
- третьего – 700°.
Из тугоплавких (твердых) припоев наиболее примечательными являются припои на основе серебра
Их универсальность (можно паять все металлы, кроме алюминия, магния и легкоплавких металлов),
- прочность,
- пластичность,
- коррозионная стойкость,
- высокая температура плавления
ставят их в первый ряд среди других припоев.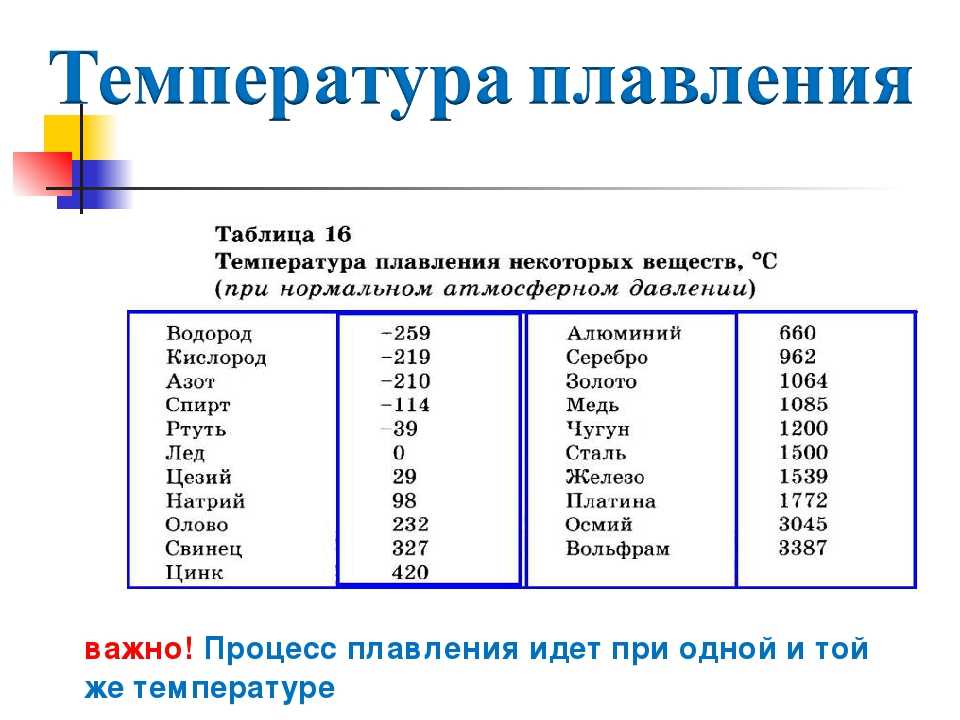 Даже относительная дороговизна нисколько не умаляет их достоинств.
Даже относительная дороговизна нисколько не умаляет их достоинств.
Из припоев на основе серебра некоторые умельцы отливают мормышки!
В (табл. 3) приведены основные марки серебряных припоев. Цифра в марке припоя показывает количество (в %) серебра, остальное — в основном медь.
Таблица 3 Основные марки серебряных припое
| Марка припоя | Температура плавления, о С | Марка припоя | Температура плавления, о С |
| ПСр 72 | 779 | ПСр 44 | 800 |
| ПСр 71 | 795 | ПСр 40 | 605 |
| ПСр 70 | 755 | ПСр 37,5 | 810 |
| ПСр 62 | 700 | ПСр 25 | 775 |
| ПСр 50 | 850 | ПСр 12М | 825 |
| ПСр 45 | 725 | ПСр 10 | 850 |
Флюсы
Назначение флюсов при пайке:
- защита зачищенных деталей от окисления,
- удаление с поверхности металла пленки окислов,
- улучшение смачивания припоем спаиваемых деталей.

Все многообразие флюсов можно разделить на три группы:
- некоррозионные
- слабокоррозионные
- и коррозионные.
Некоррозионные флюсы (их еще называют защитными) не растворяют пленку окислов на металле, а лишь защищают при пайке тщательно зачищенную поверхность. После окончания пайки остатки флюса можно не удалять с поверхности спаянных деталей, так как он не вызывает коррозии.
Слабокоррозионные флюсы участвуют в разрушении пленки окислов. Остатки флюса необходимо удалять.
Коррозионные (активные) флюсы энергично разрушают пленку окислов, поэтому иногда удается спаивать незачищенные металлические детали. Удалять остатки флюса после пайки обязательно!
Отдельную группу составляют борсодержащие флюсы для пайки тугоплавкими припоями
К некоррозионным флюсам относятся неактивированные флюсы на основе канифоли (табл.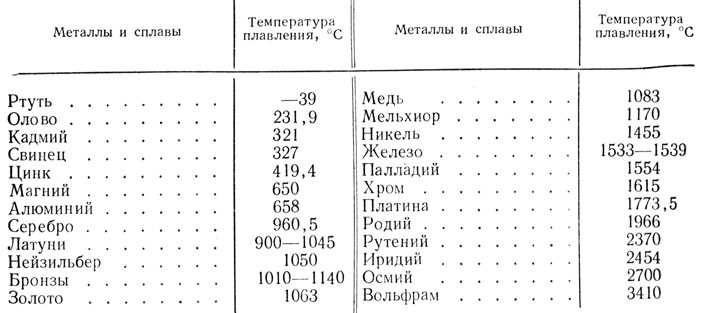 4).
4).
Максимальная рабочая температура этих флюсов 300°!
Таблица 4 Флюсы на основе канифоли
| Компоненты, % вес. | Что и чем паяется |
| Канифоль-40, бензин-50 керосин – 10 |
| Канифоль-30, Этиловый спирт – 70 |
| Канифоль-24, стеарин -1, Этиловый спирт – 75 |
| Канифоль-6,глицерин-16, Этиловый спирт (денатурат)-78 |
К слабокоррозионным флюсам относится большая группа активированных флюсов на основе канифоли, но есть и такие, где канифоль отсутствует (табл. 5).
- первые флюсы имеют максимальную рабочую температуру – 300°
- вторые – 350°
Таблица 5 Флюсы на основе канифоли, глицерина и спирта
| Пайка меди и ее сплавов, серебра (редко — стали) свинцово-оловянистыми припоями | |
| Компоненты, % вес. | Что и чем паяется |
| Канифоль – 30, Этиловый спирт – 60, уксусная кислота – 10 |
| Канифоль – 38, Этиловый спирт – 50, ортофосфорная кислота – 12 |
| Канифоль – 24, Этиловый спирт – 75, хлористый цинк – 1 |
Читать также: Горячекатаный профиль что это такое
Основу почти всех коррозионных (активных) флюсов составляют хлориды металлов и, в частности, хлористый цинк.
Максимальная рабочая температура этих флюсов до 400°! (табл. 6)
Таблица 6 Флюсы на основе хлоридов металлов
| Хлористый цинк – 40, вода – 60 |
| Хлористый цинк – 30, хлористый амоний – 10, вода – 60 |
| Хлористый цинк – 30, солянная кислота – 30, вода – 40 |
| Хлористый цинк – 70, хлористый натрий – 15, хлористый амоний – 15 |
В отдельной таблице приводятся флюсы для пайки нержавеющих сталей
Максимальная рабочая температура этих флюсов 400°!
Таблица 7 Флюсы для пайки нержавеющих сталей
Для пайки и лужения стали, меди, ее сплавов, никеля, серебра. | |
| Хлористый цинк – 40, двухлористое олово – 5, хлорная медь – 0,5, соляная кислота – 3,5, вода – 51 | Пайка стали припоями с большим содержанием свинца |
| Хлористый цинк – 40, хлористый натрий – 5, хлорная медь – 1, хлористый калий – 1, соляная кислота – 1, вода – 52 | Пайка стали и меди (и сплавов) припоями с большим содержанием свинца и цинка. |
| Хлористый натрий – 15, хлористый амоний – 1,5, соляная кислота – 36, спирт денатурат – 12,8, ортофосфорная кислота – 2,2, хлористое железо – 0,6, вода – 31,9 | Пайка углеродистых сталей. |
| Компоненты, % вес | Применение |
| Хлористый цинк (насыщенный раствор) – 100 |
| Хлористый цинк (насыщенный раствор) – 75, соляная кислота – 25 |
| Хлористый цинк (насыщенный раствор) – 90, уксусная кислота – 10 |
| Ортофосфорная кислота – 100 |
| Ортофосфорная кислота – 99, сернокислая медь – 50 |
| Хлористый цинк – 30, хлористый амоний – 10, хлорная медь – 10, соляная кислота – 50 |
| Хлористый цинк – 50, хлористый амоний – 5, соляная кислота – 1, вода – 44 |
Как уже было сказано, флюсы для пайки тугоплавкими припоями сводятся в отдельную группу, состоящую из двух подгрупп:
– флюсы для пайки медными припоями (табл.
Таблица 8 Флюсы для пайки медными припоями
| Пайка нержавеющей стали | |
| Компоненты, % вес | Применение |
| Бура (прокаленная) -100 | Пайка углеродистых сталей и меди медно-цинковыми припоями |
| Бура (прокаленная) – 80, борная кислота – 20 | Пайка молоуглеродистых сталей и меди |
| Бура (прокаленная) -50, борная кислота – 50, все разводится концентрированным раствором хлористого цинка | Пайка нержавеющих сталей, меди медными припоями |
| Бура (прокаленная) – 12, борная кислота – 78, флористый кальций – 10 | Пайка нержавеющих сталей, меди медными припоями |
– флюсы для пайки серебряными припоями (табл. 9)
Табица 9 Флюсы для пайки серебряными припоями
| Компоненты, % вес | Применение |
| Хлористый кальций – 50, хлористый барий – 50 |
| Бура (прокаленная) – 80, борная кислота – 20 |
| Бура (прокаленная) – 50, борная кислота – 35, фтористый кальций – 15 |
| Бура (прокаленная) – 30, тетрафторборат калия – 70 |
Порядок изготовления флюса влияет на его качество
Ниже (табл.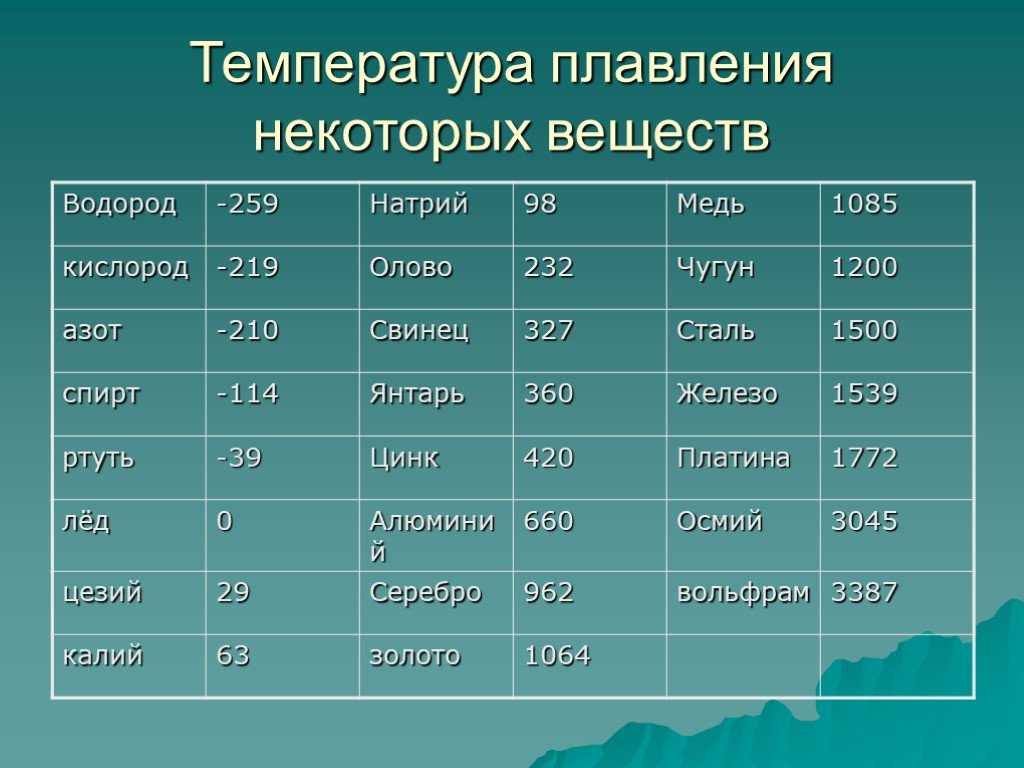 10) приводится порядок приготовления некоторых флюсов. Взяв за основу приготовление одного флюса, можно правильно приготовить другой флюс с такими же компонентами или несколько отличными.
10) приводится порядок приготовления некоторых флюсов. Взяв за основу приготовление одного флюса, можно правильно приготовить другой флюс с такими же компонентами или несколько отличными.
Таблица 10 Приготовление флюса
Канифоль, этиловый спирт, уксусная кислота
Размолотую в порошок канифоль растворить в подогретом спирте и после охлаждения добавить уксусную кислоту
Канифоль, стеарин, хлористый цинк, хлористый аммоний, вазелин, вода
Размолотую канифоль тщательно смешать со стеарином. Порошок хлористого цинка и хлористого аммония залить водой и размешать, Разогреть то и другое. Второй раствор влить в расплавленную канифоль со стеарином. Размешать и добавить вазелин.
Ортофосфорная кислота, этиловый спирт, вода
Этиловый спирт разбавляют водой и к раствору добавляют ортофосфориую кислоту
Хлористый цинк, хлористый аммоний, вода
В горячей воде растворяется хлористый аммоний.
После охлаждения раствора к нему добавляется хлористый цинк.
Хлористый цинк, двухло-ристое олово, хлорная медь, хлористый калий, соляная кислота, вода
В части горячей воды с соляной кислотой растворить днухлористое олово и хлорную медь. В другой части воды растворить хлористый цинк и хлористый калий. Первый раствор влить во вто-рой и тщательно перемешать.
Хлористый калий, хлористый литий, фтористый натрий, хлористый цинк
Псе порошкообразные компоненты смешан., расплавить и после остывания размолоть. Хранить в плотно закрывающейся стеклянной посуде.
| Пайка серебрянными припоями всех металлов и сплавов, кроме алюминия и магния | |
| Компоненты | Порядок приготовления |
| Бура | Расплавить буру, охладить и размолоть до порошкообразного состояния. Хранить в плотно закрывающейся стеклянной посуде. |
| Бура, борная кислота | Прокаленую и размолотую буру смешать с нужным количеством борной кислоты. Хранить в плотно закрывающейся стеклянной посуде. |
Для изготовления припоя из отдельных компонентов пользуются правилом: сначала расплавляют более тугоплавкий металл, а в нем остальные помере убывания температуры плавления.
Пайка является одним из способов соединения двух деталей, при котором плавится только соединяющий материал, а поверхности самих элементов полностью сохраняются. С помощью такого способа можно соединять разнородные материалы, довольно мелкие элементы, хрупкие микросхемы, соединять или нарастать провода, крепить пластины из твердых сплавов, осуществлять антикоррозийную обработку.
Чаще всего делать сплавку приходиться по латуни, которая является сплавом цинка и меди. Поэтому перед началом работ паяльником следует изучить особенности применения этого материала.
Пайка латуни – некоторые особенности
Чаще всего пайка латуни выполняется газовой горелкой, а в качестве припоя применяется бура, олово или другие аналогичные материалы. В домашних условиях для такой работы можно использовать паяльник или специальный графитовый электрод.
В принципе пайка латуни напоминает обработку чугуна, меди, стали. Однако она имеет свои тонкости и особенности, которые обязательно необходимо учитывать.
Для пайки латуни очень важно подобрать флюс. В процессе соединения с поверхности обрабатываемого сплава должна быть удалена оксидная пленка. Обыкновенный канифольно-спиртовый флюс этого сделать не способен, поэтому необходимо использовать более активные компоненты, содержащие в своей основе хлористый цинк.
Читать также: Аппарат для изготовления пива в домашних условиях
Припой для пайки латуни следует подбирать особенно тщательно. Для работы со сплавом, в котором большое содержание меди, отлично подойдут медно-фосфорные и серебряные компоненты. Можно использовать и саму латунь, но при этом нужно учитывать, что ее температура плавления в качестве припоя должна быть ниже, чем у основного сплава. Довольно часто латунь соединяют с помощью твердого припоя, например, L — CuP 6. Такие соединения получаются очень прочными.
Ход работы
Спаивание нержавейки выполняют следующим образом:
- Сначала поверхность тщательно зачищается наждачной бумагой или напильником.

- Далее место спайки обрабатывается флюсом, а именно паяльной кислотой.
- Затем поверхности требуется залудить – нанести на них тонкий слой припоя, содержащий олово и свинец. Бывает, что припой с первого раза нанести не представляется возможным. В таком случае придется применить кисточку, содержащую металлические жилы. Ими будет гораздо удобнее снимать окисную пленку, предотвращающую лужение.
- Используя паяльник и припой, выполняют спаивание деталей.
Процесс пайки латуни
Для максимальной эффективности работ необходимо подготовить следующие материалы и инструменты:
- газовую горелку;
- медь;
- графитовый тигель;
- серебро;
- асбестовое основание;
- борную кислоту.
В некоторых случаях может понадобиться бронза.
Подготовка припоя
В первую очередь необходимо подготовить тенол, в состав которого будет входить две части серебра и одна часть меди. Для этого с помощью газовой горелки медь и серебро необходимо будет расплавить и отвесить нужное количество материала. Далее, сплавы помещаются в тигель и греются все той же газовой горелкой.
Далее, сплавы помещаются в тигель и греются все той же газовой горелкой.
Расплавленные медь и серебро перемешиваются с помощью проволочки, и тигель ставится в холодную воду. Застывший припой расплющивается и нарезается. Затем крупным напильником из него натирается стружка.
Размеры графитового тигеля должны быть примерно 20х20 миллиметров. Изготовить его можно из графитовых углей (контактные троллейбусные элементы).
Подготовка флюса
Для этого берется 20 грамм порошка буры и 20 грамм порошка борной кислоты. Ингредиенты тщательно перемешиваются и заливаются 250 миллилитрами воды. Затем полученная смесь подвергается кипячению и остужается.
Для соединения латунных деталей можно применить и готовые составы. Среди отечественных хорошо зарекомендовали себя флюсы:
Из импортных можно отметить флюс-пасты немецкого производителя Chemet.
Припой и флюс готовы, теперь можно приступать непосредственно к пайке. Для этого подготовленные детали необходимо аккуратно положить на основание из асбеста и приступать к процессу пайки.
- Поверхность соединяемых деталей обработать флюсом и очень аккуратно посыпать стружкой припоя.
- Теперь спаиваемые элементы нужно потихоньку греть. Делать это следует медленно и осторожно, чтобы они не перегрелись и не деформировались.
- Сначала нагреть надо чуть-чуть, чтобы припой немного расплавился и схватил детали. Потом примерно до 700 градусов. Припой будет затекать в щели и крепко спаивать элементы. На этом этапе особое внимание надо уделить температуре плавления. Разница плавления латунных деталей и припоя составляет всего 50 градусов, поэтому надо следить за тем, чтобы не перегреть обрабатываемые материалы. В противном случае можно получить один большой слиток.
- Полученный в результате шов должен иметь один цвет со спаиваемым материалом. Происходит это из-за диффузии основного металла в припой.
- Последний этап – это очистка полученного изделия от остатков флюса в виде наплывов и стекловидных капель.
 Чтобы от них избавиться, изделие нужно промыть в трехпроцентной горячей серной кислоте. Для этого элементы следует опустить в нее на короткое время и затем тщательно промыть проточной водой. Нагреть серную кислоту можно в пробирке из кварцевого стекла, поместив ее на газовую плиту. Чтобы самим не взаимодействовать с кислотой, обработанные детали перед очисткой рекомендуется на что-нибудь подвязать.
Чтобы от них избавиться, изделие нужно промыть в трехпроцентной горячей серной кислоте. Для этого элементы следует опустить в нее на короткое время и затем тщательно промыть проточной водой. Нагреть серную кислоту можно в пробирке из кварцевого стекла, поместив ее на газовую плиту. Чтобы самим не взаимодействовать с кислотой, обработанные детали перед очисткой рекомендуется на что-нибудь подвязать.
Если сравнивать такой метод пайки с соединением элементов при помощи олова, то простотой он не отличается. Но время будет потрачено не зря, так как соединение будет иметь повышенную надежность и прочность.
Как выполнить спайку газовой горелкой
Как паять латунь? Процедура заключается в следующем:
- Перед началом процесса нужно разогреть металлы. Выполняется эта работа на жаропрочных материалах. Специалисты советуют воспользоваться асбестовой пластиной.
- Спаиваемые детали нужно совместить друг с другом.
- Поверхности в месте спаивания тщательно протереть флюсом.

- Произвести нарезку серебряного припоя. В конечном итоге он должен представлять собой стружку, которую следует насыпать на место соединения металлов.
- В газовой горелке отрегулировать пламя. Для схватывания припоя с поверхностями металлов место соединения сначала прогревается слабым огнем.
- Выставить газовую горелку на 750 градусов для основного нагрева. На латунной поверхности должен образоваться красный оттенок. Припоем заполняются все зазоры, далее он растекается по всему месту соединения.
- Выключить горелку и дать время изделию для остывания. Процедура считается выполненной правильно, если получился шов, который мало отличается от металла.
- Место соединения промыть, чтобы удалить остатки флюса.
Латунь – пайка паяльником
Латунь и медь или латунь и материалы, содержащие медь, можно соединять низкотемпературной пайкой с помощью паяльника мощностью в 100 Вт.
В качестве припоя необходимо использовать оловянно-свинцовый сплав ПОС60 или выше. Флюсом может послужить ортофосфорная или паяльная кислота.
Флюсом может послужить ортофосфорная или паяльная кислота.
Перед работой с латунью следует удалить окисную пленку и обезжирить поверхность. Пайка должна производиться при хорошем разогреве паяльника.
Кроме этого, перед пайкой необходимо уделять тщательное внимание обработке поверхности флюсом, которая проводится непосредственно перед поднесением разогретого паяльника с припоем.
С помощью паяльника можно соединять латуни с применением припоев из серебра (ПСр40 и выше). Однако мощность паяльника должна быть от 0,5 до 1 кВт, а температура разогрева — от 500С. Флюс рекомендуется использовать на основе буры или можно применить концентрированную ортофосфорную кислоту.
Таким способом можно заливать различные образовавшиеся в латунных массивных изделиях (радиаторах) дефекты.
Как это сделать
Для пайки латуни лучше всего воспользоваться серебряным припоем. Желательно, чтобы местом плавки был специальный тигель, приспособленный для значительных термических воздействий. В качестве материала для тиглей могут быть использованы контактные угольные элементы для троллейбуса. В нагретом состоянии они не представляют ценности, а домашний умелец может их приспособить для изготовления припоя. В данном изделии следует сделать выемку 20 х 20 мм. Далее к ней следует проделать канавку. Извлекать припой будет легче, если ее ширина составит 0,5 см.
В качестве материала для тиглей могут быть использованы контактные угольные элементы для троллейбуса. В нагретом состоянии они не представляют ценности, а домашний умелец может их приспособить для изготовления припоя. В данном изделии следует сделать выемку 20 х 20 мм. Далее к ней следует проделать канавку. Извлекать припой будет легче, если ее ширина составит 0,5 см.
Припой делают из серебра и меди (2:1). После взятия нужного количества металлов их следует поместить в тигель. Их термообработка осуществляется газовой горелкой. Некоторые мастера расходный материал предварительно крошат. В таком случае процедура плавки протекает гораздо проще. Далее в состав добавляют стальной или керамический (фарфоровый) стержень. Паять латунь можно тогда, когда припой кустарного изготовления полностью застынет.
Читать также: Чем точить ножи из нержавеющей стали
Пайка латунью
Сплавы из латуни в качестве припоя довольно часто применяются в строительстве при работе с большинством металлов. С их помощью можно соединять детали из меди, стали и даже чугуна.
С их помощью можно соединять детали из меди, стали и даже чугуна.
Так, например, чугунные элементы достаточно трудно сварить, так как для этого необходим специальный электрод, флюс и серьезный разогрев. В то же время их достаточно легко можно соединить с помощью латунного припоя.
Очень распространен способ пайки латунью при соединении труб встык, где очень важно, чтобы постоянным оставалось их внутреннее сечение. После применения такого метода внешние габариты остаются практически неизменными, внутреннее сечение сохраняется, а стык надежно герметизируется.
С помощью латунного припоя можно соединять различные детали систем охлаждения в электронных приборах, медные трубки жидкой системы охлаждения в мощных серверах.
Однако следует иметь в виду, что латунные швы по прочности уступают сварному соединению, поэтому относиться к ним следует бережно.
В некоторых случаях применяется лужение или пайка латунью стали. Ее используют для нанесения на поверхность деталей из стали антикоррозийного покрытия. Лужение чаще всего подходит для обработки небольших единичных изделий, в промышленных масштабах оно практически не применяется.
Лужение чаще всего подходит для обработки небольших единичных изделий, в промышленных масштабах оно практически не применяется.
При соединении деталей из низколегированных и углеродистых сталей иногда используется твердая пайка, где латунный припой должен иметь температуру плавления выше 450 градусов.
В процессе пайки латунных сплавов следует иметь в виду, что могут выделяться ядовитые для человека пары цинка. Поэтому в помещении, где будут проводиться работы, должна быть хорошая вентиляция.
При наличии всех необходимых материалов и инструментов и строгом соблюдении рекомендаций, результаты пайки латуни будут самыми положительными. Всю работу можно сделать самостоятельно, не прибегая к помощи специалистов, которая стоит весьма недешево.
Латунь
Латунь, от немецкого Latun, это двойной или многокомпонентный сплав на основе меди, где основным легирующим элементом является цинк (до 50%), иногда с добавлением олова, никеля, свинца, марганца, железа и других элементов. Хотя цинк был открыт только в XVI веке, латунь была известна уже древним римлянам, т.е. до н.э. До конца XVIII в. латунь получали плавкой меди с цинковой рудой, смешанной с древесным углём. В XIX в. этот способ был вытеснен прямым сплавлением меди с металлическим цинком, такая латунь впервые была получена в Англии в 1781 году. В Западной Европе и России в XIX веке латунь использовали в качестве поддельного золота.
Хотя цинк был открыт только в XVI веке, латунь была известна уже древним римлянам, т.е. до н.э. До конца XVIII в. латунь получали плавкой меди с цинковой рудой, смешанной с древесным углём. В XIX в. этот способ был вытеснен прямым сплавлением меди с металлическим цинком, такая латунь впервые была получена в Англии в 1781 году. В Западной Европе и России в XIX веке латунь использовали в качестве поддельного золота.
Латунь имеет плотность — 8300—8700 кг/м³, удельную теплоёмкость при 20 °C — 0,377 кДж·кг−1·K−1 и удельное электрическое сопротивление — (0,07-0,08)×10−6 Ом·м. Температура плавления латуни в зависимости от состава достигает 880—950 °C. Латунь плавится при температуре ниже точки плавления меди, с увеличением содержания цинка температура плавления понижается. Латунь достаточно хорошо сваривается и прокатывается. Хотя поверхность латуни, если не покрыта лаком, чернеет на воздухе, в общем, она лучше сопротивляется действию атмосферы, чем медь и намного медленней изнашивается. Латунь имеет жёлтый цвет и отлично полируется, поэтому широко используется в качестве недорогих декоративных покрытий и изделий «под золото».
Латунь имеет жёлтый цвет и отлично полируется, поэтому широко используется в качестве недорогих декоративных покрытий и изделий «под золото».
Варьирование температуры обработки и массовой доли (и состава) примесей позволяет получать различные механические свойства латуней. Некоторые латуни куются и обрабатываются только «на холодную», некоторые – только при определенном нагреве. Но все латуни, при нагреве около 90% от точки плавления, становятся хрупкими, что позволяет их дробить в мелкодисперсный «песок».
Висмут и свинец оказывают вредное влияние на латунь, уменьшая способность к деформации в горячем состоянии.
Благодаря хорошей обрабатываемости давлением в горячем и холодном состояниях, высоким механическим свойствам, красивому цвету и сравнительной дешевизне, латуни являются самыми распространёнными из медных сплавов. Легкость обработки позволяет получать латунные листы, ленты, прутки, трубы, вить пружины и ламели, пружинные контакты, проволоку, а также штамповать детали любой сложности (деформируемые латуни), изготавливать отливки (литейные латуни, При увеличении содержания цинка, цвет латуни изменяется от красноватого до светло-желтого.
Простые латуни это сплавы меди только с цинком. Латуни, содержащие до 10% Zn, называют томпаками, а от 10 до 20% — полутомпаками. Такие сплавы, отличаются хорошей коррозионной стойкостью и повышенной пластичностью, их используют для изготовления радиаторных и конденсаторных труб, листов и ленты для плакирования стали. Латунь, содержащую около 30% Zn и способную к глубокой вытяжке, называют патронной и широко применяют для изготовления изделий холодной штамповкой, а также прессованием и волочением. Латуни используются также в общем машиностроении, приборостроении, теплотехнике и многих др. отраслях промышленности.
Для улучшения механических, антикоррозионных и других свойств, к двойным сплавам меди с цинком добавляют алюминий, олово, железо, марганец, никель, кремний, свинец и другие элементы (в сумме примерно до 10%). Многокомпонентные (или специальные) латуни называют алюминиевыми, кремнистыми, алюминиево-никелевыми, железомарганцовистыми и т. п. Латунь, содержащая около 15% Zn и 0,5% Al, имеет красивый золотистый цвет и повышенную стойкость против атмосферной коррозии; такой сплав используют как заменитель золота для знаков отличия и художественных изделий. Латуни с добавкой до 1,5% Sn (так называемые морские латуни) имеют повышенную стойкость против коррозии в морской воде. Добавка свинца (до 3%) делает стружку ломкой и позволяет получать при обработке резанием поверхность высокой чистоты (автоматная латунь). Свинцовистые латуни применяются в автомобильной и часовой промышленности (часовые латуни).
п. Латунь, содержащая около 15% Zn и 0,5% Al, имеет красивый золотистый цвет и повышенную стойкость против атмосферной коррозии; такой сплав используют как заменитель золота для знаков отличия и художественных изделий. Латуни с добавкой до 1,5% Sn (так называемые морские латуни) имеют повышенную стойкость против коррозии в морской воде. Добавка свинца (до 3%) делает стружку ломкой и позволяет получать при обработке резанием поверхность высокой чистоты (автоматная латунь). Свинцовистые латуни применяются в автомобильной и часовой промышленности (часовые латуни).
Многие латуни, содержащие более 20—30% Zn, склонны к коррозионному растрескиванию из-за одновременного действия остаточных напряжений в изделии и коррозионного воздействия аммиака, а также сернистого газа во влажной атмосфере. Это явление называют сезонной болезнью латуни, т. к. усиленное коррозионное растрескивание происходит в месяцы с повышенной влажностью воздуха. Растрескивание предотвращают, применяя отжиг для уменьшения остаточных напряжений (при 250—300°С).
Порядок маркировки
Принята следующая маркировка. Сплав латуни обозначают буквой «Л», после чего следует буквы основных элементов, образующих сплав. В марках деформируемых латуней первые две цифры после буквы «Л» указывают среднее содержание меди в процентах. Например, Л70 — латунь, содержащая 70 % Cu. В случае легированных деформируемых латуней указывают ещё буквы и цифры, обозначающие название и количество легирующего элемента, ЛАЖ60-1-1 означает латунь с 60 % Cu, легированную алюминием (А) в количестве 1 % и железом в количестве 1 %. Содержание Zn определяется по разности от 100 %. В литейных латунях среднее содержание компонентов сплава в процентах ставится сразу после буквы, обозначающей его название. Например, латунь ЛЦ40Мц1,5 содержит 40 % цинка (Ц) и 1,5 % марганца (Мц).
Деформируемые латуни
Томпак (фр. tombac, от малайск. tambaga — медь) — латунь с содержанием 90—97% меди. Обладает высокой пластичностью, антикоррозионным и антифрикционными свойствами, хорошо сваривается со сталью, его применяют для изготовления биметалла сталь-латунь. Благодаря золотистому цвету, томпак используют для изготовления художественных изделий, знаков отличия и фурнитуры.
Обладает высокой пластичностью, антикоррозионным и антифрикционными свойствами, хорошо сваривается со сталью, его применяют для изготовления биметалла сталь-латунь. Благодаря золотистому цвету, томпак используют для изготовления художественных изделий, знаков отличия и фурнитуры.
Двойные деформируемые латуни
Марка | Область применения
|
Л96, Л90, Л85, Л80 | Детали машин, приборов теплотехнической и химической аппаратуры, змеевики, сильфоны и др. |
Л70 | Гильзы химической аппаратуры, отдельные штампованные изделия |
Л68 | Большинство штампованных изделий |
Л63 | Гайки, болты, детали автомобилей, конденсаторные трубы |
Л60 | Толстостенные патрубки, гайки, детали машин |
Многокомпонентные деформируемые латуни
Марка | Область применения |
ЛА77-2 | Конденсаторные трубы морских судов |
ЛАЖ60-1-1 | Детали морских судов. |
ЛАН59-3-2 | Детали химической аппаратуры, электромашин, морских судов |
ЛЖМа59-1-1 | Вкладыши подшипников, детали самолетов, морских судов |
ЛН65-5 | Манометрические и конденсаторные трубки |
ЛМц58- 2 | Гайки, болты, арматура, детали машин |
ЛМцА57-3-1 | Детали морских и речных судов |
ЛO90-1, ЛO70-1, ЛO62-1, ЛO60-1 | Конденсаторные трубы теплотехнической аппаратуры |
ЛС63-3, ЛС74-3 | Детали часов, втулки |
ЛС64-2 | Полиграфические матрицы |
ЛС60-1, ЛС59-1 | Гайки, болты, зубчатые колеса, втулки |
ЛЖС58-1-1 | Детали, изготовляемые резанием |
ЛК80-3 | Коррозионностойкие детали машин |
ЛМш68-0,05 | Конденсаторные трубы |
ЛАНКМц75- 2- 2,5- 0,5- 0,5 | Пружины, манометрические трубы |
Литейные латуни
Марка | Область применения |
ЛЦ16К4 | Детали арматуры |
ЛЦ23А6ЖЗМц2 | Массивные червячные винты, гайки нажимных винтов |
ЛЦЗОАЗ | Коррозионно-стойкие детали |
ЛЦ40С | Литые детали арматуры, втулки, сепараторы, подшипники |
ЛЦ40МцЗЖ | Детали ответственного назначения, работающие при температуре до 300 °C |
ЛЦ25С2 | Штуцера гидросистемы автомобилей |
Большую часть лома латуни, поступающего на наш приемный пункт, составляют различные сантехнические детали, краны, фланцы, метизы, обрезки труб, радиаторы и змеевики. Часто встречаются латунные вкладыши, сепараторы подшипников, различные токарные детали — втулки, переходники, шпильки и прочее. Лом электротехнической латуни — трущиеся контакты и втулки валов, различные щетки и токосъемники.
Часто встречаются латунные вкладыши, сепараторы подшипников, различные токарные детали — втулки, переходники, шпильки и прочее. Лом электротехнической латуни — трущиеся контакты и втулки валов, различные щетки и токосъемники.
Поскольку латунь применяется в промышленности довольно широко, образуется большое количество латунной стружки. Данный вид отходов латуни получается при механической обработке латунных заготовок, такой как фрезерование, сверление, токарная обработка.
ООО «Красмет» закупает весь спектр лома и отходов латуни и других медных сплавов.
В случае, если Вы хотите продать лом и отходы латуни или других медных сплавов, заключить договор о поставках металлолома в адрес нашей компании, заказать вывоз металлолома, а также получить информацию по вопросам приема металлолома, ценам на металлолом на момент сдачи, позвоните нам и Вас сориентируют по ценам и условиям покупки лома и отходов латуни и стоимости услуг.
Телефоны специалистов:
+7 391 293 30 32
Так же обратиться к нам можно по электронной почте:
Латунь в гранулах (100 г)
Состав: Cu 67%, Zn 33%
Наличие уточняйте у менеджеров магазина
В наличии
430 ₽
Латунь в гранулах (100 г) теперь в вашей корзине покупок
К сравнению
В избранное
Категории:
Металлы, присадки
- Обзор
Латунь отлично полируется, сваривается и прокатывается, она устойчива к жару и коррозии.
Температура плавления латуни колеблется в пределах 900–950ºC.
Состав: Cu 67%, Zn 33%
С этим товаром также покупают
Цинк в гранулах (100 г)
270 ₽
0
Медь бескислородная в гранулах (100 г)
300 ₽
0
Формомасса PRESTIGE ORO (1 кг)
300 ₽
0
Медь в иголках (100 г)
540 ₽
0
Бура техническая (250 г)
в банке ПЭТ
130 ₽
0
02-004 Дискодержатель с винтом и гайкой
Хвостовик Ø2,35
30 ₽
0
02-008 Шкуркодержатель прямой широкий
Хвостовик Ø2,35
30 ₽
0
Бронза в гранулах (100 г)
510 ₽
0
Флюс для пайки TECHNOFLUX (100 мл)
240 ₽
0
02-109 Круг муслиновый желтый на держателе Ø22 мм.

35 ₽
0
02-101 Щетка крацовочная стальная на держателе Ø22 мм.
35 ₽
0
Борная кислота техническая (250 г)
в банке ПЭТ
160 ₽
0
Фарносов В.
 Литье для начинающих. Олово, латунь и бронза в полевых условиях
Литье для начинающих. Олово, латунь и бронза в полевых условиях
Статья публикуется в рамках проекта «Деревня средневековых ремёсел – воссоздание мастерских для четырёх средневековых ремёсел, размещённых в туристическом объекте – «деревня Кауп», реализованного в 2018 году субсидии из бюджета Калининградской области.
Все описанные объекты находятся на городище недалеко от п. Романово Зеленоградского района Калининградской области. Можно приехать, поучаствовать в мастер-классах, пообщаться с мастерами, дополнительная информация здесь: kaup39.ru
В этой статье мы хотим показать вам, что лить простые вещи не так сложно, как кажется. Вам обязательно потребуется изучение специальной литературы, однако, литье доступно практически каждому, и для того, чтобы начать, не требуется дорогое оборудование.
Литье олова
Оборудование
- Костер
- Тигель (керамический или металлический)
- Меха (достаточно небольших костровых)
- Формы (из металла, глины или мыльного камня)
- Клещи/плоскогубцы
Материалы
- Уголь/дрова
- Олово
Все оборудование легко сделать самим. Температура плавления олова всего 231,9°C, его можно лить – его можно лить в силиконовые, гипсовые, деревянные и глиняные формы. Можно попробовать историческим способом лить прямо в форму из мыльного камня, она будет постепенно разрушаться при изъятии изделия, но срок ее службы мы пока не установили.
Температура плавления олова всего 231,9°C, его можно лить – его можно лить в силиконовые, гипсовые, деревянные и глиняные формы. Можно попробовать историческим способом лить прямо в форму из мыльного камня, она будет постепенно разрушаться при изъятии изделия, но срок ее службы мы пока не установили.
Маленькие костровые меха легко сделать самим или купить в магазине, где продается все для пикников.
Для литья олова в качестве тигеля также подойдет металлический ковшик, главное чтобы он выдержал длительное нахождение на огне. Горячий тигель вы берете клещами или плоскогубцами.
При заливке олова в форму из камня или глины ее необходимо сперва разогреть, особенно если форма содержит мелкие детали.
Такую литейку вы можете за 15 минут разложить где угодно, главное сделать меха, тигель и формы.
Подробнее о реконструкции оловянного литья вы можете прочитать в этой статье: http://kaup.ru/index.php/rec/materials/49-litjo-v-kamennuyu-formu.html
Литье латуни
Оборудование:
- Глиняная печь/горн
- Тигель (керамический или металлический)
- Кузнечные меха
- Формы для отливки восковок из мыльного камня
- Клещи
- Деревянное или железное ведро для воды
Материалы:
- Уголь
- Глина
- Воск
- Флюс
- Вода
Этапы процесса:
- Заливка воска в форму из мыльного камня
- Извлечение восковки и аккуратное обмазывание ее глиной
- Сушка заготовки
- Выпаривание воска в печи, нагрев глиняной формы и, одновременно, разогрев и плавка латуни в тигеле
- Литье латуни в форму
При заливке воска формы необходимо слегка разогреть.
От начала процесса до отливки изделия обычно проходит не менее 1 недели, необходимо, чтобы глиняные формы высохли.
В случае с латунью глиняные формы можно поставить выпариваться в ту же печь/горн, которые используются для плавки латуни, но немного сбоку, где температура не так высока. Формы не должны превратиться в керамику, температура обжига начинается от 600 °C, а температура плавления латуни 880—950 °C.
В идеале нужна отдельная печь или костер для форм, и отдельная для тигелей. После выпаривания воска форма не должна остыть, так что не вытаскивайте ее раньше времени из огня. Температура в горне у вас будет такая, что для вытаскивания тигеля необходимы клещи с длинными ручками. Также запаситесь ведром с водой, сопло и клещи достаточно быстро раскаляются докрасна и их необходимо периодически остужать, окуная в воду.
После заливки в форму расплавленный металл прикрывается картошкой или яблоком, влага внутри превращается в пар, который создаёт давление и проталкивает жидкий металл в форму.
Кузнечные меха вам придется сделать самостоятельно, в интернете много руководств на эту тему. Клещи можно заказать в кузнечной мастерской или купить в специализированном магазине.
После остывания формы с отливкой, разбиваем форму.
После вынимания из формы у отливки следует удалить литник и снять заусеницы.
Литье бронзы
Оборудование:
- Печь для плавления бронзы
- Печь для разогрева форм
- Тигель (керамический или металлический)
- Большие кузнечные меха
- Формы для отливки восковок из мыльного камня
- Клещи
Материалы:
- Уголь
- Глина
- Воск
- Флюс
Разница в литье между латунью и бронзой только в температуре плавления металла. Если горн для латуни можно сделать за полдня из глины, то для бронзы нужна серьезная стационарная печь. Температура плавления бронзы 930—1140 °C. Эта разница около 100 °C , как оказалось, недостижима на открытом огне. Печь делается таким образом, чтобы сопло мехов не соприкасалось с горящими углями, в печи есть отверстие для сопла, но до углей металл не должен доходить. Пример конструкции печи:
Температура плавления бронзы 930—1140 °C. Эта разница около 100 °C , как оказалось, недостижима на открытом огне. Печь делается таким образом, чтобы сопло мехов не соприкасалось с горящими углями, в печи есть отверстие для сопла, но до углей металл не должен доходить. Пример конструкции печи:
В какие формы вообще можно лить цветной металл?
Чаще всего формы изготавливаются из глины, есть техники литья в песок, землю и дерево, а также современная технология литье в силиконовые формы.
Что такое мыльный камень и где его взять?
Мыльный камень — талькохлорит, в раннем средневековье использовался для литейных форм, скульптур и светильников. Сейчас купить его можно практически в любом магазине для саун и бань (для проекта мы покупали в “Гидрокомфорте”), продается коробками, лучше брать не обвалованный, а колотый — у него встречаются ровные сколы, требующие меньше обработки.
Как вырезать форму из мыльного камня?
Камень нужно отшлифовать до гладкой, почти отражающей поверхности. Мыльный камень очень хорошо подвергается обработке и вырезать форму в нём довольно легко, но сначала камень нужно подготовить. Камень нужно отшлифовать до гладкой, почти отражающей поверхности. Для этого нужна ровная гладкая поверхность и несколько листов наждачной бумаги разной маркировки. Хорошим вариантом для наших целей будет последовательное использование 40-80-120-180-280-400. В конце две половинки формы притираются друг о друга с добавлением воды, чтобы при их соединении не было люфта и просветов. На одной из половинок рисуется силуэт будущего изделия, затем выцарапывается по контору острой железной палочкой и дальше внутренний объём вырезается маленькими штихелями. Когда одна половина готова, нужно засыпать порошком, который остался после резки форму и аккуратно приложить сверху вторую половину, тогда порошок отпечатает на ней контур. Далее вырезается вторая сторона и литник.
Мыльный камень очень хорошо подвергается обработке и вырезать форму в нём довольно легко, но сначала камень нужно подготовить. Камень нужно отшлифовать до гладкой, почти отражающей поверхности. Для этого нужна ровная гладкая поверхность и несколько листов наждачной бумаги разной маркировки. Хорошим вариантом для наших целей будет последовательное использование 40-80-120-180-280-400. В конце две половинки формы притираются друг о друга с добавлением воды, чтобы при их соединении не было люфта и просветов. На одной из половинок рисуется силуэт будущего изделия, затем выцарапывается по контору острой железной палочкой и дальше внутренний объём вырезается маленькими штихелями. Когда одна половина готова, нужно засыпать порошком, который остался после резки форму и аккуратно приложить сверху вторую половину, тогда порошок отпечатает на ней контур. Далее вырезается вторая сторона и литник.
Какой воск лучше использовать — ювелирный или пчелиный?
Конечно, ювелирный воск более удобен, в расплавленном состоянии он плотный и тягучий, а когда остывает — становится твёрдым и пластичным, он легко достаётся из формы, не ломается и не размазывается по ней.
Для чего нужен флюс, какой конкретно, в какой момент его использовать и где купить?
Флюс в кузнечном и литейном деле нужен для многих операций — пайки, кузнечной сварке, плавки и восстановительной плавки. В основном флюс нужен для растворения окислов и ограничения доступа кислорода. Самый универсальный флюс — натрий тетраборнокислый (https://ru.wikipedia.org/wiki/%D0%A2%D0%B5%D1%82%D1%80%D0%B0%D0%B1%D0%BE%D1%80%D0%B0%D1%82_%D0%BD%D0%B0%D1%82%D1%80%D0%B8%D1%8F) или просто бура. Он засыпается в тигель в момент плавления металла. Буру можно купить в магазинах промышленной химии или на складах стройматериалов (в Калининграде мы покупаем в «Регион-снабжении»).
Где взять олово, латунь и бронзу?
На складе цветного металлопроката или заказать по интернету (это выйдет значительно дороже). В Калининграде мы знаем два склада: «Курган-Балт» и «Балтцветмет».
Важный момент: чистое олово, без примесей свинца, стоит достаточно дорого, но если вы планируете отлитые изделия использовать в качестве украшений, посуды или игрушек, ни в коем случае не покупайте более дешевый припой, который активно предлагают продавцы.
Что стоит почитать тем, кто хочет заниматься литьем?
Книги по литейному производству, например «Основы технологии литейного производства» и «Справочник рабочего-литейщика».
Ред. Н. Давыдова
Латунь — Sciencemadness Wiki
Латунная оболочка и полоса
Латунь — название, данное наиболее распространенному медно-цинковому сплаву. Благодаря своим свойствам и эксплуатационным характеристикам он широко применяется в механических и электрических устройствах, а также во многих бытовых объектах и установках.
Содержимое
- 1 Состав
- 2 Свойства
- 3 Наличие
- 4 Подготовка
- 5 проектов
- 6 Обращение
- 6.1 Безопасность
- 6.2 Хранение
- 6.3 Утилизация
- 7 См. также
- 8 Каталожные номера
- 8.1 Соответствующие темы Sciencemadness
Состав
Обычные латунные сплавы состоят из 55–80 % меди и 45–15 % цинка, остальное — свинец, алюминий или кремний. Иногда встречаются никелевые и оловянные латуни. Никельсодержащую латунь (НЕ никелированную) легко отличить от обычной латуни, так как она слегка магнитится.
Иногда встречаются никелевые и оловянные латуни. Никельсодержащую латунь (НЕ никелированную) легко отличить от обычной латуни, так как она слегка магнитится.
Свойства
Фазовая диаграмма системы медь-цинк.
Латунь представляет собой металлический сплав соломенно-желтого цвета, часто напоминающий золото, с плотностью от 8,4 до 8,73 г/см 3 и температурой плавления от 900 до 940 °C, оба эти свойства зависят от сплава. Латунь податлива, хотя на это свойство сильно влияет ее состав.
Латунь образует защитное покрытие из оксида/карбоната цинка, которое предохраняет ее от дальнейшего окисления. Присутствие алюминия в латуни улучшит пассивацию.
Подобно меди, латунь не искрит при ударе или резке угловой шлифовальной машиной, что делает ее полезной в тех случаях, когда может возникнуть опасность возгорания.
Латунь медленно подвергается воздействию аммиака, образуя темно-синий раствор комплекса тетраамина меди.
Многие кислоты, такие как соляная кислота или серная кислота, только растворяют цинк из латуни, обнажая медь. Сильные основания достигают аналогичного эффекта. Окислители, такие как разбавленная азотная кислота, растворяют как медь, так и цинк из латуни.
Элементарная ртуть атакует латунь, образуя амальгаму с цинком и, в конечном итоге, с медью.
Доступность
Латунь доступна во всех хозяйственных магазинах в различных формах, таких как трубы, фитинги, инструменты, игрушки, украшения, ручки и т. д.
Латунный лом можно получить из выброшенных или поврежденных предметов, таких как фитинги, трубы, старые дверные ручки, водопроводные краны, навесные замки, различные музыкальные инструменты, корпуса нагревательных элементов, разъемы с головками для винтов старых ламп и т. д. Его также можно утилизировать. из различных старых электронных компонентов, таких как: радиаторы, штыревые разъемы, корпуса устройств, болты и винты, розетки, опоры электрических контактов и т. д.
д.
Если вы живете в США или имеете доступ к стрельбищу, пустые латунные гильзы также могут быть хорошим источником.
Из-за своей цены лом латуни предпочтительнее, хотя, если вам нужен определенный латунный сплав, вам придется его купить.
Плавить латунь немного сложнее, чем плавить алюминий, свинец или цинк в импровизированном литейном цеху из-за ее высокой температуры плавления, но вполне возможно плавить латунь дома, используя самодельную печь. Проблема при плавке латуни заключается в том, что цинк будет кипеть близко к температуре плавления латуни, что приведет к ее возгоранию и выделению вредной пыли ZnO.
Подготовка
Латунь можно получить путем сплавления цинка с медью в нужных пропорциях. Это осложняется тем, что температура кипения цинка (907°С) ниже температуры плавления меди (1085°С). Таким образом, сначала нужно расплавить медь, а затем добавить цинк. Часть цинка немедленно закипит, что приведет к «вспышке» с зеленым пламенем и белым дымом оксида цинка, а часть сплавится с медью. Для учета таких потерь необходимо добавлять избыток цинка. После сплавления цинк становится намного более стабильным (но все же будет несколько испаряться). Затем сплав следует энергично перемешать для гомогенизации металла.
Для учета таких потерь необходимо добавлять избыток цинка. После сплавления цинк становится намного более стабильным (но все же будет несколько испаряться). Затем сплав следует энергично перемешать для гомогенизации металла.
Чтобы ограничить выкипание цинка, полезно тщательно контролировать температуру. Добавление цинка сразу после расплавления меди, по-видимому, значительно ограничивает кипение. Использование флюса для покрытия (например, буры) также может быть полезным.
Проекты
- Литые красивые металлические предметы
- Сделать предметы устойчивыми к морской воде
- Источник меди и цинка
Обращение
Безопасность
Будучи медным сплавом, латунь обладает противомикробными свойствами, хотя образуемый ею пассивирующий слой снижает ее эффективность.
Старые сорта латуни, как правило, содержали вредный свинец.
Когда латунь расплавляется, например, при изготовлении латунных сплавов с нуля или отливке латунного лома, выделяются белые пары оксида цинка. Это может вызвать лихорадку металлического дыма, гриппоподобное состояние, которое может длиться несколько дней. NIOSH рекомендует для защиты от паров оксида цинка использовать противоаэрозольный респиратор не ниже N95.[1] Его следует носить в дополнение к любому средству защиты от тепла при работе с расплавленными металлами.
Это может вызвать лихорадку металлического дыма, гриппоподобное состояние, которое может длиться несколько дней. NIOSH рекомендует для защиты от паров оксида цинка использовать противоаэрозольный респиратор не ниже N95.[1] Его следует носить в дополнение к любому средству защиты от тепла при работе с расплавленными металлами.
Хранение
Предметы из латуни следует хранить вдали от кислот и аммиака.
Утилизация
Латунь лучше всего перерабатывается.
См. также
- Бронза
- Медь
Ссылки
Соответствующие нити Sciencemadness
- Обнаружение свинца в латуни?
- термит (медь/латунь)
- Медное/латунное покрытие и защита от питья
- Конденсатор OTC Латунь
- Латунь с гальваническим покрытием со свинцом
- Цинк в латуни не реагирует с кислотами?
- Извлечение цинка из латуни
- Процедура рафинирования латуни?
- Изготовление латуни Pinchbeck
Где находится точка плавления латуни?
Вопрос задан: Ольгой Куигли, доктором медицины
Оценка: 4,6/5
(22 голоса)
Температура плавления латуни: Красный: 1810-1880°F/990-1025°C . Желтый: 1660-1710°F/905-932°C .
Желтый: 1660-1710°F/905-932°C .
Какова температура плавления латуни?
Температура плавления 1880 F (1025 C) . Латунь: 1700 F (927 C) Латунь представляет собой сплав меди.
Можно ли плавить латунь в домашних условиях?
Металл, желтый сплав меди и цинка, плавится при 788 градусов по Фаренгейту и кипит при 1742 по Фаренгейту. … Сегодня люди могут плавить латунь дома . Латунь используется для изготовления различных предметов, включая пули, солнечные часы и скульптуры. Латунь также используется для изготовления дверных ручек, монет и болтов.
Плавится ли латунь раньше стали?
Латунь имеет относительно низкую температуру плавления по сравнению с железом, сталью или золотом , но все же требует специальной печи. Многие начинающие любители металлообработки начинают с алюминия, который легче плавить, но латунь часто является следующим шагом.
Какой металл легче всего расплавить?
В общем, алюминий легко плавится и до него легко добраться. Совет: многие люди расплавляют пустые алюминиевые банки из-под газировки, чтобы создать алюминиевые металлические формы. Нагревайте алюминий, пока он полностью не расплавится.
Совет: многие люди расплавляют пустые алюминиевые банки из-под газировки, чтобы создать алюминиевые металлические формы. Нагревайте алюминий, пока он полностью не расплавится.
Справочник по температурам плавления металлов (ºF)
Найдено 21 связанных вопросов
Какой металл имеет самую высокую температуру плавления?
Из всех металлов в чистом виде вольфрам имеет самую высокую температуру плавления (3422 °C, 6192 °F), самое низкое давление паров (при температурах выше 1650 °C, 3000 °F) и самую высокую прочность на растяжение.
Можно ли плавить латунь в стальном тигле?
Загрузите в тигель латунь, которую хотите расплавить. Используйте тигель, изготовленный из смеси глины и графита, т.к. металлические тигли могут расплавиться во время процесса.
Используйте тигель, изготовленный из смеси глины и графита, т.к. металлические тигли могут расплавиться во время процесса.
При какой температуре размягчается латунь?
Для медных и латунных сплавов физический процесс отличается, и температура мягкого отжига составляет от 300°C до 650°C для медных сплавов и от 425°C до 650°C для латунных сплавов .
Как определить, что это латунь?
Цельная латунь не обладает магнитными свойствами. Если магнит прилипает, предмет обычно стальной или чугунный с латунным покрытием. Если магнит не прилипает, вы можете продолжить проверку, поцарапав скрытую область острым предметом. Если вы видите блестящую желтую царапину, предмет, скорее всего, из цельной латуни.
Можно ли плавить латунь на костре?
Чтобы расплавить собственный металл на костре, не нужны вентиляторы, воздуходувки , древесный уголь или другие крайности. Пока горел огонь, я сделал форму, поместив латунную трубу диаметром 1 1/2 дюйма и длиной около 2 дюймов поверх большого плоского куска нержавеющей стали. … На самом деле они довольно быстро растаяли.
… На самом деле они довольно быстро растаяли.
Упрочняет ли латунь закалка?
Закалка латуни в воде НЕ закаляет латунь . Латунные изделия твердеют из-за проклейки, обжига и т. д. Поэтому латунь трескается после многократных обжигов и нагрузок, если они не были отожжены.
Какая разница между латунью и бронзой?
Латунь и бронза являются металлическими сплавами, что означает, что они представляют собой комбинацию двух или более различных металлов. Латунь состоит из меди и цинка, тогда как бронза состоит из меди и олова , иногда с добавлением других элементов, таких как фосфор или алюминий.
Какой материал лучше всего подходит для тигля?
Тигли и их крышки изготавливаются из материалов, устойчивых к высоким температурам, обычно фарфор, оксид алюминия или инертный металл . Одним из первых применений платины было изготовление тиглей. Керамика, такая как оксид алюминия, цирконий и особенно магнезия, выдерживает самые высокие температуры.
Имеет ли латунь ценность лома?
Желтая латунь также часто встречается в сантехнических материалах и трубах. … Мы заплатим вам около 1,50 доллара за фунт за латуни. Просто убедитесь, что ваша латунь чистая, в ней нет пластика, резины или стали. Следующий чрезвычайно ценный вид лома – это медь.
Медь сегодня чего-нибудь стоит?
Латунь принесет вам около . от 90 до 1,50/фунт . Если у вас есть латунь, которая не является ломом, вы можете попытаться продать ее на онлайн-рынке, через объявления или на распродажах. Имейте в виду, что если вы продаете его через Интернет, вам нужно будет отправить его, а доставка хэви-метала недешева.
Какой самый твердый металл?
Четыре самых прочных и твердых металла на Земле
- Вольфрам: самый прочный металл на Земле. Из всех металлов вольфрам лидирует по прочности на растяжение. …
- Хром: самый твердый металл на Земле. Хром – самый твердый металл, известный человеку.
 …
… - : самый прочный сплав на Земле. …
- Титан.
Сталь
Какой металл не плавится?
15 металлов с самой низкой температурой плавления: ртуть , франций, цезий, галлий, рубидий, калий, натрий, индий, литий, олово, полоний, висмут, таллий, кадмий и свинец.
Похожие вопросы
- 27Какова температура плавления латуни в градусах Фаренгейта?
- 45Что такое температура плавления латуни?
- 45Имеет ли латунь фиксированную температуру плавления?
- 33Какова температура плавления латунного припоя?
Реклама
Популярные вопросы
- 19Должны ли роялти включаться в себестоимость проданных товаров?
- 33Как связаться с эмитентом карты?
- 40Что означает прекондиционированный авокадо?
- 19Откуда взялся сагиттальный?
- 25Печ — это слово?
- 23Когда в Индии ликвидировали оспу?
- 40Кто-нибудь может пройти верификацию в тиндере?
- 24Что значит без музыки?
- 28Цикады появятся в 2021 году?
- 15Учитывается ли пристроенный гараж в квадратных метрах?
Топ-10 идей и источников вдохновения для плавления металлов
Сохранено с youtube. com
com
Плавление алюминиевых банок в домашних условиях — простой процесс переработки своими руками
Сегодня я буду плавить около 300 алюминиевых банок дома, в литейном цехе на заднем дворе. Я хранил эти банки из-под пива и содовой какое-то время, и я превращу их в…
Переработка алюминиевых банок
Поделки из алюминиевых банок
Изделия из металла
Самодельный металл
Переработанный металл
Scrap Metal
Переработанные ремесла
Metal Art
DIY Crafts
Дополнительная информация …
Shane Сохраняли на металле/сварке
Советы по сбережения
.
Сварные кончики
TIG Swisd
Металлическая сварка
Идеи сварки
Сварка Art
Сварные штучки
Сварка Таблица
Металлические проекты
Сварные проекты 9
0003
Подробнее…
Терри Потрясающий ☆✪☮(͡๏̯͡๏)★✌☀ сохранено в Art ☂ Glass-Cool✿ஜ(༻ ⌘༺)ஜॐ✿
Project
3
3 С медными трубками
Проекты с медными трубками. Медные трубы — излюбленный материал многих ремесленников, которые ценят его красоту и гибкость. Медная трубка мягче и легче сгибается, чем медная труба, но при этом достаточно прочная, чтобы стоять самостоятельно. Проекты из медных труб включают в себя скульптуры и сооружения для сада, а также предметы для дома…
Медные трубы — излюбленный материал многих ремесленников, которые ценят его красоту и гибкость. Медная трубка мягче и легче сгибается, чем медная труба, но при этом достаточно прочная, чтобы стоять самостоятельно. Проекты из медных труб включают в себя скульптуры и сооружения для сада, а также предметы для дома…
Mopper DIY
DIY Metal
Scrap Metal
Медный метал. Медное ремесло
Сохранено с ehow.com
Как плавить латунь
Спасите латунные трубы и фитинги из старого дома или здания для вашего следующего проекта.
Metal Shop
DIY Metal
Scrap Metal
Metal Crafts
Scrap Gold
переработанные металлические
DIY Crafts
Metal Work Project для ковки
Сохранено с offgridworld.com
Плавка алюминиевых банок с самодельным мини-металлическим тиглем за 20 долларов
Создайте свой собственный мини-литейный цех для плавки алюминиевых банок
Металлические рабочие проекты
Metal Art Projects
Металлические рабочие инструменты
Сварные проекты
Алюминиевые ремесла
Aluminum Cans
Metal Crafts
Металлическое дерево стены
Металлические настенные подвески
Meth Artain. .0003
.0003
Классы сварки
СВОДЫ СВЯЗИ
ГУД СВОРКА
Металлическая сварочная сварка
КОВМЕРИЯ МЕТАЛЛА
СВОДА
Дизайн сварки
Gulding Shop
Metal Project Дастин Ретерфорд сохранен в разделе «Сделай сам»
Сохранено с сайта hyperallergic.com
Как женщины-скульпторы раздвигают границы металла как среды
«Хэви-метал», выставленный в Национальном музее женщин в искусстве, демонстрирует женщин-художников, работающих со стереотипно мужским материалом.
Плавание металлов
Пеллинговая точка
Витраж с витражом
Kugel
Инсталляционное искусство
Художник на работе
Metal Art
Sculpture Art
Sculpting
. Скульптура
Сохранено с wikihow.com
Как плавить медь (с иллюстрациями) — wikiHow
Медь — это переходный металл, который легко проводит тепло и электричество, что делает его ценным материалом при изготовлении множества предметов. Медь выплавляется либо в виде слитков для хранения или продажи, либо для отливки других предметов, таких как…
Медь выплавляется либо в виде слитков для хранения или продажи, либо для отливки других предметов, таких как…
La Forge
Forge Diy
Металлообрабатывающие проекты
Металлообрабатывающие инструменты
Metal Art Diy
Изделия из металла 9
Донна Моррис сохранена в DIY
Термит — это материал, используемый при сварке для сплавления металлов. Это смесь металлического алюминия и оксида железа (оксида железа), которая производит расплавленное железо после окислительно-восстановительной реакции. Когда алюминий и кислород в смеси объединяются,…
Survival Weapons
Apocalypse Survival
Survival Tools
Survival Prepping
Emergency Preparedness
Survival Rifle
Allume Gaz
Melting Metal
Homemade Weapons
More information…
Chrisna SnymanC
Крисна Снайман сохранена на научной ярмарке
Сохранено с сайта expertlychosen. com
com
Чистый галлий
Галлий — это металл, который практически мгновенно тает в руке! На ощупь похож на ртуть, но не токсичен. Идеальный подарок для студентов-физиков и любителей науки
Плавание металла
Плавание точки
Lover Science
Учитель науки
Жидкий металл
WTF Fun Facts
Странные факты
Сумасшедшие факты
Смешные факты
Подробнее …
. в Подарки любителям науки
Характеристики легкоплавких сплавов
Производители по всему миру полагаются на качественные материалы для создания ряда деталей, оборудования и продуктов для предприятий и потребителей. В процессе сборки различные материалы могут быть соединены вместе для обеспечения герметичности, отлиты в форме до заданной формы или согнуты в новом направлении без разрушения. Легкоплавкие сплавы, также называемые легкоплавкими, имеют состав, который позволяет металлу переходить в жидкое или полужидкое состояние при низких температурах, а затем повторно затвердевать. Эти легкоплавкие сплавы идеальны, так как позволяют соединять или отливать детали при температурах ниже 300 градусов.
Эти легкоплавкие сплавы идеальны, так как позволяют соединять или отливать детали при температурах ниже 300 градусов.
Правильный выбор легкоплавкого сплава важен для обеспечения того, чтобы соединяемая, отливаемая или гнутая деталь сохраняла свою прочность и долговечность для применения. Поскольку производимое оборудование и детали подвергаются воздействию экстремальных давлений, напряжений и температур, вам необходимо иметь более полное представление о выбранных легкоплавких сплавах и их характеристиках во время затвердевания.
Распространенные легкоплавкие сплавы и их характеристики
Существует широкий спектр доступных легкоплавких сплавов. Тем не менее, некоторые из них ограничены в использовании из-за их хрупкости, токсичности и реакционных свойств. Некоторыми из этих элементов являются висмут, галлий, олово, индий, цинк, кадмий, теллур, сурьма, таллий, ртуть и свинец. Многие из этих минералов также могут быть добавками, добавляемыми при образовании легкоплавких сплавов. Сегодня мы обсудим четыре основных сплава: висмут, галлий, олово и индий.
Сегодня мы обсудим четыре основных сплава: висмут, галлий, олово и индий.
На основе олова: Олово — это один из распространенных легкоплавких сплавов на основе олова, который используется. Обычно в основе состава сплава будет около 50% элемента олова. Производители выбирают олово из-за его пластичности, когда им нужен металл с пластичными характеристиками, поскольку он может быть отлит в форму и придан форму, не становясь хрупким.
На основе висмута: Сплавы висмута будут иметь состав, который менее пластичен, чем олово, поскольку он может стать хрупким. Производители используют висмут из-за его способности расширяться, когда он плавится, а затем затвердевает, поскольку он может расширяться до 3,3%. Чем больше висмута в сплаве, тем больше он расширяется. Он дешевле, чем другие представленные сплавы, и наименее токсичен, поскольку его можно использовать в приложениях, где присутствует питьевая вода.
На основе индия: Сплавы индия можно использовать для приклеивания к золотым, стеклянным и керамическим поверхностям, а также к другим материалам. Он также может сваривать сам себя и обладает способностью смачивать как неметаллические, так и металлические поверхности. При поиске пластичного элемента, который предлагает фантастическую усталостную прочность и различные низкие температуры плавления, производители могут выбрать сплавы индия для своих применений.
Он также может сваривать сам себя и обладает способностью смачивать как неметаллические, так и металлические поверхности. При поиске пластичного элемента, который предлагает фантастическую усталостную прочность и различные низкие температуры плавления, производители могут выбрать сплавы индия для своих применений.
На основе галлия: Из-за чрезвычайно низкой температуры плавления сплавы на основе галлия способны плавиться, когда их держат в руке. Он превращается в жидкость при комнатной температуре, поскольку производители часто используют его для управления температурным режимом. Его также можно использовать для смачивания неметаллических и металлических поверхностей, включая стекло и фарфор. Подобно висмуту, галлий может становиться плотным и хрупким при затвердевании.
Характеристики плотности
Одной из основных причин использования легкоплавких сплавов является их изменение при плавлении и последующем затвердевании. Некоторые сплавы являются эвтектическими и мгновенно становятся чистой жидкостью, в то время как другие являются неэвтектическими и переходят в полужидкое состояние, которое имеет тип вязкой текстуры, прежде чем стать жидким. Легкоплавкие сплавы также изменяют плотность при затвердевании. Такие сплавы, как висмут и галлий, будут сильно расширяться в жидком состоянии, а затем станут плотными при переходе обратно в твердое состояние.
Легкоплавкие сплавы также изменяют плотность при затвердевании. Такие сплавы, как висмут и галлий, будут сильно расширяться в жидком состоянии, а затем станут плотными при переходе обратно в твердое состояние.
Важно знать плотность сплава, поскольку производителю необходимо знать, насколько он уменьшится или расширится. Если металл сжимается слишком сильно, он может не создать надлежащей связи с другими материалами или не иметь необходимой прочности, необходимой для противостояния нагрузкам. Если он расширится слишком сильно, он может стать хрупким при превращении обратно в твердое тело, поскольку сплав может выйти из строя во время работы продукта или оборудования.
Различные плотности сплавов также могут быть важны для производителей в зависимости от того, как они планируют использовать сплав. Для деликатных украшений вы можете не захотеть, чтобы материал расширялся слишком сильно, так как это может привести к повреждению окружающего металла, который должен оставаться неповрежденным. Вы также должны обратить внимание на удлинение, прочность, модуль растяжения и предел текучести сплава в процессе производства.
Вы также должны обратить внимание на удлинение, прочность, модуль растяжения и предел текучести сплава в процессе производства.
Здесь, в Belmont Metals, мы предлагаем различные легкоплавкие сплавы и металлы для различных применений в производственном процессе. Мы работаем уже 121 год, так как наше современное оборудование может предоставить вам подходящие легкоплавкие сплавы для ваших нужд.
Металлы, которые плавятся, и их свойства
Процесс плавки металла увлекательный и невероятно полезный для человечества. Однако все ли металлы плавятся? И плавятся ли одни металлы легче, чем другие? Читай дальше что бы узнать.
Содержание
- 1 Все ли металлы плавятся?
- 2 Какой металл легче всего расплавить?
- 2.1 Ртуть
- 2.2 Франций
- 2.3 Цезий
- 2.4 Галлий
- 2.5 Рубидий
- 4.1 Вольфрам
- 4.2 Ниобий
- 4.3 Молибден
- 4.4 Тантал
- 4.
 5 Рений
5 Рений
- 5 Металл для ювелирных изделий можно плавить дома?
Все ли металлы плавятся?
Да, все металлы плавятся. Их температуры плавления значительно различаются из-за различных факторов, таких как прочность связи, атомный вес и то, является ли это чистым металлом или сплавом.
Чтобы понять этот процесс, давайте сначала посмотрим, что такое «плавление».
В твердом состоянии ионы металлов упакованы в определенные оптимизированные структуры, известные как атомные решетки. Их удерживает вместе сила межатомных связей, при этом каждый из них вибрирует с определенной частотой. С повышением температуры эти связи ослабевают, позволяя атомам отдаляться друг от друга и вибрировать более энергично. Когда эти межатомные связи достаточно ослабевают, связи разрываются, и твердое тело становится жидким. При экстремальных температурах эти связи становятся настолько слабыми, что металлы закипают и превращаются в газ. Этого мы практически не можем добиться для большинства металлов, поскольку для этого требуются температуры, намного превышающие те, которые могут быть получены в большинстве печей.
Какой металл легче всего расплавить?
Температура плавления металлов сильно различается, в основном в зависимости от атомного веса и прочности межатомных связей. Некоторые металлы находятся в жидком состоянии даже при комнатной температуре.
Ртуть
Обозначение: Hg, Точка плавления: -37,89°F (-38,83°C)
Ртуть представляет собой жидкость при комнатной температуре. Также известный как ртуть, он выглядит как блестящая серебристая жидкость, которая намного тяжелее воды. Ртуть токсична, поэтому всегда работайте с ней в перчатках.
Франций
Символ: Fr, Температура плавления: 80,6⁰F (27⁰C)
Франций, самый электроположительный из всех известных элементов, встречается невероятно редко. Он также очень реакционноспособен и радиоактивн, с максимальным периодом полураспада 22 минуты. Это означает, что вы не увидите этот хэви-метал в таком виде очень долго. Этот металл также невероятно мягкий из-за большого размера его атомов.
Цезий
Обозначение: Cs, температура плавления: 83,3°F (28,5°C)
Цезий, теплый серебристо-золотой металл, бурно реагирует с водой. Как и в случае с францием, цезий также является мягким из-за большого размера атома. Атомы цезия являются самыми большими из всех известных элементов. В жидкой форме цезий выглядит как бледное жидкое золото. Благодаря его низкой температуре плавления вы можете сделать это, держа в руке контейнер с цезием.
Галлий
Обозначение: Ga, температура плавления: 85,58⁰F (29,76⁰C)
Галлий — широко доступный металл сероватого цвета. Поскольку он имеет низкую токсичность, его часто используют вместо ртути в домашних экспериментах. Его низкая температура плавления позволяет ему таять в руке в перчатке или в горячих жидкостях. Фокусники часто используют его в фокусе «исчезающая ложка».
Рубидий
Обозначение: рубидий, температура плавления: 102,7⁰F (39,3⁰C)
Рубидий — мягкий серебристо-белый металл с высокой реакционной способностью. Он бурно реагирует с водой и самовозгорается с образованием оксида рубидия.
Он бурно реагирует с водой и самовозгорается с образованием оксида рубидия.
Температура плавления различных металлов
Температура плавления металлов зависит от множества факторов, таких как атомный вес, прочность межатомных связей и чистота металла. Чистые металлы имеют тенденцию плавиться более равномерно, чем их легированные аналоги. Однако все металлы плавятся более равномерно, чем другие неметаллические вещества, такие как лед. Это связано с высокой теплопроводностью металла — металлы обычно намного плотнее, чем неметаллические вещества. Эта плотность обеспечивает равномерное распределение тепла по всему куску металла, даже если только небольшая его часть подвергается воздействию тепла. Это объясняет, почему слесари могут безопасно плавить и формировать большие куски металла, нагревая только его часть.
Температура плавления некоторых популярных металлов в порядке возрастания.
Какие металлы не плавятся?
Хотя все металлы плавятся, некоторые металлы имеют чрезвычайно высокую температуру плавления. Эти металлы обычно используются в огнеупорах, поскольку они могут выдерживать необычно высокие температуры без деформации — мы называем их «тугоплавкими металлами». Тугоплавкие металлы также могут выдерживать необычно высокий износ, что делает их невероятно прочными и долговечными.
Эти металлы обычно используются в огнеупорах, поскольку они могут выдерживать необычно высокие температуры без деформации — мы называем их «тугоплавкими металлами». Тугоплавкие металлы также могут выдерживать необычно высокий износ, что делает их невероятно прочными и долговечными.
Все тугоплавкие металлы имеют температуру плавления выше 2000⁰C, обладают высокой твердостью при комнатной температуре, химически инертны и имеют высокую плотность.
Вольфрам
При температуре 6170⁰F (3410⁰C) вольфрам имеет самую высокую температуру плавления среди всех известных металлов. Даже при высоких температурах вольфрам остается прочным. Таким образом, он широко используется в приложениях, требующих как высокой температуры, так и высокой прочности.
Вольфрам часто сплавляют с никелем, железом и медью – все это в количестве не более 10%. Из-за высокой температуры плавления компоненты из вольфрама производятся методом порошковой металлургии. Здесь легированные металлы не имеют высокого коэффициента диффузии и, следовательно, не проникают далеко внутрь компонента. По этой причине внутренняя часть вольфрамовых сплавов, как правило, состоит из чистого вольфрама.
По этой причине внутренняя часть вольфрамовых сплавов, как правило, состоит из чистого вольфрама.
Ниобий
Ниобий имеет температуру плавления 4491⁰F (2477⁰C). Этот светло-серый кристаллический металл похож на титан по твердости и пластичности, сравнимой с железом. Из-за своей низкой реакционной способности ниобий часто используется в качестве альтернативы никелю в ювелирных изделиях.
Используемый в основном в сплавах, даже 1% включение ниобия значительно повышает прочность металла. Это также повышает температурную стабильность сплавов. Ниобий, считающийся технологически важным элементом, широко используется в сверхпроводящих сплавах, атомной промышленности, электронике, оптике и других технических приложениях.
Молибден
Молибден имеет температуру плавления 4753⁰F (2623⁰C) и используется в тех же целях, что и вольфрам. Хотя сплавы молибдена уступают сплавам вольфрама, они более управляемы и менее затратны в производстве, что делает их идеальными для конкретных применений.
Наиболее распространенным молибденовым сплавом является TZM (титан-цирконий-молибден), который включает титан в количестве 0,5%, цирконий в количестве 0,08% и молибден в качестве остатка. ТЗМ обладает необычайно устойчивым сопротивлением ползучести и используется при рабочих температурах выше 1940⁰F (1060⁰C).
Легирование 70% молибдена 30% вольфрама дает Mo-30W, сплав с высокой стойкостью к расплавленному цинку. Предприятия по производству цинка в значительной степени полагаются на Mo-30W для своих форм для литья.
Молибден устойчив к жидкой ртутной коррозии и имеет низкий коэффициент трения, что объясняет его включение в смазки и масла, требующие высокого уровня надежности и производительности.
Тантал
При температуре плавления 5458⁰F (3017⁰C) тантал является наиболее стойким к коррозии из всех известных веществ. Он широко используется в медицинской и хирургической областях, а также в высокоагрессивных средах.
Тантал имеет чрезвычайно высокую объемную емкость, что делает его важным компонентом в миниатюрных электронных компонентах и схемах. Танталовые конденсаторы широко используются в сотовых телефонах и компьютерах.
Танталовые конденсаторы широко используются в сотовых телефонах и компьютерах.
Рений
Рений, недавно обнаруженный тугоплавкий металл, имеет температуру плавления 5765 ⁰F (3185 ⁰C). Поскольку это редкий металл, он является самым дорогим из всех тугоплавких металлов. Включение рения в металлические сплавы небольшими порциями повышает прочность на растяжение и пластичность. При этом рений наиболее широко используется в качестве катализатора различных промышленных химических реакций.
Можно ли плавить металл дома для украшений?
Многие украшения сделаны из металлов, особенно из золота, серебра, меди и никеля. Хотя металлические украшения обычно изготавливаются с использованием специального оборудования, вы можете плавить серебро дома, чтобы делать новые украшения. Имейте в виду, что серебро плавится при температуре 1763,24 ⁰F (961,8 ⁰C), поэтому вы должны использовать защитное снаряжение при попытке этого процесса.
Вот список необходимого оборудования:
- Тигель: термостойкий контейнер для плавки серебра.

- Источник тепла: должна работать паяльная лампа.
- Форма: для придания формы расплавленному серебру. Можно использовать различные продукты, в том числе песок или смесь гипса и талька в пропорции 3:1.
- Термостойкие щипцы для работы с тиглем.
- Защитное снаряжение: термостойкие перчатки и фартук, возможно, лицевой щиток.
Прежде чем начать, подготовьте форму – более простые формы с большей вероятностью дадут желаемый результат. Как только это будет сделано, пришло время расплавить ваше серебро. Если вы используете большой кусок серебра, используйте пару ножниц, чтобы разрезать его на маленькие кусочки. Это гарантирует, что металл плавится равномерно. Имейте в виду, что украшения обычно не сделаны из чистого серебра. По этой причине температура плавления часто меняется.
Когда металл станет жидким, залейте его в форму с помощью щипцов. Быстрое плавное движение гарантирует, что металл заполнит форму до того, как она снова затвердеет. Теперь просто подождите, пока он остынет, прежде чем вынимать его из формы.
Теперь просто подождите, пока он остынет, прежде чем вынимать его из формы.
Заключительные мысли
Хотя все металлы плавятся, их температуры плавления сильно различаются. Некоторые металлы являются жидкостями при комнатной температуре, в то время как другие имеют невероятно высокие температуры плавления. Не то чтобы вы знали, насколько сильно различаются металлы, мы надеемся, что вы думаете о металлах с новым интересом и любопытством.
Температура плавления металлов и сплавов – Teng Tools USA
Главная
/
Блог
/
Точка плавления металлов и сплавов
Кит Кросби | Последнее обновление 09 апреля 2020 г.
| Металл | °С | °F |
| Адмиралтейская латунь | 900 – 940 | 1650 – 1720 |
| Алюминий | 660 | 1220 |
| Алюминиевый сплав | 463 – 671 | 865 – 1240 |
| Алюминий Бронза | 600 – 655 | 1190 – 1215 |
| Баббит | 249 | 480 |
| Бериллий | 1285 | 2345 |
| Бериллиевая медь | 865 – 955 | 1587 – 1750 |
| Висмут | 4}»> 271,4 | 520,5 |
| Латунь, красный | 1000 | 1832 |
| Латунь, желтая | 930 | 1710 |
| Кадмий | 321 | 610 |
| Хром | 1860 | 3380 |
| Кобальт | 1495 | 2723 |
| Медь | 1084 | 1983 |
| 1063 | 1945 | |
| Железо, кованое | 1482 – 1593 | 2700 – 2900 |
| Железо, серое литье | 1127 – 1204 | 2060 – 2200 |
| Чугун, ковкий | 1149 | 2100 |
| Свинец | 5}»> 327,5 | 621 |
| Магний | 650 | 1200 |
| Магниевый сплав | 349 – 649 | 660 – 1200 |
| Марганец | 1244 | 2271 |
| Марганцевая бронза | 865 – 890 | 1590 – 1630 |
| Меркурий | 86}»> -38,86 | -37,95 |
| Молибден | 2620 | 4750 |
| Никель | 1453 | 2647 |
| Палладий | 1555 | 2831 |
| Фосфор | 44 | 111 |
| Платина | 1770 | 3220 |
| Родий | 1965 | 3569 |
| Кремний | 1411 | 2572 |
| Чистое серебро | 961 | 1761 |
| Серебро, Стерлинг | 893 | 1640 |
| Углеродистая сталь | 1425 – 1540 | 2600 – 2800 |
| Нержавеющая сталь | 1510 | 2750 |
| Олово | 232 |

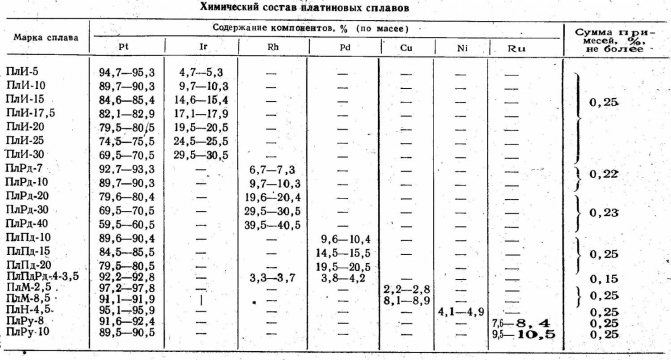
 86
86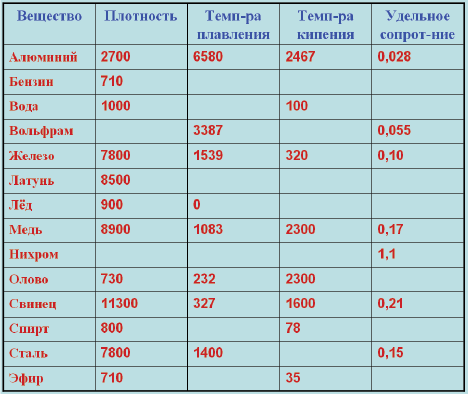 °С)
°С)