Виды коррозии и их суть: Виды коррозии | Руководство по выбору материалов
Содержание
Коррозия и виды коррозии — Металл
Коррозия и виды коррозии — Металл
Термин коррозия происходит от латинского «corrosio», что означает разъедать, разрушать. Этот термин характеризует как процесс разрушения, так и результат.
Среда, в которой металл подвергается коррозии (коррозирует) называется коррозионной или агрессивной средой.
В случае с металлами, говоря об их коррозии, имеют в виду нежелательный процесс взаимодействия металла со средой. Физико-химическая сущность изменений, которые претерпевает металл при коррозии является окисление металла.
Любой коррозионный процесс является многостадийным:
- Необходим подвод коррозионной среды или отдельных ее компонентов к поверхности металла.
- Взаимодействие среды с металлом.
- Полный или частичный отвод продуктов от поверхности металла (в объем жидкости, если среда жидкая).
Коррозионный процесс является самопроизвольным, следовательно G=G-G (G и G относятся к начальному и конечному состоянию соответственно). Если G>G то G<0, т.е. коррозионный процесс возможен; G>0 коррозионный процесс невозможен; G=0 система металл-продукт находится в равновесии. То есть можно сказать, что первопричиной коррозии металла является термодинамическая неустойчивость металлов в заданной среде.
Если G>G то G<0, т.е. коррозионный процесс возможен; G>0 коррозионный процесс невозможен; G=0 система металл-продукт находится в равновесии. То есть можно сказать, что первопричиной коррозии металла является термодинамическая неустойчивость металлов в заданной среде.
1. Классификация коррозионных процессов.
- По механизму процесса различают химическую и электрохимическую коррозию металла.Химическая коррозия — это взаимодействие металлов с коррозионной средой, при котором окисляется металл и восстанавливается окислительные компоненты коррозионной среды протекают в одном акте. Так протекает окисление большинства металлов в газовых средах содержащих окислитель (например, окисление в воздухе при повышении температуры).Электрохимическая коррозия — это взаимодействие металла с коррозионной средой, при котором ионизация атомов металла и восстановление окислительной компоненты среды происходит не водном акте, и их скорости зависят от электродного потенциала металла. По такому процессу протекают, например, взаимодействие металла с кислотами.

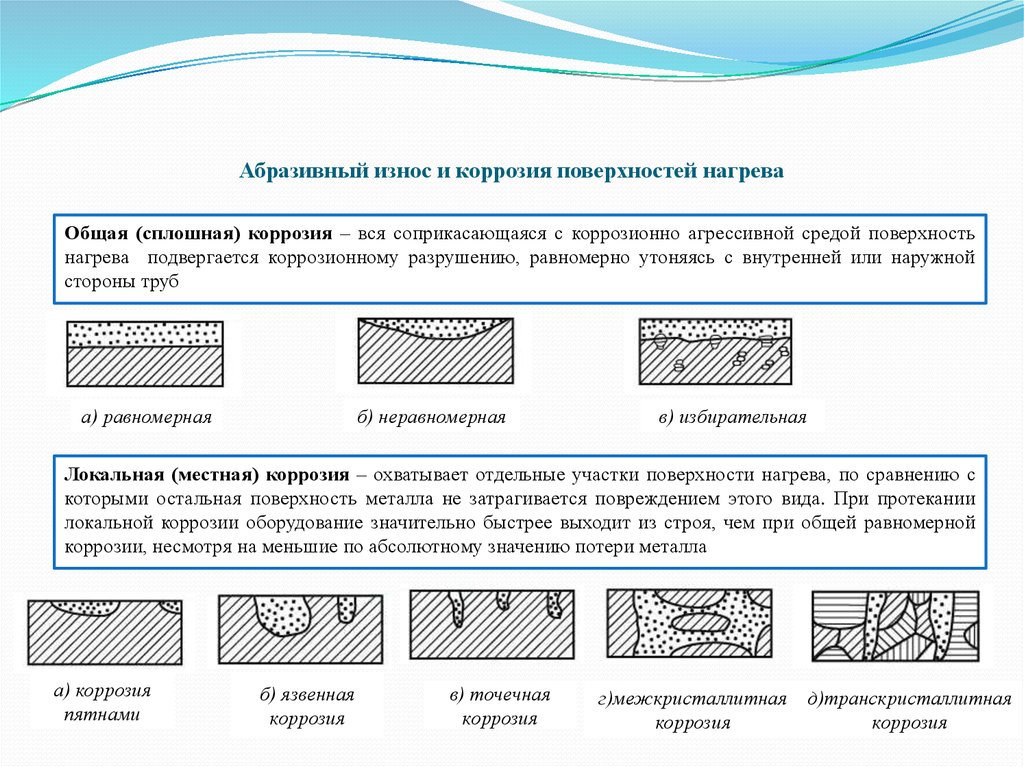
- По характеру коррозионного разрушения.Общая или сплошная коррозия при которой коррозирует вся поверхность металла. Она соответственно делится на равномерную (1а), не равномерную (1б) и избирательную (1в), при которой коррозионный процесс распространяется преимущественно по какой-либо структурной составляющей сплава.Местная коррозия при которой коррозируют определенные участки металла:
- коррозия язвами — коррозионные разрушения в виде отдельных средних и больших пятен (коррозия латуни в морской воде)
- межкристаллическая коррозия при ней процесс коррозии распространяется по границе металл-сплав (алюминий сплавляется с хромоникелем) и другие виды коррозии.
- По условиям протекания процесса.
- Газовая коррозия — это коррозия в газовой среде при высоких температурах. (жидкий металл, при горячей прокатке, штамповке и др.)
- Атмосферная коррозия — это коррозия металла в естественной атмосфере или атмосфере цеха (ржавление кровли, коррозия обшивки самолета).

- Жидкостная коррозия — это коррозия в жидких средах: как в растворах электролитов, так и в растворах не электролитов.
- Подземная коррозия — это коррозия металла в почве
- Структурная коррозия — коррозия из-за структурной неоднородности металла.
- Микробиологическая коррозия — результат действия бактерий
- Коррозия внешним током — воздействие внешнего источника тока (анодное или катодное заземление)
- Коррозия блуждающими токами — прохождение тока по непредусмотренным путям по проекту.
- Контактная коррозия — сопряжение разнородных электрохимических металлов в электропроводящей среде.
- Коррозия под напряжением — одновременное воздействие коррозионной среды и механического напряжения.
1.2 Показатель скорости коррозии.
Для установления скорости коррозии металла в данной среде обычно ведут наблюдения за изменением во времени какой-либо характеристики, объективно отражающей изменение свойства металла.
Чаще всего в коррозионной практике используют следующие показатели.
- Показатель изменения массы — изменение массы образца в результате коррозии отнесенный к единице поверхности металла S и к единице времени (например, г/м ч) в зависимости от условий коррозии различают:
- отрицательный показатель изменения массы
- положительный показатель изменения массы
- Объемный показатель коррозииПрименительно к электрохимической коррозии когда процесс катодной деполяризации осуществляется за счет разряда ионов водорода, например, по схеме 2Н + 2е = Н, или ионизация молекул кислорода О + 4е +2НО = 4ОН; вводятся соответственно кислородный (К ) и водородный (К ) показатель соответственно.Водородный показатель коррозии — это объем выделившегося Н в процессе коррозии, отнесенный к Su .
Кислородный показатель коррозии — это объем поглощенного в процессе О , отнесенный к Su .
- Показатель сопротивления.Изменение электрического сопротивления образца металла за определенное время испытаний также может быть использован в качестве показания коррозии (К).
 КR = ( R/Ro)100% за время t
КR = ( R/Ro)100% за время tгде Ro и R электрическое сопротивление образца соответственно до и после коррозии.
У этого способа есть некоторый недостаток толщина металла во все время испытаний должна быть одинаковой и по этой причине чаще всего определяют удельное сопротивление, т.е. изменение электрического сопротивления на единицу площади образца (см, мм) при длине равной единице. Этот метод имеет ограничения применения (для листового металла не более 3мм). Наиболее точные данные получают для проволочных образцов. Этот метод не пригоден для сварных соединений.
- Механический показатель коррозии.Изменение какого-либо свойства металла за время коррозии . Сравнительно часто пользуются изменением предела прочности.Глубина коррозионного разрушения может быть средней или максимальной. Глубинный показатель коррозии можно использовать для характеристики как равномерной., так и неравномерной коррозии (в том числе и местной) металлов. Он удобен для сравнения скорости коррозии металла с различными плотностями.
 Переход от массового, токового и объемного к глубинному возможен при равномерной коррозии.
Переход от массового, токового и объемного к глубинному возможен при равномерной коррозии.
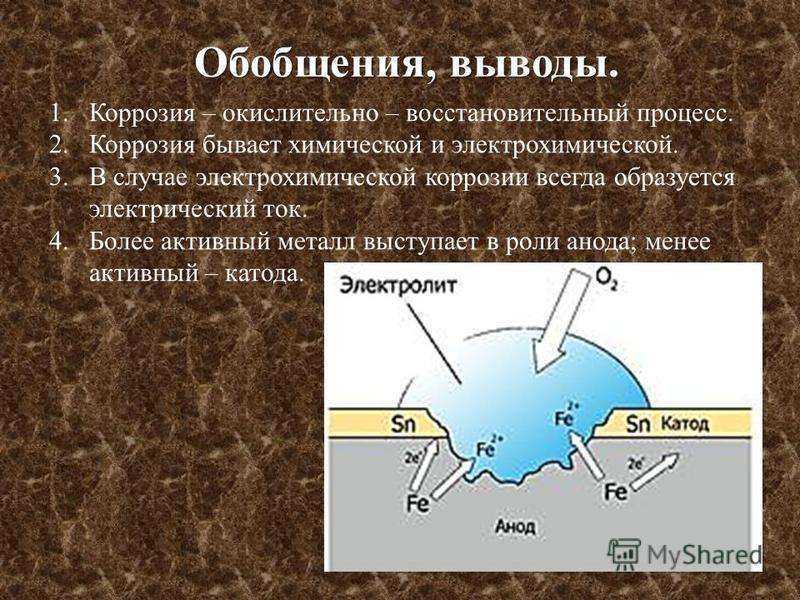
2. Электрохимическая коррозия.
Электрохимическая коррозия является наиболее распространенным типом коррозии металлов. По электрохимическому механизму коррозируют металлы в контакте с растворами электролитов (морская вода, растворы кислот, щелочей, солей) . В обычных атмосферных условиях и в земле металлы коррозируют также по электрохимическому механизму , т.к. на их поверхности имеются капли влаги с растворенными компонентами воздуха и земли. Электрохимическая коррозия является гетерогенным и многостадийным процессом. Ее причиной является термодинамическая неустойчивость металлов в данной коррозионной среде.
Термодинамика электрохимической коррозии металлов.
Стремлением металлов переходить из металлического состояния в ионное для различных металлов различно. Вероятность такого перехода зависит также от природы коррозионной среды. Такую вероятность можно выразить уменьшением свободной энергии при протекании реакции перехода в заданной среде при определенных условиях.

Следовательно, для электрохимического растворения металла необходимо присутствие в растворе окислителя (деполяризатора, который бы осуществлял катодную реакцию ассимиляции электронов), обратимый окислительно-восстановительный потенциал которого положительнее обратимого потенциала металла в данных условиях.
Катодные процессы при электрохимической коррозии могут осуществляться различными веществами.
- ионами
- молекулами
- оксидами и гидрооксидами (как правило малорастворимыми продуктами коррозии, образованными на поверхности металлов)
- органическими соединениями
В коррозионной практике в качестве окислителей-деполяризаторов, осуществляющих коррозию, выступают ионы водорода и молекулы растворенного в электролите кислорода.
При увеличении активности ионов металла (повышение концентрации ионов металла в растворе), потенциал анода возрастает, что приводит к торможению растворения металла. Понижение активности металла, напротив, способствует растворению металла.
 В ходе коррозионного процесса изменяются не только свойства металлической поверхности, но и контактирующего раствора (изменение концентрации отдельных его компонентов). При уменьшении, например, концентрации деполяризатора, у катодной зоны может оказаться, что катодная реакция деполяризации термодинамически невозможна.
В ходе коррозионного процесса изменяются не только свойства металлической поверхности, но и контактирующего раствора (изменение концентрации отдельных его компонентов). При уменьшении, например, концентрации деполяризатора, у катодной зоны может оказаться, что катодная реакция деполяризации термодинамически невозможна.Гомогенные и гетерогенные пути электрохимической коррозии.
Причину коррозии металлов в растворах, не содержащих одноименных ионов, объясняет теория необратимых потенциалов. Эта теория рассматривает поверхность металлов как однородную, гомогенную. Основной и единственной причиной растворения (коррозии) таких металлов является термодинамическая возможность протекания анодного и катодного актов. Скорость растворения (коррозии) будет определяться кинетическими факторами. Но гомогенную поверхность металлов можно рассматривать как предельный случай, который может быть реализован, например, в жидких металлах. (ртуть и амальгамы металлов). Для твердых металлов такое допущение будет ошибочным, хотя бы потому что различные атомы сплава (и чистого металла) занимают различное положение в кристаллической решетке.
 Наиболее сильное отклонение от гомогенной конструкции будет наблюдаться при наличии в металле инородных включений, интерметаллидов, границ зерен и т.д. В этом случае, разумеется, поверхность является гетерогенной. Установлено, что даже при наличии на поверхности металла неоднородностей в целом поверхность остается эквипотенциальной.
Наиболее сильное отклонение от гомогенной конструкции будет наблюдаться при наличии в металле инородных включений, интерметаллидов, границ зерен и т.д. В этом случае, разумеется, поверхность является гетерогенной. Установлено, что даже при наличии на поверхности металла неоднородностей в целом поверхность остается эквипотенциальной.Таким образом, неоднородность поверхностей сплава не может являться основной причиной общей коррозии металла. Наиболее существенной в подобных случаях является ионизация растворения анодной составляющей вблизи катодной составляющей, это возможно, если на поверхности металлической конструкции возникают гальванические элементы. Рассмотрим некоторые из них:
а) неоднородность металлической фазы, обусловленная неоднородностью сплава, а также в результате микро и макровключений.
б) неоднородность поверхности металла в следствие наличия границ блоков и зерен кристаллов, выход дислокаций на поверхность, анизотропность кристаллов.
в), г) неоднородность защитных пленок на поверхности за счет микро и макропор пленки (в), за счет неравномерного образования на поверхности вторичных продуктов коррозии (г) и др.

Мы рассмотрели два крайних механизма саморастворения металлов: равномерное растворение идеально гомогенной поверхности и растворения (в основном локальное) микроэлементов при пространственном разделении катодных и анодных зон (процессов).
В общем случае, необходимо считаться с возможностью протекания на анодных участках наряду с основными анодными процессами катодных процессов, на катодных же участках могут протекать с пониженной скоростью анодные процессы растворения.
Можно сделать вывод, что нет оснований противопоставлять «гомогенный» и «гетерогенный» пути протекания коррозионных процессов. Правильнее будет их рассматривать как факторы, взаимно дополняющие друг друга. Основной же причиной коррозии металлов остается по-прежнему термодинамическая вероятность протекания в данных условиях на металле анодных процессов ионизации металла и сопряженного с ним катодного процесса деполяризации.
Анодные процессы при электрохимической коррозии металлов.
Термодинамические основы.
Для протекания коррозионного процесса существенным является состояние форма соединения , в котором находится катион металла в растворе. Ионизация металла с последующим переходом в раствор простых компонентов металла представляет лишь одно из возможных направлений анодных процессов. Форма их конкретного состояния во многом определяется как природой металла и контактирующей с ним средой , так и направлением и величиной поляризующего тока (или электродного потенциала). Переходя в раствор, коррозирующий металл вступает в связь либо с растворителем, либо с компонентами раствора. При этом могут образовываться простые и комплексные соединения с различной растворимостью и с различной адгезией к поверхности металла. При высоких положительных значениях потенциала на аноде возможен процесс окисления воды с выделением кислорода. В зависимости от того, какие процессы или их сочетания протекают на аноде, они могут в значительной мере (а иногда и полностью) контролировать суммарный процесс коррозии.

Причины анодного растворения металлов.
Простейшими анодными реакциями являются такие , в результате которых образуются растворимые гидратированные и комплексные катионы,. которые отводятся от анода путем диффузии, миграции (перенос за счет электрического поля) или конвекции.
Полярные молекулы жидкости электростатически взаимодействуют с заряженными ионами, образуют сольватные (в случае воды-гидратные) комплексы. Обладающие значительно меньшим запасом энергии чем ионы в кристаллической решетки металла. Величину этого понижения можно оценить, исходя из соображений предложенных Борном. Полный электрический заряд в вакууме обладает энергией, равной потенциальной энергии. Для определения величины энергии заряда представим, что проводящая сфера радиусом r имеет заряд q. Внесение еще одной части заряда dq в сферу должно быть встречено отталкивающими силами df=qdq/r. Поистине огромное уменьшение энергии иона в водном растворе указывает на устойчивость такого состояния в нем.
 Таким образом, причиной перехода атомов металла с поверхности и их ионизация является электростатическое взаимодействие (сольватация) ионов металла с полярными молекулами растворителя.
Таким образом, причиной перехода атомов металла с поверхности и их ионизация является электростатическое взаимодействие (сольватация) ионов металла с полярными молекулами растворителя.Анодная пассивность металлов.
При значительном торможении анодной реакции ионизации металла скорость коррозионного процесса может понизится на несколько порядков. Такое состояние металла принято называть анодной пассивностью. Пассивность можно определить следующим образом: пассивность — состояние повышенной коррозионной устойчивости металла или сплава (в условиях, когда термодинамически он является реакционно способным), Вызванное преимущественным торможением анодного процесса т.е. может произойти так, что в реальных условиях скорость коррозии «активных» элементов оказывается весьма незначительной в следствии наступления пассивного состояния. Например, титан расположенный левее цинка, и хром, расположенный рядом с цинком, в следствии наступления пассивности оказываются более коррозионностойкими в большинстве водных сред, чем цинк.
 На склонность к пассивному состоянию влияет природа системы металл-раствор. Наибольшую склонность к переходу в пассивное состояние проявляют Ti,Ni,Al,Mg,Fe,Co и др.
На склонность к пассивному состоянию влияет природа системы металл-раствор. Наибольшую склонность к переходу в пассивное состояние проявляют Ti,Ni,Al,Mg,Fe,Co и др.Наступление пассивного состояния приводит к значительному изменению формы анодной поляризационной кривой. Кривая может быть разбита на несколько характерных участков:
Но начиная с В становится возможным процесс образования защитного слоя (фазового или адсорбционного), скорость которого растет при смещении потенциала в положительную сторону. Это приводит к торможению анодного растворения (BD). В точке D, соответствующей потенциалу ( потенциал начала пассивации) скорость образования защитного слоя равна скорости его растворения. Далее идет рост защитного слоя, экранирующего поверхность, скорость анодного растворения резко понижается (DE). В точке Е, соответствующей потенциалу полной пассивации металл оказывается в пассивном состоянии. На участке EF (область пассивного состояния) скорость анодного процесса не зависит от потенциала, а определяется скоростью химического растворения защитной пленки.
 Ток соответствующий области пассивного состояния, называется током пассивного состояния (i ). Положительнее F возможна ( -потенциал перепассивации) новая ветвь активного растворения с образованием катионов более высокой валентности.
Ток соответствующий области пассивного состояния, называется током пассивного состояния (i ). Положительнее F возможна ( -потенциал перепассивации) новая ветвь активного растворения с образованием катионов более высокой валентности.При высоких положительных потенциалах возможен локализованный пробой оксидной пленки — металл начинает растворятся по типу питтинга (PP’) называют потенциалом питтингообразования.
Металл запассивированный в данной среде, может сохраняться в пассивном состоянии некоторое время в непассивирующей среде.
3. Деполяризация.
При наличии в растворе газообразного кислорода и не возможностью протекания процесса коррозии с водородной деполяризацией основную роль деполяризатора исполняет кислород коррозионные процессы, у которых катодная деполяризация осуществляется растворенным в электролите кислородом, называют процессами коррозии металлов с кислородной деполяризацией. Это наиболее распространенный тип коррозии металла в воде, в нейтральных и даже в слабокислых солевых растворах, в морской воде, в земле, в атмосфере воздуха.
Коррозия металла с кислородной деполяризацией в большинстве практических случаев происходит в электролитах, соприкасающихся с атмосферой, парциальное давление кислорода в которой Р=0,21 атм. Следовательно, при определении термодинамической возможности протекания коррозионного процесса с кислородной деполяризацией следует производить учитывая реальное парциальное давление кислорода в воздухе (см. табл.). Т.к. значения (V ) очень положительны, то условия соблюдаются в очень многих случаях. В следующей таблице приведены значения ЭДС и изменения изобарно-изотермических потенциалов коррозионных процессов с кислородной деполяризацией:
Изучение восстановления кислорода на неблагородных металлах (а именно они представляют наибольший интерес с точки зрения коррозии) затрудняется тем, что при катодной поляризации электрода металл может иметь потенциал более положительный, чем равновесный и, следовательно, подвергается окислению (ионизации).
При катодной поляризации в определенном интервале потенциалов будут происходить одновременно два процесса восстановление кислорода и окисление металла.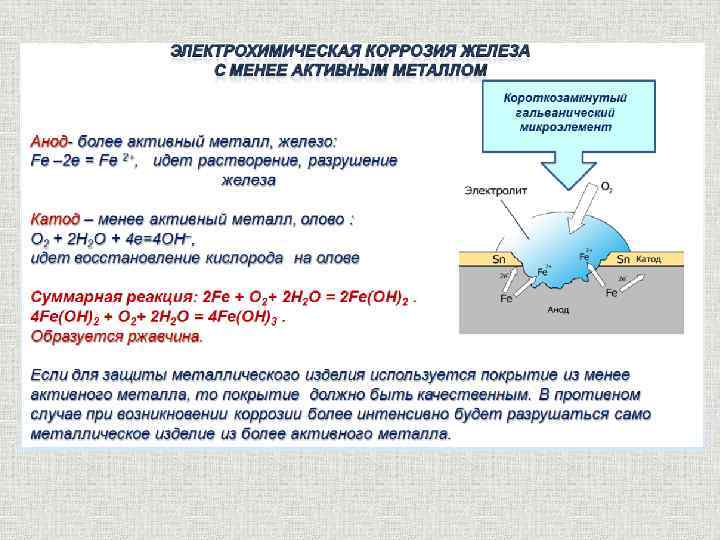 Окисление металла прекратится когда потенциал металла будет равен или станет отрицательнее равновесного потенциала металла. Эти обстоятельства затрудняют изучение процессов кислородной деполяризации.
Окисление металла прекратится когда потенциал металла будет равен или станет отрицательнее равновесного потенциала металла. Эти обстоятельства затрудняют изучение процессов кислородной деполяризации.
Список используемой литературы
1. Исаев «Коррозия металлов»
2. Жук «Курс коррозии и защиты металлов»
+7 800 201-25-58
+7 495 198-17-23
+7 495 767-10-42
[email protected]
Спасибо! Ваше сообщение успешно отправлено!
Компания*
Номер телефона*
ФИО*
Электронная почта*
Загрузить файл
Интересующая услуга
Своими словами
И снова о коррозии
Автор: Josef Dominik
Перевод: Игнатова Д.В., специалист по маркетингу ООО ЗВК «БЕРВЕЛ»
Согласно данным, предоставленным специалистами лаборатории NASA по коррозионным технологиям в космическом центре Кеннеди, расходы, связанные с коррозией металлов в США, составляют примерно 276 млрд долларов в год. Эта огромная сумма включает в себя прямые и косвенные издержки, связанные с коррозией. В США по последним данным ущерб от коррозии и затраты на борьбу с ней составили 4-5% от ВВП. Эта цифра ежегодно растёт. Согласно статистике состояния окружающей среды более 250000 тонн серной кислоты ежедневно выпадает в виде кислотного дождя в северном полушарии. По оценкам экспертов каждую секунду коррозия «съедает» более 5 тонн стали. Поэтому стоит в очередной раз задуматься о проблеме коррозии.
Эта огромная сумма включает в себя прямые и косвенные издержки, связанные с коррозией. В США по последним данным ущерб от коррозии и затраты на борьбу с ней составили 4-5% от ВВП. Эта цифра ежегодно растёт. Согласно статистике состояния окружающей среды более 250000 тонн серной кислоты ежедневно выпадает в виде кислотного дождя в северном полушарии. По оценкам экспертов каждую секунду коррозия «съедает» более 5 тонн стали. Поэтому стоит в очередной раз задуматься о проблеме коррозии.
Предотвращение коррозии
Подсчитано, что более 25% ущерба от коррозии можно было бы избежать, своевременно используя средства противокоррозионной защиты. Обязательным условием эффективного предотвращения образования коррозии является знание всех коррозионных процессов, а также свойств применяемого металла и состояния окружающей среды. Типичный пример неправильного соблюдения этих простых условий показан на рис.1. Много раз подчёркивалось, что борьба с коррозией начинается ещё на стадии проектирования и строительства. Рис. 2 демонстрирует неправильное проектирование крытого плавательного бассейна.
Рис. 2 демонстрирует неправильное проектирование крытого плавательного бассейна.
Рис. 1
Рис. 2 и 3
В данном случае проектировщик произвёл крепление опорных болтов из нержавеющей хромоникелевой стали к бетонному потолку. Предполагалось, что все параметры и размеры были выполнены верно, но оказалось, что была допущена серьёзная ошибка. Проектировщик не учёл тот факт, что в целях соблюдения санитарно-гигиенических норм в бассейне регулярно проводится хлорирование воды. Пары хлорида проникли в пространство между потолком и крышей и, как следствие, началась коррозия нержавеющей хромоникелевой стали. Как известно, этот вид стали не устойчив к воздействию хлора, поэтому возникла проблема ослабления поперечного сечения болтов (рис. 3). В результате произошло обрушение целого потолка. Более того, внешний контроль опорных болтов не проводился.
Какую полезную информацию можно извлечь из данного случая?
1. Даже нержавеющая сталь при определённых условиях подвержена коррозии.
Даже нержавеющая сталь при определённых условиях подвержена коррозии.
2. Эффективное предупреждение коррозии предполагает безупречные знания воздействия окружающей среды на свойства металлов.
3. Опорные болты должны подвергаться регулярному внешнему контролю.
4. Технология водоподготовки в бассейне не была учтена проектировщиком.
5. Некачественное выполнение проектной документации.
Подобных примеров возникновения коррозии много. Главной причиной преждевременного возникновения коррозии является человеческий фактор, то есть пренебрежение и недооценивание важности проблемы защиты от коррозии на стадии проектирования. Коррозия — это многостадийный сложный процесс, который необходимо изучать целостно. Только изучив саму суть коррозионного процесса и виды коррозии, можно приступать к изучению, разработке методов защиты.
С практической точки зрения, эффективно разделять коррозию на видимую, менее видимую и невидимую. К первой группе относится поверхностная коррозия. Поверхностная коррозия характеризуется равномерным разрушением металла по всей поверхности. Это наименее опасный вид коррозии, потому что её можно легко обнаружить и устранить.
Поверхностная коррозия характеризуется равномерным разрушением металла по всей поверхности. Это наименее опасный вид коррозии, потому что её можно легко обнаружить и устранить.
Однако существуют и более опасные, малозаметные виды коррозии:
• местная коррозия;
• контактная коррозия;
• межкристаллитная коррозия;
• коррозионное растрескивание.
Самым опасным видом коррозии является невидимая межкристаллитная (интеркристаллитная) коррозия. В этом случае разрушение происходит по границам кристаллов и внешняя поверхность металла не имеет заметных следов коррозии.
Особенно опасным является водородное охрупчивание металла (рис. 4), так как проявления практически невозможно заметить даже под микроскопом. Высокопрочные стали наиболее подвержены водородному охрупчиванию. Предупреждение коррозии в данном случае основано на обезводороживании или применении устойчивых к охрупчиванию сплавов. Для гарантированного предотвращения водородной хрупкости у сталей с прочностью более 1000 Н/мм2 целесообразно применять «бестоковые» способы цинкования, при нанесении которых наводороживание деталей не происходит. К таким относятся горячее цинкование, цинк-ламельные покрытия, покрытие типа «Дакромет» и другие на основе высокодисперсного цинка.
К таким относятся горячее цинкование, цинк-ламельные покрытия, покрытие типа «Дакромет» и другие на основе высокодисперсного цинка.
Рис. 4
Выводы
В заключении стоит отметить, что коррозия всегда существовала и будет существовать. Без сомнения, миллиардные ежегодные убытки привели к тому, что люди стали бороться с этим вредным воздействием. Можно с уверенностью говорить о том, что все виды коррозии приводят к потере не самого металла, а ценных металлоконструкций, на строительство которых тратятся огромные деньги. Стоит помнить о том, что преждевременное разрушение конструкции из-за воздействия коррозии может привести к непредвиденным последствиям. К сожалению, проблему коррозии нельзя избежать, но любую проблему можно решить при правильно организованном, грамотном подходе. Существует немало «ключей» (методов) к предотвращению коррозии, однако их нужно заблаговременно и правильно применять.
Дата: 03.05.18
Источник: Fastener World Inc.
Что вызывает окисление или ржавчину металлов?
Техническая библиотека » Темы по металлизации » Что вызывает окисление или «ржавение» металлов?
Все металлы, за исключением драгоценных металлов, окисляются под воздействием кислорода и электролита (т.е. атмосферной влаги). Это химическая реакция поверхности металла с кислородом, присутствующим в воздухе, которая вызывает коррозию (или окисление) части металла и образование соответствующего оксида металла на поверхности. В некоторых металлах, таких как сталь, образовавшиеся продукты коррозии очень заметны и рыхлы. Все видели красный цвет окиси железа (ржавчины) на плохо защищенных стальных изделиях. Образовавшаяся красная ржавчина, как правило, чешуйчатая и рыхлая, легко отпадает, подвергая все больше и больше основного материала воздействию окружающей среды. Однако такие металлы, как нержавеющая сталь (сталь с добавлением никеля и хрома), также окисляются. Разница в том, что образующиеся оксиды никеля и хрома представляют собой более однородный и прочный оксидный слой, который защищает основной материал, «изолируя» поверхность от дальнейшего окисления после образования.
Разница в том, что образующиеся оксиды никеля и хрома представляют собой более однородный и прочный оксидный слой, который защищает основной материал, «изолируя» поверхность от дальнейшего окисления после образования.
Рисунок F.1: Дуплексная никелевая система
В дополнение к поверхностному окислению, которое происходит на отдельных металлах, любые два разнородных металла, находящиеся в контакте друг с другом с электролитом (таким как атмосферная влага или вода), образуют коррозионную ячейку. . Это основа аккумуляторов, используемых в повседневных продуктах. Один из двух контактирующих металлов будет подвергаться коррозии в большей степени, чем другой, и образовывать соответствующий оксид этого металла. Какой металл подвергается коррозии, основано на том, что химики называют электродвижущей серией металлов. Выбор того, какой слой покрытия использовать, является важным, поскольку гальванопокрытие по своей сути представляет собой процесс помещения двух разнородных металлов в контакт друг с другом. Гальванический слой (или слои) может быть либо анодным покрытием (покрытие корродирует в большей степени, чем подложка), либо катодным покрытием (подложка корродирует в большей степени, чем гальванический слой). Независимо от того, является ли покрытие анодным или катодным, сильно влияет на то, как система отделки будет работать после эксплуатации, и у каждого есть свои преимущества и недостатки.
Гальванический слой (или слои) может быть либо анодным покрытием (покрытие корродирует в большей степени, чем подложка), либо катодным покрытием (подложка корродирует в большей степени, чем гальванический слой). Независимо от того, является ли покрытие анодным или катодным, сильно влияет на то, как система отделки будет работать после эксплуатации, и у каждого есть свои преимущества и недостатки.
На рисунке F.1 показано поперечное сечение двухслойного (дуплексного) никелированного изделия в качестве примера катодного покрытия. Коррозия возникает между двумя разнородными слоями никеля (блестящий никель и полублестящий никель), что заставляет коррозию распространяться в поперечном направлении. Использование двух слоев разнородного никеля помогает предотвратить гальваническую атаку между основной сталью и слоем покрытия.
Узнайте об APT
Видео компании APT
Подход APT к отделке металлов уникален, поскольку мы являемся не только компанией, занимающейся гальванопокрытием и порошковым покрытием, но и предоставляем нашим клиентам полный спектр услуг по инженерной обработке поверхностей. Дополнительные услуги, которые мы предлагаем, включают в себя: поддержку проектирования поверхностей, услуги инженерного проектирования/строительства, инженерные услуги полного качества и специальную группу обслуживания клиентов. Посмотрите видео о нашей компании, чтобы узнать больше!
Дополнительные услуги, которые мы предлагаем, включают в себя: поддержку проектирования поверхностей, услуги инженерного проектирования/строительства, инженерные услуги полного качества и специальную группу обслуживания клиентов. Посмотрите видео о нашей компании, чтобы узнать больше!
Преимущества порошковой окраски по сравнению с окраской мокрым распылением
Защита металлических компонентов имеет решающее значение для долговечности конечного продукта. Обработка поверхности с помощью порошкового покрытия или мокрой окраски является обычным решением для защиты различных компонентов. Как порошковое покрытие, так и системы влажной окраски содержат одинаковые смолы, добавки и пигменты; тем не менее, есть заметные различия между…
Подробнее >
Последние сообщения
- Преимущества порошковой окраски перед мокрой окраской распылением
- Как предотвратить коррозию позолоченных контактов или клемм
- В чем разница между золотыми и посеребренными разъемами или контактами?
- Преимущества золотого покрытия
- Обсуждение металлической отделки и охраны окружающей среды
Популярные сообщения в блогах
- Толщина позолоты разъемов
- Твердое золочение против мягкого золочения — что подходит для моего применения?
- Азотная пассивация против лимонной кислоты
- Серебряное покрытие меди или медных сплавов
- Серебряное покрытие нержавеющей стали и жаропрочных сплавов
Что такое коррозия и как ее предотвратить? — Судовые покрытия
Слово «коррозия» происходит от латинского «corrodere», что переводится как «грызть на куски».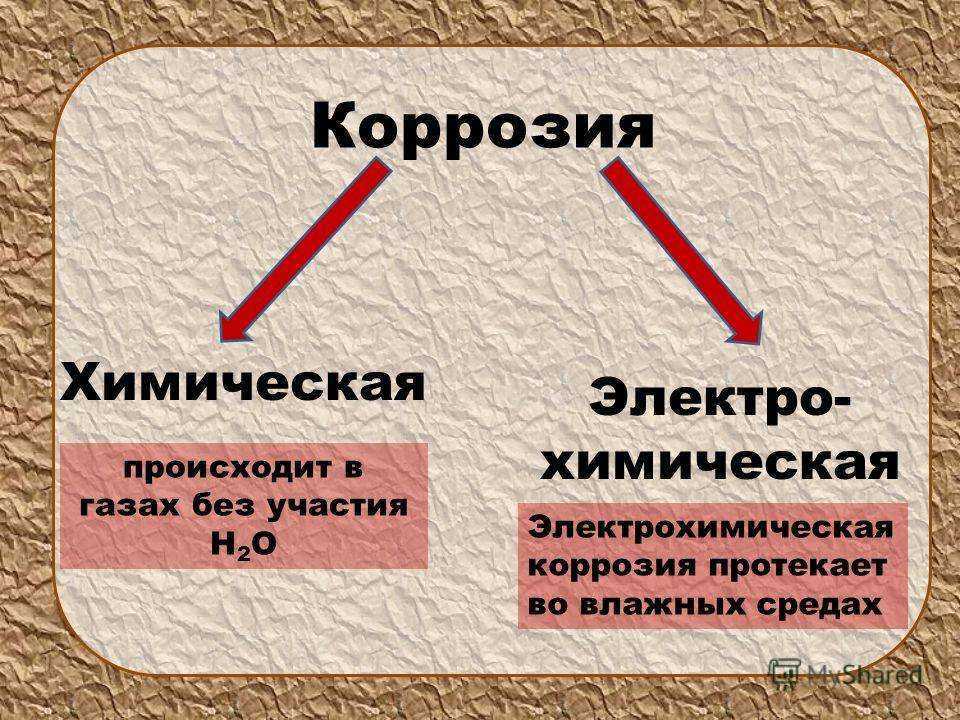 Для морских применений мягкая сталь остается металлом номер один для конструкционных целей, ее главный недостаток заключается в том, что она легко подвергается коррозии в морской воде. Предотвращение коррозии требует устранения или подавления с помощью катодной защиты и/или покрытий. Ремонт покрытия на море может стоить до 100 раз дороже первоначального покрытия, поэтому стоит сделать все правильно с первого раза.
Для морских применений мягкая сталь остается металлом номер один для конструкционных целей, ее главный недостаток заключается в том, что она легко подвергается коррозии в морской воде. Предотвращение коррозии требует устранения или подавления с помощью катодной защиты и/или покрытий. Ремонт покрытия на море может стоить до 100 раз дороже первоначального покрытия, поэтому стоит сделать все правильно с первого раза.
Что такое коррозия?
Коррозия — это естественный процесс, при котором материалы, обычно металлы, движутся к своему наинизшему возможному энергетическому состоянию, что приводит к спонтанной реакции между материалом и окружающей средой, что приводит к деградации этого материала. Слово происходит от латинского « corrodere» , что переводится как «грызть на куски».
Для морских применений мягкая сталь остается металлом номер один для конструкционных целей благодаря ее относительно низкой стоимости, механической прочности и простоте изготовления.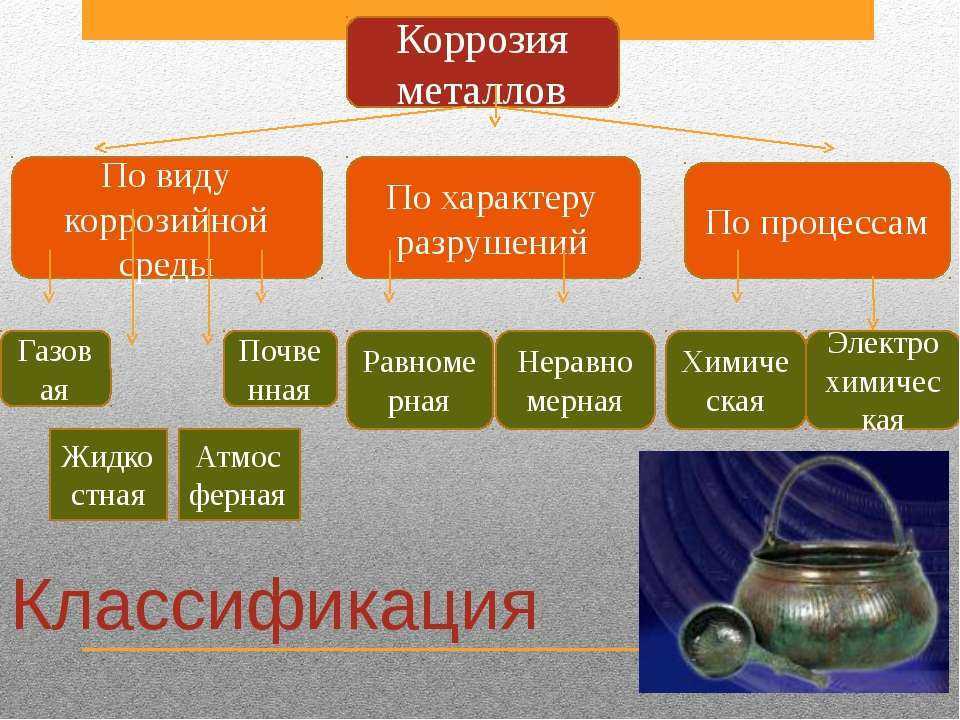 Его главный недостаток заключается в том, что он легко подвергается коррозии в морской воде и, если его не защитить должным образом, быстро теряет прочность, что может привести к разрушению конструкции. На приведенной ниже диаграмме показан цикл коррозии. От добычи оксида железа, производства стали до коррозии.
Его главный недостаток заключается в том, что он легко подвергается коррозии в морской воде и, если его не защитить должным образом, быстро теряет прочность, что может привести к разрушению конструкции. На приведенной ниже диаграмме показан цикл коррозии. От добычи оксида железа, производства стали до коррозии.
Изображение: ResearchGate
Ремонт морских покрытий может в 100 раз превышать стоимость первоначального покрытия, а по оценкам NACE International общая стоимость морской коррозии составляет от 50 до 80 долларов США. миллиардов каждый год. Источник: Морская промышленность. 2018. Морская промышленность. [ОНЛАЙН] Доступно по адресу: https://www.nace.org/Corrosion-Central/Industries/Maritime-Industry/ .
При правильном планировании судовладельцы могут гарантировать, что их суда работают с максимальной производительностью и сохраняют экономическую эффективность, сохраняя при этом состояние своих активов. Если причиной износа стала плохая подготовка поверхности, то единственное решение — удалить краску и начать заново. Стоит сделать это правильно с первого раза.
Если причиной износа стала плохая подготовка поверхности, то единственное решение — удалить краску и начать заново. Стоит сделать это правильно с первого раза.
Два типа коррозии, особенно актуальные для морской промышленности, — это точечная коррозия и бактериальная коррозия.
Как предотвратить коррозию
Для предотвращения коррозии необходимо устранить или подавить ее двумя основными методами: катодной защитой и покрытиями . Как правило, системы катодной защиты используются в сочетании с системами покрытий.
Катодная защита
Целью катодной защиты является подавление протекающей электрохимической реакции. В нормальных коррозионных условиях протекание тока от анода приводит к потере металла на анодном участке, что приводит к защите металла на катодном участке.
Защиту можно обеспечить, сделав структуру, которую вы хотите защитить, катодной, используя два метода:
- Защитные аноды:
Когда два разнородных металла погружаются в морскую воду, металл с наименьшим электрическим потенциалом подвергается наибольшей коррозии.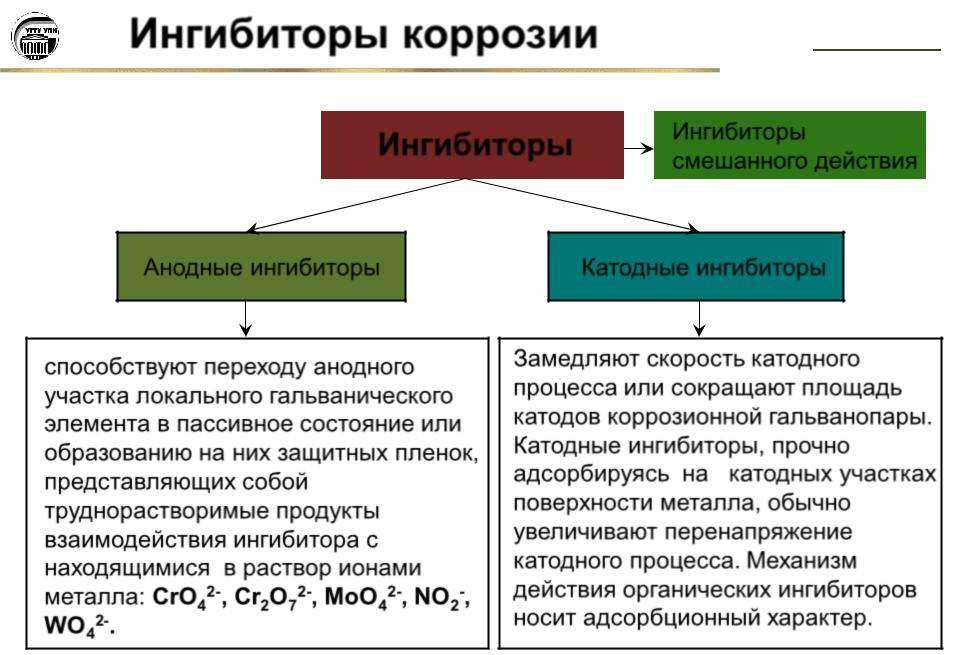 Например, скорость коррозии мягкой стали можно контролировать, соединив ее с цинком, поскольку в этом случае он станет анодом и будет подвергаться коррозии. В этом примере цинковый анод обозначается как расходуемый анод , потому что он медленно расходуется (корродирует) в процессе защиты.
Например, скорость коррозии мягкой стали можно контролировать, соединив ее с цинком, поскольку в этом случае он станет анодом и будет подвергаться коррозии. В этом примере цинковый анод обозначается как расходуемый анод , потому что он медленно расходуется (корродирует) в процессе защиты.
Еще одно применение цинка в качестве расходуемого анода — цинковое покрытие стали; либо в форме гальванизации или металлизации, либо в краске, которая содержит высокие уровни активного цинка.
- Системы токов под давлением:
Корпус судна можно сделать катодным с помощью источника постоянного тока. Приложенный ток применяется в противоположном направлении, чтобы нейтрализовать ток коррозии и преобразовать корродирующий металл из анода в катод. В этом примере отрицательный вывод постоянного тока подключен к защищаемому трубопроводу. Анод остается внутри, чтобы увеличить электрический контакт с окружающей средой.
Изображение: Основные принципы катодной защиты
Покрытия
рабочая среда.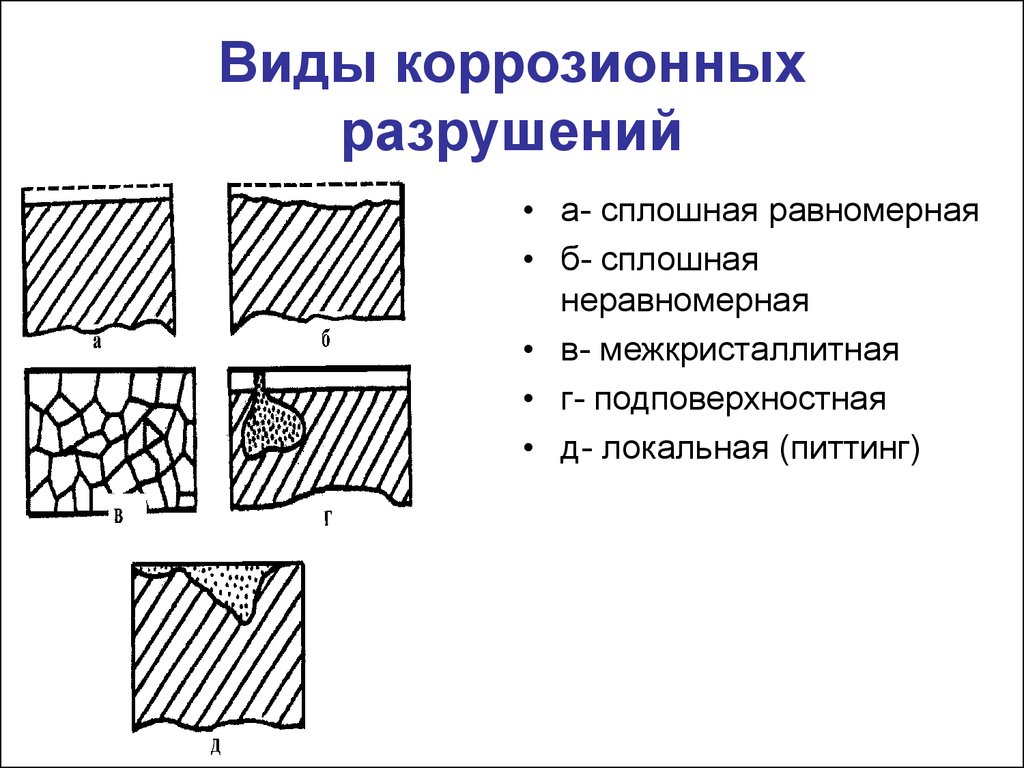
Низкая проницаемость и хорошая «мокрая адгезия», то есть адгезия при погружении, считаются наиболее важными аспектами защиты от коррозии с помощью покрытий.
- Адгезия
Для максимальной адгезии покрытий стальные поверхности перед окраской должны быть чистыми, сухими и свободными от масла, ржавчины, солей и других загрязнений.
- Проницаемость
Сильно сшитые, химически отверждаемые системы, вероятно, будут иметь относительно низкие характеристики проницаемости, и толщина пленки может повлиять на это. Как правило, более толстые пленки задерживают прохождение кислорода и воды к поверхности стали. Таким образом, пленка с большой толщиной (>400 мкм сухой пленки) может обеспечить высокую степень защиты от коррозии, которая лучше всего достигается в многослойных системах, а не в однослойном.
- Поврежденное покрытие s
Покрытия в процессе эксплуатации могут подвергаться механическим повреждениям.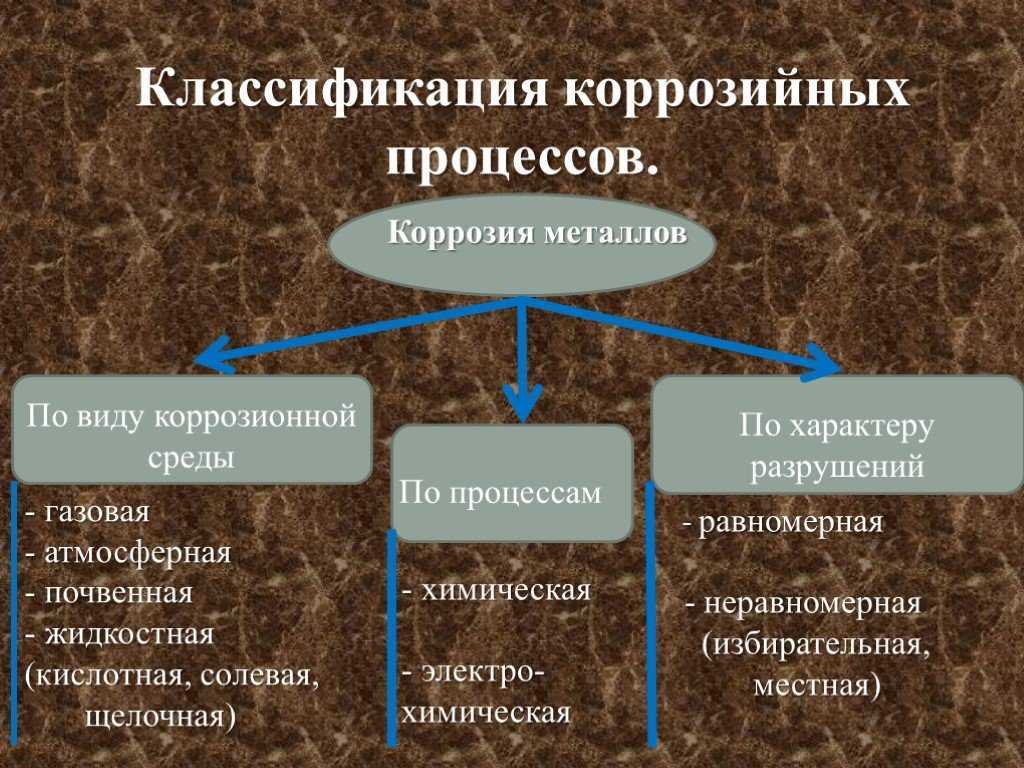 Таким образом, поддержание защиты от коррозии лучше всего достигается с помощью покрытий, которые обеспечивают как стойкость к истиранию, так и защиту от коррозии. Рекомендуется, чтобы покрытия имели хорошую стойкость к «подрезанию», т. е. стойкость к ползучести под пленочной коррозией на поврежденных участках.
Таким образом, поддержание защиты от коррозии лучше всего достигается с помощью покрытий, которые обеспечивают как стойкость к истиранию, так и защиту от коррозии. Рекомендуется, чтобы покрытия имели хорошую стойкость к «подрезанию», т. е. стойкость к ползучести под пленочной коррозией на поврежденных участках.
Другие механизмы, используемые для предотвращения коррозии в непогруженных надводных зонах, включают:
- Использование антикоррозионных пигментов, таких как фосфат цинка. Этот пигмент малорастворим и может образовывать молекулярный слой, препятствующий коррозии, на поверхности стали.
- Использование металлического цинка в качестве расходуемого пигмента, по сути, разработка системы катодной защиты «на месте».
Наш успех в предотвращении коррозии:
Многие клиенты AkzoNobel добились успеха в предотвращении коррозии с помощью Intershield 300. Подробнее:
- « Samco Raven» взлетает с Intershield 300 после 15 лет эксплуатации .

