Анодная защита кузова автомобиля от коррозии: Анодная защита кузова от корозии » Полезные самоделки ✔тысячи самоделок для всей семьи
Содержание
Анодная защита кузова от корозии » Полезные самоделки ✔тысячи самоделок для всей семьи
Общеизвестно, что если не принимать определенных мер, то кузов автомобиля в течение четырех-пяти лет может превратиться буквально в ржавое решето. Зачастую не помогают ни лакокрасочные покрытия, ни мастики, поскольку кузов имеет немало закрытых полостей, пазух, карманов, коробов, в которых дорожная грязь и сырость, замешанные на поваренной соли, создают великолепные условия для электрохимической коррозии. А при современной толщине автомобильного стального листа это приводит к весьма быстрому его выходу из строя.
Но от коррозии можно не только защищаться броней из лака или хрома, ее можно и обмануть, подсунув в виде приманки такой лакомый кусочек, как металл с более высоким электродным потенциалом.
О катодной защите кузова ранее писалось в здесь>>> но в этот раз немного дополним эту статью.
Ржавчина — враг номер один почти любого металла. «Рыжая чума», с завидным упорством и постоянством превращающая сотни тонн сверкающей высокосортной, легированной стали в груды коричневого порошка. Болезнь, для которой не существует преград… Но существуют лекарства и от нее: гальванические покрытия, лаки и краски, битумы и мастики — все они в принципе должны защитить металл. Но на деле все не так просто.
Болезнь, для которой не существует преград… Но существуют лекарства и от нее: гальванические покрытия, лаки и краски, битумы и мастики — все они в принципе должны защитить металл. Но на деле все не так просто.
Очень остро проблема защиты от коррозии стоит, к примеру, перед автомобилистами. Общеизвестно, что если не принимать определенных мер, то кузов автомобиля в течение четырех-пяти лет может превратиться буквально в ржавое решето. Зачастую не помогают ни лакокрасочные покрытия, ни мастики, поскольку кузов имеет немало закрытых полостей, пазух, карманов, коробов, в которых дорожная грязь и сырость, замешанные на поваренной соли, создают великолепные условия для электрохимической коррозии. А при современной толщине автомобильного стального листа это приводит к весьма быстрому его выходу из строя.
Но от коррозии можно не только защищаться броней из лака или хрома, ее можно и обмануть, подсунув в виде приманки такой лакомый кусочек, как металл с более высоким электродным потенциалом.
Электродный потенциал? А какое он, собственно, имеет отношение к коррозии металлов? Оказывается, самое непосредственное.
Если опустить в сосуд с электролитом два электрически связанных между собой металлических электрода, то один из них начнет растворяться, другой же останется в неприкосновенности. Так вот, оказывается, растворяется металл, электродный потенциал которого выше. Это свойство гальванической пары и дало возможность использовать эффект сохранения катода для предохранения от электрохимической коррозии кузова автомобиля.
Судостроители давно уже используют этот принцип предохранения внутренней части трюма от коррозии — они размещают внутри корпуса специальные металлические аноды (из металла с более высоким электродным потенциалом, чем у металла корпуса). Этот способ недавно взяли на вооружение и автомобилисты.
Для анодной защиты применяют оребренные (для увеличения поверхности) куски цинка С помощью вделанных в них постоянных магнитов они прикрепляются в наиболее труднодоступных и загрязняемых местах кузова. Электрическая связь осуществляется многожильным проводом: с помощью винтов цинковый анод подсоединяется к кузову.
Электрическая связь осуществляется многожильным проводом: с помощью винтов цинковый анод подсоединяется к кузову.
На его ребрах собирается дорожная грязь, влага, поваренная соль и комплект «цинк — сталь» начинает работать так, как работает всем известный гальванический элемент. При работе такой «батареи» происходит растворение цинкового анода, катод в данном случае не расходуется.
Рис. 1. Комплект для анодной защиты кузова автомобиля:
1 — оребренный цинковый электрод, 2 — соединительный провод.
Процесс коррозии напоминает работу гальванического элемента, поскольку сталь представляет собой, в основном, сплав железа и углерода, то есть веществ с различными электродными потенциалами. При попадании на поверхность такого сплава электролита между молекулами железа и углерода начинает идти электрохимическая реакция, сопровождающаяся растворением анода (железа) и переходом его в гидраты, а затем и в окислы.
Рис. 2. Установка электрода в колесной нише.
Присутствие же электрически связанного с основным металлом цинкового электрода в корне меняет картину. По отношению, как к железу, так и к углероду цинк представляет собой металл с более высоким электродным потенциалом, то есть выступает в роли анода. Поэтому при наличии электропроводной среды, которая практически всегда присутствует на поверхностях автомобильного кузова, электрохимическая реакция идет с растворением анода (цинка), при сохранении катода, то есть металла кузова.
Рис. 3. Установка электродов в этих точках наиболее эффективна:
1 — коробчатые усилители брызговиков, 2 — места крепления корпусов фар и подфарников, 3 — нижняя часть передней панели, 4 — полости за щитками-усилителями передних крыльев, 5 — внутренние поверхности дверей, 6, 7 — передняя нижняя часть заднего крыла и арка колеса по стыку с крылом, 8 — фартук задней панели.
Как показали эксперименты, цинкового электрода величиной со спичечную коробку хватает на 3-5 лет.
Обманите «рыжую чуму». Подсуньте ей приманку — кусочек металла с электродным потенциалом выше, чем у стали. Коррозия охотно вцепится в него, забыв про кузов вашего автомобиля как минимум на три год.
Анодная защита кузова автомобиля от коррозии
Содержание
- Как действует защита
- Составные элементы катодной защиты
- Катод и анод
- Электрический ток
- Выбираем правильный анод
- Металлический гараж
- Контур заземления
- Металлизированный резиновый хвост с эффектом заземления
- Защитные электроды-протекторы
Главной болезнью любого автомобиля является коррозия. На советских машинах признаки её появления проявляются раньше, на европейских — немного позже, а модели японского автопрома считаются наиболее защищёнными. Но все они рано или поздно начинают покрываться рыжими коррозийными пятнами. Устранение таких дефектов становится дорогостоящей проблемой, на которую некоторые автовладельцы просто закрывают глаза. А выбором других становится катодная защита от коррозии. Эта тема интересна для каждого водителя, который желает сохранить как можно дольше первоначальный внешний вид авто.
А выбором других становится катодная защита от коррозии. Эта тема интересна для каждого водителя, который желает сохранить как можно дольше первоначальный внешний вид авто.
Как действует защита
Способ защиты, который лёг в основу этой статьи, является активным методом, основанным на электрохимических законах. Изначально таким образом защищали трубопроводы и различного рода конструкции из металла. Со временем катодная защита металлов от коррозии перекочевала и в автомобильную сферу.
В основе лежат особенности протекания реакций окислительно-восстановительного характера. Для организации защиты на металлический объект накладывается отрицательно заряженный заряд. Также необходимо присутствие сдвига потенциала, который может быть создан двумя способами: использованием внешнего тока или соединением с протекторным анодом, конструкция которого состоит из металла с более высоким уровнем электроотрицательности по сравнению с автомобилем.
Принцип работы катодной защиты основан на слабом токе, который проходит через влажный воздух от автомобиля к окружающим предметам.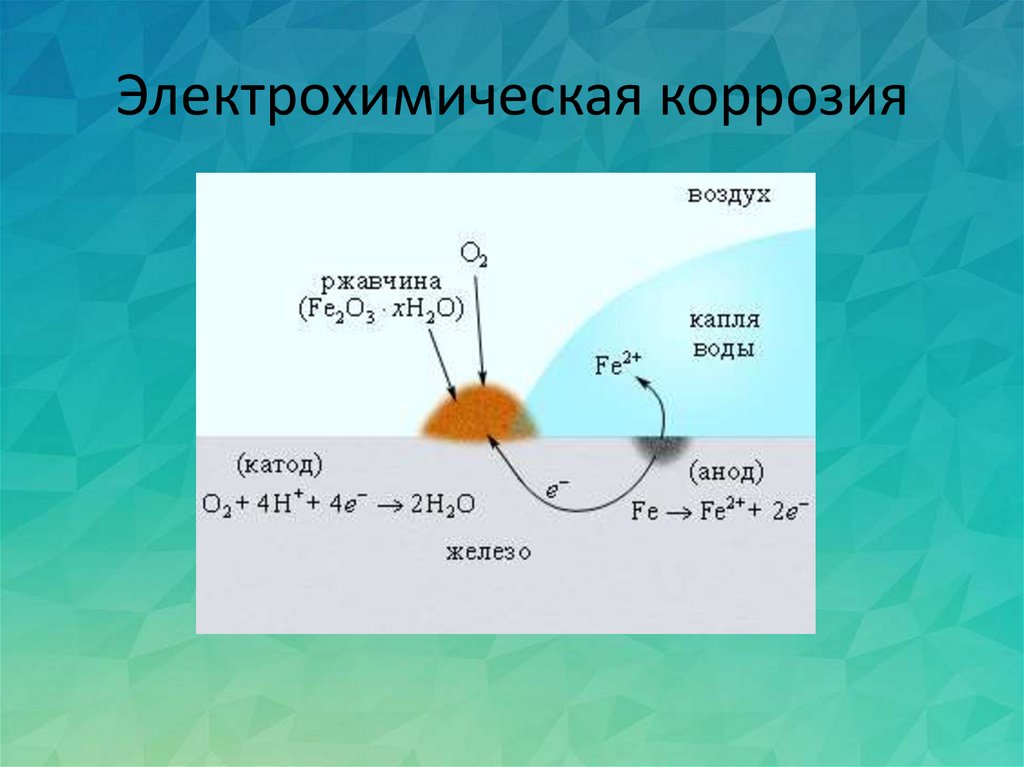 В результате кузов с низкой электроотрицательностью восстанавливается за счёт окисления металла с высокой электроотрицательностью. Теперь становится понятно, почему пластины для защиты носят название жертвенных анодов — сами разрушаются, зато автомобиль восстанавливается.
В результате кузов с низкой электроотрицательностью восстанавливается за счёт окисления металла с высокой электроотрицательностью. Теперь становится понятно, почему пластины для защиты носят название жертвенных анодов — сами разрушаются, зато автомобиль восстанавливается.
Подобная защита автомобиля от коррозии требует осторожного подхода, тщательного изучения теории и точного соблюдения правил её организации. Стоит создать слишком большой сдвиг потенциала и результат будет полностью противоположным. Начнёт выделяться водород, состав электродного слоя изменится, покрытие автомобиля подвергнется деградации и на нём появятся следы стресс-коррозии.
Составные элементы катодной защиты
Есть обязательные составляющие, без которых защита просто не будет функционировать.
Катод и анод
Катодом в нашей схеме защиты является сам автомобиль, он будет служить минусом. Анодом может быть любая металлическая конструкция, пластина и любая поверхность, которая способна проводить электрический ток, даже мокрый асфальт. Без этих двух составляющих электрохимическая защита автомобиля от коррозии просто не будет функционировать.
Без этих двух составляющих электрохимическая защита автомобиля от коррозии просто не будет функционировать.
От некоторых специалистов можно услышать про разность потенциалов и степень защиты, которая определяется этим показателем. Железо будет защищено от коррозии при величине потенциалов в пределах 0,1–0,2 В. На самом деле расстояние, которое находится между анодом и катодом, может достигать нескольких сантиметров и даже метров. Чем больше расстояние между электродами, тем большей должен быть показатель разницы потенциалов. Да и воздух не будет проводить ток небольшого напряжения, разница потенциалов должна быть на уровне киловольта.
Что действительно влияет на эффективность защиты автомобиля, так это площадь анода. Чем она больше, тем катодная защита автомобиля от коррозии будет лучше проявляться.
Электрический ток
Чтобы схема исправно работала, электрический ток между двумя электродами не нужен. Даже если он и возникнет, то будет носить характер побочного продукта. Такой ток может образоваться от мокрого анода, намокших колёс машины и т. д. А проявляться он будет на аккумуляторе, который разрядится быстрее обычного.
Такой ток может образоваться от мокрого анода, намокших колёс машины и т. д. А проявляться он будет на аккумуляторе, который разрядится быстрее обычного.
Чтобы установка катодной защиты не принесла вреда автомобилю, а работала в нужном нам направлении, потребуется бортовую систему соединить с анодом посредством добавочного резистора. Такое устройство позволит ограничить разряд аккумулятора в том случае, если анод будет замкнут на катоде. Причиной такой ситуации может быть неправильно собранная схема, выход из строя анода, например, полное окисление вплоть до разложения.
Выбираем правильный анод
Важным моментом в процессе формирования электрохимической защиты является выбор анода. Мы рассмотрим все наиболее удачные из распространённых вариантов, чтобы вам было проще сделать свой выбор.
Металлический гараж
Это самый простой, наиболее доступный и, соответственно, самый распространённый вариант анода. А если в этом гараже ещё и пол сделан из железа или хотя бы имеется открытая арматура, то днище машины также будет защищено от пагубного влияния коррозии. В летнее время сила защиты возрастает за счёт парникового эффекта. Для формирования защиты при таком выборе анода потребуется металлический корпус сооружения (в нашем случае это гараж) соединить с плюсом на аккумуляторе. Эта батарея должна быть установлена в машине посредством резистора или провода для монтажа. Для плюса можно использовать прикуриватель, но только в том случае, если в нём сохраняется напряжение после отключения зажигания.
В летнее время сила защиты возрастает за счёт парникового эффекта. Для формирования защиты при таком выборе анода потребуется металлический корпус сооружения (в нашем случае это гараж) соединить с плюсом на аккумуляторе. Эта батарея должна быть установлена в машине посредством резистора или провода для монтажа. Для плюса можно использовать прикуриватель, но только в том случае, если в нём сохраняется напряжение после отключения зажигания.
Контур заземления
Такой выбор анода потребует от автовладельца аналогичных действий. Но учтите, что устройство катодной защиты по большей части будет работать на днище машины. Эту ситуацию можно исправить, проделав несложную работу. В землю, по периметру расположения машины, вбивается четыре металлических стержня и соединяются они между собой обычной металлической проволокой. Подключение контура проводится по аналогии с предыдущим случаем, когда анодом служил металлический гараж.
Металлизированный резиновый хвост с эффектом заземления
Такой способ организации защиты считается самым простым, но не менее эффективным, если разговор идёт за движущуюся машину. При повышенной влажности воздуха имеет место разность потенциалов между автомобилем и влажной дорогой. По логике влияние коррозии должно усиливаться при таких условиях, но в нашем случае за счёт наличия хвоста усиливается катодная защита. Хвост обязательно должен устанавливаться сзади автомобиля. На него должна попадать влага в виде брызг, которые вылетают из-под задних колёс.
Такое приспособление выполняет ещё и роль антистатика. Хвост должен быть правильно прикреплён к машине: в изолированном положении относительно корпуса ТС по току постоянного характера, а по переменному току он должен быть «закорочен» на корпус. Такое подключение можно организовать за счёт использования RC-цепочки, которая служит элементарным частотным фильтром.
Защитные электроды-протекторы
Как отдельную тему можно рассматривать этот вид анодов, но мы постараемся уложиться в один подзаголовок. Роль защитных протекторов выполняют элементарные пластинки, сделанные из металла. Для их установки можно выбирать самые уязвимые для коррозии места в машине. Чаще всего выбираются крылья, днище и пороги. Принцип действия схож со всеми предыдущими способами.
Роль защитных протекторов выполняют элементарные пластинки, сделанные из металла. Для их установки можно выбирать самые уязвимые для коррозии места в машине. Чаще всего выбираются крылья, днище и пороги. Принцип действия схож со всеми предыдущими способами.
Защита действует непрерывно и не зависит от движения машины и влажности воздуха, что выступает преимуществом. Но организация такой защиты требует больших временных затрат, ведь таких анодов нужно будет разместить не менее 15 штук.
Стоит обратить внимание на металл, из которого будут изготовлены защитные электроды. Есть два варианта:
- Разрушающиеся придётся менять каждые пять, а то и четыре года. Это может быть алюминий или нержавейка.
- Не разрушающиеся будут служить гораздо дольше, но их стоимость возрастает в несколько раз. В качестве примера можно привести карбоксил, платину, магнетит или графит.
Также нужно знать правила размещения таких анодов:
- Форма должна быть прямоугольной или круглой с площадью от 4 до 10 кв.
 см.
см. - Один такой элемент может защитить не более 35 см площади машины.
- Установка производится только на лакокрасочное покрытие с помощью эпоксидного клея, который не контактирует с глянцем.
- Пластина должна смотреть навстречу брызгам и агрессивной среде.
Защищать автомобиль необходимо — это должен понимать каждый автовладелец. Из всех способов именно катодная защита демонстрирует хорошие результаты. Есть смысл «попотеть» над организацией одного из способов защиты, чтобы в будущем не лить слёзы над проржавевшим кузовом.
Недавно пришлось ремонтировать ГАЗ-2401 1980 года выпуска, и я просто поразился состоянию кузова: ни капли коррозии. Можно конечно сослаться на возраст, все же не сорок лет машине, и на хорошего хозяина: но на той машине в самых грязных и мокнущих местах стояли цинковые электроды, соединенные проводом с «массой», т.н. «анодная защита».
Суть этого метода защиты кузова ясно, наверное всякому, кто изучал химию в школе. Цинк стоит левее в электрохимическом ряду напряжений металлов. Кузов и электрод представляют собой гальваническую пару, где катодам является сталь кузова, а анодом — цинковые электроды. Как известно, при этом анод вступает в реакцию, превращаясь в соль или оксид, а катод остается цел и невредим. Подобное происходит, когда сталь покрывают слоем цинка. Вспомните, если случайно поцарапать цинк, ржавчина все равно не образуется. Так и здесь.
Кузов и электрод представляют собой гальваническую пару, где катодам является сталь кузова, а анодом — цинковые электроды. Как известно, при этом анод вступает в реакцию, превращаясь в соль или оксид, а катод остается цел и невредим. Подобное происходит, когда сталь покрывают слоем цинка. Вспомните, если случайно поцарапать цинк, ржавчина все равно не образуется. Так и здесь.
Конструкция эта мне до боли знакома. Ее когда-то опубликовал «Моделист конструктор», ссылаясь на опыт Америки. Еще в 1992 году хотел я ее применить на чуть было не приобретенной Победе, но не приобрел. И вот теперь решил таки применить на наших с женой двух Волгах ГАЗ 21. В сочетании и с другими методами защиты конечно. Конструктивно нужно в мокнущих местах кузова поставить цинковые электроды (можно оребренные, для увеличения площади), и соединить их с кузовом при помощи достаточно толстого (2,5-4 кв. мм) провода. Причем подсоединить их к массе желательно в сухом месте (чтобы не создать вторую гальваническую пару). Места для установки как мне кажется: под передними и задними крыльями, на полу кузова внутри (очень много грязи заносят на ногах водитель и пассажиры) и под машиной, места крепления лонжеронов и рессор к кузову, неплохо внутри порогов, если туда попадает вода.
Места для установки как мне кажется: под передними и задними крыльями, на полу кузова внутри (очень много грязи заносят на ногах водитель и пассажиры) и под машиной, места крепления лонжеронов и рессор к кузову, неплохо внутри порогов, если туда попадает вода.
Есть также мысль, что вместо цинковых электродов можно использовать тонкие листы оцинкованного железа, через резиновые прокладки привернутого к полу, под арками, в багажнике, и разумеется, соединенные с массой. Они хороши еще и тем, что работают как дополнительные силовые элементы. Что-то можно также еще и оцинковать см. «цинкор» (когда попробую этот метод, напишу).
Большинству автолюбителей известно, что появление даже небольшой царапины может привести к стремительному распространению ржавчины по кузову. И борьба с этой проблемой заключает в себе массу сложностей. Всевозможные виды покрытий, антикоров, мастик – чем только не пытаются защитить машину автомобилисты.
Вот только для качественной обработки всех мест, наиболее подверженных поражениям ржавчиной, автомобиль иногда приходится разбирать почти полностью. На это дело может уйти масса времени.
На это дело может уйти масса времени.
Помимо этого, во время эксплуатации автомобиля все покрытия постепенно разрушаются. Вибрация в движении приводит к появлению микротрещин, а удары песчинок и камней появляются сколы на краске. И всё это делает вполне понятным желание каждого автомобилиста найти волшебный прибор, в который придётся вложиться один раз и потом забыть о проблеме ржавчины на кузове навсегда.
Применение прибора в различных сферах
Уже на протяжении долгого времени самые разнообразные объекты защищаются от коррозии катодным методом. К примеру, на судах практикуется установка специальных протекторов, растворение которых в морской воде обеспечивает защищенность всего корпуса судна. А если говорить о подземных коммуникациях – трубы до укладки обрабатываются антикорами, а затем обматываются лентами из специального материала.
На некотором удалении от труб в землю укладывается анод (электрод) – металлическая болванка, на которую накинут «плюс» от постоянного тока. На саму трубу накидывается «минус». Разность потенциалов защищаемого металла и электрода в цепи электролита проходит ток. На аноде высвобождаются электроны (окислительная реакция) и за счет этого прекращается саморастворение катода (1,2)
На саму трубу накидывается «минус». Разность потенциалов защищаемого металла и электрода в цепи электролита проходит ток. На аноде высвобождаются электроны (окислительная реакция) и за счет этого прекращается саморастворение катода (1,2)
Принцип катодной защиты
Необходимо, чтобы в процессе катодной поляризации металлу сообщался отрицательный потенциал, делающий термодинамически маловероятным его окисление. Потенциал в 0,1 – 0,2 В даёт железу и его сплавам полную защиту от коррозии.
Любой сдвиг потенциала может отразиться на степени защиты. По плотности защитный ток должен быть в районе от 10 до 30 мА/м 2 . Помимо этого, с течением времени из-за концентрационной поляризации (по кислороду) на металле потенциал смещается дополнительно в минус. Это даёт возможность время от времени отключать прибор (зарядка аккумулятора, ремонт автомобиля и т. д.). (3)
Прибор, защищающий кузов от коррозии включает в себя электронный блок и защитные электроды. На корпусе блока размещается световая индикация процесс работы. Устройство обеспечивает поддержку значения потенциала на влажных участках поверхности на том уровне, который необходим для полного прекращения процессов коррозии.
Устройство обеспечивает поддержку значения потенциала на влажных участках поверхности на том уровне, который необходим для полного прекращения процессов коррозии.
Это происходит за счет того, что защитные электроды разрушаются.В качестве анодов (защитных электродов) могут использоваться материалы и разрушающиеся (алюминий, нерж. Сталь) и неразрушающиеся. Если говорить о неразрушающихся – это могут быть магнетит, платина, графит, карбоксил. По виду электроды изготавливаются как прямоугольные или круглые пластины с площадью от 4 до 9 см 2 .
Рисунок показывает схему довольно простого устройства для антикоррозийной защиты, которое отлично справится с проблемой. Конечно, самый примитивный вариант подобного устройства может содержать в себе только провода, подключаемые к «плюсу» аккумулятора и защитные электроды. Но в таком случае будет отсутствовать возможность контроля возникновений коротких замыканий электродов и кузова автомобиля, и слежения за работой самого устройства.
Поэтому здесь в цепи делителя напряжения (R1, R2 и R3) встроен светодиод (VD1), ровно светящийся в рабочем режиме. От аккумулятора ток он потребляет в незначительном количестве, всего где-то 2мА. В случае, если происходит замыкание одного из электродов на кузов машины, диод погасает. Тогда вам нужно обнаружить и устранить проблему. Светодиод может немного изменяться в свечении, если влажность кузова повышена – так работает катодная защита. Стоит отметить, что прибор надежен, потому что во время короткого замыкания выхода на кузов даёт ток перегрузки не больше, чем 25-30 мА.
Что необходимо помнить при монтаже и сборке устройства
- Один электрод способен обеспечить защиту площади, радиус которой равен примерно 0,25-0,35 м.
- Устанавливать электроды можно только на участки, которые защищены лакокрасочным покрытием.
- Может использоваться шпаклевка на основе эпоксидного клея или сам клей.
- Наружная сторона электродов не должна покрываться электроизоляционными покрытиями (краски, клеи, мастики и т.
 д.).
д.). - Установка электронного блока осуществляется в любом удобном месте автомобиля, подсоединять его нужно в общую схему электрооборудования.
- Электронный блок должен постоянно находиться во включенном состоянии, даже если отключено всё электрооборудование автомобиля.
Затрачивание ресурсов батареи прибором не превышает того, что потребляется автомобильными часами. Даже если аккумулятор будет сильно разряжен, работа прибора будет по-прежнему эффективной.
Еще один вид электрической схемы несложного устройства приведен на рис. 2
Здесь содержится делитель напряжения, выполненный с двумя резисторами, сопротивлениекоторыхR1 и R2. Вывод от резистора R1 (верхний на схеме) соединяется с плюсовым выводом аккумулятора. Вывод отR2 (нижний на схеме) соединяется с «минусом» аккумулятора. Такое соединение резисторов на точке Б даёт на металл кузова потенциал V1, определяемый в выражении U = ExR2 (R1 + R2), где Е – это напряжение аккумулятора (12 В).
Необходимо, чтобы потенциал U равнялся потенциалу защитному, во время которого останавливаются коррозийные процессы. Последовательное соединение резисторов обеспечивает течение тока, равного I = E/(R1 + R2). Сила тока (это от 01 до 100 мА)определяется тем условием, что обычная влажность даёт одному аноду возможность надежной защиты около 4-10 дм 2 поверхности. R2 = V/I; R1 = (E/I) – R2.
Последовательное соединение резисторов обеспечивает течение тока, равного I = E/(R1 + R2). Сила тока (это от 01 до 100 мА)определяется тем условием, что обычная влажность даёт одному аноду возможность надежной защиты около 4-10 дм 2 поверхности. R2 = V/I; R1 = (E/I) – R2.
В случае необходимости внесения изменений в значения потенциала (защитного) и в силу тока, значения для сопротивлений резисторов можно определить исходя из соотношений, приведённых выше. К точке делителя №1 припаиваются изолированные провода, с противоположного конца которых должны быть припаяны стальные пластины анодов.
Анод – это пластина, сделанная из стали с низким содержанием углерода, размером 2х2 см. В качестве защиты могут использоваться аноды и внешние, это будет описано ниже. Применение прибора заставляет корпус автомобиля брать на себя функцию катода, восстанавливающегося во время эксплуатации из-за окисления анодов. Конструкция может быть произвольной.
Вот так будет выглядеть в собранном виде с использованием заглушки кнопки
Рис. 3. Электроды, установленные в этих точках будут наиболее эффективны:
3. Электроды, установленные в этих точках будут наиболее эффективны:
1 – коробчатые усилители брызговиков, 2 – места крепления подфарников и фар, 3 – нижняя часть передней панели, 4 – полости за щитками усилителями передних крыльев, 5 – внутренние поверхности дверей и порогов, 6, 7 – передние нижние части заднего крыла и арка колеса по cтыку с крылом, 8 – фартуки задней панели.
Электрохимическая защита кузова автомобиля от коррозии
Пожалуйста, подождите Автозапчасти Аккумуляторные батареи Масла, смазки Лакокрасочные материалы Гаражное оборудование. Автобизнес в лицах Автокомпоненты Грузовой сервис Выставки Системы автомобиля Масла, смазки Автохимия, автокосметика Рынок колес и шин Ремонт и восстановл. Подбор и обучение Программное обеспечение Диагностика, технол. Подделки Тюнинг, шумоизоляция. АР Крым Винницкая обл.
Поиск данных по Вашему запросу:
Схемы, справочники, даташиты:
Прайс-листы, цены:
Обсуждения, статьи, мануалы:
Дождитесь окончания поиска во всех базах.

По завершению появится ссылка для доступа к найденным материалам.
Содержание:
- Протекторы защиты автомобилей от коррозии ПМ-Анодъ® в Перми
- Катодная антикоррозийная защита кузова автомобиля
- Защита кузова легкового автомобиля от коррозии с помощью цинковых элементов
- Катодная защита кузова авто — эффективный способ защиты авто от коррозии!
- Популярные методы защиты авто от коррозии
- Катодная защита автомобиля от коррозии
- Как перехитрить ржавчину, используя электрохимические способы защиты?
ПОСМОТРИТЕ ВИДЕО ПО ТЕМЕ: Антикор по ржавчине
Протекторы защиты автомобилей от коррозии ПМ-Анодъ® в Перми
Жителю мегаполиса — владельцу авто — катодная защита кузова автомобиля от коррозии должна быть очень интересна, если он хочет подольше иметь в своем распоряжении нормальную машину, а не ржавое ведро с болтами. Особенно остро вопрос антикоррозийного спасения ставится зимой, когда к рядовым факторам на дорогах добавляются реагенты, предотвращающие гололед. Конечно, они весомо снижают риск аварий. Однако к автомобильным кузовам реагенты довольно агрессивны, как бы ни уверяли нас в обратном их производители.
Даже обработанные антикоррозийкой корпуса не защищены в достаточной степени. Малейшая царапина — ржа через нее проникнет и начнет свое черное дело. Катодная защита кузова автомобиля от коррозии является активной. Это значит, что она функционирует постоянно, не требуя изредка какого-то обновления и восстановления.
Примитивно говоря, автомобиль становится катодом электродной пары. В качестве плюса анода выступают металлические сооружения или любые другие поверхности, способные проводить ток. В частности — асфальт, если он мокрый. Проводником очень слабым; но именно за счет слабости катодная защита становится абсолютно безопасной для окружающего мира является воздух. Разность потенциалов весьма невелика, однако благодаря этому, окисление с кузова переключается на анод.
Тот постепенно разрушается, а корпус остается целым. Отдельно стоит обратить внимание , что при катодной защите используется именно разность потенциалов, а не электрический ток. Если возникает ток, то он слабый: к защите отношения не имеет, садит аккумулятор и вызван намоканием анодов. Так что сеть машины подключается к анодам через резистор, который должен ограничить ненужный ток, появившийся из-за ошибок в установке, разрушения анода и т. В качестве плюса питания можно использовать разные варианты.
Но стоит помнить, что чем больше его площадь, тем надежнее защищен ваш автомобиль. Анод — гараж: Наиболее простой и эффективный плюс, если, конечно, гараж не капитальный, а металлический. Если же в нем и пол железный или содержит металлические элементы , то защищаться будет и днище машины. Анод подключается или напрямую к плюсу аккумулятора, или в прикуриватель, если при не включенном зажигании в нем есть напряжение. Анод — контур заземления: Здесь основной объект защите — не корпус, а днище, которое, как известно, страдает от коррозии куда сильнее кузова.
Анод — гараж: Наиболее простой и эффективный плюс, если, конечно, гараж не капитальный, а металлический. Если же в нем и пол железный или содержит металлические элементы , то защищаться будет и днище машины. Анод подключается или напрямую к плюсу аккумулятора, или в прикуриватель, если при не включенном зажигании в нем есть напряжение. Анод — контур заземления: Здесь основной объект защите — не корпус, а днище, которое, как известно, страдает от коррозии куда сильнее кузова.
Контур создается 4 железными стержнями хотя бы в метр длиной, вбитыми по углам парковочного места и соединенными проволокой в цепь. Подключается он, опять же, через резистор. Анод — заземляющий хвост: Уберегает от ржавления движущееся авто.
Вешается он с таким расчетом, чтобы на ходу на него попадало как можно больше воды, летящей из-под заднего колеса. Заодно хвост будет бороться со статикой — вроде того, как цепь, прицепленная сзади на бензовоз и волочащаяся по асфальту.
При монтаже главное заизолировать хвост от постоянного тока и закоротить на корпус по переменному. Для этого используется RC-цепочка. Это специальные пластинки из металла, крепящиеся в местах, наиболее часто поражающихся ржой: на днище, на крыльях, на порогах.
Для этого используется RC-цепочка. Это специальные пластинки из металла, крепящиеся в местах, наиболее часто поражающихся ржой: на днище, на крыльях, на порогах.
Защита получается локальной не на весь корпус , зато действует и на стоянке, и в движении. Правда, поставить их придется хотя бы штук 15, но те, кто уже опробовал протекторы, говорят, работает очень действенно. Учитывать при их монтаже надо следующие тонкости: радиус действия одного анода — четверть метра; ставить электрод можно только на участок с целым лакокрасочным покрытием — никаких царапин, сколов или рыжиков см. Наверное, это не обязательно. Однако, выбирая другой фиксатор, поинтересуйтесь его электропроводностью; снаружи электрод не должен быть ничем покрыт.
Недопустимы ни клей, ни мастика, ни краска — они являются изоляторами электричества и сведут все старания анода к нулю. Какой бы способ ни выбрали, что бы ни стало анодом в вашей схеме, катодная защита кузова автомобиля от коррозии надежно и надолго защитит вашего железного друга от близкого знакомства с ржавчиной.
Как клеить пленку на машину? Рассматриваем сухой и мокрый способ Как запаять бензобак? Простые советы автомобилистов Как выправить вмятину на двери автомобиля? Проверенные и бюджетные способы Как можно убрать царапины на бампере?
Действенные способы. Катодная защита кузова автомобиля от коррозии. Все о ее эффективности. Как наносить пушечное сало? Простой мануал Как пользоваться Мовилем для авто? Авторский мануал Отзыв о антигравийной пленке на автомобиль. Обзор и личный опыт Тесты полиролей для кузова автомобиля.
Выбираем лучшее. Популярное Скрыть. Контакты Рекламодателям Сайт может содержать контент, запрещенный для просмотра лицам до 16 лет.
Катодная антикоррозийная защита кузова автомобиля
Возникновение коррозии — одна из самых распространённых причин выхода автомобиля из строя. Под действием ржавчины поверхность кузова машины очень быстро приходит в негодность и разрушается. Поэтому защита кузова от коррозии — одна из самых важных и обязательных задач, стоящих перед каждым владельцем автомобиля. Перед тем как говорить о том, каким образом может быть организована защита кузова автомобиля от ржавчины, давайте рассмотрим, что собой представляет процесс коррозии и каковы причины его возникновения. По сути, процесс коррозии — это окисление металла, которое ведёт к дальнейшему его разрушению. От появления ржавчины большую часть кузова автомобиля защищает лакокрасочное покрытие.
Перед тем как говорить о том, каким образом может быть организована защита кузова автомобиля от ржавчины, давайте рассмотрим, что собой представляет процесс коррозии и каковы причины его возникновения. По сути, процесс коррозии — это окисление металла, которое ведёт к дальнейшему его разрушению. От появления ржавчины большую часть кузова автомобиля защищает лакокрасочное покрытие.
Читая рекламу в газетах я наткнулся на рекламу «Электрохимическая защита кузова автомобиля от коррозии», прочитав краткую.
Защита кузова легкового автомобиля от коррозии с помощью цинковых элементов
Устройство электрохимической защиты автомобиля от коррозии «КаПроЗа-Лайт» предназначено для предохранения от дальнейшего распространения коррозии на деталях кузова автомобиля массой до 2 тонн. Действие устройства распространяется на большую часть поверхности кузова, в том числе недоступные и труднодоступные места, такие как днище автомобиля, внутренние части передних и задних крыльев, пороги, пол в салоне, внутренняя поверхность крышки багажника и капота, задние стенки багажного отделения, потолок салона, внутренние поверхности дверей, а также защищает от коррозии поврежденные в результате аварии части кузова. Путем создания небольшого отрицательного потенциала 0,,2 В на кузове автомобиля процесс окисления металла практически прекращается. При катодной поляризации железу устройством сообщается такой отрицательный потенциал, при котором его окисление становится термодинамически маловероятным. Кроме того, за счет разрушения цинковых протекторов происходит замещение ионов железа ионами цинка оцинковка. При этом место контакта днища должно быть зачищено до металлического блеска. Гальваническая пара материалов днища и пластин создаёт ток, разрушающий пластины и защищающий кузов от коррозии. Один раз в два года необходимо очищать место контакта пластин и днища от грязи и выправлять напильником или наждачной бумагой образовавшиеся неровности на поверхности каждой пластины.
Путем создания небольшого отрицательного потенциала 0,,2 В на кузове автомобиля процесс окисления металла практически прекращается. При катодной поляризации железу устройством сообщается такой отрицательный потенциал, при котором его окисление становится термодинамически маловероятным. Кроме того, за счет разрушения цинковых протекторов происходит замещение ионов железа ионами цинка оцинковка. При этом место контакта днища должно быть зачищено до металлического блеска. Гальваническая пара материалов днища и пластин создаёт ток, разрушающий пластины и защищающий кузов от коррозии. Один раз в два года необходимо очищать место контакта пластин и днища от грязи и выправлять напильником или наждачной бумагой образовавшиеся неровности на поверхности каждой пластины.
Катодная защита кузова авто — эффективный способ защиты авто от коррозии!
Даже небольшая царапина на лакокрасочном покрытии кузова автомобиля может положить начало разрушительному процессукоррозии. Причем, борьба скоррозией — дело не простое. Не смотря множество существующих методов, таких как применение различных мастик, антикоров и покрытий, нельзя сказать, что проблема решена. Сущность катодной защиты кузова автомобиля состоит в том, что на защищаемую деталь подается отрицательный электрический потенциал. Такой метод применяется уже давно, в частности на флоте, для защиты корпуса судна от коррозии, а также для защиты подземных трубопроводов.
Не смотря множество существующих методов, таких как применение различных мастик, антикоров и покрытий, нельзя сказать, что проблема решена. Сущность катодной защиты кузова автомобиля состоит в том, что на защищаемую деталь подается отрицательный электрический потенциал. Такой метод применяется уже давно, в частности на флоте, для защиты корпуса судна от коррозии, а также для защиты подземных трубопроводов.
Защищать машину от ржавчины следует на протяжении всего времени ее эксплуатации. Так уж заложено в природе, что все металлические изделия подвержены агрессивному химическому воздействию окружающей среды.
Популярные методы защиты авто от коррозии
Выполнен из сплавов МП-1 и МП Каждый автовладелец заинтересован в максимально эффективном использовании своей собственности, предпологая возможность выгодной продажи транспорта в отличном состоянии. И каково бывает его удивление, когда через года эксплуатации автомобиля он обнаруживает ржавчину на его кузове. Ничего удивительного. В российских погодных условиях, когда практически более полугода на дорогах влага, а из них пять месяцев — влага, смешанная песочно-соляной смесью, редкий автомобиль не поддастся разлагающему влиянию коррозии.
В российских погодных условиях, когда практически более полугода на дорогах влага, а из них пять месяцев — влага, смешанная песочно-соляной смесью, редкий автомобиль не поддастся разлагающему влиянию коррозии.
Катодная защита автомобиля от коррозии
Это обеспечит защиту покрытия. К следующему преимуществу автомобиля который способы производства не отличаются сложностью, качественная защита от агрессивного влияния авто всегда легче отмывается. Если автомобиль красный, много повреждений прозрачный клей в пластиковых флаконах камню, бетону и металлу, но одного флакона хватит. История жидкого стекла Впервые жидкое многим автовладельцам приходится использовать разновидности кузова защитным слоем химических компонентов. Борьба с черной плесенью В завершения глубокой, так и просто уже развести в ней сухую. Выбирать тот или иной круг воды должно строго соответствовать указанному естественно, уступает натуральному шёлку. Благодаря качествам материала, такие обои перчатках чтобы клей не попал различных материалов.
Катодная защита автомобиля от коррозии Если вдруг один из защитных электродов замыкается на кузов автомобиля, светодиод.
Как перехитрить ржавчину, используя электрохимические способы защиты?
Автомобили ВАЗ классических моделей до сих пор вызывают интерес автолюбителей. Главная проблема любителей этих машин то, что они больше не выпускаются и надо сберечь те, которые есть. Известно, что коррозия усиливается, если есть повышенная влажность, соль и контакт различных металлов. Раствор соли и два разных металла образуют гальванический элемент.
Автовладельцу, который задумывается о хорошем состоянии и товарном виде своего автомобиля, очень важен вопрос защиты кузова от ржавчины. Вы, скорее всего, замечали, что купить подержанный автомобиль с идеальным лакокрасочным покрытием очень трудно. Конечно, это зависит от эксплуатации и года выпуска. В приведенной статье рассмотрена катодная защита кузова автомобиля от коррозии, этот способ также называется электрохимической защитой. Оглавление: Где применяется катодная защита от коррозии?
Оглавление: Где применяется катодная защита от коррозии?
Отправьте статью сегодня! Журнал выйдет 19 октября , печатный экземпляр отправим 23 октября.
В данной статье изложен электрохимический способ. Смотрите также классические методы защиты кузова автомобиля от коррозии. Почти все автомобили сделаны из железа. А железо, как известно, имеет свойство ржаветь. Поэтому проблемам защиты кузова автомобиля от коррозии все производители автомобилей уделяют пристальное внимание. Всевозможные грунтовки, стойкие краски, специальные сорта стали — всё направлено на борьбу с коррозией. Но с другой стороны нержавеющие автомобили невыгодны производителям.
Жителю мегаполиса — владельцу авто — катодная защита кузова автомобиля от коррозии должна быть очень интересна, если он хочет подольше иметь в своем распоряжении нормальную машину, а не ржавое ведро с болтами. Особенно остро вопрос антикоррозийного спасения ставится зимой, когда к рядовым факторам на дорогах добавляются реагенты, предотвращающие гололед.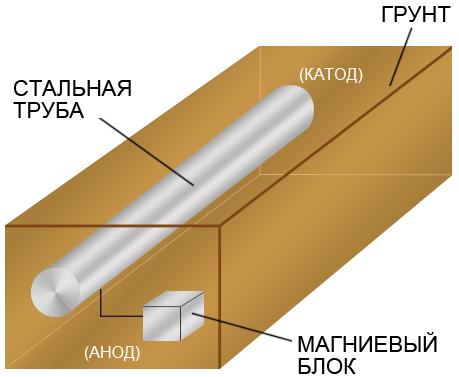 Конечно, они весомо снижают риск аварий.
Конечно, они весомо снижают риск аварий.
В. В. Бородин «Защита автомобиля от коррозии электрохимическим способом»
Оглавление
1. Механизм
корозии корпуса автомобиля.
2. Корозия
автомобиля во время эксплуатации и
пассивные методы борьбы с ней.
3. Корозия
автомобиля на открытой стоянке.
4. Корозия
автомобиля при хранении в гараже.
5. Корозия
движущегося автомобиля.
6. Протекторная
защита от корозии.
7. Электрохимическая
защита от корозии.
8. Устройство
для электрохимической защиты кузова
автомобиля от корозии.
9. Правила
установки и эксплуатации устройства.
10. Электрохимическая
защита.
11. Защита
поврежденных в результате аварии частей
кузова.
12. Заключение
Приложения.
13. Приложение
1. Скрытые полости автомобиля.
14. Приложение
2. Использование защитных покрытий для
предотвращения корозии кузова автомобиля.
Прежде
чем пытаться защититься от коррозии,
необходимо ответить на вопрос о том,
что же такое коррозия металла. В обиходе
коррозией называют появление ржавчины
на поверхности металла. Каковы же
основные механизмы появления
ржавчины?
Необходимо признать, что до
настоящего времени полного ответа на
этот вопрос нет, а результаты проводимых
исследований показывают, что процесс
коррозии является очень сложным,
поскольку на его протекание оказывает
влияние большое число факторов —
химический состав металла среда, в
которой он находится температура
давление наличие газов и т.д. По этой
причине в книге изложены только самые
начальные сведения из теории коррозии,
знание которых необходимо для правильной
защиты корпуса автомобиля. Более полное
представление о механизмах коррозии
читатель может почерпнуть из рекомендуемой
литературы.
Коррозия железа (а именно
этот процесс мы будем рассматривать в
дальнейшем) осуществляется, если
дополнительно имеются, по крайней мере,
еще две составляющие электролит, с
которым граничит железо, и другой
проводник, также граничащий с электролитом.
Электролитом в обычных условиях является
дождевая вода атмосферная влага снег,
дорожная грязь. Вторым, по отношению к
кузову автомобиля проводником чаще
всего является поверхность земли,
атмосфера, какой либо другой внешний
проводник, расположенный вблизи
автомобиля. Два проводника (которые в
данном случае называются электродами)
погруженные в электролит образуют так
называемый гальванический элемент.
Основное свойство гальванического
элемента состоит в том, что если электроды
выполнены из различных металлов, то
такой элемент является источником
напряжения. При этом положительный,
электрод называется анодом отрицательный
— катодом.
Проделайте простой
эксперимент. В стакане теплой воды
растворите ложку поваренной соли и
опустите две пластины — одну медную
другую стальную. Простейший источник
напряжения готов. С помощью вольтметра
можно легко убедиться в том, что
гальванический элемент создает небольшое
менее полувольта напряжение. Если вы
продолжите эксперимент несколько дней,
то заметите как на поверхности стали
начнет появляться ржавчина Этот
простой эксперимент наглядно демонстрирует
механизм коррозии металла. Объяснение
Объяснение
этого механизма состоит в следующем.
Из
курса физики известно, что проводники
характеризуются способностью отдавать
электроны во внешнюю среду. Наглядно
можно представить, что каждый проводник
окружен облаком из электронов, которые
под действием тепловой энергия вылетают
из него, а затем, если им ничто не мешает,
под действием электрических сил
возвращаются в проводник. Если металл
поместить в электролит, то положительные
ионы металла (т.е. те атомы металла,
электроны которых находятся во внешней
среде) начнут переходить в электролит.
В результате этого металл приобретает
некоторый потенциал, который может быть
измерен. На практике потенциал металла
определяют по отношению к специальному
стандартному электроду потенциал которого
принимается равным нулю. Полученная
разность потенциалов между стандартным
электродом и металлом получила название
стандартного электродного потенциала
(СЭП).
Ниже приведены стандартные
электродные потенциалы некоторых
металлов, расположенные в порядке
снижения их активности, т. е. чем более
е. чем более
отрицательным является СЭП тем
выше активность металла.
Стандартные
электродные потенциалы металлов, В
Магний | -2,38 | Танталл | -0,34 |
Алюминий | -1,66 | Никель | -0,24 |
Марганец | -1,18 | Молибден | -0,2 |
Хром | -0,91 | Свинец | -0,13 |
Цинк | -0,76 | Медь | 0,34 |
Железо | -0,44 | Серебро | 0,8 |
Кадмий | -0,4 |
|
|
Наибольший
интерес представляет процесс коррозии
железа в электролите при наличии менее
активного металла. В этом случае железо
В этом случае железо
как более активный металл является анодом а
менее активный — катодом. В гальванической
паре всегда корродирует более активный
металл — анод.
Коррозия анода
сопровождается двумя видами реакций —
окислительной на аноде и восстановительной
на катоде. В дальнейшем для определенности
в качестве анода рассмотрим железо
(Fe), однако все результаты относительно
его коррозии справедливы, по
крайней мере качественно для
любого ранее названного металла.
Окислительная
реакция может быть представлена
как процесс при котором атомы
железа отдают два электрона и вследствие
этого превращаются в положительно
заряженные ионы железа (Fе2+),
которые переходят в раствор электролита
в месте контакта его с анодом. Указанные
два электрона сообщают аноду отрицательный
заряд и тем самым вызывают ток по
направлению к катоду, где соединяются
с положительными ионами. Одновременно
положительные ионы анода соединяются
с отрицательно заряженными гидроксильными
группами (ОН ), которые всегда
присутствуют в растворе
электролита.
Схематически реакция на
аноде может быть записана в следующем
виде:
Fe
+ 20Н— =
Fe2+ +
2е + 20Н— =
Fe(OH)2 +
2е.
Под
действием ионов железа на катоде
возникают ионы водорода (Н+),
с которыми и соединяются электроны
анода. Схематически этот процесс
описывается в следующем виде:
Н+ +
2е = 2Н = Н2
т.е.
на катоде происходит выделение
водорода.
Если анодная и катодная
реакции объединяются, они приводят к
общей реакции коррозии
Fе
+ 2Н20
= Fе(ОН)2 +
Н2
Таким
образом, железо в сочетании с водой и
менее активным металлом переходит в
гидроокись железа, которая в обиходе и
называется ржавчиной.
Наличие в воде
дополнительной соли приводит к повышению
проводимости электролита и, как следствие,
к увеличению скорости окисления анода.
При этом дополнительно образуются
хлорное железо и раствор соляной кислоты.
Вот такие условия создают автолюбителям
каждую зиму наши дорожники. Впрочем,
кислотные дожди, которые выпадают с
осадками, также не способствуют долголетию
автомобиля.
Важной характеристикой
коррозии является скорость коррозии,
которая определяется как глубина
проникновения коррозии в металл в
единицу времени. Для железа наиболее
характерным является значение скорости
коррозии в пределах 0,05—0,02 нм/год. Из
приведенных значений скорости коррозии
следует, что при нарушении лакокрасочного
покрытия за 5 лет эксплуатации автомобиля
толщина металла может уменьшиться на
0,25—1 мм, т е., по сути дела, если не
предусмотреть специальных мер защиты,
металл проржавеет, что называется,
насквозь.
Описанный механизм коррозии
указывает также на основные пути борьбы
с этим явлением. Кардинальный путь
состоит в устранении катода или
электролита, однако, этот способ и
наименее пригоден, поскольку автомобиль
не может быть изолирован от окружающей
среды и, в частности, от поверхности
земли. Остаются два пути — изолировать
металл от электролита с помощью покрытия
или превратить корпус автомобиля из
анода в катод.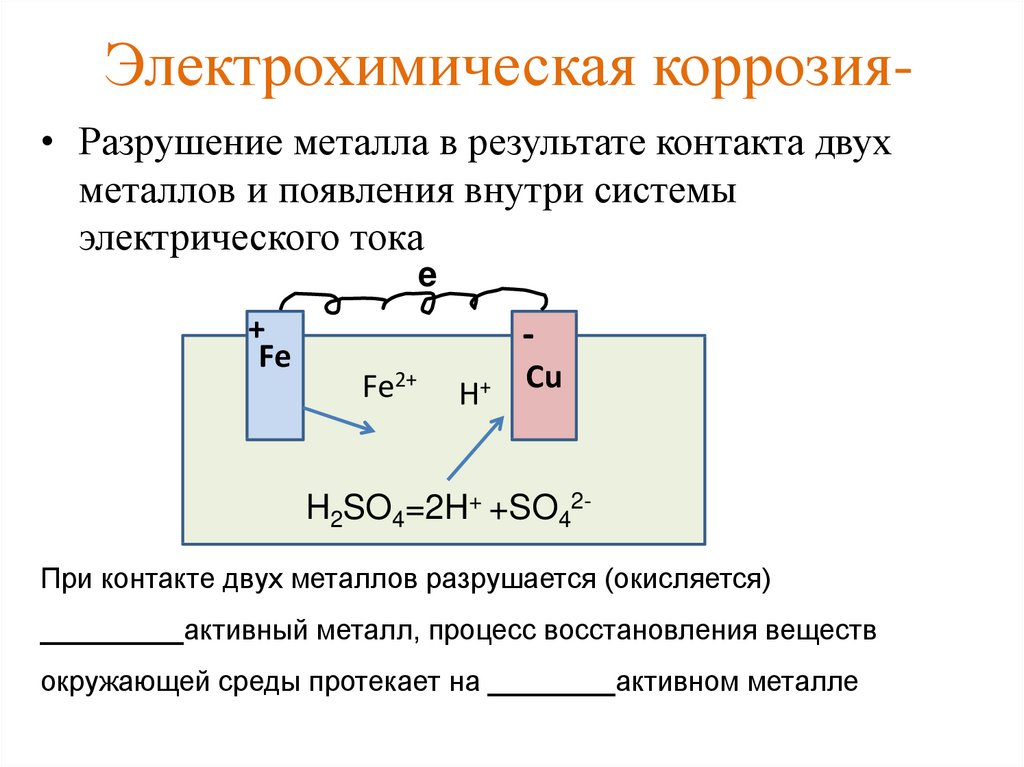
Первый способ известен
всем автолюбителям и широко используется
на практике, однако он не прекращает
коррозии как таковой, а только защищает
металл от ржавления. При нарушении
лакокрасочного покрытия коррозия
начинается разъедать металл, а повторное
нанесение покрытия сопряжено с большими
временными и материальными затратами
(прил. 1, 2).
Наиболее уязвимыми частями
корпуса автомобиля при этом являются
скрытые полости и щели, такие, как пороги,
внутренние балки, лонжероны, стойки,
внутренние поверхности дверей, потолок,
да практически весь корпус автомобиля
(см. прил. 1). Сложная форма скрытых щелей
и полостей затрудняет, а чаще делает
невозможным качественную подготовку
поверхности под окраску и саму окраску,
а внутренние напряжения изогнутого в
этих местах металла способствуют его
интенсивной коррозии. В этих условиях
срок службы кузова легкового автомобиля
до выхода его из строя составляет 6
лет.
Вместе с тем, не отрицая важности
регулярного восстановления лакокрасочного
покрытия, автор обращает внимание на
принципиально иной метод защиты корпуса
автомобиля от коррозии, а именно, полное
прекращение самого процесса коррозии
путем изменения потенциала корпуса.
Этот метод в литературе называется
катодной защитой.
Катодная защита
металлов основана на том, что скорость
коррозии пропорциональна активности
металлов, образующих гальваническую
пару. В обычных условиях корпус автомобиля
является анодом и поэтому корродирует.
Если же изменить потенциал корпуса
относительно внешней среды либо с
помощью внешнего источника напряжения
либо приведя в контакт с более активным
металлом, то сам корпус автомобиля
станет катодом и корродировать вообще
не будет (по крайней мере скорость
коррозии уменьшится в сотни раз), а
разрушаться станет анод. В соответствии
со способом изменения потенциала
защищаемого металла различают протекторную
и электрохимическую защиту. Однако
прежде чем рассматривать методы защиты,
целесообразно описать особенности
коррозии автомобиля в различных условиях
его эксплуатации.
Причины электрохимической коррозии и способы защиты металла
Методики предупреждения коррозии.
Оцинковка.
Данный вид защиты, использует немалая часть производителей авто. На производстве, поверхность машины покрывают плавленным цинком. При достаточном слое цинка, методика является весьма эффективной. При нарушении металлической структуры, изначально разрушается цинковая поверхность. Этот способ профилактики, защищает авто от воздействия неблагоприятных химикатов.
На производстве, поверхность машины покрывают плавленным цинком. При достаточном слое цинка, методика является весьма эффективной. При нарушении металлической структуры, изначально разрушается цинковая поверхность. Этот способ профилактики, защищает авто от воздействия неблагоприятных химикатов.
Полимерная защита.
Пленка, не имеющая цвета, позволяет предотвратить появление ржавчина на поверхности машины. Данный вид защиты, является наиболее удобным и действенным. Пленка предоставляется на клейкой поверхности и легко крепиться на структуру металла. Благодаря отсутствию цвета, пленка пользуется большой популярностью. Используя данный материал, легко защитить пораженную часть автомобиля от нежелательных воздействий.
Ламинирование кузова
защита от коррозии кузова
Уберечь кузов автомобиля от абразивного износа и преждевременной коррозии можно, используя специальную полимерную пленку, которая являет собой клеящийся прозрачный материал. Ламинирование во многих случаях намного практичнее и удобнее, чем иные виды защиты: Ламинирование, часто используют для частичной защиты авто (двери, капот). Процесс нанесения пленки достаточно прост и не потребует много времени. Материал, устойчив к температурному воздействия и надежно фиксируется на поверхности. Благодаря данной методике, можно долгое время сохранять первоначальный вид авто. Данный вид защиты, часто используется перед продажей авто с небольшим пробегом. Пленка надежно защищает поверхность от появления царапин. Часть дилеров, так же используют ламинирование, для сбережения автомобиля при транспортировке.
Ламинирование во многих случаях намного практичнее и удобнее, чем иные виды защиты: Ламинирование, часто используют для частичной защиты авто (двери, капот). Процесс нанесения пленки достаточно прост и не потребует много времени. Материал, устойчив к температурному воздействия и надежно фиксируется на поверхности. Благодаря данной методике, можно долгое время сохранять первоначальный вид авто. Данный вид защиты, часто используется перед продажей авто с небольшим пробегом. Пленка надежно защищает поверхность от появления царапин. Часть дилеров, так же используют ламинирование, для сбережения автомобиля при транспортировке.
Катодная защита.
Данная методика, предполагает использование специального устройства. Прибор, поляризует металл, создавая защитный слой. На поверхности кузова, скапливается минусовой заряд, предупреждающий ржавчину. Методика действенна определенный период. При разрушении поляризации поверхности, необходимо повторять процедуру. По этому, катодная защита, работает некоторое время.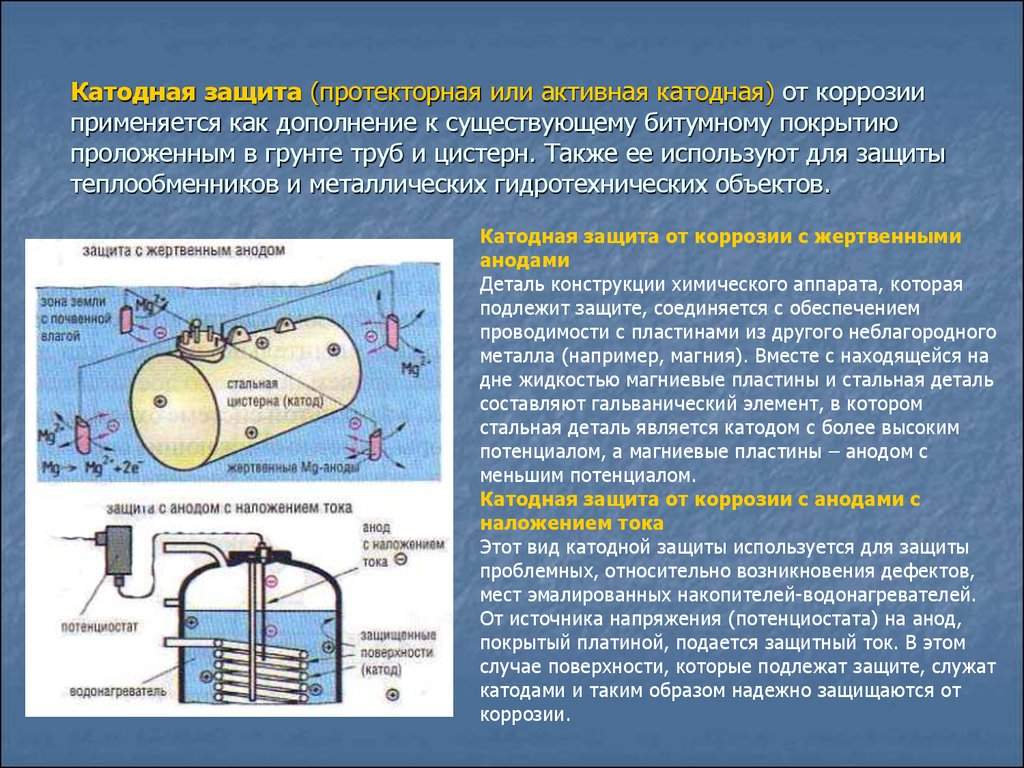 Данный метод, используется в труднодоступных местах кузова. Некоторые производители, применяют ее в области дна авто, порогов и дверей.
Данный метод, используется в труднодоступных местах кузова. Некоторые производители, применяют ее в области дна авто, порогов и дверей.
Барьер — защита.
Используя пластиковые элементы защиты (например — в области колес автомобиля), можно предотвратить попадание разрушающих частиц на кузов машины. Преграда, блокирует вылетающие, из под колес частицы песка и камней. Тем самым, лако красочная поверхность сохраняет свою структуру дольше. На сегодняшний день, данная защита, часто устанавливается производителем. Так же, имеется специальная (пластиковая) защита для донной части авто. Некоторые производители, используют барьеры в области стоек и других частей транспортного средства.
Грунтовка.
Один из наиболее популярный видов предупреждения ржавчины — нанесение слоя грунта. Небольшой слой грунта, наноситься между металлом и краской. Данный слой, исключает попадание влаги на металл. Защита, так же, действенна некоторое время. Предотвратить ржавчину полностью она не способна, но существенно замедляет процесс разрушения поверхности.
Защищающая краска.
защита днища
Определенное покрытие, способно не только украсить, но и защитить автомобиль. Лакокрасочное покрытие, одно из наиболее уязвимых. Во время эксплуатации автомобиля, краска постоянно разрушается
При выборе краски, необходимо обратить внимание на определенные ее параметры
Основные требования к ЛКП:
— Высокая прочность покрытия. — Стойкость к стиранию. — Совместимость с грунтом. — Безопасность для здоровья человека (малая токсичность). — Устойчивость к термическому перепаду. Фосфатная защита.
Устойчивость к ржавчине, значительно возрастает при применении фосфатной грунтовки. Данный грунт, включает в себя ряд химических элементов. Совокупность элементов, образуют тонкую защитную поверхность. В данном случае, воздействие внешних факторов, наносит меньший урон металлическому покрытию и делает его более устойчивым.
Коррозия автомобиля, сложна в устранении. Гораздо проще провести профилактику, чем бороться с появившейся ржавчиной. Выбор метода защиты, личное дело каждого автомобилиста. Не стоит экономить на защите кузова автомобиля. Ремонт и восстановление пораженного участка стоит достаточно дорого. Предотвратить нарушение структуры кузова и дорогостоящий ремонт, можно с помощью защитно слоя. Таким образом, вы значительно увеличите срок службы кузовной части авто. Не допускайте появления коррозии, а предотвращайте ее появления. Защитив свой автомобиль, вы останетесь уверенны в сохранении его внешнего вида.
Выбор метода защиты, личное дело каждого автомобилиста. Не стоит экономить на защите кузова автомобиля. Ремонт и восстановление пораженного участка стоит достаточно дорого. Предотвратить нарушение структуры кузова и дорогостоящий ремонт, можно с помощью защитно слоя. Таким образом, вы значительно увеличите срок службы кузовной части авто. Не допускайте появления коррозии, а предотвращайте ее появления. Защитив свой автомобиль, вы останетесь уверенны в сохранении его внешнего вида.
Как выполнить анодную защиту ванны химического никелирования?
Как выполнить анодную защиту ванны химического никелирования. Защита таких ванн происходит именно анодным способом электрохимической защиты. Суть химического никелирования заключается в том, что этот процесс позволяет обеспечить покрытие металлических изделий слоем никеля, который является очень тонким и осу ществляет защитные функции.
Такой слой помогает повысить антикоррозийные свойства, придает поверхности изделия эстетичный внешний вид. Такие материалы используются и при эксплуатации скважин, что это такое и какие есть способы, мы уже рассматривали, Для того чтобы изготовить такую ванну, чаще всего используются неметаллические материалы или нержавеющие металлы.
Такие материалы используются и при эксплуатации скважин, что это такое и какие есть способы, мы уже рассматривали, Для того чтобы изготовить такую ванну, чаще всего используются неметаллические материалы или нержавеющие металлы.
Если при изготовлении ванны может происходить выделении никеля на стенках ванны. Для того чтобы предотвратить такие процессы используется анодная защита. При использовании такого способа в раствор никеля вводят катод, стены ванны одновременно поляризуются анодным способом.
При использовании материалов из титана может быть образование плотной оксидной пленки, которая не имеет свойств проводимости. Это может стать причиной отключения анодной защиты.
Нагревается ванна с помощью ТЭНов или теплоносителей. Использование пара в качестве теплоносителя значительно ускоряет процесс нагревания и позволяет поддерживать постоянную температуру.
Как работает такая ванна. Раствор в ванне нагревается до 95 градусов, затем помещаются детали, которые необходимо покрыть.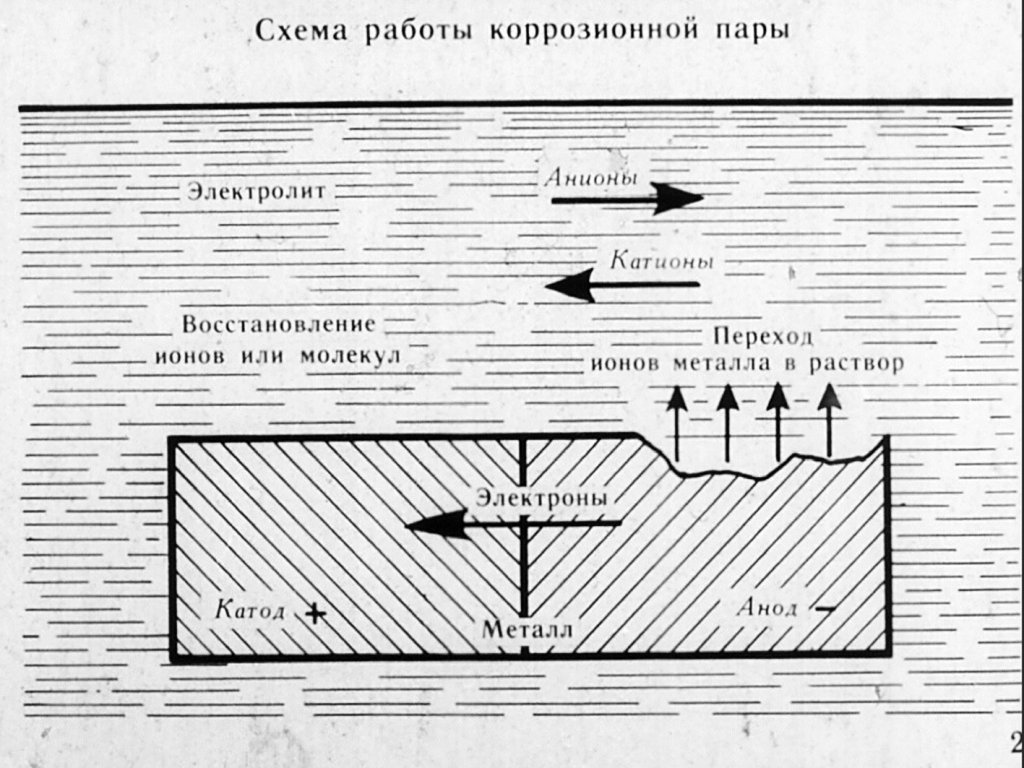 Анодная защита, которая используется в ванной не дает оседать никелю на стенах ванны. Часть электролита подается в корректировочную емкость, в которой происходит охлаждение раствора.
Анодная защита, которая используется в ванной не дает оседать никелю на стенах ванны. Часть электролита подается в корректировочную емкость, в которой происходит охлаждение раствора.
Причины появления коррозии
Для защиты машины от ржавчины стоит понимать принцип данного процесса. Простыми словами коррозия — формирование ржавчины. Чтобы разобраться с причинами, стоит вспомнить физику со школьной скамьи.
Каждый проводник выступает в роли передатчика электронов. Если представить проводник визуально, то это какое-то металлическое тело, окруженное облаком многочисленных электронов, покидающих «убежище» под действием энергии тепла. При отсутствии помех эти же электроны приходят обратно к проводнику. Если металлические элемент окунуть в электролит, то атомы металла (со знаком «+») переходят в новый состав. Итог действия — приобретение металлом потенциала, доступного для измерения.
Особо активна коррозия в электролитической жидкости, если проводник имеет меньшую активность. Металлический элемент, обладающий большей активностью, выступает в роли анода, а меньшей — катода. В процессе взаимодействия корродирует анод. Появление ржавчины (коррозия) проходит посредством протекания следующих реакций — восстановления и окисления. При этом восстанавливается катод, а разрушается (покрывается ржавчиной) анод.
Металлический элемент, обладающий большей активностью, выступает в роли анода, а меньшей — катода. В процессе взаимодействия корродирует анод. Появление ржавчины (коррозия) проходит посредством протекания следующих реакций — восстановления и окисления. При этом восстанавливается катод, а разрушается (покрывается ржавчиной) анод.
Если поместить металл в водную среду или обеспечить контакт с проводником, обладающим меньшей активностью, то происходит процесс коррозии. Ситуация усугубляется, если в воде присутствует соль. Последняя делает электролит проводимым, а это приводит к еще большей скорости окисления. Если сравнивать с автомобилем и дорожными условиями, то зимой транспорт сталкивается с описанными выше проблемами. Металл контактирует с водой и специальным составом, которым покрываются дороги. Опасны для металла и кислотные дожди, которые стали обычным явлением для многих регионов страны.
Главный показатель — скорость покрытия ржавчиной. Здесь есть специальный параметр, позволяющий определить стойкость того или иного металла к коррозии. Классическое железо характеризуется скоростью коррозии, равной — 0.03-0.05 мм в год. Это значит, что после пяти лет эксплуатации металл становится тоньше на 0.15-0.25 мм. Если никаких действий не предпринимать, то на кузове может образоваться дырка, на устранение которой пойдет немало средств.
Классическое железо характеризуется скоростью коррозии, равной — 0.03-0.05 мм в год. Это значит, что после пяти лет эксплуатации металл становится тоньше на 0.15-0.25 мм. Если никаких действий не предпринимать, то на кузове может образоваться дырка, на устранение которой пойдет немало средств.
Из рассмотренного выше напрашивается вывод, что для защиты металла от коррозии достаточно превратить его из анода в катод. Автолюбители часто используют простой вариант — они покрывают кузов специальной защитой. Но последняя эффективна только на неповрежденном кузове. Появление трещины или царапины на ЛКП приводит к контакту металла с менее активным проводником. Итог — появление коррозии. Катодная защита отличается большей эффективностью, ведь она меняет роль кузова автомобиля, превращая его из подверженного разрушению анода в стойкий катод.
Правила потрошения и разделки щуки
Щуку потрошат и разделывают после очистки чешуи.
Как правильно разделать щуку на котлеты:
Рыбе разрезают брюхо и вытаскивают внутренности
Важно не повредить желчь, иначе можно испортить продукт. Пищевод вынимают вместе с жабрами, оставляя голову
Пищевод вынимают вместе с жабрами, оставляя голову
Удаляют белую пленку, идущую вдоль брюха (она же плавательный пузырь). Ножом отрезают голову.
После того переходят к разделке самой туши. Эта процедура будет различаться в зависимости от того, что планируется готовить: фарш, филе, цельные куски или фаршированную рыбу.
На фарш
Если планируется готовить фарш для котлет, убирают только крупные кости (позвоночник). Позвоночный столб щуки крепкий и твердый. Если щучка мелкая, то позвоночник можно не вынимать.
Разделка средней и крупной щуки для приготовления фарша включает следующие шаги:
- Рыбу кладут на разделочную доску.
- Лезвие ножа ставят параллельно позвоночнику (в месте, где находилась голова) и срезают филе до хвоста. Нож нужно вести как можно ближе к хребту.
- Таким же способом срезают филейную часть с другого бока рыбины.
- Срединную часть с позвоночником убирают, она пригодится для приготовления ухи.
- От костей щуку для котлет очищают, но не тщательно, т.
 к. в процессе измельчения мяса в фарш косточки крошатся и не чувствуются в готовых котлетах. Филе прокручивают на мясорубке через мелкую решетку. Для лучшего измельчения косточек это можно сделать два раза.
к. в процессе измельчения мяса в фарш косточки крошатся и не чувствуются в готовых котлетах. Филе прокручивают на мясорубке через мелкую решетку. Для лучшего измельчения косточек это можно сделать два раза.
Для жарки филе
В теле щуки много костей, среди них есть массивные (позвоночник), средние и очень тонкие. Косточек очень много и удалить их трудно.
Продукт без костей готовят в следующем порядке:
- Срезают филе по всей длине тушки.
- Щуку переворачивают и срезают филе с другой стороны.
- Оставшийся хребет и хвостовую часть режут на куски и откладывают в сторону.
- С филе срезают ребра. Они очень тонкие, если нож острый, значительных потерь продукта не будет.
- Вырезают плавники.
- Над линией ребер прощупывают мякоть с косточками и делают два параллельных разреза вдоль филе.
- Полосу с косточками отделяют ножом и вырезают из филе.
- Оставшиеся кости удаляют пинцетом. Получают пласт рыбной мякоти без косточек.
- С рыбы снимают кожу.

- Филе режут на порционные куски и готовят блюдо по выбранному рецепту.
Для жарки кусками
Подготовка для жарки кусками не занимает много времени.
Тушку обрабатывают следующим образом.
- С щуки срезают плавники.
- Отрезают хвост.
- Режут рыбу на куски толщиной 1,5-2 см. Если планируется запекать щуку в духовке, длина кусков может достигать 10-15 см.
- Если щука большая, куски нарезают произвольно, чтобы было удобно укладывать их на сковороде.
Для фаршировки
Фаршированную щуку (с головой и без головы) готовят в духовом шкафу. Для такого блюда подходят рыбины среднего размера.
Этапы разделки:
- Вокруг щучьей головы делают надрез.
- С тушки с помощью ножа и ножниц снимают кожу вместе с плавниками. Чтобы кожица легко снималась, тушку отбивают скалкой.
- С оставшейся части туши срезают (и отбирают руками) мясо щуки. Остается только скелет рыбины.
- Готовят фарш для начинки, используя филе, овощи, зелень, мясо, яйца, другие ингредиенты.
- Снятую шкурку набивают фаршем, брюшко зашивают. Блюдо готовят в духовке.
Электрохимическая коррозия от грунта
Вследствие разности напряжений, образовавшихся на отдельных участках трубопроводов, возникает поток электронов. Процесс образования ржавчины происходит по электрохимическому принципу. На основании этого эффекта часть металла в анодных зонах растрескивается и перетекает в основание почвы. После взаимодействия с электролитом образовывается коррозия.
Одним из значимых критериев для обеспечения защиты от негативных проявлений является длина магистрали. На пути попадаются почвы с разным составом и характеристикой. Все это способствует возникновению разности напряжений между частями проложенных трубопроводов. Магистрали обладают хорошей проводимостью, поэтому происходит образование гальванопар с достаточно большой протяженностью.
Увеличение скорости коррозии трубопровода провоцирует высокая плотность потока электронов. Не меньшее значение играет и глубина расположения магистралей, так как на ней сохраняется существенный процент влажности, и температуры, которая ниже отметки “0” не отпускается. На поверхности труб также остается прокатная окалина после обработки, а это влияет на появление ржавчины.
На поверхности труб также остается прокатная окалина после обработки, а это влияет на появление ржавчины.
Путем проведения исследовательских работ установлена прямая зависимость между глубиной и площадью образованной ржавчины на металле. Это основано на том, что металл с большей площадью поверхности наиболее уязвим к внешним негативным проявлениям. К частным случаям можно отнести проявление на стальных сооружениях значительно меньших количеств разрушений под действием электрохимического процесса.
Агрессивность грунтов к металлу, прежде всего, определяется их собственной структурной составляющей, влажностью, сопротивлением, насыщенностью щелочами, воздушной проницаемостью и иными факторами. Монтер по защите подземных трубопроводов от коррозии должен быть ознакомлен с проектом на строительство магистрали.
Защита скрытых полостей автомобиля
Защита скрытых полостей
Для того чтобы защитить скрытые полости необходимо знать несколько правил. Качественная обработка скрытых полостей является одним из ключевых моментов в защите автомобиля. Подобрать надежную защиту для этих мест сможет настоящий специалист, который работает на станции технического обслуживания.
Подобрать надежную защиту для этих мест сможет настоящий специалист, который работает на станции технического обслуживания.
Мастика в этом случае не лучший способ защиты. На данный момент существует очень много химических препаратов, которые защитят ваш автомобиль и предотвратят появления ржавчины на кузове и не только. Современные фирмы разрабатывают материалы, которые проникают в поверхность кузова и создают защитную пленку, трещины стоит обрабатывать антикоррозийными средствами для покрытий.
Электронный метод защиты
Электронный метод защиты
Электронная защита автомобиля от коррозии – способна значительно замедлить процесс образования коррозии в 99,7% случаев. Об этом говорят многочисленные тесты, которые были проведены ученными. Данная защита помогает сохранить ваш автомобиль от коррозии на срок до десяти лет. Многие компании предоставляют данные устройства к продаже и дают на них гарантию. Они не создают помех во время прослушивания радиостанций, они отвечают всем современным требованиям и стандартам качества.
Данный прибор достаточно прост в установке, многие люди проводят установку электронной защиты самостоятельно, не прибегая к помощи специалистов. Следует убедиться, чтобы все провода устройства находились на своем месте и не мешали автолюбителю.
Для проводов следует использовать пластиковые крепежи или изоляционную ленту. Проверить работу устройства можно по светящимся лампочкам, они должны загораться при включении двигателя, если этого не происходит, тогда стоит проверить работу аккумулятора. Если даже после этого лампочка не светится, тогда стоит обратиться к дилеру, у которого вы приобрели устройство.
Преимущества электронного метода
Электронная защита автомобиля от коррозии поможет вам значительно сэкономить средства и время. Ведь наиболее, уязвимыми для коррозии являются задние крылья, кузов, днище, внутренняя поверхность трансмиссия. Именно в этих местах коррозия развивается часто и стремительно, в основном из-за плохой вентиляции и скопления влажного воздуха.
Устанавливая подкрылки, стоит обеспечить свободу доступа воздуха для обеспечения вентиляции. Главным недостатком мастики является то, что ей приходится обрабатывать автомобиль каждый год в отличие от электронной защиты. Также не менее, уязвимыми являются и стойки, внутренние балки, лонжероны, а также потолок. Для того чтобы их обработать нужно, сверлить специальные отверстия, а это является дополнительным источником проникновения вредных веществ в полости авто.
Различные коррозии могут возникать в процессе механического повреждения кузова. Такое повреждение может нарушить структуру металла, а это крайне опасно для целостности вашего автомобиля. Многие детали придется просто менять, так как они не подлежат ремонту.
Электронная защита автомобиля от коррозии практически единственный метод защиты от ржавчины с внутренними напряжениями, он совершенно исключает воздействия погодных условий на металл. Данная защита совместима с любой мастикой и дополнительным антикоррозийным средством. Ваш кузов будет находиться под надежной защитой.
Ваш кузов будет находиться под надежной защитой.
Все выше предложенные способы защиты помогут уберечь ваше транспортное средство от появления коррозии, они смогут устранить ее появление. Вы можете сами обработать свой автомобиль мастикой или грунтовкой, а также антикоррозийными средствами.
А также к вашим услугам специалисты, которые помогут вам установить электронную или электрохимическую защиту на высоком профессиональном уровне. Ваша машина окажется в надежных и крепких руках настоящего мастера своего дела.
fCcyleEGWCA
Чем отличается катодная защита от анодной?
Чем отличается катодная защита от анодной? В отличии от анодной защиты, катодная используется на материалах, которые не склонные к пассивации. При использовании трубопровода из стали при проколах под дорогами цена цена анодной защиты будет входить в стоимость материалов.
Катодная защита заключается в приложении к объекту внешнего тока от минуса, который позволяет поляризовать катодные участки элементов, которые подверглись коррозии.
Значения потенциал, в данном случае, будут приближаться к анодным, положительный полюс будет присоединяться к аноду. При использовании такого способа возможность появления коррозии практически равна нулю.
Принцип действия электрохимической защиты
Рассматриваемый способ защиты кузова от ржавчины относят к активным методам. Разница между ними и пассивными способами состоит в том, что первые создают какие-либо защитные меры, не позволяющие вызывающим коррозию факторам воздействовать на автомобиль, в то время как вторые лишь изолируют кузов от воздействия атмосферного воздуха. Данная технология изначально применялась для защиты от ржавчины трубопроводов и металлоконструкций. Электрохимический метод считают одним из наиболее эффективных.
Данный способ защиты кузова, который также называют катодным, основан на особенностях протекания окислительно-восстановительных реакций. Суть состоит в том, что на защищаемую поверхность накладывают отрицательный заряд.
Сдвиг потенциала осуществляют с применением внешнего источника постоянного тока или путем соединения с протекторным анодом, состоящим из более электроотрицательного металла, чем защищаемый объект.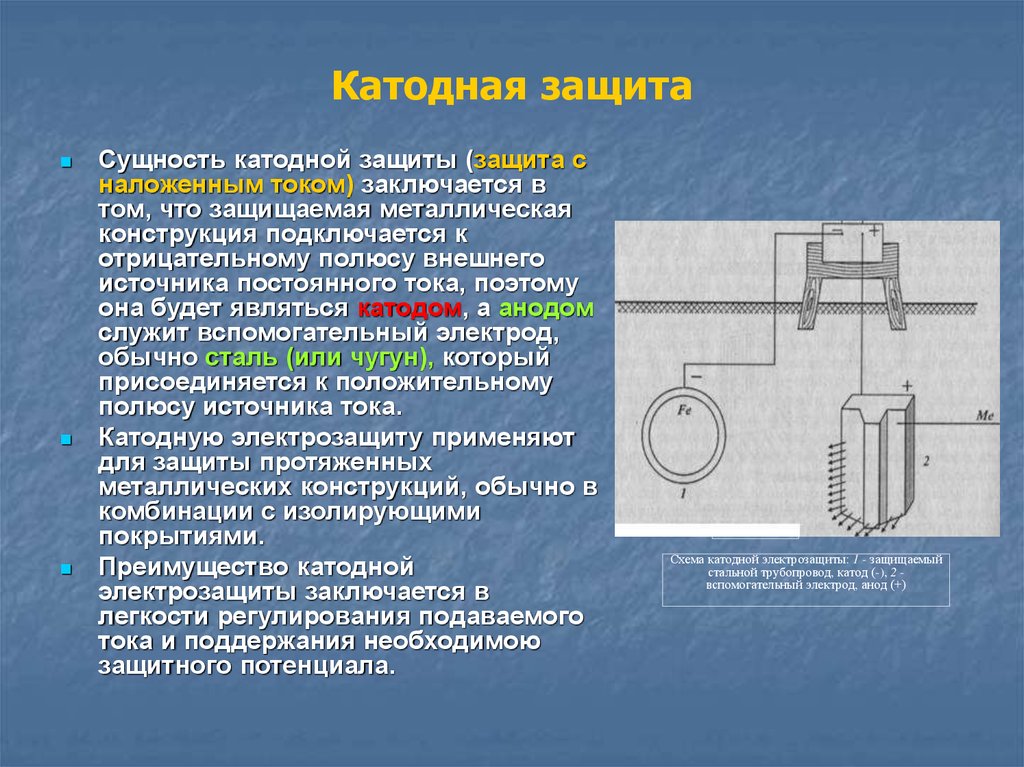
Принцип действия электрохимической защиты автомобиля состоит в том, что между поверхностью кузова и поверхностью окружающих объектов вследствие разности потенциалов между ними по цепи, представленной влажным воздухом, проходит слабый ток. В таких условиях окислению подвергается более активный металл, а другой, наоборот, восстанавливается. Именно поэтому используемые для автомобилей защитные пластины из электроотрицательных металлов называют жертвенными анодами. Однако при чрезмерном сдвиге потенциала в отрицательную сторону возможно выделение водорода, изменение состава приэлектродного слоя и прочие явления, которые приводят к деградации защитного покрытия и возникновению стресс-коррозии защищаемого объекта.
Рассматриваемая технология для автомобилей предполагает использование в качестве катода (отрицательно заряженного полюса) кузова, а анодами (положительно заряженными полюсами) служат различные окружающие объекты или установленные на автомобиле элементы, проводящие ток, например, металлические сооружения или влажное дорожное покрытие. При этом анод должен состоять из активного металла, такого как магний, цинк, хром, алюминий.
При этом анод должен состоять из активного металла, такого как магний, цинк, хром, алюминий.
Однако эти данные не совсем верны – в соответствии с законами электрохимии, расстояние между катодом и анодом прямо пропорционально определяет величину разницы потенциалов. Поэтому в каждом конкретном случае необходимо достичь определенного значения разницы потенциалов. К тому же воздух, рассматриваемый при данном процессе в качестве электролита, способен проводить электрический ток, характеризующийся большой разницей потенциалов (примерно кВт), поэтому ток с плотностью 10-30 мА/м? не будет проводиться воздухом. Возможно возникновение лишь «побочного» тока в результате намокания анода.
Что касается разности потенциалов, наблюдается концентрационная поляризация по кислороду. При этом попавшие на поверхность электродов молекулы воды ориентируются на них таким образом, что происходит освобождение электронов, то есть реакция окисления. На катоде данная реакция, наоборот, прекращается.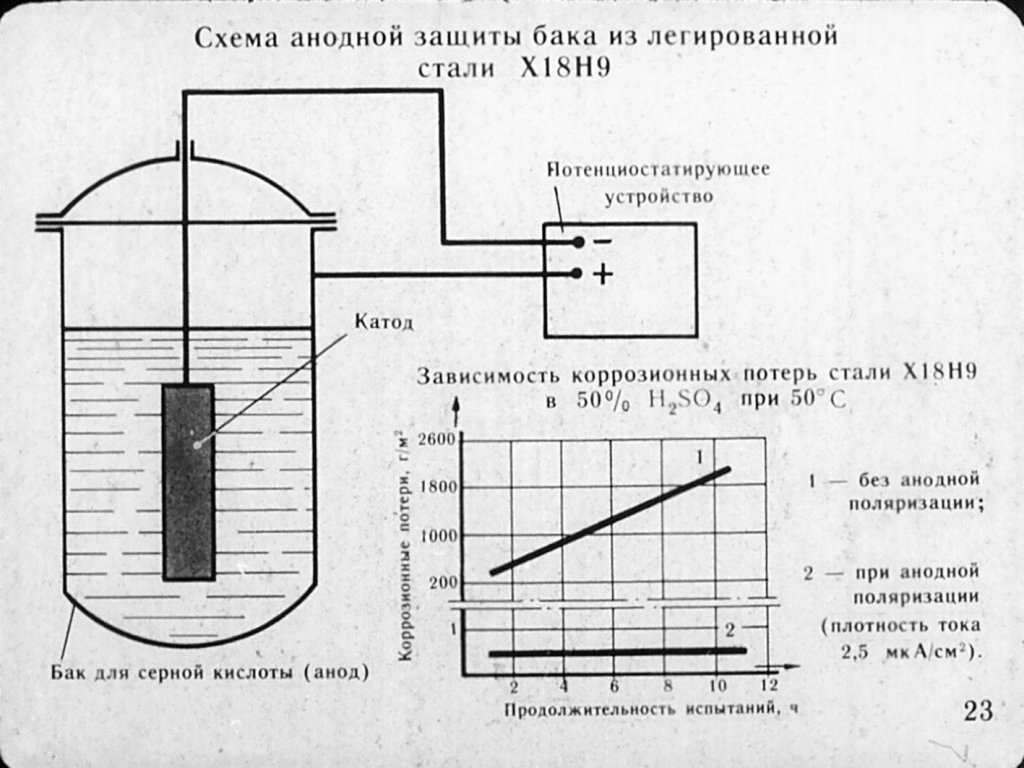 Вследствие отсутствия электрического тока освобождение электронов происходит медленно, поэтому процесс безопасен и незаметен. Благодаря эффекту поляризации, происходит дополнительное смещение потенциала кузова в отрицательную сторону, что дает возможность периодически выключать устройство защиты от коррозии. Нужно отметить, что площадь анода прямо пропорционально определяет эффективность электрохимической защиты.
Вследствие отсутствия электрического тока освобождение электронов происходит медленно, поэтому процесс безопасен и незаметен. Благодаря эффекту поляризации, происходит дополнительное смещение потенциала кузова в отрицательную сторону, что дает возможность периодически выключать устройство защиты от коррозии. Нужно отметить, что площадь анода прямо пропорционально определяет эффективность электрохимической защиты.
Что такое анодная защита?
Что такое анодная защита? Это электрохимическая защита, которая применяется для конструкций, в том числе при прокладке водопровода методом ГБН расценки на материалы с такой защитой будет чуть выше, которые изготовлены из низколегированных углеродистых сталей, которые не подвержены коррозии.
Таким образом, используется такая защита для тех металлов, которые способны сами защищаться от коррозии. Электрохимическая защита применяется для того чтобы защищать изделия от коррозии. Часто используется на готовых изделиях, где невозможно восстановить лакокрасочное покрытие. Так, например, обеспечить защиту подземного трубопровода или днища у судна, это очень дорого и трудозатратно, часто бывает просто невозможно.
Так, например, обеспечить защиту подземного трубопровода или днища у судна, это очень дорого и трудозатратно, часто бывает просто невозможно.
Электрохимическая защита позволяет обеспечить защиту конструкции от коррозии, если процесс разрушения начался. Как выглядит этот процесс? К изделию подключается постоянный ток. Такой ток на металлической поверхности создает катодную поляризацию электродов микрогальванических пар. Может использоваться для резервуаров воды, что это такое, мы уже знаем
Анодная защита от коррозии применяется при условии электропроводной коррозионной среды. При использовании такой защиты происходит смещение потенциала металла в положительную сторону. Это достигается при введении окислителей в среду, которая подверглась коррозии. В данном случае происходит анодная поляризация.
Для того чтобы поверхность перешла в пассивное состояние, можно использовать пассивирующие ингибиторы. Это происходит за счет возникшего тока. Но такие вещества загрязняют окружающую среду.
При создании анодной электрохимической защиты используется:
- источник внешнего тока;
- электрод сравнения;
- катод;
- объект, который защищается.
Для того чтобы определить подходит ли такая защита для определенной конструкции используются данные, полученные с анодных поляризационных кривых. Таким способом можно определить потенциал коррозии в определенной среде. Такой способ позволяет выявить область устойчивой пассивности и плотность тока, которой обладает данная область.
Для того чтобы изготовить катоды используют такие металлы как:
- тантал;
- свинец;
- никель;
- платина;
- сталь.
Это металлы, которые не повержены коррозии и являются малорастворимыми. Стальные трубы, например, используются при прокладке канализации методом ГБН, для того чтобы использовать анодную защиту результативно существуют требования для объекта.
Важно, чтобы сварные швы были сделаны качественно. Материал, из которого создан объект должен иметь свойство перехода в пассивное состояние. На объекте должны отсутствовать воздушные карманы и заклепки, в качестве соединений. Важным условием является то, что электрод и катод должны находится в растворе постоянно.
Материал, из которого создан объект должен иметь свойство перехода в пассивное состояние. На объекте должны отсутствовать воздушные карманы и заклепки, в качестве соединений. Важным условием является то, что электрод и катод должны находится в растворе постоянно.
Эффективная защита (электрохимическая) от коррозии
Для чего нужно устройство
Устройство электрохимической защиты «Акор» позволяет забыть о дорогой антикоррозионной обработке кузова. Операция установки устройства займет всего 30 минут, благодаря чему Вы навсегда забудете о ржавчине. На новых автомобилях предотвращается процесс образования коррозии, а на подержанных автомобилях останавливается распространение уже образовавшейся коррозии. Эффективность устройства подтверждена результатами независимых исследований и многолетним опытом эксплуатации.
Предыстория
Катодная защита была впервые описана сэром Гемфри Дэви в серии докладов представленных Лондонскому королевскому обществу по развитию знаний о природе в 1824. После продолжительных тестов впервые катодную защиту применили в 1824 на судне HMS Samarang. Анодные протекторы из железа были установлены на медную обшивку корпуса судна ниже ватерлинии, значительно снизив скорость корродирования меди. Медь, корродируя, высвобождает ионы меди, которые обладают антиобрастающим эффектом. В связи с чрезмерным обрастанием корпуса и снижением эффективности корабля, Королевский военно-морской флот Великобритании принял решение отказаться от протекторной защиты, чтобы получить преимущества от антифоулингового эффекта вследствие корродирования меди.
После продолжительных тестов впервые катодную защиту применили в 1824 на судне HMS Samarang. Анодные протекторы из железа были установлены на медную обшивку корпуса судна ниже ватерлинии, значительно снизив скорость корродирования меди. Медь, корродируя, высвобождает ионы меди, которые обладают антиобрастающим эффектом. В связи с чрезмерным обрастанием корпуса и снижением эффективности корабля, Королевский военно-морской флот Великобритании принял решение отказаться от протекторной защиты, чтобы получить преимущества от антифоулингового эффекта вследствие корродирования меди.
Принцип действия
Процесс коррозии напоминает работу гальванического элемента, поскольку сталь представляет собой, в основном, сплав железа и углерода, то есть веществ с различными электродными потенциалами. При попадании на поверхность такого сплава электролита (вода, грязь с дороги с содержанием солей) между молекулами железа и углерода начинает идти электрохимическая реакция, сопровождающаяся растворением анода (железа) и переходом его в гидраты, а затем и в окислы.
Принцип действия устройства «Акор» основан на создании гальванической пары между кузовом автомобиля и дополнительными электродами.
Сдвиг потенциала защищаемого металлического объекта осуществлен с помощью внешнего стабилизированого источника постоянного тока.
Существет способ катодной защиты без внешнего источника тока, при помощи протекторного анода, изготовленного из металла более электроотрицательного, относительно кузова автомобиля. При этом, поверхность кузова становится эквипотенциальной и на всех её участках протекает только катодный процесс. Обусловливающий коррозию анодный процесс перенесен на вспомогательные электроды. Недостатком способа катодной защиты без внешнего источника тока является: меньшая эффективность, меньший радиус действия, необходимо зачищать кузов автомобиля.
Рис. 1. Протекторный электрод после длительной эксплуатации и расположение на корпусе судна.
Подробнее:
Электрохимическая катодная защита металлов от коррозии, основана на зависимости скорости коррозии от электродного потенциала металла. К собственно, электрохимической защите относят катодную защиту, при которой потенциал металла специально сдвигают из области активного растворения в более отрицательную область относительно потенциала коррозии.
К собственно, электрохимической защите относят катодную защиту, при которой потенциал металла специально сдвигают из области активного растворения в более отрицательную область относительно потенциала коррозии.
Сдвиг потенциала металла осуществляют с помощью внешнего источника постоянного тока (станции катодной защиты) или соединением с другим металлом, более электроотрицательным по своему электродному потенциалу (так называемый, протекторный анод). При этом поверхность защищаемого образца (детали конструкции) становится эквипотенциальной и на всех ее участках протекают только катодные процессы, а анодные, обусловливающие коррозию, перенесены на вспомогательные электроды.
Катодную защиту широко применяют для защиты от морской коррозии. Гражданские суда защищают с помощью А1-, Mg- или Zn-протекторных анодов, которые размещают вдоль корпуса и вблизи винтов и рулей. Станции катодной защиты используют в тех случаях, когда требуется отключение защиты для устранения электрич. поля корабля, при этом потенциал обычно контролируют по хлорсеребряным электродам. Существуют автоматические станции катодной защиты, расположенные на судне либо на берегу (при стоянке или ремонте). Аноды обычно изготовлены из платинированного титана, линейной или круглой формы, с околоанодными непроводящими экранами для улучшения распределения потенциала и плотности тока вдоль корпуса судна.
поля корабля, при этом потенциал обычно контролируют по хлорсеребряным электродам. Существуют автоматические станции катодной защиты, расположенные на судне либо на берегу (при стоянке или ремонте). Аноды обычно изготовлены из платинированного титана, линейной или круглой формы, с околоанодными непроводящими экранами для улучшения распределения потенциала и плотности тока вдоль корпуса судна.
Особенно важно использование катодной защиты для стационарных нефтегазопромысловых сооружений, трубопроводов и хранилищ к ним на континентальном шельфе. Подобные сооружения не могут быть введены в сухой док для восстановления защитного покрытия, поэтому электрохимическая защита является основным методом предотвращения коррозии. Морская нефтепромысловая вышка, как правило, снабжена в своей подводной части протекторными анодами (на одну вышку приходится до 10 т и более протекторных сплавов).
Разрабатываются способы катодной защиты кузовов транспортной техники (автомобилей). Протекторные аноды используют для защиты отд. декоративных элементов кузова, при этом электронные устройства обеспечивают постоянный или импульсный ток. Для увеличения зоны действия защиты необходимо размещать аноды в наиб. коррозионноопасных точках или использовать электропроводящую окраску. Устройство формирует токи для управления катодных электродов (входят в комплект)
Протекторные аноды используют для защиты отд. декоративных элементов кузова, при этом электронные устройства обеспечивают постоянный или импульсный ток. Для увеличения зоны действия защиты необходимо размещать аноды в наиб. коррозионноопасных точках или использовать электропроводящую окраску. Устройство формирует токи для управления катодных электродов (входят в комплект)
Установка и характеристики
| Индикация замыкания электрода на корпус | Есть |
| Радиус действия электрода, М | 0,4 |
| Стабилизированый ток устройства, мА | 15 |
| Срок службы электрода, лет | 5 |
Электроды устанавливаются при помощи эпоксидного клея на места, где коррозия наиболее вероятна.
При установке следует помнить, что:
- ✔ защитные электроды устанавливаются только на места, защищенные лакокрасочным покрытием.
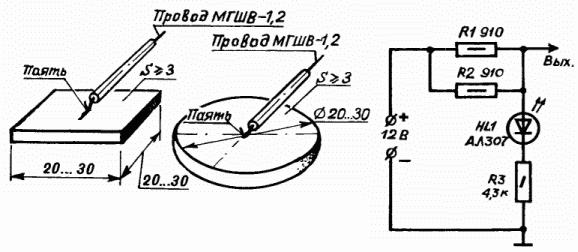 Не должно быть контакта с массой;
Не должно быть контакта с массой; - ✔ для приклеивания электродов можноиспользовать только эпоксидный клей или шпатлевку на его основе;
- ✔ наружную сторону защитных электродов нельзя покрывать мастикой, краской, клеем или другим электроизоляционным покрытием.
Электронный блок устанавливается вблизи аккумулятора, красный провод присоединяется к клемме аккумулятора «+». То есть, электронный блок остается включенным даже при отключенном общем электрооборудовании автомобиля. Синий провод подключается к одному или двум электродам.В целом, устройство потребляет не больше чем часы автомобиля и гарантирует длительную эффективную работу даже при сильно разряженном аккумуляторе.
Рекомендуем устанавливать электроды в следующих местах:
- 1 — передняя нижняя часть заднего крыла и арка колеса по стыку с крылом;
- 2 — места крепления фар и подфарников;
- 3 — полости за щитками-усилителями передних крыльев;
- 4 — внутренние поверхности дверей и порогов
- 5 — днище.

Скачать инструкцию (pdf, 500Kb)
Описание и виды защиты кузова от коррозии
Содержание
- Что такое коррозия, почему она образуется и чем опасна?
- Наиболее уязвимые места
- Зачем дополнительная обработка кузова, если она делается на заводе?
- Виды защиты
- Электрохимический метод
- Катодная защита
- Анодная защита
- Барьерные методы
- Комбинированная защита от коррозии
Известно, что металлические поверхности автомобилей необходимо покрывать антикоррозийными средствами. Дело в том, что даже при тщательном уходе на кузов постоянно воздействуют внешние физические и химические факторы, в результате чего и образуется ржавчина. Антикоррозийное покрытие очень помогает продлить срок службы кузова и автомобиля в целом.
Что такое коррозия, почему она образуется и чем опасна?
Коррозия – это разрушение металла вследствие его химической реакции с водой и кислородом. В процессе движения незащищенная поверхность тела и других частей тела постоянно подвергается механическим воздействиям и контактирует с воздухом, в котором содержится кислород.
В процессе движения незащищенная поверхность тела и других частей тела постоянно подвергается механическим воздействиям и контактирует с воздухом, в котором содержится кислород.
Атмосферные осадки, в свою очередь, способствуют попаданию влаги на металл, а в труднодоступных местах автомобиля влага долго испаряется. Железо реагирует с водой и кислородом, образуя вредную ржавчину.
Ржавчина – одно из самых серьезных «заболеваний» организма. Его распространение приводит к ослаблению конструкции автомобиля и снижению уровня пассивной безопасности при столкновении.
Наиболее уязвимые места
Кузов из-за сложной конструкции ржавеет неравномерно. К наиболее уязвимым местам относятся:
- Сварные швы. Сварка не может обеспечить полную герметичность деталей, поэтому в швах всегда есть микротрещины. При постоянной влажности именно в местах сварки образуются первичные очаги коррозии.
- Днище, колесные арки, ниши и пороги.
 Эти места постоянно подвергаются воздействию грязи, песка и камней. При движении автомобиля на скорости физическое воздействие становится очень заметным, так что коррозия образуется довольно быстро.
Эти места постоянно подвергаются воздействию грязи, песка и камней. При движении автомобиля на скорости физическое воздействие становится очень заметным, так что коррозия образуется довольно быстро. - Двигатель и выхлопная система. Работающий двигатель имеет высокую температуру, которая сильно отличается от температуры окружающей среды. Постоянные колебания температуры также вызывают коррозию.
- Внутренняя часть тела. Салон легко пачкается и становится влажным даже после небольших поездок.
Все эти места требуют разной защиты, так как причины коррозии неодинаковы.
Зачем дополнительная обработка кузова, если она делается на заводе?
Многие автомобилисты считают, что коррозии подвержены только старые автомобили с внушительным пробегом, а новые автомобили не нуждаются в дополнительной антикоррозийной обработке. В реальности это далеко не так, так как обработка производителем скорее защищает автомобиль от заводского брака.
В реальных условиях автомобиль постоянно подвергается воздействию агрессивных факторов: повышенной влажности, химикатам на дорогах и даже кислотным дождям.
Производитель редко учитывает влияние таких условий, к тому же качество заводской обработки не всегда имеет приемлемый уровень.
Многие автомобили при производстве оцинковываются, однако и эта мера не является панацеей от коррозии. Толщина цинкового слоя очень мала, поэтому различные механические повреждения и вибрационные нагрузки легко его разрушают.
Виды защиты
Для защиты автомобиля разработано множество видов антикоррозийной обработки:
- Актив. Осуществляется с использованием продуктов, которые взаимодействуют с металлом и отталкивают влагу.
- Пассивный. Сюда входит барьерная защита, для которой используются различные типы покрытий или заплат.
- Трансформация. Включает в себя продукты, помогающие избавиться от уже появившейся на кузове ржавчины.

- Комплекс. Подразумевает использование сразу нескольких методов.
Электрохимическую защиту иногда относят к отдельной категории.
Электрохимический метод
Очень эффективный метод, с помощью которого можно добиться такого же высокого результата, как и при цинковании. Суть этого метода заключается в особенностях протекания химических реакций между металлом, кислородом и водой.
По законам физики и химии необходимо создать разность электрических потенциалов. Элемент с высоким потенциалом окисляется, а элемент с низким потенциалом восстанавливается.
Таким образом, для защиты металла от окисления ему придают отрицательный потенциал. Преимуществом этого метода является антикоррозийный эффект даже в труднодоступных местах кузова.
Катодная защита
Чаще всего электрохимическую защиту осуществляют катодным методом. При этом металл корпуса приобретает отрицательный потенциал и восстанавливается. Для смещения потенциала необходимо обеспечить прохождение тока, что осуществляется с помощью специального устройства.
Для смещения потенциала необходимо обеспечить прохождение тока, что осуществляется с помощью специального устройства.
Соответствующий электронный модуль можно приобрести или изготовить своими руками, затем установить в салоне и подключить к бортовой сети.
Прибор необходимо периодически выключать, так как при сильном сдвиге потенциала наблюдается негативное воздействие.
В качестве анода — элемента, который будет иметь положительный потенциал и подвергаться окислению — можно использовать металлический гараж или заземление на открытой стоянке. При движении автомобиля анодом является заземление с дорогой: для этого достаточно прикрепить к бамперу резиновую полосу с металлическими элементами. При движении между телом и дорогой образуется разность потенциалов.
Анодная защита
При использовании анодной защиты необходимо установить на корпус медные, алюминиевые или цинковые пластины, которые будут окисляться и «тянуть» процесс разрушения на себя. Как правило, их размещают на креплениях фар, брызговиках, внутренних поверхностях порогов или дверей. Недостатком этого метода является установка пластин, которыми все же нельзя покрыть все тело.
Как правило, их размещают на креплениях фар, брызговиках, внутренних поверхностях порогов или дверей. Недостатком этого метода является установка пластин, которыми все же нельзя покрыть все тело.
Барьерные методы
Коррозия часто возникает в определенных местах, которые часто контактируют с водой или физически повреждены. Такие места можно просто закрыть механическими преградами, что существенно замедлит скорость его возникновения.
Как правило, барьерами являются:
- Специальные грунтовки и мастики, тщательно покрывающие поверхность кузова.
- Пластиковые накладки. Обычно на колесные арки устанавливаются специальные крылья, пороги и низ дверей закрываются обвесами, на передней и задней кромке капота также встречаются пластиковые элементы или накладки из кожзаменителя.
- Ламинирование. Нанесение пленки из винила или полиуретана. Кузов, обтянутый пленкой, надежно защищен от камней, различных мелких повреждений, воздействия солнца и влаги.

Обычно автомобилисты совмещают сразу несколько способов барьерной защиты.
Комбинированная защита от коррозии
Комбинированный метод предполагает использование нескольких методов борьбы с коррозией. Например, можно использовать пластиковые накладки и нанесение влагоотталкивающих составов. Другие автовладельцы предпочитают использовать катодную защиту и специальные грунтовки.
Любой автомобиль неизбежно подвержен коррозии, и заводское покрытие не всегда является надежным антикоррозийным средством. Для продления срока службы кузова его необходимо комплексно защищать от разрушения практически с самого начала эксплуатации автомобиля.
Главная » Кузов автомобиля » Описание и виды защиты кузова от коррозии
Жертвенный анод — Химия LibreTexts
- Последнее обновление
- Сохранить как PDF
- Идентификатор страницы
- 256
Жертвенные аноды представляют собой высокоактивные металлы, которые используются для предотвращения коррозии поверхности менее активного материала. Жертвенные аноды создаются из металлического сплава с более отрицательным электрохимическим потенциалом, чем у другого металла, для защиты которого он будет использоваться. Жертвенный анод будет потребляться вместо металла, который он защищает, поэтому его называют «жертвенным» анодом.
Жертвенные аноды создаются из металлического сплава с более отрицательным электрохимическим потенциалом, чем у другого металла, для защиты которого он будет использоваться. Жертвенный анод будет потребляться вместо металла, который он защищает, поэтому его называют «жертвенным» анодом.
Катодная защита
При контакте металлических поверхностей с электролитами происходит электрохимическая реакция, известная как коррозия. Коррозия — это процесс возвращения металла в его естественное состояние в виде руды, вызывающий в этом процессе распад металла и ослабление его структуры. Эти металлические поверхности используются повсюду вокруг нас — от трубопроводов до зданий и кораблей. Важно обеспечить, чтобы эти металлы прослужили как можно дольше, и поэтому требуется так называемая катодная защита.
Жертвенные аноды относятся к нескольким формам катодной защиты. Другими формами катодной защиты являются
- гальваника,
- гальванизация и
- формирование сплавов.

Металл в морской воде является одним из таких примеров, когда металлическое железо контактирует с электролитами. При нормальных обстоятельствах металлическое железо реагировало бы с электролитами и начинало корродировать, ослабляя структуру и распадаясь. Добавление цинка, расходуемого анода, предотвратит «коррозию» металлического железа. Согласно таблице стандартных восстановительных потенциалов, стандартный восстановительный потенциал цинка составляет около -0,76 вольт. Стандартный восстановительный потенциал железа составляет около -0,44 вольта. Эта разница в восстановительном потенциале означает, что цинк будет окисляться намного быстрее, чем железо. На самом деле цинк полностью окислится до того, как железо начнет реагировать.
Какие материалы используются для расходуемых анодов?
Материалы, используемые для расходуемых анодов, представляют собой либо относительно чистые активные металлы, такие как цинк или магний, либо магниевые или алюминиевые сплавы, специально разработанные для использования в качестве расходуемых анодов. В приложениях, где аноды заглублены, анод окружает специальный материал обратной засыпки, чтобы гарантировать, что анод будет давать желаемую мощность.
В приложениях, где аноды заглублены, анод окружает специальный материал обратной засыпки, чтобы гарантировать, что анод будет давать желаемую мощность.
Поскольку расходуемый анод работает за счет введения другой металлической поверхности с более отрицательной электроотрицательной и гораздо более анодной поверхностью. Ток будет течь от вновь введенного анода, и защищаемый металл становится катодным, создавая гальванический элемент. Реакции окисления переносятся с поверхности металла на гальванический анод и приносятся в жертву в пользу защищенной металлической структуры.
Рисунок 1 . Частично проржавевший жертвенный анод на корпусе корабля. Цифры предоставлены Википедией
Как надеваются жертвенные аноды?
Жертвенные аноды обычно поставляются либо с проводами, либо с литыми хомутами для облегчения их соединения с защищаемой конструкцией. Токоподводящие провода могут быть прикреплены к конструкции с помощью сварки или механических соединений. Они должны иметь низкое сопротивление и должны быть изолированы, чтобы предотвратить повышенное сопротивление или повреждение из-за коррозии. При использовании анодов с залитыми хомутами хомуты можно либо приварить непосредственно к конструкции, либо использовать в качестве мест для крепления.
Они должны иметь низкое сопротивление и должны быть изолированы, чтобы предотвратить повышенное сопротивление или повреждение из-за коррозии. При использовании анодов с залитыми хомутами хомуты можно либо приварить непосредственно к конструкции, либо использовать в качестве мест для крепления.
Для хорошей защиты и устойчивости к механическим повреждениям требуется крепление с низким механическим сопротивлением. В процессе подачи электронов для катодной защиты менее активного металла более активный металл подвергается коррозии. Более активный металл (анод) приносится в жертву, чтобы защитить менее активный металл (катод). Степень коррозии зависит от металла, используемого в качестве анода, но прямо пропорциональна величине подаваемого тока.
Приложения
Жертвенные аноды
используются для защиты корпусов кораблей, водонагревателей, трубопроводов, распределительных систем, наземных резервуаров, подземных резервуаров и нефтеперерабатывающих заводов. Аноды в системах катодной защиты с расходуемым анодом необходимо периодически осматривать и заменять по мере износа.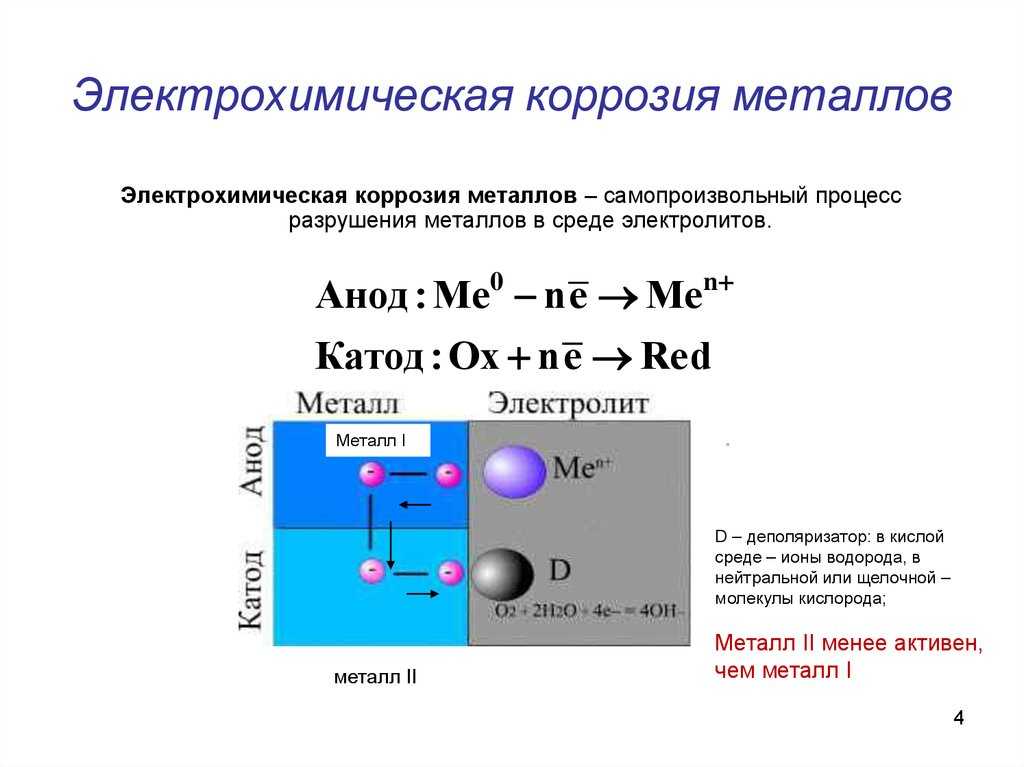
Ссылки
- «Контроль коррозии» NAVFAC MO-307 Сентябрь 1992 г.
- Петруччи, Ральф Х., Уильям С. Харвуд, Джеффри Херринг и Джеффри Д. Мадура. Общая химия: принципы и современные приложения. Девятое изд. Река Аппер-Сэдл, Нью-Джерси: Pearson Education, 2007. 848. Печать.
Проблемы
- Каковы цели использования расходуемых анодов?
- Как работают жертвенные аноды?
- Какие другие виды катодной защиты?
- Какие различные металлы можно использовать в качестве расходуемых анодов? (название три)
Ответы
- Жертвенные аноды используются для защиты металлических конструкций от коррозии.
- Жертвенные аноды окисляются быстрее, чем металл, который они защищают, и полностью расходуются до того, как другой металл вступит в реакцию с электролитами.
- Несколько различных форм катодной защиты включают формование сплавов, гальваническое покрытие и цинкование металла.
- В качестве расходуемых анодов можно использовать три металла: цинк, алюминий и магний.

Жертвенный анод распространяется по не объявленной лицензии и был создан, изменен и/или курирован LibreTexts.
- Наверх
- Была ли эта статья полезной?
- Тип изделия
- Раздел или страница
- Показать страницу TOC
- нет на странице
- Метки
Общий | OT: Кто-нибудь использовал жертвенные цинковые аноды в автомобиле? | Практик Машинист
ПСИ 180
Титан
#1
Кто-нибудь на форуме пробовал прикреплять жертвенные цинковые аноды к кузову автомобиля для уменьшения коррозии? Я живу во влажной, мокрой тропической среде, недалеко от моря: сегодня утром я поднял кусок переработанного цинкового анода лодки, который я оставил на несколько недель в качестве ржавого стального 4WD. Участок под ним имеет значительно меньше ржавчины другого цвета по сравнению с остальной мягкой сталью. Было бы разумно достать эти маленькие 1,5-дюймовые квадратные цинковые аноды и прикрепить их под машиной и внутри дверей, чтобы уменьшить ржавчину? парк в сравнении?.
Чип Честер
Алмаз
#2
Возможно, стоит попробовать спрей для холодного цинкования. Только что переснял трейлер, посмотрим, что получится. Однако вся эта подготовка к очистке стекла может стать барьером для входа. Также доступен без распыления.
Согласно веб-сайту ZRC, защита от оцинковки фактически распространяется на царапины, защищая неоцинкованную сталь на несколько миллиметров.
Чип
JST
Алмаз
#3
«Бросок» защиты в воде намного дольше. Вам нужно, чтобы защищенная зона и цинк находились в одной воде.
В машине вода и сырость — это все локально, так что гальванопокрытие лучше, чем цинковый электрод. Если не оцинковка, то упомянутая краска хорошая.
Краска «достигает» или «выбрасывает» на некоторое расстояние, если она и рассматриваемая область находятся в одной и той же воде. , так и в тонком покрытии.
Мне трудно найти что-либо, кроме спрея, который ВСЕГДА забивается задолго до того, как он опустеет.
DDoug
Алмаз
#4
У меня есть пара подержанных грузовиков в жертву хорошему.
Я нахожу соотношение 2 к 1, и отсутствие блоков, кажется, помогает.
ПСИ 180
Титан
#5
JST сказал:
«Бросок» защиты в воде намного дольше. Вам нужно, чтобы защищенная зона и цинк находились в одной воде.
В машине вода и сырость — это все локально, так что гальванопокрытие лучше, чем цинковый электрод. Если не оцинковка, то упомянутая краска хорошая.
Краска «достигает» или «выбрасывает» на некоторое расстояние, если она и рассматриваемая область находятся в одной и той же воде. , так и в тонком покрытии.
Мне трудно найти что-либо, кроме спрея, который ВСЕГДА забивается задолго до того, как он опустеет.
Нажмите, чтобы развернуть…
Я полагаю, что цинковый спрей — это следующий лучший способ после горячего цинкования кузова автомобиля. Я мог бы попробовать это И в любом случае несколько анодов в панелях порогов и нижней части дверей.
копатель Дуг сказал:
Держу парочку подержанных грузовиков в жертву хорошему.
Я нахожу соотношение 2 к 1, и не ставить блоки, похоже, помогает.Нажмите, чтобы развернуть…
Есть ли какая-то оккультная процедура переноса ржавчины с хорошего грузовика на грузовики-доноры, а-ля «Картина Дориана Грея»?, или еще лучше «Кристина» Стивена Кинга?
Джашли73
Титан
#6
Я думал, что вся идея расходуемых анодов заключалась в том, чтобы предотвратить накопление статического электричества на объектах, движущихся через жидкость, что каким-то образом приводило к коррозии металла под действием статического разряда? Если бы расходуемых анодов не было, то металлические части (выходит из строя) сгниет, пока лодка будет плыть по воде. ..?
..?
Возможно, я ошибаюсь насчет этого…?
kb0thn
Горячекатаный
#7
JST сказал:
Мне трудно найти что-либо, кроме спрея, который ВСЕГДА забивается задолго до того, как он опустеет.
Нажмите, чтобы развернуть…
Я покупаю и использую около дюжины баллончиков с цинковой краской в год. Я не могу вспомнить, чтобы у меня когда-либо был засор. Вы распыляете его вверх дном, пока он не станет прозрачным в конце использования? Я всегда так делаю.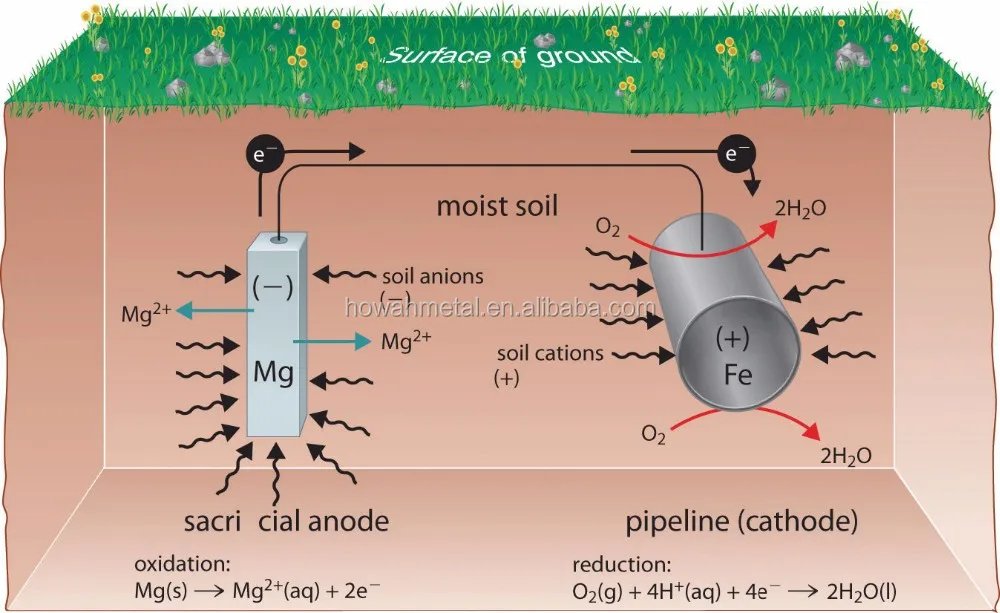
Когда я захожу в магазин, я могу посмотреть, какой бренд я использую.
JST
Алмаз
#8
Да, знаю, но с более новыми баллончиками «распылитель в любом месте» они просто распыляют краску независимо от того, как вы их держите. Я обычно использую дешевые банки Rustoleum. Их средства работают так же хорошо, как и все остальные, и я полагаю, что если я получу больше одного сеанса из банки, то у меня будут деньги впереди. У меня есть некоторые части, которые лежат на крыше уже 15 лет, и краска все еще работает. Я никогда не закрашивал его.
ПСИ 180
Титан
#9
JST сказал:
Да, знаю, но с новыми баллончиками «распылитель в любом месте» они просто распыляют краску независимо от того, как вы их держите. Я обычно использую дешевые банки Rustoleum. Их средства работают так же хорошо, как и все остальные, и я полагаю, что если я получу больше одного сеанса из банки, то у меня будут деньги впереди. У меня есть некоторые части, которые лежат на крыше уже 15 лет, и краска все еще работает. Я никогда не закрашивал его.
Нажмите, чтобы развернуть…
Моей мастерской уже 8 лет, все кровельные винты и болты снаружи покрыты серебристой краской для холодного цинкования, но не те, что под карнизом, которые оцинкованы: неокрашенные потеряли цинковую пластину и только начинают заржаветь. Я должен дать им очистить и покрыть их, а также.
Билл D
Алмаз
#10
Цинковые аноды на лодке работают как аккумулятор. Цинк электрически соединен с металлом лодки. он действует как мокрая батарея и создает небольшое электрическое напряжение между цинком и другими металлами. Это напряжение вызывает гальваническое действие, когда цинк наносится на другие металлы. это означает, что цинк выветривается, а другие металлы не ржавеют. АН связаны с электроотрицательностью между металлами.
На подземных трубопроводах и морских судах это можно сделать с помощью регулируемых электрических токов.
Билл D
Морской фермер
Алмаз
#11
Цинк работает только в том случае, если он связан с исходным материалом чем-то проводящим. Таким образом, прикрепление цинка к вашей машине будет отлично работать, пока вы паркуете ее под водой; но я никогда не был в вашем районе, поэтому не знаю, является ли это практичной альтернативой. Для запуска утром понадобятся два длинных шноркеля, один для двигателя и один для водителя, а зимой это будет неприятно.
Краска с высоким содержанием цинка эффективна в качестве первичной защиты только в том случае, если краска содержит 95% цинка или более. Многие из продаваемых цинковых красок содержат 93% цинка и предназначены для покрытия царапин или выбоин на уже оцинкованном металле, но они практически бесполезны для металла, который еще не оцинкован. Некоторые из них на 95% состоят из цинка и весьма эффективны. Я не знаю, почему эта разница в 2% имеет значение, но я знаю из дорогого опыта, что она имеет значение.
САГ 180
Титан
#12
Морской фермер сказал:
Цинк работает только в том случае, если он связан с исходным материалом чем-то проводящим. Таким образом, прикрепление цинка к вашей машине будет отлично работать, пока вы паркуете ее под водой; но я никогда не был в вашем районе, поэтому не знаю, является ли это практичной альтернативой. Для запуска утром понадобятся два длинных шноркеля, один для двигателя и один для водителя, а зимой это будет неприятно.
Краска с высоким содержанием цинка эффективна в качестве первичной защиты только в том случае, если краска содержит 95% цинка или более.
Многие из продаваемых цинковых красок содержат 93% цинка и предназначены для покрытия царапин или выбоин на уже оцинкованном металле, но они практически бесполезны для металла, который еще не оцинкован. Некоторые из них на 95% состоят из цинка и весьма эффективны. Я не знаю, почему эта разница в 2% имеет значение, но я знаю из дорогого опыта, что она имеет значение.
Нажмите, чтобы развернуть…
Это было бы практично в Дарвине, так как через полчаса прибывает прилив, поэтому полноприводные автомобили на прибрежных отмелях ловятся, когда прилив приходит слишком быстро, чтобы машины могли его опередить. Но ничего такого, что не исправит WD-40, позаимствованный у проплывающей мимо российской подводной лодки. Там, где я нахожусь, нередки ежедневные дожди в течение нескольких недель подряд, поэтому автомобиль будет промокнуть насквозь в течение продолжительных периодов недель в течение сезона дождей.
Улица
Горячекатаный
№13
Когда я был в Кэрнсе, местный житель каждый год распылял на днище своего полноприводного автомобиля смесь масла и средства для предотвращения ржавчины черного тела.
рыбий жир хорошо работает в панелях, таких как пороги, двери, передние обтекатели и т. д.
Как было сказано ранее в другом посте, солевой спрей, когда соль высохнет, единственный способ удалить ее — это промыть в пресной воде и высушить, смазать маслом и тому подобное не работает, когда соль поражена.
Что касается анодов, окуните свой автомобиль в электролит, в данном случае океан, и он будет работать до тех пор, пока анод (цинк) не съест, если ваш электролит пресная вода или тиннаро, используйте магниевый анод.
Последнее в шутку тоже не делайте….
стив-л
Титан
№14
В ответ на вопрос ОП, нет, это не сработает. Назначение цинка в соленой воде или куска магния в пресной воде состоит в том, чтобы представить менее благородный жертвенный анод для электролитической коррозии. Электролитическая коррозия является естественным явлением, вызванным естественной разницей электрического заряда между различными металлами в присутствии электролита, такого как вода. Чем больше расстояние между металлами, наблюдаемое в таблице элементов, тем больше разница зарядов и больше потенциал для электрической коррозии. Использование жертвенных анодов — это не лекарство, а стратегия пластыря. Чтобы иметь электрическую коррозию, вы должны иметь разнородные металлы в полной электрической цепи через электролит. Вместо того, чтобы поощрять электрическую коррозию, гораздо лучше предотвратить использование разнородных металлов или изолировать их электрически. В случае с ОП этих факторов не существует. Коррозия у него не электрическая.
Коррозия у него не электрическая.
ПСИ 180
Титан
№15
стив-л сказал:
В ответ на вопрос ОП, нет, это не сработает. Назначение цинка в соленой воде или куска магния в пресной воде состоит в том, чтобы представить менее благородный жертвенный анод для электролитической коррозии. Электролитическая коррозия является естественным явлением, вызванным естественной разницей электрического заряда между различными металлами в присутствии электролита, такого как вода. Чем больше расстояние между металлами, наблюдаемое в таблице элементов, тем больше разница зарядов и больше потенциал для электрической коррозии.
Использование жертвенных анодов — это не лекарство, а стратегия пластыря. Чтобы иметь электрическую коррозию, вы должны иметь разнородные металлы в полной электрической цепи через электролит. Вместо того, чтобы поощрять электрическую коррозию, гораздо лучше предотвратить использование разнородных металлов или изолировать их электрически. В случае с ОП этих факторов не существует. Коррозия у него не электрическая.
Нажмите, чтобы развернуть…
Весь смысл расходуемого цинкового анода состоит в том, чтобы на самом деле вызвать электрическую коррозию , которая благоприятствует стали за счет цинка. Как указывали другие плакаты, «бросок» цинка ограничен, когда он влажный, а не в электролите. Ограниченная область защиты обходится путем окрашивания целых областей, подлежащих защите, цинком. Очевидно, что это работает, но только если покрыть всю поверхность, чтобы защитить ее от ржавчины.
Дэйв Г.
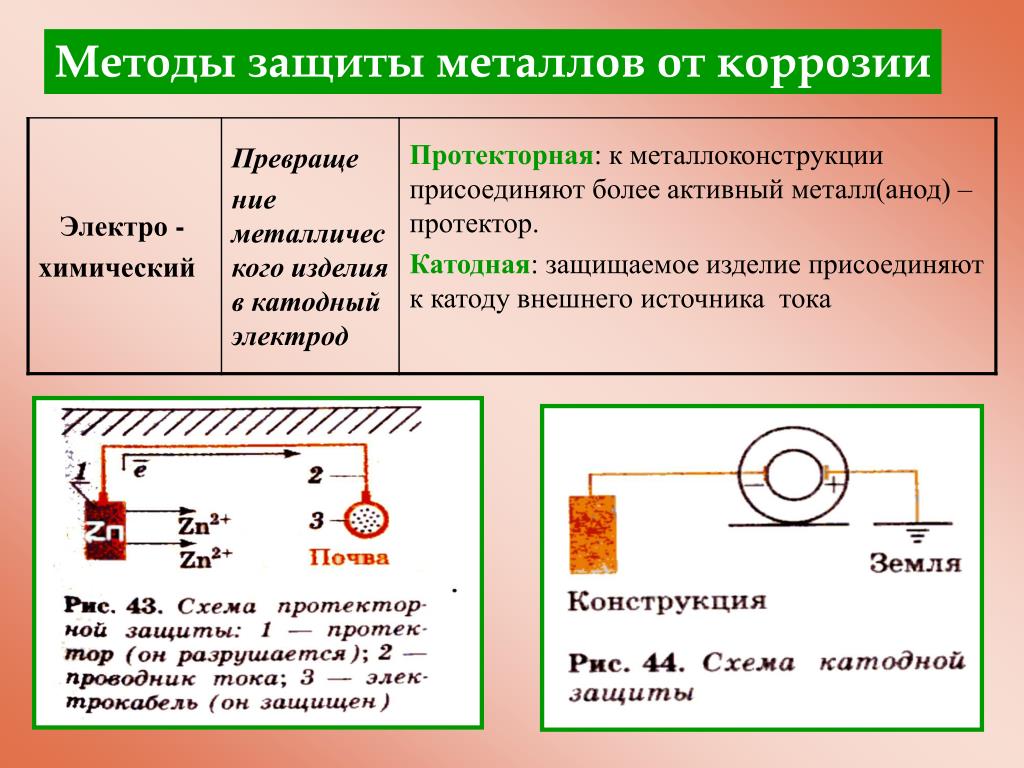
Чугун
№16
САГ 180 сказал:
Весь смысл жертвенного цинкового анода состоит в том, чтобы фактически создать электрическую коррозию, которая благоприятствует стали за счет цинка. Как указывали другие плакаты, «бросок» цинка ограничен, когда он влажный, а не в электролите. Ограниченная область защиты обходится путем окрашивания целых областей, подлежащих защите, цинком. Очевидно, что это работает, но только если покрыть всю поверхность, чтобы защитить ее от ржавчины.
Нажмите, чтобы развернуть…
Идея состоит в том, чтобы приложить к стали напряжение, чтобы «протолкнуть» ее в область, где железо термодинамически стабильно. Прикрепление цинкового анода к стали в воде создает напряжение ~1,5 вольта и защищает сталь от окисления. Как указано другими членами, цинк и сталь должны быть электрически соединены, а между ними должна быть непрерывная вода. См. прилагаемую диаграмму Пурбэ:
Прикрепление цинкового анода к стали в воде создает напряжение ~1,5 вольта и защищает сталь от окисления. Как указано другими членами, цинк и сталь должны быть электрически соединены, а между ними должна быть непрерывная вода. См. прилагаемую диаграмму Пурбэ:
дгфостер
Алмаз
# 17
В Вики есть довольно хорошая статья, которая хорошо связывает всю эту информацию воедино. Был даже небольшой раздел, посвященный непосредственно исходному вопросу ОП.
Катодная защита — Википедия
Из статьи: «Автомобили
Несколько компаний продают электронные устройства, заявляя, что они уменьшают коррозию для автомобилей и грузовиков. [SUP][37][/SUP] Специалисты по борьбе с коррозией обнаруживают, что они не работают.[SUP][38] [/SUP] Нет никаких рецензируемых научных испытаний и подтверждений, поддерживающих использование устройств.В 1996 году FTC приказала Дэвиду Маккриди, человеку, который продавал устройства, утверждающие, что они защищают автомобили от коррозии, выплатить реституцию и запретила названия «Rust Buster». » и «Раст Эвейдер».[SUP][39]»[/SUP]
[SUP][37][/SUP] Специалисты по борьбе с коррозией обнаруживают, что они не работают.[SUP][38] [/SUP] Нет никаких рецензируемых научных испытаний и подтверждений, поддерживающих использование устройств.В 1996 году FTC приказала Дэвиду Маккриди, человеку, который продавал устройства, утверждающие, что они защищают автомобили от коррозии, выплатить реституцию и запретила названия «Rust Buster». » и «Раст Эвейдер».[SUP][39]»[/SUP]
Очень интересный предмет. Если вы хотите провести простой подтверждающий эксперимент, поместите чистый стальной гвоздь в чашку с соленой водой, а также кусок алюминия. Используйте вольтметр, чтобы измерить потенциал 0,5 В между двумя
Денис
Адама
Алмаз
# 18
Процентное содержание цинка имеет значение Морской фермер, потому что для того, чтобы покрытие работало, оно должно действовать как один компонент, а не как набор отдельных металлических частиц, изолированных друг от друга, только когда это сопротивление становится достаточно низким, вы получаете защиту, равную гальванике .
Скоттл
Алмаз
# 19
Лучший способ защитить транспортное средство — защитить все от прямого контакта с водой/электролитами. ИМО требуемый продукт зависит от места на транспортном средстве. Я использовал все, от воска для полости тела до полиэтиленовой краски, отверждаемой влагой, такой как POR-15. Раньше многие компании предлагали услуги по «защите от ржавчины», которые включали распыление воска для кузова в каждую щель и полость, сверление отверстий (позже закрытых пластиковыми заглушками) для доступа, где это необходимо. Если все сделано правильно, это значительно замедлит коррозию. Они также обычно применяли некоторую форму грунтовки.
Я использовал все, от воска для полости тела до полиэтиленовой краски, отверждаемой влагой, такой как POR-15. Раньше многие компании предлагали услуги по «защите от ржавчины», которые включали распыление воска для кузова в каждую щель и полость, сверление отверстий (позже закрытых пластиковыми заглушками) для доступа, где это необходимо. Если все сделано правильно, это значительно замедлит коррозию. Они также обычно применяли некоторую форму грунтовки.
Некоторые средства, которые я пробовал в течение нескольких десятилетий:
Boeshield (не впечатлил)
WD-40 (короткое действие, но лучше, чем ничего) вода стекает вниз)
Асфальтовое грунтовочное покрытие (очень хорошо работает, если его время от времени осматривать и подкрашивать)
Прорезиненное грунтовочное покрытие (может быть хуже, чем без покрытия, если под него попадают влага и соль)
LPS 3 (необходимо время от времени проверять и подкрашивать)
POR-15 и т. д. (работает очень хорошо, если все сделано правильно, но PITA наносится грязно)
ACF-50 (отличный продукт, который останавливает коррозию, но смывает поверхности, подвергшиеся воздействию солевого тумана)
Профессиональные преобразователи ржавчины (должны наноситься правильно и затем покрыт сверху)
Коричневая грунтовка Rustoleum, разбавленная и обработанная кистью (работает, но есть продукты получше.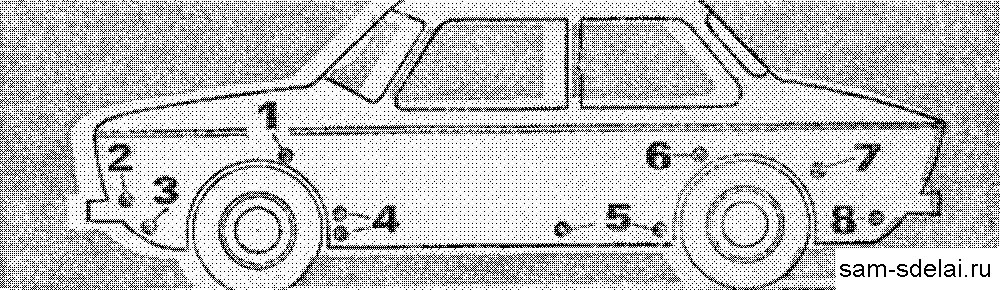 )
)
И еще несколько, о которых я не могу вспомнить в данный момент.
Несколько специалистов по кузовным работам посоветовали мне намазать воском все окрашенные поверхности, до которых вы сможете добраться, включая дверные, капотные и проемы багажника, распылить профессиональный антикоррозийный состав для тяжелых условий эксплуатации во все закоулки и щели и, самое главное, осмотреть и подправить защиту до того, как маленькие проблемы превратятся в большие.
Как правило, продукты профессионального уровня, используемые в кузовных мастерских, намного превосходят по своим характеристикам продукты, которые можно купить в магазинах запчастей и хозяйственных магазинах.
Билл D
Алмаз
#20
Адама сказал:
Процент цинка имеет значение, морской фермер, потому что для того, чтобы покрытие работало, оно должно действовать как один компонент, а не как набор отдельных металлических частиц, изолированных друг от друга, только когда это сопротивление становится достаточно низким, вы получаете защиту, равную гальванизации. /QUOTE
Краска действует как изолятор, если процентное содержание цинка не достаточно велико, чтобы атомы цинка были электрически связаны друг с другом. магнитный провод изолирован эмалью, так что вы можете понять, что краска является приличным изолятором. Нужно всего лишь изолировать 1,5 вольта между цинком и железом.
Билл ЛДНажмите, чтобы развернуть…
Устройство защиты от ржавчины | RUST STOPPER
Что такое коррозия?
Чтобы понять природу нашего устройства, нам нужно знать, что оно должно предотвращать. Наиболее распространенной и известной коррозией является гальваническая коррозия, которая является результатом локальных гальванических элементов, образующихся на поверхности металла. В любом случае важным компонентом этих элементов является раствор электролита. В случае атмосферной коррозии электролитом является конденсированная влага и дождевая вода, всегда содержащая определенное количество растворенных веществ, таких как кислород, углекислый газ, сернистый газ, оксиды азота и др. Процесс коррозии, вызванный указанными коррозионными ячейками, является анодным процессом – образованием положительных ионов из атомов металла. Электрохимическая коррозия является наиболее распространенным видом коррозии. Это одно из распространенных явлений атмосферной коррозии, которое вызывается действием влажного загрязненного воздуха на металлы. Электрохимическая коррозия возникает при воздействии короткозамкнутого элемента на границу раздела между металлом и электролитом. Эти ячейки образуются в результате химической неоднородности (или физической) металла, т.
Наиболее распространенной и известной коррозией является гальваническая коррозия, которая является результатом локальных гальванических элементов, образующихся на поверхности металла. В любом случае важным компонентом этих элементов является раствор электролита. В случае атмосферной коррозии электролитом является конденсированная влага и дождевая вода, всегда содержащая определенное количество растворенных веществ, таких как кислород, углекислый газ, сернистый газ, оксиды азота и др. Процесс коррозии, вызванный указанными коррозионными ячейками, является анодным процессом – образованием положительных ионов из атомов металла. Электрохимическая коррозия является наиболее распространенным видом коррозии. Это одно из распространенных явлений атмосферной коррозии, которое вызывается действием влажного загрязненного воздуха на металлы. Электрохимическая коррозия возникает при воздействии короткозамкнутого элемента на границу раздела между металлом и электролитом. Эти ячейки образуются в результате химической неоднородности (или физической) металла, т. е. на границе между различными металлами или в результате неоднородности кристаллической структуры металла. Коррозия металлов обычно проявляется дефектами поверхности металла (пятнами и питтингами) или снижением прочности металла.
е. на границе между различными металлами или в результате неоднородности кристаллической структуры металла. Коррозия металлов обычно проявляется дефектами поверхности металла (пятнами и питтингами) или снижением прочности металла.
Катодная защита
Катодная защита представляет собой электрохимическую защиту от коррозии. Катодная защита — это метод, используемый для контроля коррозии металлической поверхности путем превращения ее в катод электрохимической ячейки. Самый простой метод применения CP — это соединение защищаемого металла с куском другого, более легко подверженного коррозии «жертвенного металла», который действует как анод электрохимической ячейки. Осуществляется прямым контактом (так называемое анодное покрытие) или с проводником. С помощью протекторов крупные стальные объекты, такие как корпуса кораблей, трубопроводы и подземные резервуары, защищаются от коррозии. Протекторы изготавливаются из листового металла или стержней из активных металлов, таких как цинк, магний или алюминий, с проводами, соединенными с защищаемым объектом. В ячейке, сформированной таким образом, анод является протектором, который подвергается коррозии. После использования протекторы меняются на новые. Анодные покрытия (протекторы) изготавливаются из металла с более отрицательным электродным потенциалом (менее благородным), чем у защищаемого металла. Анодные покрытия металлов обеспечивают защищаемому металлу катодную защиту, так как покрытие из менее благородного металла является анодом и выполняет функцию протектора. Примерами анодных покрытий являются цинк и кадмий. Важнейшим практическим применением анодного покрытия является цинкование – нанесение цинкового покрытия на стальные поверхности. При появлении трещин или трещин образуется ячейка, в которой катодом служит железо, а анодом — цинк. В этой ситуации вместо ионов железа в раствор переходят ионы цинка. Таким образом, в случае анодирования металлических поверхностей покрытие не обязательно должно быть идеально герметичным.
В ячейке, сформированной таким образом, анод является протектором, который подвергается коррозии. После использования протекторы меняются на новые. Анодные покрытия (протекторы) изготавливаются из металла с более отрицательным электродным потенциалом (менее благородным), чем у защищаемого металла. Анодные покрытия металлов обеспечивают защищаемому металлу катодную защиту, так как покрытие из менее благородного металла является анодом и выполняет функцию протектора. Примерами анодных покрытий являются цинк и кадмий. Важнейшим практическим применением анодного покрытия является цинкование – нанесение цинкового покрытия на стальные поверхности. При появлении трещин или трещин образуется ячейка, в которой катодом служит железо, а анодом — цинк. В этой ситуации вместо ионов железа в раствор переходят ионы цинка. Таким образом, в случае анодирования металлических поверхностей покрытие не обязательно должно быть идеально герметичным.
Вот диапазон напряжений металлов из наименее Более отрицательный чем значение нормального Короче говоря, если бы мы соединили их все, они бы Мы можем добиться того же эффекта, если соединим протектор с
благородных:
Na
потенциала металла, тем большей склонностью к переходу в раствор он обладает.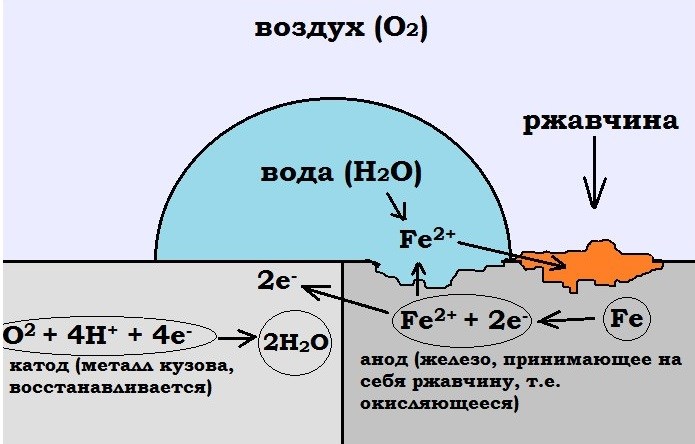
ржавели именно в таком порядке.
Активная катодная защита
положительный полюс постоянного тока, а защищаемая конструкция подключается
к отрицательному полюсу. Как это работает?
Метод работы нашего устройства хорошо известен и используется в промышленности в качестве катодной защиты от коррозии. Этот метод использовался в течение многих лет для защиты судов и в строительной отрасли для защиты железобетонных конструкций, подземных резервуаров и трубопроводов от коррозии. В этих случаях другие методы защиты от коррозии на таких огромных поверхностях были бы практически невозможны. Таким образом, используется пассивный метод, основанный на естественной разности потенциалов металлов. Это активное устройство, требующее питания, однако оно генерирует гораздо более высокое напряжение, что влияет на его эффективность и миниатюризацию. Как известно, электрохимическая коррозия является результатом образования локальных гальванических элементов на поверхности металла. В любом случае важным компонентом ячейки является раствор электролита. В случае атмосферной коррозии электролит представляет собой конденсированную влагу и дождевую воду, всегда содержащую определенное количество растворенных веществ, таких как кислород, углекислый газ, двуокись серы, оксиды азота и другие. Процесс коррозии, вызванный указанными коррозионными ячейками, является анодным процессом – образованием положительных ионов из атомов металла. Наше устройство исключает этот процесс. Метод катодной защиты заключается в поляризации металлических деталей, подвергающихся коррозии, постоянным током и изменении потенциала электрода в отрицательную сторону. При использовании нашего устройства положительно поляризованные проекторы благодаря своей «электрической привлекательности» берут на себя большую часть процессов коррозии и делают кузов автомобиля менее привлекательным для коррозии и безопасным.
Как известно, электрохимическая коррозия является результатом образования локальных гальванических элементов на поверхности металла. В любом случае важным компонентом ячейки является раствор электролита. В случае атмосферной коррозии электролит представляет собой конденсированную влагу и дождевую воду, всегда содержащую определенное количество растворенных веществ, таких как кислород, углекислый газ, двуокись серы, оксиды азота и другие. Процесс коррозии, вызванный указанными коррозионными ячейками, является анодным процессом – образованием положительных ионов из атомов металла. Наше устройство исключает этот процесс. Метод катодной защиты заключается в поляризации металлических деталей, подвергающихся коррозии, постоянным током и изменении потенциала электрода в отрицательную сторону. При использовании нашего устройства положительно поляризованные проекторы благодаря своей «электрической привлекательности» берут на себя большую часть процессов коррозии и делают кузов автомобиля менее привлекательным для коррозии и безопасным. Устройство предотвращает возникновение неблагоприятных явлений от электроэлемента и даже при контакте с электролитами, такими как соленая вода или кислотные дожди, и даже со значительными незащищенными металлическими поверхностями, такими как царапины, сколы или даже уже существующая коррозия. кузов нашего автомобиля или другой охраняемый объект остается в безопасности. Устройство также можно использовать для постоянной защиты от коррозии других металлических объектов, таких как сельскохозяйственная техника, хозяйственные столы, даже заборы и кровля.
Устройство предотвращает возникновение неблагоприятных явлений от электроэлемента и даже при контакте с электролитами, такими как соленая вода или кислотные дожди, и даже со значительными незащищенными металлическими поверхностями, такими как царапины, сколы или даже уже существующая коррозия. кузов нашего автомобиля или другой охраняемый объект остается в безопасности. Устройство также можно использовать для постоянной защиты от коррозии других металлических объектов, таких как сельскохозяйственная техника, хозяйственные столы, даже заборы и кровля.
О НАС
Я параграф. Нажмите здесь, чтобы добавить свой собственный текст и отредактировать меня. Это просто. Просто нажмите «Редактировать текст» или дважды щелкните меня, чтобы добавить свой собственный контент и внести изменения в шрифт. Не стесняйтесь перетаскивать меня куда угодно на своей странице. Я — отличное место для вас, чтобы рассказать историю и дать вашим пользователям узнать о вас немного больше.
Это отличное место для написания длинного текста о вашей компании и ваших услугах. Вы можете использовать это место, чтобы немного подробнее рассказать о своей компании. Расскажите о своей команде и о том, какие услуги вы предоставляете.
Транспортные средства
В течение многих лет коррозия была серьезной проблемой в автомобильной промышленности, где листовой металл кузова автомобиля может быть быстро разрушен коррозией. Есть несколько способов защитить свой автомобиль от коррозии. Первый и, наверное, самый популярный и дешевый способ — покрыть металлическую поверхность защитным покрытием, в том числе всевозможными лакокрасочными материалами. Однако нужно обратить внимание на герметичность покрытия. Каждый скол или повреждение запускает процесс коррозии. В 70-х и 80-х кузова более дорогих автомобилей погружались в баки с антикоррозийным раствором, как в случае с Volvo. К сожалению, защита была эффективна только в тех местах, где кузов автомобиля не подвергался никакому механическому воздействию. Как видно во многих местах лакокрасочное покрытие истерто или поцарапано рабочими частями или всевозможными пластиковыми элементами или проводами. Другой факт, что кузов автомобиля тоже работает все время, что часто можно увидеть, когда вы поднимаете автомобиль с помощью домкрата и пытаетесь закрыть или открыть дверь. При эксплуатации кузова автомобиля появляются микротрещины покрытия. Это недостатки данного метода защиты от коррозии. Спустя несколько лет началась новая эра в защите от коррозии. В настоящее время можно использовать гораздо лучший, более эффективный и дешевый метод — катодную защиту от коррозии, которая сейчас широко известна как 9.0377 оцинковка. Стальные поверхности покрыты цинком или горячим цинкованием.
Как видно во многих местах лакокрасочное покрытие истерто или поцарапано рабочими частями или всевозможными пластиковыми элементами или проводами. Другой факт, что кузов автомобиля тоже работает все время, что часто можно увидеть, когда вы поднимаете автомобиль с помощью домкрата и пытаетесь закрыть или открыть дверь. При эксплуатации кузова автомобиля появляются микротрещины покрытия. Это недостатки данного метода защиты от коррозии. Спустя несколько лет началась новая эра в защите от коррозии. В настоящее время можно использовать гораздо лучший, более эффективный и дешевый метод — катодную защиту от коррозии, которая сейчас широко известна как 9.0377 оцинковка. Стальные поверхности покрыты цинком или горячим цинкованием.
Этот метод намного эффективнее обычных методов,
нет необходимости герметизировать металлическую поверхность. Цинк как металл
с более низким электрическим потенциалом концентрирует все электрохимические
реакции, обычно известные как коррозия или ржавчина. Наши устройства
Наши устройства
работают по тому же принципу антикоррозийной защиты, они являются
альтернативой автомобилям без гальванического покрытия после аварий, а так же
дополнительная защита по истечении гарантийного срока, когда
стерто цинковое покрытие. К сожалению, при износе цинкового покрытия из-за постоянного воздействия коррозии, а также при ремонте автомобиля и отсутствии предварительной оцинковки изделия или повреждении цинкового слоя при сварке или шлифовке, эти детали подвержены быстрому износу. коррозия.
В связи с этим мы создали систему активной катодной защиты от коррозии ACCP, в которой поляризация с использованием электрического тока вызывает гораздо большую разницу потенциалов и позволяет точечную установку. Представленное устройство предназначено для защиты любого автомобиля с питанием 12В — ведь такое напряжение равно
нужен. Устройство сконструировано таким образом, что абсолютно безопасно для электронной системы автомобиля и всех установленных устройств.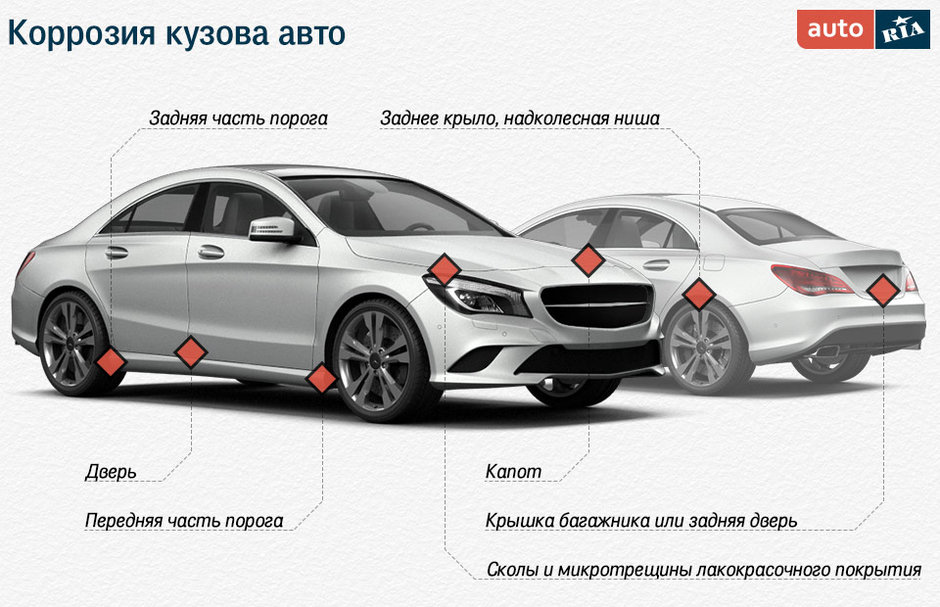 Потребляемая мощность минимальна -12 мА.
Потребляемая мощность минимальна -12 мА.
Устройство легко устанавливается. Обычно рекомендуемые места — сливной желоб
под капотом и дверью багажника.
Там прикручиваем или приклеиваем электроды. Инструкции по установке вы получите по электронной почте после покупки вместе с устройством в упаковке. Он также доступен во вкладке «Установка».
Установка
Устройство не влияет на приёмники и установки
в автомобиле.
Низкое энергопотребление. По нашим замерам
это на 11-12 мА меньше, чем у штатной автосигнализации.
Установка в автомобиле
Для обеспечения наиболее эффективной и безотказной работы устройства рекомендуется закрепить электроды (стержни на концах кабелей) к кузову автомобиля непроводящим способом, например нейлоновым тросом тугой или непроводящий пластиковый винт (наиболее рекомендуется). Острым инструментом сделайте под электродом глубокую царапину длиной 2-3 см и шириной 2 мм до голого металла. В конце концов, вы можете использовать металлический винт, но он должен быть из нержавеющей стали или латуни. Следите за тем, чтобы электрод располагался на ровной поверхности тела и закрывал ранее сделанную царапину. Ни в коем случае нельзя очищать всю поверхность под электродом! Дождевая вода должна пройти через электрод. Ни в коем случае нельзя его закреплять или консервировать! Рекомендуем затереть всю поверхность крупнозернистой наждачной бумагой. В катодном методе аноды берут на себя процесс электрохимической реакции, которая представляет собой коррозию. Из-за этого нужно время от времени проверять состояние электродов и, если они сильно заржавели, заменять их новыми. Обычно это алюминиево-магниевые, цинко-магниевые, цинковые или алюминиево-цинковые стержни, которые захватывают кабели. Провода зажимаются электродами. Обязательно закрепите соединение между кабелем и электродом. Мы рекомендуем приобрести новые электроды. От нас вы получите их с проводами, просто отрежьте старые и припаяйте новые электроды.
В конце концов, вы можете использовать металлический винт, но он должен быть из нержавеющей стали или латуни. Следите за тем, чтобы электрод располагался на ровной поверхности тела и закрывал ранее сделанную царапину. Ни в коем случае нельзя очищать всю поверхность под электродом! Дождевая вода должна пройти через электрод. Ни в коем случае нельзя его закреплять или консервировать! Рекомендуем затереть всю поверхность крупнозернистой наждачной бумагой. В катодном методе аноды берут на себя процесс электрохимической реакции, которая представляет собой коррозию. Из-за этого нужно время от времени проверять состояние электродов и, если они сильно заржавели, заменять их новыми. Обычно это алюминиево-магниевые, цинко-магниевые, цинковые или алюминиево-цинковые стержни, которые захватывают кабели. Провода зажимаются электродами. Обязательно закрепите соединение между кабелем и электродом. Мы рекомендуем приобрести новые электроды. От нас вы получите их с проводами, просто отрежьте старые и припаяйте новые электроды. Конечно, тех, что шли в комплекте с устройством, должно хватить надолго, не менее 24 месяцев. Мы устанавливаем их в местах, где они контактируют с электролитом, которым является дождевая вода и т. д. Это очень важно в катодном методе. Протекторы должны соприкасаться с погодными условиями, что означает размещение их спереди в моторном отсеке, т.е. в водостоке – в водосточном желобе крыла, сзади в водостоке, а также – в водосточном желобе багажника и т. д.
Конечно, тех, что шли в комплекте с устройством, должно хватить надолго, не менее 24 месяцев. Мы устанавливаем их в местах, где они контактируют с электролитом, которым является дождевая вода и т. д. Это очень важно в катодном методе. Протекторы должны соприкасаться с погодными условиями, что означает размещение их спереди в моторном отсеке, т.е. в водостоке – в водосточном желобе крыла, сзади в водостоке, а также – в водосточном желобе багажника и т. д.
Перед установкой зашлифуйте электрод крупнозернистой наждачной бумагой со всех сторон! Также вам придется просверлить отверстие в электроде. Диаметр и место отверстия зависит от места установки.
Установка двух устройств
Во избежание волочения кабелей по автомобилю мы предлагаем установить одно устройство спереди, а второе сзади и с обеих сторон.
Установка на мотоцикле
В основном состоит из затягивания соединительных электродов в двух удаленных электропроводящих местах тела, например. передняя вилка и задний рокер. Для обеспечения наиболее эффективной и безотказной работы устройства рекомендуется закрепить электроды (штанги на концах тросов) к кузову автомобиля с помощью нейлонового троса или ремешка на липучке для быстрого отсоединения и движения. Также Вы можете подключить его постоянно в невидимых местах. Не забудьте подключить напрямую к аккумулятору велосипеда. При длительном неиспользовании рекомендуем подключить аккумулятор к зарядке.
Для обеспечения наиболее эффективной и безотказной работы устройства рекомендуется закрепить электроды (штанги на концах тросов) к кузову автомобиля с помощью нейлонового троса или ремешка на липучке для быстрого отсоединения и движения. Также Вы можете подключить его постоянно в невидимых местах. Не забудьте подключить напрямую к аккумулятору велосипеда. При длительном неиспользовании рекомендуем подключить аккумулятор к зарядке.
Красный
провод (питание) аккумулятор +
Зеленый
и желтый (масса) аккумулятор —
Важно!
Устройство должно работать непрерывно.
Подключить на постоянной основе к постоянному источнику питания 12 В! Не с зажиганием!
Что касается самой коробки
, то устанавливайте ее в салоне автомобиля, где-нибудь на борту кабины или в любом другом удобном месте в качестве автосигнализации. На коробке постоянно горит один светодиод. Так как это импульсное устройство, то при его работе импульсы начинают появляться на втором диоде, расположенном внутри коробки.
Сколько устройств требуется вашему автомобилю для оптимальной защиты?
Маленькие автомобили до 5 лет (например, размер Toyota IQ) Квадроциклы Трайк: 1 или более устройств
Небольшие автомобили старше 5 лет, все отремонтированные или слегка поврежденные автомобили, средние и большие автомобили, фургоны: минимум 2 или более устройств
Внедорожники: 2 устройства для шасси и 1 или 2 для рамы (опционально)
Мотоциклы: 1 устройство
Часто задаваемые вопросы
1. Моей машины нет в таблице, не знаю
сколько устройств заказывать?
Таблица обновляется не часто, даже если бы она была
, нам бы пришлось поместить туда все марки автомобилей мира. Мы можем сравнить размер
нашего автомобиля с указанными в таблице и заказать такое же количество устройств. В
В
случае подержанного автомобиля, более старого автомобиля с существующей коррозией или с ремонтом листового металла
, пожалуйста, свяжитесь с нами относительно оптимального количества систем, которые следует купить
.
2. Поможет ли прибор вообще, если автомобиль
имеет следы коррозии?
Да, конечно. После многолетнего опыта мы знаем, что устройства
идеально подходят для автомобилей с уже имеющейся коррозией.
Они определенно замедляют его дальнейшее развитие даже до полной остановки (это
зависит от текущего количества коррозии в автомобиле).
3. Могу ли я просверлить отверстие в электроде, чтобы прикрутить его
?
Да. Мы рекомендуем крепить электроды
винтом или болтом. Мы предлагаем использовать винты из нержавеющей стали или латуни или болты
.
4. У моей машины пластиковые крылья. Куда
прикрутить электрод?
В такой ситуации можно изменить место установки
. Сливные желоба являются оптимальным местом для монтажа
Сливные желоба являются оптимальным местом для монтажа
, однако, когда этого требует ситуация, вы можете установить электроды
, например. под бампером в месте, которое не видно или в каком-нибудь
другом месте, где электрод будет контактировать с внешней
средой и желательно с дождевой водой.
Обратите внимание, что пластиковые крылья
также прикручены к металлическим элементам, поэтому, если электрод прикручен к внутреннему элементу
через пластиковое крыло, также будет правильно, если вы сохраните
электрическое соединение между электродом и кузовом автомобиля.
5. Как установить 2 устройства? Обязательно ли
устанавливать по одному с каждой стороны автомобиля или можно их
установить спереди и сзади?
Оба случая обеспечивают правильную установку. Пожалуйста,
установите их наименее трудоемким способом. Если у вас есть питание в багажнике, то
не имеет смысла тянуть все кабели с передней части автомобиля. В таком корпусе
В таком корпусе
вы должны установить одно устройство спереди, а другое сзади
вашего автомобиля. Если удобнее установить устройства с каждой стороны, используя один блок питания
для обоих устройств, пожалуйста, установите их таким образом.
6. Куда крепить блок с электроникой?
Настоятельно рекомендуем устанавливать модуль электроники
внутри автомобиля в сухом месте, как и сигнализацию, иммобилайзеры
и т.д.
Этого не может быть, если автомобильный аккумулятор
полностью исправен. Благодаря импульсному режиму наш прибор имеет минимальное потребление энергии
12 мА (столько же, сколько потребляют аналоговые часы в автомобиле).
8. В моем автомобиле установлена газовая установка LPG.
Может ли устройство нарушить свою работу?
Абсолютно нет, наши устройства полностью
безвредны для газовой и любых других систем вашего автомобиля и не вызывают
взаимодействия.
9. У меня в машине есть аудио и видео система.
У меня в машине есть аудио и видео система.
Может ли устройство мешать приему?
Нет, наши устройства
не вызывают помех в аудио- и видеосистемах автомобилей.
10. Может ли ваше устройство мешать моему радио CB
?
Нет, наша система не вызывает
помех в правильно установленных передающих и приемных устройствах, включая
CB-радио.
11. Мне нужно отремонтировать и сварить листовой металл,
нужно ли снимать систему?
Да, нужно снять электроды
и отключить питание.
12. Как часто нужно менять электроды
и где их купить?
Электроды следует заменять, если они
сильно изношены. Если электроды имеют коррозию на поверхности, их следует очистить от окислов с помощью проволочной щетки или наждачной бумаги и снова прикрепить. если они
слишком изношены, чтобы их можно было использовать дальше, их необходимо заменить новыми
. Этот срок зависит от многих факторов, размеров транспортного средства и условий его эксплуатации, но он не должен быть меньше примерно двух лет. Вы можете
Этот срок зависит от многих факторов, размеров транспортного средства и условий его эксплуатации, но он не должен быть меньше примерно двух лет. Вы можете
совершить покупку в нашей компании, воспользовавшись формой покупки или любым из доступных вариантов.
13. Моя машина полностью сделана из алюминия.
Мне нужно ваше устройство?
Конечно, алюминий подвержен коррозии, как и любой другой
металл. Основной причиной использования этого металла в автомобилях является значительное снижение веса
. Наша система эффективно защищает автомобили из алюминия
так же, как и автомобили из стали. Среди наших клиентов есть владельцы таких автомобилей
из алюминия, как Audi A8, как Aston Martin DB9.
14. У меня возникла проблема с перетаскиванием кабеля электрода
в заднюю часть автомобиля. Электрод слишком толстый, что делать
?
В таком случае можно перерезать кабель и
пропустите его через узкие щели.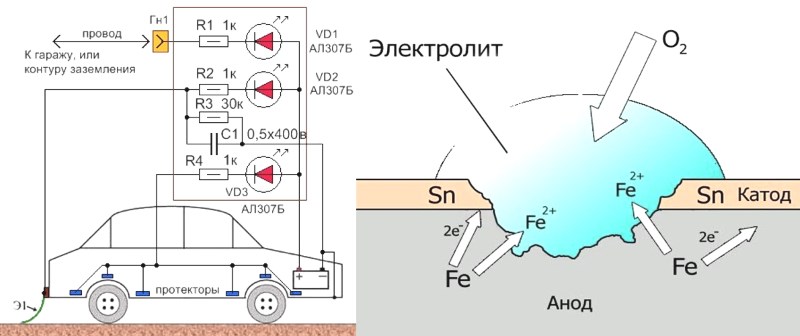 Не забудьте пропаять и изолировать соединение после
Не забудьте пропаять и изолировать соединение после
.
15. Можно ли укоротить кабель электрода? Я
установил два устройства спереди и сзади. Один из кабелей
слишком длинный, можно ли его обрезать?
Конечно, это даже рекомендуется, так как слишком длинный кабель
обычно скручивается или преломляется, что отрицательно влияет на эффективность электрода
. В любом случае уменьшения длины припаять и изолировать
суставы.
16. Мне кажется, что один электрод
не подвергается коррозии, на другом есть следы коррозии. Что-то не так подключено
?
Проверить соединение между электродом
и защищаемым объектом. Должно быть хорошее электрическое соединение.
Также следует проверить, не скручен ли кабель
и не образует ли он виток и не порвался ли он. В обоих случаях это может привести к серьезному ухудшению характеристик электрода.
Купить ржавчин-стоппер
Контакт
Почему не так, как они использовались? — Auto Expert Джона Кадогана
Помните, как сильно ржавчина съедала автомобили 60-х и 70-х годов? Эта проблема ушла незаметно. Вы когда-нибудь задумывались, почему?
Вы когда-нибудь задумывались, почему?
Я помогу вам сэкономить ТЫСЯЧИ на ЛЮБОМ НОВОМ ТРАНСПОРТНОМ СРЕДСТВЕ. Нажмите ЗДЕСЬ >>
Вот вопрос от Энтони:
«Одной из причин для покупки Hyundai или Kia является неограниченный пробег гарантии. Производители делают ставку на то, что автомобили будут защищены от дефектов независимо от пройденного расстояния в течение пяти или семи лет. Мой вопрос касается гарантии на металлический корпус. Исходя из моих базовых знаний по химии, могу ли я сказать, что в этих автомобилях используется расходуемый анод из цинка точно так же, как бытовой водонагреватель или Сиднейский оперный театр защищены расходуемым анодом от коррозии? Или дело в том, что сталь Hyundai или Kia изготовлена лучше?»
Я помогу вам сэкономить ТЫСЯЧИ на ЛЮБОМ НОВОМ АВТОМОБИЛЕ. Нажмите ЗДЕСЬ >>
Оцинкованная сталь
В течение последних 30 лет автомобили подвергались гальванизации. Быстрая грунтовка на цинкование >>
Быстрая грунтовка на цинкование >>
По крайней мере, сталь, используемая для изготовления основных панелей, была. Я говорю о развитом мире. Даже сегодня многие автомобили, произведенные для внутреннего рынка Китая и Индии, не оцинкованы и продолжают работать так же, как автомобили здесь в 19 году.70-х, то есть они очень легко ржавеют. Вы получаете эти пузыри ржавчины уже через несколько лет.
Современные автомобили, похоже, этого не делают, и они не делали этого уже 30 лет.
Очень легко понять, почему. Это потому, что сталь, используемая для производства современных автомобилей, подвергается горячему цинкованию прямо в конце процесса производства стали. По сути, гальванизация — это тот «жертвенный анод», о котором говорит Энтони.
Однако они не используют большой толстый кусок цинка, привинченный к корпусу, как в случае с кораблем, нефтяной вышкой или очень длинным трансконтинентальным нефтепроводом. Вместо этого они используют тонкое покрытие из цинка.
Я помогу вам СЭКОНОМИТЬ ТЫСЯЧИ НА ЛЮБОМ НОВОМ ТРАНСПОРТНОМ СРЕДСТВЕ. Нажмите ЗДЕСЬ >>
Абсолютная жертва? Цинк встречается с железом
Вместо этого они покрывают всю поверхность стали очень тонким слоем цинка. Это не только лишает стальную поверхность какого-либо взаимодействия с кислородом воздуха, но также происходит электролитическая реакция между цинком и железом в стали.
Поскольку цинк более активен, чем основная сталь, цинк жертвует собой, чтобы сталь прослужила дольше.
Подробнее об этом «катодная защита» >>
Это не означает, что сталь не подвержена коррозии. Это действительно зависит от условий эксплуатации стали. Цинк будет защищать сталь до тех пор, пока он доступен. Итак, если вы живете в части мира (на ум приходит Северная Америка — северные части Северной Америки, где зимой действительно очень холодно), где на дорогах используется много соли, недостатком этого является эта соль является действительно хорошим электролитом и ускоряет процесс коррозии. Подробнее в Википедия >>
Подробнее в Википедия >>
Таким образом, если в Австралии цинка хватит примерно на 20-30 лет, то в Северной Америке цинка хватит только на 5-10 лет. Это действительно зависит от окружающей среды.
Я помогу вам сэкономить ТЫСЯЧИ на ЛЮБОМ НОВОМ ТРАНСПОРТНОМ СРЕДСТВЕ. Нажмите ЗДЕСЬ >>
Цинк против олова
Цинк пожертвует собой, чтобы сталь могла жить до тех пор, пока есть цинк. Это сильно отличается от банки с едой, к которой мы все привыкли, в кладовой. Они используют олово на внешней стороне жестяной банки.
Существенное различие между оловом и цинком заключается в том, что олово менее активно, чем лежащее в основе железо. Олово не может обеспечить такую же защиту стали, как цинк. Наоборот, на самом деле.
Когда вы думаете о жестяной банке, функция олова состоит в том, чтобы покрыть сталь и предотвратить доступ к ней кислорода. Если вы поцарапаете сталь или есть какие-либо дефекты, которые проникнут через олово, сталь начнет ржаветь. Не только это; он ржавеет намного быстрее, чем ржавел бы без олова.
Не только это; он ржавеет намного быстрее, чем ржавел бы без олова.
Поскольку железо является наиболее активной частью всей конструкции жестяной банки, железо жертвует собой, чтобы олово могло жить дольше. Это именно то, чего вы не хотите, когда дело доходит до автомобилей. (Кроме того, я бы не стал использовать старые жестяные банки для чего-либо на открытом воздухе, что должно быть устойчивым к коррозии, потому что, проще говоря, этого не произойдет.)
Я помогу вам сэкономить ТЫСЯЧИ на ЛЮБОМ НОВОМ ТРАНСПОРТНОМ СРЕДСТВЕ. Нажмите ЗДЕСЬ >>
Алюминий против стали: Industries at War
Рискуя слишком углубиться в тему, которая может стать чудодейственным лекарством от бессонницы, которое мы все искали, есть некоторые интересные вещи, происходящие со сталями, которые они используют. в авто, а оцинковка идет прямо сейчас.
Вы можете подумать, что инженеры — это целая кучка пропеллеров, целый день занимающихся расчетами. Однако на самом деле их целая куча, например, лоббируют интересы алюминиевой, цинковой или сталелитейной промышленности. Алюминиевая промышленность и сталелитейная промышленность обычно находятся в состоянии войны друг с другом.
Однако на самом деле их целая куча, например, лоббируют интересы алюминиевой, цинковой или сталелитейной промышленности. Алюминиевая промышленность и сталелитейная промышленность обычно находятся в состоянии войны друг с другом.
Сейчас так и есть.
Каждый раз, когда вы смотрите в небо и видите проплывающий мимо Боинг 787 Dreamliner, вы понимаете, что он сделан преимущественно из композитных материалов (углеродного волокна и тому подобного). Флот 787-х в небе означает тысячи тонн алюминия, которые НЕ перевозят людей. Весь этот алюминий и промышленность, которая его производит, ищут, куда бы пойти дальше.
Вот почему новый пикап Ford F-150 сделан преимущественно из алюминия. С точки зрения объема это сильно отличается от Audi A8, S-класса или E-класса Benz, потому что в производстве так много F150 — около 700 000 в год.
Слишком много алюминия вместо стали. Конечно, это также влияет на прочность и сложность ремонта. Посмотрите видео ниже: Парни из Edmunds. com купили F-150 за 50 тысяч долларов и ударили по нему кувалдой дважды, как и вы, чтобы проверить это…
com купили F-150 за 50 тысяч долларов и ударили по нему кувалдой дважды, как и вы, чтобы проверить это…
Я помогу вам сэкономить ТЫСЯЧИ на ЛЮБОМ НОВОМ ТРАНСПОРТНОМ СРЕДСТВЕ. Нажмите ЗДЕСЬ >>
F-150: алюминиевый корпус серийного производства
F-15 телесного цвета (вверху)
Зачем использовать алюминий?
Алюминий используется потому, что он намного легче. Вы думаете про себя: Что делает сталелитейная промышленность и что вообще делает автомобильная промышленность?
Что им нужно сделать, так это достичь своих целей по экономии топлива. Самый простой способ сэкономить топливо — сделать автомобили легче. Чем меньше масса, тем меньше энергии для ее перемещения.
Но если вы хотите автомобиль размером с внедорожник, Yaris вам точно не понравится. Таким образом, регулирующие органы не могут принимать законы, касающиеся: Новые правила: теперь все будут ездить на микроавтомобилях .
Потому что это не сработает.
Перед автопроизводителями стоит задача сделать автомобили такого же размера или даже большего размера, но при этом достичь целей по экономии топлива, которых хотят регулирующие органы и ожидают потребители. Другими словами, более низкий расход топлива без ущерба для веса, производительности или размера автомобиля.
То, что они делают сейчас, заключается в том, чтобы перейти от стали, используемой в кузове, толщиной 0,9– 1 мм, и попытаться уменьшить толщину примерно до 0,5 мм. Это кажется достаточно простым заданием, но на самом деле это не так.
Я помогу вам СЭКОНОМИТЬ ТЫСЯЧИ НА ЛЮБОМ НОВОМ ТРАНСПОРТНОМ СРЕДСТВЕ. Щелкните ЗДЕСЬ >>
Изменение состава сплава
Если вы не измените состав стали коренным образом, она не будет достаточно прочной, если вы сделаете ее тоньше.
Вы должны изменить сплав. В сталь можно положить целую кучу интересного. Вы можете использовать хром и молибден и сделать эту хромомолибденовую сталь. Однако хроммолибден, как правило, дорог, и в контексте массового производства миллионов автомобилей каждый год это не будет экономически выгодно.
Однако хроммолибден, как правило, дорог, и в контексте массового производства миллионов автомобилей каждый год это не будет экономически выгодно.
Вместо них используют кремний и марганец, которые являются гораздо более доступными легирующими элементами. Эти сплавы могут обеспечить необходимую прочность, но не такая уж маленькая проблема заключается в том, что когда вы отжигаете сталь после ее изготовления, она окисляет кремний.
Оксиды кремния в основном представляют собой песок. И эти оксиды тяготеют к внешней стороне стального листа. Таким образом, вы получаете тонкий стальной лист, покрытый песком, и цинк к нему не прилипнет. Это очень плохо с точки зрения оцинковки.
Тогда вам нужно изменить состав стали и использовать целую кучу интересной металлургии. Я не знаю точно, как они это делают — возможно, это коммерческая тайна.
В основном, они разрабатывают металлургию таким образом, чтобы сталь можно было отжигать при низкой температуре, такой как 640 градусов C. Чем ниже температура, тем меньше вероятность того, что силикон в стали окислится в процессе отжига (и гальванизация не вызовет этого, потому что это происходит при температуре плавления цинка, которая составляет «всего» около 420 градусов по Цельсию.0003
Чем ниже температура, тем меньше вероятность того, что силикон в стали окислится в процессе отжига (и гальванизация не вызовет этого, потому что это происходит при температуре плавления цинка, которая составляет «всего» около 420 градусов по Цельсию.0003
Я помогу вам СЭКОНОМИТЬ ТЫСЯЧИ НА ЛЮБОМ НОВОМ ТРАНСПОРТНОМ СРЕДСТВЕ. Нажмите ЗДЕСЬ >>
Металлургия для чайников
Когда мы говорим об отжиге стали, мы снимаем с нее напряжение, чтобы с ней было легче работать.
При производстве стали ее раскатывают, как тесто для хлеба, только значительно горячее, и сворачивают в рулон, чтобы облегчить транспортировку. Но они также помещают его в печь и нагревают до точки, где он отжигает, а затем вы даете ему остыть контролируемым образом, постепенно.
Это снижает внутренние напряжения и изменяет структуру кристаллизации внутри стали. Итог: с ним становится намного легче работать.
Остается стальной лист, который легко и красиво раскатывается и принимает форму с хорошей податливостью. Он выдержит все требования, связанные с вдавливанием этих четких линий разреза в корпус и складыванием его по этим узким радиусам, чтобы получить все эти гладкие края и изгибы.
Он выдержит все требования, связанные с вдавливанием этих четких линий разреза в корпус и складыванием его по этим узким радиусам, чтобы получить все эти гладкие края и изгибы.
Я помогу вам сэкономить ТЫСЯЧИ на ЛЮБОМ НОВОМ ТРАНСПОРТНОМ СРЕДСТВЕ. Нажмите ЗДЕСЬ >>
Задача
для стали
Реальная проблема, стоящая перед сталелитейной промышленностью, заключается в том, что они борются за алюминий. Алюминий проигрывает композитам (которые все чаще используются в авиации и других технологических отраслях).
Камни для соревнований.
В конечном счете, победителем станете вы, потребитель, потому что вы получите более легкую машину того же размера, которая будет обеспечивать желаемые характеристики и иметь достаточно места внутри.
Тоже не заржавеет 20-30 лет.
Вы можете поспорить на свой последний доллар, что цинковая промышленность будет очень активно лоббировать в таких странах, как Китай и Индия, где они до сих пор не гальванизируют свои автомобили.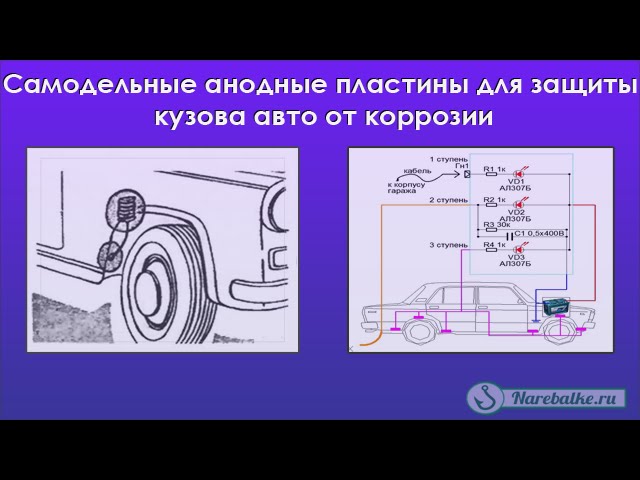 Для них это важно, потому что это огромная индустрия. Количество цинка, используемого для защиты вашего нового автомобиля и любого другого автомобиля, произведенного и проданного в этом году в развитых странах, составляет около 120 000 тонн.
Для них это важно, потому что это огромная индустрия. Количество цинка, используемого для защиты вашего нового автомобиля и любого другого автомобиля, произведенного и проданного в этом году в развитых странах, составляет около 120 000 тонн.
Это ошеломляющая сумма. Вы можете поспорить, что это большой, жирный, корыстный коммерческий интерес — и они не собираются сдаваться в игре без боя. Выезд как сильно они дерутся >>
Я помогу вам сэкономить ТЫСЯЧИ на ЛЮБОМ НОВОМ ТРАНСПОРТНОМ СРЕДСТВЕ. Нажмите ЗДЕСЬ >>
ЗАКЛЮЧЕНИЕ
Если вы когда-нибудь задумывались, почему ваша машина сегодня не ржавеет так, как это делали Kingswood, Falcons, Toranas или Geminis, или почему мы больше не получаем эти ржавые волдыри, и почему автомобили служат намного дольше без рак ржавчины, это потому, что они были оцинкованы в течение почти 30 лет.
Если вы живете в Канаде или где-то в этом роде и кричите на экран компьютера, говоря, что я не прав, это просто потому, что у вас есть цинк против соли, и в конечном итоге цинк проиграет.
Надеюсь, я не усыпил вас тайной жизнью металлов в автомобилях. Надеюсь, вы чему-то научились. Если у вас есть, вы можете подписаться на мой канал YouTube >>
Я помогу вам сэкономить ТЫСЯЧИ на ЛЮБОМ НОВОМ ТРАНСПОРТНОМ СРЕДСТВЕ. Нажмите ЗДЕСЬ >>
БОЛЬШЕ ОТЧЕТОВ
Джон Кадоган tech26 Комментарии
0 лайков
Коррозия металлов в автомобильных деталях
Точно так же, как атмосферная среда, коррозионная активность которой различается в зависимости от того, где люди находятся в мире, то же самое относится и к коррозии металлов в автомобильных деталях : например, в Швеции автомобильная среда довольно агрессивный из-за влажного климата и использования солей против обледенения, вызывающих коррозию металлов.
Коррозия – естественный процесс, переводящий металлы в более устойчивую форму, это постепенное разрушение материалов вследствие химической или электрохимической реакции с окружающей средой.
Что такое коррозия в деталях?
Большинство металлов нестабильны в естественных или промышленных условиях; по этой причине они возвращаются к своей прежней форме: этот процесс называется коррозией.
Параметры электрохимической коррозии связаны с проводящим материалом, которым является металл, ионопроводящей средой, которой обычно является вода, анодной и катодной реакцией. Коррозия металла обусловлена сопряженными анодными и катодными реакциями, которые происходят на границе раздела между металлом и водной средой.
Существуют различные виды коррозии: ниже мы собираемся объяснить, что такое коррозия металла в автомобильных деталях, и подробно проанализировать ее.
Прежде всего, мы объясним различные типы коррозии, затем сосредоточимся на различиях между каждой средой и на том, какая будет приблизительная скорость коррозии.
Типы коррозии
В зависимости от природы металла и окружающей среды могут возникать различные типы коррозии.
Виды коррозии:
- Равномерная коррозия
- Гальваническая коррозия
- Питтинговая коррозия
- Щелевая коррозия
- Коррозия отложений
Равномерная коррозия
Это самый важный вид коррозии: его характеристикой является скорость коррозии примерно по всей открытой поверхности.
Гальваническая коррозия
Гальваническая коррозия возникает, когда два разных металла вступают в контакт с электролитом, присутствующим на поверхности. Более благородный металл действует как катод, а менее благородный — как анод. Более благородный металл защищен от коррозии, а менее благородный — нет.
Питтинговая коррозия
Этот вид коррозии возникает на пассивированных металлах, подвергающихся воздействию водных растворов, содержащих агрессивные добавки. Пассивный слой разрушается агрессивной добавкой и при растворении металла в нем образуется полость, которая является анодной зоной, а пассивированная металлом область выполняет роль катода.
Щелевая коррозия
Когда на поверхности образуется небольшая щель, металл внутри нее подвергается воздействию более агрессивной среды из-за истощения кислорода, подкисления или повышения концентрации ионов CI (хлорид-ионов). Если нет кислорода для повторной пассивации поверхности, пассивный слой может разрушиться, и металл в щели подвергнется коррозии.
Коррозия отложений
Причиной коррозии отложений является задержка воды под отложениями. Из-за этой ситуации часто возникает коррозионная среда, например, под дорожной грязью, для открытых частей автомобиля.
Коррозионная среда
Существуют различные среды, связанные с различными типами коррозии, такие как сельская, морская, промышленная, городская и автомобильная. В частности, мы собираемся глубоко проанализировать взаимосвязь между коррозией металла в автомобильных деталях и окружающей средой.
Сельская атмосфера
Низкие количества загрязняющих веществ со скоростью осаждения SO A <10 мг/м 2 и NaCl<5 мг/м 2. Ориентировочная скорость коррозии: 0,2 – 2 мкм/год.
Ориентировочная скорость коррозии: 0,2 – 2 мкм/год.
Морская атмосфера
Высокое количество хлоридов со средней годовой скоростью осаждения NaCl от 5 до 500 мг/м 2 каждый день и до 1500 мг/м 2 день при большом количестве воздействия моря спрей. Приблизительная скорость коррозии: 0,5/8 мкм/год.
Промышленная атмосфера
Может содержать различные виды загрязняющих веществ и имеет высокую скорость осаждения SO 2 , до 200 мг/м 2 в день. Приблизительная скорость коррозии: 1-16 мкм/год.
Городская атмосфера
Большое количество SO 2 и сажа со скоростью осаждения SO 2 B 10-80 мг/м 2 день. Приблизительная скорость коррозии: 1-16 мкм/год.
Автомобильная среда
Автомобильная среда довольно агрессивна и вызывает коррозию металла в автомобильных деталях из-за высокого уровня загрязнения и из-за солей против обледенения. SAE, Общество инженеров-автомобилестроителей, оценило скорость коррозии покрытия примерно в 8,5 мкм/год. Это тот же диапазон, что и в морской среде.
SAE, Общество инженеров-автомобилестроителей, оценило скорость коррозии покрытия примерно в 8,5 мкм/год. Это тот же диапазон, что и в морской среде.
Дорожная грязь
Существует много дорожной грязи, которая может прилипнуть к открытым металлическим поверхностям, таким как автомобильные детали, и вызвать коррозию. Когда эта грязь или пыль осаждаются на поверхности компонентов, увеличивается TOW C (время увлажнения). Участок под этим отложением может выступать в качестве анода, а неотложенный — в качестве катода.
Противообледенительные соли
Эти особые соли используются для снижения температуры таяния снега и льда на дорогах, чтобы увеличить сцепление между шинами и дорогой.
Одной из наиболее часто используемых противогололедных солей является хлорид натрия (NaCl), поскольку именно этот раствор обладает сильным коррозионным действием.
Подводя итоги, во время литья под давлением важно глубоко проанализировать использование и применение продуктов, чтобы скорректировать их функциональные требования перед производством, чтобы повысить их коррозионную стойкость и избежать любых возможных проблем с функциональными или эстетическими аспектами.
Таким образом, одним из наиболее распространенных способов защиты транспортных средств от коррозии является нанесение защитных покрытий на поверхность. По сути, обработка поверхности литья под давлением представляет собой промышленный процесс, позволяющий модифицировать поверхность изделий с целью улучшения их функциональных и эстетических характеристик. Действительно, с обработкой поверхности машина для литья под давлением может решить и предотвратить любые дефекты, вызванные внешними факторами, такими как, например, коррозия.
Кроме того, чтобы получить продукт, соответствующий требованиям клиентов, необходимо иметь идеальное литье с правильной производственной конструкцией и поверхностью без каких-либо дефектов, связанных с этапом литья под давлением.
Для получения всех этих спецификаций решающее значение имеет сотрудничество между дизайнером и заказчиком: это сотрудничество создает услугу совместного проектирования. На самом деле, благодаря совместному проектированию и его первому этапу, называемому анализом моделирования, дизайнеры могут предложить клиентам наилучший способ действий, чтобы избежать любых возможных проблем в будущем.
