Чем химическая коррозия отличается от электрохимической коррозии: Чем химическая коррозия отличается от электрохимической?
Содержание
Коррозия металлов — презентация онлайн
Похожие презентации:
Химические свойства металлов. Коррозия металлов
Электрохимическая коррозия металлов
Коррозия металлов
Коррозия металлов и способы защиты от неё. (11 класс)
Коррозия металлов
Коррозия металлов
Коррозия материалов
Коррозия металлов
Коррозия металлов
Коррозия металлов
1. Коррозия металлов
Выполнила: ученица 11Б класса
Анна Абрамова
2. Обычно под коррозией металла понимают его окисление под влиянием кислот, которые присутствуют в растворах, контактирующих с
металлическим изделием, либо кислорода
воздуха. Коррозия наиболее часто поражает
металлы, находящиеся левее водорода в так
называемом ряду напряжений. Впрочем,
коррозионному разрушению подвержены и
многие другие материалы
(неметаллические), например строительный
бетон.
3. Виды коррозии
Химическая
коррозия
Электрохимическая
коррозия
4.
 Химическая коррозия. Под таким явлением понимают разрушение металла, вызываемое контактом коррозионной среды и материала.
Химическая коррозия. Под таким явлением понимают разрушение металла, вызываемое контактом коррозионной среды и материала.
Причем при подобном взаимодействии
наблюдается сразу два процесса:
— коррозионная среда восстанавливается;
— металл окисляется.
6. Электрохимическая коррозия металлов отличается от химической тем, что последняя протекает без электротока. А первопричина этих
видов коррозии, коей является
термодинамическая неустойчивость, остается
неизменной. Металлы легко переходят в
разные состояния (включая и более
устойчивые), причем в этом случае отмечается
снижение их термодинамического потенциала.
7. Существуют далее приведенные виды химической коррозии: — в жидких составах, которые не причисляются к электролитами; — газовая.
8. К жидкостям-неэлектролитам относят составы, неспособные проводить электроток: — неорганические: сера в расплавленном состоянии,
жидкий бром;
— органические: бензин, керосин, хлороформ
и иные.
9. Процесс химического ржавления чаще всего идет в пять этапов: 1. Сначала к поверхности металла подходит окислитель. 2. На
поверхности начинается хемосорбция реагента.
3. После этого начинает формироваться оксидная
пленка (взаимодействие металла и окислителя).
4. Десорбция материала и оксидов.
5. Фиксируется диффузия в жидкость-неэлектролит
оксидов.
10. Электрохимическая коррозия. Окислительно-восстановительная реакция, происходящая в средах, проводящих ток (в отличие от
химической коррозии). Процесс
происходит при соприкосновении двух
металлов или на поверхности металла,
содержащего включения, которые
являются менее активными
проводниками (это может быть и
неметалл).
11. На аноде (более активном металле) идет окисление атомов металла с образованием катионов (растворение). На катоде (менее
активном проводнике) идет
восстановление ионов водорода или молекул
кислорода с образованием соответственно
водорода Н2↑ или гидроксид-ионов ОН.
Катионы водорода и растворенный кислород —
важнейшие окислители, вызывающие
электрохимическую коррозию.
12. Скорость коррозии тем больше, чем сильнее отличаются металлы (металл и примеси) по своей активности (для металлов — чем дальше
друг от друга они расположены в ряду
напряжений). Значительно усиливается
коррозия при увеличении температуры.
Спасибо за внимание
15. Хемосорбция Поглощение одного вещества другим, сопровождающееся проявлением химических сил
← Назад
Хемосорбция
Поглощение одного вещества
другим, сопровождающееся
проявлением химических сил
16. Десорбция Процесс удаления адсорбированного вещества с поверхности адсорбента
← Назад
Десорбция
Процесс удаления
адсорбированного вещества с
поверхности адсорбента
English
Русский
Правила
Коррозия металлов. Виды и особенности. Защита и принцип действия
Коррозия металлов – это процесс разрушения металлической поверхности в результате неблагоприятного воздействия окружающей среды. Ее причиной является термодинамическая неустойчивость материала к влиянию различных веществ, которые с ним контактируют.
Ее причиной является термодинамическая неустойчивость материала к влиянию различных веществ, которые с ним контактируют.
Разрушение поверхностей наступает вследствие химического или электрохимического взаимодействия неблагоприятной среды. Обе разновидности являются одинаково пагубными для изделий из металла.
Химическая коррозия
Данный процесс осуществляется в среде, которая не производит передачу электрического тока. Он наблюдается, например, при нагреве, в результате чего осуществляется образование химических соединений, таких как сульфиды, а также различные виды пленок. Нередко образованные сплошные пленки становятся непроницаемыми и консервируют поверхность, поэтому последующая коррозия металлов останавливается. Такой защитный слой можно встретить на поверхности из алюминия, хрома, никеля и свинца. Пленка на стали или чугуне является непрочной, поэтому ее наличие не останавливает дальнейшее продвижение разрушения вглубь материала.
Химическая коррозия может быть двух видов:
- Газовой.

- Жидкостной.
Газовая возникает в результате действия агрессивной газовой среды или пара на поверхность металла, что сопровождается повышенными температурами. Благодаря горячей среде на поверхности отсутствует конденсат. В качестве газа может применяться кислород, диоксид серы, водяной пар, сероводород и так далее. Подобное коррозийное влияние может вызывать абсолютное разрушение активного металла, за исключением случаев, когда образуется защитная непроницаемая пленка.
Жидкостная коррозия металлов возникает в жидкостных средах, которые не способны передавать электричество. В первую очередь она наблюдается при контакте металлов с сырой нефтью, нефтепродуктами или смазочными маслами. При наличии в таких веществах небольшой доли воды, коррозия переходит в электрохимическую.
В обоих вариантах химической коррозии скорость разрушения является пропорциональной химической реакции, с которой окислитель проникает сквозь созданную оксидную пленку на поверхности.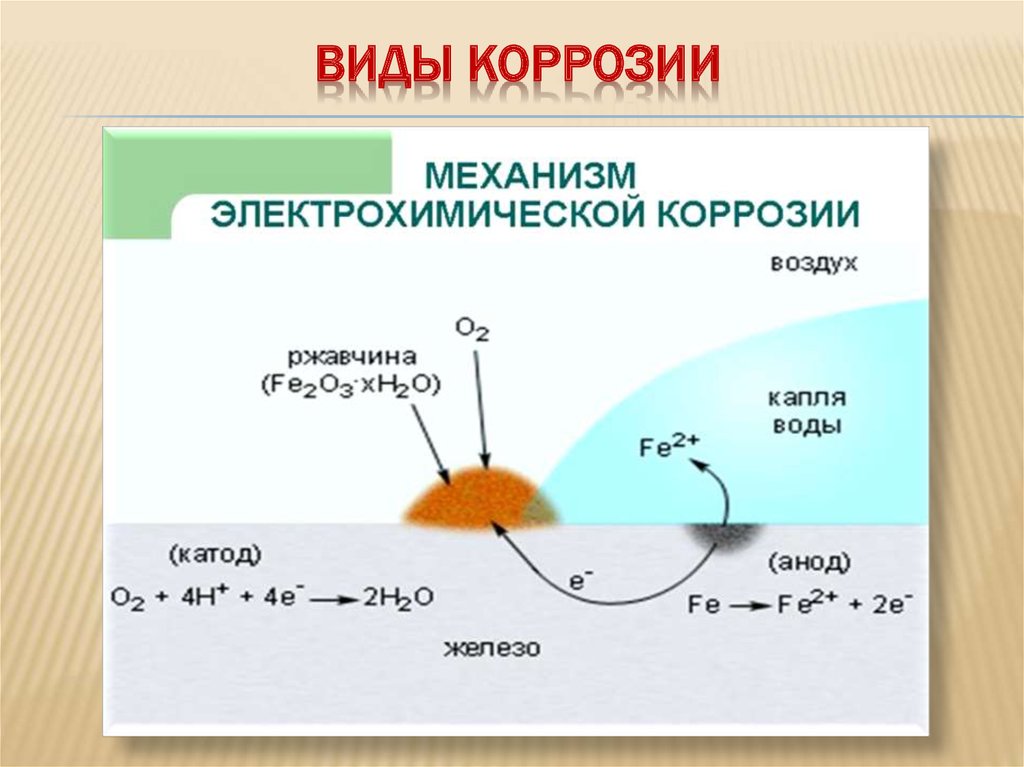
Электрохимическая коррозия металлов
Эта разновидность разрушения поверхности металла происходит в среде, которая может передавать электрический ток. В результате данного процесса наблюдается изменение состава металла. Атомы удаляются от кристаллической решетки в результате анодного или катодного воздействия. При анодном влиянии ионы металла переходят в раствор жидкости, которая его окружает. При катодном влиянии получаемые при анодном процессе электроны связываются с окислителем. Наиболее распространенной является электрохимическая коррозия под воздействием водорода или кислорода.
Процесс влияния электрохимической коррозии на металлы зависит от уровня их активности. По данному критерию их разделяют на 4 группы:
- Активные.
- Средней активности.
- Малоактивные.
- Благородные.
Активные имеют высокую нестабильность. Для них характерно возникновение коррозии даже в нейтральной водной среде, которая лишена растворенного кислорода или окислителей. Ярким представителем такого металла является кадмий.
Ярким представителем такого металла является кадмий.
Металлы средней активности располагаются на таблице химических элементов между кадмием и водородом. Они неподвержены началу разрушения в нейтральной жидкостной среде лишенной кислорода, но начинают интенсивно поддаваться коррозии при влиянии кислот.
Малоактивные металлы располагаются в таблице Менделеева между водородом и родием. Они не подвергаются влиянию коррозии при контакте с нейтральными жидкостями и кислой средой. Для активизации процесса их разрушения необходимо наличие кислорода или прочих окислителей.
Благородные металлы отличаются стабильностью, благодаря чему подвержены коррозии только при воздействии кислой среды при условии контакта с сильными окислителями. К перечню благородных металлов относится платина, золото, палладий и иридий.
Электрохимическая коррозия металлов является самой распространенной, поскольку естественные условия, в которых хранятся и эксплуатируются металлические изделия, зачастую подвержены влиянию влажной среды.
Различают следующие виды электрохимической коррозии:
- Электролитная – наблюдается при контакте с растворами солей, кислотами, оснований, в том числе и обычной водой.
- Атмосферная – наблюдается в условиях атмосферы, где содержатся испарения воды. Данный вид является самым распространенным, именно он влияет на практически все металлические изделия.
- Почвенная – наблюдается в результате воздействия влажной почвы, в составе которой могут содержаться различные химические элементы ускоряющие процесс разрушения металла. При воздействии с кислыми почвами процесс коррозии наблюдается наиболее агрессивно. Грунты с песком воздействуют медленней всего.
- Аэрационная – является более редкой и наблюдается в тех случаях, если к разным поверхностям металла оказывается неравномерный доступ воздуха. В результате неоднородного воздействия линии переходов между такими участками начинают разрушаться.
- Морская коррозия металлов подразумевает разрушение от влияния морской воды.
 Она выделяется в отдельную группу, поскольку данная жидкость отличается высоким содержанием солей и растворенных органических веществ. Это делает ее более агрессивной.
Она выделяется в отдельную группу, поскольку данная жидкость отличается высоким содержанием солей и растворенных органических веществ. Это делает ее более агрессивной. - Биокоррозия – данный вид разрушения возникает при условии воздействия на поверхность металла бактериями, которые в результате жизнедеятельности вырабатывают углекислый газ и прочие вещества.
- Электрокоррозия – такой вид разрушения металла наблюдается при воздействии на него блуждающих токов, что характерно для подземных сооружений, в частности рельсов метрополитена, стержней заземления, трамвайных линий и т.д.
Методы защиты от коррозии
Голая поверхность подавляющего большинства металлов склонна к быстрой коррозии, поэтому для снижения разрушающего воздействия применяются различные способы защиты.
Покрытие изоляционными слоями:
- Другим металлом.
- Цементным раствором.
- Лаками.
- Красками.
- Битумом.

Одним из самых эффективных способов защиты от коррозии является покрытие поверхности одного металла другим, менее склонным к коррозии. Примером такого технического решения является оцинковка, когда сталь защищается слоем цинка. Внутренний металл полностью изолирован до тех пор, пока цинк в результате естественной коррозии, которая протекает очень медленно, полностью не разрушится, оголив сталь. Такой метод защиты является одним из самых эффективных, поскольку покрывной металл полотна удерживается на основании, поэтому его невозможно срывать слоями. Недостаток метода заключается в том, что при механическом воздействии можно сцарапывать тонкую защитную пленку.
Покрытие металла защитным цементным раствором, битумом, лаками и красками является также очень распространенным решением, которое все же уступает оцинковке. Это связано с неоднородностью составов основания и покрытия. В результате низкой адгезии краски готовое покрытие будет отслаиваться. Такая защита может покрываться трещинами, обеспечивая доступ влаги.
Коррозия металлов может быть приостановлена при наличии химического покрытия:
- Оксидирование.
- Фосфатирование.
- Азотирование.
- Воронение.
- Цементация.
Поверхность металла подвергается влиянию различных веществ, фосфатов, азота или оксидов, в результате чего создаются пленки, которые благодаря своей непроницаемости предотвращают разрушение. Такие методы применимы в первую очередь для сталей. Также распространенным решением является воронение стали, когда поверхность металла взаимодействует с органическими веществами. Обработанные таким способом поверхности приобретают темный цвет, напоминающий крыло ворона, за что данный метод и получил свое название. Одним из наиболее эффективных вариантов химического покрытия является цементация, когда на поверхность воздействуют углеродом, в результате чего создается корка вступившего в реакцию металла.
Для защиты от коррозии черных металлов может применяться технология изменения их состава. Добавление различных соединений позволяет получить сплавы, отличающиеся большей устойчивостью к коррозии. Примером такого соединения является нержавеющая сталь.
Добавление различных соединений позволяет получить сплавы, отличающиеся большей устойчивостью к коррозии. Примером такого соединения является нержавеющая сталь.
Самым необычным является протекторная защита, которая подразумевает покрытие сооружений из одного металла пластинами из более активного металла, так называемого протектора. Поскольку он имеет более отрицательный потенциал, то выступает в роли анода. Защищаемая поверхность используется как катод. Они соединяются между собой проводником тока, благодаря чему создаются неблагоприятные условия для протектора. Как следствие разрушению поддается именно он, в то время как ценное сооружение остается целым.
Более редким решение является изменение состав окружающей среды. В таких условиях коррозия металлов замедляется или не происходит. Данный метод подразумевает очистку состава жидкости или газа от кислот и солей, вызывающих разрушение. Такой метод применим далеко не во всех случаях, поскольку отличается техническими сложностями и определенной дороговизной.
 Его используют в разных механизмах. К примеру, могут применять в определенных средах только те металлы, для которых те не агрессивны.
Его используют в разных механизмах. К примеру, могут применять в определенных средах только те металлы, для которых те не агрессивны.
Похожие темы:
- Степень защиты IP. Маркировка. Выбор устройств
- Преобразователь ржавчины. Виды и работа. Применение
Коррозия — электрохимическая
Коррозия — электрохимическая
| Коррозия и ухудшение состояния окружающей среды |
| ||||||||||||||
| Электрохимический Процессы · схема иллюстрирует электрохимическую реакцию, происходящую на поверхности | |||||||||||||||
| · реакции окисления и восстановления находятся в равновесии, так что в случае От кого: | |||||||||||||||
Измерения электрохимической коррозии — гальваническая коррозия Gamry Instruments
Обзор электрохимических основ коррозии
Большая часть коррозии металлов происходит в результате электрохимических реакций на границе раздела между металлом и раствором электролита. Например, тонкая пленка влаги на поверхности металла образует электролит для атмосферной коррозии. Второй пример: влажный бетон является электролитом для усиления коррозии арматурных стержней в мостах. Хотя большая часть коррозии происходит в воде, коррозия в неводных системах не является чем-то неизвестным.
Например, тонкая пленка влаги на поверхности металла образует электролит для атмосферной коррозии. Второй пример: влажный бетон является электролитом для усиления коррозии арматурных стержней в мостах. Хотя большая часть коррозии происходит в воде, коррозия в неводных системах не является чем-то неизвестным.
Коррозия обычно происходит со скоростью, определяемой равновесием между противоположными электрохимическими реакциями. Одной из реакций является анодная реакция, при которой металл окисляется, высвобождая электроны в металл. Другой является катодной реакцией, в которой частицы раствора (часто O 2 или H + ) восстанавливаются, удаляя электроны из металла. Когда эти две реакции находятся в равновесии, поток электронов от каждой реакции уравновешивается, и суммарный поток электронов (электрический ток) не возникает. Две реакции могут происходить на одном металле или на двух разнородных металлах (или металлических участках), которые электрически связаны.
Рисунок 1 иллюстрирует этот процесс. По вертикальной оси отложен электрический потенциал, по горизонтальной оси отложен логарифм абсолютного тока. Теоретический ток для анодной и катодной реакций представлен прямыми линиями. Изогнутая линия — это общий ток: сумма анодного и катодного токов. Это ток, который вы измеряете, когда измеряете потенциал металла своим потенциостатом. Острая точка на кривой на самом деле является точкой, где ток меняет полярность при изменении реакции с анодной на катодную или наоборот. Острая точка вызвана построением графика вдоль логарифмической оси. Использование логарифмической оси необходимо из-за широкого диапазона значений тока, которые должны быть зарегистрированы во время эксперимента по коррозии. Из-за явления пассивности ток во время коррозионного эксперимента часто изменяется на шесть порядков.
Рис. 1. Процесс коррозии с указанием анодной и катодной составляющих тока.
Потенциал металла является средством, с помощью которого анодная и катодная реакции поддерживаются в равновесии. Обратитесь к рисунку 1. Обратите внимание, что ток каждой полуреакции зависит от электрохимического потенциала металла. Предположим, что анодная реакция высвобождает слишком много электронов в металл. Таким образом, избыточные электроны сдвигают потенциал металла в сторону отрицательного, что замедляет анодную реакцию и ускоряет катодную. Это противодействует начальному возмущению системы.
Обратитесь к рисунку 1. Обратите внимание, что ток каждой полуреакции зависит от электрохимического потенциала металла. Предположим, что анодная реакция высвобождает слишком много электронов в металл. Таким образом, избыточные электроны сдвигают потенциал металла в сторону отрицательного, что замедляет анодную реакцию и ускоряет катодную. Это противодействует начальному возмущению системы.
Равновесный потенциал металла при отсутствии электрических соединений с металлом называется потенциалом холостого хода, E oc . В большинстве экспериментов по электрохимической коррозии первым этапом является измерение E oc .
Значение либо анодного, либо катодного тока при E oc называется током коррозии, I corr . Если бы мы могли измерить I corr , мы могли бы использовать его для расчета скорости коррозии металла. К сожалению, я корр. нельзя измерить напрямую. Однако его можно оценить с помощью электрохимических методов. В любой реальной системе I корр и скорость коррозии зависят от многих параметров системы, включая тип металла, состав раствора, температуру, движение раствора, историю металла и многие другие.
В любой реальной системе I корр и скорость коррозии зависят от многих параметров системы, включая тип металла, состав раствора, температуру, движение раствора, историю металла и многие другие.
Приведенное выше описание процесса коррозии ничего не говорит о состоянии поверхности металла. На практике многие металлы при коррозии образуют на своей поверхности оксидный слой. Если оксидный слой препятствует дальнейшей коррозии, говорят, что металл пассивируется. В некоторых случаях локальные участки пассивной пленки разрушаются, что приводит к значительной коррозии металла на небольшом участке. Это явление называется точечной коррозией или просто точечной коррозией.
Поскольку коррозия происходит в результате электрохимических реакций, электрохимические методы идеально подходят для изучения процессов коррозии. В электрохимических исследованиях образец металла с площадью поверхности несколько квадратных сантиметров используется для моделирования металла в коррозионной системе. Образец металла погружают в раствор, характерный для среды металла в исследуемой системе. Дополнительные электроды погружаются в раствор, и все электроды подключаются к устройству, называемому потенциостатом. Потенциостат позволяет изменять потенциал металлического образца контролируемым образом и измерять протекающий ток в зависимости от приложенного потенциала.
Образец металла погружают в раствор, характерный для среды металла в исследуемой системе. Дополнительные электроды погружаются в раствор, и все электроды подключаются к устройству, называемому потенциостатом. Потенциостат позволяет изменять потенциал металлического образца контролируемым образом и измерять протекающий ток в зависимости от приложенного потенциала.
Полезны как поляризация с контролируемым потенциалом (потенциостатическая), так и поляризация с регулируемым током (гальваностатическая). При потенциостатической поляризации измеряется ток, а при гальваностатической — потенциал. Это обсуждение будет сосредоточено на методах с контролируемым потенциалом, которые гораздо более распространены, чем гальваностатические методы. За исключением зависимости потенциала холостого хода от времени, электрохимического шума, гальванической коррозии и некоторых других, потенциостатический режим используется для нарушения равновесного процесса коррозии. Когда потенциал металлического образца в растворе отклоняется от E oc , это называется поляризацией образца.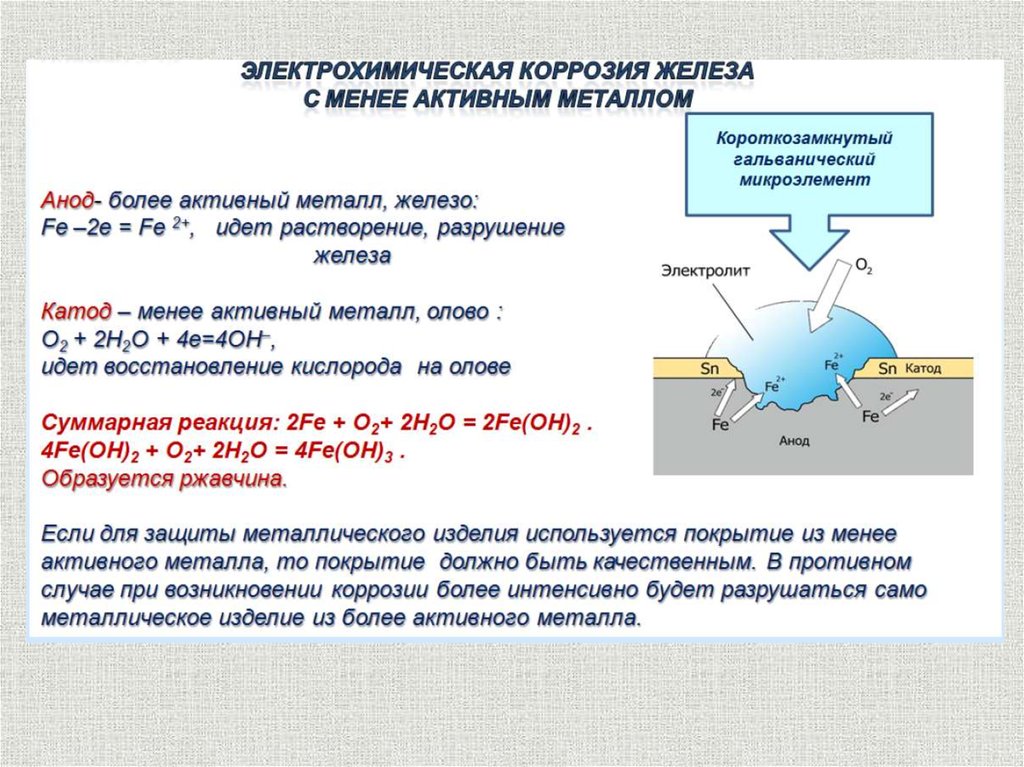 Отклик (то есть результирующий ток) металлического образца измеряется по мере его поляризации. Ответ используется для разработки модели коррозионного поведения образца.
Отклик (то есть результирующий ток) металлического образца измеряется по мере его поляризации. Ответ используется для разработки модели коррозионного поведения образца.
Количественная теория коррозии
В предыдущем разделе мы указывали, что I corr нельзя измерить напрямую. Во многих случаях вы можете оценить его по данным зависимости тока от напряжения. Вы можете измерить логарифмическую кривую зависимости тока от потенциала в диапазоне около половины вольта. Развертка напряжения сосредоточена на E ок . Затем вы подгоняете измеренные данные к теоретической модели процесса коррозии.
Модель, которую мы используем для процесса коррозии, предполагает, что скорость как анодного, так и катодного процессов контролируется кинетикой реакции переноса электрона на поверхности металла. Обычно это относится к коррозионным реакциям. Электрохимическая реакция под кинетическим контролем подчиняется уравнению. 1, уравнение Тафеля.
В этом уравнении
я | — это ток в результате реакции |
I 0 | — константа, зависящая от реакции, называемая током обмена . |
Е | — электродный потенциал |
Е 0 | — равновесный потенциал (постоянный для данной реакции) |
β | 90 167 — постоянная Тафеля реакции (постоянная для данной реакции, выраженная в вольтах на декаду. 90 168 |
Уравнение Тафеля описывает поведение одной изолированной реакции. В системе коррозии у нас есть две противоположные реакции: анодная и катодная.
Уравнения Тафеля для анодной и катодной реакций в коррозионной системе можно объединить для получения уравнения Батлера-Фольмера (уравнение 2).
где
я | — измеренный ток от ячейки в амперах |
I корр | — ток коррозии в амперах |
Е | — электродный потенциал |
E корр | — потенциал коррозии в вольтах |
β а | 90 167 – анодная постоянная Тафеля β в вольтах на декаду 90 168 |
β в | 90 167 – катодная β-постоянная Тафеля в вольтах на декаду 90 168 |
Что означает уравнение. 2 предсказать кривую зависимости тока от напряжения? В E corr каждый экспоненциальный член равен единице. Следовательно, ток ячейки равен нулю, как и следовало ожидать. Рядом с Е corr оба экспоненциальных члена вносят вклад в общий ток. Наконец, поскольку потенциал управляется потенциостатом далеко от E corr , преобладает один экспоненциальный член, а другим членом можно пренебречь. Когда это происходит, график зависимости логарифмического тока от потенциала становится прямой линией.
2 предсказать кривую зависимости тока от напряжения? В E corr каждый экспоненциальный член равен единице. Следовательно, ток ячейки равен нулю, как и следовало ожидать. Рядом с Е corr оба экспоненциальных члена вносят вклад в общий ток. Наконец, поскольку потенциал управляется потенциостатом далеко от E corr , преобладает один экспоненциальный член, а другим членом можно пренебречь. Когда это происходит, график зависимости логарифмического тока от потенциала становится прямой линией.
График зависимости log I от Е называется графиком Тафеля. График Тафеля на рисунке 1 был создан непосредственно из уравнения Батлера-Фольмера. Обратите внимание на линейные участки кривой тока ячейки.
На практике многие коррозионные системы контролируются кинетическим путем и, таким образом, подчиняются уравнению. 2. Кривая логарифмической зависимости тока от потенциала, линейная по обе стороны от E corr , указывает на кинетический контроль изучаемой системы.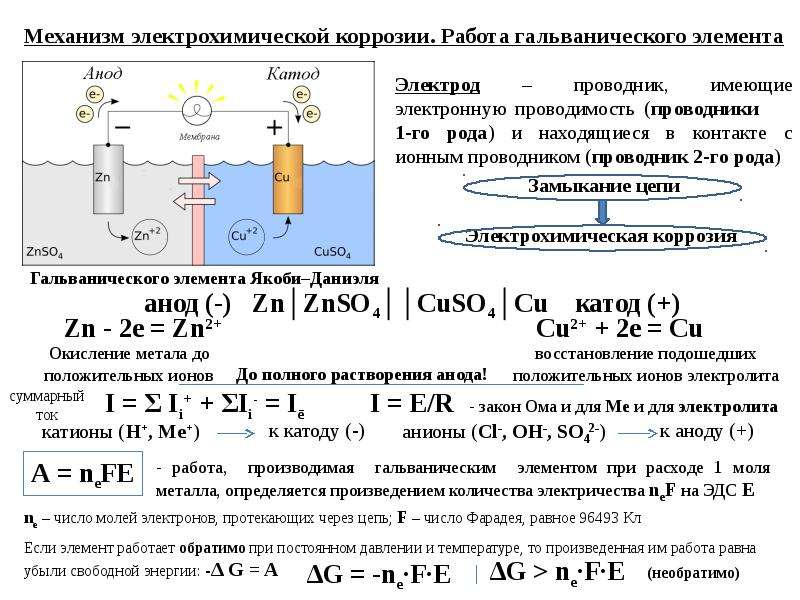 Однако могут быть осложнения, такие как:
Однако могут быть осложнения, такие как:
- Концентрационная поляризация, когда скорость реакции контролируется скоростью, с которой реагенты достигают поверхности металла. Часто катодные реакции демонстрируют концентрационную поляризацию при более высоких токах, когда диффузия кислорода или иона водорода недостаточно быстрая, чтобы поддерживать кинетически контролируемую скорость.
- Образование оксида, которое может привести или не привести к пассивации. Этот процесс может изменить поверхность тестируемого образца. Исходная поверхность и измененная поверхность могут иметь разные значения констант в уравнении. 2.
- Другие эффекты, которые изменяют поверхность, такие как предпочтительное растворение одного компонента сплава, также могут вызывать проблемы.
- Смешанный контрольный процесс, в котором одновременно происходит более одной катодной или анодной реакции, может усложнить модель. Примером смешанного контроля является одновременное восстановление кислорода и иона водорода.

- Наконец, падение потенциала в результате протекания тока ячейки через сопротивление раствора ячейки вызывает ошибки в кинетической модели. Этот последний эффект, если он не слишком серьезный, может быть устранен с помощью IR-компенсации в потенциостате.
В большинстве случаев осложнения, подобные перечисленным выше, вызывают нелинейность графика Тафеля. С осторожностью используйте результаты, полученные из графика Тафеля без четко определенной линейной области.
Классический анализ Тафеля выполняется путем экстраполяции линейных частей логарифмического графика зависимости тока от потенциала обратно к их пересечению. См. рис. 2 (который является перепечатанным рис. 1 с аннотациями, демонстрирующими анализ). Величина либо анодного, либо катодного тока на пересечении равна I корр . К сожалению, многие реальные системы коррозии не обеспечивают достаточную линейную область для точной экстраполяции. Большинство современных программ для испытаний на коррозию, таких как Corrosion Techniques от Gamry Instruments, выполняют более сложную численную подгонку к уравнению Батлера-Фольмера. Измеренные данные подходят к уравнению. 2 путем корректировки значений E corr , I corr , β a и β c . Преимущество метода подбора кривой состоит в том, что он не требует полностью развитой линейной части кривой.
Измеренные данные подходят к уравнению. 2 путем корректировки значений E corr , I corr , β a и β c . Преимущество метода подбора кривой состоит в том, что он не требует полностью развитой линейной части кривой.
Рис. 2. Классический анализ Тафеля.
Сопротивление поляризации
Ур. 2 можно еще больше упростить, ограничив потенциал очень близким к E corr . Вблизи E corr кривая зависимости тока от напряжения приближается к прямой линии. Наклон этой линии имеет единицы сопротивления (Ом). Наклон поэтому называется поляризационным сопротивлением, R p . Значение R p можно объединить с оценкой коэффициентов β, чтобы получить оценку тока коррозии.
Если мы аппроксимируем экспоненциальные члены в уравнении. 2 с первыми двумя членами разложения в ряд по степеням ( ) и упрощением, мы получаем одну форму уравнения Штерна-Гири:
распространяется в небольшом диапазоне потенциалов, который очень близок к E oc (обычно ±10 мВ). Численная аппроксимация кривой дает значение сопротивления поляризации R p . Данные поляризационного сопротивления не дают никакой информации о значениях коэффициентов β. Следовательно, чтобы использовать уравнение 3, вы должны указать значения β. Их можно получить из графика Тафеля или оценить на основе вашего опыта работы с тестируемой системой.
Численная аппроксимация кривой дает значение сопротивления поляризации R p . Данные поляризационного сопротивления не дают никакой информации о значениях коэффициентов β. Следовательно, чтобы использовать уравнение 3, вы должны указать значения β. Их можно получить из графика Тафеля или оценить на основе вашего опыта работы с тестируемой системой.
Расчет скорости коррозии на основе тока коррозии
Численный результат, полученный путем подгонки данных о коррозии к модели, обычно представляет собой ток коррозии. Нас интересуют скорости коррозии в более удобных единицах скорости проникновения, таких как миллиметры в год. Как ток коррозии используется для определения скорости коррозии? Предположим, реакция электролитического растворения с участием химического вещества S:
S ® S n + + n e–
Вы можете связать поток тока с массой с помощью закона Фарадея.
Q = nFM Ур.
 4
4
где
Q | — заряд в кулонах, полученный в результате реакции частиц S . |
п | — число электронов, переданных на молекулу или атом S . |
Ф | — постоянная Фарадея = 96 485 кул/моль |
М | — количество молей частиц S, реагирующих с . |
Более полезная форма уравнения. 4 требует понятия эквивалентного веса. Эквивалентный вес (EW) — это масса частиц S, которые будут реагировать с зарядом в один фарадей. Для атомарного вида EW = AW /n (где AW — атомный вес вида).
Вспоминая, что M = m /AW и подставляя в уравнение. 4 получаем:
, где m — масса прореагировавших частиц S.
В случаях, когда коррозия происходит равномерно по всей поверхности металла, скорость коррозии можно рассчитать в единицах расстояния в год. Будьте осторожны: этот расчет действителен только для однородной коррозии; он резко недооценивает проблему, когда возникает локальная коррозия!
Для сложного сплава, который подвергается равномерному растворению, эквивалентная масса представляет собой средневзвешенное значение эквивалентных масс компонентов сплава. В качестве весового коэффициента используется мольная доля, а не массовая доля. Если растворение неравномерное, для расчета EW может потребоваться измерение продуктов коррозии.
Преобразование потери веса в скорость коррозии (CR) выполняется просто. Нам нужно знать плотность d и площадь образца A. Заряд определяется выражением Q = It, где t — время в секундах, а I — ток. Мы можем подставить значение постоянной Фарадея. Изменение уравнения 5,
, где
я корр | Ток коррозии в амперах |
К | Константа, определяющая единицы измерения скорости коррозии |
РЭБ | Эквивалентный вес в граммах/эквивалент |
д | Плотность в г/см 3 |
А | Площадь образца в см 2 |
Таблица 1. Константы скорости коррозии
Константы скорости коррозии
Единицы измерения скорости коррозии | К | Единицы |
мм/год (мм/год) | 3272 | мм (А-см-год) |
миллидюймов/год (млн/год) | 1,288 × 10 5 | миллидюймов (А-см-год) |
ИК-компенсация
Когда вы пропускаете ток между двумя электродами в проводящем растворе, в растворе всегда есть области с разными потенциалами. Большая часть общего изменения потенциала происходит очень близко к поверхности электродов. Здесь градиенты потенциала в значительной степени вызваны градиентами концентрации ионов, возникающими вблизи металлических поверхностей. Кроме того, всегда существует разность потенциалов (падение потенциала), вызванная протеканием тока через сопротивление в объеме раствора.
Кроме того, всегда существует разность потенциалов (падение потенциала), вызванная протеканием тока через сопротивление в объеме раствора.
В электрохимическом эксперименте потенциал, который вы хотите контролировать или измерять, представляет собой потенциал образца металла (называемого рабочим электродом) относительно электрода сравнения. Обычно нас не интересуют падения потенциала, вызванные сопротивлением растворов, потому что они незначительны в типичных растворах электролитов, таких как 1 M H 2 SO 4 или 5% NaCl.
Потенциостаты Gamry Instruments, как и все современные электрохимические приборы, представляют собой трехэлектродные потенциостаты. Они измеряют и контролируют разность потенциалов между нетоковедущим эталонным электродом и одним из двух токоведущих электродов (рабочим электродом). Падение потенциала вблизи другого токоведущего электрода (противоэлектрода) не имеет значения при использовании трехэлектродного потенциостата.
Тщательное размещение электрода сравнения может компенсировать часть падения ИК-излучения, возникающего из-за тока ячейки, I, протекающего через сопротивление раствора, R. Вы можете думать об электроде сравнения как о взятии пробы потенциала где-то вдоль сопротивления раствора. Чем ближе он к рабочему электроду, тем ближе вы к измерению потенциала без ИК-ошибок. Однако на практике полная компенсация ИК-излучения не может быть достигнута за счет размещения электрода сравнения из-за конечных физических размеров электрода. Часть сопротивления ячейки, которая остается после размещения электрода сравнения, называется некомпенсированным сопротивлением, R и .
Вы можете думать об электроде сравнения как о взятии пробы потенциала где-то вдоль сопротивления раствора. Чем ближе он к рабочему электроду, тем ближе вы к измерению потенциала без ИК-ошибок. Однако на практике полная компенсация ИК-излучения не может быть достигнута за счет размещения электрода сравнения из-за конечных физических размеров электрода. Часть сопротивления ячейки, которая остается после размещения электрода сравнения, называется некомпенсированным сопротивлением, R и .
Потенциостаты Gamry могут использовать ИК-компенсацию прерывания тока или положительной обратной связи для динамической коррекции нескомпенсированных ошибок сопротивления. В методе прерывания тока ток ячейки периодически отключается на очень короткое время. При отсутствии протекания тока через растворное сопротивление его ИК-падение мгновенно исчезает. Падение потенциала на поверхности электрода остается постоянным в быстром временном масштабе. Разность потенциалов с протекающим током и без него является мерой некомпенсированного падения IR.
Потенциостат выполняет измерение прерывания тока сразу после получения каждой точки данных. Потенциостат фактически снимает три показания потенциала: E 1 перед отключением тока, E 2 и E 3 во время отключения (см. рис. 3). Обычно последние два используются для экстраполяции разности потенциалов ∆E до точного момента, когда ток был прерван. Время прерывания зависит от тока ячейки. Время прерывания составляет 40 мкс в диапазонах с более высоким током. В более низких диапазонах тока прерывание длится дольше.
Рисунок 3 . Потенциал прерывания тока в зависимости от времени.
В режимах с управляемым потенциалом приложенный потенциал может быть динамически скорректирован с учетом измеренной ИК-ошибки одним из нескольких способов. В простейшем из них ошибка IR из предыдущей точки применяется как поправка к приложенному потенциалу. Например, если требуется свободный от ИК-потенциала 1 В, а измеренная ИК-ошибка составляет 0,2 В, потенциостат применяет 1,2 В. Коррекция всегда отстает на одну точку, так как ИК-ошибка от одной точки применяется для исправления приложенного потенциал для следующего пункта. В дополнение к этому обычному режиму потенциостат Gamry Instruments предлагает более сложные режимы обратной связи, в которых две точки на кривой затухания усредняются.
Коррекция всегда отстает на одну точку, так как ИК-ошибка от одной точки применяется для исправления приложенного потенциал для следующего пункта. В дополнение к этому обычному режиму потенциостат Gamry Instruments предлагает более сложные режимы обратной связи, в которых две точки на кривой затухания усредняются.
По умолчанию в режимах с управляемым потенциалом ошибка потенциала, измеренная с помощью прерывания тока, используется для корректировки приложенного потенциала. В режимах управляемого тока коррекция не требуется. Если выбрана компенсация ИК, измеренная ошибка ИК вычитается из измеренного потенциала. Таким образом, все зарегистрированные потенциалы свободны от ИК-ошибки.
Подробное теоретическое обсуждение некомпенсированного сопротивления см. в Keith B. Oldham, et al., Analytical Chemistry, 72 (2000), 39.72 и 3981.
Условные обозначения тока и напряжения
Полярность тока при электрохимических измерениях может быть непостоянной. Текущее значение -1,2 мА может означать разные вещи для работников разных областей электрохимии или в разных странах, или даже для разных потенциостатов. Для аналитического электрохимика это представляет собой 1,2 мА анодного тока. Для ученого-коррозиониста это соответствует 1,2 мА катодного тока. Потенциостат Gamry Instruments в режиме по умолчанию следует соглашению о коррозии для тока, в котором положительные токи являются анодными, а отрицательные — катодными. Для удобства наших пользователей по всему миру потенциостаты Gamry Instruments могут задать полярность тока в соответствии с вашими предпочтениями с помощью простой команды программного обеспечения.
Текущее значение -1,2 мА может означать разные вещи для работников разных областей электрохимии или в разных странах, или даже для разных потенциостатов. Для аналитического электрохимика это представляет собой 1,2 мА анодного тока. Для ученого-коррозиониста это соответствует 1,2 мА катодного тока. Потенциостат Gamry Instruments в режиме по умолчанию следует соглашению о коррозии для тока, в котором положительные токи являются анодными, а отрицательные — катодными. Для удобства наших пользователей по всему миру потенциостаты Gamry Instruments могут задать полярность тока в соответствии с вашими предпочтениями с помощью простой команды программного обеспечения.
Полярность потенциала также может быть источником путаницы. При измерении электрохимической коррозии равновесный потенциал, принимаемый металлом в отсутствие электрических соединений с металлом, называется потенциалом разомкнутой цепи, E oc . Мы используем термин коррозионный потенциал, E corr , для потенциала в электрохимическом эксперименте, при котором ток не течет, что определяется численной подгонкой данных зависимости тока от потенциала. В идеальном случае значения E oc и E corr идентичны. Одна из причин, по которой эти два напряжения могут различаться, заключается в том, что во время сканирования произошли изменения на поверхности электрода.
В идеальном случае значения E oc и E corr идентичны. Одна из причин, по которой эти два напряжения могут различаться, заключается в том, что во время сканирования произошли изменения на поверхности электрода.
В большинстве современных потенциостатов все потенциалы указываются или сообщаются как потенциал рабочего электрода относительно электрода сравнения или потенциала холостого хода. Первый всегда помечен как «vs. E ref », а последний как «vs. Е oc ». Уравнения для преобразования одной формы потенциала в другую:
E по сравнению с E
oc = (E по сравнению с E ref ) – E oc
E по сравнению с E
ref = (E против E oc ) + E oc
Независимо от того, соответствуют ли потенциалы E ref или E oc , используется одно соглашение о знаках. Чем больше положительный потенциал, тем он более анодный. Более анодные потенциалы ускоряют окисление на рабочем электроде. И наоборот, отрицательный потенциал ускоряет восстановление на рабочем электроде.
Более анодные потенциалы ускоряют окисление на рабочем электроде. И наоборот, отрицательный потенциал ускоряет восстановление на рабочем электроде.
Некоторые ссылки по теории коррозии и электрохимическим испытаниям на коррозию
DC Electrochemical Test Methods, N.G. Томпсон и Дж.Х. Пайер, Национальная ассоциация инженеров-коррозионистов. ISBN: 1-877914-63-0.
Принципы и предотвращение коррозии, Денни А. Джонс, Прентис-Холл, 1996. ISBN 0-13-359993-0.
Метод сопротивления поляризации для определения мгновенных скоростей коррозии, J.R. Scully, Corrosion, 56 (2000), 199. , ПА 19428. Их можно найти в томе 3.02 стандартов ASTM:
G 5: Измерения потенциостатической и потенциодинамической анодной поляризации
G 59: Измерения сопротивления поляризации
G 61: Измерения циклической поляризации для локализованной коррозионной восприимчивости железа, никеля — и сплавы на основе кобальта
G 100: Циклическая гальванолестничная поляризация
G 106: Проверка алгоритма и оборудования для измерения электрохимического импеданса
G 108: Электрохимическая потенциокинетическая реактивация (ЭПР) для обнаружения сенсибилизации
G 150: Электрохимические испытания нержавеющих сталей при критической температуре точечной коррозии
Электрохимические методы в коррозионной инженерии, Национальная ассоциация инженеров-коррозионистов, 1986.


