Что ржавеет на воздухе: Почему железо ржавеет? | Пневмопортал
Содержание
Почему железо ржавеет и как этот процесс предотвратить
Главная » Борьба со ржавчиной
Автор Анна Фомина На чтение 3 мин Просмотров 1.8к. Опубликовано
Железо, определенно, является одним из самых важных металлов в мире. Он относительно прочный, легкий и пластичный, что делает его эффективным материалом для изготовления бесчисленных продуктов. Однако в естественном состоянии железо очень подвержено коррозии. Со временем универсальный металл подвергнется коррозии, что приведет к образованию оксида железа, который больше известен как ржавчина.
Наука, стоящая за ржавчиной
Железо, как и железные сплавы, ржавеет из-за химической реакции, известной как окисление. Когда железо подвергается воздействию влаги или кислорода, происходит окисление. Во время этой химической реакции железо превращается в оксид железа. Оксид железа обычно имеет красноватый шелушащийся вид, который со временем становится все хуже. Если оставить этот факт без внимания, оксид железа распространится, тем самым поставив под угрозу физическую целостность железа.
Если оставить этот факт без внимания, оксид железа распространится, тем самым поставив под угрозу физическую целостность железа.
Железо может ржаветь под воздействием воздуха или влаги. И кислород, и влага являются катализаторами ржавления. Когда железо подвергается воздействию воздуха или влаги, окисление превращает его в оксид железа.
Антикоррозийная обработка железа
Металлообрабатывающие и производственные предприятия могут защитить свои металлические изделия от ржавчины. Например, цинкование – это распространенный процесс антикоррозионной обработки железа. Он предполагает нанесение защитного покрытия на поверхность металлической заготовки. При гальванике цинк наносится на поверхность железа. Слой цинка действует как барьер между железом и окружающей средой. В результате железо не контактирует с воздухом или влагой. Если предположить, что слой цинка не поврежден, оцинкованное железо не должно ржаветь.
Еще одна распространенная антикоррозионная обработка железа – это покрытие поверхности.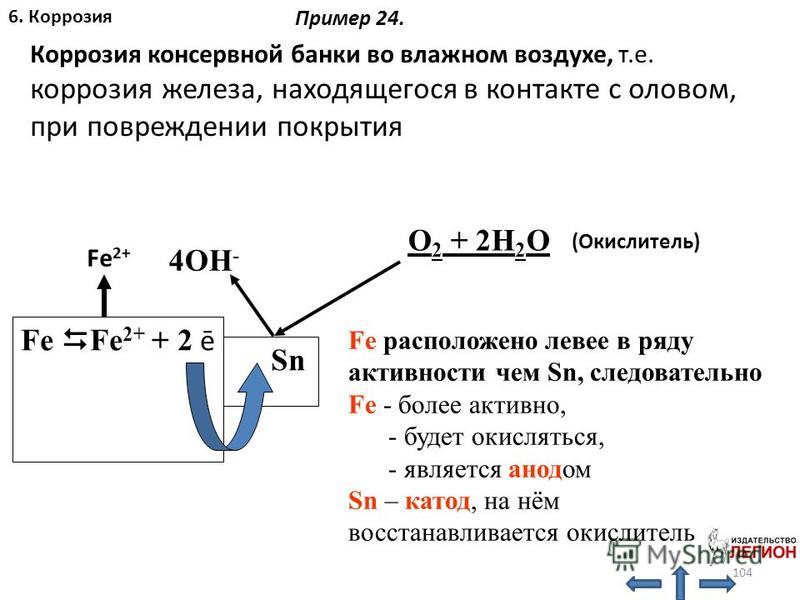 Гальваника поверхности включает нанесение никеля или хрома. Поскольку никель и хром не содержат железа, они не подвержены коррозии. Покрытие поверхности – более сложная антикоррозионная обработка, но она очень эффективна для защиты железа от ржавчины.
Гальваника поверхности включает нанесение никеля или хрома. Поскольку никель и хром не содержат железа, они не подвержены коррозии. Покрытие поверхности – более сложная антикоррозионная обработка, но она очень эффективна для защиты железа от ржавчины.
Такая простая вещь, как покраска поверхности железа, может защитить ее от ржавчины. Как и в случае гальванизации, покраска создает барьер на поверхности железа. Наличие краски создает барьер между железом и окружающей средой. Однако недостатком покраски железа является то, что она не держится так долго, как другие виды обработки поверхности.Использование кованого железа вместо чистого железа также может защитить от ржавчины. Кованое железо имеет более высокое содержание углерода, чем чистое железо, и с большим содержанием углерода, и, естественно, лучше защищено от ржавчины. С учетом сказанного, чистое железо, кованое железо и чугун могут ржаветь под воздействием влаги или воздуха.
Рекомендуем эффективный состав для удаления ржавчины с металлов — «РжавоМед-У»
почему железо ржавеет
виды, особенности, защита от коррозии
Атмосферная коррозия металлов – один из основных факторов риска при использовании металлоконструкций на открытом воздухе. Процесс начинается под действием внешних факторов и приводит к постепенному разрушению материала.
Процесс начинается под действием внешних факторов и приводит к постепенному разрушению материала.
В этом материале мы расскажем о том, как формируется такой тип коррозии, в чем его опасность и какие средства используют для защиты металла.
Понятие и виды атмосферной коррозии
Появление ржавчины стимулируется микроклиматом, наблюдаемым в нижних слоях атмосферы. Материалы без дополнительной защиты постепенно начинают страдать от такой проблемы.
При этом, атмосферная коррозия не такая стремительная и губительная, как почвенная и морская. Это дает возможность использовать специальные средства для защиты от нее и продлевать длительность эксплуатаций изделий из металла.
Особенность атмосферной коррозии заключается в том, что у разных материалов и в зависимости от климата, ее протекание сильно отличается.
Есть 3 вида атмосферной коррозии:
Сухая атмосферная коррозия
В этом случае повреждение начинается и без воздействия влаги – на поверхности металла не появляется характерной деструктивной пленки из жидкости.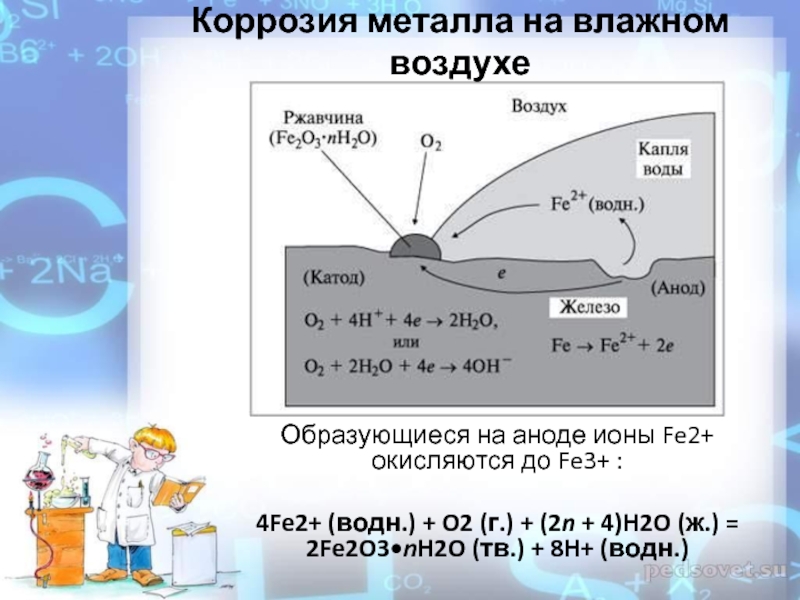 Для протекания процесса, нужно чтобы влажность окружающей среды была меньше 60%.
Для протекания процесса, нужно чтобы влажность окружающей среды была меньше 60%.
По своей сути процесс – химический. Он слишком стремителен в силу образования окислительного слоя – он постепенно замедляет распространение ржавения внутрь. Аналогичный принцип используется и при пассивации металлов.
Если рассматривать течение процесса подробнее, его делят на два этапа:
- Быстрый. Начинается при соприкосновении необработанного материала с воздухом.
- Медленный. Постепенное протекание ржавения металла после того, как на нем появился слой окислов.
При этом ржавчина, пусть и медленно, но распространяется. Поверхность постепенно темнеет, а структура материала начинает разрушаться, теряет прочность.
Интенсивность протекания процесса будет зависеть от температуры окружающей среды. Если она высокая, скорость увеличится. Толщина пленки варьируется в зависимости от самого материала. Доказано, что дополнительным стимулятором развития процесса становится рассеивание в атмосфере агрессивных газов.
Влажная атмосферная коррозия
Такой тип коррозии стимулируется появлением слоя влаги на металле. Для России такой тип повреждений наиболее характерен. Если влажность воздуха превышает 60%, риск развития коррозийного поражения увеличивается.
Уйти от него невозможно – даже при утреннем выпадении росы влажность уже оказывается достаточной, чтобы покрыть деталь опасной пленкой.
Риск поражения также увеличивается из-за высокого уровня загрязненности воздуха, контакта с агрессивными химическими средами.
Конденсация влаги проходит по трем основным механизмам:
- Химический. Влага начинает накапливаться, потому что коррозийные продукты начинают контактировать с влажным воздухом. Это усугубляет процесс, потому ржавые участки сильнее задерживают воду.
- Капиллярная. Возникает в трещинах, зазорах и щелях.
- Абсорбционная. Связана с действием одноименных сил на стальной поверхности.
Часто в развитии процесса участвуют все три механизма, но на разных этапах его появления. Итог один – материал теряет прочность и постепенно начинает разрушаться.
Итог один – материал теряет прочность и постепенно начинает разрушаться.
Мокрая атмосферная коррозия
Быстрый и опасный тип атмосферной коррозии. Начинает появляться при стопроцентной влажности воздуха, когда на металле скапливаются капли воды.
Также процесс характерен и для тех конструкций, которые постоянно помещены в воду. Если вода загрязнена, имеет повышенную кислотность или концентрацию соли, риск только увеличивается.
Как факторы влияют на появление коррозии
Когда мы рассмотрели виды атмосферной коррозии, пришло время внимательнее оценить факторы ее возникновения и развития.
На изделие их может воздействовать сразу несколько, а при усугублении влияния скорость только растет.
Среди распространенных факторов:
Повышенная влажность воздуха
Как уже было описано выше, она создает пленку разной толщины, которая начинает разрушать материал.
Главный параметр – относительная атмосферная влажность. Она начинает значительно влиять на металл, когда уровень превышает 60%.
При стопроцентной влажности, развивается мокрая коррозия, затрагивающая практически все виды материалов.
В зависимости от сплава, критический уровень влажности может меняться. Так сталь, цинк, медь и никель начинают ржаветь при показателях выше 70%.
Техногенное загрязнение воздуха становится дополнительным фактором порчи при влажности.
Газовый состав атмосферы
Можно легко заметить, что при аналогичной влажности, уровне осадков и периодичности туманов, в разных регионах материалы ржавеют с отличной друг от друга скоростью. Причина заключается в составе атмосферы. Рассеянные в ней газы могут значительно ускорять процесс.
Наиболее опасная среди всех примесей – диоксид серы. Она дает стимулирование скорости процесса в десятки раз. Некоторые виды газов могут выступать как депассиваторы, а также отражаться на поверхности даже если она прошла обработку.
Именно по этой причине, если вы проводите установку металлоконструкции в промышленном районе с большим количеством опасных производств, нужно внимательно выбирать место. Особенно это актуально при использовании нестабильных металлов, таких, как цинк, кадмий или железо.
Особенно это актуально при использовании нестабильных металлов, таких, как цинк, кадмий или железо.
Также стоит отметить, что при высокой влажности этот негативный фактор только усугубляется.
Уровень содержания твердых частиц
Речь идет как про пассивные, так и про активные включения. Они влияют на электропроводность влаги, стимулируют ее накопление, выступают как депассиваторы.
К наиболее опасным соединениям относятся такие, как (Nh5)2SO4 и Na2SO4. Они могут быть рассеяны в воздухе в виде пыли и легко переносятся ветром. Именно по этой причине рядом с уже сильно проржавевшими металлическими изделиями коррозия начинает развиваться быстрее, чем в обычной обстановке.
Температура
Так как в нашей полосе наиболее распространена именно влажная или мокрая коррозия, температура играет важную роль в испарении воды. Когда столбик термометра опускается ниже, происходит медленное испарение воды, а значит, деталь ржавеет быстрее.
Также не стоит забывать и о географическом факторе. Он сочетает в себе все три описанных. В разных регионах отличается влажность, уровень осадков и другие факторы.
Он сочетает в себе все три описанных. В разных регионах отличается влажность, уровень осадков и другие факторы.
Кроме того, меняется состав атмосферы, наличие посторонних крупных включений и загрязнителей. Потому одинаковые по составу сплавы ржавеют с разной скоростью даже в разных районах одного города, не говоря уже о регионе.
Как протекает атмосферная коррозия?
Чтобы перейти к вопросу защиты от атмосферной коррозии, важно рассмотреть сам механизм ее протекания.
Представим металлическую заготовку и попробуем посмотреть на нее через микроскоп.
Так вы быстро увидите сформированную на поверхности тонкую пленку. Это электролит. В зависимости от того, в каких условиях хранился или использовался металл, электролит формируется из продуктов коррозии или атмосферной влаги.
При контакте с воздухом, на материале начинается развитие катодного процесса с параллельным замедлением анодного. Если атмосфера сильно загрязнена, состав электролита может меняться, на него начинают воздействовать агрессивные примеси газов и других частиц.
Когда критическая масса набирается, металл ржавеет. Процесс проникает все глубже внутрь. На финальных стадиях в листах появляются дыры, а металлические детали становятся хрупкими. Большинство механизмов защиты от действия атмосферы направлены на то, чтобы изначально не дать процессу случиться.
Как защититься от атмосферной коррозии
Защита от угрозы повреждения металла – это очень важное условие увеличения длительности эксплуатации изделий. Явление появления ржавчины хорошо изучено и для уменьшения риска используется несколько основных средств:
- Нанесение специальных покрытий. Они могут быть как металлическими, так и неметаллическими. При нанесении металлического используется цинк, никель и другие материалы. К неметаллической группе относятся многочисленные смазки, ЛКП, специальные пасты. Многие из них могут применяться не только для защиты, но и в качестве ингибиторов атмосферной коррозии на уже пораженных деталях. Так удается замедлить или блокировать распространение разрушения.

- Стабилизация уровня влажности воздуха. При условии, что воздух чистый, без сильной концентрации вредных примесей, опасных паров, уровень относительной влажности можно поддерживать на отметке в 50%. Это не устранит опасности развития сухой коррозии, но общий риск порчи значительно уменьшит.
- Использование ингибиторов. Так называются вещества, которые способны замедлить или заблокировать распространение коррозийного поражения. Обычно используются вещества летучего типа – от нитритов и бензоатов до карбонатов. Они могут применяться в различных видах – от пропитки до закачивания внутрь металлической емкости.
- Легирование. Обеспечивается на этапе выплавки стали. Такие вещества как медь, хром, никель, титан и некоторые другие помогают существенно уменьшить скорость анодной реакции. На выходе металлу также будет требоваться дополнительная защита, но и сам по себе он хорошо противостоит угрозе.
Мы знаем, как защитить материал от порчи
Так как распространение ржавчины нужно не допустить – она может полностью вывести из строя металлическое изделие, намного выгоднее изначально подумать о правильной защите. Мы справляемся с задачей методом цинкования. Он помогает создать на поверхности защитный слой, который не допускает контакта с воздухом и водой.
Мы справляемся с задачей методом цинкования. Он помогает создать на поверхности защитный слой, который не допускает контакта с воздухом и водой.
У нас три цеха горячего цинкования и одна из самых глубоких ванн в Центральном федеральном округе. Это позволяет выполнять крупные заказы и работать с массивными изделиями.
Оставьте заявку на сайте или звоните нам, чтобы оформить заказ услуги или получить ответы на интересующие вас вопросы.
Вернуться к статьям
Поделиться статьей
Сколько кислорода используется, когда железная вата ржавеет? | Эксперимент
Попробуйте выполнить это практическое задание, чтобы выяснить, сколько кислорода используется при ржавчине, и рассчитать процентное содержание кислорода в воздухе.
Когда железо ржавеет, вода и кислород воздуха реагируют с железом с образованием оксида железа. В этом эксперименте студенты помещали железную вату в пробирку, наполненную воздухом, и помещали ее в стакан с водой, чтобы она ржавела. Когда железная вата вступает в реакцию, ржавеет и удаляет кислород из воздуха, вода поднимается по трубе. Наблюдая за изменением объема воздуха в трубке, учащиеся могут рассчитать концентрацию кислорода в воздухе.
Наблюдая за изменением объема воздуха в трубке, учащиеся могут рассчитать концентрацию кислорода в воздухе.
Этот эксперимент необходимо провести в течение двух уроков с интервалом примерно в неделю. Практическая работа, вероятно, займет не более 20 минут на любом уроке.
Оборудование
Аппаратура
- Пробирка (см. примечание 3 ниже)
- Стакан, 100 см 3
- Линейка
Химикаты
- Железная вата
Примечания по охране труда и технике безопасности
- Прочтите наше стандартное руководство по охране труда и технике безопасности.
- Железная вата, Fe(s) – см. карточку опасности CLEAPSS HC055A.
- Пробирки, использованные в этом эксперименте, могут покрыться ржавчиной. Их можно очистить с помощью «Stain Devil»®.
Процедура
Источник: Королевское химическое общество
Поскольку в процессе ржавления расходуется кислород, учащиеся могут наблюдать, как объем воздуха в пробирке уменьшился железную вату в пробирку и смочить ее водой. Слейте лишнюю воду.
Слейте лишнюю воду.
Учебные заметки
Учащиеся должны понимать, что ржавление – это реакция окисления железа кислородом.
железо + кислород → оксид железа
Однако это не все, поскольку образование ржавчины является сложным процессом. Существует множество веб-сайтов, доступных для поиска Google, которые предоставляют более подробную информацию по мере необходимости.
На основании двух измерений длины столба воздуха – до и после образования ржавчины – учащиеся должны быть в состоянии рассчитать процент воздуха, который был удален в результате реакции ржавления. Это должно быть около 20%, что примерно соответствует процентному содержанию кислорода в воздухе.
Вы можете спросить учащихся, как они могут показать, что реакция завершена – они могут предложить оставить ее еще на неделю или около того, чтобы посмотреть, не израсходован ли еще воздух. Железа в этом эксперименте присутствует в избытке, так что оно не все заржавеет. Больше 20% воздуха потребляться не будет (при условии, что оборудование правильно загерметизировано), так как весь кислород израсходован.
Дополнительная информация
Это ресурс проекта «Практическая химия», разработанного Фондом Наффилда и Королевским химическим обществом. Эта коллекция из более чем 200 практических заданий демонстрирует широкий спектр химических концепций и процессов. Каждое задание содержит исчерпывающую информацию для учителей и техников, включая полные технические примечания и пошаговые инструкции. Практические занятия по химии сопровождают практические занятия по физике и практической биологии.
© Фонд Наффилда и Королевское химическое общество
Проверка здоровья и безопасности, 2016 г.
Что вызывает ржавчину? — Ignite Industrial Technologies
Вы наверняка видели ржавчину на старых автомобилях или зданиях и других металлических поверхностях и задавались вопросом, что это такое. Многие люди обычно думают, что ржавчина — это просто окисление, и на самом деле не знают, что ее вызывает. Итак, что вызывает ржавчину?
Что создает ржавчину?
Ржавчина – это оксид железа, продукт реакции между железом и кислородом в присутствии воды или влаги воздуха. Кислород реагирует с железом с образованием оксида железа, который также известен как ржавчина. Вода помогает кислороду реагировать с железом, обеспечивая источник влаги.
Ржавчина представляет собой серьезную проблему для многих отраслей промышленности, поскольку она может привести к износу и разрушению металлических поверхностей. Его также может быть очень трудно удалить после того, как он сформировался. Ржавчина может вызвать серьезные проблемы для зданий, сооружений, автомобилей и других ценных металлических изделий.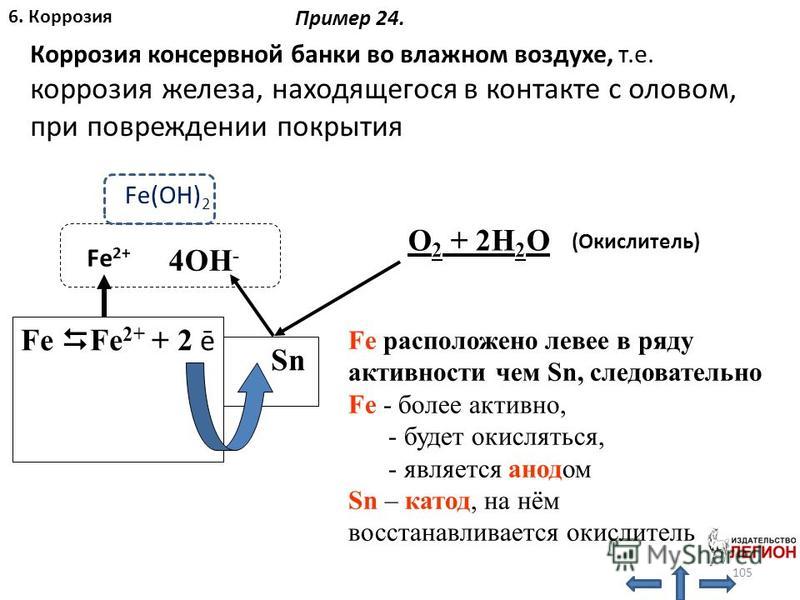
Прежде всего важно понять, что вызывает ржавчину, чтобы предотвратить ее образование. Промышленности и другим организациям, использующим металлические предметы, необходимо принимать меры для максимально возможной защиты своего имущества от ржавчины и других форм коррозии.
Процессы образования ржавчины
Ржавчина – это оксид железа, который образуется, когда железо или сплав, содержащий железо, подвергается воздействию кислорода и влаги в течение длительного времени. Полученный красновато-коричневый цвет обусловлен образованием гидратированного оксида железа (III).
Ржавление — это электрохимический процесс, который начинается с переноса электронов от металла к кислороду. Это создает в металле дефицит электронов, который необходимо восполнить за счет потока электронов из более электроотрицательного вещества.
Для появления ржавчины должны присутствовать три фактора: железо, кислород и вода. Ржавчина образуется, когда эти три элемента объединяются и создают электрохимическую реакцию. железо + вода + кислород → гидратированный оксид железа (III). Именно гидратированная часть делает ржавчину коричневой, а не красной.
железо + вода + кислород → гидратированный оксид железа (III). Именно гидратированная часть делает ржавчину коричневой, а не красной.
Факторы, влияющие на скорость коррозии
Когда дело доходит до коррозии, не все металлы одинаковы. Скорость ржавления зависит от различных факторов, которые можно обобщить следующим образом:
Тип металла
Некоторые металлы ржавеют легче, чем другие. Например, железо и сталь ржавеют быстрее, чем алюминий или нержавеющая сталь. Разница обусловлена электрохимическим потенциалом металла. Чистые металлы обычно более реакционноспособны и, следовательно, более подвержены ржавчине.
Сплавы из нержавеющей стали содержат не менее 10,5% хрома. Хром образует тонкий слой оксида на поверхности стали, который защищает ее от дальнейшего ржавления. Если ваши приборы ржавеют, это может быть связано с тем, что они изготовлены из менее устойчивого к коррозии стального сплава.
Наличие влаги
Ржавчина не может образоваться без воды. Причина, по которой железные трубы часто ржавеют изнутри, заключается в том, что на металле конденсируется водяной пар. Присутствие влаги ускоряет процесс ржавчины, потому что она обеспечивает электролит, необходимый для протекания реакции.
Причина, по которой железные трубы часто ржавеют изнутри, заключается в том, что на металле конденсируется водяной пар. Присутствие влаги ускоряет процесс ржавчины, потому что она обеспечивает электролит, необходимый для протекания реакции.
Нелегированные металлы особенно подвержены коррозии во влажной среде. Вот почему вы часто видите, что оцинкованная сталь или кованое железо ржавеют быстрее, чем другие виды металла.
Присутствие кислорода
Ржавчина может образовываться только в присутствии кислорода. Если вы живете в сухом климате, ваши металлические поверхности могут меньше ржаветь. Это связано с тем, что для протекания реакции требуется кислород, и он более доступен во влажном воздухе.
Вам нужно помнить, что в воде или во влажных местах содержится не только кислород. Углекислый газ в воздухе также может обеспечить кислород, необходимый для образования ржавчины. В присутствии воды углекислый газ реагирует с образованием угольной кислоты. Этот электролит может ускорить процесс ржавчины и вызвать коррозию.
Таким образом, даже если вы не живете во влажном климате, ваши металлические поверхности все равно могут ржаветь под воздействием углекислого газа и воды.
Присутствие других химических веществ
Ржавчина также может образовываться при наличии других химических веществ. Например, соль ускоряет процесс ржавчины, разъедая металл. Вот почему часто можно увидеть, как железные перила и заборы быстрее ржавеют у океана.
Кислоты также могут ускорить процесс ржавчины. Это связано с тем, что они разрушают оксидный слой, который образуется на поверхности металла, подвергая металл воздействию кислорода и воды, что ускоряет процесс коррозии.
Основания также могут способствовать коррозии. Это связано с тем, что они нейтрализуют кислоты, образующиеся на поверхности металла, подвергая его воздействию кислорода и воды. Поэтому, если вы живете в районе с высоким уровнем загрязнения, ваши металлические поверхности могут ржаветь с большей вероятностью.
Температура
Температура также может влиять на скорость коррозии. В общем, чем выше температура, тем быстрее процесс ржавчины. Это связано с тем, что молекулы воды и кислорода более активны при более высоких температурах, и им легче проникать через поверхность металла и вступать в реакцию с железом.
В общем, чем выше температура, тем быстрее процесс ржавчины. Это связано с тем, что молекулы воды и кислорода более активны при более высоких температурах, и им легче проникать через поверхность металла и вступать в реакцию с железом.
Как предотвратить появление ржавчины
Предотвращение образования ржавчины — это бесконечная битва, потому что существует множество способов, при которых металл может подвергаться воздействию кислорода и влаги. Ниже приведены некоторые общие советы по предотвращению ржавчины:
- Содержите металл в чистоте и сухости. Всякий раз, когда металл становится влажным, вытрите его насухо как можно скорее, чтобы предотвратить образование ржавчины. Металлы, такие как автомобильные двигатели и шайбы промышленных деталей, следует очищать неукоснительно.
- Нанести антикоррозионное покрытие. Это может быть краска, порошковое покрытие, масло или воск. Главное, чтобы металл был полностью покрыт, чтобы кислород и влага не могли добраться до него.

- Храните металл в прохладном, сухом месте. Храните металл в помещении с контролируемым климатом, чтобы предотвратить образование ржавчины.
- Регулярно проверяйте на наличие ржавчины. Регулярно проверяйте металл на наличие признаков ржавчины и немедленно удаляйте его. Вы можете использовать обезжириватели после первоначальной очистки.
- Используйте нержавеющие крепежные детали. При соединении металла с другим металлом используйте крепеж из устойчивого к ржавчине материала, такого как нержавеющая сталь.
Связанные вопросы
Что вызывает ржавчину при намокании?
Перекись водорода, также известная как h3O2, вызывает ржавчину при намокании. Он делает это, окисляя металл, который затем создает ржавчину.
Как удалить ржавчину?
Да! Есть несколько способов удалить ржавчину, включая шлифование, использование химического средства для удаления ржавчины, использование качественного обезжиривателя или электролитический процесс с последующей окраской металла.

