Электрохимическое полирование: Электролиты электрохимической полировки различного назначения
Содержание
Сухое электрохимическое полирование для обработки изделий после 3D-печати
Постобработка деталей является одной из основных стадий процесса аддитивного производства и на текущий момент самой трудоемкой.
По статистике, постобработка занимает от 30 до 70 % времени, потраченного на весь процесс аддитивного производства. Одной из основных причин такого распределения времени является то, что постобработка практически всегда выполняется вручную. Это позволяет сделать вывод, что узкое место аддитивного производства заключается в постобработке изделия, а не в его печати.
На текущий момент все технологии постобработки сосредоточены над решением двух основных задач: улучшения качества поверхности и удаления поддержек.
В конце 2017 года была представлена уникальная технология по улучшению качества поверхности — DryLyte, о ней здесь и пойдет речь.
DryLyte — это технология сухого электрохимического шлифования и полирования металлических изделий с помощью переноса ионов металла посредством свободных твердых тел (рис. 1). Отличительной особенностью и уникальностью DryLyte является то, что жидкости не используются в качестве электролитов. Также, в отличие от традиционного способа полирования, обработка по технологии DryLyte сохраняет исходные формы изделия, включая углы и режущие кромки, происходит процесс объемного шлифования и полирования, при котором обрабатывается вся поверхность детали, какую бы сложную геометрию она ни имела.
1). Отличительной особенностью и уникальностью DryLyte является то, что жидкости не используются в качестве электролитов. Также, в отличие от традиционного способа полирования, обработка по технологии DryLyte сохраняет исходные формы изделия, включая углы и режущие кромки, происходит процесс объемного шлифования и полирования, при котором обрабатывается вся поверхность детали, какую бы сложную геометрию она ни имела.
Рис. 1. Электрополирование металлических изделий по технологии DryLyte
Технология DryLyte обеспечивает зеркальную поверхность высочайшего качества, обработку за один шаг (рис. 2) и, что самое важное, позволяет предварительно рассчитать затраты. В 2018 году DryLyte была удостоена самой престижной премии в области технологий для аддитивного производства за лучшее решение для постобработки — TCT Awards.
а) контргайка
б) лопатка
в)
г)
Рис. 2. Изделия до и после обработки
Генеральный директор компании TopStanok Евгений Андреевич Кузьмин поделился кейсом внедрения технологии DryLyte для обработки напечатанных стоматологических изделий.
В компанию обратилась международная стоматологическая компания 3DMED, деятельность которой сосредоточена на производстве систем исправления прикуса на основе собственных запатентованных технологий с использованием аддитивного производства взамен традиционного литейного.
Одно из выпускаемых изделий, систему зубных брекетов (рис. 3), компания производит с помощью SLM-печати. Сами изделия имеют размер немногим больше спичечной головки и достаточно сложную индивидуальную геометрию, исходящую из особенностей поверхности зубов пациента (рис. 4). Изделия устанавливаются непосредственно в ротовую полость и в связи с этим имеют высокие требования к финальному качеству поверхности и к безопасности.
Рис. 3. Система зубных брекетов с напечатанными изделиями
Рис. 4. Напечатанное металлическое изделие до и после обработки по технологии DryLyte
Учитывая вышеперечисленные характеристики, полировка изделия производилась исключительно вручную и занимала большое количество времени. Этап приемки качества изделия также был временнозатратным, так как каждый раз оператор допускал различные ошибки в процессе полировки или, что еще хуже, совершал брак. В случае брака приходилось печатать новое изделие и еще сильнее затягивать и без того долгий процесс производства.
Этап приемки качества изделия также был временнозатратным, так как каждый раз оператор допускал различные ошибки в процессе полировки или, что еще хуже, совершал брак. В случае брака приходилось печатать новое изделие и еще сильнее затягивать и без того долгий процесс производства.
Помимо этого компания попадала в большую зависимость от операторов постобработки: после их увольнения знания уходили вместе с сотрудниками, новых приходилось подолгу обучать. Оператор — достаточно подвижная категория специалистов, и делать это приходилось часто.
После очередного увольнения сотрудника компанией было принято решение искать автоматизированные решения для полировки, и она обратилась в TopStanok. Компания и ранее обращалась к различным специалистам, но на тот момент никто из инжиниринговых компаний не смог предложить автоматизированное решение для полировки таких мелких и сложных изделий.
Задача от заказчика была достаточно тривиальная — автоматизировать весь процесс постобработки, минимизировать необходимость участия человека в процессе, повысить эффективность и получить стабильное качество обработки от изделия к изделию.
Мы предложили решение для массовой полировки изделий, установку сухого электрохимического полирования Dlyte. На тот момент у нас было реализовано несколько проектов и огромное количество технологических тестов, и мы достаточно точно могли спрогнозировать результат обработки. Единственной загвоздкой являлся держатель деталей для обработки 96 изделий за раз — примерно такое количество два оператора успевали обработать за день. Наши технологи совместно с производителем разработали новый, на базе стандартного ювелирного держателя, причем даже с удвоенной вместимостью, что актуально для растущей компании.
Приведем цифры по проекту.
Во‑первых, удалось добиться шероховатости поверхности изделия на ответственных поверхностях Ra 0,08 мкм, ранее же, при ручной полировке, нельзя было даже приблизиться к таким цифрам. Во‑вторых, впервые получилось отполировать замок изделия, до этого элемент не полировался ввиду труднодоступности.
Время обработки в пересчете на единицу изделия сократилось более, чем в 5 раз: с 5 минут до 56 секунд. Сократилась в 3,36 раза стоимость полировки единицы изделия (без учета амортизации) при недельном объеме полирования 480 единиц. При увеличении недельного объема производства до 960 единиц и использовании увеличенного держателя стоимость сокращалась в 6,23 раза. Это позволило обрабатывать за один рабочий день весь объем напечатанных за неделю изделий и освободить оператору 32 часа в неделю для реализации других задач. Этап приемки качества полирования партии изделий сократился до 5 минут на всю партию.
Сократилась в 3,36 раза стоимость полировки единицы изделия (без учета амортизации) при недельном объеме полирования 480 единиц. При увеличении недельного объема производства до 960 единиц и использовании увеличенного держателя стоимость сокращалась в 6,23 раза. Это позволило обрабатывать за один рабочий день весь объем напечатанных за неделю изделий и освободить оператору 32 часа в неделю для реализации других задач. Этап приемки качества полирования партии изделий сократился до 5 минут на всю партию.
Таким образом, производственный цикл существенно сократился, а производительность выросла. Это позволило внедрить дополнительную линейку изделий, более дешевого ценового диапазона. Данная линейка долгое время была в планах компании, но ее ввод подразумевал существенное увеличение штата операторов, что влекло за собой дополнительные организационные сложности и расходы в связи с этим реализация проекта была отложена.
В результате проделанной работы был получен полностью автоматизированный, а самое важное, прогнозируемый процесс полировки изделия, стандартное качество от изделия к изделию независимо от партии.
В данном кейсе была использована самая маленькая установка Dlite серии 1 с объемом рабочей зоны 6 литров. Для сравнения — самая большая установка Dlyte больше описанной в 200 раз и имеет объем рабочей зоны 1200 литров.
Проведя огромное количество технологических тестов, мы можем с уверенностью заявить, что Dlyte — универсальный инструмент для финальной обработки и подходит как для полировки мелких изделий ювелирного типа, так и для партий крупногабаритных изделий, как, например, лопатка турбины. ■
Автор: Парфенов Дмитрий Андреевич, Евгений Кузьмин, TopStanok
Источник журнал «Аддитивные технологии» № 4-2019
Сухое электрохимическое полирование для обработки изделий после 3D-печати, TopStanok, журнал «Аддитивные технологии» № 4-2019, Технология DryLyte, решение для постобработки — TCT Awards, аддитивное производство, стоматологическая компания 3DMED, SLM
Способ электрохимического полирования серебра и его сплавов импульсным током
Авторы патента:
Галанин С. И.
И.
Гришина Е.П.
Иванова О.А.
C25F3/16 — полирование
Изобретение относится к области электрохимических методов финишной обработки поверхностей, а именно к способам электрохимического полирования сложнопрофильных поверхностей. Способ включает полирование в водном растворе тиосульфата натрия концентрацией 600-1300 г/л при 14-20°С импульсным униполярным током прямоугольной формы в течение 5-8 минут при следующих параметрах импульсов: длительность (2-5)10-3 секунд, скважность 1,25-3, амплитудная плотность тока 8-12 А/см2. Технический результат — повышение качества полирования поверхности серебра и его сплавов.
Изобретение относится к области электрохимических методов финишной обработки поверхностей, а именно к способам электрохимического полирования сложнопрофильных поверхностей.
Известен способ электрохимического полирования серебра в аммиачно-нитратном электролите при использовании постоянного тока анодной плотностью 10-15 А/дм2 [Электрохимическое полирование серебра в аммиачно-нитратном электролите/ Юзикис Л.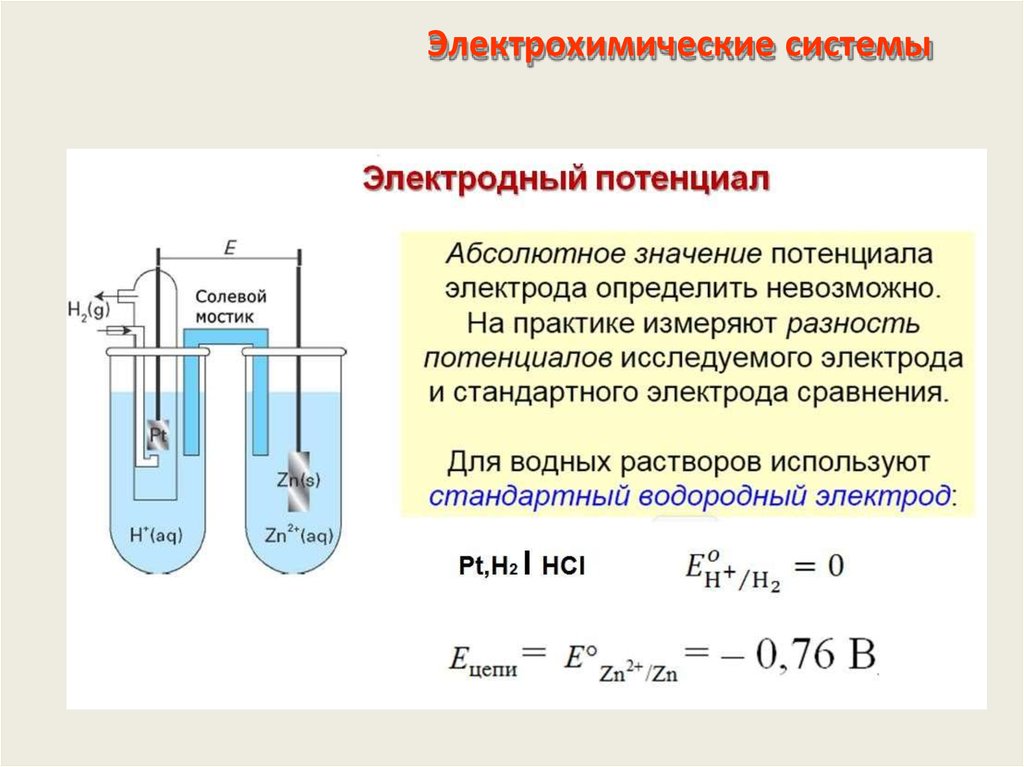 А., Янкаускас Т.Ю., Бучинскас Д.А. и др. // Журнал прикладной химии. 1979. т.52. №7. с.1659-1661].
А., Янкаускас Т.Ю., Бучинскас Д.А. и др. // Журнал прикладной химии. 1979. т.52. №7. с.1659-1661].
Недостатками известного способа являются:
— использование относительно недолговечного электролита с резким запахом;
— отсутствие рекомендаций по режимам полирования сплавов серебра, наиболее распространенных в ювелирной промышленности.
Наиболее близким к заявляемому техническому решению является способ электролитического полирования серебра в растворе тиосульфата натрия концентрацией 600-1300 г/л при плотности анодного тока 4-5 А/дм2 и температуре электролита 25°С [Никулин В.Н., Цыпин М.З. Электролитическая полировка серебра в растворах тиосульфата натрия// Журнал прикладной химии. 1960. т.39. №2. с.469-471] при рекомендациях полирования при прерывистом токе с продолжительностями периодов пребывания образца под током и без тока 4-5 сек при плотности тока 5-6 А/дм2 при температуре электролита 25°С (прототип).
Указанный способ имеет существенные недостатки в том, что, во-первых, не позволяет осуществлять полирование поверхности ювелирных сплавов на основе серебра с достаточным качеством; во-вторых, не обладает достаточной стабильностью воспроизведения качества поверхности.
Техническая задача изобретения — повышение качества полирования поверхности серебра и его сплавов.
Поставленная техническая задача достигается тем, что электрохимическое полирование производят в водном растворе тиосульфата натрия концентрацией 600-1300 г/л при 14-20°С импульсным униполярным током прямоугольной формы в течение 5-8 минут при следующих параметрах импульсов: длительность (2-5)10-3 секунд, скважность 1,25-3, амплитудная плотность тока 8-12 А/см2.
Суть способа можно пояснить следующим образом. Наилучшее качество обработанной поверхности обеспечивается при условии электрохимической обработки в области транспассивного анодного растворения. Поддержание анодной поверхности в этой области возможно только при использовании импульсов тока определенных амплитудно-временных параметров. Большая концентрация тиосульфата натрия, являющегося комплексообразователем для ионов серебра, позволяет формировать прианодный вязкий слой, экранирующий микровпадины на анодной поверхности. Это позволяет осуществлять преимущественное растворение микровыступов, приводящее к сглаживанию высоты микронеровностей поверхности и появлению блеска. Использованием коротких импульсов тока определенных амплитудно-временных параметров поддерживаются необходимые скорости этих процессов.
Поддержание анодной поверхности в этой области возможно только при использовании импульсов тока определенных амплитудно-временных параметров. Большая концентрация тиосульфата натрия, являющегося комплексообразователем для ионов серебра, позволяет формировать прианодный вязкий слой, экранирующий микровпадины на анодной поверхности. Это позволяет осуществлять преимущественное растворение микровыступов, приводящее к сглаживанию высоты микронеровностей поверхности и появлению блеска. Использованием коротких импульсов тока определенных амплитудно-временных параметров поддерживаются необходимые скорости этих процессов.
ПРИМЕРЫ КОНКРЕТНОГО ИСПОЛНЕНИЯ
1. Операция — электрохимическое полирование поверхности серебра Ср99. Электролит — водный раствор тиосульфата натрия концентрацией 600 г/л. Температура раствора 18°С. Продолжительность обработки 5 минут при следующих параметрах импульсов: длительность 210-3 сек, скважность 1,25, амплитудная плотность тока 8 А/см2.
В результате обработки показатели микрошероховатости поверхности изменились с RZ=0,20 мкм до RZ=0,02 мкм. Блеск поверхности изменился от 100 до 160% (по сравнению с исходной поверхностью).
2. Операция — электрохимическое полирование поверхности ювелирного сплава на основе серебра СрМ925. Электролит — водный раствор тиосульфата натрия концентрацией 1300 г/л. Температура раствора при 14°С. Продолжительность обработки составила 8 минут при следующих параметрах импульсов: длительность 310-3 сек, скважность 2, амплитудная плотность тока 10 А/см2.
В результате обработки показатели микрошероховатости поверхности изменились с RZ=0,35 мкм до RZ=0,05 мкм. Блеск поверхности изменился от 100 до 140% (по сравнению с исходной поверхностью).
Формула изобретения
Способ электрохимического полирования серебра и его сплавов импульсным током, осуществляемый в водном растворе тиосульфата натрия концентрацией 600-1300 г/л при 14-20°С, отличающийся тем, что полирование производят импульсным униполярным током прямоугольной формы в течение 5-8 мин при следующих параметрах импульсов: длительность (2-5)10-3 с, скважность 1,25-3, амплитудная плотность тока 8-12 А/см2.
Похожие патенты:
Способ импульсного электрохимического глянцевания золота и его сплавов // 2184801
Изобретение относится к области электрохимических методов финишной обработки поверхностей, а именно к способам электрохимического глянцевания сложнопрофильных поверхностей
Способ электрохимического полирования металлических изделий // 2168565
Электролит для электрохимической размерной обработки // 2163525
Изобретение относится к области машиностроения и может быть использовано, в частности, для электрохимической размерной обработки (ЭХРО) железокобальтникелевых сплавов
Способ полирования изделий // 2116391
Изобретение относится к электрохимической обработке и может быть применено в процессах электрополирования в различных областях техники: в электротехнической промышленности, в приборостроении, при производстве музыкальных инструментов и в декоративных целях в мебельной промышленности
Подвеска для полирования на механизированных линиях // 2090664
Изобретение относится к обработке поверхности металла, а именно к электрохимическому полированию на механизированных линиях с автооператорами, и может быть использовано для нанесения покрытий в гальваническом производстве, использующем механизированные или автоматизированные линии с автооператорами
Автоматизированный комплекс электроимпульсного полирования деталей // 2049163
Изобретение относится к электрохимической обработке деталей и может быть использовано для полирования изделий из различных металлических материалов, а также удаления заусенцев и скругления острых кромок в различных отраслях машиностроения, приборостроения и производства товаров народного потребления
Раствор для электрохимического полирования латуней // 2026894
Раствор для электрохимического полирования металлов // 2023767
Изобретение относится к электрохимической обработке металлов
Электролит для полирования металлов // 1832138
Способ электролитно — плазменного полирования изделий сложной формы // 1775508
Изобретение относится к электрохимическим методам обработки металлов, в частности к электролитно-плазменному полированию изделий сложной пространственной формы
Способ электрохимического полирования // 2229543
Изобретение относится к электрохимической обработке металлических изделий и может быть использовано в машиностроении и приборостроении, например, при доводке внутренних и наружных поверхностей
Способ изготовления полотенцесушителя // 2283903
Изобретение относится к технологии изготовления сантехнического отопительного оборудования и оборудования для сушки полотенец
Способ обработки отливок из сплавов на основе золота // 2284381
Изобретение относится к области электрохимических методов обработки поверхностей, а именно: к способам электрохимического полирования сложнопрофильных поверхностей отливок из сплавов на основе золота
Способ модификации поверхностного слоя металлических изделий // 2288300
Изобретение относится к области химико-физической обработки поверхностного слоя металлических изделий из титана и его сплавов с целью изменения их поверхностных свойств
Способ электрохимического полирования сплавов на основе золота импульсным биполярным током // 2288978
Изобретение относится к области электрохимических методов финишной обработки поверхностей, а именно к способам электрохимического полирования сложнопрофильных поверхностей
Способ изготовления микроострий // 2326992
Изобретение относится к методам изготовления микроострий и может быть использовано для изготовления зондов для туннельных микроскопов, точечных автоэлектронных источников, образцов для автоэмиссионной и атомно-зондовой микроскопии, микроманипуляторов для биологии
Ручной инструмент-электрод для электрохимического полирования // 2342472
Изобретение относится к области электрохимической обработки металлов и может применяться для ручного электрохимического полирования различных изделий, в том числе с пространственно-сложными поверхностями
Способ электролитно-плазменной обработки деталей // 2355828
Изобретение относится к электролитно-плазменной обработке, в частности полированию, металлических изделий из нержавеющих сталей, титана и титановых сплавов и может быть использовано в турбомашиностроении при полировании лопаток
Способ электролитно-плазменного полирования металлических изделий // 2355829
Изобретение относится к электролитно-плазменному полированию металлических изделий, преимущественно из хромосодержащих нержавеющих сталей и сплавов, а также титана и титановых сплавов, и может быть использовано в турбомашиностроении при обработке лопаток
Способ электролитно-плазменной обработки деталей // 2357019
Изобретение относится к электролитно-плазменному полированию металлических изделий и может быть использовано в турбомашиностроении при обработке рабочих и направляющих лопаток паровых турбин, лопаток газоперекачивающих установок и компрессоров газотурбинных двигателей
3.
 4.2. Трудовая функция \ КонсультантПлюс
4.2. Трудовая функция \ КонсультантПлюс
3.4.2. Трудовая функция
Наименование | Обработка сложных поверхностей с параметром шероховатости Ra 0,8 … 1,6 на электрохимическом станке | Код | D/02.4 | Уровень (подуровень) квалификации | 4 |
Происхождение трудовой функции | Оригинал | X | Заимствовано из оригинала | ||
Код оригинала | Регистрационный номер профессионального стандарта |
Трудовые действия | Запуск электрохимического станка для обработки сложных поверхностей с параметром шероховатости Ra 0,8 … 1,6 |
Обработка наружных и внутренних поверхностей сложной формы с параметром шероховатости Ra 0,8 . | |
Обработка тонкостенных и хрупких деталей | |
Электрохимическое полирование с шероховатостью ниже Ra 0,8 | |
Электрохимическая доводка деталей в размер | |
Контроль подачи, циркуляции и охлаждения электролита по системе ЧПУ | |
Контроль межэлектродного промежутка по системе ЧПУ | |
Подналадка станка во время обработки с корректировкой режимов обработки | |
Необходимые умения | Запускать электрохимический станок в рабочем режиме для обработки сложных поверхностей с параметром шероховатости Ra 0,8 … 1,6 |
Обрабатывать наружные и внутренние поверхности сложной формы с параметром шероховатости Ra 0,8 … 1,6 | |
Обрабатывать тонкостенные и хрупкие детали со сложными поверхностями | |
Выполнять электрохимическое полирование | |
Выполнять электрохимическую доводку деталей со сложными поверхностями в размер | |
Контролировать состояние электролита в зоне обработки | |
Контролировать состояние электролита в баке электрохимического станка | |
Производить подналадку электрохимического станка с корректировкой режимов обработки во время обработки | |
Пользоваться функциями контроля основных параметров электрохимической обработки системы ЧПУ | |
Контролировать работу источников питания | |
Менять полярность в зависимости от технологии обработки | |
Необходимые знания | Устройство и принцип работы электрохимических двух- и трехкоординатных станков с ЧПУ различных типов и мощностей |
Назначение основных механизмов и органов управления электрохимическими двух- и трехкоординатными станками с ЧПУ различных типов и мощностей | |
Кинематика электрохимических двух- и трехкоординатных станков с ЧПУ различных типов и мощностей | |
Способы и приемы обработки наружных и внутренних поверхностей сложной формы с параметром шероховатости Ra 0,8. | |
Особенности электрохимической обработки тонкостенных и хрупких конструкций | |
Системы цифровой индикации, применяемые в электрохимических станках | |
Системы ЧПУ, применяемые в электрохимических станках | |
Связь между режимами обработки, точностью и производительностью | |
Электроды-инструменты, применяемые при электрохимической доводке | |
Технология электрохимической доводки | |
Технология электрохимического полирования | |
Виды и характеристики электролитов, применяемых при электрохимическом полировании | |
Конструкции основных узлов электрохимических станков | |
Принцип действия различных электрических схем электрохимических станков | |
Влияние параметров электрохимической обработки на технологический процесс | |
Методы проверки электрических схем | |
Встроенные функции управления подачей электролита | |
Встроенные функции слежения за межэлектродным промежутком | |
Функции контроля электрического тока | |
Правила и способы подналадки электрохимических двух- и трехкоординатных станков с ЧПУ различных типов и мощностей | |
Особенности электрохимической обработки тонкостенных и хрупких конструкций | |
Особенности обработки с поливом и с погружением | |
Особенности работы с прямой и обратной полярностью | |
Особенности работы с постоянным и переменным током | |
Виды и правила применения средств индивидуальной и коллективной защиты при выполнении работ на электрохимических станках | |
Требования охраны труда, пожарной, промышленной, экологической безопасности и электробезопасности | |
Другие характеристики | — |
|
КАТЕГОРИИ: Археология
ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрации Техника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Балочные системы. Определение реакций опор и моментов защемления
|
⇐ ПредыдущаяСтр 25 из 28Следующая ⇒ Цель работы – изучение процесса электролиза, основных правил разряда ионов на электродах и количественных закономерностей при протекании электродных процессов. Знакомство с практикой электрохимических измерений. Практическое применение электролиза для электрохимического полирования металлов, исследование механизма этого процесса и определение параметров оптимального режима электрополирования, обеспечивающего наилучшее качество поверхности. Теоретическое введение Электролиз с растворимым анодом широко применяется для различных технологических целей, например для очистки металлов от примесей, электрофрезерования или для обработки поверхности металлов. В последнем случае в результате анодного растворения металлов при определенных значениях плотности тока и напряжения в электролизере, а также при применении электролитов определенного состава происходит выравнивание поверхности металла анода вплоть до зеркального блеска. При анодном растворении начиная с некоторых значений потенциалов электрода скорость растворения металла, т.е. количество ионов, переходящих в раствор в единицу времени, становится больше скорости отвода ионов. В результате в прианодном слое концентрация ионов металлов возрастает и образуется слой электролита с повышенной вязкостью, что приводит к уменьшению скорости движения ионов и к снижению общей величины тока. Однако толщина этого вязкого слоя не везде одинакова вследствие шероховатости поверхности металла, поэтому на ее выступах, где толщина слоя меньше, скорость растворения будет больше, что и приводит к выравниванию поверхности изделия. Факт образования вязкого слоя, а следовательно и возможности полирования, можно установить по вольт-амперной характеристике электролизера – зависимости . Наличие вязкого слоя, а также границы его существования определяются «провалом» на вольт-амперной кривой. Существование вязкого слоя, обеспечивающее эффект полирования, зависит не только от режима, например, от напряжения на клеммах электролитической ванны, но и от состава электролита. Как правило, для увеличения вязкости применяют очень концентрированные кислоты. Поэтому при работе с ними необходимо проявлять крайнюю осторожность. Ниже приводятся составы электролитов, применяемых для электрополирования наиболее распространенных металлов и сплавов: ● алюминий и его сплавы: фосфорная кислота H3PO4 – 60%; серная кислота H2SO4 – 40%. ● медь и ее сплавы: фосфорная кислота –75%, хромовый ангидрид Cr2O3 – 7,5%; ● никель и его сплавы: серная кислота – 70%; ● углеродистые и малолегированные стали: фосфорная кислота –75%, хромовый ангидрид – 5%; ● нержавеющие стали: фосфорная кислота – 43%, серная кислота –1,5%. При электрополировании в ряде случаев не удается добиться зеркальной поверхности по следующим причинам: 1) из-за образования питтингов (мест точечной коррозии) вследствие длительной задержки пузырьков кислорода на поверхности металла; 2) из-за образования непрозрачных и окрашенных плёнок, состоящих из оксидов или солей, вследствие неправильного режима электрополирования или неоптимального состава электролита; 3) из-за плохой предварительной механической обработки металла, оставляющей глубокие царапины на его поверхности; 4) из-за присутствия в электролите взвешенных частиц, которые дают направленное движение пузырькам кислорода, вследствие чего на поверхности металла образуются полосы.
Оборудование 1. Выпрямитель переменного тока ВС-24. 2. Электролизер со свинцовыми катодами и раствором электролита (70% Н2S04). 3. Миллиамперметр. 4. Милливольтметр. 5. Пластинки металла (Ni) для полирования (аноды). Последовательность выполнения работы 1. Собрать или проверить собранную схему установки для полирования (см. рис. 6.5). Электролизер и миллиамперметр, соблюдая полярность (анод А «+»; катод К «–»), следует подсоединить последовательно к выпрямителю. Милливольтметр подсоединяется к электролизеру параллельно. 2. Измерить с помощью линейки площадь поверхности никелевой пластинки с обеих сторон (см2) и зачистить пластинку наждачной бумагой. 3. Присоединить пластинку к аноду и погрузить в электролизер с электролитом. 4. Снять вольт-амперную характеристику анода, для этого поставить регулятор тока выпрямителя в крайнее левое положение и включить прибор.
Рис.
5. Рассчитать плотности тока (А/см2) и на миллиметровой бумаге построить зависимость плотности тока (ось ординат) от напряжения (ось абсцисс). 6. Представить график преподавателю для получения трех режимов полирования. 7. Для полирования использовать три никелевые пластинки. Зачистить их поверхность до одинакового состояния и отполировать каждую в течение трех минут в указанных режимах, следя за величиной напряжения. 8. Осторожно (кислота концентрированная!) извлечь образцы из зажима крышки электролизера, смыть остатки кислоты под слабой струей воды из водопроводного крана и промокнуть пластинки фильтровальной бумагой. 9. Визуально определить типы дефектов на поверхности металла и по состоянию лучшего образца определить оптимальный режим полирования, записать наблюдения в тетрадь. 10. Составить уравнения электрохимических процессов, протекающих на аноде и катоде электролизера. КОНТРОЛЬНЫЕ ВОПРОСЫ И ЗАДАЧИ 1. 2. Объясните механизм электрохимического полирования. 3. Какие дефекты могут возникнуть при электрополировании и в чем причина их возникновения? 4. Какие процессы протекают на аноде и катоде при полировании алюминия, меди, никеля и железа в кислых растворах? ⇐ Предыдущая19202122232425262728Следующая ⇒ Читайте также: Техника прыжка в длину с разбега Организация работы процедурного кабинета Области применения синхронных машин Оптимизация по Винеру и Калману | |||||||||||||||||||||||||||
|
|
Последнее изменение этой страницы: 2021-03-10; просмотров: 147; Нарушение авторского права страницы; Мы поможем в написании вашей работы!
infopedia.
|
Изготовление Ванны Электрохимической Полировки | с 1998
+375333902151
+74994040900
Гальванические
линии
Главная
статьи
Проекты
Контакты
Наше предприятие разрабатывает и изготавливает ванны
электрохимического и химического полирования. Основным материалом для изготовления ванн полирования является полипропилен (PP) футерованый Поливинилиденфторидом (PVDF, фторопласт), ванны небольшого размера производятся полностью из Фторопласта (PVDF) . В производстве емкостного оборудования мы используем исключительно листовые полимерные материалы фирмы SIMONA AG (Германия).
Принцип работы ванны полирования:
Оформить Заявку
Опросный лист
для заявки
Пример Комплектации и Конструкции Ванны полирования
Состав полирования (ТИПОВЫЕ), температурные режимы и требования к материалу ванны:
Этапы изготовления ванны полирования
1 ЭТАП | Техническое задание
Гальванические ванны разрабатываются и изготавливаются индивидуально — основываясь на техническом задании Заказчика.

Внутренние размеры ванн могут быть рассчитаны нашими специалистами по нормативам, основываясь на производительности и загрузки гальванической ванны, либо Заказчик предъявляет свои требования.
Применяемость излишних внутренних размеров ванн зачастую влечет удорожание стоимости емкостного оборудования, дополнительного и последующих эксплуатационных расходов.2 ЭТАП | разработка и согласование
Инженер-технологами по гальваническому оборудованию нашего предприятия определяются требуемая комплектация гальванической ванны, химическая стойкость к применяемому раствору и согласовывается спецификация оборудования с Заказчиком.
Конструкторским отделом производится расчет материалов и ребер жесткости в специализированном программном обеспечении. Разрабатываются чертежи для двухстороннего согласования и направления оборудования в производство.
3 ЭТАП | производство
Для изготовления ванн применяются современные технологии и технологическое оборудование, позволяющие из листовых полимерных материалов изготавливать ванны, не имеющие сварных угловых швов.
 Гнутые углы обечайки имеют ровную по структуре, не искаженную локальным тепловым воздействием внутреннюю поверхность. За счет исключения угловых сварных швов ванна имеет большую прочность и долговечность эксплуатации.
Гнутые углы обечайки имеют ровную по структуре, не искаженную локальным тепловым воздействием внутреннюю поверхность. За счет исключения угловых сварных швов ванна имеет большую прочность и долговечность эксплуатации.Емкостное оборудование из полимерных материалов мы производим используя исключительно материалы производства фирмы SIMONA AG (Германия).
4 ЭТАП | тестирование и контроль качества
На предприятии внедрена и функционирует с 2009 года система менеджмента качества на соответствие требованиям СТБ ISO 9001-2015, установлен контроль качества выпускаемой продукции
и производятся следующие виды Испытаний:- входной контроль;
- стендовые испытания;
- приемо-сдаточные;
- периодические.
Все испытания проводятся по программам, разработанной СООО «ФОРТЭКС – ВОДНЫЕ ТЕХНОЛОГИИ». Приемо-сдаточные испытания включают себя проверку на:
- соответствие габаритных размеров;
- недопущение трещин в сварных швах и остаточных деформаций;
- герметичность;
- выдержкой под испытательной нагрузкой (на днище, стенки)
5 ЭТАП | предварительная приемка
Мы всегда приглашаем наших Заказчиков произвести предварительную приемку оборудования на территории нашего предприятия пред его отгрузкой.
 Оборудование в полном комплекте выставляется в специально отведенном отапливаемом помещении или в одном из цехов. Возможна личная и дистанционная приемка оборудования.
Оборудование в полном комплекте выставляется в специально отведенном отапливаемом помещении или в одном из цехов. Возможна личная и дистанционная приемка оборудования.
Сертификаты производства:
Отзывы по гальваническим ваннам:
опросный лист
заполнить онлайн
Заполните онлайн!
полирование Деталей. Свойства и применение
Электрохимическое полирование — процесс анодной обработки изделий с дефектами (шероховатости, заусенцы и так далее) или без них, под действием электрического тока в растворах окислителей для их удаления и придания покрытию деталей декоративных и высоких коррозионных свойств, увеличения коэффициента отражения, прочности и других поверхностных характеристик.
Химическое полирование — процесс образования на поверхности изделия пассивных слоев, которые преимущественно растворяют выступы, обеспечивая сглаживания и выравнивания поверхности в растворах сильных окислителей, без применения электрического тока. Процесс сопровождается выделением газов и испарением паров основных компонентов растворов. Из-за этого срок службы электролитов химического полирование значительно короче, чем у электрохимического.
Процесс сопровождается выделением газов и испарением паров основных компонентов растворов. Из-за этого срок службы электролитов химического полирование значительно короче, чем у электрохимического.
Функции процесса полирования
- Придание декоративных свойств покрытию
- Очистка деталей между позициями
- Предварительная подготовка поверхности
- Выявление дефектов у готовых изделий
Полированию подвергаются детали различной конфигурации из благородных металлов, стали, медных и алюминиевых сплавов, реже полируются гальванические покрытия.
Химическое полирование в основном применяют при обработке деталей сложной конфигурации и больших размеров.
5 причин обратиться к нам
производство
с 1998 года
гарантия
2 года
15 000 м2
производства
поставили
свыше 100 ванн
опытные
специалисты
Бесплатная Консультация
Электронная почта*
Телефон
Похожее оборудование:
СООО «ФОРТЭКС-ВОДНЫЕ ТЕХНОЛОГИИ»
Республика Беларусь
Витебск, Терешковой 25А
Минск, Независимости 169
23 года производим оборудование для гальванических и химических предприятий
О Предприятии
Гальванические линии
Гальванические ванны
Гальваническое оборудование
Очистные сооружения
Наши проекты
Контактная информация
Свяжитесь с нами:
info@galvanoline. by
by
+375 33 390 21 51
+7 499 404 09 00
Copyright © 1998-2021 СООО «ФОРТЭКС-ВОДНЫЕ ТЕХНОЛОГИИ» Все Права Защищены.
Что такое электрополировка | Harrison Electropolishing
Электрополировка — это электрохимический процесс, при котором поверхностный материал удаляется путем анодного растворения. Электрополировка удаляет поверхностный материал, начиная с выступающих точек в пределах микроскопической текстуры поверхности. Удалив эти точки, процесс электрополировки улучшит качество поверхности металла, такого как нержавеющая сталь, никель и хастеллой, сделав поверхность более гладкой и отражающей. Общие детали и компоненты, подвергаемые электрополировке, включают резервуары, трубопроводы, фитинги, стержни, диски, крупные детали и поверхности и многое другое.
СВЯЖИТЕСЬ С НАМИ
Преимущества электрополировки
Преимущество электрополировки заключается в том, что она обеспечивает более гладкую, отражающую поверхность, что снижает адгезию продукта и улучшает очищаемость поверхности. Возможно, более важно то, что электрополировка предпочтительно растворяет свободное железо, включения и внедренные частицы с поверхности заготовки. Этот процесс улучшает приповерхностный химический состав материала и способствует формированию улучшенного коррозионностойкого поверхностного слоя.
Возможно, более важно то, что электрополировка предпочтительно растворяет свободное железо, включения и внедренные частицы с поверхности заготовки. Этот процесс улучшает приповерхностный химический состав материала и способствует формированию улучшенного коррозионностойкого поверхностного слоя.
Harrison Electropolishing — ведущий поставщик услуг по электрополировке для промышленных и высокочистых производств. С момента открытия в 1980 году мы постоянно работали над расширением и улучшением наших услуг. Сегодня, имея более 50 сотрудников и расширенный рабочий график, Harrison Electropolishing хорошо подходит для предоставления услуг электрополировки во множестве отраслей промышленности.
ПРОМЫШЛЕННЫЕ СТАНДАРТЫ
АСТМ Б912
Стандартные технические условия
для пассивации нержавеющей стали с использованием электрополировки
ПОЛУ F17
Спецификация
для высокочистых электрополированных трубок из нержавеющей стали 316L, трубных заглушек и фитингов, изготовленных из трубок
ПОЛУ F19
Спецификация для отделки смачиваемых поверхностей
компонентов из электрополированной нержавеющей стали 316LАСМЭ БПЭ
Спецификация для биотехнологического оборудования в фармацевтической промышленности, компонентов системы распределения или конвейерных лент
Процесс электрополировки
Электрополировка осуществляется путем создания электрохимической ячейки, в которой полируемый материал заряжается анодно. Катод сформирован так, чтобы отражать геометрию рабочей поверхности, и оба погружены в ванну с нагретым электролитом. При подаче постоянного тока электрический заряд вынуждает ионы металла растворяться с рабочей поверхности из нержавеющей стали. В зависимости от продолжительности процесса электрополировки и допусков на размеры детали, подлежащей электрополировке, количество материала, которое можно удалить, колеблется от 0,0003 дюйма до 0,003 дюйма.
Катод сформирован так, чтобы отражать геометрию рабочей поверхности, и оба погружены в ванну с нагретым электролитом. При подаче постоянного тока электрический заряд вынуждает ионы металла растворяться с рабочей поверхности из нержавеющей стали. В зависимости от продолжительности процесса электрополировки и допусков на размеры детали, подлежащей электрополировке, количество материала, которое можно удалить, колеблется от 0,0003 дюйма до 0,003 дюйма.
Перед электрополировкой
Ключом к процессу электрополировки является разница в плотности тока на поверхности. В пределах микроскопического профиля поверхности плотность тока выше в верхних точках и меньше в нижних. Скорость реакции электрополировки прямо пропорциональна плотности тока. Повышенная плотность тока в приподнятых точках заставляет металл растворяться быстрее в этих точках и, таким образом, имеет тенденцию к выравниванию материала поверхности. После обработки электрополировкой заготовка проходит ряд этапов для нейтрализации, промывки, очистки и сушки поверхностей.
Возможности электрополировки
Наши возможности позволяют обрабатывать детали любых размеров. В то время как большая часть технологического оборудования может поместиться в наших резервуарах для электрополировки, мы разработали запатентованные технологии для электрополировки более крупных компонентов. Эти запатентованные технологии позволяют нам обрабатывать оборудование любого размера на нашем предприятии или в полевых условиях.
Цех электрополировки
- Цех площадью 25 000 квадратных футов, расширенный и обновленный в 2021 г.
- Чистое помещение класса 1000 площадью 360 квадратных футов
- Четыре мостовых крана
- Грузоподъемность 15 000 фунтов
- Четыре стационарные линии электрополировки
- Расширенные рабочие баки
Применение электрополировки
Компания Harrison является лидером в области электрополировки для следующих отраслей и областей применения:
- Marine
- Paper & Pulp
- Petrochemical
- Pharmaceutical
- Semiconductor
- Oil & Gas
- Biotech
- Polymer
- Solar
- Nuclear
Benefits of Electropolishing
Learn more about some of the Преимущества электрополировки.
ЧИТАТЬ ДАЛЕЕ
Электрополировка нержавеющей стали
Нержавеющая сталь сочетает желаемые механические свойства с известным и проверенным уровнем коррозионной стойкости.
ЧИТАТЬ ДАЛЕЕ
Электрополировка никеля
Никелевые сплавы, включая хастеллой, инконель и монель, требуют особого внимания при электрополировке.
ЧИТАТЬ ДАЛЕЕ
Электрополировка Hastelloy
Электрополировка Hastelloy может обратить вспять неблагоприятные последствия деградации в реальных условиях производства и обработки.
ЧИТАТЬ ДАЛЕЕ
Спецификации ASME BPE
ASME-BPE — это ведущий стандарт проектирования и изготовления оборудования и систем, используемых в производстве биофармацевтических препаратов.
ЧИТАТЬ ДАЛЕЕ
Электрополировка конвейерных лент
Компания Harrison Electropolishing разработала и смонтировала систему непрерывной полировки, предназначенную для электрополировки конвейерных лент из нержавеющей стали.
ЧИТАТЬ ДАЛЕЕ
Портфолио электрополировки
Посмотрите наше портфолио работ по электрополировке.
ЧИТАТЬ ДАЛЕЕ
Исследование механизма электрохимического полирования меди с наблюдением за диффузией акцепторов воды
Введение
Электрохимическое полирование меди (ЭХП) представляет собой электрохимический процесс, который делает поверхность меди гладкой, когда медные электроды анодно поляризованы в электролитах ЭХП. Этот метод Cu ECP имеет несколько преимуществ, таких как процесс на основе раствора, в котором используется простое оборудование, селективность по отношению к проводящей подложке и отсутствие механических повреждений. Благодаря этим уникальным свойствам процесс Cu ECP можно использовать в различных приложениях для обработки поверхностей в косметических целях (Du and Suni, 2004), для подложек для выращивания графена (Zhang et al., 2012), для образцов TEM и EBSD ( Sun et al., 2005; Lapeire et al., 2013), а также для планаризации Cu в полупроводниковых соединениях (Chang et al., 2002; Chang et al., 2003; Padhi et al., 2003; Liu et al., 2005). ; Suni and Du, 2005; West et al., 2005; Liu et al., 2006; Liu et al., 2006). Несмотря на множество потенциальных возможностей Cu ECP, его фактические механизмы все еще остаются спорными.
Этот метод Cu ECP имеет несколько преимуществ, таких как процесс на основе раствора, в котором используется простое оборудование, селективность по отношению к проводящей подложке и отсутствие механических повреждений. Благодаря этим уникальным свойствам процесс Cu ECP можно использовать в различных приложениях для обработки поверхностей в косметических целях (Du and Suni, 2004), для подложек для выращивания графена (Zhang et al., 2012), для образцов TEM и EBSD ( Sun et al., 2005; Lapeire et al., 2013), а также для планаризации Cu в полупроводниковых соединениях (Chang et al., 2002; Chang et al., 2003; Padhi et al., 2003; Liu et al., 2005). ; Suni and Du, 2005; West et al., 2005; Liu et al., 2006; Liu et al., 2006). Несмотря на множество потенциальных возможностей Cu ECP, его фактические механизмы все еще остаются спорными.
Простой механизм ЭХП Cu в концентрированных растворах фосфорной кислоты был впервые предложен теорией вязких пленок Жаке (Jacquet, 1936). На подложке Cu образуется голубоватый вязкий слой, толщина которого различна между его выступами и впадинами. Эта разница означает, что сопротивления на выступах отличаются от сопротивлений во впадинах, и, следовательно, возникает ВТП. Эта теория была поставлена под сомнение теорией диффузии Элмора (Elmore, 1939; Elmore, 1940), согласно которой толщина диффузионного слоя ионов Cu от поверхности Cu до объема электролита различна на выступах и во впадинах. Эти разные толщины диффузионного слоя влияют на предельный ток реакции растворения Cu. В выступах предельный ток выше, а во впадинах меньше. Следовательно, эти явления вызывают ЭКП. Затем, в отличие от этой теории, Эдвардс (1953) предложенная теория акцепторной диффузии, в которой ECP определяется диффузией анионных акцепторов, таких как (PO 4 ) 3−, (HPO 4 ) 2− и (H 2 PO 4 ) − на поверхность меди из объема электролита. Скорости ECP зависят от диффузии акцепторов на поверхность Cu; скорость диффузии высока на выступах и низка во впадинах.
Эта разница означает, что сопротивления на выступах отличаются от сопротивлений во впадинах, и, следовательно, возникает ВТП. Эта теория была поставлена под сомнение теорией диффузии Элмора (Elmore, 1939; Elmore, 1940), согласно которой толщина диффузионного слоя ионов Cu от поверхности Cu до объема электролита различна на выступах и во впадинах. Эти разные толщины диффузионного слоя влияют на предельный ток реакции растворения Cu. В выступах предельный ток выше, а во впадинах меньше. Следовательно, эти явления вызывают ЭКП. Затем, в отличие от этой теории, Эдвардс (1953) предложенная теория акцепторной диффузии, в которой ECP определяется диффузией анионных акцепторов, таких как (PO 4 ) 3−, (HPO 4 ) 2− и (H 2 PO 4 ) − на поверхность меди из объема электролита. Скорости ECP зависят от диффузии акцепторов на поверхность Cu; скорость диффузии высока на выступах и низка во впадинах.
После тщательной оценки этих механизмов механизм соляной пленки и механизм акцептора воды стали считаться основными процессами, объясняющими поведение Cu ECP. Ландольт. (1987) впервые описал механизм соляной пленки, при котором соли осаждаются, когда концентрация ионов металлов на поверхности Cu, образующаяся в результате реакции растворения, превышает предел растворимости; на поверхности Cu образуется пленка осажденной соли. Из-за этой солевой пленки растворение металла ограничивается диффузией ионов металла из пленки в объем электролита. Напротив, механизм акцептора воды аналогичен теории акцепторной диффузии Эдварда, за исключением того, что акцептором является вода, а не анионные акцепторы. И в отличие от соляно-пленочного механизма, наиболее важным фактором полирующего эффекта является не диффузия ионов меди в объем электролита, а диффузия акцепторов воды на поверхность меди.
Ландольт. (1987) впервые описал механизм соляной пленки, при котором соли осаждаются, когда концентрация ионов металлов на поверхности Cu, образующаяся в результате реакции растворения, превышает предел растворимости; на поверхности Cu образуется пленка осажденной соли. Из-за этой солевой пленки растворение металла ограничивается диффузией ионов металла из пленки в объем электролита. Напротив, механизм акцептора воды аналогичен теории акцепторной диффузии Эдварда, за исключением того, что акцептором является вода, а не анионные акцепторы. И в отличие от соляно-пленочного механизма, наиболее важным фактором полирующего эффекта является не диффузия ионов меди в объем электролита, а диффузия акцепторов воды на поверхность меди.
Между этими двумя механизмами механизм акцептора воды был более признан исследованиями электрохимической импедансной спектроскопии (ЭИС) (Glarum and Marshall, 1985a, Glarum and Marshall, 1985b; Vidal and West, 1995a, Vidal and West, 1995b), которые показали, что обедненный водой слой действует как вязкая пленка, поэтому решающим фактором становится реакция управления массопереносом акцепторов воды. Вагнер. (1954) математически проанализировали идеальный процесс ЭХП Cu, основанный на механизме акцептора воды, и различные другие исследования предложили механизмы для объяснения поведения ЭХП Cu (Hoar and Rothwell, 19).64; Кодзима и Тобиас, 1973 год; Pointu и др., 1981; Pointu et al., 1983a, Pointu et al., 1983b). Механизм акцептора воды остается наиболее приемлемым на основе предыдущих исследований. Однако механизмы ЭХП Cu все еще остаются спорными, поскольку процесс ЭХП сложен, и на процесс влияет множество факторов, таких как ион металла, анионы и акцепторы. Поэтому необходимы новые анализы для прямого объяснения и подтверждения поведения ЭХП Cu.
Вагнер. (1954) математически проанализировали идеальный процесс ЭХП Cu, основанный на механизме акцептора воды, и различные другие исследования предложили механизмы для объяснения поведения ЭХП Cu (Hoar and Rothwell, 19).64; Кодзима и Тобиас, 1973 год; Pointu и др., 1981; Pointu et al., 1983a, Pointu et al., 1983b). Механизм акцептора воды остается наиболее приемлемым на основе предыдущих исследований. Однако механизмы ЭХП Cu все еще остаются спорными, поскольку процесс ЭХП сложен, и на процесс влияет множество факторов, таких как ион металла, анионы и акцепторы. Поэтому необходимы новые анализы для прямого объяснения и подтверждения поведения ЭХП Cu.
Соответственно, в этой статье мы сообщаем о механизмах и поведении Cu ECP с использованием традиционных методов электрохимического анализа и нового метода электрохимического анализа. Таким образом, было проведено сравнение и изучение электрохимического поведения ЭХП Cu при различных потенциалах ЭХП. В дополнение к этим обычным анализам количество воды на различных расстояниях от подложки Cu оценивали путем измерения токов реакции электролиза воды с использованием системы сканирующей электрохимической микроскопии (СЭХМ) для прямого наблюдения и проверки поведения ЭХП Cu на основе акцептора воды. механизм. Основываясь на данных, мы здесь обсуждаем механизмы, поведение и критические факторы Cu ECP.
механизм. Основываясь на данных, мы здесь обсуждаем механизмы, поведение и критические факторы Cu ECP.
Материалы и методы
Сначала мы провели типичный анализ и эксперименты в ячейке объемом 100 мл с обычной трехэлектродной системой. Трехэлектродная система состояла из электроосажденной медной подложки в качестве рабочего электрода, покрытой платиной титановой пластины в качестве противоэлектрода и насыщенного электрода Ag/AgCl (3M насыщенного KCl) в качестве электрода сравнения. Для изготовления рабочих электродов затравочные слои Ti (20 нм)/Cu (200 нм) наносили на пластину Si методом испарения, а пленку Cu гальваностатически осаждали при -50 мА/см 9 .0167 2 на 300 с на подложках Si/Ti (20 нм)/Cu (200 нм) площадью 1 × 1 см 2 .
Химические вещества реактивной чистоты использовались для всех экспериментов по электроосаждению Cu и Cu ECP. Электролиты для электроосаждения Cu состояли из 1,0 М сульфата меди (CuSO 4 , 99,5%, YAKURI, Япония), 0,58 М серной кислоты (H 2 SO 4 , 95%, Daejung Chemicals & Metals, Корея), и 1,9 мМ соляной кислоты (HCl, 35%, Daejung Chemicals & Metals, Корея) в 100 мл деионизированной воды с сопротивлением 18,6 МОм. 85% фосфорных кислот (H 3 PO 4 ) использовались в качестве электролитов для Cu ECP.
85% фосфорных кислот (H 3 PO 4 ) использовались в качестве электролитов для Cu ECP.
Традиционный электрохимический анализ, осаждение и полировку проводили с использованием потенциостата/гальваностата (VersaSTAT 4, AMETEK Inc., США). Для анализа электрохимического поведения и соответствующего выбора потенциала ECP был проведен анализ LSV в диапазоне потенциалов от потенциала разомкнутой цепи (OCP) до 2,5 В относительно Ag/AgCl со скоростью сканирования 10 мВ/с без перемешивания. После подбора потенциалов ВТП 0,25, 0,375, 0,50, 0,90 и 1,30 В, подложки Cu электрохимически полировали при потенциале 1,3 В в 85%-ной фосфорной кислоте без перемешивания. Поверхности электрохимически полированных медных подложек исследовали с помощью сканирующей электронной микроскопии с полевой эмиссией (FESEM; MIRA3, TESCAN Orsay Holding, a.s., Чехия). Анализ EIS также проводился при выбранных потенциалах ECP с амплитудой 10 мВ в диапазоне частот от 50 кГц до 10 Гц, чтобы понять поведение Cu ECP. EIS и SECM были выполнены после «предварительного кондиционирования», при котором выбранный потенциал применялся в течение 60 с к подложкам Cu в фосфорной кислоте, чтобы установить стационарное состояние интерфейса на подложках Cu (Grimm et al., 19).92).
EIS и SECM были выполнены после «предварительного кондиционирования», при котором выбранный потенциал применялся в течение 60 с к подложкам Cu в фосфорной кислоте, чтобы установить стационарное состояние интерфейса на подложках Cu (Grimm et al., 19).92).
Для оценки количества акцепторов воды на различных расстояниях от медной подложки были измерены токи электролиза с помощью электрохимического сканирующего зонда системы SECM. Конфигурация ячейки для этого анализа показана на рисунке 1. Электроды состояли из наконечника Pt (диаметр 10 мкм) и медной подложки для рабочего электрода, Pt-провода для противоэлектрода и электрода Ag/AgCl (3 M KCl насыщенный) для электрода сравнения. Наконечник Pt и подложка Cu располагались вместе с каждым потенциостатом в качестве рабочих электродов. Эти конфигурации были идентичны типичной конфигурации анализа SECM. На основе конфигурации электродов растворы и реакции для анализа проиллюстрированы на рисунке 2. Для анализа растворов использовали 85% фосфорную кислоту, и детали процесса следующие. Во-первых, когда потенциал подложки Cu был приложен к 0,25 ~ 1,3 В, реакция растворения Cu происходила на поверхности подложки Cu с этими двухэтапными реакциями (Matlosz et al., 19).94; Han and Fang, 2019):
Во-первых, когда потенциал подложки Cu был приложен к 0,25 ~ 1,3 В, реакция растворения Cu происходила на поверхности подложки Cu с этими двухэтапными реакциями (Matlosz et al., 19).94; Han and Fang, 2019):
Cu→Cuad2++2e−(1)
Cuad2++6H2O→[Cu(h3O)6]2+(2)
РИСУНОК 1 . Схема конфигурации ячейки для измерения тока электролиза воды с использованием системы SECM.
РИСУНОК 2 . Схема измерения электродных реакций для измерения тока электролиза воды в системе SECM. Ионы Cu растворялись из подложки Cu при приложении потенциала от 0,25 до 1,3 В. Молекулы воды гидратировали растворенные ионы Cu. Выделение кислорода происходит на наконечнике Pt приложенным потенциалом 3,5 В после предварительного кондиционирования в течение 60 с. Наконечник Pt перемещался со скоростью сканирования 5 мкм/с.
После 60 с предварительного кондиционирования к медной подложке был приложен потенциал наконечника Pt до 3,5 В для достижения устойчивого состояния диффузии акцептора воды. Реакция выделения кислорода в результате разложения воды происходила на поверхности зонда с платиновым наконечником со следующей реакцией: величины, и эти токи были измерены на различных расстояниях от наконечника Pt до подложки Cu. Начальное расстояние наконечника от подложки Cu было установлено равным 1 мкм, чтобы предотвратить протекание постоянного тока между наконечником Pt и подложкой Cu; затем расстояние до кончика варьировалось от 1 мкм до 1500 мкм при скорости сканирования 5 мкм/с. Все электрохимические анализы проводили при 20°С.
Реакция выделения кислорода в результате разложения воды происходила на поверхности зонда с платиновым наконечником со следующей реакцией: величины, и эти токи были измерены на различных расстояниях от наконечника Pt до подложки Cu. Начальное расстояние наконечника от подложки Cu было установлено равным 1 мкм, чтобы предотвратить протекание постоянного тока между наконечником Pt и подложкой Cu; затем расстояние до кончика варьировалось от 1 мкм до 1500 мкм при скорости сканирования 5 мкм/с. Все электрохимические анализы проводили при 20°С.
Результаты и обсуждение
LSV представляет собой фундаментальный и мощный метод анализа для изучения электрохимического поведения Cu ECP. Поэтому мы сначала провели анализ LSV в 85% фосфорной кислоте, и полученная вольтамперограмма показана на рисунке 3. В начальном диапазоне потенциалов анодный ток начал увеличиваться до 0,375 В. Согласно Shieh et al. (2004), эти анодные токи в этом диапазоне потенциалов связаны с прямым растворением меди, что приводит к тусклым протравленным поверхностям. При превышении 0,375 В анодный ток снижался до 0,50 В. Это явление указывает на образование пассивирующего слоя на поверхности анода. Когда потенциал ЭХП был приложен выше 0,50 В, ток оставался почти постоянным до 1,7 В. Эта область плато тока обычно считается реакцией Cu ЭХП (Jacquet, 19).36; Элмор, 1939 год; Гларум и Маршалл, 1985а; Ландольт, 1987; Хан и Фанг, 2019). После этого плато тока ток снова увеличился от потенциала выше 1,7 В за счет реакции выделения кислорода (Shieh et al., 2004), что вызвало серьезные ямки травления.
При превышении 0,375 В анодный ток снижался до 0,50 В. Это явление указывает на образование пассивирующего слоя на поверхности анода. Когда потенциал ЭХП был приложен выше 0,50 В, ток оставался почти постоянным до 1,7 В. Эта область плато тока обычно считается реакцией Cu ЭХП (Jacquet, 19).36; Элмор, 1939 год; Гларум и Маршалл, 1985а; Ландольт, 1987; Хан и Фанг, 2019). После этого плато тока ток снова увеличился от потенциала выше 1,7 В за счет реакции выделения кислорода (Shieh et al., 2004), что вызвало серьезные ямки травления.
РИСУНОК 3 . Линейная скан-вольтамперограмма субстрата Cu в 85% фосфорной кислоте. Развертку выполняли со скоростью сканирования 10 мВ/с.
В дополнение к интерпретации предыдущих работ мы выбрали пять потенциальных точек для точной интерпретации результатов LSV: 1) 0,25 В как потенциал до точки пика, 2) 0,375 В как потенциал в точке пика, 3) 0,50 V как потенциал после точки пика, 4) 0,90 В и 5) 1,30 В как потенциалы в области плато. Затем подложки Cu были анодно поляризованы в пяти потенциальных точках с плотностью заряда 2,5 Кл/см 2 ; их верхние СЭМ-изображения представлены на рис. 4. По сравнению с СЭМ-изображениями Cu-подложки до поляризации (рис. 4A) эффект Cu ECP наблюдался при всех потенциалах ECP (рис. 4C–F), за исключением 0,25 В, где тускло наблюдалась протравленная медь (рис. 4В). Эти результаты показывают, что реакция растворения Cu на Cu-подложке или на границе раздела между Cu-подложкой и фосфорной кислотой начала изменяться по пиковому потенциалу. Соответственно, мы проанализировали разницу в реакциях растворения или межфазных условиях между потенциалом до точки пика и потенциалами после точки пика.
Затем подложки Cu были анодно поляризованы в пяти потенциальных точках с плотностью заряда 2,5 Кл/см 2 ; их верхние СЭМ-изображения представлены на рис. 4. По сравнению с СЭМ-изображениями Cu-подложки до поляризации (рис. 4A) эффект Cu ECP наблюдался при всех потенциалах ECP (рис. 4C–F), за исключением 0,25 В, где тускло наблюдалась протравленная медь (рис. 4В). Эти результаты показывают, что реакция растворения Cu на Cu-подложке или на границе раздела между Cu-подложкой и фосфорной кислотой начала изменяться по пиковому потенциалу. Соответственно, мы проанализировали разницу в реакциях растворения или межфазных условиях между потенциалом до точки пика и потенциалами после точки пика.
РИСУНОК 4 . СЭМ-изображения анодно поляризованных подложек Cu в 85% фосфорной кислоте при различных потенциалах с плотностью заряда 2,5 Кл/см 2 : (A) до поляризации, (B) 0,25 В, (C) 0,375 V, (D) 0,50 В, (E) 0,90 В и (F) 1,30 В. 1985a, Гларум и Маршалл, 19 лет.85б; Ландольт, 1987; Видал и Уэст, 1995а, Видал и Уэст, 1995b). Одной из них является модель соляной пленки, в которой соли Cu осаждаются на подложке Cu, когда растворение Cu превышает предел растворения солей Cu. Другая модель — это модель диффузии акцепторов воды, в которой акцепторы воды распространяются по направлению к подложке из меди. Однако в обеих моделях механизм ECP все еще остается спорным. Поэтому, чтобы точно определить состояние интерфейса поверхности меди во время ЭХП, мы провели анализ ЭИС в пяти потенциальных точках, описанных ранее.
1985a, Гларум и Маршалл, 19 лет.85б; Ландольт, 1987; Видал и Уэст, 1995а, Видал и Уэст, 1995b). Одной из них является модель соляной пленки, в которой соли Cu осаждаются на подложке Cu, когда растворение Cu превышает предел растворения солей Cu. Другая модель — это модель диффузии акцепторов воды, в которой акцепторы воды распространяются по направлению к подложке из меди. Однако в обеих моделях механизм ECP все еще остается спорным. Поэтому, чтобы точно определить состояние интерфейса поверхности меди во время ЭХП, мы провели анализ ЭИС в пяти потенциальных точках, описанных ранее.
На рис. 5 показаны схематические графики Найквиста во всем диапазоне частот, где R s — растворное сопротивление от левой точки пересечения полуокружности, R p — поляризационное сопротивление от диаметра полуокружности, а C dl — емкость двойного слоя, рассчитанная из соотношения ω max = 1/R p C дл . ω max представляет частоту, когда Z img имеет максимальное значение в полукруге. В области низких частот угол линии увеличился примерно с 45 o до 90 o (по вертикали) по мере увеличения потенциала полировки. Этот результат может быть связан с диффузией акцептора воды и будет обсуждаться позже. Графики Найквиста для Cu ECP в 85% фосфорной кислоте в соответствии с потенциалом ECP были получены при двух временах предварительного кондиционирования, 0 с и 60 с, что соответствует фигуре 6A и фигуре 6B соответственно.
В области низких частот угол линии увеличился примерно с 45 o до 90 o (по вертикали) по мере увеличения потенциала полировки. Этот результат может быть связан с диффузией акцептора воды и будет обсуждаться позже. Графики Найквиста для Cu ECP в 85% фосфорной кислоте в соответствии с потенциалом ECP были получены при двух временах предварительного кондиционирования, 0 с и 60 с, что соответствует фигуре 6A и фигуре 6B соответственно.
РИСУНОК 5 . Схематический график Найквиста в соответствии с частотным диапазоном.
РИСУНОК 6 . Графики Найквиста для медных подложек при различных потенциалах полировки в 85% фосфорной кислоте, измеренные в соответствии со временем предварительной обработки (A) 0 с и (B) 60 с. Частоты были установлены в диапазоне от 50 кГц до 10 Гц.
Результаты подгонки графиков Найквиста обобщены в таблице 1. В области высоких частот значения R с почти соответствовали 6,0 Ом см 2 независимо от потенциала полировки и времени предварительной обработки. Эти результаты, то есть R s не изменились, свидетельствовали о диффузии акцепторов воды, поскольку в модели соляной пленки R s изменялись в зависимости от полирующего потенциала (Vidal and West, 1995a). Однако R p увеличивался, а C dl уменьшался по мере увеличения анодного потенциала. Эти изменения R p и C dl с различными полирующими потенциалами отличались от результатов EIS водоакцепторного механизма, измеренных Видалем и Вестом (19).95а). Наши значения R p и C dl изменялись при изменении времени предварительного кондиционирования. Эти изменения, связанные с потенциалами и временем прекондиционирования, можно объяснить изменениями как толщины соляной пленки, так и толщины обедненного слоя в модели соляной пленки и модели акцептора воды соответственно (Grimm et al., 1992).
Эти результаты, то есть R s не изменились, свидетельствовали о диффузии акцепторов воды, поскольку в модели соляной пленки R s изменялись в зависимости от полирующего потенциала (Vidal and West, 1995a). Однако R p увеличивался, а C dl уменьшался по мере увеличения анодного потенциала. Эти изменения R p и C dl с различными полирующими потенциалами отличались от результатов EIS водоакцепторного механизма, измеренных Видалем и Вестом (19).95а). Наши значения R p и C dl изменялись при изменении времени предварительного кондиционирования. Эти изменения, связанные с потенциалами и временем прекондиционирования, можно объяснить изменениями как толщины соляной пленки, так и толщины обедненного слоя в модели соляной пленки и модели акцептора воды соответственно (Grimm et al., 1992).
ТАБЛИЦА 1 . Подгонка результатов графиков Найквиста в зависимости от времени предварительного кондиционирования и приложенных потенциалов.
На низкочастотные области наших графиков Найквиста значительное влияние оказали потенциалы и время предварительной обработки. Когда графики Найквиста были получены при применении полирующих потенциалов без предварительного кондиционирования (рис. 6А), линия в низкочастотной области начала демонстрировать импеданс Варбурга от 0,50 до 1,30 В. Угол изменился до 90° в низкочастотных областях, когда полирующие потенциалы превышали 0,90 В. На графиках Найквиста, полученных при времени предварительного кондиционирования 60 с (рис. 6B), импеданс Варбурга наблюдался по пиковому потенциалу, 0,375 В, как видно на рис. 3. Когда мы сравнили графики Найквиста в условиях 0,375 В между временами предварительного кондиционирования 0 с (рис. 6А) и 60 с (рис. 6В), ЭХП меди происходила, когда реакция растворения меди регулировалась реакцией управления массопереносом воды. акцепторы. Вертикальные линии наблюдались, когда анодные потенциалы превышали 0,50 В.
Эти результаты подтвердили, что все линии низкочастотной области связаны с процессом диффузии из-за импеданса Варбурга. В частности, вертикальные линии в низкочастотной области при высоких потенциалах ЭКП были связаны с элементами Варбурга конечного пространства (FSW), в которых условием диффузии является ограниченный диффузионный слой и ограниченное электроактивное вещество (Oldenburger et al., 2019). ). Это указывало на два возможных условия диффузии, одно из которых представляет собой пористую соляную пленку, а другое — обедненный водоакцепторный слой (Гримм и др., 19).92; Матлош и др., 1994). Однако в предыдущих отчетах Видала и Уэста не было пояснений по поводу низкочастотной области. (1995a), Видаль и Уэст. (1995b), поэтому до сих пор неясно, какой механизм был правильным. Для интерпретации этих результатов потребовался дополнительный анализ, поэтому мы разработали новый метод анализа, который может непосредственно наблюдать диффузию акцепторов воды.
В частности, вертикальные линии в низкочастотной области при высоких потенциалах ЭКП были связаны с элементами Варбурга конечного пространства (FSW), в которых условием диффузии является ограниченный диффузионный слой и ограниченное электроактивное вещество (Oldenburger et al., 2019). ). Это указывало на два возможных условия диффузии, одно из которых представляет собой пористую соляную пленку, а другое — обедненный водоакцепторный слой (Гримм и др., 19).92; Матлош и др., 1994). Однако в предыдущих отчетах Видала и Уэста не было пояснений по поводу низкочастотной области. (1995a), Видаль и Уэст. (1995b), поэтому до сих пор неясно, какой механизм был правильным. Для интерпретации этих результатов потребовался дополнительный анализ, поэтому мы разработали новый метод анализа, который может непосредственно наблюдать диффузию акцепторов воды.
Чтобы наблюдать за диффузией акцепторов воды на различных расстояниях от подложки Cu, мы измерили ток электролиза воды в результате реакции выделения кислорода с помощью системы SECM. Конфигурация ячейки измерительной системы и схема метода измерения представлены на рис. 1, 2 соответственно. В трехэлектродной системе в измерительную ячейку устанавливались два рабочих электрода (Pt-наконечник и Cu-подложка). На подложке Cu реакция растворения Cu происходила при анодном приложении потенциалов. На концевом Pt-электроде количество акцепторов воды оценивали с помощью реакции выделения кислорода, которая наблюдалась в LSV на рисунке 3, когда потенциалы превышали 1,7 В. Поэтому потенциал на концевом Pt-электроде был установлен на 3,5 В для достаточный электролиз остальных акцепторов воды, и реакция выделения кислорода могла происходить без растворения платинового электрода.
Конфигурация ячейки измерительной системы и схема метода измерения представлены на рис. 1, 2 соответственно. В трехэлектродной системе в измерительную ячейку устанавливались два рабочих электрода (Pt-наконечник и Cu-подложка). На подложке Cu реакция растворения Cu происходила при анодном приложении потенциалов. На концевом Pt-электроде количество акцепторов воды оценивали с помощью реакции выделения кислорода, которая наблюдалась в LSV на рисунке 3, когда потенциалы превышали 1,7 В. Поэтому потенциал на концевом Pt-электроде был установлен на 3,5 В для достаточный электролиз остальных акцепторов воды, и реакция выделения кислорода могла происходить без растворения платинового электрода.
Сначала к подложке из меди прикладывали потенциал в течение 60 с (предварительное кондиционирование, описанное ранее). Затем к платиновому наконечнику подавали потенциал и измеряли ток платинового острия при перемещениях от поверхности подложки Cu к объему электролита. Два профиля электролиза воды из этого эксперимента представлены на рисунке 7. Профили расстояния между наконечником и током наконечника и профили расстояния I V / I OCP (средн.) до наконечника показаны в левой и правой частях рисунка. 7 соответственно. я V /I OCP (Avg.) — расстояние между наконечником — это отношение тока наконечника при приложенном потенциале «V» на медной подложке и среднего тока наконечника при потенциале разомкнутой цепи (OCP) медной подложки.
Профили расстояния между наконечником и током наконечника и профили расстояния I V / I OCP (средн.) до наконечника показаны в левой и правой частях рисунка. 7 соответственно. я V /I OCP (Avg.) — расстояние между наконечником — это отношение тока наконечника при приложенном потенциале «V» на медной подложке и среднего тока наконечника при потенциале разомкнутой цепи (OCP) медной подложки.
РИСУНОК 7 . Профили токов электролиза воды, измеренные с помощью SECM в 85% фосфорной кислоте (слева) токов наконечника и (справа) I V /I OCP (СРЕДН.) на расстоянии наконечника от подложки Cu. Я В и Я OCP означают токи наконечника при приложенном потенциале «V» и OCP подложки Cu. Система измерения показана на рис. 2.
Эти профили показали, что профиль тока зонда меняется в зависимости от потенциала медной подложки. В ОКП подложки Cu ток был практически постоянным независимо от положения концевого электрода, так как акцепторы воды на реакцию растворения Cu не расходовались. По мере увеличения потенциалов ВТП на подложке из меди токи острия уменьшались; токи наконечника на поверхности Cu (расстояние между наконечником Pt и подложкой Cu: 1 мкм) составляли 590 нА, 200 нА, 72 нА, 45 нА, 23 нА и 21 нА, когда потенциал ECP был OCP, 0,25, 0,375, 0,50, 0,90 и 1,30 В соответственно. Токи наконечника увеличивались, когда наконечник Pt перемещался в направлении объема электролита при всех анодных потенциалах. Эти результаты показали, что на количество акцепторов воды влияли потенциалы ECP, потому что величина тока наконечника пропорциональна количеству акцепторов воды. Таким образом, профили свидетельствовали о механизме диффузии акцепторов воды.
По мере увеличения потенциалов ВТП на подложке из меди токи острия уменьшались; токи наконечника на поверхности Cu (расстояние между наконечником Pt и подложкой Cu: 1 мкм) составляли 590 нА, 200 нА, 72 нА, 45 нА, 23 нА и 21 нА, когда потенциал ECP был OCP, 0,25, 0,375, 0,50, 0,90 и 1,30 В соответственно. Токи наконечника увеличивались, когда наконечник Pt перемещался в направлении объема электролита при всех анодных потенциалах. Эти результаты показали, что на количество акцепторов воды влияли потенциалы ECP, потому что величина тока наконечника пропорциональна количеству акцепторов воды. Таким образом, профили свидетельствовали о механизме диффузии акцепторов воды.
Используя эти профили электролиза воды и доказанный механизм диффузии акцепторов воды, можно также объяснить результаты LSV и EIS. В LSV на рисунке 3 явление полировки возникало при пиковом потенциале 0,375 В. Такое поведение LSV может показаться поведением анодной пассивации, но этот пик возник из-за истощения акцепторов воды. Кроме того, явления полировки наблюдались после потенциальной области, в которой происходило истощение и диффузия акцепторов воды на поверхности Cu; следовательно, диффузия акцептора воды была тесно связана с эффектами полировки Cu. Результаты графиков Найквиста (рис. 6) также можно объяснить диффузией акцепторов воды. В области высоких частот C dl уменьшался, а R p увеличивался по мере увеличения потенциала ВТП, поскольку толщина диффузионного слоя акцептора воды увеличивалась при увеличении потенциала ВКФ. Поэтому сложность реакции растворения Cu увеличивалась из-за недостаточного количества акцепторов воды. Наличие вертикальной линии в низкочастотной области указывает на то, что эти условия соответствуют условию диффузии СТП, при котором вязко-диффузионный слой и акцепторы воды были согласованы со слоем ограниченной диффузии и электроактивным веществом, ограниченным водой, соответственно. Следовательно, диффузионное поведение FSW было вызвано этим значительным и вязким диффузионным слоем акцепторов воды.
Кроме того, явления полировки наблюдались после потенциальной области, в которой происходило истощение и диффузия акцепторов воды на поверхности Cu; следовательно, диффузия акцептора воды была тесно связана с эффектами полировки Cu. Результаты графиков Найквиста (рис. 6) также можно объяснить диффузией акцепторов воды. В области высоких частот C dl уменьшался, а R p увеличивался по мере увеличения потенциала ВТП, поскольку толщина диффузионного слоя акцептора воды увеличивалась при увеличении потенциала ВКФ. Поэтому сложность реакции растворения Cu увеличивалась из-за недостаточного количества акцепторов воды. Наличие вертикальной линии в низкочастотной области указывает на то, что эти условия соответствуют условию диффузии СТП, при котором вязко-диффузионный слой и акцепторы воды были согласованы со слоем ограниченной диффузии и электроактивным веществом, ограниченным водой, соответственно. Следовательно, диффузионное поведение FSW было вызвано этим значительным и вязким диффузионным слоем акцепторов воды. Эти новые электрохимические измерения выявили схему механизма ЭХП Cu, которая представлена на рисунке 8. В исходном состоянии ЭХП Cu (рис. 8A), когда к подложке Cu прикладывался потенциал выше 0,375 В, происходили значительные реакции растворения Cu как в выступы и впадины субстрата Cu, потому что многие акцепторы воды гидратировали ионы Cu. Однако концентрация акцепторов воды на поверхности Cu быстро уменьшалась по мере приложения потенциала; акцепторы воды в конечном итоге истощались из-за гидратации ионов Cu, а реакция растворения Cu регулировалась реакцией управления переносом массы акцепторов воды. Следовательно, акцепторы воды преимущественно распространялись на выступы поверхности, которые растворялись быстрее, чем впадины (рис. 8В). В результате быстрого растворения на выступах поверхность Cu сглаживалась.
Эти новые электрохимические измерения выявили схему механизма ЭХП Cu, которая представлена на рисунке 8. В исходном состоянии ЭХП Cu (рис. 8A), когда к подложке Cu прикладывался потенциал выше 0,375 В, происходили значительные реакции растворения Cu как в выступы и впадины субстрата Cu, потому что многие акцепторы воды гидратировали ионы Cu. Однако концентрация акцепторов воды на поверхности Cu быстро уменьшалась по мере приложения потенциала; акцепторы воды в конечном итоге истощались из-за гидратации ионов Cu, а реакция растворения Cu регулировалась реакцией управления переносом массы акцепторов воды. Следовательно, акцепторы воды преимущественно распространялись на выступы поверхности, которые растворялись быстрее, чем впадины (рис. 8В). В результате быстрого растворения на выступах поверхность Cu сглаживалась.
РИСУНОК 8 . Схема механизма электрохимического полирования меди: исходное состояние (А) и стационарное состояние (Б) .
Заключение
Мы успешно определили механизм Cu ECP, используя различные стандартные методы электрохимического анализа, а также наш новый метод электрохимического анализа. Из анализа LSV эффект полировки Cu наблюдался, когда потенциал был выше 0,375 В. Анодные потенциалы были выбраны для анализов EIS и SECM. Низкочастотная область полученных графиков Найквиста указывала на то, что диффузия акцепторов воды была связана с явлениями полировки Cu в анализах EIS. Затем профили токов электролиза воды и расстояния позволили впервые наблюдать диффузию акцепторов воды из анализов SECM. Эти профили свидетельствовали о том, что механизм акцептора воды, скорее всего, объясняет явление полировки. Знание точного механизма Cu ECP будет полезно для новых интерпретаций, конструкций и приложений ECP.
Заявление о доступности данных
Исходные материалы, представленные в исследовании, включены в статью/дополнительные файлы, дальнейшие запросы можно направлять соответствующим авторам.
Вклад авторов
KP и JL в равной степени внесли свой вклад в эту работу и являются первым автором. Ю.К. особенно способствовал настройке оборудования и проведению экспериментов. SY и BY являются главными организаторами и консультантами этой работы.
Финансирование
Это исследование было поддержано Программой фундаментальных научных исследований через Национальный исследовательский фонд Кореи (NRF), финансируемой Министерством науки, ИКТ и т.д. Планирование будущего (№ 2015R1A5A1037548). Это исследование также было поддержано Национальным исследовательским фондом Кореи (NRF) (№ NRF-2020R1A2C2009).462). Эта работа также была поддержана Программой технологических инноваций (Разработка нецианидного раствора для золотых ударов и процесса покрытия для процесса соединения полупроводниковых устройств, 20017189), финансируемой Министерством торговли и промышленности; Energy (MOTIE, Корея).
Конфликт интересов
Авторы заявляют, что исследование проводилось при отсутствии каких-либо коммерческих или финансовых отношений, которые могли бы быть истолкованы как потенциальный конфликт интересов.
Примечание издателя
Все претензии, изложенные в этой статье, принадлежат исключительно авторам и не обязательно представляют претензии их дочерних организаций или издателя, редакторов и рецензентов. Любой продукт, который может быть оценен в этой статье, или претензии, которые могут быть сделаны его производителем, не гарантируются и не поддерживаются издателем.
Сокращения
ЭХП, электрохимическое полирование; EIS, спектроскопия электрохимического импеданса; LSV, линейная сканирующая вольтамперометрия; SEM, сканирующая электронная микроскопия; СЭКМ; сканирующая электрохимическая микроскопия; FSW, конечное пространство Варбурга; OCP, потенциал холостого хода.
Ссылки
Chang, S.-C., Shieh, J.-M., Dai, B.-T., Feng, M.-S., Li, Y.-H., Shih, C.H., et др. (2003). Суперполировка для выравнивания межблочных соединений из дамасской меди. Электрохим. Твердотельный латыш. 6 (5), Г72–Г74. doi:10.1149/1.1565853
Полный текст CrossRef | Google Scholar
Chang, S. -C., Shieh, J.-M., Huang, C.-C., Dai, B.-T., and Feng, M.-S. (2002). Влияние структуры на эффективность планаризации электрополировки Cu. Япония. Дж. Заявл. физ. 41 (12), 7332–7337. doi:10.1143/Jjap.41.7332
-C., Shieh, J.-M., Huang, C.-C., Dai, B.-T., and Feng, M.-S. (2002). Влияние структуры на эффективность планаризации электрополировки Cu. Япония. Дж. Заявл. физ. 41 (12), 7332–7337. doi:10.1143/Jjap.41.7332
Полный текст CrossRef | Google Scholar
Ду, Б., и Суни, И.И. (2004). Механистические исследования электрополировки Cu в фосфорнокислых электролитах. Дж. Электрохим. соц. 151 (6), C375–C378. doi:10.1149/1.1740783
Полный текст CrossRef | Google Scholar
Эдвардс, Дж. (1953). Механизм электропокрытия меди в растворах фосфорной кислоты. Дж. Электрохим. соц. 100 (7), 189С–С194. doi:10.1149/1.2781122
Полный текст CrossRef | Google Scholar
Elmore, WC (1939). Электролитическая полировка. J. Appl. физ. 10 (10), 724–727. doi:10.1063/1.1707257
Полный текст CrossRef | Google Scholar
Elmore, WC (1940). Электролитическая полировка. II. J. Appl. физ. 11 (12), 797–799. doi:10.1063/1. 1712738
1712738
Полный текст CrossRef | Google Scholar
Гларум С. Х. и Маршалл Дж. Х. (1985a). Анодное растворение меди в фосфорной кислоте: I. Вольтамперометрия и колебательное поведение. Дж. Электрохим. соц. 132 (12), 2872–2878. doi:10.1149/1.2113686
Полный текст CrossRef | Google Scholar
Glarum, SH, and Marshall, JH (1985b). Анодное растворение меди в фосфорной кислоте. II. Импедансное поведение. Дж. Электрохим. соц. 132 (12), 2878–2885. doi:10.1149/1.2113687
Полный текст CrossRef | Google Scholar
Гримм Р. Д., Уэст А. С. и Ландольт Д. (1992). Исследование импеданса по переменному току анодно сформированных солевых пленок на железе в растворе хлорида. Дж. Электрохим. соц. 139 (6), 1622–1629. doi:10.1149/1.2069467
Полный текст CrossRef | Google Scholar
Хан В. и Фанг Ф. (2019). Фундаментальные аспекты и последние разработки в области электрополировки. Междунар. J. Производство станков 139, 1–23. doi:10.1016/j.ijmachtools.2019.01.001
doi:10.1016/j.ijmachtools.2019.01.001
Полный текст CrossRef | Google Scholar
Хоар, Т. П., и Ротвелл, Г. П. (1964). Влияние потока раствора на анодную полировку. Медь в водной о-фосфорной кислоте. Electrochimica Acta 9 (2), 135–150. doi:10.1016/0013-4686(64)85001-5
Полный текст CrossRef | Google Scholar
Jacquet, PA (1936). Об анодном поведении меди в водных растворах ортофосфорной кислоты. Пер. Электрохим. соц. 69 (1), 629–655. doi:10.1149/1.3498234
Полный текст CrossRef | Google Scholar
Кодзима К. и Тобиас К.В. (1973). Интерпретация импедансных свойств пленки поверхности анода при электрополировке меди в фосфорной кислоте. Дж. Электрохим. соц. 120 (9), 1202–1205. doi:10.1149/1.2403661
Полный текст CrossRef | Google Scholar
Ландольт, Д. (1987). Основные аспекты электрополировки. Electrochimica Acta 32 (1), 1–11. doi:10.1016/0013-4686(87)87001-9
Полный текст CrossRef | Google Scholar
Лапейр Л. , Мартинес Ломбардия Э., Вербекен К., Де Граев И., Кестенс Л. А. И. и Террин Х. (2013). Влияние соседних зерен на микроскопическое коррозионное поведение зерна в поликристаллической меди. Коррозионная наука. 67, 179–183. doi:10.1016/j.corsci.2012.10.017
, Мартинес Ломбардия Э., Вербекен К., Де Граев И., Кестенс Л. А. И. и Террин Х. (2013). Влияние соседних зерен на микроскопическое коррозионное поведение зерна в поликристаллической меди. Коррозионная наука. 67, 179–183. doi:10.1016/j.corsci.2012.10.017
Полный текст CrossRef | Google Scholar
Лю Ф.К., Ду Т., Дубуст А., Цай С. и Хсу В.-Ю. (2006а). Планаризация Cu при электрохимической механической планаризации. Дж. Электрохим. соц. 153 (6), C377–C381. doi:10.1149/1.2186180
Полный текст CrossRef | Google Scholar
Лю С.-Х., Ши Дж.-М., Чен С., Дай Б.-Т., Хенсен К. и Ченг С.-С. (2005). Двухаддитивные электролиты для суперпланаризации дамасских металлов Cu. Электрохим. Твердотельный латыш. 8 (3), С47–С50. doi:10.1149/1.1854124
Полный текст CrossRef | Google Scholar
Лю С.-Х., Ши Дж.-М., Чен К., Хенсен К. и Ченг С.-С. (2006б). Роль добавок в электрополировке дамасской меди. Дж. Электрохим. соц. 153 (6), C428–C433. doi:10.1149/1.2193348
doi:10.1149/1.2193348
Полный текст CrossRef | Google Scholar
Матлош М., Магайно С. и Ландольт Д. (1994). Импедансный анализ модельного механизма электрополировки с ограничением акцептора. Дж. Электрохим. соц. 141 (2), 410–418. doi:10.1149/1.2054741
Полный текст CrossRef | Google Scholar
Ольденбургер М., Бедурфтиг Б., Груле А., Гримсманн Ф., Рихтер Э., Финдейзен Р. и др. (2019). Исследование низкочастотного импеданса Варбурга литий-ионных аккумуляторов с помощью измерений в частотной области. Дж. Энерг. Склад 21, 272–280. doi:10.1016/j.est.2018.11.029
Полный текст CrossRef | Google Scholar
Падхи Д., Яхалом Дж., Гандикота С. и Диксит Г. (2003). Планаризация тонких медных пленок электрополировкой в фосфорной кислоте для приложений ULSI. Дж. Электрохим. соц. 150 (1), G10–G14. doi:10.1149/1.1523415
Полный текст CrossRef | Google Scholar
Pointu, B., Braizaz, M., Poncet, P., and Rousseau, J. (1981). Фотоэффекты на границе Cu/h4PO4. J. Electroanalytical Chem. Межфазная электрохимия 122, 111–131. doi:10.1016/S0022-0728(81)80144-1
(1981). Фотоэффекты на границе Cu/h4PO4. J. Electroanalytical Chem. Межфазная электрохимия 122, 111–131. doi:10.1016/S0022-0728(81)80144-1
Полный текст CrossRef | Google Scholar
Pointu, B., Braizaz, M., Poncet, P., and Rousseau, J. (1983a). Фотоэффекты на границе Cu/h4PO4: Часть II. Ленточная модель интерфейса в темноте. J. Electroanalytical Chem. Межфазная электрохимия 151 (1), 65–77. doi:10.1016/S0022-0728(83)80424-0
Полный текст CrossRef | Google Scholar
Pointu, B., Braizaz, M., Poncet, P., and Rousseau, J. (1983b). Фотоэффекты на границе Cu/h4PO4: Часть III. Интерпретация фототоков на границе раздела. J. Electroanalytical Chem. Межфазная электрохимия 151 (1), 79–87. doi:10.1016/S0022-0728(83)80425-2
Полный текст CrossRef | Академия Google
Ши, Дж.-М., Чанг, С.-К., Ван, Ю.-Л., Дай, Б.-Т., Ченг, С.-С., и Тинг, Дж. (2004) . Уменьшение ямок травления электрополированной меди добавками. Дж. Электрохим. соц. 151 (7), C459–C462. doi:10.1149/1.1757461
соц. 151 (7), C459–C462. doi:10.1149/1.1757461
Полный текст CrossRef | Google Scholar
Сунь Б. Б., Ван Ю. Б., Вен Дж., Ян Х., Суй М. Л., Ван Дж. К. и др. (2005). Артефакты, возникающие в металлических стеклах во время подготовки образцов для ПЭМ. Scripta Materialia 53 (7), 805–809. doi:10.1016/j.scriptamat.2005.06.007
Полный текст перекрестной ссылки | Google Scholar
Суни И.И. и Ду Б. (2005). Планаризация Cu для обработки ULSI электрохимическими методами: обзор. IEEE Trans. Полуконд. Производство. 18 (3), 341–349. doi:10.1109/Tsm.2005.852091
Полный текст CrossRef | Google Scholar
Видаль Р. и Уэст А.С. (1995a). Электрополировка меди в концентрированной фосфорной кислоте: I . Экспериментальные выводы. Дж. Электрохим. соц. 142 (8), 2682–2689. Дои: 10.1149/1.2050074
Полнотекстовая перекрестная ссылка | Google Scholar
Видаль Р. и Уэст А.С. (1995b). Электрополировка меди в концентрированной фосфорной кислоте: II. Теоретическая интерпретация. Дж. Электрохим. соц. 142 (8), 2689–2694. doi:10.1149/1.2050075
Теоретическая интерпретация. Дж. Электрохим. соц. 142 (8), 2689–2694. doi:10.1149/1.2050075
Полный текст CrossRef | Google Scholar
Вагнер, К. (1954). Вклад в теорию электрополировки. Дж. Электрохим. соц. 101(5) , 225–228. дои: 10.1149/1.2781235
Полнотекстовая перекрестная ссылка | Google Scholar
West, AC, Deligianni, H., Andricacos, PC (2005). Электрохимическая планаризация металлизации межсоединений. IBM J. Res. Дев. 49(1) , 37–48. doi:10.1147/rd.491.0037
Полный текст CrossRef | Google Scholar
Чжан Б., Ли В. Х., Пинер Р., Холманов И., Ву Ю., Ли Х. и др. (2012). Низкотемпературное химическое осаждение из паровой фазы графена из толуола на электрополированную медную фольгу. Acs Nano 6 (3), 2471–2476. doi:10.1021/nn204827h
PubMed Abstract | Полный текст перекрестной ссылки | Google Scholar
Оборудование для электрополировки | Technic Inc.

Автоматические и ручные системы электрополировки
Системы электрополировки бывают различных конфигураций, каждая из которых имеет собственный диапазон производственных возможностей для обеспечения требуемой точности, а также конкретной формы и размера обрабатываемых деталей. Technic предлагает широкий спектр технологий для оборудования для электрополировки, которые гарантируют, что устройство будет соответствовать вашим потребностям.
Всестороннее сотрудничество Technic с клиентами на этапе проектирования обеспечивает гибкость системы, простоту эксплуатации и обслуживания, а также интеграцию рабочего процесса в вашу текущую работу. Дополнительное внимание уделяется будущим обновлениям, расширению системы или внедрению экономичной автоматизации. Ваш инженер по применению Technic может помочь вам выбрать наилучшую систему электрополировки для вашего применения, а также предложить ряд вариантов получения максимальной отдачи от ваших инвестиций в оборудование.
- MP500 Закрытая радиальная автоматика Подробнее
- SBE ® для пакетной обработки мелких деталей Подробнее
- Закрытые линейные автоматические подъемные системы Подробнее
- Оборудование для обработки рулонов Подробнее
- Лабораторные и прототипные системы с ручным управлением Подробнее
Что такое электрополировка?
Электрополировка представляет собой электрохимический процесс, аналогичный гальванике, но в обратном порядке. Процесс электрополировки работает на микроскопическом уровне, чтобы сгладить поверхность металлической детали.
Процесс электрополировки
Электрополировка — это электрохимический процесс, используемый для сглаживания металлических поверхностей путем удаления микроскопических количеств материала с поверхности изделия. Металлическая заготовка погружается в ванну с электролитом с регулируемой температурой, когда она подключена к анодному (положительному) положению в цепи постоянного тока. Ток проходит от анода, где металл растворяется, к катоду, где выделяется водород. Электролиты, используемые для большинства промышленных электрополировок, обычно представляют собой концентрированные смеси кислот, таких как серная кислота и фосфорная кислота. Для некоторых металлов можно использовать щелочные процессы. Выступающие элементы профиля поверхности детали растворяются быстрее, чем материал в углублениях.
Ток проходит от анода, где металл растворяется, к катоду, где выделяется водород. Электролиты, используемые для большинства промышленных электрополировок, обычно представляют собой концентрированные смеси кислот, таких как серная кислота и фосфорная кислота. Для некоторых металлов можно использовать щелочные процессы. Выступающие элементы профиля поверхности детали растворяются быстрее, чем материал в углублениях.
Системы электрополировки для исследований и промышленности доступны в ручном и автоматическом режимах. Автоматические системы могут быть непрерывными или периодическими. Каждая электрополировальная установка проектируется по индивидуальному заказу и поставляется с инструментами, специальными приспособлениями и аксессуарами, необходимыми для успешной работы. Независимо от сложности применения, конструкция может быть разработана для обеспечения необходимой отделки, точности и аккуратности.
Технические характеристики электрополировки
- Стандарты ASME BPE для электрополировки биотехнологического оборудования
- SEMI F19, Спецификации электрополировки для полупроводниковых приложений
- ASTM B 912-00, Пассивация нержавеющей стали с помощью электрополировки
- ASTM E1558, Стандартное руководство по электролитической полировке металлографических образцов
Типичные характеристики системы
- Модульная конструкция
- Изготовление коррозионностойкое
- Водосберегающий ополаскиватель
- Сбор данных
- Полностью закрытая рабочая зона
- Минимальное обслуживание
- Паровой или электрический нагрев
- Ручной или автоматизированный режим
Преимущества системы
- Простота в эксплуатации
- Простота обслуживания
- Воспроизводимые результаты
- Минимизация отходов
- Контролируемая среда
Обслуживаемые отрасли
- Медицинский
- Промышленный
- Аэрокосмическая отрасль
- Автомобилестроение
- Архитектурный
- Декоративный
- Потребитель
- Военный
- png?itok=kbwk173B» data-thumb-alt=»MP500 — Automatic Radial Style Electropolishing»>
MP500 — Автоматическая радиальная электрополировка
MP500 — Экран управления автоматической радиальной электрополировкой
Серия Medi500 — ручная лабораторная система/система прототипирования
Medi2000 — Закрытая автоматическая радиальная транспортная система
- jpg?itok=PY3guW6m» data-thumb-alt=»Mini Lab Manual Laboratory/Prototyping System»>
Мини-лаборатория Ручная лабораторная система/система прототипирования
Настольная ручная лабораторная система/система прототипирования
Электрод с носиком (SBE) — ручная пакетная обработка мелких деталей
Medi1500 — Закрытая боковая транспортная система
Электрополировка Информация и ассоциации
Электрохимический процесс полировки Delmet
Процесс электрохимической полировки
Когда поверхностная отделка компонента без извержения особенно важна для требовательного применения или, из -за конфимации самого элемента, самого элемента, самого элемента. другие виды обработки поверхности сложны или дороги, этот процесс, безусловно, является одной из наиболее приемлемых альтернатив. Например, в первом случае рассмотрите компоненты, используемые в электронной промышленности и внутрикостных имплантатах, а во втором рассмотрите компоненты с очень высоким соотношением пустоты/твердой части, такие как сетки, сетки, перфорированные листы и т. д.
другие виды обработки поверхности сложны или дороги, этот процесс, безусловно, является одной из наиболее приемлемых альтернатив. Например, в первом случае рассмотрите компоненты, используемые в электронной промышленности и внутрикостных имплантатах, а во втором рассмотрите компоненты с очень высоким соотношением пустоты/твердой части, такие как сетки, сетки, перфорированные листы и т. д.
Существуют также особые случаи, когда отделка поверхности чрезвычайно важна в определенных областях применения, например, в вопросе гигиены материала. Это также связано с возможностью перехода материала в вещество или окружающую среду, с которой он вступает в контакт, или с загрязнением другими металлами, что может создать проблемы с коррозией или изменить его физические характеристики при вводе компонента в эксплуатацию.
Основными отраслями, в которых для определенных компонентов необходимо уделять особое внимание отделке поверхности, являются пищевая, фармацевтическая, химическая и электронная отрасли.
Во всех этих случаях необходимо гарантировать особенно высокую коррозионную стойкость, а также «инертность» поверхностей компонентов по отношению к обрабатываемым веществам.
Электролитическая полировка позволяет получить чрезвычайно «чистую» и гладкую поверхность, что является необходимым условием для предотвращения трещин, подверженных коррозии. Понятие «шероховатость»
Каждая металлическая поверхность, если рассмотреть ее очень внимательно под большим увеличением, имеет профиль, более или менее похожий на профиль, показанный на рис. 1. Морфология этого профиля определяется циклами механической обработки, которым подвергалась заготовка, поэтому внешний вид неравномерный. поверхности, как показано на схеме, тесно связана с технологическим циклом, который прошел материал, т. е. с инструментами, обрабатывающими заготовку.
Помимо профиля на рисунке показана средняя линия, разделяющая профиль таким образом, что сумма площадей над ним равна сумме площадей под ним. Наконец, на рисунке показана базовая длина, которая состоит из длины профиля, выбранного для оценки шероховатости. Если мы рассмотрим две декартовы оси (xy), где ось x совпадает со средней линией, мы увидим, как различные значения y, положительные или отрицательные, представляют отклонения отдельных точек на профиле от средней линии. 9Рис. 1 – График профиля шероховатости.
Наконец, на рисунке показана базовая длина, которая состоит из длины профиля, выбранного для оценки шероховатости. Если мы рассмотрим две декартовы оси (xy), где ось x совпадает со средней линией, мы увидим, как различные значения y, положительные или отрицательные, представляют отклонения отдельных точек на профиле от средней линии. 9Рис. 1 – График профиля шероховатости.
Таким образом, значение шероховатости определяется как сумма по абсолютной величине всех точек ординат (y) относительно средней линии:
, где «n» указывает число рассматриваемых ординат.
Значение шероховатости измеряется в микронах (мкм) — наиболее широко используемой единице измерения, включенной как в итальянские, так и в зарубежные стандарты.
Однако есть несколько других параметров для выполнения этого измерения, таких как Rmax, определяемое в микронах как расстояние между самой высокой точкой и самой низкой точкой профиля; или Rm, определяемый как среднее значение шероховатости Rmax, измеренное на 5 соседних участках основания. В дополнение к ним существуют и другие важные параметры, позволяющие полностью охарактеризовать профиль поверхности: они относятся не к «вертикальным» вариациям профиля по отношению к средней линии (как видно для определения Ra, Rmax, Rm), а к «горизонтальным» явлениям, то есть пространствам между различными вершинами.
В дополнение к ним существуют и другие важные параметры, позволяющие полностью охарактеризовать профиль поверхности: они относятся не к «вертикальным» вариациям профиля по отношению к средней линии (как видно для определения Ra, Rmax, Rm), а к «горизонтальным» явлениям, то есть пространствам между различными вершинами.
Из вышеизложенного видно, что нельзя выразить тесную связь между шероховатостью и видом обработки поверхности данного металлического материала, так как эта связь зависит от многих факторов.
Даже если ответ представляет значительную ценность с эстетической точки зрения, следует иметь в виду, что в целом металл с очень шероховатой поверхностью, безусловно, более подвержен коррозии по сравнению с тем же металлом с более гладкой поверхность.
Эта концепция еще более верна, если мы рассматриваем самопассивирующиеся материалы, такие как нержавеющая сталь (см. брошюру «Подразделение обработки»). самопассивации имеет смысл, что чем больше значение шероховатости, тем больше «пиков» и «впадин», то есть положительных значений «y» и отрицательных значений «y». Это, очевидно, создает «почву», которая очень склонна удерживать различные виды отложений, которые могут быть источником коррозионного воздействия.
Это, очевидно, создает «почву», которая очень склонна удерживать различные виды отложений, которые могут быть источником коррозионного воздействия.
И наоборот, чем более гладкой является поверхность (особенно на самопассивирующихся металлах), поэтому при очень ограниченных значениях «y» «рельеф» поверхности металла менее склонен удерживать отложения.
В результате может быть видно, что низкое значение шероховатости также влияет на способность металла очищаться, очищаться или дезинфицироваться
Хотя, как упоминалось выше, не может быть двусторонней корреляции между типом отделки и шероховатостью поверхности, были проведены чисто экспериментальные испытания на некоторых образцах для проверки значений шероховатости, записанных в различных состояниях чистовой обработки..
Естественно, значения следует рассматривать как ориентировочные, и их можно считать действительными только для данной конкретной совокупности отобранных образцов.
На рис. 2 представлены диаграммы шероховатости, полученные на испытанных образцах. Затем эти значения были помещены в логарифмическую шкалу (рис. 3). Наконец, в таблице 1 приведены значения шероховатости, выраженные в миллиметрах, для трех видов отделки: прокаткой, истиранием и электрополировкой.
Затем эти значения были помещены в логарифмическую шкалу (рис. 3). Наконец, в таблице 1 приведены значения шероховатости, выраженные в миллиметрах, для трех видов отделки: прокаткой, истиранием и электрополировкой.
Рис. 2 — Диаграммы шероховатости. Рис.
Таблица 1 – Шероховатость поверхности, измеренная на листах из нержавеющей стали перпендикулярно направлению прокатки.
Теперь посмотрим, из чего именно состоит обработка электролитическим полированием.
ПРИНЦИП ПРОЦЕССА
Схематически процесс можно описать следующим образом: система представляет собой анодную ванну с электролитическим раствором, в которой электролизера, а катод обычно изготавливается из меди, нержавеющей стали AISI 304 или, иногда, из свинца, пластины.
Резервуар, содержащий раствор электролита, обычно имеет внутреннюю облицовку из пластмассы, кислотоупорного кирпича или свинца (рис. 4).
Рис. 4 — Анод состоит из полируемого изделия.
Электрооборудование должно обеспечивать подачу постоянного тока напряжением 5 ÷ 15 В, а плотность тока относительно обрабатываемой поверхности обычно не превышает 0,5 А/см2, поэтому необходимо иметь сила тока пропорциональна суммарным поверхностям всех заготовок, обрабатываемых одновременно.
Температура ванны всегда выше температуры окружающей среды и должна быть установлена в соответствии с типом раствора и типом обрабатываемого материала.
Принцип электролитической полировки противоположен гальваническому осаждению. Он заключается в удалении материала путем селективного растворения поверхности заготовки, служащей анодом, в электролитической ванне под действием внешнего источника тока.
Растворение металла геометрически выравнивает заготовку, без межкристаллитного разрушения и без механического, термического или химического воздействия на материал.
В процессе полирования под действием тока на поверхности заготовок образуется так называемая полировальная пленка, порошкообразный слой воды, вязкий с газообразованием, с высоким сопротивлением диффузии, электрохимическая активность медленно размывается тонкий поверхностный слой (в среднем от 20 до 30 мкм) обрабатываемой детали. Форма, которую принимает эта эрозия, чрезвычайно важна, поскольку она придает электрополировке одну из ее основных характеристик, также определяемую как микроудаление заусенцев. Микрозаусенцы обработанной детали и «выступы» на поверхности постепенно удаляются, и поверхность становится все более гладкой.
Точки шероховатости с размерами меньше толщины полировальной пленки предпочтительно удаляются, что приводит к микроскопическому сглаживанию и нивелированию. Макроскопические структуры сглажены и округлы на поверхности, но не выровнены.
Толщина слоев, удаляемых электрохимической полировкой, может быть точно воспроизведена посредством плотности тока и времени обработки.
Большинство металлов и сплавов, которые могут использоваться технически, могут быть обработаны электрохимической полировкой, при которой обычно используются электролиты, состоящие из концентрированных смесей минеральных кислот.
ХАРАКТЕРИСТИКИ ПОВЕРХНОСТИ
Электрохимическая полировка устраняет поврежденные поверхностные слои, загрязнённые посторонними материалами, таким образом, что заполняет их чистую поверхность вместе с напряжениями и микротрещинами на конечной поверхности неповрежденная базовая структура рассматриваемого материала.
Электрохимически полированная поверхность является металлически чистой, полированной и микроскопически компактной, а также значительно меньше выступает по сравнению с механически обработанными поверхностями. Эта поверхность имеет низкий уровень потенциальной энергии и, как правило, свободна от местных растягивающих и сжимающих напряжений.
Макроскопически характеризуется некоторой остаточной рябью, размер которой зависит от исходного поверхностного слоя, продолжительности электрохимической полировки и тонкости кристаллической структуры. Эта остаточная рябь обычно не имеет существенного значения с точки зрения функционального поведения поверхностей, но тем не менее дает ложное впечатление о качестве поверхности, если для ее определения приводятся только значения шероховатости.
Это геометрические данные, которые не являются решающими для функционального сравнения поверхностей, полученных с помощью различных процедур.
Степень блеска электрохимически полированных поверхностей в целом выше, чем механически полированных, однако — за счет остаточной ряби — наблюдается не эффект зеркального блеска, а слегка рассеянное отражение. При электрополировке трудно добиться полировки до зеркального блеска, чего можно добиться при механической полировке.
Электрохимически полированные поверхности не имеют заусенцев, чешуек, микрозаусенцев и микротрещин по всей поверхности, даже в труднодоступных местах.
УЛУЧШЕННЫЕ ФУНКЦИОНАЛЬНЫЕ ХАРАКТЕРИСТИКИ ПОВЕРХНОСТЕЙ
При электрохимической полировке снижается износ поверхностей скольжения и металлопластиковых муфт.
Кроме того, электрохимическое полирование применяют для повышения сопротивления усталости, благодаря устранению зарождения трещин, для снижения потерь на облучение в гелиопоглотителях и теплообменниках, для снижения температурных потерь в жидких газах, для улучшения характеристик в высоких частотными методами, для проведения предварительной обработки перед гальваническим, химическим или физическим напылением, для улучшения технических характеристик пайки и сварки, а также для повышения скорости дегазации в высоковакуумных системах.
Очень важной областью применения электрохимической полировки является удаление заусенцев с поверхностей и кромок в области точной механики, машиностроения, электротехники, гидравлики и пневматической промышленности.
КОРРОЗИОННАЯ СТОЙКОСТЬ И ПАССИВНОСТЬ
Благодаря устранению местных элементов, таких как примеси, структурные дефекты и напряжения, имеют лучшую коррозионную стойкость нержавеющие стали.
При электрохимическом полировании на поверхности заготовок выделяется кислород, который обогащается в полировальной пленке и приводит к образованию пассивных слоев, содержащих оксиды, сразу после отключения полирующего тока.
Электрохимическая полировка создает, особенно на поверхностях из нержавеющей стали, идеальные условия для образования пассивного слоя, в котором небольшое обогащение легирующими элементами хромом и никелем является дополнительным преимуществом.
Было проведено несколько исследований с целью сравнения поведения механически обработанных поверхностей с поверхностями, обработанными электрополировкой, с тем же типом нержавеющей стали.
Рис. 5 – Слева – поверхность трубы, полученной горячей прокаткой и травлением. Справа та же трубка после электролитической полировки.
Все проведенные испытания в различных условиях как по температуре, так и по концентрации коррозионно-активных элементов позволяют сделать вывод о том, что электрохимическая обработка, пусть и не очень тщательная, повышает коррозионную стойкость материала.
В качестве доказательства вышеизложенного можно указать, например, параметр CPT (критическая температура точечной коррозии), который представляет собой критическую температуру, при которой начинается точечная коррозия для трех типов отделки: травление, сатинирование и электрополировка. , для стальной трубы AISI 316 L (EN 1.4404). Этот параметр можно соотнести со способностью нержавеющей стали сопротивляться «локальным триггерам коррозии», таким как «точечная коррозия». В связи с этим в Таблице 2 и на Рисунке 7 показаны данные, полученные из: «Влияние различных условий поверхности на стойкость к точечной коррозии труб из нержавеющей стали типа EN 1.4404» Троэлса Матесена, Торбена С. Нильсена, Яна Элькьяера Франтсена, Force Technology, Brøndby. , Дания и Джон Колд, Энн Р. Бойе-Мёллер, Датский технологический институт, Колдинг, Дания
Таблица 2. Критические температуры точечной коррозии, определенные в соответствии с ASTM G150
a. Эквивалент стойкости к точечной коррозии, PRE = Cr +3,3 Mo + 16 N
Эквивалент стойкости к точечной коррозии, PRE = Cr +3,3 Mo + 16 N
значительно выше при электрополировке.
Положительное влияние электрополировка обработки на потенциал намысленности очевидно из графика на рисунке 6.
Рис. 6. температур (поляризация). Сравнение травления, сатинирования и электрополировки труб из стали AISI 316 L (EN 1.4404) в растворе с 5% хлора.
СТАНДАРТЫ
Основными стандартами, касающимися электролитической полировки, как для самого процесса, так и для подготовки образцов для испытаний, являются международные стандарты ISO и американские стандарты ASTM.
Однако в коммерческих целях часто также делаются ссылки на все еще широко используемые стандарты отдельных европейских стран, такие как немецкий DIN.
Вот наиболее значимые, как международные, так и национальные:
- ISO 15730
- АСТМ В-912
- АСТМ Е-712
- DIN 8590
- VDI 3401 (фольга 2)
ПРИМЕРЫ ПРИМЕНЕНИЯ
0002
Ниже приведен список примеров продуктов, которые прошли обработку электролитическим полированием с чисто функциональной целью, т.е. для улучшения химико-физических характеристик поверхности нержавеющей стали, из которой состоит сама деталь.
Рис. 7 — Процесс для фармацевтической отрасли, в EN 1. 4401 (AISI 316). Он был отполирован сатином с зернистостью 240, а затем подвергнут внутренней электрополировке с шероховатостью, равной Ra 0,40 мкм.
4401 (AISI 316). Он был отполирован сатином с зернистостью 240, а затем подвергнут внутренней электрополировке с шероховатостью, равной Ra 0,40 мкм.
Фиг. Обработка сложной поверхностной сетки оставляет микроскопические заусенцы, которые удаляются электрополировкой.
Fig. 9 — Four-position manifold (dispenser) in EN 1.4401 (AISI 316 ) используется в фармацевтической промышленности. Выполнена обработка: зеркальная механическая предварительная полировка и последующая электрополировка внутренняя и наружная с конечной шероховатостью Ra менее 0,10 мм.
Выполнена обработка: зеркальная механическая предварительная полировка и последующая электрополировка внутренняя и наружная с конечной шероховатостью Ra менее 0,10 мм.
Рис. 10 — Электрополированные Стэнестные стальные компоненты.
0004
Рис. 11 — Плесень для мороженого в EN 1,4301 (AISI 304), где высокая глюс и опорожнение пищевого продукта.
11 — Плесень для мороженого в EN 1,4301 (AISI 304), где высокая глюс и опорожнение пищевого продукта.
Рис. ), установленный у входа в новую школу Бичвуд в Слау (Беркшир) в честь строительства нового здания.
Электрохимическое восстановление промышленных ванн, используемых для электрополировки нержавеющей стали ограничить диапазон применимых плотностей тока. В связи с этим продление срока эксплуатации промышленных ванн является серьезной задачей. Применение электрохимического восстановления в процессе восстановительных промышленных ванн позволило снизить его загрязнение и, как следствие, повысить качество поверхности электрополированных образцов из нержавеющей стали марки 304. Сравнивалось влияние загрязнения электрополировочной ванны на такие параметры электрополированных образцов, как шероховатость, блеск, уменьшение массы и коррозионная стойкость.
 Проведенные испытания включали восстановление загрязненной промышленной ванны катодным восстановлением и контроль загрязнения ванны с помощью эмиссионной спектрометрии ИСП-ОЭС. Потенциодинамические испытания в среде 0,5 М хлора с целью определения влияния электрохимического восстановления в гальванической ванне на поверхностное сопротивление показали, что стойкость к питтинговой коррозии образцов, электрополированных в ванне после восстановления, снижается примерно на 0,1 В по сравнению с образцами, электрополированными до снижение. Расчеты, проведенные для 24 измерений коррозионной стойкости, показали, что различия между результатами были значительными. Обработка в ванне приводит к улучшению шероховатости и блеска примерно на 500 GU (единиц блеска). При этом снижение массы снижается даже на 13 % по сравнению с процессом, проводимым в ванне до восстановления. Это может иметь положительное влияние, замедляя процесс загрязнения ванны и, как следствие, уменьшая негативное воздействие на окружающую среду.
Проведенные испытания включали восстановление загрязненной промышленной ванны катодным восстановлением и контроль загрязнения ванны с помощью эмиссионной спектрометрии ИСП-ОЭС. Потенциодинамические испытания в среде 0,5 М хлора с целью определения влияния электрохимического восстановления в гальванической ванне на поверхностное сопротивление показали, что стойкость к питтинговой коррозии образцов, электрополированных в ванне после восстановления, снижается примерно на 0,1 В по сравнению с образцами, электрополированными до снижение. Расчеты, проведенные для 24 измерений коррозионной стойкости, показали, что различия между результатами были значительными. Обработка в ванне приводит к улучшению шероховатости и блеска примерно на 500 GU (единиц блеска). При этом снижение массы снижается даже на 13 % по сравнению с процессом, проводимым в ванне до восстановления. Это может иметь положительное влияние, замедляя процесс загрязнения ванны и, как следствие, уменьшая негативное воздействие на окружающую среду.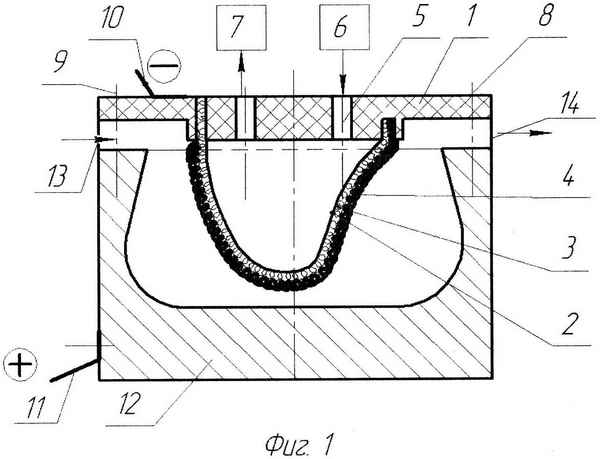 Еще одним аргументом в пользу сокращения промышленных ванн является замедление процесса загрязнения катода в процессе электрополировки. В промышленных условиях это может расширить возможности проведения процесса без необходимости восстановления или замены катода.
Еще одним аргументом в пользу сокращения промышленных ванн является замедление процесса загрязнения катода в процессе электрополировки. В промышленных условиях это может расширить возможности проведения процесса без необходимости восстановления или замены катода.
1. Введение
Практическое использование процесса электрополировки (EP) восходит к 1930-м годам. В настоящее время эта технология является широко известным видом промышленной обработки поверхностей, используемым во всем мире. Вместе с развитием технологий возросла потребность в поверхностях с гладкой, однородной, очень чистой и коррозионностойкой поверхностью. В настоящее время процесс электрополировки применяется как при производстве предметов быта, так и элементов специальной техники [1, 2].
Описанные в литературе применения процесса электрополировки включают также его использование для обработки поверхности таких элементов, используемых в биомедицине, как стенты или имплантаты [3–8].
Процесс электрополировки позволяет сгладить, придать блеск и улучшить внешний вид поверхности элемента. Этому также может предшествовать механическая полировка [9]. Электрополировка также позволяет сглаживать модифицированные поверхности из стали марки 316L, изготовленной по технологии ALM (аддитивное производство слоев). Были также попытки электрополировки покрытий, изготовленных с использованием TSC (термораспылительные покрытия). Однако полученный поверхностный слой состоял из смеси α и γ , что затрудняло электрополировку [10]. Электрополировка может поддерживаться воздействием магнитного поля, что может улучшить шероховатость поверхности и, в некоторых случаях, коррозионную стойкость [11–13]. Однако магнитная электрополировка пока не получила широкого применения в промышленности. Электрополировка также повышает коррозионную стойкость поверхности за счет влияния пассивного слоя, содержащего в том числе оксиды и гидроксиды хрома [14, 15]. Одним из основных преимуществ электрохимической обработки является возможность получения хорошего качества поверхности даже для элементов сложной формы.
Этому также может предшествовать механическая полировка [9]. Электрополировка также позволяет сглаживать модифицированные поверхности из стали марки 316L, изготовленной по технологии ALM (аддитивное производство слоев). Были также попытки электрополировки покрытий, изготовленных с использованием TSC (термораспылительные покрытия). Однако полученный поверхностный слой состоял из смеси α и γ , что затрудняло электрополировку [10]. Электрополировка может поддерживаться воздействием магнитного поля, что может улучшить шероховатость поверхности и, в некоторых случаях, коррозионную стойкость [11–13]. Однако магнитная электрополировка пока не получила широкого применения в промышленности. Электрополировка также повышает коррозионную стойкость поверхности за счет влияния пассивного слоя, содержащего в том числе оксиды и гидроксиды хрома [14, 15]. Одним из основных преимуществ электрохимической обработки является возможность получения хорошего качества поверхности даже для элементов сложной формы. Однако даже после процесса электрополировки на поверхности могут быть определенные дефекты, в том числе возникшие в результате длительного использования электролита, неправильной плотности тока или локального перегрева электролита. К наиболее распространенным дефектам относятся эффект «апельсиновой корки», тени, подтеки и неравномерная полировка материала [16, 17].
Однако даже после процесса электрополировки на поверхности могут быть определенные дефекты, в том числе возникшие в результате длительного использования электролита, неправильной плотности тока или локального перегрева электролита. К наиболее распространенным дефектам относятся эффект «апельсиновой корки», тени, подтеки и неравномерная полировка материала [16, 17].
Интенсивная эксплуатация фосфорно-серных ванн в промышленных масштабах и загрязнение таких ванн ионами металлов существенно влияет на увеличение времени процесса электрополировки, ухудшение шероховатости и блеска получаемых поверхностных слоев [18]. Таким образом, представляется целесообразным поиск путей хотя бы частичного улучшения свойств загрязненных технологических ванн, в том числе устранения ионов меди, никеля, железа и хрома, мигрирующих в ванну при анодном растворении. В литературе имеются многочисленные публикации, авторы которых пытались найти рациональные пути потенциального удаления металлов из сточных вод с использованием электрохимических методов. Эффективное удаление ионов меди из разбавленных промышленных сточных вод проводили в электрохимическом реакторе с пластинчатым электродом [19].]. Особый интерес представляет случай очистки сточных вод гальванического цеха, так как в результате практически полностью восстановилось содержание меди в растворе. В процессе использовался электролизер с катодным и анодным пространствами, разделенными мембраной. Катод представлял собой сетку из нержавеющей стали, а анод — титановую решетку, покрытую оксидом рутения [20]. Извлечение никеля из сточных вод возможно как электрохимическими, так и химическими методами. Электрохимические методы позволяют получать относительно чистый металл, но их нельзя применять с широко используемыми растворами на основе хлоридов, так как их восстановление может привести к выделению высокотоксичного газообразного хлора. Примером может служить метод химической дестабилизации отработанного раствора никелевого покрытия, в результате которого происходит катодное восстановление ионов никеля и образование никеля в виде порошка [21].
Эффективное удаление ионов меди из разбавленных промышленных сточных вод проводили в электрохимическом реакторе с пластинчатым электродом [19].]. Особый интерес представляет случай очистки сточных вод гальванического цеха, так как в результате практически полностью восстановилось содержание меди в растворе. В процессе использовался электролизер с катодным и анодным пространствами, разделенными мембраной. Катод представлял собой сетку из нержавеющей стали, а анод — титановую решетку, покрытую оксидом рутения [20]. Извлечение никеля из сточных вод возможно как электрохимическими, так и химическими методами. Электрохимические методы позволяют получать относительно чистый металл, но их нельзя применять с широко используемыми растворами на основе хлоридов, так как их восстановление может привести к выделению высокотоксичного газообразного хлора. Примером может служить метод химической дестабилизации отработанного раствора никелевого покрытия, в результате которого происходит катодное восстановление ионов никеля и образование никеля в виде порошка [21]. В исследовании Хана [22] анализируется эффективность удаления ионов никеля и цинка из загрязненного раствора. 50-часовой процесс, проведенный с использованием анода из нержавеющей стали и алюминиевого катода, привел к уменьшению содержания ионов никеля в растворе на 70%. Бакаев и др. проанализирована электрохимическая регенерация электролитов электрополировки хромистой стали с применением регенератора с мембраной и углеродным катодом волокнистой структуры, что позволило ускорить процесс в 10 раз. В результате было восстановлено примерно 50% железа [23].
В исследовании Хана [22] анализируется эффективность удаления ионов никеля и цинка из загрязненного раствора. 50-часовой процесс, проведенный с использованием анода из нержавеющей стали и алюминиевого катода, привел к уменьшению содержания ионов никеля в растворе на 70%. Бакаев и др. проанализирована электрохимическая регенерация электролитов электрополировки хромистой стали с применением регенератора с мембраной и углеродным катодом волокнистой структуры, что позволило ускорить процесс в 10 раз. В результате было восстановлено примерно 50% железа [23].
Цель исследования — оценить влияние восстановительных промышленных фосфорно-серных ванн электрополировки на качество поверхности, получаемой в процессе электрополировки. Автор проанализировал влияние катодного восстановления на блеск, шероховатость поверхности и коррозионную стойкость электрополированной хромоникелевой стали.
2. Экспериментальные процедуры
2.1. Материалы
Испытания проводились на нержавеющей стали AISI 304 следующего состава (мас. %): 0,037 % C, 0,42 % Si, 0,057 % N, 1,28 % Mn, 0,029% P, 0,002 % S, 18,13 % Cr, 8,04 % Ni и остальное Fe. Образцы вырезали из холоднокатаных листов нержавеющей стали толщиной 1,5 мм.
%): 0,037 % C, 0,42 % Si, 0,057 % N, 1,28 % Mn, 0,029% P, 0,002 % S, 18,13 % Cr, 8,04 % Ni и остальное Fe. Образцы вырезали из холоднокатаных листов нержавеющей стали толщиной 1,5 мм.
Испытания проводились на трех типах образцов. Для восстановления в технологической ванне с применением катодного восстановления использовались прямоугольные образцы шириной 40 мм и длиной 150 мм с двумя крепежными отверстиями диаметром 7 мм, расположенными в верхней части. Для исключения влияния неравномерного погружения на границу между фазами верхняя часть электродов была закреплена непроводящей тефлоновой лентой, обеспечивающей площадь воздействия 67 см 2 . Перед электролизом электроды механически полировали наждачной бумагой зернистостью № 400, № 600 и № 800.
Испытания качества поверхности после электрополировки проводились на образцах шириной 30 мм и длиной 90 мм с отверстием диаметром 12 мм, расположенным на расстоянии 5 мм от верхней кромки. Верхняя часть образцов была защищена лентой из ПТФЭ, в результате чего площадь экспонируемой поверхности составила 35 см 2 .
Ячейка Metrohm для испытаний на коррозию объемом 1 литр позволяет проводить измерения образцов, обеспечивая площадь экспонируемой поверхности 1 см 2 . В связи с этим испытания проводились на образцах диаметром 16,7 мм и толщиной 1,5 мм, с отверстием диаметром 1 мм на расстоянии 1 мм от края образца.
Все типы образцов были изготовлены из одного и того же куска листового металла. Перед обработкой образцы обезжиривали в ультразвуковой мойке в ацетоне в течение 20 минут. После процесса восстановления образцы промывали в дистиллированной воде, а после электрополировки дополнительно в дистиллированной воде в ультразвуковой мойке.
2.2. Экспериментальная схема
Оборудование для восстановления и электрополировки состояло из следующих элементов: лабораторный блок питания КП-131 (КП-Электроника), счетчик электрического заряда (КП-Электроника), управляемая механическая мешалка EUROSTAR 60 (ИКА), водяная баня (Пилот ONE Huber CC-K12) и разработанную схему (рис. 1). Схема изготовлена из медного листа толщиной 1,5 мм. Все соединения были выполнены таким образом, чтобы обеспечить протекание тока с помощью медных болтовых соединений. Для отделения катода от анода использовались непроводящие элементы в виде полиэтиленовых кубиков, соединенных с рамой с помощью медных болтов.
1). Схема изготовлена из медного листа толщиной 1,5 мм. Все соединения были выполнены таким образом, чтобы обеспечить протекание тока с помощью медных болтовых соединений. Для отделения катода от анода использовались непроводящие элементы в виде полиэтиленовых кубиков, соединенных с рамой с помощью медных болтов.
В процессе катодного восстановления катод располагался в центре корпуса, а аноды располагались на расстоянии 40 мм от центральной оси. Для процесса электрополировки анод располагался по центру, а два катода располагались на меньшем расстоянии, то есть на расстоянии 20 мм от центральной оси.
2.3. Восстановление с использованием метода катодного восстановления
Проведенные исследования касались степени восстановления технологической ванны после процесса электрополировки методом катодного восстановления. Испытуемая ванна длительное время использовалась в промышленных целях, поэтому исходный уровень ее загрязнения был очень высоким (концентрация ионов Fe : Cr : Ni : Cu = 50 : 15 : 2,2 : 1,45 г·дм -3 ). Процесс восстановления применяли к 2000 см 3 технологической ванны, помещенной в стеклянный стакан на водяной бане и постоянно перемешиваемой с использованием механической мешалки. Процесс проходил в следующих условиях: температура 50°С, скорость перемешивания 50 об/мин, плотность тока 0,0015 А·см -2 . Продолжительность процесса восстановления составила 15 циклов по 12 часов каждый. Общая продолжительность процесса электролиза составила 180 часов. После окончания каждого цикла электролиза продолжительностью 720 минут электроды промывали в дистиллированной воде, а катод заменяли новым. После надлежащего перемешивания электролита образец объемом 2 см 3 был собран для тестирования ICP.
Процесс восстановления применяли к 2000 см 3 технологической ванны, помещенной в стеклянный стакан на водяной бане и постоянно перемешиваемой с использованием механической мешалки. Процесс проходил в следующих условиях: температура 50°С, скорость перемешивания 50 об/мин, плотность тока 0,0015 А·см -2 . Продолжительность процесса восстановления составила 15 циклов по 12 часов каждый. Общая продолжительность процесса электролиза составила 180 часов. После окончания каждого цикла электролиза продолжительностью 720 минут электроды промывали в дистиллированной воде, а катод заменяли новым. После надлежащего перемешивания электролита образец объемом 2 см 3 был собран для тестирования ICP.
2.4. Электрополировка
Процесс электрополировки проводили как для ванны без электрохимического восстановления (без ЭВ), так и с электрохимическим восстановлением (с ЭВ) в стеклянном стакане, содержащем 2000 см 3 технологической ванны, в следующих условиях: температура 55°С , скорость перемешивания 50 об/мин, плотность тока 5 А·дм -2 . Испытывались три варианта продолжительности процесса: 45, 90 и 180 минут. Полученные образцы промывали в дистиллированной воде и подвергали испытаниям на шероховатость и блеск поверхности. Дополнительно определяли уменьшение массы в результате анодного растворения.
Испытывались три варианта продолжительности процесса: 45, 90 и 180 минут. Полученные образцы промывали в дистиллированной воде и подвергали испытаниям на шероховатость и блеск поверхности. Дополнительно определяли уменьшение массы в результате анодного растворения.
2.5. Тесты ICP
Собранные образцы были подвергнуты тестам ICP-OES (опто-эмиссионная спектроскопия с индуктивно связанной плазмой) с использованием прибора Thermo Scientific iCAP 7000 Series ICP-OES с автоматическим устройством подачи образцов и программным обеспечением, изготовленным Qtegra Intelligent Scientific Data Solution. .
2.6. Тесты на блеск
Блеск тестировали с использованием гониофотометра Rhopoint IQ, измеряющего блеск под углами 20/60/85°. В качестве основного измерения из доступных параметров оборудования был выбран угол блеска 20°. Согласно рекомендациям производителя [24], для измерения высокоглянцевых покрытий и полированных металлов следует использовать угол измерения 20°, так как он позволяет получить повышенную точность и разрешение. Для каждого образца было проведено шесть измерений.
Для каждого образца было проведено шесть измерений.
2.7. Испытания на шероховатость
Испытания на шероховатость проводились с использованием прибора для измерения шероховатости поверхности Mitutoyo Surftest SJ-301. Для каждого образца было проведено шесть измерений на центральной оси, параллельной верхнему краю образца, на равных расстояниях.
2.8. Оптический профилометр поверхности
Для количественного сравнения неровностей большой площади, наблюдаемых на поверхности анализируемых образцов, визуализация была проведена с использованием профилографа поверхности Sensofar S Neox, позволяющего получать количественную информацию о топографии поверхности с разрешением десятков нанометров на длине до 10 см. Всякий раз, когда необходимо было проанализировать область, которая выходила за пределы диапазона сканирования за один проход, процесс сшивания проводился с использованием специального программного обеспечения SensoMAP Standard. Это же программное обеспечение использовалось для подготовки визуализации записанных данных. Количественную оценку полученных профилей проводили с использованием программного обеспечения SPIP производства Image Metrology [25]. Следует отметить, что количественный анализ изменений шероховатости поверхности, вызванных различными факторами, неоднократно успешно применялся для оценки влияния той или иной среды на анализируемый материал [26–29].].
Количественную оценку полученных профилей проводили с использованием программного обеспечения SPIP производства Image Metrology [25]. Следует отметить, что количественный анализ изменений шероховатости поверхности, вызванных различными факторами, неоднократно успешно применялся для оценки влияния той или иной среды на анализируемый материал [26–29].].
2.9. Испытания на коррозионную стойкость
Стойкость к точечной коррозии стали после электрополировки в ванне с ЭО и без ЭО оценивали в потенциодинамических испытаниях. Коррозионный раствор представлял собой 0,5 M NaCl с температурой 25 ± 1°C. Испытания проводились с использованием потенциостата Solartron SI 1287 производства AMETEK. Использовалась коррозионная испытательная ячейка Metrohm объемом 1 дм 3 с водяной завесой, соединенной с водяной баней. Использовалась схема из трех электродов, где испытуемый электрод представлял собой анализируемую сталь, противоэлектрод — платиновый электрод, а электрод сравнения — насыщенный каломельный электрод. Полученные данные были проанализированы с использованием специального программного обеспечения CorrView.
Полученные данные были проанализированы с использованием специального программного обеспечения CorrView.
3. Результаты и обсуждение
3.1. Электрохимическое восстановление технологической ванны
Проведенные ИСП-тесты отобранных образцов позволили определить содержание ионов металлов (медь, никель, железо, хром) как в ванне до электрохимического восстановления, так и на различных стадиях процесса электрохимического восстановления. Результаты испытаний, проведенных этим методом, представлены в виде диаграмм изменения содержания ионов меди и никеля в анализируемом растворе (рис. 2). Несмотря на скоропортящуюся способность загрязняющих веществ, накапливающихся на катоде в процессе, наблюдалось постепенное удаление ионов меди и никеля из ванны в зависимости от продолжительности электролиза. Эффективность удаления меди и никеля в анализируемом процессе составила 53 % и 47 % соответственно. Полученные результаты могут служить основой для оценки продолжительности процесса, необходимого для полного удаления меди и никеля из раствора. Для меди процесс должен длиться более 340 часов, для никеля — более 380 часов. Реализация такого процесса в промышленных масштабах была бы чрезвычайно трудоемкой и энергозатратной. В очень кислой среде (pH около 1) из раствора можно удалить в основном медь и никель. Попытка удалить железо и хром из анализируемого процесса не увенчалась успехом. Согласно первоначальным ожиданиям, их содержание в растворе практически не изменилось. Полученные результаты демонстрируют возможность удаления части загрязнений на месте их появления, непосредственно в технологической ванне. Однако в промышленных условиях проведение процесса восстановления в ванне было бы очень трудоемким. Таким образом, авторы данной статьи рассматривали возможность увеличения поверхности катодов, так как в противном случае процесс потребовал бы слишком больших усилий и был бы неоправданным с экономической точки зрения.
Для меди процесс должен длиться более 340 часов, для никеля — более 380 часов. Реализация такого процесса в промышленных масштабах была бы чрезвычайно трудоемкой и энергозатратной. В очень кислой среде (pH около 1) из раствора можно удалить в основном медь и никель. Попытка удалить железо и хром из анализируемого процесса не увенчалась успехом. Согласно первоначальным ожиданиям, их содержание в растворе практически не изменилось. Полученные результаты демонстрируют возможность удаления части загрязнений на месте их появления, непосредственно в технологической ванне. Однако в промышленных условиях проведение процесса восстановления в ванне было бы очень трудоемким. Таким образом, авторы данной статьи рассматривали возможность увеличения поверхности катодов, так как в противном случае процесс потребовал бы слишком больших усилий и был бы неоправданным с экономической точки зрения.
3.2. Исследования поверхности
Шероховатость поверхности и блеск измерялись как для полученных образцов, так и для образцов после процесса электрополировки.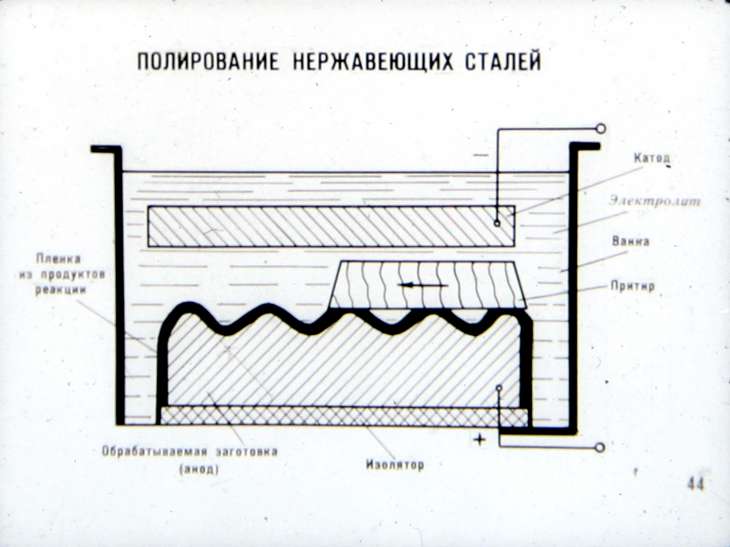 Для минимизации влияния качества поверхности исходных образцов на результаты электрополировки все испытания по электрополировке проводились на таких рядных образцах, которые характеризовались шероховатостью поверхности Ra = 0,16 µ м (рис. 3). Это позволило получить одинаковые начальные условия для всех электрополированных образцов. Процесс электрополировки проводили в двух различных вариантах ванны: промышленной без ЭП и с ЭП. Для ванны без ЭП значение шероховатости после процесса электрополировки ухудшилось по сравнению с исходными образцами, а для ванны с ЭП отмечено постепенное улучшение при увеличении продолжительности процесса (рис. 3, а). В отдельных сериях наилучшие результаты по шероховатости поверхности как у ванны с ЭР (Ra = 0,13 мкм м) и без ЭР (Ra = 0,18 мкм м) при длительности процесса 90 мин. Результаты остальных параметров амплитудной шероховатости, таких как асимметрия шероховатости поверхности Rsk и эксцесс Rku (рис. 3(б)) были значительно улучшены после процесса электрополировки.
Для минимизации влияния качества поверхности исходных образцов на результаты электрополировки все испытания по электрополировке проводились на таких рядных образцах, которые характеризовались шероховатостью поверхности Ra = 0,16 µ м (рис. 3). Это позволило получить одинаковые начальные условия для всех электрополированных образцов. Процесс электрополировки проводили в двух различных вариантах ванны: промышленной без ЭП и с ЭП. Для ванны без ЭП значение шероховатости после процесса электрополировки ухудшилось по сравнению с исходными образцами, а для ванны с ЭП отмечено постепенное улучшение при увеличении продолжительности процесса (рис. 3, а). В отдельных сериях наилучшие результаты по шероховатости поверхности как у ванны с ЭР (Ra = 0,13 мкм м) и без ЭР (Ra = 0,18 мкм м) при длительности процесса 90 мин. Результаты остальных параметров амплитудной шероховатости, таких как асимметрия шероховатости поверхности Rsk и эксцесс Rku (рис. 3(б)) были значительно улучшены после процесса электрополировки. Для образцов, подвергнутых электрополировке в течение 90 минут и более, полученные результаты Rsk и Rk были близки к ожидаемым значениям (Rsk = 3; Rku = 0).
Для образцов, подвергнутых электрополировке в течение 90 минут и более, полученные результаты Rsk и Rk были близки к ожидаемым значениям (Rsk = 3; Rku = 0).
Уменьшение массы образцов после электрополировки увеличивалось пропорционально продолжительности процесса. Учитывая полученные результаты, не рекомендуется увеличивать время процесса электрополировки, так как потеря веса велика, а эффект при этом лишь незначительно улучшается. Также было установлено, что образцы, подвергнутые электрополировке в ванне с ЭО, характеризовались меньшей потерей массы, чем обработанные в ванне с ЭО, что в сочетании с полученной меньшей шероховатостью и улучшенным блеском является важным преимуществом (табл. 1, Рисунок 3). По мере увеличения продолжительности процесса различия в потере массы образцов с ЭР и без нее становились меньше, хотя и оставались значительными. Их было, соответственно, 13%, 9% и 7% для процесса длительностью 45 мин, 90 мин и 180 мин.
Наилучшие результаты по глянцу поверхности были получены после электрополировки для ванны с ЭП продолжительностью 90 минут — увеличение примерно на 500 GU. Для ванны без ЭР 90-минутная продолжительность также дала относительно лучшие результаты, хотя в этом случае прирост достиг лишь 300 GU (рис. 4). Попытка продлить процесс на более длительное время (180 минут) привела к ухудшению полученных результатов блеска как для ванны с ЭО, так и без нее.
Для ванны без ЭР 90-минутная продолжительность также дала относительно лучшие результаты, хотя в этом случае прирост достиг лишь 300 GU (рис. 4). Попытка продлить процесс на более длительное время (180 минут) привела к ухудшению полученных результатов блеска как для ванны с ЭО, так и без нее.
В свете проведенных исследований для промышленных ванн, сильно загрязненных ионами меди, железа, хрома, никеля, рекомендуется использовать относительно низкие плотности тока. Результаты, полученные с использованием метода оптического профилирования поверхности при плотности тока 0,05 А·см −2 , показали, что образцы, прошедшие электрополировку в ванне с ЭО, характеризуются более гладкой поверхностью (Sq = 0,22 мк м; Sz = 0,770 мк м), чем образцы, прошедшие электрополировку в ваннах без ЭО (Sq = 0,27 мк м; Sz = 1,044 мкм м) (рис. 5).
3.3. Влияние плотности тока
Для анализа влияния плотности тока на результаты электрополировки процесс проводился с использованием вышеуказанных ванн без ЭП и с ЭП, при двух различных плотностях тока. Шероховатость поверхности измеряли как для образцов в состоянии поставки, так и для образцов после процесса электрополировки. Приложенные плотности тока составляли соответственно 0,05 А·см −2 для I = 1,75 A и 0,20 A·см −2 для I = 4,00 A. Открытая поверхность была скорректирована таким образом, чтобы получить одинаковую удельную нагрузку. Для образцов, прошедших электрополировку при более высоких плотностях тока, были отмечены появляющиеся подтеки на всей экспонируемой поверхности, что привело к значительному ухудшению шероховатости поверхности образцов после электрополировки по сравнению с исходными образцами, как для ванн без ЭО, так и с ЭП.
Шероховатость поверхности измеряли как для образцов в состоянии поставки, так и для образцов после процесса электрополировки. Приложенные плотности тока составляли соответственно 0,05 А·см −2 для I = 1,75 A и 0,20 A·см −2 для I = 4,00 A. Открытая поверхность была скорректирована таким образом, чтобы получить одинаковую удельную нагрузку. Для образцов, прошедших электрополировку при более высоких плотностях тока, были отмечены появляющиеся подтеки на всей экспонируемой поверхности, что привело к значительному ухудшению шероховатости поверхности образцов после электрополировки по сравнению с исходными образцами, как для ванн без ЭО, так и с ЭП.
Детальный осмотр возникающих дефектов позволил обнаружить, что на поверхности материала образовались продолговатые впадины. Их ориентация по отношению к положению образцов при электрополировке была вертикальной. Поверхность была проанализирована с использованием профилографа поверхности для измерения расстояния между этими впадинами. Полученные результаты позволили провести количественное сравнение наблюдаемых результатов процесса электрополировки. Полученные профили были положены в основу расчета следующих параметров: Δ Z , максимальная разница высот в пределах образца; Sz — разность уровней в усредненной группе волнистостей; Sq — среднеквадратическая шероховатость по профилю; и FFT_ampl, сумма амплитуд двух первых гармонических составляющих FFT, которые количественно определяют неровности поверхности. В силу специфики каждого из этих коэффициентов и типа информации, которую они несут, их сопоставление может быть интерпретировано в зависимости от анализируемой проблемы. Однако с точки зрения замеченных волнистостей наиболее ярко различия проявляются на Δ Z коэффициент. Эти значения были присвоены записанным профилям поверхности (рис. 6).
Полученные результаты позволили провести количественное сравнение наблюдаемых результатов процесса электрополировки. Полученные профили были положены в основу расчета следующих параметров: Δ Z , максимальная разница высот в пределах образца; Sz — разность уровней в усредненной группе волнистостей; Sq — среднеквадратическая шероховатость по профилю; и FFT_ampl, сумма амплитуд двух первых гармонических составляющих FFT, которые количественно определяют неровности поверхности. В силу специфики каждого из этих коэффициентов и типа информации, которую они несут, их сопоставление может быть интерпретировано в зависимости от анализируемой проблемы. Однако с точки зрения замеченных волнистостей наиболее ярко различия проявляются на Δ Z коэффициент. Эти значения были присвоены записанным профилям поверхности (рис. 6).
Для образцов, электрополированных при плотности тока 0,05 А·см −2 , разница в шероховатости Ra после процесса составила ±0,03 µ м. В то же время для образцов, электрополированных при плотности тока 0,20 А·см -2 , отмечено увеличение шероховатости даже на 0,1 мк м по сравнению с шероховатостью исходного образца. Представленные параметры аналогичны с точки зрения трендов. Однако из-за их чувствительности к характерным морфологическим элементам видны некоторые различия. Например, параметр шероховатости Sq учитывает, кроме волнистости, еще и мелкие морфологические детали, к которым не чувствительны другие параметры. С другой стороны, FFT_ampl относится только к неровностям, обнаруженным в профилях алгоритмами DFFT.
В то же время для образцов, электрополированных при плотности тока 0,20 А·см -2 , отмечено увеличение шероховатости даже на 0,1 мк м по сравнению с шероховатостью исходного образца. Представленные параметры аналогичны с точки зрения трендов. Однако из-за их чувствительности к характерным морфологическим элементам видны некоторые различия. Например, параметр шероховатости Sq учитывает, кроме волнистости, еще и мелкие морфологические детали, к которым не чувствительны другие параметры. С другой стороны, FFT_ampl относится только к неровностям, обнаруженным в профилях алгоритмами DFFT.
Авторы проанализировали пороговую плотность тока электрополировки, при которой можно заметить возникающие в процессе дефекты. Для температуры 55°С пороговое значение составляет 0,17 А·см -2 . Никаких пятен при этой плотности тока замечено не было. По мере увеличения плотности эффекты становятся более заметными, от небольших пятен на нижнем крае при 0,18 A·см −2 до четких пятен примерно на 1 см от нижнего края при 0,19 A·см −2 , до заметных пятен по всей поверхности при 0,20 А·см −2 (табл. 2).
2).
Появление дефектов после процесса электрополировки наблюдалось также в стали марки 316Л, где приложение температуры 55°С и плотности тока 0,20 А·см −2 приводило к появлению поверхностных дефектов (подтеков на электрополированных образцов) в ванне с серной кислотой(VI), ортофосфорной кислотой, гликолем, щавелевой кислотой и ацетанилидом.
В то же время применение высоких плотностей тока при электрополировании стали 304 или 316 в незагрязненных ваннах, содержащих ортофосфорную кислоту(V), серную кислоту(VI) и органические добавки, т.е. триэтиламин, глицерин, триэтаноламин, этаноламина, диэтаноламина и бутилдигликоля не приводит к возникновению поверхностных дефектов [30].
3.4. Загрязнение катода после процесса электрополировки
После проведенных процессов электрополировки продолжительностью 45, 90 и 180 минут было замечено изменение внешнего вида катодов в зависимости от типа используемой ванны. В ваннах с ЭО на катоде накапливалось значительно меньше загрязняющих веществ, чем в ваннах без ЭВ (рис. 7).
7).
В промышленных условиях загрязнения, накапливающиеся на катодах в процессе, снижают достижимый диапазон плотности тока, что приводит к необходимости периодической очистки или замены катодов. Катоды, используемые в восстановленной ванне, загрязняются через более длительное время, так как содержание ионов меди в ванне ниже. Это может оказать положительное влияние на протекание процесса в промышленных условиях за счет отсутствия необходимости частой очистки катодов после процесса.
3.5. Испытания на коррозионную стойкость
Потенциодинамические испытания в 0,5 M растворе NaCl были использованы для определения влияния восстановления в ванне на изменение потенциала развития питтинга ( E pit ) и потенциала анодно-катодного переноса ( E КА ) образцов после процесса электрополировки (рис. 8). После определения стационарного потенциала анализируемых образцов были проведены потенциодинамические испытания, начиная со значения потенциала ниже на 0,25 В от ранее определенного стационарного потенциала. Испытания проводились при скорости сканирования 1 мВ/с. После достижения потенциала, при котором плотность тока увеличилась примерно на три порядка до значения 1·10 -4 А·см -2 , направление поляризации меняли и измерения продолжали до момента пересечения возвращающейся кривой с исходной. Было проведено 12 измерений в двух сериях, для ванн с ЭР и без нее. Затем из полученных потенциодинамических кривых считывали значения E pit и E KA (табл. 3).
Испытания проводились при скорости сканирования 1 мВ/с. После достижения потенциала, при котором плотность тока увеличилась примерно на три порядка до значения 1·10 -4 А·см -2 , направление поляризации меняли и измерения продолжали до момента пересечения возвращающейся кривой с исходной. Было проведено 12 измерений в двух сериях, для ванн с ЭР и без нее. Затем из полученных потенциодинамических кривых считывали значения E pit и E KA (табл. 3).
На основании измерений, проведенных для образцов, прошедших электрополировку в ваннах без ЭО и с ЭО, было замечено, что полученные E яма результаты были ок. 0,5 V SCE, , что было аналогично результатам, полученным в предыдущих исследованиях [30]. В то же время установлено, что для образцов, электрополированных в ванне с ЭВ, многие результаты были ниже 0,5 V SCE , а для образцов, электрополированных в ванне без ЭВ, большинство результатов превышало это значение. В связи с этим авторы решили проанализировать значимость различий между полученными результатами с использованием методов анализа данных, используемых в различных видах оценки данных, в том числе в медицине, химическом анализе или технике [31–34].
В связи с этим авторы решили проанализировать значимость различий между полученными результатами с использованием методов анализа данных, используемых в различных видах оценки данных, в том числе в медицине, химическом анализе или технике [31–34].
Анализ нормальности с использованием критерия Шапиро-Уилка не показал значительного отклонения от нормального распределения. Анализ различий между средними значениями E pit показал, что среднее значение было значительно ниже для образцов, электрополированных в ванне с ЭВ (0,462 ± 0,056 В ЭВ ), чем в ванне без ЭВ (0,552 ± 0,13 В ЭВ). ). Кроме того, сравнение дисперсии показало, что диапазон вариабельности результатов был намного выше в группе без ER (критерий Левена).
Полученные результаты показывают, что восстановление технологической ванны приводит к ухудшению стойкости электрополированных образцов к точечной коррозии. Однако следует отметить, что результаты, полученные для этой серии, характеризовались более высокой повторяемостью, чем для ванн без ЭР (рис. 9). Медиана и квартильный диапазон для образцов, электрополированных в ванне с ЭО, составили соответственно 0,45 В СЭЭ и 0,43–0,49 В СЭЭ , а для ванн без ЭУ 0,57 В9.0165 SCE и 0,46–0,66 V SCE . Аналогичный анализ, как и для E ямы , был проведен для E KA. Существенных различий между результатами для образцов, подвергнутых электрополировке в ваннах с ЭО и без него, не обнаружено.
9). Медиана и квартильный диапазон для образцов, электрополированных в ванне с ЭО, составили соответственно 0,45 В СЭЭ и 0,43–0,49 В СЭЭ , а для ванн без ЭУ 0,57 В9.0165 SCE и 0,46–0,66 V SCE . Аналогичный анализ, как и для E ямы , был проведен для E KA. Существенных различий между результатами для образцов, подвергнутых электрополировке в ваннах с ЭО и без него, не обнаружено.
4. Выводы
В анализируемом процессе восстановления в технологической ванне с применением катодного восстановления эффективность удаления меди и никеля составила соответственно 53% и 47%. Полученные результаты позволяют оценить продолжительность процесса, необходимого для полного удаления меди (340 ч) и никеля (380 ч) из раствора. Однако реализация такого процесса в промышленных масштабах потребовала бы очень много времени и энергии.
Для ванны без ЭП значение шероховатости после процесса электрополировки ухудшилось по сравнению с исходными образцами, а для ванны с ЭП отмечено постепенное улучшение при увеличении продолжительности процесса. Испытания качества поверхности после электрополировки показали, что наилучшие результаты, как для ванн с ЭП (Ra = 0,13 мкм мкм; блеск 638 GU), были получены при процессе электрополировки продолжительностью 90 минут.
Испытания качества поверхности после электрополировки показали, что наилучшие результаты, как для ванн с ЭП (Ra = 0,13 мкм мкм; блеск 638 GU), были получены при процессе электрополировки продолжительностью 90 минут.
Уменьшение массы образцов после электрополировки увеличивалось пропорционально продолжительности процесса. Также было отмечено, что образцы, прошедшие электрополировку в ванне с ЭО, характеризовались меньшей потерей массы по сравнению с образцами, прошедшими электрополировку в ванне без ЭО, при всех вариантах продолжительности процесса. В то же время для ванн с ЭВ на катод осаждается значительно меньше загрязнений, чем для ванн без ЭВ. В промышленных условиях загрязнения, накапливающиеся на катодах в процессе, снижают достижимый диапазон плотности тока, что приводит к необходимости периодической очистки или замены катодов. Катоды, используемые в восстановленной ванне, загрязняются через более длительное время, так как содержание ионов меди в ванне ниже. Это может оказать положительное влияние на протекание процесса в промышленных условиях за счет отсутствия необходимости частой очистки катодов после процесса.
Доступность данных
Данные, используемые для подтверждения результатов этого исследования, в настоящее время находятся под эмбарго, а результаты исследования могут быть коммерциализированы после завершения исследования. Запросы данных через 24 месяца после публикации этой статьи будут рассмотрены соответствующим автором.
Конфликт интересов
Авторы заявляют об отсутствии конфликта интересов.
Благодарности
Работа выполнена при поддержке Национального центра исследований и разработок (NCBiR) в рамках программы LIDER (№ LIDER/22/0187/L-7/15/NCBR/2016).
Ссылки
S. M. Aguilar-Sierra и E. F. Echeverría, «Улучшение электрополировки сплава 1100 Al для солнечных тепловых применений», Journal of Materials Engineering and Performance , vol. 27, нет. 3, стр. 1387–1395, 2018.
Посмотреть по адресу:
Сайт издателя | Google Scholar
Е.
 Лычковска, П. Лочинский и Э. Хлебус, «Электрополировка нержавеющей стали», Перемышль Химический , том. 92, стр. 1364–1366, 2013.
Лычковска, П. Лочинский и Э. Хлебус, «Электрополировка нержавеющей стали», Перемышль Химический , том. 92, стр. 1364–1366, 2013.Посмотреть по адресу:
Google Scholar
R. Rokicki, T. Hryniewicz, C. Pulletikurthi, K. Rokosz и N. Munroe, «На пути к улучшению коррозионной стойкости и улучшению биосовместимости нитиноловых медицинских устройств», Журнал «Материаловедение и производительность» , том. 24, нет. 4, стр. 1634–1640, 2015.
Посмотреть по адресу:
Сайт издателя | Google Scholar
С. Хабибзаде, Л. Ли, Д. Шум-Тим, Э. К. Дэвис и С. Оманович, «Электрохимическая полировка как метод обработки поверхности нержавеющей стали 316L: на пути к улучшению биосовместимости», Corrosion Science , vol. 87, стр. 89–100, 2014.
Посмотреть по адресу:
Сайт издателя | Google Scholar
Н.
 Элиаз и О. Ниссан, «Инновационные процессы электрополировки медицинских устройств из нержавеющей стали», Journal of Biomedical Materials Research Part A , vol. 83, нет. 2, стр. 546–557, 2007 г.
Элиаз и О. Ниссан, «Инновационные процессы электрополировки медицинских устройств из нержавеющей стали», Journal of Biomedical Materials Research Part A , vol. 83, нет. 2, стр. 546–557, 2007 г.Посмотреть по адресу:
Сайт издателя | Google Scholar
P. Sojitra, C. Engineer, D. Kothwala, A. Raval, H. Kotadia и G. Mehta, «Электрополировка сердечно-сосудистых стентов из нержавеющей стали 316LVM: исследование удаления материала, шероховатости поверхности и коррозии». поведение» Тенденции в области биоматериалов и искусственных органов , vol. 23, pp. 115–121, 2010.
Посмотреть по адресу:
Google Scholar
М. Хайдопулос, С. Туржон, К. Сарра-Бурне, Г. Ларош и Д. Мантовани, «Развитие оптимизированный электрохимический процесс для последующего покрытия нержавеющей стали 316 для применения в стентах», Journal of Materials Science: Materials in Medicine , vol.
 17, нет. 7, стр. 647–657, 2006 г.
17, нет. 7, стр. 647–657, 2006 г.Посмотреть по адресу:
Сайт издателя | Академия Google
H. Zhao, J. Van Humbeeck, J. Sohier и I. De Scheerder, «Электрохимическая полировка коронарных стентов с прорезями из нержавеющей стали 316L», Journal of Materials Science: Materials in Medicine , vol. 13, нет. 10, стр. 911–916, 2002.
Посмотреть по адресу:
Сайт издателя | Google Scholar
T. Hryniewicz и K. Rokosz, «Анализ результатов XPS электрополировки и магнитоэлектрополировки нержавеющей стали AISI 316L в различных условиях», Технология поверхностей и покрытий , том. 204, нет. 16–17, стр. 2583–2592, 2010.
Посмотреть по адресу:
Сайт издателя | Google Scholar
C. Rotty, M. L. Doche, A. Mandroyan, J.
 Y. Hihn, G. Montavon и V. Moutarlier, «Сравнение характеристик электрополировки TSC, ALM и литой нержавеющей стали 316L в h4PO4/h3SO4», Поверхности и интерфейсы , том. 6, стр. 170–176, 2017.
Y. Hihn, G. Montavon и V. Moutarlier, «Сравнение характеристик электрополировки TSC, ALM и литой нержавеющей стали 316L в h4PO4/h3SO4», Поверхности и интерфейсы , том. 6, стр. 170–176, 2017.Посмотреть по адресу:
Сайт издателя | Академия Google
K. Rokosz, T. Hryniewicz, and S. Raaen, «Отношение Cr/Fe по данным XPS-спектров магнитоэлектрополированной нержавеющей стали AISI 316L, аппроксимированных линиями гауссово-лоренцевой формы», Tehnički Vjesnik , vol. 21, нет. 3, стр. 533–538, 2014.
Просмотр по адресу:
Google Scholar
Т. Хриневич и К. Рокош, «Исследование некоторых свойств поверхности нержавеющей стали AISI 316L после магнитоэлектрополировки», и физика, химия , том. 123, нет. 1, стр. 47–55, 2010.
Посмотреть по адресу:
Сайт издателя | Google Scholar
С.
 Дж. Ли и Дж. Дж. Лай, «Влияние параметров процесса электрополировки (ЭП) на коррозионную стойкость нержавеющей стали 316L», Journal of Materials Processing Technology , vol. 140, нет. 1–3, стр. 206–210, 2003.
Дж. Ли и Дж. Дж. Лай, «Влияние параметров процесса электрополировки (ЭП) на коррозионную стойкость нержавеющей стали 316L», Journal of Materials Processing Technology , vol. 140, нет. 1–3, стр. 206–210, 2003.Посмотреть по адресу:
Сайт издателя | Google Scholar
С. Э. Зимняк, М. Хэнсон и П. К. Сандер, «Влияние электрополировки на коррозионное поведение нержавеющей стали 304 в высокотемпературной гидрогенизированной воде», Corrosion Science , vol. 50, нет. 9, стр. 2465–2477, 2008.
Посмотреть по адресу:
Сайт издателя | Google Scholar
С. Е. Зимняк и М. Хэнсон, «Коррозионное поведение нержавеющей стали 304 в высокотемпературной гидрогенизированной воде», Corrosion Science , vol. 44, нет. 10, стр. 2209–2230, 2002.
Посмотреть по адресу:
Сайт издателя | Google Scholar
В.
 Урлеа и В. Браиловски, «Электрополировка и допуски, связанные с электрополировкой, для компонентов из сплава Ti-6Al-4V, селективно расплавленных в порошковом слое», Журнал технологии обработки материалов , том. 242, стр. 1–11, 2017 г.
Урлеа и В. Браиловски, «Электрополировка и допуски, связанные с электрополировкой, для компонентов из сплава Ti-6Al-4V, селективно расплавленных в порошковом слое», Журнал технологии обработки материалов , том. 242, стр. 1–11, 2017 г.Посмотреть по адресу:
Сайт издателя | Google Scholar
C. A. Huang, JH Chang, WJ Zhao и S. Y. Huang, «Изучение поведения электрополировки латуни 73 в 70% растворе H 3 PO 4 с использованием вращающегося дискового электрода», Materials Химия и физика , вып. 146, нет. 3, стр. 230–239, 2014.
Посмотреть по адресу:
Сайт издателя | Академия Google
П. Лочински, Е. Лычковска, А. Павелчик и Б. Щигел, «Влияние эксплуатации ванны на эффективность процесса электрополировки стали», Przemysl Chemiczny , vol. 5, pp. 846–848, 2012.

Посмотреть по адресу:
Google Scholar
C. Solisio, M. Panizza, P. Paganelli, and G. Cerisola, «Электрохимическое восстановление меди (II) из промышленные стоки, часть I: монополярные пластинчатые электроды», Resources, Conservation and Recycling , том. 26, нет. 2, стр. 115–124, 1999.
Посмотреть по адресу:
Сайт издателя | Google Scholar
М. Хансом, К. Пруксаторн, С. Дамронглерд, Х. Вернь и П. Дювернёй, «Электрохимическая обработка тяжелых металлов (Cu2+, Cr6+, Ni2+) из промышленных сточных вод и моделирование восстановления меди», Water Research , vol. 39, нет. 4, стр. 610–616, 2005 г.
Посмотреть по адресу:
Сайт издателя | Google Scholar
Тевтул Ю.А., Нечипоренко О., Винклер И. Извлечение ионов никеля и меди из отработанных технологических растворов.
 1333 NATO Science for Peace and Security Series C: Environmental Security , pp. 235–238, Springer, Berlin, Germany, 2010.
1333 NATO Science for Peace and Security Series C: Environmental Security , pp. 235–238, Springer, Berlin, Germany, 2010.Просмотр по адресу:
Google Scholar ионов никеля из сточных вод с использованием плоских электродов», Торонто, Онтарио, Канада , 2005 г., https://digital.library.ryerson.ca/islandora/object/RULA%3A2365.
Посмотреть по адресу:
Google Scholar
Бакаев В.В., Федоров Е.А., Флеров В.Н. Электрохимическая регенерация электролитов полировки хромсодержащих сталей.1333 Российский журнал прикладной химии , том. 74, нет. 11, стр. 1962–1964, 2001.
Посмотреть по адресу:
Сайт издателя | Google Scholar
https://www.konicaminolta.eu/fileadmin/content/eu/Measuring_Instruments/2_Products/1_Colour_Measurement/5_Gloss_Meters/Rhoipoint/Rhopoint_iQ_pl_08_13.
 pdf.
pdf.https://www.imagemet.com/.
П. Лочински, А. Сикора и Б. Щигель, «Морфология поверхности и состав пассивной пленки после травления и электрополировки», Поверхностная инженерия , том. 33, нет. 5, стр. 395–403, 2017.
Посмотреть по адресу:
Сайт издателя | Google Scholar
M. Moczała, M. Karpińska, M. Poznar, P. Dobryszycki и A. Sikora, «Применение листа плазмы аргона в процессе травления кристаллов карбоната кальция для испытаний с помощью АСМ», Materials Science- Польша , vol. 36, нет. 1, стр. 75–79, 2018 г.
Посмотреть по адресу:
Сайт издателя | Google Scholar
А. Сикора, «Новый подход к исследованию изменения шероховатости неоднородных материалов, облученных УФ-светом и визуализированных с помощью атомно-силовой микроскопии, с поддержкой точного повторяющегося позиционирования области сканирования», Наука и техника измерений , vol.
 28, нет. 3, ID статьи 034016, 2017.
28, нет. 3, ID статьи 034016, 2017.Посмотреть по адресу:
Сайт издателя | Google Scholar
А. Сикора, А. Грабарек, Л. Моронь, М. Валецкий и П. Крыла, «Исследование разрушения материалов на основе полиэтилена световым излучением с помощью атомно-силовой микроскопии», IOP Conference Серия: Материаловедение и инженерия , вып. 113, Артикул ID 012016, 2016.
Вид:
Сайт издателя | Google Scholar
P. Lochyński, E. Łyczkowska, K. Kuczewski и B. Szczygieł, «Точечная коррозия травленой и электрополированной Cr-Ni нержавеющей стали», Przemysl Chemiczny , vol. 93, pp. 762–765, 2014.
Просмотр по адресу:
Google Scholar
D.P. Aun, I.F.D.C. Peixoto, M. Houmard, and V.T.L. Buono, «Улучшение NiTi-сверхэластичных эндодонтических инструментов 90 16 6 6 90 ”, Материаловедение и инженерия: C , том.
 68, стр. 675–680, 2016.
68, стр. 675–680, 2016.Посмотреть по адресу:
Сайт издателя | Google Scholar
Ю. Суеока, М. Сакакибара и К. Сера, «Поведение тяжелых металлов при взаимодействии лишайников с отходами шахт на заброшенном руднике на юго-западе Японии», Metals , vol. 5, нет. 3, стр. 1591–1608, 2015.
Посмотреть по адресу:
Сайт издателя | Google Scholar
А. Аль-Ахмари, М. Ашфак, А. Альфаифи, Б. Абдо, А. Аломар и А. Дауд, «Прогнозирование качества поверхности γ-TiAl, полученного в процессе аддитивного производства, с использованием метода поверхности отклика. », Journal of Mechanical Science and Technology , vol. 30, нет. 1, стр. 345–352, 2016 г.
Посмотреть по адресу:
Сайт издателя | Google Scholar
Ф.
 Дж. Понтес, Дж. Р. Феррейра, М. Б. Силва, А. П. Пайва и П. П. Балестасси, «Искусственные нейронные сети для моделирования шероховатости поверхности процессов обработки», , Международный журнал передовых технологий производства, , том. 49, нет. 9–12, стр. 879–902, 2010.
Дж. Понтес, Дж. Р. Феррейра, М. Б. Силва, А. П. Пайва и П. П. Балестасси, «Искусственные нейронные сети для моделирования шероховатости поверхности процессов обработки», , Международный журнал передовых технологий производства, , том. 49, нет. 9–12, стр. 879–902, 2010.Посмотреть по адресу:
Сайт издателя | Академия Google
Copyright
Copyright © 2018 Paweł Lochyński et al. Это статья с открытым доступом, распространяемая в соответствии с лицензией Creative Commons Attribution License, которая разрешает неограниченное использование, распространение и воспроизведение на любом носителе при условии надлежащего цитирования оригинальной работы.
Как сохранить раствор для электрохимической полировки труб из нержавеющей стали
Электрохимическая полировка аналогична электрополировке. Перед электрополировкой трубку из нержавеющей стали необходимо тщательно обезжирить и очистить обеззараживающим порошком, чтобы масло не загрязнило ванну для полировки. Необходимо часто измерять относительную плотность раствора для электрополировки во время использования. Если относительная плотность меньше указанного значения формулы, это указывает на то, что раствор для электрополировки содержит слишком много воды. Метод выпаривания можно использовать для нагревания раствора до температуры выше 80°C для удаления избытка воды. Недостаточный объем можно дополнить фосфорной кислотой и серной кислотой согласно соотношению формулы. Перед тем, как труба из нержавеющей стали попадет в резервуар для электрохимической полировки, лучше всего слить или высушить воду, прикрепленную к трубе. Если относительная плотность слишком высока и превышает указанное значение формулы, это означает, что влажность слишком низкая. Следует добавить небольшое количество воды, чтобы снизить относительную плотность до указанного значения. По возможности лучше периодически анализировать решение и своевременно вносить коррективы по результатам.
Необходимо часто измерять относительную плотность раствора для электрополировки во время использования. Если относительная плотность меньше указанного значения формулы, это указывает на то, что раствор для электрополировки содержит слишком много воды. Метод выпаривания можно использовать для нагревания раствора до температуры выше 80°C для удаления избытка воды. Недостаточный объем можно дополнить фосфорной кислотой и серной кислотой согласно соотношению формулы. Перед тем, как труба из нержавеющей стали попадет в резервуар для электрохимической полировки, лучше всего слить или высушить воду, прикрепленную к трубе. Если относительная плотность слишком высока и превышает указанное значение формулы, это означает, что влажность слишком низкая. Следует добавить небольшое количество воды, чтобы снизить относительную плотность до указанного значения. По возможности лучше периодически анализировать решение и своевременно вносить коррективы по результатам.
Из-за растворения поверхности трубы из нержавеющей стали в процессе полировки содержание железа, никеля и хрома в растворе будет постепенно увеличиваться. В это время раствор постепенно теряет свою полирующую способность. Какая бы высокая температура или большой ток не включали, это не поможет восстановить полирующую способность. Проанализируйте раствор, если содержание железа превышает 60 г/л и превышает содержание трехвалентного хрома, раствор устарел. Существует два метода регенерации полировального раствора и восстановления полирующей способности. Один из методов заключается в правильном разбавлении раствора водой для снижения кислотности. Такие примеси, как железо, хром и никель, можно частично осадить в виде солей, удалить осадок на дне резервуара, а затем нагреть и выпарить для удаления воды и восстановления исходной относительной плотности. Этот метод более громоздкий в работе. Нужно потреблять больше энергии и времени. Другой метод заключается в замене части раствора. Лучше всего оставить 20% старого раствора и добавить 80% нового раствора. Его можно обрабатывать с меньшим количеством электричества или без него, и вскоре можно будет осуществить обычную полировку.
В это время раствор постепенно теряет свою полирующую способность. Какая бы высокая температура или большой ток не включали, это не поможет восстановить полирующую способность. Проанализируйте раствор, если содержание железа превышает 60 г/л и превышает содержание трехвалентного хрома, раствор устарел. Существует два метода регенерации полировального раствора и восстановления полирующей способности. Один из методов заключается в правильном разбавлении раствора водой для снижения кислотности. Такие примеси, как железо, хром и никель, можно частично осадить в виде солей, удалить осадок на дне резервуара, а затем нагреть и выпарить для удаления воды и восстановления исходной относительной плотности. Этот метод более громоздкий в работе. Нужно потреблять больше энергии и времени. Другой метод заключается в замене части раствора. Лучше всего оставить 20% старого раствора и добавить 80% нового раствора. Его можно обрабатывать с меньшим количеством электричества или без него, и вскоре можно будет осуществить обычную полировку.
В процессе полировки на поверхности катодной свинцовой пластины будет осаждаться толстый слой железа, никеля и других примесей, что повлияет на поверхностную проводимость катода, что приведет к снижению тока и катодного тока плотность полируемой поверхности не повысится, что серьезно влияет на качество полировки. Поэтому необходимо вовремя удалять отложения на катодной пластине, иногда образующие твердую толстую пленку, удалить которую можно только сильным взбиванием, и, наконец, промыть, чтобы вся цепь оставалась незасоренной.
Отношение площади катода к площади анода регулируется на уровне 1/2 площади анода. В этом случае удается предотвратить рост трехвалентного хрома, а избыточный трехвалентный хром окисляется до шестивалентного хрома на поверхности анода. Слишком много трехвалентного хрома может легко привести к старению полировальной жидкости. Расстояние между катодом и анодом слишком велико, увеличивается сопротивление, увеличивается потребляемая мощность, раствор легко нагревается, что сказывается на качестве полировки. Если расстояние слишком мало, легко вызвать короткое замыкание и воспламенение и сжечь продукты черного цвета. Расстояние между катодом и анодом предпочтительно составляет от 100 до 300 мм. Для полировки некоторых сложных труб большого диаметра из нержавеющей стали можно изготовить пиктографические катоды, обеспечивающие равномерное распределение анодного тока. Специально для внутренней поверхности труб из нержавеющей стали во внутреннее отверстие помещается соответствующий пиктографический катод, чтобы все части внутреннего отверстия были равномерно отполированы.
Если расстояние слишком мало, легко вызвать короткое замыкание и воспламенение и сжечь продукты черного цвета. Расстояние между катодом и анодом предпочтительно составляет от 100 до 300 мм. Для полировки некоторых сложных труб большого диаметра из нержавеющей стали можно изготовить пиктографические катоды, обеспечивающие равномерное распределение анодного тока. Специально для внутренней поверхности труб из нержавеющей стали во внутреннее отверстие помещается соответствующий пиктографический катод, чтобы все части внутреннего отверстия были равномерно отполированы.
Во время электрохимической полировки из-за высокой плотности тока и подачи большого тока трубка из нержавеющей стали должна быть отрезана при входе и выходе из бака для полировки. Не подвешивайте и не снимайте светильник с электричеством, чтобы предотвратить образование электрических искр, вызывающих электролиз, и взрыв смеси водорода и кислорода, скопившейся на поверхности бака.
Поскольку через жидкость для ванны проходит сильный ток, он нагревает жидкость для ванны. При непрерывной работе должны быть приняты меры по охлаждению, и для охлаждения постоянно нагревающейся жидкости ванны используется холодильник. Температура полирующего раствора должна поддерживаться в пределах указанного диапазона процесса, чтобы скорость полировки и выравнивания поверхности трубы из нержавеющей стали поддерживалась на нормальном уровне, чтобы эффективно снизить вязкость электролита, уменьшить толщину. слизистой оболочки анода, ускоряют диффузию растворенных продуктов анода и ускоряют конвекцию раствора. Это полезно для десорбции пузырьков воздуха, остающихся на аноде, и позволяет избежать пятен и ямок. Слишком высокая температура вызовет перегрев раствора, ускорит превращение шестивалентного хрома в трехвалентный и легко вызовет поверхностную коррозию. При слишком низкой температуре повышается вязкость раствора и утолщается слизистая оболочка на поверхности анода, что не способствует диффузии растворенных на аноде веществ и значительно снижает полирующий и выравнивающий эффект.
При непрерывной работе должны быть приняты меры по охлаждению, и для охлаждения постоянно нагревающейся жидкости ванны используется холодильник. Температура полирующего раствора должна поддерживаться в пределах указанного диапазона процесса, чтобы скорость полировки и выравнивания поверхности трубы из нержавеющей стали поддерживалась на нормальном уровне, чтобы эффективно снизить вязкость электролита, уменьшить толщину. слизистой оболочки анода, ускоряют диффузию растворенных продуктов анода и ускоряют конвекцию раствора. Это полезно для десорбции пузырьков воздуха, остающихся на аноде, и позволяет избежать пятен и ямок. Слишком высокая температура вызовет перегрев раствора, ускорит превращение шестивалентного хрома в трехвалентный и легко вызовет поверхностную коррозию. При слишком низкой температуре повышается вязкость раствора и утолщается слизистая оболочка на поверхности анода, что не способствует диффузии растворенных на аноде веществ и значительно снижает полирующий и выравнивающий эффект.
При электрохимической полировке трубы из нержавеющей стали плотность анодного тока почти пропорциональна растворению металла. Только подбирая плотность анодного тока и регулируя ее в определенном диапазоне анодных потенциалов, можно получить хорошее качество электрохимической полировки. Наилучшее значение плотности анодного тока должно быть основано на различных составах электролита, фактической полировке и наблюдении за лучшими результатами полировки. Значение в порядке. При соответствующей плотности анодного тока, согласно теории слизистой оболочки, преимущественно растворяются выступающие части микроскопической поверхности, что способствует выравниванию и отделке поверхности. Если плотность анодного тока слишком мала, на поверхности трубы из нержавеющей стали происходит общее растворение анода, и эффект полировки не может быть достигнут. Плотность анодного тока слишком велика, слизистая разрушается, кислород бурно осаждается в потоке газа, поверхность перегревается, что приводит к более быстрому растеканию раствора для электрополировки, слизистая разрушается, больше не существует, возникает электрохимическая коррозия. Поэтому плотность анодного тока в процессе электрополировки необходимо поддерживать на оптимальном уровне, т. е. в пределах заданного диапазона процесса.
Поэтому плотность анодного тока в процессе электрополировки необходимо поддерживать на оптимальном уровне, т. е. в пределах заданного диапазона процесса.
Движение анода ускоряет диффузию растворенного на аноде продукта, который играет роль перемешивания, эффективно удаляя пузырьки на поверхности анода, избегая образования полос в воздушном потоке и предотвращая поверхность трубка из нержавеющей стали от чрезмерной коррозии в результате локального перегрева. Движение анода помогает увеличить плотность анодного тока и улучшить качество электрохимически полированной поверхности трубы из нержавеющей стали. Ионы активного хлора в растворе для электрохимической полировки не допускаются. Ионы хлора могут разрушить защитную слизистую оболочку, образующуюся на поверхности при электрохимической полировке, и вызвать коррозионную точечную коррозию на поверхности трубки из нержавеющей стали. Ионы хлорида могут окисляться при высокой плотности тока анода, превращаясь в газообразный хлор, улетучиваться и удаляться. Источник хлорид-ионов может быть введен в ванну без промывки после травления соляной кислотой, либо введения примесных хлорид-ионов в сырье.
Источник хлорид-ионов может быть введен в ванну без промывки после травления соляной кислотой, либо введения примесных хлорид-ионов в сырье.
Наилучшее соотношение шестивалентного берклия и трехвалентного хрома, шестивалентный хром окисляется в растворе для электрохимической полировки и оказывает пассивирующее защитное действие на поверхность трубы из нержавеющей стали. Трехвалентный хром влияет на сохранение электрополировки. Если в свежеприготовленной жидкости для электрополировки не происходит химической реакции образования трехвалентного хрома, нельзя получить хорошую полируемую поверхность. Только при электролизе некоторого количества трехвалентного хрома в растворе может появиться идеальная полируемая поверхность. Если к формуле добавить хромовый ангидрид, то есть шестивалентный хром будет генерировать водород на катоде, чтобы восстановить часть шестивалентного хрома до трехвалентного хрома посредством электролитической реакции; если в формуле нет хромового ангидрида, трехвалентный хром должен быть растворен в трубке из нержавеющей стали анодом из хрома. Вот почему свежеприготовленная жидкость для электролитической полировки должна быть полностью подвергнута электролизу, прежде чем можно будет выполнять обычную полировку. В раствор, содержащий хромовый ангидрид, добавляют желатин или глицерин, они могут иметь сильную восстановительную реакцию с хромовым ангидридом, и часть шестивалентного хрома переходит в трехвалентный хром. Шестивалентный хром имеет желтый цвет, а трехвалентный хром – зеленый. Они окрашивают раствор в электролите в желто-зеленый цвет. Поэтому электролитическую полировку можно проводить только после обработки электризацией. Наилучшее качество полировки достигается на средней стадии электролитического процесса, а раствор для электролитической полировки должен оставаться желто-зеленым в процессе производства. В это время, по данным химического анализа, соотношение шестивалентного хрома к трехвалентному хрому составляет 3:7. Чтобы сохранить это соотношение, можно наблюдать за цветом электролита. Если цвет желтый, это указывает на то, что электролит содержит шестивалентный хром.
Вот почему свежеприготовленная жидкость для электролитической полировки должна быть полностью подвергнута электролизу, прежде чем можно будет выполнять обычную полировку. В раствор, содержащий хромовый ангидрид, добавляют желатин или глицерин, они могут иметь сильную восстановительную реакцию с хромовым ангидридом, и часть шестивалентного хрома переходит в трехвалентный хром. Шестивалентный хром имеет желтый цвет, а трехвалентный хром – зеленый. Они окрашивают раствор в электролите в желто-зеленый цвет. Поэтому электролитическую полировку можно проводить только после обработки электризацией. Наилучшее качество полировки достигается на средней стадии электролитического процесса, а раствор для электролитической полировки должен оставаться желто-зеленым в процессе производства. В это время, по данным химического анализа, соотношение шестивалентного хрома к трехвалентному хрому составляет 3:7. Чтобы сохранить это соотношение, можно наблюдать за цветом электролита. Если цвет желтый, это указывает на то, что электролит содержит шестивалентный хром. High, вы можете добавить необходимое количество желатина или глицерина, чтобы уменьшить часть шестивалентного хрома до трехвалентного хрома, или произвести трехвалентный хром путем электролиза с большим катодом и маленьким анодом. Если цвет темно-зеленый, это указывает на то, что электролит содержит высокое содержание трехвалентного хрома. Добавьте соответствующее количество раствора ангидрида хрома, растворенного в воде в соответствии с пропорцией, или проведите электролиз полирующего раствора с большим анодом и небольшим католитом, чтобы частично преобразовать трехвалентный хром в шестивалентный хром. Время от времени можно улучшать качество полировки раствора.
High, вы можете добавить необходимое количество желатина или глицерина, чтобы уменьшить часть шестивалентного хрома до трехвалентного хрома, или произвести трехвалентный хром путем электролиза с большим катодом и маленьким анодом. Если цвет темно-зеленый, это указывает на то, что электролит содержит высокое содержание трехвалентного хрома. Добавьте соответствующее количество раствора ангидрида хрома, растворенного в воде в соответствии с пропорцией, или проведите электролиз полирующего раствора с большим анодом и небольшим католитом, чтобы частично преобразовать трехвалентный хром в шестивалентный хром. Время от времени можно улучшать качество полировки раствора.
Если плотность анодного тока составляет 20 мА во время электролитической полировки и время составляет 4 часа, наблюдайте с помощью инструментального металлографического микроскопа, количество съема металла с внутреннего диаметра резьбы трубы из нержавеющей стали составляет около 0,001 мм в минуту, а величина съема металла наружного диаметра резьбы 0,002 мм, профиль зуба в основном неизменен, только вершина зуба слегка притуплена. Плотность анодного тока увеличивается, и пропорционально увеличивается выбрасываемый металл. Для размеров прецизионных труб из нержавеющей стали следует учитывать величину съема металла после электрохимической полировки.
Плотность анодного тока увеличивается, и пропорционально увеличивается выбрасываемый металл. Для размеров прецизионных труб из нержавеющей стали следует учитывать величину съема металла после электрохимической полировки.
Электрохимическая полировка деталей после электросварки или термической обработки. Трубу из нержавеющей стали после электросварки или термической обработки дважды проводят при электрохимической полировке. Первый раз он входит в разделку и полирует 3-5 минут и выводит ее на окисление рыхлого сварочного шлака и термообработку. Используйте проволочную щетку, чтобы очистить его от кожи, или постучите небольшим молотком, а затем войдите в канавку во второй раз и полируйте ее в течение 3–5 минут, чтобы получить лучшие результаты.
После электрохимической полировки трубы из нержавеющей стали, если нет последующей обработки, такой как гальванизация, окраска и другие процессы, должны быть пассивированы и нейтрализованы. Роль нейтрализации заключается в полном удалении кислых веществ, адсорбированных на поверхности после электрохимической полировки и пассивации.

 .. 1,6
.. 1,6 .. 1,6
.. 1,6 Электрохимическое полирование металлов
Электрохимическое полирование металлов Все правила по сольфеджио
Все правила по сольфеджио
 В результате этого процесса не только улучшается качество обработки поверхности самого металла, но и, если оно имеется, покрытия на металле, за счет удаления внешнего неравномерного слоя покрытия или дефектов на металле, возникших при его механической обработке. После электрополирования благодаря большей однородности поверхности увеличивается коррозионная стойкость металлов.
В результате этого процесса не только улучшается качество обработки поверхности самого металла, но и, если оно имеется, покрытия на металле, за счет удаления внешнего неравномерного слоя покрытия или дефектов на металле, возникших при его механической обработке. После электрополирования благодаря большей однородности поверхности увеличивается коррозионная стойкость металлов. При дальнейшем повышении потенциала начинается процесс электролиза воды с интенсивным выделением на аноде кислорода, пузырьки которого срывают вязкий слой. Вследствие этого величина тока возрастает, а качество электрополирования снижается.
При дальнейшем повышении потенциала начинается процесс электролиза воды с интенсивным выделением на аноде кислорода, пузырьки которого срывают вязкий слой. Вследствие этого величина тока возрастает, а качество электрополирования снижается. ;
;
 Плавно поворачивая регулятор тока вправо, установить необходимое значение напряжения (см. табл.) и записать сразу показания миллиамперметра, не дожидаясь постоянного значения тока, при этом рассчитать цену каждого деления шкалы обоих измерительных приборов. Проводить электрополирование при 7-8 значениях величины тока. Следить за тем, чтобы напряжение на электролизере не превышало 4 В, иначе в результате окисления воды на аноде будет выделяться кислород, который вместе с водородом, выделяющимся на катоде, может образовать гремучий газ.
Плавно поворачивая регулятор тока вправо, установить необходимое значение напряжения (см. табл.) и записать сразу показания миллиамперметра, не дожидаясь постоянного значения тока, при этом рассчитать цену каждого деления шкалы обоих измерительных приборов. Проводить электрополирование при 7-8 значениях величины тока. Следить за тем, чтобы напряжение на электролизере не превышало 4 В, иначе в результате окисления воды на аноде будет выделяться кислород, который вместе с водородом, выделяющимся на катоде, может образовать гремучий газ. 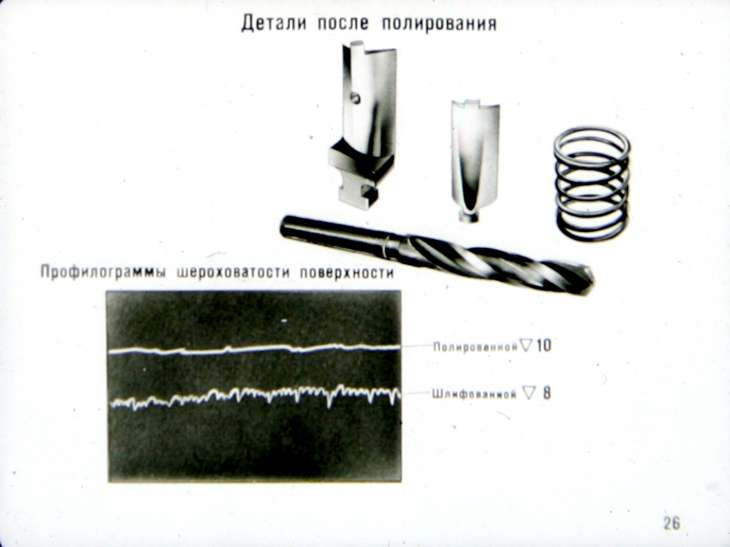 6.5. Установка для электрополирования
6.5. Установка для электрополирования Объясните «ход» вольт-амперной кривой.
Объясните «ход» вольт-амперной кривой. su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь — 161.97.168.212 (0.007 с.)
su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь — 161.97.168.212 (0.007 с.)