Как определить никель в домашних условиях: Как определить никель в домашних условиях
Содержание
описание и свойства металла, виды, сферы применения и месторождения
История
Название металла имеет немецкое происхождение. Так именуют в немецком фольклоре духа гор. Он подбрасывал старателям, разыскивающим медь, ее имитацию (никелин).
Nickel по-немецки – озорник.
Путь к признанию был извилистым:
- Промышленники обнаружили присутствие металла в «купферникеле» (по-немецки – «упрямая» медь) в 1751 году. Шведский металлург Август Кронштедт опознал соединение как никелево-мышьяковое.
- Никель классифицировали как «полуметалл».
- Спустя 24 года швед Томас Бергман доказал, что это просто металл.
- Немецкий химик Иоганн Рихтер получил чистый никель восстановлением никелевого купороса (1804 год), дал его научное описание.
Металл обрел международный статус.
Историческая хроника
Первые упоминания о никеле встречаются в исторических хрониках 1751 года. Обработчик металлов А. Ф. Кронштедт из Швеции обнаружил его наличие в некоторых химических веществах. Его исследования строились на анализе соединений с мышьяком. После открытия, его отнесли к веществам, которые лишь частично имеют свойства характерные для металлов. Долгое время шли дискуссии по поводу этого определения. В 1775 г. Соотечественник Кронштедта Т. Брегман окончательно доказал его принадлежность к простым веществам. Конец спорам положил химик из Германии И. Рихтер, которому в 1804 г. удалось выделить металл путем обработки его купороса.
Обработчик металлов А. Ф. Кронштедт из Швеции обнаружил его наличие в некоторых химических веществах. Его исследования строились на анализе соединений с мышьяком. После открытия, его отнесли к веществам, которые лишь частично имеют свойства характерные для металлов. Долгое время шли дискуссии по поводу этого определения. В 1775 г. Соотечественник Кронштедта Т. Брегман окончательно доказал его принадлежность к простым веществам. Конец спорам положил химик из Германии И. Рихтер, которому в 1804 г. удалось выделить металл путем обработки его купороса.
Физико-химические характеристики
Никель устойчив к окислению. Это свойство обеспечивает тонкая поверхностная пленка оксида NiO, появляющаяся при обычных температурах.
| Свойства атома | |
| Название, символ, номер | Ни́кель / Niccolum (Ni), 28 |
| Атомная масса (молярная масса) | 58,6934(4) а. е. м. (г/моль) |
| Электронная конфигурация | [Ar] 3d8 4s2 |
| Радиус атома | 124 пм |
| Химические свойства | |
| Ковалентный радиус | 115 пм |
| Радиус иона | (+2e) 69 пм |
| Электроотрицательность | 1,91 (шкала Полинга) |
| Электродный потенциал | -0,25 В |
| Степени окисления | 0, +2, +3 |
| Энергия ионизации (первый электрон) | 736,2 (7,63) кДж/моль (эВ) |
| Термодинамические свойства простого вещества | |
Плотность (при н. у.) у.) | 8,902 г/см³ |
| Температура плавления | 1726 K (1453 °C, 2647 °F) |
| Температура кипения | 3005 K (2732 °C, 4949 °F) |
| Уд. теплота плавления | 17,61 кДж/моль |
| Уд. теплота испарения | 378,6 кДж/моль |
| Молярная теплоёмкость | 26,1 Дж/(K·моль) |
| Молярный объём | 6,6 см³/моль |
| Кристаллическая решётка простого вещества | |
| Структура решётки | кубическая гранецентрированая |
| Параметры решётки | 3,524 Å |
| Температура Дебая | 375 K |
| Прочие характеристики | |
| Теплопроводность | (300 K) 90,9 Вт/(м·К) |
| Номер CAS | 7440-02-0 |
Центрированная по граням структура обуславливает стойкость к нагрузкам, а особенности строения электронных оболочек атомов – свойство намагничивания.
Месторождения
Никель не относится к редкоземельным металлам – на планете его достаточно (0,01% по массе). В земной коре обнаружен исключительно в связанном виде.
В земной коре обнаружен исключительно в связанном виде.
Предполагается, что из его сплава с железом состоит земное ядро.
Второй источник самородного металла – железные метеориты.
Крупными залежами располагают страны Тихоокеанского бассейна:
- Австралия;
- Индонезия;
- Новая Каледония;
- Филиппины.
Мировые запасы никелевых руд исчисляются миллионами тонн.
Российские месторождения сосредоточены на Урале, в Воронежской и Мурманской областях, возле Норильска.
Медно-никелевые руды залегают в зонах глубинных разломов на древних щитах. Их характерная особенность – постоянный минеральный состав руд, среди которых кобальт, платиноиды, золото.
Втрое богаче по запасам месторождения экзогенного типа.
Физические параметры
Никель — это серебристо-белый металл, не теряющий внешнего облика на воздухе. Он имеет гранецентрированную кубическую структуру. Пространственная группа имеет формулу Fm3m. В чистом виде этот материал отличается пластичностью и легко поддаётся переработке методом давления. У этого металла имеются следующие характеристики:
В чистом виде этот материал отличается пластичностью и легко поддаётся переработке методом давления. У этого металла имеются следующие характеристики:
- сопротивление 0,0684 мкОм∙м;
- линейное тепловое расширение =13,5∙10−6 K−1 при 0 C;
- объёмное тепловое расширение =38—39∙10−6 K−1;
- модуль упругости 196—210 ГПа.
Способы добычи и переработки
Почти весь никель получают из гарниерита (зеленой никелевой руды) и колчедана.
Добыча проходит стандартным для большинства руд закрытым (шахтным) способом.
Извлеченное сырье восстанавливают тремя методами:
- Взаимодействием с угольной пылью во вращающихся печах-трубах. Полученные железо-никелевые окатыши избавляют от серы, затем прокаливают, обрабатывают раствором аммиака. На подкисленный раствор воздействуют электролитом, получая металл.
- Из оксидной руды металл восстанавливают алюминотермическим способом.
- Карбонильный метод. Из руды получают медно-никелевый штейн, над которым под давлением запускают СО.
 Получается тетракарбонилникель. Это летучее соединение, поэтому разлагается от воздействия тепла. Металл получается особо чистым.
Получается тетракарбонилникель. Это летучее соединение, поэтому разлагается от воздействия тепла. Металл получается особо чистым.
Карбонильный способ фигурирует в литературе также как метод Монда.
Динамика курса
Выпуск никеля ежегодно составляет 4,4-4,8 млн. тонн. Согласно прогнозу экспертов, стоимость никелевой руды будет примерно 9000$ за 1 т., в течение 12 месяцев. В этом году избыток металла составит порядка 100 тыс. т. Цену на руду фиксирует биржа LME, где покупают фьючерс на сырье. В России подобного нет, поэтому подходящий способ инвестиций — покупка акций компании НорНикель (см. Куда инвестировать деньги?).
Классификация сплавов
Классификация никелевых сплавов основывается на составе и свойствах.
Кислотостойкие
Сплавы с присадкой-легированием другими металлами:
- Хром, вольфрам придают сплаву стойкости в агрессивных окислительных средах.
- Соединения с медью или молибденом используются в агрессивных неокислительных средах.

Стойкость к коррозии обеспечивают кремний, алюминий.
Жаропрочные
Сплавы типа «никель + хром + присадка других легирующих элементов». Такими элементами выступают алюминий, вольфрам, титан, молибден, стронций, другие.
Такие сплавы металлов востребованы для изготовления узлов силовых установок, подверженных максимальным нагрузкам.
Никелирование
Так называют нанесение покрытия на поверхность другого материала. Задача такого обеспечение защиты изделия от коррозии. Нанесение покрытия проводят в гальванической ванне. Для проведения качественной гальванической операции, применяют электролиты содержащие в своем составе соли натрия, бора, различные поверхностно – активные компоненты и глянцующие элементы. Толщина никелевого покрытия составляет до 36 мкм. Для повышения качества нанесенного покрытия допускается поверх никеля наносить слой хрома.
Существует способ нанесения никеля без применения электричества. То есть нанесение покрытия выполняют в смеси, включающей в себя соли никеля и натрия.
Сферы применения
О руде, по описанию похожей на медь, знали еще саксонские горняки в Средние века. Она использовалась как зеленый пигмент для окраски стекол.
С тех пор, благодаря изучению свойств и характеристик металла, область применения расширилась.
Никель – один из лучших металлов-катализаторов. Другие плюсы: малая активность, устойчивость к агрессивной химии, вязкость, пластичность, ковкость.
Его применяют самостоятельно и в сплавах.
Чистый никель
Беспримесный никель востребован промышленным производством:
- Покрытие, стойкое коррозии. Применяется для защиты железа, алюминия, магния, цинка, чугуна, нелегированных сталей. Попутно снижает стоимость изделий.
- Приборы, котлы, тигли с постоянными физико-химическими характеристиками, устойчивые к коррозии.
- Резервуары для перевозки и хранения химических реагентов (включая едкие щелочи), эфирных масел.
- Трубы для перекачки щелочей, других агрессивных субстанций на предприятиях химического комплекса.

- Инструментарий для науки, медицины.
- Детали приборов радиолокации, телевидения, дистанционного управления процессами на атомных станциях.
Порошкообразный никель используют как катализатор при производстве спиртов, ароматических углеводородов, других соединений. Это связка при изготовлении сверхтвердых материалов, засыпка для фильтрования газообразных химических продуктов.
Сплавы
Известно более трех тысяч композиций никеля с металлами:
- Самые распространенные – с железом, кобальтом, хромом, молибденом, алюминием, титаном, бериллием.
Все нержавеющие стали содержат никель, поскольку этот металл повышает химическую стойкость сплава.
- Медно-никелевое соединение монель (никеля – две трети): химия, электротехника, медицина. А также оснастка для океанских лайнеров, морских судов, портов, защитные кожухи атомных реакторов, газовые турбины, двигатели реактивных самолетов.
- Сплавы никеля вязкие, с малым коэффициентом термического расширения.
/s3/static.nrc.nl/bvhw/files/2017/01/data8325832-3c589e.jpg) Из них делают броню для нужд военно-промышленного комплекса.
Из них делают броню для нужд военно-промышленного комплекса. - Особая группа – сплавы на медной основе (нейзильбер, латунь, бронза, другие).
- Никелевые сплавы – основа современных монет (например, пятицентовика в США), обмотки струн музыкальных инструментов, брекетов.
Продукция металлургических предприятий поставляется в виде трубки, проволоки, нити, фольги, ленты, порошка, других конфигураций.
Продукция из никеля востребована там, где обязательна стойкость материалов к коррозии в агрессивных средах.
Предостережения
В составе никеля содержатся природные и искусственно созданные радиоактивные изотопы.
Это чревато проблемами со здоровьем, на бытовом уровне:
- Это аллерген, что учитывают, выбирая украшения, часы, другие изделия, контактирующие с кожей. Они могут спровоцировать контактный дерматит.
- Наличие никеля в организме человека снижает артериальное давление, провоцирует витилиго.
- Избыток металла в почве – причина болезней животных, растений.

- Особо опасны летучие соединения вещества.
Мелкодисперсный никелевый порошок самовоспламеняется при комнатной температуре.
Эти минусы не фатальны, но ими не стоит пренебрегать.
Никель в живых организмах
Если смотреть на мир снизу-вверх, то картина вырисовывается примерно такая. Под ногами у нас почва. Содержание никеля в ней больше чем в растительности. Но если рассмотреть эту растительность под той призмой, которая нас интересует, то большое содержание никеля находится в бобовых. А в злаковых культурах процент никеля возрастает.
Рассмотрим коротко среднее содержание никеля в растениях, морских и наземных животных. И конечно же, в человеке. Измерение идет в весовых процентах. Итак, масса никеля в растениях 5*10-5. Наземные животные 1*10-6, морские животные 1,6*10-4. И у человека содержание никеля 1-2*10-6.
Перспективы
Одна из главных сфер потребления никеля – щелочные батареи (аккумуляторы). Она актуализируется на волне интереса к выпуску электромобилей. Сегодня главный аккумуляторный компонент – кобальт, но он дорог, поставки из Африки проблемны. Разработаны более эффективные образцы с доминированием лития и никеля. Установлено, что благодаря никелю мощность аккумуляторов увеличивается. При этом его цена в шесть раз меньше кобальта, а предложение в 20 раз выше.
Сегодня главный аккумуляторный компонент – кобальт, но он дорог, поставки из Африки проблемны. Разработаны более эффективные образцы с доминированием лития и никеля. Установлено, что благодаря никелю мощность аккумуляторов увеличивается. При этом его цена в шесть раз меньше кобальта, а предложение в 20 раз выше.
Специалисты прогнозируют рост спроса на никель к 2025 году до 400 000 тонн (с 75 000 тонн в 2021 году).
Обработка
При использовании никеля выбирают способ нанесения защитного слоя. Для этого существует химическая и электролитическая технология.
Электролитическая
Покрытие наносится в ванне с заготовкой, электродом и электролитом. Ток подается из трансформатора или лабораторного источника. Покрытие получается однородным, наличие дефектов сводится к минимуму, поры отсутствуют. Нанесение выполняется следующим образом:
- Возьмите емкость, в которую без труда поместится деталь.
- Положите электрод и закрепите заготовку на кронштейне так, чтобы они не дотрагивались до стенок.

- Добавьте электролит.
- Найдите источник питания с мощностью до 6В и силой тока 1,2 А.
- Прикрепите к детали отрицательный заряд, а к аноду положительный.
- Включите источник питания. Помните, что в зависимости от времени подачи тока формируется разная толщина покрытия.
- Выключите ток, как только желаемый эффект получен.
- Отшлифуйте изделие, если в этом есть необходимость.
Химическая
Благодаря этому методу никелевый слой получается более прочным. Его проще реализовать дома, поскольку опыт или специальные навыки не требуются. У химической обработки есть свои недостатки: она не используется для деталей сложной формы или с шершавой поверхностью, а также неравномерно распределяется в труднодоступных местах.
Процесс нанесение слоя:
- Смешайте реактивы с водой в глубокой емкости. Важно, чтобы она не повредилась от используемых компонентов.
- Нагрейте раствор, а после закипания добавьте NaPO2h3.
- Возьмите металлическую емкость, покрытую эмалью, сделайте диэлектрический держатель.
 Конструкцию формируют так, чтобы деталь не касалась стенок.
Конструкцию формируют так, чтобы деталь не касалась стенок. - Добавьте электролит, а затем опустите на держателе деталь.
- Доведите смесь до закипания, а затем оставьте на 2–3 часа в растворе. Время регулируется в зависимости от желаемого эффекта.
- Вытащите деталь и промойте гашеной известью.
Помимо описанных способов существует черное никелирование. Его используют в декоративных или технических целях. Высокими защитными свойствами оно не обладает, но придает глубокий черный цвет из-за большого количества цинка.
Никель вокруг нас – Коммерсантъ Воронеж
О металле рассказывает Валентин Быстров, профессор, доктор технических наук, заслуженный деятель науки и техники РФ, который более 30 лет возглавлял кафедру цветных и благородных металлов Национального исследовательского технологического университета МИСИС
Серебристо-белый никель, который не тускнеет на воздухе и одарен многими полезными для человека свойствами, с самого своего рождения оказался пасынком в семье похожих по внешнему виду металлов.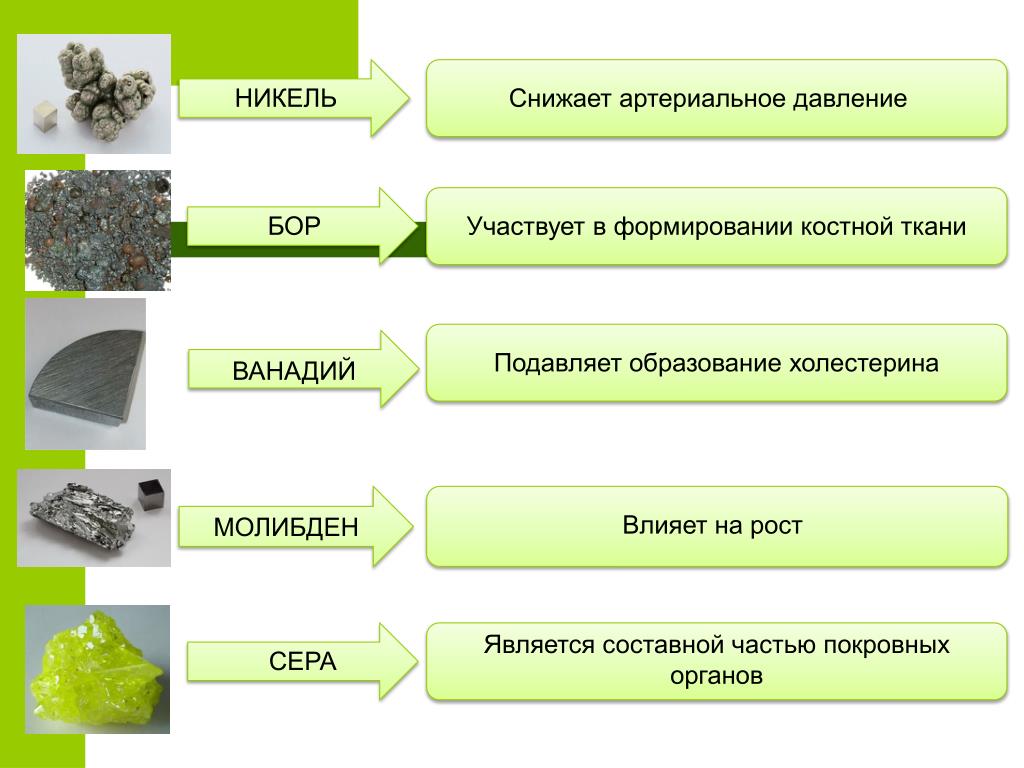 Серебро и платина получили статус драгоценных, стали любимцами королей, знати и монетных дворов. Дешевый и удивительно легкий алюминий обрел почетный статус «крылатого металла». Более юный палладий тоже причислен к драгметаллам. Его все более широко применяют в ювелирной промышленности, а в автоиндустрии его используют в качестве основного катализатора выхлопных газов. А вот на никель несправедливо клеветали задолго до его официального рождения в 1751 году. Тогда его исследовал и внес в галерею химических элементов шведский минералог Кронштедт. Он дал металлу имя злого духа гор немецкой мифологии – Nicolaus, или «хитрый бездельник».
Серебро и платина получили статус драгоценных, стали любимцами королей, знати и монетных дворов. Дешевый и удивительно легкий алюминий обрел почетный статус «крылатого металла». Более юный палладий тоже причислен к драгметаллам. Его все более широко применяют в ювелирной промышленности, а в автоиндустрии его используют в качестве основного катализатора выхлопных газов. А вот на никель несправедливо клеветали задолго до его официального рождения в 1751 году. Тогда его исследовал и внес в галерею химических элементов шведский минералог Кронштедт. Он дал металлу имя злого духа гор немецкой мифологии – Nicolaus, или «хитрый бездельник».
Синдром Франца-Иосифа
Впрочем, недоброе имя – еще не приговор. В XVIII веке никель оставался настолько экзотическим металлом, что ценился на вес золота. Антикоррозийные и антибактерицидные свойства никеля оказались замечены, люди зажиточные стали заказывать изделия из него для домашних нужд. В частности, для монархов, занимавших трон Австро-Венгерской империи, пищу готовили исключительно в никелированной посуде, на зависть многим другим королевским дворам Европы. Лишь к концу столетия удалось наладить достаточно широкое производство никеля, и он перестал считаться предметом роскоши. Однако когда император Франц-Иосиф неожиданно заболел, а придворные врачи не смогли установить, от чего именно, всю вину свалили на никель. Его буквально объявили вне закона: специальным указом официально запретили использовать этот металл для изготовления посуды. И лишь через двадцать лет после специальных исследований запрет оказался снят.
Лишь к концу столетия удалось наладить достаточно широкое производство никеля, и он перестал считаться предметом роскоши. Однако когда император Франц-Иосиф неожиданно заболел, а придворные врачи не смогли установить, от чего именно, всю вину свалили на никель. Его буквально объявили вне закона: специальным указом официально запретили использовать этот металл для изготовления посуды. И лишь через двадцать лет после специальных исследований запрет оказался снят.
Зловредный замысел придворной медицинской камарильи, пытавшейся оправдать свою профессиональную несостоятельность «кознями» никеля, ярче всего опровергла судьба самого Франца-Иосифа, ставшего старейшим правящим монархом Европы. Он занимал трон Австро-Венгрии 68 лет и скончался в 1916 году, в 86 лет, пережив всех горе-лекарей, заклеймивших никель. Итак, в качестве кухонного благодетеля никель полностью реабилитировали. В наших домах медно-никелевый сплав, дополнительно одеваемый в никелированную «рубашку», полновесно заменил столовое серебро. При этом никель не просто ярко блестит, похваливая добросовестность домохозяйки. Никелированная посуда отличается высокой стойкостью к коррозии и отличными бактерицидными свойствами, щадит витамины и другие полезные вещества.
При этом никель не просто ярко блестит, похваливая добросовестность домохозяйки. Никелированная посуда отличается высокой стойкостью к коррозии и отличными бактерицидными свойствами, щадит витамины и другие полезные вещества.
Известна характеристика популярной посуды немецкой фирмы Zepter: «Наборы кухонной посуды “Цептер” сделаны из высококачественной нержавеющей стали с использованием новейших технологий. Кастрюли и скороварки этого бренда имеют термоаккумулирующее дно, позволяющее равномерно распределять тепло, а также встроенный термоэлемент, контролирующий температурный режим при приготовлении пищи. “Цептер”-посуда позволяет готовить еду без дополнительного использования воды, соли и жиров. В итоге питательная ценность еды возрастает, а продукты сохраняют витамины, минеральные вещества, природный вкус и аромат». Возразить тут нечего. А вот добавить нужно: формула цептеровской нержавейки – 18 частей хрома на 10 частей никеля.
Двойной стандарт
Диетологи пишут трактаты о важной роли в пищевых продуктах кальция, магния, калия, железа и других микроэлементов. Никель практически игнорируют. Между тем биологическая роль никеля архиважная: он активно участвует в структурной организации и функционировании основных клеточных компонентов – ДНК, РНК и белка. Кроме того, занимается гормональной регулировкой организма.
Никель практически игнорируют. Между тем биологическая роль никеля архиважная: он активно участвует в структурной организации и функционировании основных клеточных компонентов – ДНК, РНК и белка. Кроме того, занимается гормональной регулировкой организма.
По кроветворной роли никель сродни кобальту: он является мощным стимулятором образования эритроцитов в кроветворной ткани костного мозга, синтеза гемоглобина, повышает усвоение организмом железа. В сочетании с кобальтом, железом, медью участвует в других процессах кроветворения, а самостоятельно — в обмене жиров и обеспечении клеток кислородом. Так называемый дивалентный никель занимается внутриклеточным транспортом и связями. Кроме того, никель служит важным структурным компонентом некоторых ферментов.
Ежедневное потребление никеля должно составлять 100–300 мкг. Никелем богаты такие продукты, как какао, шоколад, орехи, высушенные бобы, горох, зерно, семечки и яйца. Немало его также в гречихе, моркови и листовом салате, луке и укропе, в смородине, вишне и грибах, Но тут следует учитывать, что в желудочно-кишечном тракте человека успешно всасывается только от 1 до 10% никеля, поступившего с пищей. С водой никель усваивается лучше – на 20–25%. Однако целый ряд продуктов сильно снижает абсорбцию никеля: молоко, кофе, чай, апельсиновый сок, а также все, что богато аскорбиновой кислотой. Поскольку именно они наиболее частые гости на обеденном столе, переизбыток никеля нам явно не грозит. Природа, впрочем, мудра и устроила так, что при дефиците железа, беременности и кормлении грудью человеческий организм начинает усваивать никель гораздо лучше.
С водой никель усваивается лучше – на 20–25%. Однако целый ряд продуктов сильно снижает абсорбцию никеля: молоко, кофе, чай, апельсиновый сок, а также все, что богато аскорбиновой кислотой. Поскольку именно они наиболее частые гости на обеденном столе, переизбыток никеля нам явно не грозит. Природа, впрочем, мудра и устроила так, что при дефиците железа, беременности и кормлении грудью человеческий организм начинает усваивать никель гораздо лучше.
В медицине никелевые сплавы наиболее широко применяются при изготовлении имплантатов. И в этой сфере, где никель столько доброго сделал человеку, его сейчас пытаются ошельмовать. Особенно жаркая полемика идет вокруг металлокерамических зубных протезов. Те, кто ведет на них атаку – а это главным образом стоматологические ассоциации ряда западноевропейских стран — Германии, Голландии, Швейцарии, Швеции и Норвегии, — утверждают, что никель, составляющий металлическую основу коронок, опасен для здоровья и жизни. В прессе по этому поводу уже высказался заведующий кафедрой госпитальной ортопедической стоматологии Московского государственного медико-стоматологического института, доктор медицинских наук, профессор Игорь Лебеденко: «…Мы живем в век нечистоплотной информации. Свою кандидатскую диссертацию, множество научных работ и изобретений в области материаловедения я посвятил именно стоматологическим сплавам… И могу со всей ответственностью сказать, что металлокерамические зубные протезы, изготовленные без нарушения технологий, из разрешенных к применению Минздравом России стоматологических материалов абсолютно безвредны для организма. Единственное “но” — индивидуальная непереносимость. Ведь и на золотые изделия бывает аллергия. Металлы, входящие в состав стоматологических сплавов, — нормальные компоненты нашего организма. А потому, в отличие от синтетических материалов, не могут вызвать непредсказуемую реакцию. Человеческий организм содержит массу ферментов, и внутри почти каждого — металлы, в том числе хром, кобальт и никель. Говорить о том, что они опасны, просто некорректно.
Свою кандидатскую диссертацию, множество научных работ и изобретений в области материаловедения я посвятил именно стоматологическим сплавам… И могу со всей ответственностью сказать, что металлокерамические зубные протезы, изготовленные без нарушения технологий, из разрешенных к применению Минздравом России стоматологических материалов абсолютно безвредны для организма. Единственное “но” — индивидуальная непереносимость. Ведь и на золотые изделия бывает аллергия. Металлы, входящие в состав стоматологических сплавов, — нормальные компоненты нашего организма. А потому, в отличие от синтетических материалов, не могут вызвать непредсказуемую реакцию. Человеческий организм содержит массу ферментов, и внутри почти каждого — металлы, в том числе хром, кобальт и никель. Говорить о том, что они опасны, просто некорректно.
…В тот момент, когда я писал кандидатскую диссертацию по никель-хромовым сплавам, вышел переводной труд, в котором говорилось, что никель вызывает рак. Это “открытие” должно было перечеркнуть всю мою научную работу. Тогда я нашел первоисточник, он назывался: «Никель вызывает рак?» Именно так, с вопросительным знаком. В нем речь шла о том, что нет ни одного документально подтвержденного случая, когда никелевые сплавы, используемые для зубных протезов, у кого-либо вызвали бы перерождение. В 100% случаев, где были никелевые сплавы, никакой вредной реакции, которая отличалась бы от реакции на имплантацию известных сплавов, не содержащих никель, я не обнаружил. Клинически для людей, у которых нет аллергических реакций, сплавы с никелем хороши и доступны по цене. В США они были базовыми для протезирования военнослужащих. Это серьезный аргумент в их пользу: в высокоразвитых странах армия и дети — святое, и для них наверняка не будут использовать вредные компоненты».
Тогда я нашел первоисточник, он назывался: «Никель вызывает рак?» Именно так, с вопросительным знаком. В нем речь шла о том, что нет ни одного документально подтвержденного случая, когда никелевые сплавы, используемые для зубных протезов, у кого-либо вызвали бы перерождение. В 100% случаев, где были никелевые сплавы, никакой вредной реакции, которая отличалась бы от реакции на имплантацию известных сплавов, не содержащих никель, я не обнаружил. Клинически для людей, у которых нет аллергических реакций, сплавы с никелем хороши и доступны по цене. В США они были базовыми для протезирования военнослужащих. Это серьезный аргумент в их пользу: в высокоразвитых странах армия и дети — святое, и для них наверняка не будут использовать вредные компоненты».
А вот результаты тестирования дентальных имплантатов, которое провели врач-стоматолог высшей категории, главврач московского инновационного стоматологического центра «НАНО-ДЕНТ» Р.Гизатуллин и врач-стоматолог высшей категории, заслуженный изобретатель РФ Л. Гурфинкель. Цитируем: «Интерметаллиды никеля, включая популярный в стоматологии никелид титана, устойчивы к коррозии, жаропрочны и окалиностойки. Материалы на их основе не проявляют никаких канцерогенных действий».
Гурфинкель. Цитируем: «Интерметаллиды никеля, включая популярный в стоматологии никелид титана, устойчивы к коррозии, жаропрочны и окалиностойки. Материалы на их основе не проявляют никаких канцерогенных действий».
Резюме из всего вышесказанного простое: хороший зубной протез по доступным ценам – металлокерамический, в том числе – содержащий никелевые сплавы. А западноевропейские стоматологи сейчас усиленно внедряют целый ряд новых, более дорогостоящих материалов. Идет ожесточенная конкурентная борьба, в которой все средства хороши. В том числе – двойные стандарты. Профессор Лебеденко не без иронии отмечает: «Сейчас, например, в России, как и во всем мире, сплавы из бериллия запрещены для применения в медпрактике. Хотя некоторые фирмы втихую ввозят их из-за рубежа, в том числе из Швейцарии, больше всех кричащей о вреде бериллия. Почему они до сих пор выпускаются? Да потому, что бериллий опасен лишь при литье. Если он переплавляется неправильно, без соблюдения правил техники безопасности, то бериллиевая пыль, попадая при дыхании в организм, может вызвать нежелательные реакции. В остальном сплавы с бериллием, например “Ультратек”, замечательные. Бериллий улучшает литейные свойства сплава, его беленькая оксидная пленка идеально подходит для облицовочных процессов, керамика на нее прекрасно “ложится”. В 1970-е годы в клиниках Четвертого управления сильным мира сего делали не только коронки из содержащего золото сплава “Дегудент”, но и из “Ультратека”, в основе которого никель и бериллий. Главное, чтобы в соответствии с решением, принятым Европейским комитетом по нормам, максимально допустимая доля бериллия в зуботехнических сплавах не превышала 0,02%».
В остальном сплавы с бериллием, например “Ультратек”, замечательные. Бериллий улучшает литейные свойства сплава, его беленькая оксидная пленка идеально подходит для облицовочных процессов, керамика на нее прекрасно “ложится”. В 1970-е годы в клиниках Четвертого управления сильным мира сего делали не только коронки из содержащего золото сплава “Дегудент”, но и из “Ультратека”, в основе которого никель и бериллий. Главное, чтобы в соответствии с решением, принятым Европейским комитетом по нормам, максимально допустимая доля бериллия в зуботехнических сплавах не превышала 0,02%».
Тысячи профессий
Никелевые сплавы, число которых перевалило уже на четвертую тысячу, окружают нас со всех сторон. Так, во многих бытовых нагревательных приборах установлены нихромовые спирали. Платинит заменяет дорогостоящую платину, когда нужно впаять металл в стекло, например, в шприцах и электролампах. Упругий элинвар — отличный материал для пружин, особенно часовых. Пермаллой находит все более широкое применение в телефонии и радиотехнике.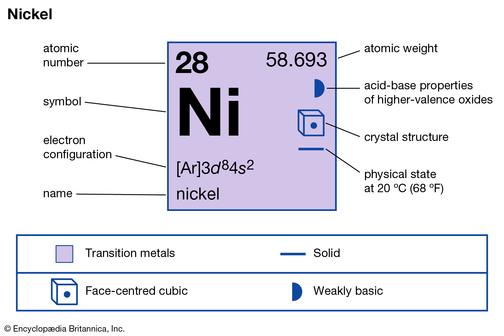 Обладающий «памятью» и поэтому не поддающийся деформации нитинол упорно возвращается к прежней форме – он полюбился изготовителям современных, особо прочных оправ для очков. Из никелевых сплавов делают швейные иголки, заклепки для джинсов и модной одежды. Различные никелевые соединения нашли активное применение в косметике и бытовой химии. А никель-кадмиевые аккумуляторы и батарейки мы вообще используем буквально на каждом шагу.
Обладающий «памятью» и поэтому не поддающийся деформации нитинол упорно возвращается к прежней форме – он полюбился изготовителям современных, особо прочных оправ для очков. Из никелевых сплавов делают швейные иголки, заклепки для джинсов и модной одежды. Различные никелевые соединения нашли активное применение в косметике и бытовой химии. А никель-кадмиевые аккумуляторы и батарейки мы вообще используем буквально на каждом шагу.
Медно-никелевые сплавы широко задействованы многими странами в чеканке монет, и современные российские не исключение. Любопытно, что именно в этом качестве никель служил людям задолго до своего официального открытия. Древние китайцы еще во II веке до н.э. начали выплавлять сплав никеля с медью и цинком – пакфонг. С легкой руки китайцев он стал пользоваться спросом и в других странax, включая Бактрию — государство, расположенное на месте современных постсоветских среднеазиатских республик. Именно бактрийцам, судя по всему, принадлежит приоритет в чеканке монет из медно-никелевых сплавов, а именно из китайского памфонга. Сейчас, конечно же, такие монеты – нумизматическая редкость. Одна из них, выпущенная в 235 году до н.э., хранится в Британском музее в Лондоне.
Сейчас, конечно же, такие монеты – нумизматическая редкость. Одна из них, выпущенная в 235 году до н.э., хранится в Британском музее в Лондоне.
Известны случаи аллергических реакций в виде кожной сыпи при частом контакте с монетами, содержащими никель. Но их не так уж много, никакого сравнения с арахисовым маслом или цветочной пыльцой. А вот если никеля в кожных покровах не хватает – дерматит практически гарантирован. Примечательно, что многие страны Евросоюза, всячески призывающего ограничить содержание никеля в продукции, контактирующей с кожей человека, невозмутимо продолжают чеканить монеты в 1 евро и других достоинств именно из медно-никелевых сплавов.
Напомним также, что в США монетка в 5 центов носит обиходное название «никель». Пятицентовики из медно-никелевого сплава с изображением одного из авторов Декларации независимости (1776 г.) и третьего президента США Томаса Джефферсона выпускают с 1938 г. многомиллионными тиражами. А вот счет даймам (десятицентовым монетам) и квотерам (25-центовым) ежегодно идет на миллиарды. Обе эти монеты с 1965 г. тоже делают из медно-никелевого сплава.
Обе эти монеты с 1965 г. тоже делают из медно-никелевого сплава.
Нас не обманешь
Обратите внимание: на никель, как правило, клевещут недобросовестные «специалисты». Но наш народ не обманешь, ему этот металл, оклеветанный саксонцами, австрийскими айболитами и некоторыми алчными дантистами, пришелся по душе. По народной традиции, через 12 лет семейной жизни супружеская пара отмечает особый юбилей — никелевую свадьбу. Поскольку это стойкий к внешним воздействиям металл, он подтверждает, что любовь супругов выдержала испытания, что их единство не удалось разрушить никаким невзгодам. Вместе с тем никелевая свадьба служит им напоминание о том, что отношения следует и впредь поддерживать в блестящей форме. На никелевую свадьбу лучшие подарки – кастрюли, кофейники, самовары из нержавеющей хромоникелевой стали, столовые приборы из сплавов никеля и серебра, мельхиора.
с медью, алюминием, титаном, хромом
Никель – серебристо-серый, пластичный, ковкий металл. Относится к переходным металлам, то есть, может проявлять и кислотные, и щелочные свойства. В нормальных условиях никель покрывается оксидной пленкой, а потому и малоактивен. Отличие от других схожих элементов состоит в том, что его оксидная пленка не уменьшает блеск. И сегодня мы расскажем вам об использовании никеля в промышленности, применении его сплавов в строительстве и иных сферах жизни.
Относится к переходным металлам, то есть, может проявлять и кислотные, и щелочные свойства. В нормальных условиях никель покрывается оксидной пленкой, а потому и малоактивен. Отличие от других схожих элементов состоит в том, что его оксидная пленка не уменьшает блеск. И сегодня мы расскажем вам об использовании никеля в промышленности, применении его сплавов в строительстве и иных сферах жизни.
СТРУКТУРА
Имеет гранецентрированную кубическую решетку с периодом a = 0,35238 å нм, пространственная группа Fm3m. Эта кристаллическая структура устойчива к давлению, по меньшей мере 70 ГПа. При обычных условиях никель существует в виде b-модификации, имеющей гранецентрированную кубическую решётку ( a = 3,5236 å). Но никель, подвергнутый катодному распылению в атмосфере h 2 , образует a-модификацию, имеющую гексагональную решётку плотнейшей упаковки ( а = 2,65 å, с = 4,32 å), которая при нагревании выше 200 °С переходит в кубическую. Компактный кубический никель имеет плотность 8,9 г/см3 (20 °С), атомный радиус 1,24 å
Биологическая роль [ править | править код ]
Никель относится к числу микроэлементов, необходимых для нормального развития живых организмов. Однако о его роли в живых организмах известно немного. Известно, что никель принимает участие в ферментативных реакциях у животных и растений. В организме животных он накапливается в ороговевших тканях, особенно в перьях. Повышенное содержание никеля в почвах приводят к эндемическим заболеваниям — у растений появляются уродливые формы, у животных — заболевания глаз, связанные с накоплением никеля в роговице. Токсическая доза (для крыс) — 50 мг. Особенно вредны летучие соединения никеля, в частности, его тетракарбонил Ni(CO)4. ПДК соединений никеля в воздухе составляет от 0,0002 до 0,001 мг/м 3 (для различных соединений).
Однако о его роли в живых организмах известно немного. Известно, что никель принимает участие в ферментативных реакциях у животных и растений. В организме животных он накапливается в ороговевших тканях, особенно в перьях. Повышенное содержание никеля в почвах приводят к эндемическим заболеваниям — у растений появляются уродливые формы, у животных — заболевания глаз, связанные с накоплением никеля в роговице. Токсическая доза (для крыс) — 50 мг. Особенно вредны летучие соединения никеля, в частности, его тетракарбонил Ni(CO)4. ПДК соединений никеля в воздухе составляет от 0,0002 до 0,001 мг/м 3 (для различных соединений).
СВОЙСТВА
Никель — ковкий и тягучий металл, из него можно изготовлять тончайшие листы и трубки. Предел прочности при растяжении 400—500 Мн/м2, предел упругости 80 Мн/м2 , предел текучести 120 Мн/м2; относительное удлинение 40%; модуль нормальной упругости 205 Гн/м2; твёрдость по Бринеллю 600—800 Мн/м2. В температурном интервале от 0 до 631К (верхняя граница соответствует Кюри точке ). Ферромагнетизм никеля обусловлен особенностями строения внешних электронных оболочек его атомов. Никель входит в состав важнейших магнитных материалов и сплавов с минимальным значением коэффициента теплового расширения (пермаллой, монель-металл, инвар и др.).
Ферромагнетизм никеля обусловлен особенностями строения внешних электронных оболочек его атомов. Никель входит в состав важнейших магнитных материалов и сплавов с минимальным значением коэффициента теплового расширения (пермаллой, монель-металл, инвар и др.).
Немного истории
За много лет до этого чудесного открытия горняки из Саксонии были знакомы с рудой, которую можно было принять за медную руду. Попытки извлечь из этого материала медь были тщетными. Почувствовав себя обманутыми, руду стали называть «купферникель» (по-русски — «медный дьявол»).
Этой рудой заинтересовался эксперт по минералам Крондстедт. После долгих трудов получился новый металл, который и назвали никелем. Эстафету по исследованию перехватил Бергман. Он еще больше очистил металл и пришел к заключению, что данный элемент напоминает железо.
ЗАПАСЫ И ДОБЫЧА
Никель довольно распространён в природе — его содержание в земной коре составляет около 0,01%(масс.). В земной коре встречается только в связанном виде, в железных метеоритах содержится самородный никель (до 8%). Содержание его в ультраосновных породах примерно в 200 раз выше, чем в кислых (1,2кг/т и 8г/т). В ультраосновных породах преобладающее количество никеля связано с оливинами, содержащими 0,13 — 0,41% Ni. В растениях в среднем 5·10−5 весовых процентов никеля, в морских животных — 1,6·10−4, в наземных — 1·10−6, в человеческом организме — 1…2·10−6.
Содержание его в ультраосновных породах примерно в 200 раз выше, чем в кислых (1,2кг/т и 8г/т). В ультраосновных породах преобладающее количество никеля связано с оливинами, содержащими 0,13 — 0,41% Ni. В растениях в среднем 5·10−5 весовых процентов никеля, в морских животных — 1,6·10−4, в наземных — 1·10−6, в человеческом организме — 1…2·10−6.
Основную массу никеля получают из гарниерита и магнитного колчедана. Силикатную руду восстанавливают угольной пылью во вращающихся трубчатых печах до железо-никелевых окатышей (5—8% Ni), которые затем очищают от серы, прокаливают и обрабатывают раствором аммиака. После подкисления раствора из него электролитически получают металл. Карбонильный способ (метод Монда): Вначале из сульфидной руды получают медно-никелевый штейн, над которым пропускают СО под высоким давлением. Образуется легколетучий тетракарбонилникель [Ni(CO)4], термическим разложением которого выделяют особо чистый металл. Алюминотермический способ восстановления никеля из оксидной руды: 3NiO + 2Al = 3Ni +Al2O3
Электролитическое никелирование
Суть технологии электролитического никелирования металлических деталей, имеющей и другое название – «гальваническое никелирование», можно рассмотреть на примере того, как выполняется омеднение поверхности изделия из металла. Такую процедуру можно проводить как с применением электролитического раствора, так и без него.
Такую процедуру можно проводить как с применением электролитического раствора, так и без него.
Деталь, которая будет в дальнейшем обрабатываться в электролитическом растворе, подвергается тщательной обработке, для чего с ее поверхности при помощи наждачной бумаги удаляют оксидную пленку. Затем обрабатываемое изделие промывается в теплой воде и обрабатывается содовым раствором, после чего снова промывается водой.
Крупные детали лучше очищать пескоструйным аппаратом
Сам процесс никелирования выполняется в стеклянной емкости, в которую заливается водный раствор (электролит). В составе такого раствора содержится 20% медного купороса и 2% серной кислоты. Обрабатываемую деталь, на поверхность которой необходимо нанести тонкий слой меди, в растворе электролита помещают между двумя анодами из меди. Чтобы запустить процесс омеднения, на медные аноды и обрабатываемую деталь необходимо подать электрический ток, величину которого рассчитывают, исходя из показателя 10–15 мА на один квадратный сантиметр площади детали. Тонкий слой меди на поверхности изделия появляется уже через полчаса его нахождения в растворе электролита, причем такой слой будет тем толще, чем дольше будет протекать процесс.
Тонкий слой меди на поверхности изделия появляется уже через полчаса его нахождения в растворе электролита, причем такой слой будет тем толще, чем дольше будет протекать процесс.
Схема установки для электролитического никелирования
Нанести медный слой на поверхность изделия можно и по другой технологии. Для этого необходимо изготовить кисточку из меди (можно использовать многожильный провод, предварительно сняв с него изоляционный слой). Такую кисточку, сделанную своими руками, надо зафиксировать на деревянной палочке, которая будет служить ручкой.
Изделие, поверхность которого предварительно зачищают и обезжиривают, помещают в емкость из диэлектрического материала и заливают электролитом, в качестве которого можно использовать насыщенный водный раствор медного купороса. Самодельную кисточку подключают к плюсовому контакту источника электрического тока, а обрабатываемую деталь – к его минусу. После этого приступают к процедуре омеднения. Заключается она в том, что кисточкой, которую предварительно обмакивают в электролит, проводят над поверхностью изделия, не прикасаясь к ней. Наносить покрытие, применяя такую методику, можно в несколько слоев, что позволит сформировать на поверхности изделия слой меди, на котором практически отсутствуют поры.
Наносить покрытие, применяя такую методику, можно в несколько слоев, что позволит сформировать на поверхности изделия слой меди, на котором практически отсутствуют поры.
Схема простого приспособления для нанесения покрытия
Электролитическое никелирование выполняется по схожей технологии: при его осуществлении тоже используется раствор электролита. Так же, как и в случае с омеднением, обрабатываемое изделие располагают между двумя анодами, только в данном случае они изготовлены из никеля. Аноды, помещенные в раствор для никелирования, подключаются к плюсовому контакту источника тока, а изделие, подвешенное между ними на металлической проволоке, – к минусовому.
Для осуществления никелирования, в том числе и выполняемого своими руками, используются электролитические растворы двух основных типов:
- водный раствор, включающий в свой состав сернокислый никель, натрий и магний (14:5:3), 2% борной кислоты, 0,5% поваренной соли;
- раствор на основе нейтральной воды, содержащий в своем составе 30% сульфата никеля, 4% хлорида никеля, 3% борной кислоты.

Электролит блестящего никелирования с добавкой органических блескообразователей (натриевых солей)
Выравнивающий электролит блестящего никелирования. Подходит для поверхностей с низким классом очистки
Чтобы приготовить электролитический раствор, сухую смесь из вышеуказанных элементов заливают одним литром нейтральной воды и тщательно перемешивают. Если в полученном растворе образовался осадок, от него избавляются. Только после этого раствор можно использовать для выполнения никелирования.
Обработка по данной технологии обычно длится полчаса, при этом используют источник тока с напряжением 5,8–6 В. Результатом является поверхность, покрытая неравномерным матовым цветом серого цвета. Чтобы она стала красивой и блестящей, необходимо ее зачистить и выполнить ее полировку. Следует иметь в виду, что такая технология не может быть использована для деталей, отличающихся высокой шероховатостью поверхности или имеющих узкие и глубокие отверстия. В таких случаях покрытие поверхности металлического изделия слоем никеля следует выполнять по химической технологии, которую также называют чернением.
Электролит для осаждения черного никеля
Суть технологической операции чернения заключается в том, что на поверхность изделия сначала наносится промежуточное покрытие, основой которого может быть цинк или никель, а на верхней части такого покрытия формируется слой черного никеля толщиной не более 2 мкм. Покрытие никелем, выполненное по технологии чернения, смотрится очень красиво и обеспечивает надежную защиту металла от негативного воздействия различных факторов внешней среды.
В отдельных случаях металлическое изделие одновременно подвергают сразу двум технологическим операциям, таким как никелирование и хромирование.
ПРОИСХОЖДЕНИЕ
Месторождения сульфидных медно-никелевых руд связаны с лополитоподобными или плитообразными массивами расслоенных габброидов, приуроченных к зонам глубинных разломов на древних щитах и платформах. Характерной особенностью медно-никелевых месторождений всего мира является выдержанный минеральный состав руд: пирротин, пентландит, халькопирит, магнетит; кроме них в рудах встречаются пирит, кубанит, полидимит, никелин, миллерит, виоларит, минералы группы платины, изредка хромит, арсениды никеля и кобальта, галенит, сфалерит, борнит, макинавит, валлерит, графит, самородное золото.
Экзогенные месторождения силикатных никелевых руд повсеместно связаны с тем или иным типом коры выветривания серпентенитов. при выветривании происходит стадийное разложение минералов, а также перенос подвижных элементов, с помощью воды из верхних частей коры в нижние. Там эти элементы выпадают в осадок в виде вторичных минералов. В месторождениях этого типа заключены запасы никеля в 3 раза превышающие его запасы в сульфидных рудах, а запасы некоторых месторождений достигают 1 млн т. и более никеля. Крупные запасы силикатных руд сосредоточены на Новой Каледонии, Филиппинах, Индонезии, Австралии и др. странах. Среднее содержание в них никеля равно 1.1-2%. Кроме того в рудах часто содержится кобальт.
Химическое никелирование
Процедуру химического никелирования изделий из металла выполняют по следующей схеме: обрабатываемую деталь на некоторое время погружают в кипящий раствор, в результате чего на ее поверхности оседают частички никеля. При применении такой технологии электрохимическое воздействие на металл, из которого изготовлена деталь, отсутствует.
Результатом использования такой технологии никелирования является формирование на поверхности обрабатываемой детали никелевого слоя, который прочно связан с основным металлом. Наибольшей эффективности такой способ никелирования позволяет добиться в тех случаях, когда с его помощью обрабатываются предметы, изготовленные из стальных сплавов.
Комплект для нанесения никелированного покрытия химическим способом
Выполнять такое никелирование в домашних условиях или даже в условиях гаража нетрудно. При этом процедура никелирования проходит в несколько этапов.
- Сухие реактивы, из которых будет приготовлен электролитический раствор, смешиваются с водой в эмалированной посуде.
- Полученный раствор доводят до кипения, а затем в него добавляют гипофосфит натрия.
- Изделие, которое необходимо подвергнуть обработке, помещают в электролитический раствор, причем делают это так, чтобы оно не касалось боковых стенок и дна емкости. Фактически надо изготовить бытовой аппарат для никелирования, конструкция которого будет состоять из эмалированной емкости соответствующего объема, а также диэлектрического кронштейна, на котором будет фиксироваться обрабатываемая деталь.

- Продолжительность кипения электролитического раствора в зависимости от его химического состава может составлять от одного часа до трех.
- После завершения технологической операции уже никелированная деталь извлекается из раствора. Затем ее промывают в воде, в составе которой содержится гашеная известь. После тщательной промывки поверхность изделия подвергается полированию.
Читать также: Звонок беспроводной уличный влагозащищенный с двумя динамиками
Процесс никелировки в домашних условиях
Электролитические растворы для выполнения никелирования, которому можно подвергать не только сталь, но также латунь, алюминий и другие металлы, обязательно содержат в своем химическом составе следующие элементы – хлористый или сернокислый никель, гипофосфит натрия различной кислотности, какую-либо из кислот.
Чтобы увеличить скорость никелирования изделий из металла, в состав для выполнения этой технологической операции добавляют свинец. Как правило, в одном литре электролитического раствора выполняют никелевое покрытие поверхности, площадь которой составляет 20 см 2 . В электролитических растворах с более высокой кислотностью проводят никелирование изделий из черных металлов, а в щелочных обрабатывают латунь, осуществляют никелирование алюминия или деталей из нержавеющей стали.
В электролитических растворах с более высокой кислотностью проводят никелирование изделий из черных металлов, а в щелочных обрабатывают латунь, осуществляют никелирование алюминия или деталей из нержавеющей стали.
ПРИМЕНЕНИЕ
Подавляющая часть никеля используется для получения сплавов с другими металлами (fe, cr, cu и др.), отличающихся высокими механическими, антикоррозионными, магнитными или электрическими и термоэлектрическими свойствами. В связи с развитием реактивной техники и созданием газотурбинных установок особенно важны жаропрочные и жаростойкие хромоникелевые сплавы. Сплавы никеля используются в конструкциях атомных реакторов.
Значительное количество никеля расходуется для производства щелочных аккумуляторов и антикоррозионных покрытий. Ковкий никель в чистом виде применяют для изготовления листов, труб и т.д. Он используется также в химической промышленности для изготовления специальной химической аппаратуры и как катализатор многих химических процессов. Никель — весьма дефицитный металл и по возможности должен заменяться другими, более дешёвыми и распространёнными материалами.
Никель — весьма дефицитный металл и по возможности должен заменяться другими, более дешёвыми и распространёнными материалами.
Применяется при изготовлении брекет-систем (никелид титана), протезирования. Широко применяется при производстве монет во многих странах. В США монета достоинством в 5 центов носит разговорное название «никель». Также никель используется для производства обмотки струн музыкальных инструментов.
Никель (англ. Nickel) — Ni
| Молекулярный вес | 58.69 г/моль |
| Происхождение названия | Из немецкого Nickel, означает демон, как сокращенная форма Kupfernickel, медь дьявола |
| IMA статус | утвержден |
Параметры никеля
Никель — это металл со свойственным ему серебристо-белым цветом. При температуре 1453 °C переходит в жидкое состояние, а кипит при 2732 °C. Никель пластичен, легко поддается обработке под воздействием давления.
Химическое свойство никеля характеризуется способностью образовывать соединения с разной степенью окисления. В естественных условиях на поверхности металла возникает тонкая пленка из оксида.
В естественных условиях на поверхности металла возникает тонкая пленка из оксида.
Металл обладает высоким показателем устойчивости к коррозии. Никель не реагирует с рядом концентрированных кислот и щелочей, но активно растворяется в разбавленной азотной кислоте.
Вступая в химические реакции, никель образует летучие металлы и растворимые/нерастворимые соли
С никелем не вступают в реакцию:
- инертные газы;
- литий;
- калий;
- натрий;
- цезий;
- рубидий;
- стронций;
- барий;
- иридий;
- цезий.
С углеродным соединением никель образует карбонил — летучий переходный металл, используемый в процессе получения материалов высокого класса чистоты. Порошок никеля способен самовоспламеняться при соприкосновении с воздухом с образованием оксидов.
Никель продуцирует ряд растворимых и нерастворимых солей. Например, раствор сульфата металла придает жидкости зеленую окраску. Нерастворимые соли обычно имеют насыщенный желтый цвет.
ФИЗИЧЕСКИЕ СВОЙСТВА
| Цвет минерала | белый, светло-серебрянный |
| Цвет черты | серо белый |
| Прозрачность | непрозрачный |
| Блеск | металлический |
| Спайность | нет |
| Твердость (шкала Мооса) | 3,5 |
| Прочность | ковкий |
| Излом | зазубренный |
| Плотность (измеренная) | 7.8 — 8.2 г/см3 |
| Радиоактивность (GRapi) | 0 |
| Магнетизм | ферромагнетик |
Физиологическое действие [ править | править код ]
Никель и его соединения токсичны и канцерогенны.
Никель — основная причина аллергии (контактного дерматита) на металлы, контактирующие с кожей (украшения, часы, джинсовые заклепки). В 2008 году Американским обществом контактного дерматита никель был признан «Аллергеном года» [18] . В Европейском союзе ограничено содержание никеля в продукции, контактирующей с кожей человека [19] .
В XX веке было установлено, что поджелудочная железа очень богата никелем. При введении вслед за инсулином никеля продлевается действие инсулина и тем самым повышается гипогликемическая активность. Никель оказывает влияние на ферментативные процессы, окисление аскорбиновой кислоты, ускоряет переход сульфгидрильных групп в дисульфидные. Никель может угнетать действие адреналина и снижать артериальное давление. Избыточное поступление никеля в организм вызывает витилиго. Депонируется никель в поджелудочной и околощитовидной железах.
Никель – серебристо-серый, пластичный, ковкий металл. Относится к переходным металлам, то есть, может проявлять и кислотные, и щелочные свойства. В нормальных условиях никель покрывается оксидной пленкой, а потому и малоактивен. Отличие от других схожих элементов состоит в том, что его оксидная пленка не уменьшает блеск. И сегодня мы расскажем вам об использовании никеля в промышленности, применении его сплавов в строительстве и иных сферах жизни.
Динамика курса
Выпуск никеля ежегодно составляет 4,4-4,8 млн. тонн. Согласно прогнозу экспертов, стоимость никелевой руды будет примерно 9000$ за 1 т., в течение 12 месяцев. В этом году избыток металла составит порядка 100 тыс. т. Цену на руду фиксирует биржа LME, где покупают фьючерс на сырье. В России подобного нет, поэтому подходящий способ инвестиций — покупка акций компании НорНикель (см. Куда инвестировать деньги?).
тонн. Согласно прогнозу экспертов, стоимость никелевой руды будет примерно 9000$ за 1 т., в течение 12 месяцев. В этом году избыток металла составит порядка 100 тыс. т. Цену на руду фиксирует биржа LME, где покупают фьючерс на сырье. В России подобного нет, поэтому подходящий способ инвестиций — покупка акций компании НорНикель (см. Куда инвестировать деньги?).
Создать аккаунт
Зарегистрируйтесь для получения аккаунта. Это просто!
Никелирование — это процесс нанесения слоя никеля на поверхность изделия. Толщина слоя колеблется в пределах 1−50 мкм. Покрытия бывают черные, блестящие и матовые. Они создают надежную оболочку поверхности для защиты от окружающей среды.
Это находит широкое применение в машиностроении, пищевой промышленности и оптике. Проводится никелирование стали, цветных металлов: меди, вольфрама, алюминия, титана, а также и пластика.
Сплавы на его основе
Сплавы никеля исключительно разнообразны, а свойства их для различных отраслей народного хозяйства настолько важны, что едва ли не все составы образуют собой отдельные группы.
Никель-медные сплавы – редкой особенностью, присущей такому твердому раствору является взаимная полная растворимость металлов друг в друге. При сплавлении в любой пропорции получают однофазный однородный сплав, изменяющий свои свойства закономерно и предсказуемо. Коррозионные качества таких сплавов определяются только пропорциями веществ: при доле меди более 50% свойства ближе к качествам самой меди, при доле никеля более 50%, сплав проявляется качества присущие никелю.
Никель-медные сплавы устойчивы к действию и кислот, и щелочей. Их применяют при производстве деталей и резервуаров для аппаратуры, работающей в среде фосфорной, серной, хлорной кислот, а также деталей машин, испытывающих высокие несущие нагрузки.
- К наиболее известным составам такого рода относят монели: 70% никеля, 28% меди и 1,5–2% железа.
- Из медно-никелевых сплавов изготавливаются монеты.
- Константан – сплав из 40% никеля и 59% меди, применяется в изготовлении высокоточной аппаратуры, так как отличается износостойкостью и переносит высокие нагрузки.

Применение никеля в современной технике представлено в этом видеосюжете:
Источник: stroyres.net
Вывод
Таким образом, табачный дым, консервы, бобовые и шоколадные изделия – факторы «нон-стоп», которые приводят к перенасыщению и отравлению организма микроэлементом. Для сохранения здоровья исключите их из ежедневного меню.
Аллергикам на никель рекомендуется избегать контакта с предметами, провоцирующими реакцию, исключить прием продуктов с умеренным и высоким содержанием соединения (свыше 40 микрограмм на 100 грамм изделия), отказаться от использования косметических средств, украшений, содержащий аллерген. Помимо этого, при работе с металлом использовать средства защиты кожных покров и дыхательных путей (например, латексные перчатки, маски).
Больше свежей и актуальной информации о здоровье на нашем канале в Telegram. Подписывайтесь: https://t.me/foodandhealthru
Как определить состав металла в домашних условиях
Главная » Разное » Как определить состав металла в домашних условиях
Как определить металл
Содержание:
- Как определить металл
- Способы определения марки стали.

- Как отличить латунь от меди.
Как определить, какой металл перед вами? Этот вопрос крайне важен, например, в ситуациях, когда необходимо подобрать марку электрода или присадочного прутка, а тип материала неизвестен. При отсутствии возможности прибегнуть к специальным исследованиям — спектральному анализу или анализу на углерод — первое, что можно сделать, это провести визуальный осмотр. Процесс лучше совместить с такими способами, как высекание искры, закалка, проверка напильником, изучение залома.
Для исследования образца материала и сопоставления результата пригодятся следующие сведения:
- Черные металлы в процессе резки или при зачистке имеют серебристый цвет. При этом они быстро окисляются под воздействием воздуха и приобретает тусклый серый оттенок. Также черные металлы отличает низкая стойкость к коррозии и моментальная реакция на воздействие магнитного поля.
- Алюминий и его сплавы не реагируют на воздействие магнита. При срезе можно увидеть блестящий светлый металл, который тускнеет при окислении.
 У чистого алюминия окисленная поверхность как будто покрывается белым налетом.
У чистого алюминия окисленная поверхность как будто покрывается белым налетом. - Бронза обладает желтоватым оттенком. Слабо подвергается окислению, не магнитится.
- Медь отличается красноватым оттенком, при воздействии воздуха цвет темнеет, а на поверхности образуется зеленоватый налет. Не поддается воздействию магнитного поля. В процессе сгорания пламя приобретает зеленый цвет.
- Латунь имеет те же отличительные признаки, что и бронза, но гораздо сильнее подвержена окислению.
- Магний имеет серебристый оттенок, в момент сгорания окрашивает пламя в белый цвет. Не магнитится.
Изображение №1: различия металлов по цвету
Определение марки стали
Стальные заготовки изготавливаются из твердых металлических растворов, в основе которых — углерод и железо. В зависимости от содержания углерода материалы делятся на: низкоуглеродистые (до 0,25%), среднеуглеродистые (до 0,6%), высокоуглеродистые (0,6% и более).
Легирование сталей дополнительными материалами позволяет добиться более качественного состава с уникальными свойствами. Добавлены могут быть: титан, никель, медь, молибден и пр. Выделяют высоколегированные (от 10%), среднелегированные (до 10%) и малолегированные стали (до 2,5%).
Добавлены могут быть: титан, никель, медь, молибден и пр. Выделяют высоколегированные (от 10%), среднелегированные (до 10%) и малолегированные стали (до 2,5%).
Обычно стальные заготовки имеют маркировки, которые позволяют определить марку и другие особенности материала путем визуального осмотра. Но если таких отметок нет, можно использовать следующие способы для получения нужных сведений:
- Аккуратно срезаем верхний тонкий материала. Получившуюся стружку изучаем на предмет ломкости. Если срезать полноценный завиток невозможно или его легко сломать, значит перед вами высокоуглеродистая сталь. Материал с низким содержанием углерода даст плотную длинную стружку однородной структуры, которую будет легко срезать.
- При наличии печи можно использовать более энергозатратный метод. На заготовке делаем надрез, после чего подвергаем ее воздействию максимально высокой температуры. После закаливания проводим повторный распил. Если это потребовало небольшого усилия, как и при надрезе холодного материала, то сталь является малоуглеродистой.

- Берем точильный круг и подготавливаем рабочее место — обеспечиваем хорошее освещение, а сзади устанавливаем темный фон. Наша задача — определить тип стали по особенностям высекаемых искр. Если они яркие и их много, то материал насыщен углеродом. У мягких малоуглеродистых сталей искры тусклые, их частицы небольшие.
- С помощью точильного круга можно также определить металл по цвету искр. Так, если оттенок звездочек красный, то вы имеете дело с высокоуглеродистой сталью. Светлый сноп с небольшим количеством искр свидетельствует о том, что образец среднеуглеродистый. Если металл мало насыщен углеродом, он будет образовывать лучи соломенного цвета без звездочек на концах.
Изображение №2: определение марки стали по искре
Как отличить латунь от меди
Латунные и медные заготовки имеют визуальное сходство, но и обладают разными свойствами:
- латунь — мягкая, пластичная, тяжелая, образует спиралевидную стружку, при ударе издает низкий звук;
- медь — твердая и легкая, образует игольчатую стружку, при ударе издает высокий звук.

Чтобы определить тип материала без использования специальных инструментов, необходимо тщательно очистить изделие от загрязнений и рассмотреть под мощным белым светом. Латунь можно отличить по оранжевому, желтоватому или золотистому оттенку. Оттенок меди — красновато-коричневый. Иногда медные образцы имеют розоватый отлив.
Если исследуемое изделие имеет тонкие стенки, то его состав в некоторых случаях можно определить по степени сопротивляемости механическим нагрузкам. Так, согнуть медную заготовку довольно легко, при этом материал не будет растрескиваться и не сломается. Латунь – твердая и хрупкая, поэтому деформировать изделие будет непросто, но под воздействием больших усилий она может сломаться.
Изображение №3: сравнение цветов меди и латуни
Как определить плотность металла — Канадский институт охраны природы (CCI) Примечания 9/10
Введение
Плотность объекта — это масса объекта, деленная на его объем. Плотность является характеристикой материала, из которого изготовлен объект, и ее значение может помочь идентифицировать материал.
За исключением объектов простой формы, напрямую определить объем сложно. Простой способ определить плотность металлического объекта — взвесить его в воздухе, а затем снова взвесить, когда он будет погружен в жидкость, как описано в разделе «Наука, лежащая в основе измерений плотности».Вода — самая удобная жидкость для использования, но если объект нельзя погрузить в воду, можно использовать органические растворители, такие как этанол или ацетон. Плотность объекта можно рассчитать по двум измерениям веса и плотности жидкости.
При правильном балансе и контейнере подходящего размера этот метод можно использовать для различных объектов: больших и малых, металлических или неметаллических. Этот метод работает для сложных форм, даже для объектов с отверстиями, пока жидкость может проникать и заполнять отверстия.После того, как плотность определена, ее можно сравнить с плотностями известных материалов, чтобы сузить круг вопросов, из которых может быть сделан объект.
В этом примечании описывается процедура и необходимые материалы для определения плотности металлического объекта. Первым шагом является выполнение процедуры на одном или нескольких металлических объектах известного состава, будь то чистый металл или сплав, чтобы получить опыт использования метода и убедиться, что он используется правильно. Затем можно определить плотность неизвестных металлов.
Первым шагом является выполнение процедуры на одном или нескольких металлических объектах известного состава, будь то чистый металл или сплав, чтобы получить опыт использования метода и убедиться, что он используется правильно. Затем можно определить плотность неизвестных металлов.
Методика определения плотности металла
Оборудование и материалы, необходимые для определения плотности
- Мелкие металлические предметы, которые можно погружать в воду
- Весы с возможностью взвешивания под весами (т. Е. Могут взвешивать предметы, подвешенные под ними) и которые могут измерять с разрешением не менее 0,01 грамма (см. Раздел Весы без возможности взвешивания под весами, чтобы узнать, как адаптировать процедуру взвешивания ниже весов. баланс)
- Металлическая проволока для крепления к крючку внутри баланса (хорошо подойдет изогнутая скрепка)
- Поддерживающая подставка или платформа для удержания весов, чтобы под них можно было подвешивать предметы на крючке
- Стаканы, достаточно большие, чтобы предметы можно было полностью погрузить без перелива жидкости
- Опоры для удержания стаканов на нужной высоте под весами
- Водопроводная вода
- Калькулятор
- Нить нейлоновая (e.
 г. леска или аналогичный легкий материал) для подвешивания предметов под весами
г. леска или аналогичный легкий материал) для подвешивания предметов под весами - Одноразовые нитриловые перчатки
- Дополнительно: зажимы для крепления опоры баланса к краю счетчика
Методика определения плотности при взвешивании ниже весов
- Снимите крышку с нижней стороны весов, чтобы открыть крючок внутри.
- Поместите весы на подставку с отверстием для доступа к внутреннему крючку.
- Присоедините проволочный крюк к внутреннему крюку и затем тарируйте весы (установите на ноль).
- Подвесьте какой-либо предмет на крючок под весами, используя нейлоновую нить или аналогичный предмет, и взвесьте его в воздухе. Надевайте перчатки при работе с металлическими предметами, особенно с теми, которые предположительно содержат свинец.
- Наполните химический стакан водой и поместите его под весы.
- Поднимите стакан до полного погружения объекта. Установите подставку под стакан, чтобы удерживать его на нужной высоте.
 Убедитесь, что под объектом или в пустотах внутри объекта нет пузырей.
Убедитесь, что под объектом или в пустотах внутри объекта нет пузырей. - Взвесьте погруженный объект.
- Рассчитайте плотность, используя приведенное ниже уравнение.
- Сравните рассчитанную плотность с известными значениями плотности металлов и сплавов, используя приведенную ниже таблицу или более полные списки, доступные в справочных материалах.
- Повторите шаги 4–9 с остальными объектами.
Расчет плотности
Плотность ρ объекта или материала определяется как масса m, деленная на объем V; в символах ρ = m / V.Если объект взвешивается в воздухе, чтобы определить его фактическую массу, и взвешивается в жидкости, чтобы определить его (кажущуюся) массу в жидкости, то плотность объекта определяется по формуле:
Плотность воды 0,998 г / см 3 при 20 ° C и 0,997 г / см 3 при 25 ° C.
Результаты процедуры
Примеры объектов
На рис. 1 показаны примеры восьми различных металлических образцов, использованных для демонстрации этой процедуры.
© Правительство Канады, Канадский институт охраны природы.CCI 120260-0358
Рис. 1. Металлические предметы, используемые для демонстрации процедуры.
Измеренные плотности металлических образцов на Рисунке 1 представлены ниже.
В верхнем ряду слева направо:
- Вероятно, чугун (7,13 г / см 3 )
- Алюминий высокой чистоты (2,70 г / см 3 )
- Красноватый медный сплав (возможно, 85% меди и 15% цинка, 8,23 г / см 3 )
- Медь высокой чистоты (8.88 г / см 3 )
В нижнем ряду слева направо:
- Цинковое литье (сплав неизвестен, 7,09 г / см 3 )
- Свинец высокой чистоты (11,20 г / см 3 )
- Олово высокой чистоты (7,27 г / см 3 )
- Желтый картридж, латунь (70% меди и 30% цинка, 8,45 г / см 3 )
В каждом образце плотность определялась по приведенной выше формуле. Например, для алюминиевого объекта (б) масса оказалась равной 110. 18 г в воздухе и 69,45 г в воде, что дает плотность 2,70 г / см. 3 . Для чугунного объекта (а) масса составила 209,47 г в воздухе и 180,13 г в воде, что дает 7,13 г / см 3 . Для свинцового объекта (f) масса составила 102,44 г в воздухе и 93,31 г в воде, что дает 11,20 г / см 3 .
18 г в воздухе и 69,45 г в воде, что дает плотность 2,70 г / см. 3 . Для чугунного объекта (а) масса составила 209,47 г в воздухе и 180,13 г в воде, что дает 7,13 г / см 3 . Для свинцового объекта (f) масса составила 102,44 г в воздухе и 93,31 г в воде, что дает 11,20 г / см 3 .
Измеренные плотности алюминия, чугуна и свинца (2,70, 7,13 и 11,20 г / см 3 ) близки к известным значениям плотности (2,71, 7,20 и 11,33 г / см 3 из таблицы 1).Таким образом, предметы из алюминия и свинца легко идентифицируются по плотности.
Для изделия из чугуна одной плотности недостаточно, чтобы исключить другие металлы, такие как цинк (известная плотность 7,13 г / см 3 ). Когда плотность неизвестного металла приближается к плотности нескольких металлов и сплавов (например, цинка, железа и олова), тогда необходимо будет определить другие свойства, такие как магнетизм и цвет, чтобы помочь идентифицировать его.
Известная плотность выбранных металлов и сплавов
Известная плотность выбранных металлов и сплавов приведена в таблице 1 в порядке увеличения плотности (ASTM 2006, Lide 1998).
| Металл или сплав | Плотность (г / см 3 ) |
|---|---|
| Алюминий | 2,71 |
| Алюминиевые сплавы | 2,66–2,84 |
| цинк | 7,13 |
| Чугун (серое литье) | 7,20 |
| Олово | 7.30 |
| Сталь (углеродистая) | 7,86 |
| Нержавеющая сталь | 7,65–8,03 |
| Латунь (картридж: 70% меди, 30% цинка) | 8,52 |
| Латунь (красный: 85% меди, 15% цинка) | 8,75 |
| Нейзильбер (65% меди, 18% никеля, 17% цинка) | 8,75 |
| Бронза (85% меди, 5% олова, 5% цинка, 5% свинца) | 8.80 |
| Никель | 8,89 |
| Медь | 8,94 |
| Серебро | 10,49 |
| Свинец | 11,33 |
| Золото | 19,30 |
Реквизиты баланса
Весы с возможностью взвешивания под весами обычно поставляются с крышкой под внутренним крючком. На рис. 2 показан пример расположения крышки на дне весов.
На рис. 2 показан пример расположения крышки на дне весов.
© Правительство Канады, Канадский институт охраны природы. CCI 120260-0359
Рис. 2. Весы с возможностью взвешивания под весами.
На рис. 3 показан увеличенный вид с закрытой крышкой; на рис. 4 крышка открыта, чтобы обнажить внутренний крючок.
© Правительство Канады, Канадский институт охраны природы. CCI 120260-0360
Рис. 3. Деталь нижней стороны весов, демонстрирующая подвижную металлическую крышку, закрывающую внутренний крюк.
© Правительство Канады, Канадский институт охраны природы. CCI 120260-0361
Рис. 4. Деталь нижней стороны весов, показывающий внутренний крюк после поворота металлической крышки.
На рисунке 5 показана металлическая проволока, изогнутая в виде крючков на обоих концах. На рис. 6 показан крючок на одном конце проволоки, прикрепленный к внутреннему крючку внутри весов.
© Правительство Канады, Канадский институт охраны природы. CCI 120260-0363
Рис. 5. Проволока с загнутыми концами в виде крючка.
5. Проволока с загнутыми концами в виде крючка.
© Правительство Канады, Канадский институт охраны природы. CCI 120260-0362
Рис. 6. Деталь проволоки, загнутой в крючки с обоих концов. Верхний конец крючка прикреплен к другому крючку внутри весов.
На рис. 7 показаны весы, которые устанавливаются на подставку из оргстекла с прорезью в верхней части. Отверстие обеспечивает доступ к крючку на нижней стороне весов.
© Правительство Канады, Канадский институт охраны природы. CCI 120260-0365
Рисунок 7.Весы устанавливаются на подставку из оргстекла с крюком, который вот-вот пройдет через отверстие в подставке.
На рис. 8 показаны весы на подставке из оргстекла с прямоугольным купоном из чистой меди, взвешиваемым на воздухе. На рисунке 9 показаны весы на стенде из оргстекла с прямоугольным купоном из чистой меди, взвешиваемым в воде. Меньшая подставка из оргстекла используется для поддержки стакана на нужной высоте.
© Правительство Канады, Канадский институт охраны природы. CCI 120260-0366
CCI 120260-0366
Рис. 8. Прямоугольный купон чистой меди, взвешиваемой на воздухе.
© Правительство Канады, Канадский институт охраны природы. CCI 120260-0367
Рис. 9. Прямоугольный купон из чистой меди, погруженной в воду.
На рисунке 10 показан пример объекта с отверстием, в котором застряли пузырьки воздуха. Будьте осторожны, чтобы не захватить предметом пузырьки воздуха, так как это приведет к неточному показанию.
© Правительство Канады, Канадский институт охраны природы.CCI 120260-0375
Рис. 10. Три пузырька воздуха застряли в отверстии.
Дополнительная информация
Использование других растворителей, кроме воды
Если погружать какой-либо предмет в воду, например железо, нецелесообразно, поскольку он очень подвержен коррозии, можно использовать органический растворитель, такой как ацетон или безводный этанол. Необходимо использовать надлежащую вентиляцию и соответствующие средства индивидуальной защиты. Обратитесь к паспорту безопасности (SDS) конкретного растворителя для рекомендованного оборудования. Плотность ацетона составляет 0,790 г / см 3 , а плотность безводного этанола составляет 0,789 г / см 3 , оба при 20 ° C. Тем, кому может потребоваться использовать одну из этих жидкостей, попробуйте измерить плотность объекта, используя воду и одну из этих жидкостей, и сравните результаты.
Плотность ацетона составляет 0,790 г / см 3 , а плотность безводного этанола составляет 0,789 г / см 3 , оба при 20 ° C. Тем, кому может потребоваться использовать одну из этих жидкостей, попробуйте измерить плотность объекта, используя воду и одну из этих жидкостей, и сравните результаты.
Советы по настройке весов
Альтернативная подставка для весов
Лист фанеры с отверстием можно прижать к краю прилавка, если нет подставки для балансировки (Рисунок 11).
© Правительство Канады, Канадский институт охраны природы. CCI 120260-0296
Рис. 11. Платформа для весов, сделанная из фанеры и зажимов.
Весы без взвешивания под весами
Весы без крюка для взвешивания можно использовать для определения плотности, но для этого требуется рама, чтобы подвешивать объект под весами и переносить вес объекта на весы. Баланс должен быть установлен на платформе; может использоваться установка, аналогичная показанной на рисунке 11.(В этом случае отверстие в дереве на Рисунке 11 не требуется. ) Затем вокруг весов и платформы устанавливают четырехстороннюю рамку (имеющую форму рамки для рисунка), опираясь только на чашу весов и не касаясь ее. другая часть баланса (рисунок 12). Весы тарируют с установленными рамой и крюком, затем объект прикрепляют к крюку на раме и взвешивают в воздухе и в жидкости, как в шагах 4–9 процедуры: определение плотности металла.
) Затем вокруг весов и платформы устанавливают четырехстороннюю рамку (имеющую форму рамки для рисунка), опираясь только на чашу весов и не касаясь ее. другая часть баланса (рисунок 12). Весы тарируют с установленными рамой и крюком, затем объект прикрепляют к крюку на раме и взвешивают в воздухе и в жидкости, как в шагах 4–9 процедуры: определение плотности металла.
© Правительство Канады, Канадский институт охраны природы.CCI 120260-0298
Рис. 12. Вид спереди (левая часть рисунка) и вид сбоку (правая сторона), показывающие весы без возможности взвешивания ниже весов. Верхний сегмент прямоугольной рамки опирается на чашу весов, а предмет прикрепляется к нижнему сегменту.
Наука, лежащая в основе измерений плотности
Плавучесть и принцип Архимеда
Техника этой процедуры датируется третьим веком до нашей эры. В своей книге «Плавающие тела» Архимед Сиракузский предположил, что если объект погрузить в жидкость и взвесить, он будет легче, чем его истинный вес, на вес жидкости, которую он вытесняет. История гласит, что Архимед использовал эту идею, чтобы показать, что корона не была чистым золотом, а скорее смесью золота и серебра (Heath 1920).
История гласит, что Архимед использовал эту идею, чтобы показать, что корона не была чистым золотом, а скорее смесью золота и серебра (Heath 1920).
Объект кажется более легким в жидкости, потому что на него действует сила, называемая выталкивающей силой. Сила возникает из-за того, что давление в жидкости увеличивается с глубиной, поэтому давление на нижнюю часть объекта (толкая объект вверх) выше, чем давление сверху (толкающее его вниз). Разница между давлением, направленным вверх и вниз, дает подъемную силу.Выталкивающая сила, толкая объект вверх, действует против силы тяжести, которая тянет объект вниз. Если подъемная сила меньше силы тяжести, объект утонет, но будет казаться, что в жидкости он весит меньше, чем в воздухе. Если выталкивающая сила больше силы тяжести, объект всплывет к поверхности жидкости.
Плотность объекта рассчитывается по формуле, приведенной ранее
Когда плотность известна, ее можно использовать для расчета объема объекта по следующей формуле:
Объем объекта = (масса в воздухе) / (плотность объекта)
Подобно воде, воздух также производит подъемную силу. (Вот почему гелиевые шары плавают вверх.) Выталкивающая сила воздуха слишком мала, чтобы иметь значение в этой процедуре, но ее необходимо учитывать, когда требуется высокая точность взвешивания (Skoog et al. 2014).
(Вот почему гелиевые шары плавают вверх.) Выталкивающая сила воздуха слишком мала, чтобы иметь значение в этой процедуре, но ее необходимо учитывать, когда требуется высокая точность взвешивания (Skoog et al. 2014).
Плотность определяется по вытесненному объему
Более простой, но менее точный способ измерения плотности — поместить объект в жидкость и измерить объем вытесненной жидкости. Это можно использовать для небольших объектов, которые помещаются в градуированный цилиндр, например, чтобы решить, сделан ли объект из свинца или менее плотного металла.
Порядок действий следующий. Найдите градуированный цилиндр диаметром не намного больше, чем объект. Определите массу объекта с помощью подходящих весов. Добавьте воду в мерный цилиндр и запишите начальный объем. Полностью погрузите объект в воду, стараясь не образовывать пузырей, а затем запишите объем во второй раз. Объем объекта равен разнице конечного и начального объемов, считываемых с градуированного цилиндра, а плотность — это масса, деленная на объем объекта.
В качестве примера была измерена фигурка лося. Масса 4,088 г. На рис. 13 фигурка показана за пределами градуированного цилиндра, а на рис. 14 — в погруженном состоянии. Вода в градуированном цилиндре увеличилась с 5,0 мл до 5,6 мл, когда фигурка была погружена, что дало изменение объема на 0,6 мл. Без учета ошибок измерения объема плотность рассчитывается и составляет 4,088 г / 0,6 мл = 6,8 г / см 3 . (Примечание: 1 мл = 1 см 3 .) Это меньше плотности цинка и может предполагать сплав цинка и более легкого металла, возможно, магния или алюминия.Но с учетом небольшого объема измерения есть неточности. Объем может быть измерен только с точностью до 0,1 мл с помощью градуированного цилиндра, поэтому объем может составлять от 0,5 до 0,7 мл. Таким образом, плотность может быть где угодно от 4,088 г / 0,7 мл = 5,8 г / см 3 до 4,088 г / 0,5 мл = 8,2 г / см 3 . В этом диапазоне измерений фигурка может быть из цинка, железа, олова, стали или других сплавов, но не из чистого алюминия или чистого свинца. Фактически анализ показал, что это олово, имеющее плотность 7.30 г / см 3 .
Фактически анализ показал, что это олово, имеющее плотность 7.30 г / см 3 .
© Правительство Канады, Канадский институт охраны природы. CCI 120260-0373
Рис. 13. Небольшой металлический предмет перед погружением в воду в мерном цилиндре на 25 мл. Обратите внимание на уровень воды.
© Правительство Канады, Канадский институт охраны природы. CCI 120260-0374
Рис. 14. Небольшой металлический предмет после погружения в воду в мерном цилиндре объемом 25 мл. Уровень воды примерно на 0,6 мл больше, чем до погружения объекта.
Другое применение
Вышеуказанные процедуры можно использовать не только для идентификации металлов по их плотности.
Вес для литья металлов
При отливке скульптуры необходимо оценить количество металла, необходимое для заполнения формы модели скульптуры. Если отливаемая модель может быть погружена в воду, объем модели можно определить с помощью описанных выше методов. Тогда необходимую массу металла m можно рассчитать из объема V модели и плотности металла ρ по формуле m = ρV. (Имейте в виду, что обычно требуется дополнительный металл для заполнения каналов, которые направляют расплавленный металл в форму.)
(Имейте в виду, что обычно требуется дополнительный металл для заполнения каналов, которые направляют расплавленный металл в форму.)
Благодарности
Особая благодарность Миган Уолли, Люси ‘т Харт и Кэтрин Мачадо, бывшим стажерам CCI, за их помощь в разработке этой заметки.
Список литературы
ASTM G1-03. «Стандартная практика подготовки, очистки и оценки образцов для испытаний на коррозию». В Ежегодной книге стандартов ASTM, т. 03.02. Вест Коншохокен, Пенсильвания: Американское общество испытаний и материалов, 2006, стр.17–25.
Heath, T.L. Архимед. Нью-Йорк, Нью-Йорк: Макмиллан, 1920.
Lide, D.R., ed. CRC Справочник по химии и физике, 79-е изд. Бока-Ратон, Флорида: CRC Press, 1998, стр. 12-191–12-192.
Скуг, Д.А., Д.М. Уэст, Ф.Дж. Холлер и С. Присядь. Основы аналитической химии, 9 изд. Бельмонт, Калифорния: Брукс / Коул, 2014 г., стр. 22–23.
Написано Линдси Селвин
Également publié en version française.
© Правительство Канады, Канадский институт охраны природы, 2016
ISSN 1928-1455
.
Как определить состав почвы в вашем дворе | Home Guides
Почвы состоят из частиц разного размера, а именно из глины, ила и песка. Определение пропорции каждого типа частиц или текстуры почвы для почвы вашего двора поможет вам понять различные характеристики почвы, узнать, нужны ли поправки, и соответствующим образом скорректировать свой режим ухода за двором. Простой тест позволяет приблизительно оценить процентное содержание песка, ила и глины в почве, не отправляя образцы в лабораторию.
Соберите образцы почвы со своего двора. Выкопайте несколько сантиметров вниз, чтобы избежать растительности и органических остатков. Соберите почву с нескольких мест сбора, разбросанных по двору. Если у вас большой двор или вы подозреваете, что текстура почвы меняется в пределах двора, подумайте о том, чтобы собрать несколько образцов, хранить их по отдельности и тестировать каждый отдельно.
Разложите собранную почву на газете и дайте почве высохнуть.
Измельчите сухую почву, чтобы разбить комья. Измельчите его пестиком или аналогичным шлифовальным инструментом. Удалите все крупные камни и органический материал, не являющийся почвой.
Измельчите его пестиком или аналогичным шлифовальным инструментом. Удалите все крупные камни и органический материал, не являющийся почвой.
Вылейте измельченный грунт в прозрачную литровую или аналогичную банку так, чтобы она была заполнена на четверть. Наполните банку водой на три четверти.
Добавьте примерно 1 чайную ложку непенящегося порошка для мытья посуды или поваренной соли в банку и плотно закройте ее крышкой. Сильно встряхните банку в течение 10 минут, а затем поставьте так, чтобы вам не пришлось беспокоить ее несколько дней.
Проверьте емкость через минуту после того, как вы закончили встряхивать ее, и поставьте. Отметьте на боковой стороне банки верхний слой осевшего песка.
Отметьте на банке верхнюю часть следующего оседающего слоя, частиц ила, через два часа после того, как вы перестали трясти банку, и поставьте ее на место.
Отметьте верх последнего слоя, слоя глины, когда он полностью осядет и вода станет прозрачной. Последний слой может полностью осесть через несколько дней.
Измерьте толщину каждого отдельного слоя частиц и общую толщину образца почвы.
Рассчитайте процентное содержание каждого типа частиц в образце. Начните с деления толщины каждого слоя на общую толщину образца. Умножьте это количество на 100.
Посмотрите на треугольник текстуры почвы, чтобы определить текстуру почвы, используя рассчитанные вами проценты. Найдите процентное содержание каждого типа частиц по сторонам треугольника текстуры почвы и проследите по соответствующим линиям до центра треугольника, чтобы определить, где они пересекаются и в какой класс текстуры попадает эта точка пересечения.
.
Как ученые определяют химический состав планет и звезд?
Наиболее распространенный метод, который астрономы используют для определения состава звезд, планет и других объектов, — это спектроскопия. Сегодня для этого процесса используются инструменты с решеткой, которая распределяет свет от объекта по длине волны. Этот рассеянный свет называется спектром. Каждый элемент — и комбинация элементов — имеет уникальный отпечаток пальца, который астрономы могут искать в спектре данного объекта.Идентификация этих отпечатков пальцев позволяет исследователям определить, из чего они сделаны.
Этот рассеянный свет называется спектром. Каждый элемент — и комбинация элементов — имеет уникальный отпечаток пальца, который астрономы могут искать в спектре данного объекта.Идентификация этих отпечатков пальцев позволяет исследователям определить, из чего они сделаны.
Этот отпечаток пальца часто проявляется как поглощение света. В каждом атоме есть электроны, и эти электроны предпочитают оставаться в конфигурации с самой низкой энергией. Но когда фотоны, несущие энергию, попадают в электрон, они могут поднять его до более высоких уровней энергии. Это поглощение, и электроны каждого элемента поглощают свет на определенных длинах волн (то есть энергии), связанных с разницей между уровнями энергии в этом атоме.Но электроны хотят вернуться на свои исходные уровни, поэтому они не удерживают энергию надолго. Когда они излучают энергию, они испускают фотоны с точно такими же длинами волн света, которые были изначально поглощены. Электрон может испускать этот свет в любом направлении, поэтому большая часть света излучается в направлениях от нашего луча зрения. Таким образом, на этой длине волны в спектре появляется темная линия.
Таким образом, на этой длине волны в спектре появляется темная линия.
Поскольку длины волн, на которых возникают линии поглощения, уникальны для каждого элемента, астрономы могут измерить положение линий, чтобы определить, какие элементы присутствуют в цели.Количество поглощенного света также может предоставить информацию о том, сколько каждого элемента присутствует.
Чем больше элементов содержит объект, тем сложнее может стать его спектр. Другие факторы, такие как движение, могут влиять на положение спектральных линий, но не на расстояние между линиями от данного элемента. К счастью, компьютерное моделирование позволяет исследователям различать множество различных элементов и соединений даже в перегруженном спектре, а также определять линии, которые кажутся смещенными из-за движения.
Элисон Клесман
Младший редактор
.
mihalick — факультеты / сайты сотрудников
Пожалуйста, дважды проверьте веб-адрес или воспользуйтесь функцией поиска на этой странице, чтобы найти то, что вы ищете.
Если вы уверены, что имеете правильный веб-адрес, но столкнулись с ошибкой, пожалуйста, связаться с администрацией сайта.
Спасибо.
Возможно, вы искали…
- Михалик Ледвелл, 4 августа 2011 г., 10:54
- классификация по mihalick, 4 августа 2011 г., 10:18
.
Никелирование в домашних условиях технология
Как сделать никелирование своими руками
Всем привет! Цель статьи заключается в том, чтобы показать процесс никелирования со всех возможных сторон. А именно, как добиться высокого качества покрытия, не слишком потратится на расходные материалы и безопасно произвести гальванические работы. Мы также по возможности изготовим свой собственный электролит с нуля, вместо того, чтобы покупать специальные химические реактивы.
Если вы уже знакомы с процессом омеднения, отметьте следующее, что данный процесс имеет существенные отличия. Никель не очень хорошо растворяется (если вообще растворяется) в уксусе без специальных активаторов.
Никелирование можно использовать во множестве случаев, например:
- Создать антикоррозионное покрытие, что защитит основной металл от окисления и коррозии. Его часто используют в пищевой промышленности, для предотвращения загрязнения пищевых продуктов железом.
- Увеличить твёрдость покрываемого предмета и таким образом повысить долговечность деталей механизмов и инструментов.

- Помочь при спаивании разных металлов.
- Создать всевозможные варианты красивых декоративных отделок.
- Значительная толщина покрытия, может сделать предмет магнитным.
Примечание: Чтобы получить различные виды покрытий (на вид и по свойствам), вам будет нужно добавить дополнительные химические реактивы и металлы для получения желаемого результата. Реактивы изменят пути размещения атомов относительно себя и/или добавляют другие металлы в наносимое покрытие. Если вам нужно получить антикоррозийное покрытие, не добавляйте никаких химических реактивов в электролит, так как они могут оставить на покрытии пятна или сделать его тусклым.
Отказ от ответственности – ацетат никеля, химический состав, который мы будем изготавливать, очень ядовит. Название статьи говорит о том, что вам не нужно играть в безумные игры с сильнейшими кислотами, что могут оставить тяжелые ожоги на коже. При тех концентрациях, с которыми мы будем работать, процесс будет «относительно безопасным». Тем не менее, не забудьте вымыть руки, после того, как закончите работу и не забудьте должным образом вытереть поверхности (на которых или рядом с которыми) могли попасть остатки химического состава.
Тем не менее, не забудьте вымыть руки, после того, как закончите работу и не забудьте должным образом вытереть поверхности (на которых или рядом с которыми) могли попасть остатки химического состава.
Шаг 1: Материалы
Почти все расходные материалы можно найти в ближайшем супермаркете. Найти источник чистого никеля немного сложнее, но он не будет стоить больше, чем пару долларов. Также настоятельно рекомендую найти блок питания (AC/DC).
Материалы:
- Дистиллированный 5% уксус;
- Поваренная соль;
- Банка с закручивающейся крышкой;
- 6В батарею;
- Зажимы «крокодильчики»;
- Нитриловые перчатки;
- Бумажные полотенца;
- Кислотный абразив Cameo Stainless Steel and Aluminum Cleaner;
Чистый никель – вы можете «достать» несколькими различными путями.
- Купить две пластины никеля на eBay за
$5;

Вы также можете удалить никелевые витки/намотки со старых гитарных струн, если у вас трудности с деньгами. Это займёт немного времени, потребуется воспользоваться кусачками и плоскогубцами. Наибольшее количество никеля содержат струны, что состоят из стального ядра, которое в дальнейшем может «загрязнить» электролит.
Кроме этого можно воспользоваться никелированными дверными ручками. Я советовал бы с опаской относиться к этому варианту. Всё из-за того, что существует хороший шанс того, что они просто покрыты никелиподобным покрытием.
Настоятельно рекомендую приобрести:
- Высоковольтный блок питания (постоянное напряжение). В проекте использовал старый 13.5В зарядник для ноутбука. Можно использовать зарядки для мобильных телефонов или же старый компьютерный блок питания.
- Держатель предохранителя;
- Простой проволочный предохранитель, рассчитанный на приграничные условия эксплуатации выбранного вами блока питания.
Шаг 2: Подготавливаем блок питания
Моя версия стенда довольно сырая, зато она эффективная. Вы можете (и возможно следует) сделать небольшой ящик с банкой, предохранителем и двумя клеммами, что выведены наружу, к которым присоединены крокодильчики для подключения к блоку питания.
Вы можете (и возможно следует) сделать небольшой ящик с банкой, предохранителем и двумя клеммами, что выведены наружу, к которым присоединены крокодильчики для подключения к блоку питания.
В случае, если будете использовать зарядку для мобильного телефона, вам будет нужно выполнить следующие действия:
- Отрезать бочкообразный штекер.
- Разделить два провода и укоротить один из них на 5-8 см. Это поможет предотвратить случайное короткое замыкание.
- Зачистить от изоляции около 6 мм проводов.
- Припаять к одному из них держатель предохранителя и установить в него предохранитель.
В том же случае, если вы будете использовать зарядку для ноутбука будет нужно выполнить следующее:
- Отрезать бочкообразный штекер;
- Используя лезвие, удалите наружную изоляцию. Большинство зарядок имеют один изолированный провод, что обернут во множество медных проводов без изоляции.
- Скрутить медные провода без изоляции вместе, сформировав одну жилу.
 Это будет «земля».
Это будет «земля». - Припаять к нему держатель предохранителя.
- Зачистить около 6 мм изолированного провода и связать обо провода используя пластиковую застёжку или изоленту, таким образом он не коротнёт с оголенным проводом.
Намного более сложнее превратить компьютерный блок питания в настольный БП. Поисковик вам в помощь, вы наверняка найдёте пару статей, в которых всё подобно расписано.
Примечание относительно полярностей
При проведении процесса никелирования, нужно заранее определить полярности выводов. Полярность можно определить при помощи мультиметра (режим вольтметра). Если у вас нет под рукой прибора, вы можете смешать щепотку соли с небольшим количеством воды. Возьмите один из «крокодильчиков», подсоедините его к одному проводу и опустите в воду. Повторите подобную процедуру с другим проводом. Крокодильчик, вокруг которого будут возникать пузырьки и будет иметь отрицательную полярность.
Шаг 3: Готовим электролит
В принципе, можно приобрести различные соли никеля, но в этом же нет духа изобретателя. Я покажу, как можно изготовить ацетат никеля, намного дешевле, чем покупать хим. реактивы в магазине.
Я покажу, как можно изготовить ацетат никеля, намного дешевле, чем покупать хим. реактивы в магазине.
Заполним банку дистиллированным уксусом, оставив около 25 мм от верха. Растворим немного соли в уксусе. Количество соли не так важно, но не стоит перебарщивать (щепотки должно хватить). Причина, по которой мы добавляем соль, кроется в том, что она увеличивает электропроводность уксуса. Чем больше величина тока, что протекает через уксус, тем быстрее мы сможем растворить никель. Однако, слишком большая величина тока, приведёт к тому, что толщина покрытие будет нещадно низкой. Всё нужно делать с экономией.
В отличии от меди, никель не превратится в электролит, просто полежав некоторое время. Нам нужно растворить никель электричеством.
Поместим два куска чистого никеля в уксус с солью таким образом, чтобы части обоих кусков выглядывали из раствора (находились в воздухе) и при этом не касались друг друга. Закрепим «крокодильчик» на одном куске никеля, после чего подключим его к положительному выводу (полярность мы определили в прошлом шаге). Закрепим второй «крокодильчик» на другом куске никеля и подсоединим его к отрицательному выводу блока питания. Убедитесь в том, что зажимы не касаются уксуса, так как они растворятся в нём и приведут электролит в негодность.
Закрепим второй «крокодильчик» на другом куске никеля и подсоединим его к отрицательному выводу блока питания. Убедитесь в том, что зажимы не касаются уксуса, так как они растворятся в нём и приведут электролит в негодность.
Вокруг источника никеля, что соединён с отрицательным выводом начнут образовываться пузырьки водорода, а вокруг положительного — пузырьки кислорода. Говоря по правде, очень небольшое количество газообразного хлора (от соли) также сформируется на положительной клемме, но если вы не положили значительное количество соли или используете невысокое напряжение, то концентрация хлора, что растворяется в воде, не будет превышать допустимые пределы. Проводить работы следует на улице или в хорошо проветриваемом помещении.
Через некоторое время (в моём случае около двух часов), вы заметите, что раствор стал светло-зеленого цвета. Это ацетат никеля. Если вы получили синие, красные, желтые или любые другие цвета, — это означает, что источник никеля не был чистым. Раствор должен быть прозрачным, если он мутный — источник никеля не был чистым. Раствор и «источники никеля» могут греться во время процесса — это нормально. Если они на ощупь стали очень горячими, отключите питание, дайте им остыть в течение часа, а затем снова включите питание (повторяйте при необходимости). Возможно, вы добавили слишком много соли, что увеличило ток и мощность, рассеиваемую в виде тепла.
Раствор должен быть прозрачным, если он мутный — источник никеля не был чистым. Раствор и «источники никеля» могут греться во время процесса — это нормально. Если они на ощупь стали очень горячими, отключите питание, дайте им остыть в течение часа, а затем снова включите питание (повторяйте при необходимости). Возможно, вы добавили слишком много соли, что увеличило ток и мощность, рассеиваемую в виде тепла.
Шаг 4: Подготовка поверхности для покрытия
ПРИМЕЧАНИЕ. Некоторые металлы, такие как нержавеющая сталь, не допускают прямого никелирования. Сначала будет нужно создать промежуточный медный слой.
Итоговый результат будет зависит от чистоты поверхности, на которую будет наноситься никелевое покрытие. Даже если поверхность выглядит чистой, всё равно нужно её очистить (мылом или чистящим средством в состав которого входит кислоты).
Вы можете дополнительно очистить поверхность путем обратного гальванического разложения (т.е. «электроочисткой») в течение нескольких секунд.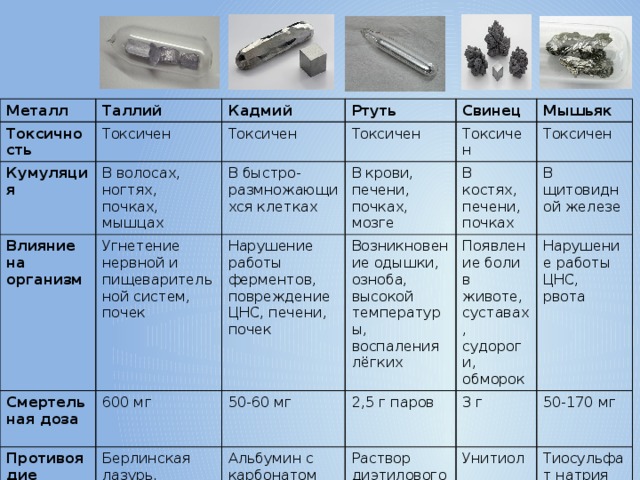 Прикрепите объект к положительному выводу, «пустой провод» к отрицательному выводу и оставьте их в растворе солей уксуса на 10-30 секунд. Это приведет к удалению остаточного окисления.
Прикрепите объект к положительному выводу, «пустой провод» к отрицательному выводу и оставьте их в растворе солей уксуса на 10-30 секунд. Это приведет к удалению остаточного окисления.
Большие поверхности можно очистить тонкой стальной щёткой и уксусом.
Шаг 5: Пришло время для гальванизации
В этом шаге в качестве источника питания будет использоваться 6В батарея. Более низкое напряжения (примерно в 1 В) позволит добиться лучшего, более блестящего и более гладкого покрытия. Для гальванопокрытия можно использовать источник питания более высокого постоянного напряжения, но полученный результат будет далек от идеала.
Поместим источник никеля в раствор ацетата никеля и подключим его к положительному выводу батареи. Закрепим другой зажим на объекте, который будет никелироваться и подключим его к отрицательному выходу аккумулятора.
Поместим объект в раствор и подождём около 30 секунд. Достанем его, повернём на 180 градусов и поместим его обратно в раствор еще на 30 секунд. Нужно менять место крепления зажима, чтобы покрыть всю поверхность. В отличие от медного покрытия, зажим не должен оставлять меток «ожогов».
Нужно менять место крепления зажима, чтобы покрыть всю поверхность. В отличие от медного покрытия, зажим не должен оставлять меток «ожогов».
Раствор вокруг объекта должен пузыриться.
Шаг 6:
Никель не окисляется при комнатной температуре и не тускнеет. Можно слегка отполировать поверхность, чтобы получить яркий блеск.
Если никелирование не такое блестящее, как хотелось бы, отполируйте его средством, которое не содержит воска или масла, а затем снова проведите гальванику покрытие.
Добавление небольшое количество олова во время первоначального покрытия, изменит цвет (олово даёт цвет белого металла, такого как серебро). Многие металлы могут быть электрически растворены в уксусе, как никель. Два основных металла, которые не могут быть электрически растворены в уксусе, — это золото и серебро (поверьте, я пробовал). С прошлого эксперимента у меня осталось немного медного электролита, который я смешал с раствором никеля. Результат — матовая, темно-серая, очень твердая поверхность, которая похожа на школьную доску.
Если вы не опытный химик, будьте очень осторожны, добавляя случайные химические вещества к гальванической ванне — вы можете запросто создать какой-то токсичный газ…
Оценка статьи:
Загрузка…
Сохранить себе в:
Adblock
detector
Как определить нихром | Аякс-металл ✅
Нихром – это одна из семи групп прецизионных (с заданными свойствами) сплавов, чьё производство регламентирует ГОСТ 10994-74. В эту группу входят 16 марок металлов с высокой сопротивляемостью току, из которых десять используются для производства нагревателей и шесть – для датчиков и резисторов с постоянным сопротивлением в заданном температурном диапазоне.
Согласно упомянутому нормативному документу, в определение нихрома включены такие характеристики сплавов:
- максимальная рабочая температура нагрева – до 1 100, 1 150, 1 200, 1 220 и 1 400 °С;
- удельное сопротивление – от 0,99–1,07 до 1,37–1,47 единицы;
- базовые элементы химического состава – никель и/или хром с массовой долей 55–78 и 15–23 % соответственно.

В Интернете часто можно встретить вопрос о том, как определить нихром в домашних условиях. Сразу скажем, что сделать это по внешнему виду металла невозможно.
Чтобы определить нихромовую проволоку, необходимо знать основные свойства этих сплавов. Прежде всего эти вещества немагнитные. Если постоянный магнит не притягивает проволоку, возможно, перед вами нихром. Такая оговорка связана с тем, что он не единственный немагнитный сплав. Если через проволоку из нихрома пустить ток, она быстро нагреется до характерного красного свечения с выделением сильного теплового излучения.
Более точный ответ, вплоть до определения марки сплава, можно получить только с использованием лабораторного оборудования. По этой причине полные характеристики продукции из нихрома обязательно указывают в сопроводительной документации, включая её маркировку и назначение.
Применение проволоки из нихрома
Точное определение проволоки из нихрома даёт ГОСТ 12766. 1-90, согласно которому она производится. Полный её сортамент включает следующие виды продукции:
1-90, согласно которому она производится. Полный её сортамент включает следующие виды продукции:
- для спиральных и других нагревателей открытого типа – для маркировки такой проволоки используют букву Н;
- для трубчатых нагревателей – обозначают аббревиатурой ТЭН;
- для резисторов – маркируются буквой С.
В зависимости от марки металла нихромовая проволока изготавливается диаметром от 0,4–3, до 0,1–7,5 мм. Маркировка этой продукции содержит следующую информацию в такой очерёдности:
- диаметр;
- марка сплава;
- назначение;
- ссылка на нормативный документ.
Отсутствие в маркировке обозначения сферы применения по умолчанию означает, что проволока предназначена для производства резисторов. Помимо проволоки, для изготовления нагревательных элементов (Н) и резисторов (С) используют ленту из нихрома, производство которой регламентирует ГОСТ 12766.2-90.
В зависимости от диаметра проволока из нихрома для промышленных потребителей поставляется намотанной на катушки, оправки или в мотках. Чтобы не задаваться вопросом, как определить, из нихрома проволока или нет, следует пользоваться услугами надёжного поставщика. Напоминаем, что нихром входит в число наиболее дорогостоящих сплавов. Поэтому не стоит приобретать такую продукцию в случайных местах.
Чтобы не задаваться вопросом, как определить, из нихрома проволока или нет, следует пользоваться услугами надёжного поставщика. Напоминаем, что нихром входит в число наиболее дорогостоящих сплавов. Поэтому не стоит приобретать такую продукцию в случайных местах.
При покупке нихромовой проволоки необходимо обращать внимание на целостность упаковки, которая в том числе предохраняет проволоку от спутывания. Отсутствие ярлыка на упаковке также даёт повод для сомнений, не позволяя определить, что в ней проволока из нихрома необходимой вам марки.
Ошибки выбора нихромовой проволоки являются основной причиной раннего выхода из строя изготовленных из неё нагревательных элементов, поскольку они рассчитаны на разный температурный режим эксплуатации. При правильном выборе проволоки из нихрома гарантийный срок её использования в зависимости от диаметра составляет от 800 до 4 000 часов в непрерывном режиме эксплуатации. Величина этого показателя растёт по мере увеличения диаметра проволоки.
Примеры применения проволоки из нихрома для нагревательных элементов
Нихромовые сплавы являются основными материалами для изготовления нагревательных элементов. Проволока или лента из нихрома обязательно используется в таких видах оборудования, как:
- кухонная техника – плиты, духовки, мармиты, посудомоечные машины и прочее;
- бытовые приборы – утюги, фены, электрочайники, стиральные машины, бойлеры и т. д.;
- лабораторное оборудование – автоклавы, сушильные печи, реостаты;
- промышленные агрегаты – печи обжига и сушки;
- разнообразная электротехническая продукция.
Тем, кого интересует, как определить нихромовую проволоку в домашних условиях с точки зрения заготовки вторсырья, можем посоветовать разборку любых нагревателей. Все они содержат нихром.
Правда, вы не сможете разделить его по маркам, а заготовители лома устанавливают приёмные цены в зависимости от содержания в нём никеля. В этом отношении в выигрышном положении оказываются промышленные потребители нихрома, которые могут сортировать вышедшие из строя нагревательные элементы по маркам сплавов. Разница в цене между ними может достигать больших значений.
Разница в цене между ними может достигать больших значений.
Подводим итоги: Определяем нихромовую проволоку
Резюмируя информацию о способах определения проволоки из нихрома, можно сказать следующее:
- отличить нихромовую проволоку от аналогичной продукции из других сплавов по внешнему виду невозможно;
- определить нихром без использования лабораторного оборудования можно – самый достоверный результат покажет пропуск тока через проволоку, но это не поможет установить марку сплава, которая является важнейшей характеристикой данной продукции;
- всё, что находится внутри спиральных и трубчатых нагревательных элементов, является нихромом;
- самым простым способом идентификации нихрома является ярлык на упаковке продукции из него;
- проволока из нихрома и нагревательные элементы из неё должны использоваться по назначению с учётом марок сплавов и температурных режимов;
- для сортировки сборного нихромового лома вам потребуется лабораторное оборудование по определению массовой доли базовых элементов химического состава сплавов.

Ошибки выбора нихромовой проволоки могут привести к значительным финансовым потерям. Если вы сомневаетесь, посоветуйтесь со специалистом.
Можно ли проверить уровень никеля дома? (Новая информация)
Никель — это серебристо-белый металл, естественным образом присутствующий в окружающей среде. Он присутствует в основном в связи с другими металлическими предметами, такими как украшения, монеты, ключи. Но его можно найти и в пищевых продуктах в небольших количествах.
В то время как большинство людей не испытывают проблем после употребления продуктов, содержащих некоторое количество никеля, у других может возникнуть иммунный ответ. Если вы один из таких людей, вы определенно задавались вопросом, есть ли способы проверить уровень никеля в домашних условиях.
Содержание
- Можно ли проверить уровень никеля дома?
- Что такое никель?
- Как узнать, нужно ли мне проверить уровень никеля?
- Какие существуют альтернативные способы проверки уровня никеля?
Можно ли проверить уровень никеля дома?
Аллергия на никель становится все более и более распространенным явлением, но не существует домашнего теста, который мог бы диагностировать это состояние. Это тесты, которые позволяют вам проверять наличие никеля на предметах и металлах, помогая вам избежать контактной сыпи, которая может быть полезной.
Это тесты, которые позволяют вам проверять наличие никеля на предметах и металлах, помогая вам избежать контактной сыпи, которая может быть полезной.
Если вы подозреваете аллергию на никель или у вас появилась сыпь неизвестного происхождения, обязательно обратитесь к врачу, который сможет поставить вам правильный диагноз.
Что такое никель?
Никель представляет собой серебристый металл, естественным образом присутствующий в окружающей среде. В смеси с другими металлами он часто используется в производстве ювелирных изделий, монет, ключей, сотовых телефонов, оправ для очков, кухонного оборудования из нержавеющей стали и многого другого.
Хотя у большинства людей нет проблем с этим элементом, у некоторых возникает аллергия, вызывающая множество неприятных симптомов. В таких случаях вам следует ограничить контакт с предметами на основе никеля.
- Брокколи с высоким содержанием никеля?
Более того, следовые количества никеля можно найти в некоторых продуктах, которые вы едите. Это также может вызвать аллергические реакции у людей, чувствительных к этому минералу.
Это также может вызвать аллергические реакции у людей, чувствительных к этому минералу.
Хорошей новостью является то, что большинство пищевых продуктов содержат следовые количества никеля, если они вообще есть. Но есть продукты с особенно высоким содержанием этого элемента. К ним относятся:
- Соя, бобы и овес
- Cocoa
- мука, рис и квиноа
- Blackberries
- Экзотические фрукты, такие как Lychees, Passufruit, OR Jambu Fruit
- Arugula, Peas, Asparagus
- Arugula, PEAS, ASPARAGUS
- Arugula, PEAS, ASPARAGUS
- , ASPARAGUS
- . Семена
- Чай
Тарелка с моллюсками
- 15 продуктов с высоким содержанием никеля, которых следует избегать
Если вы страдаете аллергией на никель, лучше избегать продуктов с высоким содержанием никеля. по возможности избежать неприятных симптомов. Никель не является элементом, который нам нужен в нашем рационе, поэтому даже те, у кого нет аллергии, могут захотеть выбирать продукты с низким содержанием никеля.
по возможности избежать неприятных симптомов. Никель не является элементом, который нам нужен в нашем рационе, поэтому даже те, у кого нет аллергии, могут захотеть выбирать продукты с низким содержанием никеля.
Это важно, так как если аллергия развилась, она необратима.
Пищевые продукты содержат никель по нескольким причинам. Во-первых, некоторые из них естественным образом содержат этот элемент из-за того, где они растут, например, какао.
- Шоколад с высоким содержанием никеля?
Другие продукты, особенно овощи, выращенные на ферме, поглощают никель из земли, в которой они выращиваются, или из пестицидов и удобрений, которыми пропитана земля. Некоторое количество никеля также может попасть в пищу, которую вы готовите в кастрюлях и сковородках. Итак, если у вас аллергия на никель, вы можете выбрать столовые приборы и кухонное оборудование, которые не сделаны из никеля.
Вы также можете убедиться, что потребляете в основном продукты, не содержащие никеля, или продукты с низким содержанием этого элемента, так как их много.
Некоторые из лучших продуктов с низким содержанием никеля включают:
- Фрукты: персики, груши, клубника, черника, бананы и ежевика.
- Овощи: болгарский перец, огурцы, баклажаны, капуста, цветная капуста и китайская капуста.
- Зерновые: макароны, белый рис, кукурузные хлопья и белый хлеб.
- Все виды мяса, кроме консервированных.
- Молочные продукты: молоко, йогурт, сливки, масло и сыр.
Как видите, существует множество продуктов, которые можно есть на диете с низким содержанием никеля. Также стоит отметить, что небольшое количество продуктов, содержащих умеренное количество никеля, все еще допустимо. Но всегда прислушивайтесь к своему организму и исключите продукты, которые ухудшают ваши симптомы.
Бок Чой с рисом
- В кофе много никеля?
Как узнать, нужно ли мне проверить уровень никеля?
Большинство людей с аллергией на никель испытывают кожные реакции, включая покраснение, раздражение, воспаление и сыпь. Обычно они возникают, когда ваша кожа вступает в контакт с предметами, содержащими никель. Но употребление продуктов, содержащих никель, также является причиной. В этих случаях симптомы могут идти еще дальше и включать:
Обычно они возникают, когда ваша кожа вступает в контакт с предметами, содержащими никель. Но употребление продуктов, содержащих никель, также является причиной. В этих случаях симптомы могут идти еще дальше и включать:
- Головную боль
- Боль в животе
- Проблемы с дыханием
- Хроническая усталость
- Воспаление
Кроме того, употребление продуктов, содержащих никель, натощак увеличивает тяжесть симптомов. Поэтому обязательно соблюдайте сбалансированную диету и избегайте продуктов с высоким содержанием никеля, если вы знаете, что страдаете аллергией на никель.
Опять же, большинству людей, не страдающих аллергией на никель, не нужно беспокоиться о приеме слишком большого количества никеля, если они соблюдают здоровую диету.
Продукты с высоким содержанием никеля по-прежнему являются отличным источником многих важных макроэлементов, витаминов и минералов. Поэтому они должны быть частью любой диеты, пусть даже в небольших количествах и нечасто.
Поэтому они должны быть частью любой диеты, пусть даже в небольших количествах и нечасто.
- Картофель с высоким содержанием никеля?
Какие существуют альтернативные способы проверки уровня никеля?
Чтобы проверить наличие аллергии на никель, вам необходимо пройти кожный тест у специалиста. Обычно тест просто включает проверку того, возникает ли у вас аллергическая реакция при контакте с никелем.
- Можно ли проверить уровень оксалатов дома?
Он также не показывает точно, сколько никеля находится в вашем организме, поскольку имеет значение любое его количество, если у вас аллергия. В результате на данный момент нет доступных вариантов домашнего тестирования. Поэтому вам нужно записаться на прием к врачу, если вы подозреваете, что у вас может быть аллергия на никель.
Существует несколько наборов для домашнего тестирования, которые могут помочь вам проверить уровень никеля на металлах и других предметах, таких как серьги и украшения. Если вы страдаете аллергией или чувствительностью к никелю, у вас также может возникнуть сыпь и инфекция в месте контакта с металлом.
Если вы страдаете аллергией или чувствительностью к никелю, у вас также может возникнуть сыпь и инфекция в месте контакта с металлом.
Таким образом, покупка такого набора для тестирования может быть хорошей идеей, чтобы избежать этой проблемы.
Аллергия на никель становится все более распространенной. В результате неудивительно, что многие люди хотят знать, есть ли варианты проверить уровень никеля в домашних условиях без посещения врача.
- Содержит ли авокадо высокое содержание никеля?
Несмотря на то, что есть способы проверить предметы и металлы на наличие никеля, самостоятельно провести тест в домашних условиях невозможно. Итак, если вы подозреваете аллергию на никель или у вас необъяснимые высыпания, проконсультируйтесь с врачом, чтобы поставить правильный диагноз.
Обнаружение катионов никеля в монетах
- Домашняя
- Обнаружение катионов никеля в монетах
Андрес Третьяков | Вт, 07. 05.2019 — 22:45
05.2019 — 22:45
Реакция хелатирования ионов никеля с органическим бидентатным лигандом диметилглиоксимом (DMG) 1 в щелочной аммиачной среде с образованием диметилглиоксима никеля, Ni(DMG) 2 , осадка красно-вишневого или малинового цвета известна с 1905, когда он был открыт русским химиком Львом Александровичем Чугаевым (см. рис. 1). Это был первый органический точечный реагент, использованный для обнаружения иона металла, поэтому ДМГ известен как реактив Чугаева. 2
The balanced ionic equation for this reaction:
Ni 2+ (aq) + 2C 4 H 8 N 2 O 2 (aq) → Ni (C 4 H 7 N 2 O 2 ) 2 (s) + 2H + (aq)
Рисунок 1: Строительное уравнение из строительства 9021.
Эта реакция до сих пор широко используется для обнаружения ионов металлического никеля из-за ее яркого окрашивания. Как качественные, так и гравиметрические определения никеля являются частью многих курсов химии. В реакции участвуют две молекулы диметилглиоксима, действующие как хелатирующие агенты для образования квадратно-плоского комплекса никеля с диметилглиоксимом . Эта реакция очень чувствительна и может использоваться в качестве подтверждающего теста на присутствие катионов никеля II даже в очень низких концентрациях.
Та же процедура может быть легко применена к металлическим предметам, которые регулярно соприкасаются с кожей, например, к монетам, украшениям, серьгам, оправам для очков, ремешкам для часов и т. д. для людей, страдающих повышенной чувствительностью кожи или дерматит называется Никелевый зуд .
Эта контактная аллергия или аллергический контактный дерматит (АКД) обычно обостряется при потоотделении.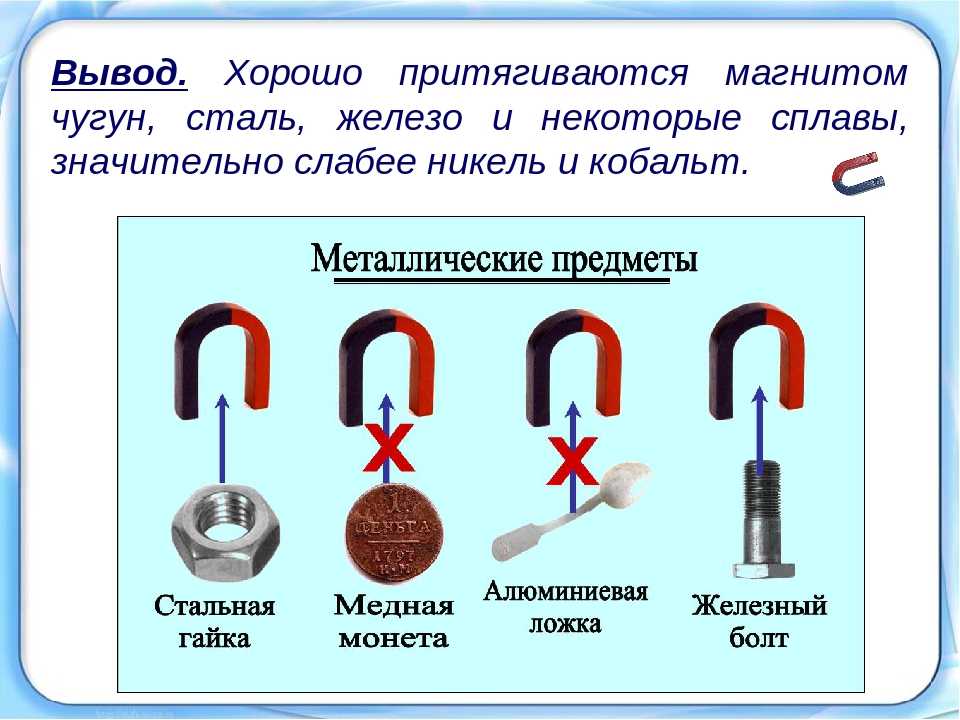 На коже, контактировавшей с металлом, появляется красная зудящая сыпь. Считается, что кислоты, присутствующие в поту, растворяют небольшое количество никеля, и именно высвобождение ионов никеля вызывает сенсибилизацию никеля, а ACD 4 может усугубить такие состояния, как кожная эритема, экзема и т. д. определенное количество выпущенных ионов вызовет реакцию. Например, сплавы, такие как многие нержавеющие стали, содержат никель, но не выделяют достаточного количества ионов никеля, чтобы вызвать чувствительность к никелю или реакции ACD никеля, если они уже чувствительны к никелю. Напротив, никелированные украшения выделяют огромное количество ионов никеля при контакте с потом с кожи и в результате ежедневного расчесывания, трения, истирания и т. д., особенно при длительном ношении.
На коже, контактировавшей с металлом, появляется красная зудящая сыпь. Считается, что кислоты, присутствующие в поту, растворяют небольшое количество никеля, и именно высвобождение ионов никеля вызывает сенсибилизацию никеля, а ACD 4 может усугубить такие состояния, как кожная эритема, экзема и т. д. определенное количество выпущенных ионов вызовет реакцию. Например, сплавы, такие как многие нержавеющие стали, содержат никель, но не выделяют достаточного количества ионов никеля, чтобы вызвать чувствительность к никелю или реакции ACD никеля, если они уже чувствительны к никелю. Напротив, никелированные украшения выделяют огромное количество ионов никеля при контакте с потом с кожи и в результате ежедневного расчесывания, трения, истирания и т. д., особенно при длительном ношении.
Неизвестно, почему у людей развивается аллергия на никель, и нет лекарства. Лучший способ предотвратить аллергическую реакцию — избегать контакта с продуктами, содержащими никель, и в этом посте мы покажем, как сделать дешевое и быстрое устройство для обнаружения никеля в домашних условиях или в лаборатории на основе реакции, описанной выше.
Видео о том, как проверить наличие никеля в различных монетах с помощью такого прибора, можно посмотреть ниже (без звука). 5
На видео показано добавление нескольких капель DMG, C 4 H 6 (NOH) 2 к разбавленному раствору сульфата никеля II с несколькими каплями раствора аммиака. Немедленно нерастворимое ярко-красное твердое вещество , называемое никель диметилглиоксим , Ni(C 4 H 8 N 2 O 2 ) 2 , выпадает в осадок из раствора. Вскоре после этого можно увидеть, как ватная палочка или ватная палочка, содержащая DMG и аммиак, трется о поверхность монеты. Если в монете присутствует никель, то ватная палочка становится красной.
Несмотря на то, что существуют коммерческие продукты для проверки металлов на наличие никеля 6 , гораздо более простую и дешевую версию можно изготовить дома или в лаборатории из легкодоступных бытовых ингредиентов. 7 Сначала возьмите несколько ватных палочек или ватных палочек и окуните их в раствор 1% диметилглиоксима (ДМГ) в этаноле (также подойдет водка) на 10 минут. ПРИМЕЧАНИЕ. DMG является легковоспламеняющимся раздражающим веществом, и его может быть трудно достать, но для изготовления большого запаса готовых шишек требуется очень небольшое количество (примерно 1 г). После того, как шишки пропитались не менее 10 минут, снимите их и дайте высохнуть на воздухе. После высыхания они готовы к использованию или могут храниться в герметичном контейнере с соответствующей маркировкой.
7 Сначала возьмите несколько ватных палочек или ватных палочек и окуните их в раствор 1% диметилглиоксима (ДМГ) в этаноле (также подойдет водка) на 10 минут. ПРИМЕЧАНИЕ. DMG является легковоспламеняющимся раздражающим веществом, и его может быть трудно достать, но для изготовления большого запаса готовых шишек требуется очень небольшое количество (примерно 1 г). После того, как шишки пропитались не менее 10 минут, снимите их и дайте высохнуть на воздухе. После высыхания они готовы к использованию или могут храниться в герметичном контейнере с соответствующей маркировкой.
Чтобы проверить наличие никеля в желаемом металлическом объекте, добавьте несколько капель разбавленного раствора аммиака (бытовой аммиак будет работать в зависимости от концентрации, более высокие концентрации дают более быстрые результаты), чтобы просто смочить кончик ватной палочки. Сначала очистите предмет влажной салфеткой и потрите наконечник о монету или предмет в течение минуты и наблюдайте, не появляется ли розово-красный цвет. Интенсивность цвета будет зависеть от того, сколько никеля присутствует или находится ли он в свободном доступе на поверхности объекта (темно-розово-красный, если он полностью сделан из никеля или никелирован), или светло-розовый, если он сплавлен с другими металлами. Интересно, что даже при плотном соединении в сплаве тест обнаружит, по крайней мере, некоторые из присутствующих катионов никеля. Монеты, сделанные из меди или цинка, не будут иметь красного цвета, но монеты/предметы из железа и стали могут давать ложноположительный результат, поскольку Fe 9Ионы 0215 2+ и Fe 3+ мешают обнаружению Ni 2+ с использованием ДМГ, поскольку в щелочных условиях он образует красно-коричневый комплекс гидроксида железа. Чтобы избежать этой ситуации, можно добавить несколько капель лимонной кислоты (лимонного сока), чтобы преобразовать комплекс железа в водорастворимый бесцветный комплекс. 8
Интенсивность цвета будет зависеть от того, сколько никеля присутствует или находится ли он в свободном доступе на поверхности объекта (темно-розово-красный, если он полностью сделан из никеля или никелирован), или светло-розовый, если он сплавлен с другими металлами. Интересно, что даже при плотном соединении в сплаве тест обнаружит, по крайней мере, некоторые из присутствующих катионов никеля. Монеты, сделанные из меди или цинка, не будут иметь красного цвета, но монеты/предметы из железа и стали могут давать ложноположительный результат, поскольку Fe 9Ионы 0215 2+ и Fe 3+ мешают обнаружению Ni 2+ с использованием ДМГ, поскольку в щелочных условиях он образует красно-коричневый комплекс гидроксида железа. Чтобы избежать этой ситуации, можно добавить несколько капель лимонной кислоты (лимонного сока), чтобы преобразовать комплекс железа в водорастворимый бесцветный комплекс. 8
Для получения отличной инфографики о составе британских монет и для использования в качестве сравнения см. The Metals in UK Coins от Compound Interest. 9 Энди Браннинг также создал аналогичный плакат для графики C&EN Periodic: композиции из монет США. 10
The Metals in UK Coins от Compound Interest. 9 Энди Браннинг также создал аналогичный плакат для графики C&EN Periodic: композиции из монет США. 10
Поскольку большая часть никеля на Земле находится в расплавленном железном ядре планеты, процент добываемого каждый год в основном поступает из космоса в виде железно-никелевых метеоритов миллионы лет назад. Металлические метеориты имеют содержание никеля от 5 до 35%, поэтому с помощью этой простой реакции можно отличить метеориты от других горных пород и образцов искусственного железа. 8
Для более глубокого анализа может быть получен контроль в виде монеты, которая, как известно, вообще не содержит металлического никеля. Во-вторых, можно приготовить стандартный раствор сульфата никеля II для визуального сравнения окрашенных испытуемых образцов с последующим колориметрическим анализом для определения концентрации никеля в каждом образце.
В заключение процедура показывает простой, удобный и дешевый способ для людей, страдающих от раздражения кожи, ограничить и/или устранить риски воздействия источников металлического никеля с помощью интересной классической химии.
УДЛИНЕНИЕ
Рис. 2: Игольчатые кристаллы Ni(DMG) 2 под 40-кратным увеличением
Капля воды, содержащая Ni(DMG) 2 , осадок помещали на предметное стекло микроскопа и исследовали. под микроскопом (см. рисунок 2). Наблюдались красные игольчатые кристаллы комплекса. Для получения более крупных кристаллов осадок растворяли в горячей разбавленной соляной кислоте и оставляли медленно испаряться. Через сутки появились длинные коричневые игольчатые кристаллы. При дроблении кристаллов с помощью стеклянной палочки наблюдался знакомый характерный красно-вишневый цвет (см. рис. 3).
Рисунок 3: измельченные кристаллы, демонстрирующие характерный блестящий красный цвет Ni (DMG) 2
Aknowledgements: I Хотел версию этого поста с советами, предложениями и конструктивными комментариями по его улучшению. Их опыт и поддержка бесценны для таких, как я, кто не публикует и не пишет научные статьи регулярно.
Ссылки
- Паспорт безопасности диметилглиоксима (DMG), созданный Global Safety Management Ink. (по состоянию на 05.05.19)
- Кауфман, Г.Б., Platinum Metal Rev., 1973, 17, (4).
- Гравиметрическое определение никеля, Truman State University CHEM 222 Lab Manual (по состоянию на 05.05.19)
- Быстрое и простое обнаружение ионов металлического никеля в монетах, канал YouTube andycapo123, опубликовано 25 апреля 2019 г. (по состоянию на 05 мая 2019 г.)
- Информационный бюллетень 1: Аллергический контактный дерматит на никель, Институт никеля. Июнь 2016 г. (по состоянию на 06.05.19)
- Набор можно купить на Amazon: https://www.amazon.co.uk/gp/product/B00EWUS86C/ref=ox_sc_act_title_6?smi… или в виде тест-полосок MQuant Nickel, продаваемых Merck
- DMG можно приобрести у поставщиков химикатов, но автор купил 10 г DMG 99% на Ebay за 6,50 фунтов стерлингов (около 8,50 долларов США). Достаточно, чтобы сделать сотни тестовых ватных палочек.

- Zamora, L.L., Zamora, S.L., Romero, M., Идентификация внеземных материалов, журнал Education in Chemistry, 9 марта 2015 г.
- The Metals in UK Coins, Andy Brunning, Compound Interest, 27 марта 2014 г. (по состоянию на 06.05.19)
- Периодическая графика: композиции монет США, Энди Браннинг, Chemical and Engineering News, Volume 94 Issue 28, 11 июля 2016 г. (по состоянию на 06.05.19)
Для получения дополнительной информации:
Brandl, Herbert, Trickkiste Chemie, Bayerischer Schulbuch Verlag, München, 1998.
Emsley, John, Nature’s Building Blocks An A-Z guide to the elements, Oxford University Press, 2003.
Концепции:
Химические изменения
Коллекция:
Потребительская химия
Демонстрации
Элементы
Охват
Реакции
63
3 9
Общая безопасность
Для лабораторных работ: См. Руководство ACS по безопасности химических лабораторий в средних школах (2016 г. ).
).
Для демонстраций: Пожалуйста, обратитесь к Руководству по безопасности химических демонстраций отдела химического образования ACS.
Прочие ресурсы по безопасности
RAMP: распознавать опасности; Оценить риски опасностей; Свести к минимуму риски опасностей; Подготовьтесь к чрезвычайным ситуациям
НГСС
Научная практика: получение, оценка и передача информации
Участие в споре на основе доказательств в 9–12 основывается на опыте K–8 и переходит к использованию соответствующих и достаточных доказательств и научных рассуждений для защиты и критики утверждений и объяснений о естественных и созданных мирах. Аргументы могут также исходить из текущих научных или исторических эпизодов в науке.
Резюме:
Участие в аргументации на основе доказательств в 9–12 основывается на опыте K–8 и переходит к использованию соответствующих и достаточных доказательств и научных рассуждений для защиты и критики утверждений и объяснений о естественных и созданных мирах. Аргументы могут также исходить из текущих научных или исторических эпизодов в науке.
Аргументы могут также исходить из текущих научных или исторических эпизодов в науке.
Оцените утверждения, доказательства и обоснование принятых в настоящее время объяснений или решений, чтобы определить достоинства аргументов.
Граница оценки:
Уточнение:
Научная практика: планирование и проведение исследований
Планирование и проведение расследований в 9-12 базируется на опыте K-8 и включает в себя исследования, которые предоставляют доказательства и тестируют концептуальные, математические, физические и эмпирические модели.
Резюме:
Планирование и проведение расследований в 9-12 основывается на опыте K-8 и включает в себя исследования, которые предоставляют доказательства и проверяют концептуальные, математические, физические и эмпирические модели. Планируйте и проводите расследование индивидуально и совместно, чтобы получить данные, которые послужат основой для доказательства, а в плане: определите типы, количество и точность данных, необходимых для получения надежных измерений, и учтите ограничения точности данных ( например, количество испытаний, стоимость, риск, время) и соответствующим образом уточнить план.
Граница оценки:
Уточнение:
Химические реакции HS-PS1-2
Учащиеся, демонстрирующие понимание, могут составить и пересмотреть объяснение результата простой химической реакции, основанное на самых удаленных электронных состояниях атомов, тенденциях в периодической таблице и знании закономерностей химических свойств.
*Более подробную информацию обо всех DCI для HS-PS1 можно найти на https://www.nextgenscience.org/dci-arrangement/hs-ps1-matter-and-its-interactions, а также дополнительные ресурсы на https://www. .nextgenscience.org.
Резюме:
Учащиеся, демонстрирующие понимание, могут построить и пересмотреть объяснение результата простой химической реакции, основанное на самых удаленных электронных состояниях атомов, тенденциях в периодической таблице и знании закономерностей химических свойств.
Граница оценки:
Оценка ограничивается химическими реакциями с участием элементов основных групп и реакциями горения.
Уточнение:
Примеры химических реакций могут включать реакцию натрия и хлора, углерода и кислорода или углерода и водорода.
Никель: спрятан у всех на виду
Неизвестный источник прочности
Люди используют никель примерно столько же, сколько производят изделия из металла. Относительно распространенный элемент — 24-й по распространенности на Земле — никель встречается в месторождениях металлических руд по всему миру. Древние ценили эти руды как источник металлов с желаемыми свойствами, такими как прочность и гибкость, и использовали их для изготовления всего, от монет до ножей, топоров и оружия. Однако желаемые свойства этих металлических сплавов часто объяснялись наличием меди или железа. На самом деле археологи определили по древним металлическим артефактам, что «железо» ранних обществ, использующих металлы, на самом деле представляло собой смесь, содержащую от 5 до 26 процентов никеля.
Задолго до того, как был выделен никель, древние китайцы разработали материал под названием пайтунг (также называемый пактонг или тутенаг), который ценился за его серебристый блеск и прочность. Согласно китайским рукописям, пайтунг использовался еще в третьем веке нашей эры в оружии, монетах и произведениях искусства. Считается, что пайтунг содержал в основном медь и никель с небольшим количеством цинка и олова.
В Европе никель также использовался в сплавах без ведома кузнецов и плавильщиков того времени. Никелевые сплавы использовались для производства пластинчатых и кольчужных доспехов в Средние века, а относительное изобилие никельсодержащих руд делало их недорогим способом придать прекрасный блеск монетам. Но только после открытия никеля в 1750 году эта обычная металлическая добавка была выделена и изучена.
Металлический дьявол
Саксония, Германия
Горнодобывающая деятельность в Саксонии в Германии в конечном итоге привела к открытию никеля. В 1750 году медеплавильщики в Саксонии обнаружили своеобразную медную руду, которая была немного светлее, чем обычно. При обработке и очистке эта руда давала необычную форму меди, которая была особенно яркой и серебристой. Было также обнаружено, что эта странная форма меди имеет совершенно другие свойства материала. Он был чрезвычайно твердым, и его нельзя было сделать ковким, несмотря на неоднократные попытки плавильщиков. Новый металл стал известен как Купферникель, что примерно переводится как «медь с дьяволом внутри». Состав этого сплава на самом деле был очень похож на пайтунг Древнего Китая.
В 1750 году медеплавильщики в Саксонии обнаружили своеобразную медную руду, которая была немного светлее, чем обычно. При обработке и очистке эта руда давала необычную форму меди, которая была особенно яркой и серебристой. Было также обнаружено, что эта странная форма меди имеет совершенно другие свойства материала. Он был чрезвычайно твердым, и его нельзя было сделать ковким, несмотря на неоднократные попытки плавильщиков. Новый металл стал известен как Купферникель, что примерно переводится как «медь с дьяволом внутри». Состав этого сплава на самом деле был очень похож на пайтунг Древнего Китая.
Никель — загадочный компонент купферникеля, придавший ему эти отличительные свойства, — был наконец «обнаружен» и выделен из минерала под названием никколит шведским минералогом бароном Акселем Фредериком Кронштедтом в 1751 году. Барон, как и саксонские плавильщики, сначала ожидал извлечь медь из этого минерала, но вместо этого его процедура дала прочный белый металл. Не имея возможности сравнить материал с каким-либо известным металлом, барон решил, что он выделил загадочный компонент купферникеля, и назвал новый металл «никель» в честь самого Дьявола, «Старого Ника».
Никель и димед
Как современные, так и древние общества использовали никель для придания блеска и уменьшения веса монет, а также для повышения их устойчивости к коррозии и износу. Но практика добавления никеля к сплавам монет стала более распространенной, поскольку страны начали переходить к системам плавающего обменного курса, в которых стоимость физического материала в монете больше не должна была соответствовать ее номинальной стоимости. Поскольку обмен валюты перестал быть привязанным к золотым и серебряным стандартам, Швейцария стала первой из многих современных стран, которая начала использовать никель в монетах. Первая монета из чистого никеля была выпущена Швейцарией в 1881 году, а Австрия и Венгрия последовали ее примеру в 189 году.3.
В конце 1850-х годов Соединенные Штаты добавили никель в свои монеты в пенни и в пять центов, которые ранее содержали в основном медь и цинк (бронзу). Слово «никель» стало популярным термином для самой пятицентовой монеты, несмотря на то, что большая часть монеты была медной (никелевая монета США 1800-х годов содержала 75 процентов меди и 25 процентов никеля). Монета пользовалась большим спросом, так как это был удобный номинал для многих предметов повседневного обихода, таких как пиво и сигары. Появление игровых автоматов и повсеместное распространение никеля в автобусах и метро также способствовало росту популярности этой монеты. Предполагается, что к 1958 Соединенные Штаты выпустили более 4 миллиардов пятицентовых монет.
Монета пользовалась большим спросом, так как это был удобный номинал для многих предметов повседневного обихода, таких как пиво и сигары. Появление игровых автоматов и повсеместное распространение никеля в автобусах и метро также способствовало росту популярности этой монеты. Предполагается, что к 1958 Соединенные Штаты выпустили более 4 миллиардов пятицентовых монет.
От метеоров к машинам
Даже через столетие после того, как был выделен никель, ученые и инженеры не в полной мере использовали его уникальные свойства. Никель — это переходный металл, который образует сплавы с множеством других переходных металлов, таких как медь, цинк, железо, серебро, кадмий и хром. Он одновременно прочен — сопротивляется разрушению при высоких нагрузках — и пластичен — скорее изгибается, чем трескается под нагрузкой. Это ценное сочетание свойств. Инженеры ищут эту комбинацию свойств при проектировании конструкций, таких как мосты, которые должны выдерживать большие нагрузки, но при этом изгибаться под давлением, а не трескаться.
Рассказы о таких чудодейственных материалах прошли через историю. Лезвия легендарных мечей древнего Дамаска и Аравии были широко известны своей чрезвычайной прочностью и твердостью. Говорят, что святые камни, такие как черный камень Каабы в Мекке, обладают магическими свойствами, вероятно, магнетизмом. Это знаменитое оружие и святые реликвии состоят из железа, упавшего с неба метеорами. Это метрическое железо часто содержит большое количество никеля. Древние оружейники, изготавливавшие из него свои клинки, наткнулись на примитивный, высокопрочный, устойчивый к ржавчине сплав из нержавеющей стали. Пройдут столетия, прежде чем наука, стоящая за этими магическими материалами, будет объяснена.
В 1700-х годах, когда промышленная революция зародилась сначала в Англии, а затем в континентальной Европе и Соединенных Штатах, развитие промышленного оборудования и, в частности, паровых двигателей породило поиск более прочных материалов, чем те, которые доступны в настоящее время. Ранние ученые-материаловеды разработали стальные сплавы, чтобы удовлетворить эту потребность. Сталь производится, когда железо соединяется с небольшим количеством углерода, что помогает стабилизировать и укрепить кристаллическую структуру железа. Добавление небольших количеств других элементов, таких как цинк, хром и никель, повышает прочность, пластичность, коррозионную стойкость и качество отделки стали.
Ранние ученые-материаловеды разработали стальные сплавы, чтобы удовлетворить эту потребность. Сталь производится, когда железо соединяется с небольшим количеством углерода, что помогает стабилизировать и укрепить кристаллическую структуру железа. Добавление небольших количеств других элементов, таких как цинк, хром и никель, повышает прочность, пластичность, коррозионную стойкость и качество отделки стали.
Спустя полвека после открытия никеля Майкл Фарадей, также известный своим открытием электромагнитной индукции и закона Фарадея, лежащего в основе современной теории поля, впервые предложил добавлять никель в сталь для улучшения ее свойств. В письме профессору де ла Риву из Королевского института в 1820 году он писал: «Нас побудила популярная идея о том, что метеоритное железо не ржавеет, попробовать влияние никеля на сталь и железо». Несмотря на первоначальные неудачи, Фарадей смог успешно сплавить небольшое количество никеля со сталью, получив материалы, которые были более прочными, но при этом податливыми и пригодными для обработки, как обычная сталь. Работа, продолженная швейцарским металлургом Дж. К. Фишером в 1824 году, привела к успешной имитации метеоритного железа.
Работа, продолженная швейцарским металлургом Дж. К. Фишером в 1824 году, привела к успешной имитации метеоритного железа.
Эти ранние открытия заложили основу для создания передовых нержавеющих и конструкционных сталей из сплавов с повышенной коррозионной стойкостью и прочностью. Стальная броня, усиленная никелем, вскоре стала использоваться на военных кораблях в середине-конце 1800-х годов. Исследования Майкла Фарадея в области электрохимии различных металлов — их способности взаимодействовать с электрическими токами — расширили использование никеля. К 1840-м годам металлурги смогли наносить никель на другие металлические поверхности, используя электрический ток для притягивания растворенных солей никеля и ионов никеля к поверхности металлических электродов. Эти покрытия обеспечили износостойкость и устойчивость к ржавчине для многих продуктов, от кухонной утвари до сантехники.
Раздувание пламени войны
Во время Первой мировой войны стоимость никеля резко возросла из-за нового спроса на высокопрочную нержавеющую сталь для оружия, боеприпасов и транспортных средств. Никель теперь был не только важным компонентом валюты, но и ценным природным ресурсом, который искали все воюющие группировки. В 1916 году немецкая подводная лодка рисковала жизнью, пытаясь прорвать британскую блокаду, чтобы получить небольшой груз канадского никеля. Успешная миссия отмечалась так же, как и традиционная военная победа; такова была ценность и важность никеля для немецкой военной машины. На пике военного производства Канада, главный в мире источник никеля, произвела около 92 миллиона фунтов никеля в год.
Никель теперь был не только важным компонентом валюты, но и ценным природным ресурсом, который искали все воюющие группировки. В 1916 году немецкая подводная лодка рисковала жизнью, пытаясь прорвать британскую блокаду, чтобы получить небольшой груз канадского никеля. Успешная миссия отмечалась так же, как и традиционная военная победа; такова была ценность и важность никеля для немецкой военной машины. На пике военного производства Канада, главный в мире источник никеля, произвела около 92 миллиона фунтов никеля в год.
Перемирие, а затем Великая депрессия заставили никелевую промышленность на мгновение погрузиться в пропасть между мировыми войнами. Производство военной техники резко сократилось, поскольку промышленный мир переориентировал свои усилия на потребительские товары. Однако достижения в области двигателей внутреннего сгорания в 1930-х годах помогли сохранить высокий спрос на определенные никелевые стали, желательные из-за их способности противостоять разрушению при высоких температурах. Это свойство имело решающее значение для таких деталей, как головки цилиндров и поршни, которые подвергаются взрывному давлению при очень высоких температурах.
Это свойство имело решающее значение для таких деталей, как головки цилиндров и поршни, которые подвергаются взрывному давлению при очень высоких температурах.
Начало Второй мировой войны снова увеличило спрос на сталь и никель. Во время конфликта производство никелевых сплавов сравнялось с объемом производства за предыдущие 54 года. Канада совместно с британским правительством фактически регулировала мировой рынок никеля во время Второй мировой войны и даже наложила ограничения на его использование в товарах второстепенного потребления. Это сильно ограничило количество никеля, доступного державам Оси, и в результате месторождения никелевой руды вскоре стали стратегической проблемой для немцев. Были начаты военные действия по взятию никелевых складов под контроль Германии. Никелевый рудник Петсамо в Финляндии, ранее остановленный вторгшейся советской армией, был захвачен немцами в 1940 и стал основным источником никеля для упрочнения стали во время войны с Германией.
Самолеты, реактивные двигатели и не только
Биплан братьев Райт
В 1903 году Орвилл и Уилбур Райт совершили транспортную революцию, подняв первый в своем роде самоходный биплан в Киттихоке, Северная Каролина. Первая мировая война ускорила разработку самолетов с двигателями, но преодолеть инженерные барьеры было бы невозможно без разработки новых аэрокосмических материалов для конструкционных компонентов и компонентов двигателей. Для снижения нагрузки на винтовые двигатели, увеличения скорости и повышения маневренности конструкции самолетов требовали высокопрочных и легких сплавов. Высокие скорости вращения и температуры авиационных двигателей также зависели от сплавов, которые могли противостоять деформации и разрушению при высоких температурах с минимальным дополнительным весом. Алюминиевые сплавы с добавками никеля и традиционные никелевые стали удовлетворили эту потребность.
Первая мировая война ускорила разработку самолетов с двигателями, но преодолеть инженерные барьеры было бы невозможно без разработки новых аэрокосмических материалов для конструкционных компонентов и компонентов двигателей. Для снижения нагрузки на винтовые двигатели, увеличения скорости и повышения маневренности конструкции самолетов требовали высокопрочных и легких сплавов. Высокие скорости вращения и температуры авиационных двигателей также зависели от сплавов, которые могли противостоять деформации и разрушению при высоких температурах с минимальным дополнительным весом. Алюминиевые сплавы с добавками никеля и традиционные никелевые стали удовлетворили эту потребность.
Новые достижения в скорости и мощности были достигнуты благодаря разработке первых реактивных двигателей во время Второй мировой войны и в 1950-х годах. Эти новые двигатели создавали струи газа под высоким давлением, используя быстро вращающиеся турбины для сжатия воздуха и выброса его через выхлопные сопла. Быстро вращающиеся турбины достигли высоких температур и напряжений, и снова потребовались новые металлические сплавы, чтобы противостоять этим силам. Никель использовался в качестве упрочняющего агента во многих из этих сплавов. Подобные потребности в стойкости к нагрузкам и температурам побудили использовать никельсодержащие сплавы в растущей космической гонке. К ракетным двигателям предъявляются те же технические требования, что и к реактивным двигателям, из-за высокой температуры и давления выхлопных газов, и они также должны выдерживать экстремальные вибрации, вызванные сгоранием ракетного топлива. Ранняя космическая промышленность использовала никель в сочетании с другими высокопрочными материалами, такими как титан, для создания новых классов суперсплавов, способных выдерживать турбулентность космического полета.
Быстро вращающиеся турбины достигли высоких температур и напряжений, и снова потребовались новые металлические сплавы, чтобы противостоять этим силам. Никель использовался в качестве упрочняющего агента во многих из этих сплавов. Подобные потребности в стойкости к нагрузкам и температурам побудили использовать никельсодержащие сплавы в растущей космической гонке. К ракетным двигателям предъявляются те же технические требования, что и к реактивным двигателям, из-за высокой температуры и давления выхлопных газов, и они также должны выдерживать экстремальные вибрации, вызванные сгоранием ракетного топлива. Ранняя космическая промышленность использовала никель в сочетании с другими высокопрочными материалами, такими как титан, для создания новых классов суперсплавов, способных выдерживать турбулентность космического полета.
Никель Сегодня
Недавние исследования показали, что обработка и рафинирование никеля могут иметь вредные последствия для здоровья. Исследования, проведенные в 1960-х годах, показали ранние признаки того, что соединения никеля, такие как карбонил никеля, могут вызывать опухоли легких у лабораторных крыс. Более поздние исследования, проведенные в 1980-х годах Агентством по охране окружающей среды США (EPA), показали, что длительное воздействие высоких концентраций пыли никелевых заводов, карбонила никеля или субсульфида никеля — прямых побочных продуктов рафинирования никеля и обработки металлов — может вызывать рак. Также было обнаружено, что вдыхание никельсодержащих паров при сварке нержавеющей стали связано с повышенным риском развития рака. Это привело к принятию федеральных норм, ограничивающих количество определенных соединений никеля, допустимых на рабочем месте и в окружающей среде.
Более поздние исследования, проведенные в 1980-х годах Агентством по охране окружающей среды США (EPA), показали, что длительное воздействие высоких концентраций пыли никелевых заводов, карбонила никеля или субсульфида никеля — прямых побочных продуктов рафинирования никеля и обработки металлов — может вызывать рак. Также было обнаружено, что вдыхание никельсодержащих паров при сварке нержавеющей стали связано с повышенным риском развития рака. Это привело к принятию федеральных норм, ограничивающих количество определенных соединений никеля, допустимых на рабочем месте и в окружающей среде.
При вдыхании некоторых форм при высоких концентрациях в течение достаточно длительного периода времени никель действительно является канцерогенным для человека. Современные методы промышленной гигиены помогли обуздать эти осложнения для здоровья, вызванные никелем.
На сегодняшний день наиболее распространенным воздействием никеля на здоровье является аллергическая реакция. Некоторые люди генетически предрасположены к чувствительности к никелю, если они достаточно часто контактируют с металлом. После сенсибилизации в месте контакта может возникнуть дерматит — аллергическая реакция на коже, вызывающая сыпь и, в крайних случаях, приступы астмы. По оценкам, от 5 до 10 процентов населения подвержены аллергии на никель.
После сенсибилизации в месте контакта может возникнуть дерматит — аллергическая реакция на коже, вызывающая сыпь и, в крайних случаях, приступы астмы. По оценкам, от 5 до 10 процентов населения подвержены аллергии на никель.
Хотя никель в основном используется в сталелитейной промышленности для усиления и повышения коррозионной стойкости высококачественных сталей, он нашел применение во множестве предметов повседневного обихода. К никельсодержащим предметам домашнего обихода относятся смесители, кухонная утварь, бытовая техника, аккумуляторные батареи (никель-кадмиевые или никель-кадмиевые), украшения и, конечно же, монеты. Подобно древним, большинство из нас, вероятно, используют изделия из никеля, даже не подозревая об этом.
Источники включают:
— Агентство регистрации токсичных веществ и заболеваний (ATSDR). 1997. Токсикологический профиль никеля. Атланта, Джорджия: Министерство здравоохранения и социальных служб США, Служба общественного здравоохранения.
— Эйчисон, Лесли. История металлов. Лондон: MacDonald and Evans Ltd., 1960.
— Энциклопедия токсикологии. изд. Филип Векслер. Бостон: Academic Press, 1998.
-Gmelins Handbuch der Inorganischen Chemie. Берлин: Springer-Verlag, 1924.
— Ховард-Уайт, Ф. Б. Никель: исторический обзор. Нью-Йорк: D. Van Nostrand Company, Inc., 1963.
— Джон Харт, Холдрен, Шнайдер и Ширли. Токсичные вещества от А до Я: Путеводитель по ежедневным опасностям загрязнения. Беркли, Калифорния: University of California Press, 1991.
-Клаасен, Кертис Д. Карасетт и Токсикология Доулла: фундаментальная наука о ядах. Нью-Йорк: McGraw-Hill, 2001.
-Нриагу, Джером О. Никель в окружающей среде. New York: Wiley, 1980.
Питер Остендорп
Центр наук об окружающей среде и гигиене
Стажер по написанию научных статей
Производители никеля | Поставщики никеля
Список поставщиков никеля
Клиенты покупают никель, чтобы помочь им в широком диапазоне применений, таких как покрытие изделий, химическое никелирование, создание металлических сплавов и изготовление изделий. Кроме того, люди могут использовать никель для получения чистой питьевой воды, электроэнергии, тепла и освещения.
Кроме того, люди могут использовать никель для получения чистой питьевой воды, электроэнергии, тепла и освещения.
Поставщики продают никель различным отраслям, таким как военная и оборонная промышленность, электроника, чеканка монет, продукты питания и напитки, аэрокосмическая промышленность, судостроение, архитектура, химия и промышленное производство. Кроме того, некоторые ювелиры используют никель в своих украшениях, но обычно они делают это только с недорогими украшениями, потому что у некоторых людей есть аллергия на никель.
Изделия из никеля – Metalmen
История
Впервые выделенный и идентифицированный как химический элемент в 1751 году, этот серебристо-белый металл был обнаружен в инструментах, датируемых 3500 г. до н.э. Археологи нашли эти древние инструменты, содержащие как минимум 2% никеля, в руинах, расположенных на территории современной Сирии.
Китайские рукописи подтверждают предположение, что китайцы использовали мельхиор (медно-никелевый или никель-медный), по крайней мере, где-то между 1700 и 1400 годами до нашей эры. В то время этот сплав называли «белой медью» или байтунгом. Позднее, примерно в 109 г.5 г. н.э. древний китайский ученый Хо Вэй записал процесс изготовления мельхиора.
В то время этот сплав называли «белой медью» или байтунгом. Позднее, примерно в 109 г.5 г. н.э. древний китайский ученый Хо Вэй записал процесс изготовления мельхиора.
Другим древним обществом, использовавшим никель, было эллинистическое общество. Между 180 г. до н.э. и 170 г. до н.э. ряд греко-бактрийских царей (Агафокл, Панталеон и Евтидем II) чеканили монеты, состоящие примерно из 20% никеля. Некоторые эксперты считают, что эти короли, правившие в Средней Азии, импортировали свой никелевый материал для монет из Китая. Это, однако, не то, что мы знаем окончательно.
Никель назван в честь озорного духа из немецкой мифологии, которого также звали Никель (как и Старый Ник). Человек, который придумал это название, шведский химик Аксель Кронштедт, получил эту идею от названия никелевой руды, которую мы теперь называем никелином или никколитом. Во времена Кронштедта эту руду называли купферникелем. Купфер означает медь, а никель относится к спрайту, никелю. Средневековые немецкие горняки, которые столкнулись с ним во время добычи меди в Рудных горах, дали ему такое название, потому что презирали его.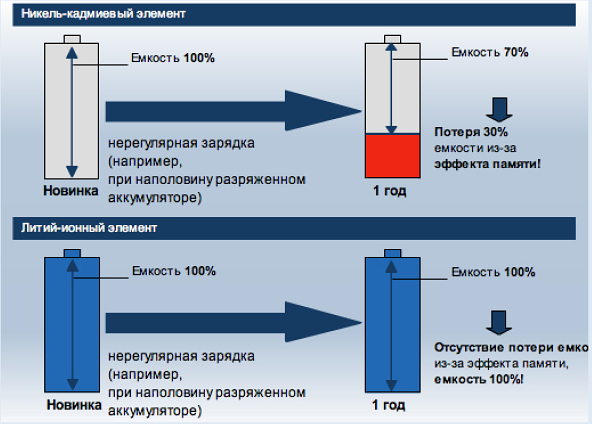 Шахтеры презирали это, потому что это не только затрудняло добычу меди, но и вызывало у них тошноту. Оказывается, им стало плохо, потому что в руде был мышьяк. Когда Кронштедт выделил никель из этой руды в 1751 году, он просто отбросил куфро.
Шахтеры презирали это, потому что это не только затрудняло добычу меди, но и вызывало у них тошноту. Оказывается, им стало плохо, потому что в руде был мышьяк. Когда Кронштедт выделил никель из этой руды в 1751 году, он просто отбросил куфро.
В 1800-х годах люди во всем мире начали использовать недавно выделенный металлический никель для покрытия и производства монет. Одним из первых никелевых сплавов, специально созданных металлургами, был никелевый сплав, который они назвали «мельхиор». Примечание: нейзильбер не содержит серебра, а содержит никель, цинк и медь. В 1866 году американское правительство отчеканило свои первые монеты на основе никеля (75% меди, 25% никеля). Они обратились к никелевым монетам, потому что никель дешев, а после Гражданской войны у правительства не было средств на изготовление монет из драгоценных металлов. Монеты, которые предшествовали никелевым монетам, такие как монеты в полцента, были сделаны из гораздо более тяжелых и дорогих материалов, таких как серебро. В 1881 году швейцарское правительство сделало еще один шаг вперед в чеканке никелевых монет, отчеканив свои первые монеты из чистого никеля.
В 1881 году швейцарское правительство сделало еще один шаг вперед в чеканке никелевых монет, отчеканив свои первые монеты из чистого никеля.
Помимо создания монет, одной из самых важных ролей никеля в 20-м веке было его использование в качестве дополнения к нержавеющей стали. Металлурги обнаружили, что добавление никеля в этот сплав может значительно повысить его коррозионную стойкость и термостойкость.
Сегодня никель является популярным металлом, который производители используют в самых разных условиях, от химических заводов до кухни. Кроме того, никель является составной частью монетной валюты многих стран и политических союзов, в том числе пятицентовой монеты Соединенных Штатов и монеты евро Европейского Союза (ЕС).
Производственный процесс
1. Добыча
Прежде чем поставщики никеля смогут очистить элемент и превратить его в пригодные для использования детали и изделия, кто-то должен извлечь его из земли. Горняки находят залежи никелевой руды в двух основных формах: латериты и залежи магматических сульфидов. Первая руда состоит в основном из гарниерита и никельсодержащего лимонита, а вторая в основном состоит из рудного минерала, называемого пентландитом.
Первая руда состоит в основном из гарниерита и никельсодержащего лимонита, а вторая в основном состоит из рудного минерала, называемого пентландитом.
2. Добывающая металлургия
Чтобы получить никель из этих месторождений, переработчики подвергают их процессу обработки никелевой руды, называемому добывающей металлургией, во время которого сырье извлекается и очищается в более очищенную форму.
Два наиболее распространенных метода металлургии включают пирометаллургическое извлечение и гидрометаллургию. С помощью подобных методов производители могут создавать соединения никеля, такие как гидроксиды никеля.
Одной из частей добывающей металлургии является стадия обжига и восстановления . Используя обычные методы обжига и восстановления, можно получить рафинированный никель с чистотой более 75%.
Однако для еще большей чистоты поставщики никеля могут продолжать перерабатывать никель. Одним из распространенных процессов является Процесс Монда , в ходе которого оксиды никеля превращаются в никель с чистотой 99%. В этом процессе используется монооксид углерода, поэтому любой металл никеля, который он очищает, превращается в соединение никеля, называемое карбонильным никелем.
В этом процессе используется монооксид углерода, поэтому любой металл никеля, который он очищает, превращается в соединение никеля, называемое карбонильным никелем.
3. Изготовление
После рафинирования поставщики никеля могут подвергать никель любому количеству производственных процессов для достижения своих целей. Наиболее распространенные методы включают химическое никелирование, холодное волочение и экструзию.
Химическое никелирование — это процесс химического восстановления. Целью этого процесса является осаждение металлического никеля на поверхность без использования электроэнергии. Для этого производители помещают никель в водный раствор, содержащий химический восстановитель. Оказавшись в водном растворе, никель и раствор вступают в реакцию, вызывая каталитическое восстановление. Каталитическое восстановление вызывает осаждение ионов никеля на поверхности продукта. Химическое никелирование позволяет получить очень однородное по толщине, форме и размеру никелирование.
Холодное волочение довольно просто. Во время этого процесса без подачи тепла производители проталкивают никелевую проволоку или трубку через ряд все более мелких штампов, чтобы уменьшить ее диаметр.
Экструзия — это редкий способ обработки никеля производителями. Если они используют его, то во время этого процесса они плавят или пропускают никель через матрицу для производства стержней, листов, стержней и труб.
Сплавы
Для получения соединений и сплавов никеля, подходящих для различных применений, поставщики никелевой руды часто комбинируют никель с другими элементами, такими как медь, алюминий, титан и хром. Несколько распространенных сплавов включают никель 200, нержавеющую сталь, ковар, инвар, монель, нихром, инконель и различные сплавы Hastelloy.
Никель 200 на 99,6% состоит из никеля, но в него добавлен ряд различных элементов, включая медь, железо, углерод, кремний, серу, магний и другие.
Нержавеющая сталь , состоящая в основном из железа, а также 18% хрома и 8% никеля, является наиболее часто используемым элементом из никелевого сплава.
Ковар представляет собой железоникелевый сплав, в основном состоящий из никеля и кобальта, сопровождаемый следовыми количествами меди, марганца и кремния. Термин «ковар» может также относиться к большой группе никелевых сплавов, которые совместимы с характеристиками теплового расширения боросиликатного стекла. Такие никелевые сплавы часто используются в качестве проводников с гальваническим покрытием в таких частях систем, как рентгеновские трубки и вакуумные трубки.
Инвар , также известный под своим химическим названием 64FeNi (или FeNi36), представляет собой однофазный сплав из никеля и железа. Часовщики и производители научных инструментов используют инвар в качестве компонента своей продукции, потому что он обладает такой высокой стабильностью размеров.
Монель — это общее название группы никелевых сплавов, которые примерно на 67% состоят из никеля и в остальном состоят из железа, меди и незначительных количеств других элементов. Монель обладает невероятной коррозионной стойкостью и поэтому используется для изготовления компонентов морского оборудования, таких как клапаны забортной воды, валы насосов и троллинговый трос.
Нихромовые сплавы или никель-хромовые сплавы представляют собой семейство суперсплавов, состоящих, помимо никеля, в основном из железа и хрома. Нихромовые сплавы обладают высокой устойчивостью к ползучести и высокой механической прочностью. Чаще всего производители никеля используют нихром для создания резистивной проволоки и нагревательных элементов, но нихром также находит применение, среди прочего, в испытаниях на пламя, стоматологии (пломбы) и фейерверках.
Инконель — еще один суперсплав или сплав с высокими эксплуатационными характеристиками, который входит в семейство сплавов. Известно, что инконель обладает необычайно высокой термостойкостью. Этот сплав состоит в основном из никеля, молибдена, ниобия и хрома, а также небольшого количества алюминия, бора, углерода, кобальта, меди, марганца, фосфора, кремния, серы и титана. Сплавы семейства Inconel хорошо подходят для экстремальных условий, где они обычно используются в качестве уплотнений, камер сгорания, лопаток газовых турбин, ядерных водо-водяных реакторов, валов электрических погружных скважинных насосов, клапанов давления и т. д.
д.
Hastelloys — это еще более суперсплавы. Они сделаны в основном из никеля, а также небольшого количества других материалов, таких как хром, молибден и т. д. Hastelloys наиболее известны своей высокой термостойкостью, отличной термостойкостью и способностью работать даже при самых больших нагрузках. Во время таких выступлений они не ямчат, не трескаются и не окисляются.
Производимая продукция
Поставщики никеля обычно имеют в наличии ряд основных никелевых изделий, включая никелевые слитки, никелевые стержни, никелевые пластины, никелевые листы и, иногда, никелевые трубки. Покупатели могут покупать эти продукты, думая, что они являются готовыми продуктами, но чаще всего они покупают их, чтобы помочь себе производить больше продуктов. Примеры включают следующее:
Производители электроники используют никель для изготовления таких продуктов, как микроволновые лампы, перезаряжаемые батареи, микрофонные капсюли и даже некоторые типы лампочек. В военной и оборонной промышленности производители используют никель и никелевые сплавы для изготовления, среди прочего, корпусов ракетных двигателей и компонентов ракет.
В военной и оборонной промышленности производители используют никель и никелевые сплавы для изготовления, среди прочего, корпусов ракетных двигателей и компонентов ракет.
Другие никелевые изделия, которые производят производители, включают медицинское оборудование, компоненты клапанов, детали фитингов, кастрюли и сковородки, оборудование для пищевой промышленности, кухонные раковины, струны для электрогитар, монеты и изделия из нержавеющей стали.
Преимущества
Есть много причин любить никель. Во-первых, никель и никелевые изделия обычно служат от 25 до 35 лет. Изделия из никеля с таким длительным сроком службы являются отличным вложением средств. Во-вторых, никель обычно предлагает более широкий диапазон термостойкости, большую ударную вязкость и лучшую коррозионную стойкость, чем другие металлические материалы. Кроме того, никель обладает уникальными магнитными и электронными свойствами. Эти свойства настолько уникальны, что в некоторых случаях никель является единственным подходящим материалом. Кроме того, никель устойчив. Его устойчивость обусловлена его энергоэффективностью, низкой стоимостью и возможностью вторичной переработки. Производители и потребители перерабатывают никель с такой последовательностью и в таких больших объемах, что, по мнению экспертов, более половины циркулирующих сегодня изделий из никелевой нержавеющей стали содержат переработанный никелевый материал.
Кроме того, никель устойчив. Его устойчивость обусловлена его энергоэффективностью, низкой стоимостью и возможностью вторичной переработки. Производители и потребители перерабатывают никель с такой последовательностью и в таких больших объемах, что, по мнению экспертов, более половины циркулирующих сегодня изделий из никелевой нержавеющей стали содержат переработанный никелевый материал.
Выбор подходящего производителя
Если вы находитесь на рынке высококачественной никелевой продукции, вам необходимо сотрудничать с надежным поставщиком никеля. Чтобы помочь вам найти тот, который подходит именно вам, мы составили список некоторых поставщиков никеля, которым мы доверяем. Проверьте их, прокрутив вверх; вы найдете профили, зажатые между информационными абзацами.
Однако перед тем, как проверить этих поставщиков, мы рекомендуем вам потратить некоторое время на то, чтобы записать требования и спецификации вашего приложения. Это сфокусирует как ваш поиск, так и любые ваши разговоры с потенциальными поставщиками. Не забудьте указать не только то, что представляет собой ваша заявка, но и такие детали, как объем вашего запроса на материалы, ваш бюджет и ваш запрос на дату доставки. Вооружившись списком спецификаций, вы готовы ознакомиться с перечисленными поставщиками. Сравните и сопоставьте их услуги и предложения продуктов с тем, что вы написали в своем списке, и выберите трех или четырех поставщиков, которые обещают больше всего. Затем обратитесь к каждому из них, чтобы подробно обсудить вашу заявку. После того, как вы поговорили с представителями каждой компании, решите, какая компания лучше всего подходит, и приступайте к работе.
Не забудьте указать не только то, что представляет собой ваша заявка, но и такие детали, как объем вашего запроса на материалы, ваш бюджет и ваш запрос на дату доставки. Вооружившись списком спецификаций, вы готовы ознакомиться с перечисленными поставщиками. Сравните и сопоставьте их услуги и предложения продуктов с тем, что вы написали в своем списке, и выберите трех или четырех поставщиков, которые обещают больше всего. Затем обратитесь к каждому из них, чтобы подробно обсудить вашу заявку. После того, как вы поговорили с представителями каждой компании, решите, какая компания лучше всего подходит, и приступайте к работе.
Зарубежный рынок
Находящийся глубоко под землей никель в основном добывается в России, на которую приходится 40% рынка, и в Канаде, которая производит 30% мировых поставок. Страны, которые производят остальные проценты, включают Австралию, Кубу, Францию, Индонезию и Новую Каледонию. Соединенные Штаты производят очень мало нового никеля; единственная открытая шахта здесь находится на Верхнем полуострове штата Мичиган. Однако, поскольку потребители и производители перерабатывают никель с такой регулярностью, работать с американским поставщиком довольно просто и недорого.
Однако, поскольку потребители и производители перерабатывают никель с такой регулярностью, работать с американским поставщиком довольно просто и недорого.
Потребительские товары: роль никеля
Потребительские товары: роль никеля | Институт никеля
Никельсодержащая нержавеющая сталь
и другие никелевые сплавы обеспечивают визуальную привлекательность, долговечность и гигиенические свойства, что делает их идеальными для использования в бытовых условиях и потребительских товарах. К ним относятся кухонные приборы, кастрюли и сковородки, раковины, краны, столовые приборы и посуда. Электронные устройства, такие как ноутбуки и мобильные телефоны, также выигрывают от этих свойств.
Нержавеющая сталь обладает механическими свойствами и долговечностью, которые делают ее одновременно функциональной и привлекательной. Более пристальный взгляд на ряд бытовых приборов покажет повсеместное распространение нержавеющей стали. Внутри он используется для внутренней части посудомоечной машины, барабана стиральной машины и сушилки. Снаружи нержавеющая сталь защищает газовый гриль от непогоды. Тем не менее, это лишь наиболее заметные области применения никелевых сплавов в повседневных потребительских товарах и лишь некоторые из ситуаций, когда никельсодержащие материалы используются в современных домах.
Снаружи нержавеющая сталь защищает газовый гриль от непогоды. Тем не менее, это лишь наиболее заметные области применения никелевых сплавов в повседневных потребительских товарах и лишь некоторые из ситуаций, когда никельсодержащие материалы используются в современных домах.
Потребительские товары представляют собой сектор роста для никельсодержащих материалов, особенно в странах с более быстрорастущей экономикой, таких как Китай и Индия. По оценкам, более 12% мирового производства никеля используется для изготовления крупной бытовой техники, в основном из нержавеющей стали.
Еще 5% мирового производства используется в форме сплава для создания электронных компонентов, используя преимущества проводящих, магнитных и экранирующих свойств никеля, а также его роль в коррозионной стойкости. Никель можно найти в нагревательных спиралях и элементах обычных электроприборов, таких как утюги для одежды, плиты, тостеры, грили, электрические одеяла, плинтусные нагреватели и паяльники. Эти хромоникелевые сплавы могут содержать 20-80% никеля, причем некоторые из них способны противостоять окислению и сохранять свою форму при температурах до 1250°C (2280°F). Никель-железные сплавы с низким тепловым расширением, содержащие 36-42 % никеля (например, Invar® (UNS K93600)), уже давно используются в биметаллических пластинах для термостатов и других устройств контроля температуры.
Эти хромоникелевые сплавы могут содержать 20-80% никеля, причем некоторые из них способны противостоять окислению и сохранять свою форму при температурах до 1250°C (2280°F). Никель-железные сплавы с низким тепловым расширением, содержащие 36-42 % никеля (например, Invar® (UNS K93600)), уже давно используются в биметаллических пластинах для термостатов и других устройств контроля температуры.
Другое использование никеля более ощутимо; металлические корпуса мобильных телефонов и другие внешние детали часто изготавливаются из нержавеющей стали. Кроме того, он необходим для многих внутренних электронных устройств компьютеров, телефонов, планшетов и других высокотехнологичных устройств. Никельсодержащие нержавеющие стали также используются при изготовлении множества других предметов повседневного обихода, от крошечных пружин в наручных часах до головок клюшек для гольфа.
Кухонные раковины
На вопрос о самой важной комнате в доме большинство людей, вероятно, назовут кухню. На каждой кухне именно мойка является наиболее интенсивно используемой из всех бытовых приборов. Сегодня большинство бытовых и промышленных моек изготавливаются из никельсодержащей нержавеющей стали. Это делает их прочными и долговечными, свойства, которые особенно подходят для предметов, которые интенсивно используются каждый день, независимо от различных пищевых продуктов и чистящих химикатов, используемых на кухне.
На каждой кухне именно мойка является наиболее интенсивно используемой из всех бытовых приборов. Сегодня большинство бытовых и промышленных моек изготавливаются из никельсодержащей нержавеющей стали. Это делает их прочными и долговечными, свойства, которые особенно подходят для предметов, которые интенсивно используются каждый день, независимо от различных пищевых продуктов и чистящих химикатов, используемых на кухне.
Большинство моек из нержавеющей стали изготовлены из штампованной верхней поверхности нержавеющей стали, в которую вварена чаша глубокой вытяжки. Именно содержание никеля в нержавеющей стали обеспечивает простоту и стабильность формовки и сварки. Большинство бытовых и промышленных моек изготавливаются из стали типа 304 (UNS S30400), которая содержит 18% хрома и 8-10% никеля. В более требовательных промышленных условиях, например, связанных с приготовлением соленой пищи, может быть более подходящим тип 316 (UNS S31600), который содержит 2% молибдена; молибден обеспечивает большую коррозионную стойкость, особенно в присутствии хлоридов.
Хотя полированная поверхность из нержавеющей стали и не является обязательной с точки зрения гигиены, она соответствует высоким стандартам, предъявляемым как к розничной торговле, так и к домашним кухням. Вот почему большинство производителей полируют поверхность изготовленных ими раковин до идеальной чистоты. Основным преимуществом нержавеющей стали перед более мягкими материалами, такими как некоторые синтетические материалы, является их твердость. Поскольку царапины и выбоины на раковине менее доступны для моющих средств, они представляют опасность для микроорганизмов. Тем не менее, устойчивость нержавеющей стали к глубоким царапинам означает, что мойки остаются гигиеничными и легко очищаются. Еще одним важным преимуществом является возможность вторичной переработки; нержавеющая сталь, используемая в производстве моек, на 100 % пригодна для вторичной переработки даже по истечении их длительного срока службы.
Дизайн интерьера и строительство
При входе в большинство современных зданий никельсодержащая нержавеющая сталь, вероятно, будет материалом, используемым для многих элементов дизайна и конструкции.
Никельсодержащая нержавеющая сталь используется повсеместно в дизайне интерьеров и строительстве; в подъезде офисного здания, в лифтах современного отеля и на стенах стильного ресторана. Никельсодержащая нержавейка имеет огромное разнообразие отделки – яркую, матовую, рельефную или тонированную. Эти разные варианты оформления идеально вписываются в современный дизайн и архитектуру интерьера. Помимо привлекательного внешнего вида, никельсодержащая нержавеющая сталь также обладает исключительной износостойкостью и устойчивостью к коррозии, что облегчает очистку поверхностей и обеспечивает их чрезвычайно длительный срок службы.
Никельсодержащая нержавеющая сталь предлагает почти бесконечный диапазон различных форм и применений, позволяя дизайнерам воплощать в жизнь свои самые творческие и инновационные идеи. В быту никельсодержащую нержавеющую сталь можно найти на кухне и в ванных комнатах, где она ценится как за свой дизайн, так и за функциональные свойства. Между тем, за стенами самые передовые системы водоотведения и сантехники используют никельсодержащую нержавеющую сталь, поскольку она долговечна и не требует особого ухода, что обеспечивает бесперебойную подачу воды.
В доме
Необходимость экономить энергию и обеспечивать максимальную энергоэффективность наших домов в настоящее время общепризнанна; Интерес к «Энергосбережению» и «Энергоэффективности» теперь повсеместен. Общество все чаще требует, чтобы производители переосмыслили то, как дома и офисы отапливаются зимой и охлаждаются летом.
Около 60% энергии, потребляемой в среднем доме, используется для обогрева помещений. Разумное решение по отоплению может иметь большое значение для экономии энергии и денег. Наиболее эффективные печи и котлы, доступные в настоящее время, используют конденсационную технологию. Эти системы потребляют на 35 % меньше энергии, чем стандартные модели.
Если большая часть энергии топлива преобразуется в полезное тепло, температура выхлопных газов становится достаточно низкой, чтобы их можно было вывести через небольшую трубу через стену дома, что устраняет необходимость в дымоходе. Конденсационные печи и котлы оснащены дополнительными усовершенствованными конструкциями теплообменников для извлечения максимального количества тепла из дымовых газов до того, как они покинут выхлопные газы. Эти теплообменники часто изготавливаются из никельсодержащей нержавеющей стали, чтобы выдерживать коррозионную природу кислого газа и жидкого конденсата.
Эти теплообменники часто изготавливаются из никельсодержащей нержавеющей стали, чтобы выдерживать коррозионную природу кислого газа и жидкого конденсата.
Именно прочность никельсодержащей нержавеющей стали позволяет экономить энергию и пространство. В частности, нержавеющая сталь необходима в процессе конденсации котла – высокая коррозионная стойкость и гладкая поверхность позволяют быстро стекать конденсату, не оставляя следов сгорания. Это гарантирует, что отопление является энергоэффективным и требует минимального обслуживания.
На кухне
На кастрюли и сковороды из никельсодержащих нержавеющих сталей часто распространяется пожизненная гарантия.
Причина, по которой производители могут предлагать такие длительные гарантии, заключается в том, что никель в составе нержавеющей стали делает эти кухонные принадлежности исключительно прочными, долговечными и простыми в уходе. Нержавеющая сталь самого высокого качества, используемая в кухонной посуде, обычно содержит 8–10 % никеля. Это обеспечивает чрезвычайно износостойкую посуду, которую можно тщательно и многократно чистить без риска потускнения или коррозии с течением времени. Кроме того, кастрюли и сковороды из никельсодержащей нержавеющей стали имеют гладкую поверхность и не имеют пор. В совокупности эти свойства означают, что посуда из нержавеющей стали может противостоять регулярному износу при использовании на оживленной кухне и сохранять первоначальный вид даже после многих лет интенсивного использования.
Это обеспечивает чрезвычайно износостойкую посуду, которую можно тщательно и многократно чистить без риска потускнения или коррозии с течением времени. Кроме того, кастрюли и сковороды из никельсодержащей нержавеющей стали имеют гладкую поверхность и не имеют пор. В совокупности эти свойства означают, что посуда из нержавеющей стали может противостоять регулярному износу при использовании на оживленной кухне и сохранять первоначальный вид даже после многих лет интенсивного использования.
Память формы в оправах очков
Падая или садясь на очки или солнцезащитные очки, вы рискуете получить большой счет.
Однако, если оправы не ломаются и чудесным образом возвращаются в исходное состояние, то, вероятно, они были изготовлены из никель-титанового сплава с памятью формы (SMA). Никель-титановые СПФ — это «умные металлы», которые «запоминают» первоначальную форму и могут быть возвращены к ней после деформации простым воздействием тепла. При деформированной оправе очков они просто возвращаются в свою первоначальную форму.
Общее название этого семейства никель-титановых сплавов — нитинол. В 1961 году исследователь из американской лаборатории обнаружил, что нитинол, полученный в «Никель-титановой военно-морской артиллерийской лаборатории», обладает этим уникальным свойством, которое теперь называется «памятью формы». Открытие свойства памяти формы произошло случайно; полоска нитинола была представлена на совещании руководства лаборатории, несмотря на то, что она была сильно изогнута. Один из участников встречи нагрел его зажигалкой; к их удивлению, полоса вернулась к своей первоначальной форме.
Аккумуляторы
В современных мобильных телефонах, ноутбуках и цифровых камерах используются никельсодержащие аккумуляторы: литий-ионные, никель-металлогидридные (NiMH) или никель-кадмиевые (NiCd).
Большинство мобильных телефонов и портативных компьютеров питаются от перезаряжаемой литий-ионной батареи. Никель является критическим компонентом механизма безопасности автоматического выключателя, используемого в этих батареях, в котором используется комбинация никеля и смолы в виде небольшого листа. При сборке в аккумуляторную батарею этот автоматический выключатель поддерживает безопасные уровни напряжения и тока во время зарядки и разрядки.
При сборке в аккумуляторную батарею этот автоматический выключатель поддерживает безопасные уровни напряжения и тока во время зарядки и разрядки.
Хотя в цифровых фотокамерах и видеокамерах иногда используются литий-ионные аккумуляторы нестандартного размера, во многих моделях вместо них используются обычные аккумуляторы типоразмера AA. Многие люди уже перешли с одноразовых щелочных батарей на новый комплект перезаряжаемых никель-металлогидридных батарей. Эти батареи, как правило, служат намного дольше, чем стандартные щелочные батареи. Кроме того, они перезаряжаемые, что означает, что их можно повторно использовать сотни раз. Это экономит деньги с течением времени и, уменьшая количество отходов, помогает защитить окружающую среду. Другой тип перезаряжаемой батареи — никель-кадмиевая, которая доступна в самых популярных размерах. Преимущество NiCd аккумуляторов в том, что они сохраняют свой заряд, когда они не используются. Однако они держат меньше заряда, что делает их более подходящими для использования там, где их можно регулярно подключать для подзарядки, например, в беспроводных домашних телефонах, пылесосах и электроинструментах.
Независимо от типа батареи, рано или поздно они достигнут стадии, когда их больше нельзя будет заряжать. В конце срока службы батареи важно, чтобы она была переработана. Переработка аккумуляторов возвращает важные материалы, включая никель, для дальнейшего использования и снижает спрос на первичные материалы. Это снижает потребность как в ресурсах, так и в энергии для производства.
Мобильные телефоны
Выход на улицу без мобильного телефона похож на выход из дома не полностью одетым или без основного аксессуара.
Хотя никель составляет всего 1 процент от общего веса мобильного телефона, он необходим для этих незаменимых устройств во многих отношениях. Помимо своей роли в батарее, никель также жизненно важен для основного электронного функционирования устройства. При открытии мобильного телефона к печатной плате прикрепляются многочисленные компоненты и электронные микросхемы. Один из них — конденсатор — является неотъемлемой частью электронной схемы. Конденсаторы последнего поколения основаны на слоях сверхтонкого никелевого порошка; это заменяет более старую и более дорогую технологию, основанную на драгоценных металлах, включая серебро и палладий.
Конденсаторы последнего поколения основаны на слоях сверхтонкого никелевого порошка; это заменяет более старую и более дорогую технологию, основанную на драгоценных металлах, включая серебро и палладий.
Кроме того, снижая стоимость компонентов, никель помогает сделать технологию мобильных телефонов более доступной для большего числа людей, а более мелкие детали позволяют делать телефоны легче и изящнее. Однако различные компоненты должны функционировать как единое интегрированное устройство, обладающее электронной проводимостью. Никель является важным компонентом для создания этой проводимости и обеспечения постоянного электрического тока в телефоне. Например, микрофоны в мобильных устройствах сделаны из резины. Путем смешивания никелевого порошка с силиконом для получения этой резины конечный продукт становится проводящим, а в результате микрофон надежен.
Вернуться к началу
Спросите у экспертов
Мы ценим вашу конфиденциальность
Файлы cookie используются для того, чтобы мы могли анонимно анализировать использование нашего веб-сайта и количество посетителей с помощью службы Google Analytics. С политикой конфиденциальности Google Analytics можно ознакомиться здесь. Мы не храним и не отслеживаем какие-либо идентифицирующие пользователя данные о вашем посещении. Вы можете отозвать свое согласие на использование файлов cookie в любое время на странице нашей Политики конфиденциальности.
С политикой конфиденциальности Google Analytics можно ознакомиться здесь. Мы не храним и не отслеживаем какие-либо идентифицирующие пользователя данные о вашем посещении. Вы можете отозвать свое согласие на использование файлов cookie в любое время на странице нашей Политики конфиденциальности.
Я принимаю файлы cookie
я отказываюсь от куки
Аллергия на никель — Как диагностировать?
Аппликационная проба, прик-тест, домашние или DYI-тесты
Когда у вас появляются высыпания на коже и появляется сыпь типа экземы при контакте с определенными предметами, у вас, вероятно, есть то, что называется «9».0019 контактная аллергическая реакция «.
Многие предметы повседневного обихода действительно содержат никель , на который у многих людей аллергия. Контакт кожи с этими предметами вызывает аллергическую реакцию и сыпь. Они обычно появляются в месте контакта с кожей, но могут
Контакт кожи с этими предметами вызывает аллергическую реакцию и сыпь. Они обычно появляются в месте контакта с кожей, но могут
Предметы повседневного обихода, содержащие никель, включают украшения, ключи, монеты, часы, компьютеры, смартфоны… И многие предметы также содержат аллергены, подобные никелю: хром и кобальт.Эти предметы включают кожаные изделия, такие как как ремни, диваны, обувь, а также строительные материалы.
АЛЛЕРГИЯ НА НИКЕЛЬ
Какие предметы повседневного обихода могут вызвать контактную экзему?
> Jewelry: necklaces, earrings, rings, and bracelets
> Watches
> Belts
> Clothing buttons
> Zippers
> Eye glasses
> Лезвия для бритвы
Если ваша кожа реагирует на такие предметы, у вас, вероятно, аллергия на никель, хром или кобальт. Или их комбинация!
Или их комбинация!
Методы пластыря и прик-теста
Теперь, чтобы подтвердить, что у вашей кожи аллергия на никель, хром или кобальт или на любой другой распространенный аллерген, вы можете попросить дерматолога или аллерголога провести конкретную диагностику аллергии. .
Наиболее распространенные из них называются «Аппаратные тесты», «Прик-тесты» или «Тесты контактной гиперчувствительности».
В тестах Path, например, небольшие количества потенциальных аллергенов (включая никель) наносятся на кожу обычно в верхней части спины. Пластыри держатся 48 часов. Если после снятия пластырей кожа воспалилась, то у вас подтверждена аллергия на никель 9.0003
Домашний тест или метод «Сделай сам» (DIY)
Существует также домашний тест, метод «сделай сам», который работает для большинства людей, чтобы проверить аллергию на никель и связанные с ним металлические аллергены. Конечно, это быстрый, простой и дешевый тест, и он не может заменить официальное обследование у дерматолога или аллерголога, особенно если у вас сильная аллергия.
В этом подходе вам нужны оба:
- Предмет, который, как вы знаете, вызывает аллергическую реакцию, например сыпь, при контакте с вашей кожей в течение определенного периода времени (например, серьги, вызывающие воспаление мочек ушей, если они были надеты на вас в течение нескольких минут), и
- Тюбик защитного крема Skintifique HPS. Этот единственный в своем роде продукт включает в себя эксклюзивную технологию CapturifiqueTM, которая специально защищает кожу от никеля, хрома и кобальта.
Первым шагом в этом подходе является нанесение небольшого количества защитного крема на кожу до того, как она соприкоснется с предметом, вызывающим аллергию (если вы очень чувствительны, вы также можете нанести немного крема на кожу). часть предмета, которая будет соприкасаться с кожей).
Если ожидаемая кожная реакция задерживается по сравнению с тем, когда она обычно начинается, или если кожной реакции просто нет (что обычно происходит у 3 из 4 человек), то, скорее всего, у вас аллергия на никель, хром или Кобальт.
Теперь вы знаете, с какими предметами следует избегать контакта… и как защитить кожу с помощью защитного крема или другого продукта от Skintifique, который также включает технологию CapturifiqueTM!
Если ваша кожа реагирует на перечисленные выше продукты и если у вас диагностирована аллергия на никель (или хром, или кобальт), вы можете использовать защитный крем Skintifique или, в качестве полноценного средства, набор для снятия аллергии на никель . Благодаря эксклюзивной технологии CapturifiqueTM Защитный крем и Увлажняющий лосьон могут задерживать металлические аллергены на поверхности кожи и предотвращать их попадание в кожу; следовательно, они предотвращают или ограничивают кожные высыпания и сыпь, даже если кожа контактировала с предметами, содержащими аллергены никеля или других металлов.
1 exclusive
technology
Capturifique™
CAPTURES Nickel allergens before they penetrate into the skin
Technologies
& patents
Skintifique’s scientists developed
Capturifique™ — революционная технология, которая делает наши продукты поистине уникальными для людей с аллергией на никель, хром и кобальт!
Укрепляет
естественный барьер кожи, предотвращая попадание никеля, хрома и кобальта в кожу и вызывая аллергические реакции и сыпь
Ограничивает или предотвращает Предотвращая попадание этих аллергенов на кожу, CAPTURIFIQUE™ воздействует на первопричину сыпи, а не только на симптомы
1 уникальный
Технология
Capturifique ™
Capture Никелевые аллергены, прежде чем они проникли в кожу
Укрепляют
. реакции и сыпь
реакции и сыпь
СТОПЫ
сенсибилизация кожи к никелю, хрому и кобальту. CAPTURIFIQUE™ воздействует на первопричину сыпи, а не только на симптомы
Нажмите кнопку ниже, чтобы открыть для себя эксклюзивный выбор продуктов Skintifique для людей с кожей, реагирующей на никель!
Откройте для себя продукты Skintifique для лечения аллергии на никель
ВАША КОЖА РЕАГИРУЕТ НА НИКЕЛЬ?
DISCOVER MILA, РУКОВОДСТВО ДЛЯ ЧУВСТВИТЕЛЬНОЙ КОЖИ
Узнайте персональный профиль безопасности любого ингредиента или продукта
Покажите мне MILA!
Узнать больше…
Аллергия на никель — Что она делает?
Аллергия на никель. Что можно есть?
Аллергия на никель — Каковы симптомы?
Аллергия на смарт-часы? Есть решение!
Освобождение
Уход по уходу за кожей
Освобождение
СКОРОК СКАЛА СКАЛИ СКАЛИ ИСКАЛЬНЫЙ СКАЛИ ИСКАЛЬНЫЙ СКАЛИКИ СВОРИ СКАЛИКА НА СКОЛОВ СКАЛИКА НА СКОЛОВАТИКАМИ СКАЛИ ИХ СКОЛОВАТА ДЛЯ СКОРОДА
.
 натуральные составы и инновационные и запатентованные технологии
натуральные составы и инновационные и запатентованные технологии
Natural
& SAFE
Our formulations are based on natural ingredients that have proven to be effective and safe for years
Technologies
& PATENTS
Our experts have разработал 2 технологии, защищенные международными патентами, что делает нашу продукцию уникальной в мире!
Сделано в
ФРАНЦИЯ
Наша продукция разработана и произведена во Франции с использованием местных ингредиентов и упаковки
ПОЧЕМУ ВЫБРАТЬ
SKINTIFIQUE
Skintifique помогает освободить чувствительную и непереносимую кожу от естественных ограничений и аллергии благодаря своим естественным составам и непереносимости. и инновационные и запатентованные технологии
Natural
& SAFE
Наши рецептуры основаны на натуральных ингредиентах, которые доказали свою эффективность и мягкость в течение 9 лет.
