Какие виды коррозии существуют: Виды коррозии | Руководство по выбору материалов
Содержание
Основные виды коррозии металлов | «ЧелМетСнаб»
Содержание:
- Методы защиты металлов от коррозии, их эффективность
- Возможно вас заинтересует
- Народнохозяйственное значение борьбы с коррозией
Коррозией металлов называется их разрушение вследствие химического или электрохимического взаимодействия с окружающей средой. По механизму протекания процесса различают два типа коррозии металлов: химическую и электрохимическую.
Химическая коррозия — это коррозийный процесс, протекающий в средах, не проводящий электрический ток. Химическая коррозия имеет место, например, при высокотемпературном нагреве стали для горячей обработки давлением или термической обработки. При этом на поверхности металла образуются различные химические соединения — оксиды, сульфиды и другие — в виде пленки.
В отдельных случаях образовавшиеся при химической коррозии пленки, особенно сплошные, предохраняют металл от дальнейшей коррозии. Например, алюминий, олово, свинец, никель и хром способны к образованию на поверхности металлов плотных защитных пленок. пленки же на поверхности стальных и чугунных изделий непрочны, способны к растрескиванию и проникновению коррозии в глубь металла.
Например, алюминий, олово, свинец, никель и хром способны к образованию на поверхности металлов плотных защитных пленок. пленки же на поверхности стальных и чугунных изделий непрочны, способны к растрескиванию и проникновению коррозии в глубь металла.
Электрохимическая коррозия обычно сопровождается протеканием электрического тока. Примерами могут служить ржавление металлических конструкций и изделий в атмосфере, корпусов судов и стальной арматуры гидросооружений в речной и морской воде и т.п.
Детальное рассмотрение механизмов химической и электрохимической коррозии показывает, что резкого различия между ними не существует. В ряде случаев возможен постепенный переход химической коррозии в электрохимическую и, наоборот, механизм коррозии металлов в растворах электролитов может иметь двоякий характер.
Коррозия по условиям протекания бывает следующая. Газовая- коррозия металла в газах при высоких температурах. Коррозия в неэлектролитах (например, коррозия стали в бензине). Атмосферная коррозия различных металлических конструкций на воздухе. Коррозия в электролитах- в проводящих электрический ток жидких средах. Почвенная (например, коррозия подземных трубопроводов). Коррозия внешним током или электрокоррозия (например, коррозия подземной трубы блуждающими токами). Контактная — электрохимическое разрушение металлов, происходящее в результате контакта различных металлов в электролите (например, коррозия деталей из алюминиевых сплавов, соприкасающихся с деталями из меди). Структурная- связанная со структурной неоднородностью металлов; например, ускорение коррозионного процесса чугуна в растворе серной кислоты в результате имеющихся в нем включений графита. Коррозия под напряжением, изменяющимся по значению и знаку, что часто вызывает коррозионную усталость- понижение предела выносливости металла. Коррозия при трении; например, разрушение шейки вала при вращении в морской воде. Щелевая, протекающая в узких щелях и зазорах между отдельными деталями. Биокоррозия- коррозия металлов под воздействием продуктов, выделяемых микроорганизмами, и пота рук человека.
Атмосферная коррозия различных металлических конструкций на воздухе. Коррозия в электролитах- в проводящих электрический ток жидких средах. Почвенная (например, коррозия подземных трубопроводов). Коррозия внешним током или электрокоррозия (например, коррозия подземной трубы блуждающими токами). Контактная — электрохимическое разрушение металлов, происходящее в результате контакта различных металлов в электролите (например, коррозия деталей из алюминиевых сплавов, соприкасающихся с деталями из меди). Структурная- связанная со структурной неоднородностью металлов; например, ускорение коррозионного процесса чугуна в растворе серной кислоты в результате имеющихся в нем включений графита. Коррозия под напряжением, изменяющимся по значению и знаку, что часто вызывает коррозионную усталость- понижение предела выносливости металла. Коррозия при трении; например, разрушение шейки вала при вращении в морской воде. Щелевая, протекающая в узких щелях и зазорах между отдельными деталями. Биокоррозия- коррозия металлов под воздействием продуктов, выделяемых микроорганизмами, и пота рук человека. По характеру коррозионных процессов и месту их распределения различают сплошную, местную и межкристаллитную коррозию. Сплошная коррозия характеризуется тем, что металлическое изделие разрушается почти равномерно и коррозия охватывает всю его поверхность. Этот вид коррозии сравнительно легко поддается контролю и оценке.
По характеру коррозионных процессов и месту их распределения различают сплошную, местную и межкристаллитную коррозию. Сплошная коррозия характеризуется тем, что металлическое изделие разрушается почти равномерно и коррозия охватывает всю его поверхность. Этот вид коррозии сравнительно легко поддается контролю и оценке.
Местная коррозия обычно бывает сосредоточенна на отдельных участках поверхности изделия. Это более опасный вид коррозии, так как распространяется на значительную глубину, а следовательно, приводит к потере работоспособности изделий. Чаще всего этот вид коррозии наблюдается в местах механических повреждений поверхности изделий. При межкристаллитной коррозии процесс разрушения начинается с поверхности изделия и распространяется в глубь его, в основном по границам зерен. Межкристаллитная коррозия вызывает хрупкость металла и значительное снижение его несущей способности. Этот часто встречающийся на практике вид коррозии является весьма опасным и обычно имеет место при термической обработке металлов или сварке. Степень коррозийной стойкости сталей существенно зависит от содержания углерода. Так, с уменьшением содержания углерода в легированной хромоникелевой стали марки Х18Н9 до 0.015% практически устраняется склонность ее к межкристаллитной коррозии.
Степень коррозийной стойкости сталей существенно зависит от содержания углерода. Так, с уменьшением содержания углерода в легированной хромоникелевой стали марки Х18Н9 до 0.015% практически устраняется склонность ее к межкристаллитной коррозии.
Методы защиты металлов от коррозии, их эффективность
Существуют многочисленные способы защиты металлов от коррозии. Выбор того или иного способа определяется конкретными условиями работы и хранения металлических изделий. Применяются следующие способы защиты: легирование сталей, нанесение металлических покрытий, электрохимическая защита.
Легирование наиболее надежно защищает металл от коррозии, причем наиболее эффективно в условиях воздействия механических напряжений и коррозийной среды. Легирование позволяет предотвратить и коррозийное растрескивание изделий.
Так, например, к группе сталей с особыми химическими свойствами относят коррозионно-стойкие стали. Их получают путем введения в углеродистые и низколегированные стали значительных добавок хрома или хрома и никеля. При содержании хрома 13, 17 и 25% хромистые стали являются не только коррозионно-, но и жаростойкими. Хромоникелевые стали обладают большей коррозионной стойкостью, чем хромистые, и находят широкое применение в химической промышленности.
При содержании хрома 13, 17 и 25% хромистые стали являются не только коррозионно-, но и жаростойкими. Хромоникелевые стали обладают большей коррозионной стойкостью, чем хромистые, и находят широкое применение в химической промышленности.
Механизм защиты сталей от коррозии их легированием различен и связан либо с повышением коррозионной стойкости всего объема металла, либо с образованием на поверхности изделия защитных пленок.
Металлические покрытия наносят на поверхность изделия тонким слоем металла, обладающего достаточной стойкостью в данной среде. Металлические покрытия придают также поверхностным слоям металлоизделий требуемую твердость, износостойкость. Различают два типа металлических покрытий- анодное и катодное. Для железоуглеродистых сплавов таким анодным покрытием может служить покрытие из цинка и кадмия. В воде и во влажном воздухе цинк покрывается слоем основной углекислой соли белого цвета, защищающим его от дальнейшего разрушения. Широкое применение получили цинковые покрытия для защиты арматуры, труб и резервуаров от действия воды и горячих жидкостей.
Металлические покрытия наносят различными способами. Наиболее часто применяется горячий метод, гальванизация и металлизация.
При горячем методе изделие погружают в расплавленный металл, который смачивает его поверхность и покрывает тонким слоем. Затем изделие вынимают из ванны и охлаждают. Таким методом изделие покрывают слоем олова или цинка. Лужение применяют при изготовлении белой жести, при устройстве покрытий на внутренних поверхностях пищевых котлов и других изделий. Цинкованием предохраняют от коррозии, например, кровельное железо, водопроводные трубы.
При гальваническом способе металлические изделия помещают в гальваническую ванну. Под действием электрического тока на поверхности изделия происходит катодное осаждение пленки защитного металла. Толщину гальванического покрытия можно регулировать в широких пределах. Покрытия получают также распылением расплавленного металла с помощью специальных металлизационных пистолетов и напылением на его поверхность защищаемого металла. Этот вид защиты используют для крупногабаритных конструкций: ж./д мостов и т. д. В качестве защитного металла используют алюминий, цинк, хром, коррозионно-стойкие стали.
Этот вид защиты используют для крупногабаритных конструкций: ж./д мостов и т. д. В качестве защитного металла используют алюминий, цинк, хром, коррозионно-стойкие стали.
Неметаллические покрытия выполняются из лаков, красок, эмалей и др. веществ и изолируют изделие от воздействия внешней среды. Эти покрытия имеют преимущество перед металлическими. Они легко наносятся на изделие, хорошо закрывают поры, не изменяют свойств металла и являются относительно дешевыми. При хранении и перевозке изделий металлические изделия покрывают специальными смазочными материалами, минеральными маслами и жирами. Для защиты изделий, работающих в высокоагрессивных средах, применяют пластмассовые покрытия из винипласта, поливинилхлорида.
Химические покрытия — защитные оксидные иные пленки- создаются при воздействии на металл сильных химических реагентов. Широко применяются также оксидирование и фосфатирование металлоизделий.
Оксидирование заключается в создании на поверхности изделия оксидной пленки, обладающей большой коррозийной стойкостью. Наиболее широко применяют оксидирование для защиты от коррозии изделий из алюминия и его сплавов.
Наиболее широко применяют оксидирование для защиты от коррозии изделий из алюминия и его сплавов.
Фосфатирование стальных изделий заключается в создании поверхностного слоя из фосфатов марганца и железа. Фосфатные покрытия используются в дальнейшем в качестве подслоя. Фосфатные покрытия часто применяются в сочетании со смазочными материалами для уменьшения трения при обработке металлов давлением, волочением, для хорошей приработке трущихся деталей машин.
В отдельных случаях прибегают к защите металлов от коррозии при помощи протекторов. Сущность протекторной защиты заключается в том, что к поверхности защищаемого изделия прикрепляют протекторы- куски металла. Образуется гальваническая пара , в которой анод- протектор, катод- изделие. В результате протектор разрушается, защищая изделие. Таким образом, защищают, например, подводные металлические части кораблей, прикрепляя к ним пластины цинка.
Возможно вас заинтересует
Народнохозяйственное значение борьбы с коррозией
Одним из основных факторов, определяющих долговечность машин и оборудования, является коррозия металлов. Потери от коррозии можно разделить на прямые и косвенные. Прямые потери- это стоимость заменяемых изделий, затраты на защитные мероприятия и безвозвратные потери металла вследствие коррозии. По подсчетам специалистов, безвозвратные потери металла в мировом масштабе составляют в настоящее время около 10…15% от объема производства стали. Косвенные потери продукта в результате утечек, снижение производительности агрегата, загрязнение продуктами коррозии целевого продукта и т.п.
Потери от коррозии можно разделить на прямые и косвенные. Прямые потери- это стоимость заменяемых изделий, затраты на защитные мероприятия и безвозвратные потери металла вследствие коррозии. По подсчетам специалистов, безвозвратные потери металла в мировом масштабе составляют в настоящее время около 10…15% от объема производства стали. Косвенные потери продукта в результате утечек, снижение производительности агрегата, загрязнение продуктами коррозии целевого продукта и т.п.
Значительная часть мощности предприятий черной металлургии затрачивается на восполнение потерь металла вследствие коррозии. Однако это далеко не полностью отражает действительный ущерб, связанный с выходом из строя изделий из металла. Значительные потери обусловлены авариями оборудования, простоями его, потерями и отходами в металлообработке, нарушениями качества продукции и в конечном счете повышением ее себестоимости и снижением производительности труда. Поэтому экономия металла, повышение качества металлов и металлоизделий, уменьшение коррозионных потерь — непременное условие повышения эффективности производства и качества продукции, которое должно обеспечиваться в государственном масштабе.
9 различных видов коррозии, поражающей материалы
Коррозия — это процесс, в результате которого материал разрушается из-за химических взаимодействий. Все материалы подвержены коррозионным явлениям, но металлы особенно подвержены коррозии, поскольку поверхностные атомы легко окисляются в определенных условиях. Существуют стали, разработанные для использования окисления в целях повышения коррозионной стойкости (например, атмосферостойкая сталь), и другие марки стали с регенеративной патиной, разработанной для снижения поверхностной коррозии (например, нержавеющая сталь). Но лишь немногие стали инженерного класса могут сравниться с передовой коррозионностойкой керамикой по химической стабильности.
В этой статье мы рассмотрим девять видов коррозии, воздействующих на материалы, чаще всего металлические сплавы.
Поскольку коррозия является серьезной проблемой во многих отраслях промышленности, особенно в строительстве, необходимо знать ее виды и причины возникновения.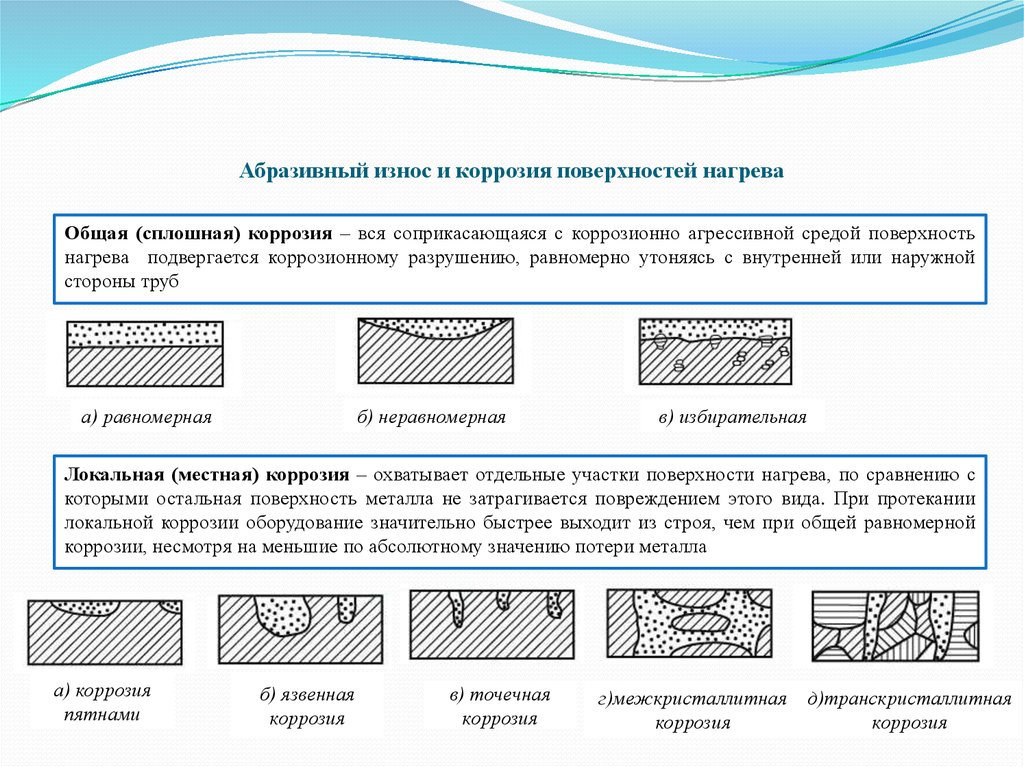
1. Растрескивание под влиянием окружающей среды
Растрескивание под влиянием окружающей среды исходя из названия возникает под воздействием факторов окружающей среды и охватывает множество условий. Этот тип коррозии может вызвать значительные повреждения за короткий период времени и включает в себя коррозионную усталость, водородное охрупчивание и коррозионное растрескивание под напряжением (КРПН). Растрескивание под влиянием окружающей среды может быть вызвано различными напряжениями, возникающими в результате таких процессов, как термообработка, остаточная холодная обработка или сварка.
2. Эрозионная коррозия
Эрозионная коррозия, сочетание эрозии и коррозии на поверхности, возникает, когда быстро движущиеся коррозионные жидкости изнашивают поверхность металла.
3. Фреттинг-коррозия
Фреттинг-коррозия возникает, когда две поверхности постоянно трутся друг о друга во время какого-либо процесса. Фреттинг и коррозия совместно возникают, когда материалы находятся под давлением во время многократного воздействия.
4. Высокотемпературная коррозия
Как следует из названия, эта коррозия возникает при экстремальных температурах (обычно выше 400 градусов цельсия). Высокотемпературная коррозия возникает из-за химического воздействия газов или расплавленных металлов. Обычно это происходит в печах, газовых турбинах и машинах, где горячий газ содержит специфические загрязняющие вещества.
5. Межкристаллитная коррозия
Межкристаллитная коррозия — это форма локализованной коррозии, которая возникает на границах зерен и вокруг них. В результате происходит изнашивание металлического сплава и снижение его прочности.
6. Питтинговая коррозия
Питтинговая коррозия — это еще один вид локализованной коррозии, в результате которой на поверхности металла образуются случайные небольшие полости или отверстия. Это происходит, когда защитный оксидный слой на поверхности начинает разрушаться, оставляя подложку уязвимой для коррозии.
7. Гальваническая коррозия
Часто называемая биметаллической коррозией, гальваническая коррозия возникает, когда один металл при контакте с электролитом преимущественно корродирует другой. Гальваническая коррозия чаще всего ассоциируется с морским применением, где хлориды в морской воде образуют углубления в стали. Она невероятно распространена в химическом производстве и при работе с расплавленным металлом. В основном она возникает в сильно кислых, щелочных и токсичных средах, которые могут разъедать металлы за считанные недели.
Гальваническая коррозия чаще всего ассоциируется с морским применением, где хлориды в морской воде образуют углубления в стали. Она невероятно распространена в химическом производстве и при работе с расплавленным металлом. В основном она возникает в сильно кислых, щелочных и токсичных средах, которые могут разъедать металлы за считанные недели.
8. Усталостная коррозия
Также известная как коррозионное растрескивание под напряжением, коррозия и длительное растягивающее напряжение прикладываются к материалу. Под высоким напряжением границы материала начинают разрываться, что приводит к образованию мелких трещин вдоль поверхности.
9. Равномерная коррозия
Это, как правило, наиболее распространенный тип коррозии и относится к процессу, при котором коррозионному воздействию подвергается весь материал. Коррозии подвергается вся поверхность, что обычно происходит с железом и сталью под воздействием природных элементов, таких как почва и вода.
Советуем вам прочитать статьи опубликованные в нашем блоге ранее: «Почему латунь, бронза и медь зеленеют?» и «40 интересных фактов о металлах».
Если вам понравилась статья, то ставьте лайк, делитесь ею со своими друзьями и оставляйте комментарии!
Основные сведения о типах коррозии проводов и кабелей
Коррозия возникает, когда в среде, окружающей материалы, происходит химическая реакция, которая начинает медленно ухудшать и ослаблять материал. Конкретные газы из окружающей среды, контактирующие с определенным металлом, в конечном итоге определяют скорость и форму коррозии. Ниже приведены девять наиболее распространенных типов коррозии и их внешний вид. Важно понимать каждый из них в проводной и кабельной промышленности, поскольку это один из ведущих факторов ухудшения .
Свяжитесь с нами и получите предложение!
1. Общая агрессивная коррозия
Эта форма коррозии возникает, когда химическая или электрохимическая реакция вызывает ухудшение состояния открытой металлической поверхности. Хотя общая агрессивная коррозия является наиболее распространенной формой коррозии металлов, она также считается самой безопасной, поскольку ее можно предсказать, управлять и часто можно предотвратить.
2. Локальная коррозия
Этот тип коррозии является локализованным и затрагивает только одну область металлической конструкции. Локальная коррозия бывает трех категорий: точечная, щелевая и нитевидная. Точечная коррозия является результатом коррозии, вызывающей небольшое отверстие (ямку) в металле, которое обычно трудно найти из-за небольшого размера. Ямочная область становится анодной, а часть оставшегося металла становится катодной, вызывая локальную гальваническую реакцию. Щелевая коррозия — это то, что происходит в щели из-за недостатка кислорода или чрезмерно кислой области. Обычно он находится вокруг прокладок, шайб и хомутов. Нитевидная коррозия может в конечном итоге привести к ослаблению конструкции. Это начинается, когда вода просачивается через окрашенные или покрытые металлом поверхности или в любом месте, где может быть дефект поверхностного покрытия.
3. Гальваническая коррозия
Эта форма коррозии будет иметь место, если два электрохимически разных металла занимают одно и то же пространство и находятся в электрическом контакте друг с другом, и металлы подвергаются воздействию электролита. Если все эти сценарии присутствуют, гальваническая коррозия будет быстро происходить с менее коррозионно-стойким металлом, становясь анодом, тогда как более коррозионно-стойкий металл будет уменьшаться, становясь катодом.
Если все эти сценарии присутствуют, гальваническая коррозия будет быстро происходить с менее коррозионно-стойким металлом, становясь анодом, тогда как более коррозионно-стойкий металл будет уменьшаться, становясь катодом.
4. Экологическая растрескивание, коррозия
Растрескивание под воздействием окружающей среды происходит, когда условия, окружающие металл, начинают воздействовать на него. Это может быть связано с некоторыми условиями, такими как химические вещества, температура и окружающая среда, связанная со стрессом. Возможно, вы слышали о коррозии под воздействием окружающей среды, называемой коррозионным растрескиванием под напряжением, коррозионной усталостью, водородной коррозией или охрупчиванием жидких металлов. Двумя наиболее распространенными случаями коррозии с растрескиванием под действием окружающей среды являются сезонное растрескивание латуни и щелочное охрупчивание стали.
5. Коррозия под действием потока (FAC)
Эта коррозия вызывается ветром или водой, «смывающей» защитный оксидный слой металлической поверхности. Как только металл обнажается, возникает коррозия под действием потока, что приводит к повреждению детали / объекта.
Как только металл обнажается, возникает коррозия под действием потока, что приводит к повреждению детали / объекта.
6. Межкристаллитная коррозия
Электрохимическое воздействие на границы зерен металла называется межкристаллитной коррозией. Это часто происходит из-за примесей на границах зерен, обогащения одним из легирующих элементов или обеднения одним из этих элементов вблизи границ зерен.
7. Коррозия селективного выщелачивания
Это происходит, когда один элемент из твердого сплава удаляется из-за коррозии. Избирательное выщелачивание чаще всего происходит при селективном удалении цинка из латунных сплавов, также известном как обесцинкование.
8. Фреттинг-коррозия.
Многократный износ, вес и вибрация на шероховатых или неровных поверхностях и неровностях контактных поверхностей, затронутых коррозионным повреждением, вызывают этот тип коррозии. Ударная техника, болтовые соединения и подшипники часто подвержены фреттинг-коррозии, а также поверхности, испытывающие сильную вибрацию.
9. Высокотемпературная коррозия
Эта коррозия может быть вызвана окислением при высоких температурах, сульфидированием и карбонизацией. Чаще всего высокотемпературная коррозия возникает в газовых турбинах, дизельных двигателях и другом оборудовании. В этих механиках коррозия начинается, когда при сгорании ванадий или сульфаты образуют соединения с низкой температурой плавления. Композиты вызывают коррозию металлических сплавов, которые в остальном устойчивы к высоким температурам и коррозии.
Виды коррозии | Руководство по выбору материалов
Чтобы найти правильное решение по материалам, нужно начать с источника проблемы.
> Просмотрите и загрузите версию Руководства по выбору материалов для печати
Обратитесь к доверенному консультантуДоступ к услугам экспертного уровня легче всего обнаружить и предсказать. Это необычно, но не неслыханно, чтобы общая коррозия приводила к катастрофическим отказам. По этой причине общую коррозию часто считают бельмом на глазу, а не серьезной проблемой. Общая коррозия протекает относительно равномерно по поверхности металла. Постепенное уменьшение толщины стенки компонента необходимо учитывать при расчете номинального давления.
По этой причине общую коррозию часто считают бельмом на глазу, а не серьезной проблемой. Общая коррозия протекает относительно равномерно по поверхности металла. Постепенное уменьшение толщины стенки компонента необходимо учитывать при расчете номинального давления.
Как он образуется
В морской или другой коррозионной среде поверхность углеродистой или низколегированной стали начинает разрушаться, что приводит к образованию окалины оксида железа, которая со временем становится толще, пока не откалывается и не образуется новая окалина. формы.
Может быть измерено с помощью
- Скорость износа материала в течение года. Например, незащищенная углеродистая сталь может отступать в морской среде на 1 мм каждый год.
- Потеря веса сплава при контакте с агрессивными жидкостями, обычно измеряемая в миллиграммах на квадратный сантиметр открытого материала в день
Возможные решения
Нержавеющая сталь 316/316L; 6-молибденовые сплавы; сплав 2507; сплав 825; сплав 625; сплав С-276; Alloy 400
Локализованная точечная коррозия в хлоридсодержащих средах
Точечная коррозия приводит к образованию небольших полостей или ямок на поверхности материала. Хотя эти ямки можно обнаружить при тщательном визуальном осмотре, они могут расти достаточно глубоко, чтобы продырявить НКТ. Питтинг чаще наблюдается в средах с высоким содержанием хлоридов при повышенных температурах.
Хотя эти ямки можно обнаружить при тщательном визуальном осмотре, они могут расти достаточно глубоко, чтобы продырявить НКТ. Питтинг чаще наблюдается в средах с высоким содержанием хлоридов при повышенных температурах.
Как это образуется
Когда защитный слой оксида (или пассивный оксидный слой) на поверхности металла разрушается, металл становится восприимчивым к потере электронов. Это заставляет железо в металле растворяться в растворе на более анодированном дне ямы, диффундировать вверх и окисляться до оксида железа или ржавчины. Концентрация раствора хлорида железа в яме может увеличиваться и становиться более кислой по мере углубления ямы. Эти изменения приводят к ускоренному росту язвы, перфорации стенок НКТ и протечкам.
Более высокие значения PREN указывают на более высокую стойкость к точечной коррозии. Питтинговая коррозия лучше всего предотвращается правильным выбором сплава. Различные металлы и сплавы можно сравнивать с помощью их эквивалентного числа сопротивления точечной коррозии (PREN), которое рассчитывается на основе химического состава материала. PREN увеличивается с более высокими уровнями хрома, молибдена и азота.
PREN увеличивается с более высокими уровнями хрома, молибдена и азота.
Возможные решения
6-молибденовые сплавы; сплав 2507; сплав 825; сплав 625; сплав С-276; Сплав 400
Локализованная щелевая коррозия в хлоридсодержащих средах
В типичной жидкостной системе щели существуют между трубками и трубными опорами или зажимами труб, между соседними участками труб, а также под грязью и отложениями, которые могут скопиться на поверхностях. Трещин практически невозможно избежать в трубных установках, а узкие щели представляют наибольшую опасность возникновения коррозии.
Как она образуется
Как и точечная коррозия, щелевая коррозия начинается с разрушения пассивного оксидного слоя, защищающего металл. Это разрушение приводит к образованию небольших ямок. Ямы становятся все больше и глубже, пока не покроют всю расщелину. В некоторых местах трубка может быть перфорирована. Щелевая коррозия возникает при гораздо более низких температурах, чем точечная коррозия.
Возможные решения
6-молибденовые сплавы; сплав 2507; сплав 825; сплав 625; сплав С-276; Alloy 400
Материал имеет значение
Когда морская вода диффундирует в щель, некоторые ионы Fe++ растворяются и не могут быстро диффундировать из тесной щели. В соленой воде отрицательно заряженные ионы хлора (Cl-) притягиваются этими положительно заряженными ионами Fe++ и начинают диффундировать в расщелину. По мере увеличения концентрации хлорида раствор в щели становится более агрессивным, вызывая растворение большего количества железа, что, в свою очередь, привлекает больше ионов хлорида для диффузии в щель. В конечном итоге щелевой раствор превращается в кислый раствор с высокой концентрацией хлоридов, который очень агрессивен.
Коррозионное растрескивание под напряжением в хлоридсодержащих средах
Коррозионное растрескивание под напряжением (SCC) опасно, поскольку оно может разрушить компонент при уровнях напряжения ниже предела текучести сплава. В присутствии ионов хлорида аустенитные нержавеющие стали подвержены SCC. Ионы взаимодействуют с материалом в вершине трещины, где растягивающие напряжения максимальны, что облегчает рост трещины. Во время выполнения SCC может быть трудно обнаружить, и окончательный сбой может произойти внезапно.
В присутствии ионов хлорида аустенитные нержавеющие стали подвержены SCC. Ионы взаимодействуют с материалом в вершине трещины, где растягивающие напряжения максимальны, что облегчает рост трещины. Во время выполнения SCC может быть трудно обнаружить, и окончательный сбой может произойти внезапно.
Как он образуется
Для возникновения SCC должны одновременно выполняться три условия:
- Металл должен быть восприимчив к SCC
- Должны существовать условия окружающей среды (жидкость или температура), способствующие SCC
- Напряжение растяжения (приложенное + остаточное) должно быть выше критического уровня
Более высокое содержание никеля показывает более высокую стойкость к SCC, индуцированному хлоридами
Возможные решения
6-молибденовые сплавы; сплав 2507; сплав 825; сплав 625; сплав С-276; Сплав 400
SSC 1
Крекинг сернистого газа или сульфидный крекинг под напряжением при высоком парциальном давлении сероводорода (H
2 S)
Крекинг сернистого газа, также известный как сульфидное растрескивание контакт с сероводородом (H 2 S) и влагой. H 2 S становится сильно коррозионным в присутствии воды. Это условие может привести к охрупчиванию материала, что приведет к растрескиванию под совместным действием растягивающего напряжения и коррозии.
H 2 S становится сильно коррозионным в присутствии воды. Это условие может привести к охрупчиванию материала, что приведет к растрескиванию под совместным действием растягивающего напряжения и коррозии.
Как он образуется
Риск SSC увеличивается при увеличении следующих факторов:
- Металл должен быть восприимчив к SSC
- Окружающая среда должна быть достаточно кислой (с высоким содержанием H 2 S)
- Напряжение растяжения (приложенное + остаточное) должно быть выше критического уровня
Повышенный риск SSC возникает, когда происходит большее количество следующих факторов, по сравнению с материалами, менее подверженными SSC:
- Твердость материала/прочность на растяжение
- Концентрация ионов водорода (нижнее значение pH)
- H 2 S парциальное давление
- Суммарное растягивающее напряжение (приложенное + остаточное)
- Время экспозиции
Риск SSC увеличивается при более низких температурах, когда материалы имеют тенденцию быть менее пластичными.
Возможные решения
Сплав 825; сплав 625; сплав С-276; Alloy 400
Материал имеет значение
Стандарт NACE MR0175/ISO 15156 описывает подходящие материалы для кислых сред при добыче нефти и газа. Дополнительные сведения о выборе компонентов для месторождений высокосернистой нефти см. в разделе Выбор компонентов жидкостной системы для использования на месторождениях высокосернистой нефти.
Водородное охрупчивание 2
Водородное охрупчивание
Атомы водорода могут диффундировать в металлы, делая их хрупкими. Все материалы, подверженные водородному охрупчиванию, также очень подвержены коррозионному растрескиванию под напряжением.
Как он формируется
Растрескивание под действием водорода может произойти, если металл подвергается статическому или циклическому растягивающему напряжению. Водород может вызывать изменения механических свойств и поведения металла, в том числе:
- Уменьшение пластичности (удлинение и уменьшение площади)
- Снижение ударной вязкости и вязкости разрушения
- Повышенная усталостная характеристика
Водородного охрупчивания можно избежать, выбрав материал, устойчивый к водороду, например, аустенитные сплавы с содержанием никеля от 10% до 30%.
Ферритные сплавы с очень низким содержанием никеля становятся значительно охрупчивающимися, в то время как аустенитные сплавы с содержанием никеля от 10% до 30% показывают относительно небольшое охрупчивание.
Источник: Г.Р. Caskey, Справочник по совместимости с водородом для нержавеющих сталей (1983)
Возможные решения
Нержавеющая сталь 316/316L
Межкристаллитная коррозия
Чтобы понять межкристаллитную коррозию (МКК), учтите, что все металлы состоят из отдельных зерен. Внутри каждого зерна атомы систематически расположены, образуя трехмерную решетку. IGC воздействует на материал по границам зерен (где соединяются зерна, из которых состоит металл).
Как образуется
Во время сварки, термической обработки или воздействия высоких температур карбиды могут начать формироваться на границах зерен. Эти осадки карбида могут увеличиваться со временем. Это образование карбида влияет на равномерное распределение элементов в металле, лишая материал, прилегающий к границам зерен, важных элементов, таких как хром.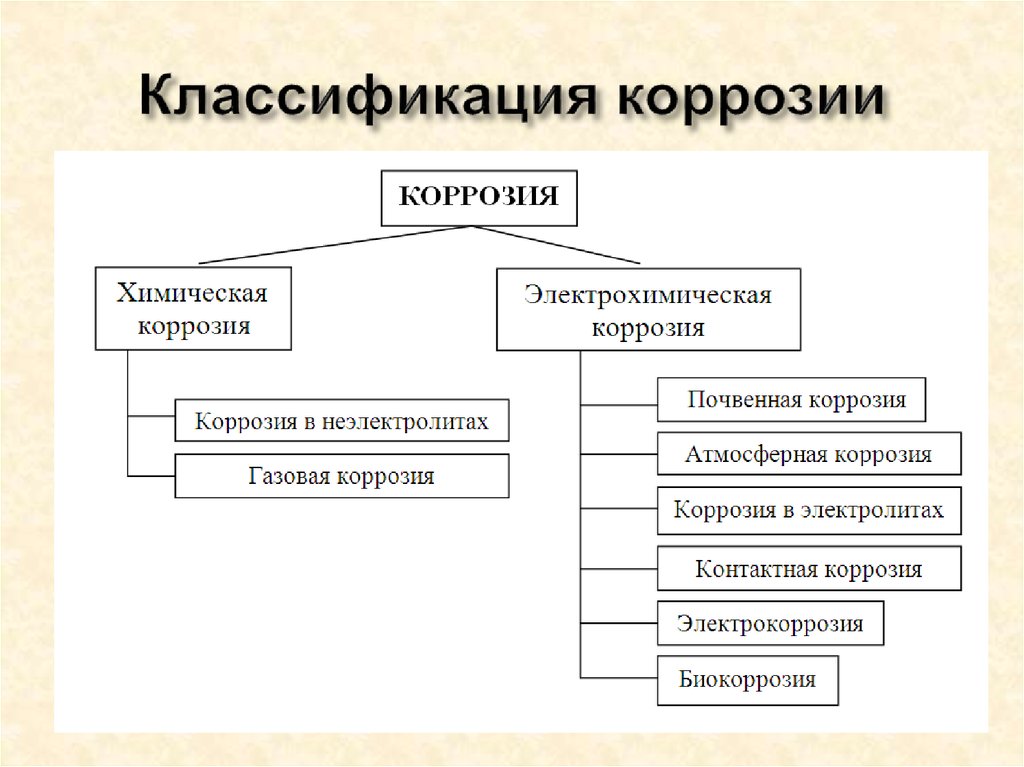 Когда коррозионные жидкости (например, кислоты) воздействуют на области, обедненные хромом, могут образовываться межкристаллитные трещины. Эти трещины могут распространяться по всему материалу и оставаться незамеченными, что делает IGC опасной формой коррозии.
Когда коррозионные жидкости (например, кислоты) воздействуют на области, обедненные хромом, могут образовываться межкристаллитные трещины. Эти трещины могут распространяться по всему материалу и оставаться незамеченными, что делает IGC опасной формой коррозии.
Возможные решения
Нержавеющая сталь 316/316L
Гальваническая коррозия в присутствии электролита
Гальваническая коррозия возникает при контакте материалов с разным электродным потенциалом в присутствии электролита.
SCE расшифровывается как насыщенный каломельный электрод. Анодный индекс: высокоблагородные материалы с «пассивными поверхностями» не так подвержены гальванической коррозии, как менее благородные материалы или благородные материалы с «активными поверхностями». В этой таблице магний является наименее благородным материалом, а графит — наиболее благородным материалом.
Пассивный слой на нержавеющей стали состоит из очень тонкой оксидной пленки с высоким содержанием хрома, которая автоматически формируется в окружающем воздухе и защищает материал от коррозии. Пассивный слой делает материал более благородным и менее подверженным коррозии. Совместимость металлов можно определить по анодному индексу, который описывает разность потенциалов или напряжений металлов, измеренных в морской воде, относительно стандартного электрода.
Пассивный слой делает материал более благородным и менее подверженным коррозии. Совместимость металлов можно определить по анодному индексу, который описывает разность потенциалов или напряжений металлов, измеренных в морской воде, относительно стандартного электрода.
Как он образуется
Когда разность потенциалов между двумя разнородными металлами в присутствии электролита слишком велика, пассивный слой материала начинает разрушаться.
Возможные решения
Во избежание гальванической коррозии выбирайте материалы с разницей напряжений не более 0,2 В. Например, фитинг из нержавеющей стали 316 (-0,05 В) с трубкой из 6-молибдена (0,00 В) приведет к возникновению напряжения 0,05 В между двумя сплавами. Это напряжение значительно меньше 0,2 В, что означает низкий риск гальванической коррозии.
Поговорите с доверенным консультантомДоступ к услугам экспертного уровня
Для получения дополнительной информации ознакомьтесь с этими дополнительными полезными справочными материалами от Swagelok.
