Коррозия медных сплавов: Коррозия меди
Содержание
5 Коррозия меди и ее сплавов, способы их защиты.
Коррозия
меди — это ее разрушение под воздействием
окружающей среды. Медь обладает высокой
коррозионной стойкостью, теплопроводностью,
электропроводностью, отлично обрабатывается
механически, пается. Значительная
коррозия меди наблюдается в окислительных
кислотах, аэрированных растворах,
которые содержат NH4+?
CN—
и другие ионы, способные с медью
образовывать комплексы.
Медь
устойчива в средах: атмочфера, морская
вода, в определенных условиях в контакте
с галогенами, неокислительных кислотах.
Медь
неустойчива в средах: сера, сероводород,
окислительные кислоты, растворы
окислительных солей тяжелых металлов
(Fe2(SO4)3,
FeCl3),
быстро движущихся водных растворах
(подвергается ударной коррозии), амины,
NH4OH
(содержащим кислород.
Скорость
протекания ударной коррозии меди в воде
сильно зависит от кол-ва растворенного
кислорода, наличием на поверхности
оксидных пленок.
На
сухом воздухе поверхность меди почти
не меняется. А при контакте с влажным
воздухом образуется нерастворимая
плнка, состоящая с продуктов коррозии
меди типа CuCO3∙Cu(OH)2.
Коррозия
меди в почве сильно зависит от значения
pH
грунта. Чем грунт щелочнее либо кислее,
тем быстрее проходит коррозия меди в
почве.При сильном насыщении почвы
микроорганизмами усиливается коррозия
меди и ее сплавов.
Луженная
медь отличается превосходной коррозионной
стойкостью. Качественное оловянное
покрытие продлевается срок службы
луженной меди до 100 лет и более.
Влияние
концентрации ионов водорода в коррозионной
среде на скорость коррозии металлов
определяется или их непосредственным
участием в электродном процессе, или
их способностью влиять на растворимость
продуктов коррозии, или возможностью
образовывать защитные оксидные
пленки
при изменении рН раствора. Увеличение
концентрации ионов водорода влияет на
скорость коррозии особенно сильно в
том случае, когда процесс коррозии
контролируется не диффузионными
стадиями, а процессом разряда ионов
водорода.
рН=-lg[H+] рН<7
– кислая рН=7 – нейтральная рН>7 –
щелочная
Каждый
Ме имеет свое оптимальное значение рН.
Р
ис.1.
Влияние рН раствора на характер
зависимости скорости коррозии для
различных металлов:1 – железа; 2 –
благородных; 3 – цинка и алюминия; 4 –
никеля и кадмия.
С
корость
движения агрессивной среды в значительной
степени определяет коррозионное
поведение металлов. С увеличением
скорости движения водопроводной воды,
не содержащей значительных количеств
солей, сначала происходит повышение
скорости коррозии железа
из-за увеличения
подвода кислорода к микрокатодам
поверхности (рис. 2, кривая 1).
Последующее снижение скорости коррозии
при достаточно быстром течении воды
объясняется тем, что обилие кислорода
приводит к пассивации анодных участков
(кислород выступает как замедлитель
коррозии). Наконец, при очень больших
скоростях движения воды снова наблюдается
увеличение скорости коррозии металла
вследствие эрозии, т. е. механического
е. механического
разруше- ния защитных пленок или даже
структуры самого металла. При наличии
в растворе значительного количества
активных анионов пассивация может не
наступить, т. е. происходит постоянное
возрастание скорости коррозии металла
с увеличением скорости движения
коррозионной среды, например в морской
воде (рис. 2, кривая 2).
С
повышением температуры скорость
электрохимической коррозии, как правило,
возрастает. Однако зависимость скорости
коррозии от температуры довольно
сложная, так как при этом приходится
учитывать уменьшение растворимости
кислорода с повышением температуры,
изменение структуры образующихся
продуктов коррозии и др. условий.
Металл / Коррозия меди и медных сплавов
Атмосферная коррозия. В атмосферных условиях медь и ее сплавы покрываются тонким равномерным слоем продуктов коррозии, Образование пленки — самозатухающий процесс, т.к. продукты коррозии защищают поверхность, металла от взаимодействия с внешней средой. Процесс образования пленки состоит из двух ровных стадий. Первая — образование первичной пленки, представляющей собой смесь оксидов и чистую закись меди. Время образования этого оксидного слоя — от нескольких месяцев до нескольких лет. С течением времени этот слой приобретает характерный для медных сплавов коричневый цвет. В отдельных случаях этот слой темнеет и может стать черным. При достижении некоторой толщины оксидного слоя на нем начинает образовываться зелёный слой солей меди. Наиболее вероятными химическими соединениями, образующимися на меди в результате коррозии, являются природные минералы. Цвет (состав и строение коррозийного слоя) зависит от присутствия в воздухе различных газов, твёрдых частиц разных веществ и др., а также от состава медного сплава.
Первая — образование первичной пленки, представляющей собой смесь оксидов и чистую закись меди. Время образования этого оксидного слоя — от нескольких месяцев до нескольких лет. С течением времени этот слой приобретает характерный для медных сплавов коричневый цвет. В отдельных случаях этот слой темнеет и может стать черным. При достижении некоторой толщины оксидного слоя на нем начинает образовываться зелёный слой солей меди. Наиболее вероятными химическими соединениями, образующимися на меди в результате коррозии, являются природные минералы. Цвет (состав и строение коррозийного слоя) зависит от присутствия в воздухе различных газов, твёрдых частиц разных веществ и др., а также от состава медного сплава.
В условиях музейного хранения процесс образования сложных по составу пленок на медных сплавах идёт чрезвычайно медленно. Тонкий и равномерный коррозионный слой покрывает всю поверхность, воспроизводя все мельчайше детали декоративной отделки, вплоть до гравировки. На выступающих деталях рельефа он стирается, и сквозь утоньшенный слой просвечивает поверхность металла. Образовавшийся на поверхности медного сплава слой, обладающей определенными физико-химическими свойствами, делающими его защитным и придающими различную окраску — от коричневой и черной до различных оттенков зеленой и голубой, называется патиной Цвет патины зависит не только от длительности взаимодействия с атмосферой и ее состава, но и от состава металла, качества его обработки, т.е. от внешних и внутренних факторов.
Образовавшийся на поверхности медного сплава слой, обладающей определенными физико-химическими свойствами, делающими его защитным и придающими различную окраску — от коричневой и черной до различных оттенков зеленой и голубой, называется патиной Цвет патины зависит не только от длительности взаимодействия с атмосферой и ее состава, но и от состава металла, качества его обработки, т.е. от внешних и внутренних факторов.
Все сформировавшиеся атмосферные патины содержат оксиды и соли. Окись меди — черного цвета, закись — красно-коричневого. Зеленые, синие и голубые цвета и оттенки патине придают различные медные минералы: сульфаты — брошантит, антлерит, средние сульфаты в виде кристаллогидратов с различным количеством кристаллизационной воды, которые являются промежуточными продуктами при образовании зеленой патины; карбонаты меди; малахит и азурит; нитраты; хлориды в виде атакамнта, паратакамита и боталлакита; иногда в патине обнаруживают хлористую медь и кристаллогидрат хлорной меди. Практически все оксиды и соли меди, образующие патину, нерастворимы в воде, негигроскопичны, нейтральны по отношению к металлической меди, за исключением хлористой меди, т.е. патина является естественной защитной и декоративной пленкой.
Практически все оксиды и соли меди, образующие патину, нерастворимы в воде, негигроскопичны, нейтральны по отношению к металлической меди, за исключением хлористой меди, т.е. патина является естественной защитной и декоративной пленкой.
Почвенная коррозия меди и ее сплавов. Коррозионные продукты на археологических изделиях из меди и медных сплавов имеют более сложный состав и строение. В основном они содержат продукты коррозии меди — медные оксиды и соли, как основы слоя, меньше — оксид олова; продуктов коррозии других элементов входящих в состав сплава, как правило, на поверхности предмета не обнаруживают. Коррозионное наслоение имеет слоистое строение с четко выраженными границами слоев. Однако СЛОИ НЕ ПЕРЕКРЫВАЮТ всю поверхность, а располагаются на отдельных участках. . Порядок расположения слоев устойчив. Наружный слой состоит ИЗ углекислых солей меди, соединенных с почвой и органическими остатками. Эти слои, идентичные по своему составу природному минералу малахиту, имеют бугристую неровную поверхность. Малахит часто смешан с азуритом синего цвета. Кроме углекислых солей, во внешнем слое содержится хлорная медь-атакамит. Иногда атакамит образует основную часть внешнего слоя, иногда отдельные пятна светло-зеленого цвета. Наружный слой продуктов коррозии на бронзе устойчив и при изменении внешних условий, например, при извлечении из почвы, превращений в нем не происходит.
Малахит часто смешан с азуритом синего цвета. Кроме углекислых солей, во внешнем слое содержится хлорная медь-атакамит. Иногда атакамит образует основную часть внешнего слоя, иногда отдельные пятна светло-зеленого цвета. Наружный слой продуктов коррозии на бронзе устойчив и при изменении внешних условий, например, при извлечении из почвы, превращений в нем не происходит.
Следующий слой, примыкающий к сохранившемуся металлу, отличается от внешнего и по цвету, и по кристаллическому строению, и по фактуре. Он красно-коричневого цвета. Основу этого образует минерал куприт, представляющий собой закись меди. Куприт очень тверд и хрупок. В куприте наблюдаются включения окиси меди черного цвета. Толщина такого оксидного слоя различна. Иногда вся сердцевина предмета состоит из оксидов с незначительными вкраплениями сохранившегося металла. В отдельных случаях куприт повторяет мельчайшие подробности рельефа.
Однако очень редко куприт образует сплошной слой на поверхности предмета, изолируя нижележащий металл, чаще он имеет трещины и полости.
В некоторых случаях под слоем куприта, а иногда и заменяя его, располагается прослойка металлической восстановленной меди, которая образуется в результате восстановительных процессов из медных солей при электрохимической коррозии. Восстановленная медь может образовывать СПЛОШНОЙ СЛОЙ, так что при очистке создается обманчивое впечатление обнаженного металлического ядра. Иногда восстановленная медь залегает чешуйками, которые при очистке легко снимаются механически.
Между слоем восстановленной меди или куприта и металла расположена наиболее активная, нестабильная медная соль, ХИМИЧЕСКИ неустойчивая и очень гигроскопичная — хлористая медь. Хлористая медь самая опасная коррозионная составляющая археологической бронзы, которая при взаимодействии с влагой окисляется и гидролизуется, превращаясь в зеленую основную хлорную медь атакамит. При этом в реакцию вовлекается металлическая медь, еще не разрушенная коррозией. Хлористая медь обычно серого или белого цвета, иногда окрашена примесями в зеленоватый цвет. За минерализованным слоем идет частично корродированный металл, коррозия в нем развивается по отдельным, наименее коррозионно стойким структурным составляющим. На оловянистой бронзе наблюдаются локальные выделения продуктов коррозии оловянной составляющей бронзы — двуокиси олова, которая соответствует минералу касситериту. Таким образом, характерной особенностью почвенной коррозии
За минерализованным слоем идет частично корродированный металл, коррозия в нем развивается по отдельным, наименее коррозионно стойким структурным составляющим. На оловянистой бронзе наблюдаются локальные выделения продуктов коррозии оловянной составляющей бронзы — двуокиси олова, которая соответствует минералу касситериту. Таким образом, характерной особенностью почвенной коррозии
Коррозионная стойкость
Медно-никелевая оболочка для защиты от коррозии в зоне брызг
Медно-никелевые сплавы
90-10 и 70-30 изначально были разработаны для морских конденсаторов и трубопроводов. Сегодня медно-никелевые сплавы хорошо зарекомендовали себя при работе с морской водой в широком диапазоне условий и применений.
Их коррозионная стойкость достигается за счет образования сложной поверхностной пленки, которая образуется при взаимодействии с самой морской водой, тем самым защищая металл под ней. Общие показатели коррозии для 9Сплавы Cu-Ni 0-10 и 70-30 в морской воде находятся в диапазоне от 0,025 до 0,0025 мм/год. Для большинства применений эти показатели позволяют сплавам прослужить весь срок службы.
Для большинства применений эти показатели позволяют сплавам прослужить весь срок службы.
Из деформируемых медных сплавов медно-никелевые сплавы обладают наилучшей стойкостью к скорости потока морской воды. Как и для всех медных сплавов, важно, чтобы скорость потока оставалась ниже рекомендуемой расчетной скорости, чтобы избежать эрозионной коррозии. В определенных условиях трубопровода максимальная скорость потока для 90-10 Cu-Ni обычно составляет около 3,5 м/с. В более открытых структурах гидродинамические условия иные и расход до начала размыва может быть значительно выше.
Медно-никелевые сплавы не чувствительны к воздействию хлоридов, в отличие от никельсодержащих нержавеющих сталей. Они обладают высокой стойкостью к хлоридной точечной коррозии, щелевой коррозии, коррозионному растрескиванию под напряжением даже при повышенных температурах. Коррозионное растрескивание под напряжением аммиака, которому могут быть подвержены медно-цинковые латунные сплавы, не встречается в медно-никелевых сплавах в морской воде.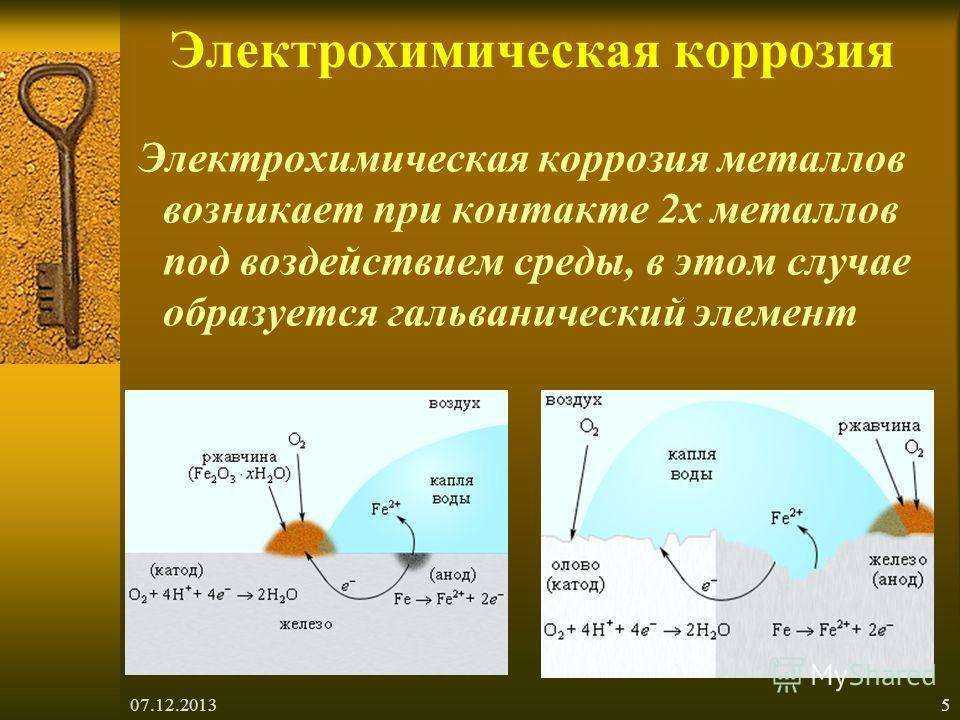
Воздействие сульфидов должно быть ограничено, особенно во время созревания защитной оксидной пленки.
Медно-никелевые сплавы относятся к середине гальванического ряда. Как и во всех биметаллических муфтах, следует избегать неблагоприятных гальванических комбинаций или принимать стандартные профилактические меры.
Содержимое
- Поверхностная пленка: Для обеспечения коррозионной стойкости необходимо образование тонкой защитной поверхностной пленки.
- Общая скорость коррозии: Скорость коррозии снижается с годами после образования хорошей поверхностной пленки.
- Локальная коррозия: информация о стойкости к точечной коррозии хлоридами, щелевой коррозии, коррозионному растрескиванию под напряжением, водородному охрупчиванию; делегирование и очаговая коррозия; воздействие аммиака.
- Точечная и щелевая коррозия: Коэффициенты сопротивления, скорость проникновения, сравнение с другими материалами.
- Коррозионное растрескивание под напряжением: Сопротивление коррозионному растрескиванию под напряжением выгодно для использования в секциях удаления воздуха.
- Влияние скорости: Информация о допустимых скоростях потока для 90-10 и 70-30 Cu-Ni в конденсаторах, теплообменниках, трубопроводных системах, пожарных сетях; предпочтительные сплавы для установок MSF; опыт работы с корпусами кораблей.
- Песчаная эрозия: загрузка песком, влияние размера частиц и C71640 для тяжелых нагрузок.
- Гальванические свойства: свойства, эффекты и рекомендации для обшивки зон брызг и корпусов лодок.
- Коррозия сульфидов: Загрязненные и сульфатредуцирующие воды могут подвергаться коррозионному воздействию сульфидов. Ссылки на ссылки по этой теме.
- Очистка морской воды: сульфат железа и хлорирование.
- Коррозия в конденсаторах и системах теплообмена: Полная статья о коррозионной стойкости конденсаторов и систем теплообмена.
Интерактивная презентация
Посетите нашу интерактивную презентацию, чтобы получить визуальный обзор свойств 90-10 и 70-30 Cu-Ni, коррозионной стойкости, поведения в условиях биологического обрастания, областей применения и рекомендаций по достижению оптимального обслуживания.
Дополнительные ссылки: Общая коррозия, аммиачная коррозия, локальная коррозия, хлорированная коррозия, песчаная эрозия, сульфидная коррозия и эффекты скорости.
Применение медно-никелевого сплава UNS C70600 для морской воды,
Вильгельм Шлейх, документ № 5222, , КОРРОЗИЯ/2005, Хьюстон, NACE International,
.Медные сплавы в морской воде: предотвращение коррозии,
Роджер Фрэнсис, публикация 225, стр. 20, 9.0050 2016 , CDA UK,
.
Медно-никелевые сплавы для защиты от коррозии в морской воде и защиты от обрастания — обзор последних достижений техники,
К.А. Пауэлл и Х.Т. Михельс, , Коррозия 2000 г., NACE International,
.Стойкость медно-никелевых сплавов к коррозии и биообрастанию,
Пауэлл, Калифорния, и Михелс, Х. Т., 9 лет.0062 Технический отчет семинара , 7044-1919, , Коррозия 2000, NACE,
Оригинальное название: Применение медно-никелевых сплавов в морских системах.
.Защита трубопроводов системы морской воды и труб теплообменника на надводных кораблях и подводных лодках HM в системах морской воды ,
Стандарт 02-781, выпуск 2, , Министерство обороны Великобритании,
Недоступно в Интернете, но запросы можно направлять в службу поддержки Dstan по адресу [email protected].
.Медно-никелевые конденсаторы и системы теплообменников,
Кирк В. и Татхилл А., Технический отчет 7044-19.19, , Семинар CDA Inc. Применение медно-никелевых сплавов в морских системах,
.
Разработка медных сплавов очень высокой прочности, устойчивых к водородному охрупчиванию и коррозионному растрескиванию под напряжением,
CDS Так, 9 лет0050 Апрель 2005 г. , Ежегодная конференция и выставка Corrosion/2005, Хьюстон, ©NACE,
.Типичные неисправности трубных систем морской воды CuNi 90/10 и способы их предотвращения,
Шлейх, Вильгельм, , Eurocorr 2004, NACE,
.
Коррозия медно-цинковых и медно-никелевых сплавов в геотермальном растворе (Конференция)
Коррозия медно-цинковых и медно-никелевых сплавов в геотермальном растворе (Конференция) | ОСТИ. GOV
GOV
перейти к основному содержанию
- Полная запись
- Другое связанное исследование
- Авторов:
Миллер, Ричард Л.
- Дата публикации:
- Исследовательская организация:
- EG & G Idaho, Inc., Айдахо-Фолс, Айдахо (США). Национальная лаборатория Айдахо
- Организация-спонсор:
- USDOE
- Идентификатор ОСТИ:
- 12103505
- Номер(а) отчета:
- КОНФ-7
-6
- Номер контракта с Министерством энергетики:
- AC07-76ID01570
- Тип ресурса:
- Конференция
- Отношение ресурсов:
- Конференция: ежегодное собрание AIME, Новый Орлеан, Луизиана (США), 18–21 февраля 1979 г.

- Страна публикации:
- США
- Язык:
- Английский
Форматы цитирования
- MLA
- АПА
- Чикаго
- БибТекс
Миллер, Ричард Л. Коррозия медно-цинковых и медно-никелевых сплавов в геотермальном растворе . США: Н. П., 1979.
Веб.
Копировать в буфер обмена
Миллер, Ричард Л. Коррозия медно-цинковых и медно-никелевых сплавов в геотермальном растворе . Соединенные Штаты.
Копировать в буфер обмена
Миллер, Ричард Л. 1979.
1979.
«Коррозия медно-цинковых и медно-никелевых сплавов в геотермальной воде». Соединенные Штаты. https://www.osti.gov/servlets/purl/12103505.
Копировать в буфер обмена
@статья{osti_12103505,
title = {Коррозия медно-цинковых и медно-никелевых сплавов в геотермальном растворе},
автор = {Миллер, Ричард Л.},
abstractNote = {},
дои = {},
URL = {https://www.osti.gov/biblio/12103505},
журнал = {},
номер =,
объем = ,
место = {США},
год = {1979},
месяц = {1}
}
Копировать в буфер обмена
Просмотр конференции (0,88 МБ)
Дополнительную информацию о получении полнотекстового документа см. в разделе «Доступность документа». Постоянные посетители библиотек могут искать в WorldCat библиотеки, в которых проводится эта конференция.
