Медь характеристика химического элемента: Характеристика переходных элементов (меди, цинка, хрома, железа) по их положению в периодической системе химических элементов Д.И. Менделеева и особенностям строения их атомов / Справочник :: Бингоскул
Содержание
Эссенциальные микроэлементы: что это, их роль в жизнедеятельности человека
Общие сведения
Минеральный состав внутриклеточной жидкости строго поддерживается на определенном уровне.
Элементы вместе с водой являются строительным материалами, кофакторами и катализаторами биохимических реакций, стабилизаторами белков и ферментов, обеспечивая постоянство осмотического давления, кислотно-щелочного баланса, процессов всасывания, секреции, кроветворения, костеобразования, свертывания крови. Благодаря присутствию элементов осуществляется процесс мышечного сокращения, нервной проводимости и внутриклеточного дыхания. Химические элементы в организме находятся в виде различных соединений и солей, их влияние на организма обусловлено дозой элемента. Для каждого элемента существует свой физиологический рабочий диапазон концентраций, обеспечивающий нормальное протекание физиологических реакций в организме.
Нарушенная экология, возросший темп жизни с неизбежным нарастанием стрессовых ситуаций, методы обработки продуктов питания, «убивающие» биологически активные вещества ведут к нарушению металло-лигандного гомеостаза и сдвигу равновесия в сторону увеличения или уменьшения концентрации элемента. Накопление элементов или их дефицит способствует активации альтернативных путей метаболизма, который в ряде случаев приводят к патологическим состояниям.
Накопление элементов или их дефицит способствует активации альтернативных путей метаболизма, который в ряде случаев приводят к патологическим состояниям.
Химические элементы классифицируются в зависимости от их роли в организме. 98% тела человека состоит из органических элементов: H, C, N, O. Вместе с неорганическими элементами Na, Mg, K, Ca, P, S, Cl они составляют основу клеток и тканей, выполняя структурообразующую функцию. К эссенциальным или жизненно необходимым микроэлементам относятся Mn, Fe, Co, Ni, Cu, Zn, Mo, Se, I, при их отсутствии нарушаются базовые реакции деления и размножение клеток. К условно-эссенциальным микроэлементам относятся Li, V, Cr, B, F, Si, As, их роль до конца не определена. Существуют также «токсические металлы», которые в минимальных концентрациях способны оказывать стимулирующее воздействие на организм, но в высоких концентрациях проявляют токсические эффекты.
Микроэлементы составляют лишь 0,02% организма, но способны изменять протекание важнейших биологических реакций.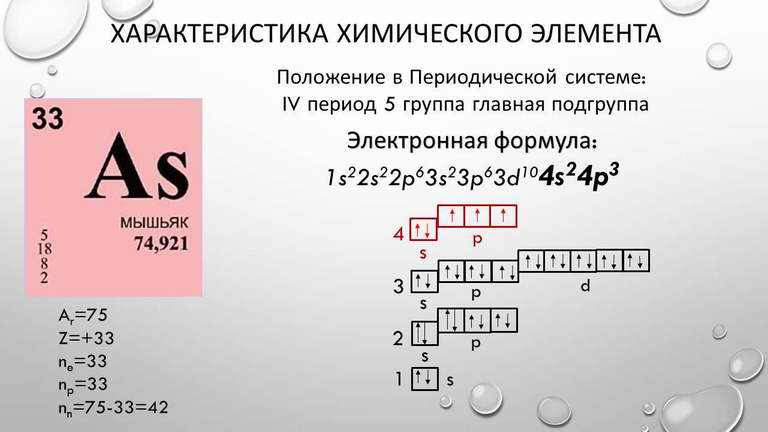 Анализ волос или мочи позволяет выявить избыточное накопление микроэлементов или их дефицит. Содержание микроэлементов в волосах отражает микроэлементный статус организма в целом, поэтому пробы волос являются интегральным показателем минерального обмена. Волосы помогают диагностировать хронические заболевания, когда они себя еще ничем не проявляют.
Анализ волос или мочи позволяет выявить избыточное накопление микроэлементов или их дефицит. Содержание микроэлементов в волосах отражает микроэлементный статус организма в целом, поэтому пробы волос являются интегральным показателем минерального обмена. Волосы помогают диагностировать хронические заболевания, когда они себя еще ничем не проявляют.
Железо (Fe)
Железо является жизненно необходимым элементом для организма. Железо входит в состав гемсодержащих белков (гемоглобин и миоглобин) и участвует в переносе кислорода. Железо также входит в состав цитохромов (сложные белки, относящиеся к классу хромопротеидов), участвующих в процессах тканевого дыхания.
Общее содержание железа в организме человека составляет 3-5 г. Из этого количества 57% находится в гемоглобине крови, 23% — в тканях и тканевых ферментах (ферритин и гемосидерин), а остальные 20% — депонированы в печени, селезенке, костном мозге, мышцах и представляют собой «физиологический резерв» железа. Железо существует в двух формах: окисленной (Fe3+) и воcстановленной (Fe2+). Восстановленная форма лучше усваивается организмом. Только 10 % поступившего железо всасывается в кишечнике.
Железо существует в двух формах: окисленной (Fe3+) и воcстановленной (Fe2+). Восстановленная форма лучше усваивается организмом. Только 10 % поступившего железо всасывается в кишечнике.
Физиологическая потребность в железе:
- мужчины: 8–10 мг/сут;
- женщины: 15–20 мг/сут;
- беременных женщины: 30–40 мг/сут;
- дети: 4–18 мг/сут.
В больших количествах восстановленная форма железа (гемовое железо), содержится: в свиной печени, говяжьих почках, сердце и печени. Окисленная форма железа (негемовое железо) содержится в неживотных продуктах: непросеянной муке, сушеных персиках, орехах, бобах, спарже, овсяном толокне.
Недостаток железа приводит к тяжелым расстройствам, наиболее важным из которых является железодефицитная анемия. Железодефицитная анемия может привести к сердечной недостаточности.
Избыточное накопление железа приводит к отложению металла в органах (печень, поджелудочная железа, суставы, сердце). Явления отравления железом выражаются рвотой, диареей, падением артериального давления, параличом ЦНС и воспалением почек. При лечении железом могут развиться запоры, так как железо связывает сероводород, что ослабляет моторику кишечника. Избыток железа в организме может привести к дефициту меди, цинка, хрома и кальция, а также к избытку кобальта.
Явления отравления железом выражаются рвотой, диареей, падением артериального давления, параличом ЦНС и воспалением почек. При лечении железом могут развиться запоры, так как железо связывает сероводород, что ослабляет моторику кишечника. Избыток железа в организме может привести к дефициту меди, цинка, хрома и кальция, а также к избытку кобальта.
Йод (I)
Йод необходим на всех этапах жизнедеятельности. Период младенчества и раннего детства являются критическими в отношении дефицита йода. Йод входит в состав гормонов щитовидной железы тироксина (T4) и трийодтиронина (T3). Йод необходим для роста и дифференцировки клеток всех тканей организма человека, внутриклеточного дыхания, регуляции трансмембранного транспорта натрия и гормонов.
Общее количество йода в организме составляет 25 мг, из них 15 мг аккумулирует щитовидная железа. Значительное количество йода содержится в печени, почках, коже, волосах, ногтях, яичниках и предстательной железе.
Физиологическая потребность в йоде:
- взрослые: 100–150 мкг/сут;
- беременные: 175–200 мкг/сут;
- дети: от 60 до 150 мкг/сут.
Богатым источником йода являются водоросли, овощи, выращенные на почве обогащенной йодом, лук, морепродукты.
При недостаточном поступлении йода у взрослых увеличиваются размеры щитовидной железы, замедляется основной обмен, наблюдается падение артериального давления. У детей недостаток йода сопровождается резкими изменениями всей структуры тела: ребенок отстает в умственном и физическом развитии.
Избыток йода в организме наблюдается при гипертиреозе. Развивается Базедова болезнь, сопровождающаяся экзофтальмом, тахикардией, раздражительностью, мышечной слабостью, потливостью, исхуданием, склонностью к диарее. Повышение основного обмена ведет к гипертермии, дистрофическим изменениям кожи и ее придатков, раннему поседению, депигментации кожи на ограниченных участках (витилиго), атрофии мышц.
Марганец (Mn)
Важен для репродуктивных функций и нормальной работы центральной нервной системы. Марганец участвует в синтезе нейромедиаторов, улучшает мышечные рефлексы, обеспечивает развитие соединительной и костной ткани, увеличивает утилизацию жиров, усиливает эффекты инсулина.
3–5 % поступившего марганца всасывается. Наиболее богаты марганцем трубчатые кости и печень, поджелудочная железа. Марганец содержится в клетках, богатых митохондриями.
Физиологическая потребность в марганце:
- взрослые: 2–5 мг/сут;
- для детей в 2 раза выше.
Особенно богаты марганцем чай, растительные соки, цельные злаковые, орехи, зеленые овощи с листьями, горох, свёкла.
При недостатке марганца нарушаются процессы окостенения во всем скелете, трубчатые кости утолщаются и укорачиваются, суставы деформируются. Нарушается репродуктивная функция яичников и яичек.
Избыток марганца усиливает дефицит магния и меди.
Медь (Cu)
Медь принимает участие в поддержание эластичности связок, сухожилий, кожи и стенок легочных альвеол, стенок капилляров, а также прочности костей. Медь входит в состав защитных оболочек нервных волокон, участвует в процессах пигментации, так как входит в состав меланина. Медь влияет на углеводный обмен, посредством усиления процессов окисления глюкозы и торможения распада гликогена мышц и печени. Медь обладает противовоспалительными действиями, помогает при борьбе с бактериальными агентами. Медь является кофактором ферментов антиоксидантной защиты и помогает нейтрализовать действие свободных радикалов.
Общее содержание меди в организме человека составляет примерно 100–150 мг. Лучше всего организм усваивает двухвалентную медь. В тонком кишечнике всасывается до 95% меди, поступившей с пищей. Основное «депо» меди в организме — печень, поскольку синтезирует белок-переносчик меди церулоплазмин.
Физиологическая потребность в меди:
- взрослые: 1 мг/сут;
- дети: от 0,5 до 1 мг/сут.

Медь содержится в овощах, бобовых, морепродуктах, яблоках.
При недостатке меди в организме наблюдаются: задержка роста, анемия, дерматозы, депигментация волос, частичное облысение, потеря аппетита, сильное исхудание, понижение уровня гемоглобина, атрофия сердечной мышцы. Избыток меди приводит к дефициту цинка и мoлибдена, а также марганца.
Молибден (Мо)
Способствует метаболизму углеводов и жиров, является важной частью фермента, отвечающего за утилизацию железа, в связи с чем помогает предупредить анемию. Принимает участие в обмене мочевой кислоты, включении фтора в состав эмали зубов, гемопоэзе.
Биодоступность молибдена составляет 50%. Молибден не депонируется в организме, а распределяется между клетками крови.
Физиологическая потребность в молибдене:
- взрослые: 45–100 мкг/сут;
- дети: от 0,5 до 1 мг/сут.
Содержится в темно-зеленых листовых овощах, неочищенном зерне, бобовых. Проявления недостаточности изучены плохо. Повышенное содержание в организме встречается очень редко.
Проявления недостаточности изучены плохо. Повышенное содержание в организме встречается очень редко.
Селен (Sе)
Элемент антиоксидантной защиты, хорошо сочетается с витамином Е. Селен помогает поддерживать должную эластичность тканей. Селен усиливает иммунитет, поэтому активно используется в онкологической практике, в лечении гепатитов, панкреатитов, кардиомиопатий. Селен защищает организм от тяжёлых металлов.
Всасывается в тонком кишечнике, депонируется в почках, печени, костном мозге.
Физиологическая потребность в селене:
- женщины: 50 мкг/сут;
- беременные: 65 мкг/сут;
- мужчины: 70 мкг/сут;
- дети: 10-50 мкг/сут.
В чистом виде встречается в природе редко, главным образом в виде примеси к сернистым металлам. Присутствует в чесноке, сале, отрубях, белых грибах, растительных маслах, морских водорослях.
При дефиците селена в организме усиленно накапливаются мышьяк и кадмий, которые, в свою очередь, еще больше усугубляют его дефицит.
Избыток селена приводит к гепато- и холецистопатиям, изменениям работы нервно-мышечного аппарата (боли в конечностях, судороги, чувство онемения). Избыток может привести к дефициту кальция.
Цинк (Zn)
Цинк входит в состав более 300 ферментов, чем объясняет его влияние на углеводный, жировой и белковый обмен веществ, на окислительно-восстановительные процессы, регуляцию активности генов. Цинк связан с правильным функционированием репродуктивной, неврологической, иммунной систем, ЖКТ и кожи. Присутствие микроэлемента важно для нормального сперматогенеза, органогенеза, работы нейромедиаторов и панкреатических ферментов, правильного развития тимуса, эпителизации ран в процессе заживления и ощущения вкуса.
В организме содержится около 1,5–3 г цинка. Цинк всасывается в тонком кишечнике. Медь является антагонистом цинка, и конкурирует с цинком за всасывание в кишечнике. 99% цинка находится внутриклеточно, 1% — в плазме. Цинк присутствует во всех органах и тканях, но в большей степени цинк депонируют предстательная железа, семенники, мышцы, кожа, волосы.
Физиологическая потребность в цинке составляет: 12 мг/сут для взрослых, 3–2 мг/сут для детей.
Наиболее богаты цинком дрожжи, пшеничные, рисовые и ржаные отруби, зерна злаков и бобовых, какао, морепродукты, грибы, лук, картофель.
При дефиците цинка наблюдается задержка роста, перевозбуждение нервной системы и быстрое утомление. Поражение кожи происходит с утолщением эпидермиса, отеком кожи, слизистых оболочек рта и пищевода, ослаблением и выпадением волос. Недостаточное поступление цинка приводит к бесплодию. Дефицит цинка может приводить к усиленному накоплению железа, меди, кадмия, свинца.
При цинковом отравлении наступает фиброзное перерождение поджелудочной железы. Избыток цинка задерживает рост и нарушает минерализацию костей.
Кобальт (Co)
Входит в состав витамина В12, участвует в обмене гормонов щитовидной железы, подавляет обмен йода, регулирует гемопоэз, усиливает всасываемость железа.
В организме 1,5 г кобальта. Биодоступность кобальта 20%. В организм кобальт депонируется в печени, костной ткани и мышцах.
Биодоступность кобальта 20%. В организм кобальт депонируется в печени, костной ткани и мышцах.
Физиологическая потребность в кобальте составляет: 10 мкг/сут для взрослых.
Кобальт содержится в печени, молоке, овощах.
Дефицит кобальта связан с В12-дефицитной анемией, вегетарианством или паразитарной инвазией. Избыток кобальта наблюдается при интоксикации кобальта (вредное производство, разрушение ортопедических имплантантов).
Никель (Ni)
Никель пролонгирует эффекты инсулина, участвует в окислении аскорбиновой кислоты, ускоряет образование дисульфидных групп.
Никель всасывается в кишечнике, биодоступность от 1 до 10 %. Запасы никеля находятся в поджелудочной железе, легких, сердце.
Физиологическая потребность в никеле составляет: 100–200 мкг/сут для взрослых.
Богаты никелем чай, гречиха, морковь и салат.
Дефицит никеля не описан. Избыток никеля наблюдается при его токсическом поступлении, злокачественных новообразованиях легких, ожогах, инсультах и инфарктах. Избыток может проявлять потерей пигментацией кожи.
Избыток может проявлять потерей пигментацией кожи.
Сталь СТ3: химический состав и свойства
Сталь – это сплав двух элементов железа, углерода, легирующих примесей, которые добавляют в металл для придания ему нужных свойств. Ст3 – это конструкционная углеродистая сталь обыкновенного качества, широко распространена во всех сферах промышленного производства. Является самым распространенным металлом для несущих строительных конструкций. Из этого сплава делают лист, профиль, трубу, двутавры и другой металлопрокат.
Химический состав
Марки стали различаются по составу, который определяет механические характеристики, область применения и свариваемость материала.
Небольшое количество легирующих элементов и высокая пластичность Ст3 делает её самым распространённым сплавом, применяемым в строительстве. Ни одна стройка не может обойтись без проката из Ст3.
Химический состав материала включает следующие элементы:
- железо – 97%;
- углерод – 0,14-0,22%;
- никель, медь, хром – каждый не больше 0,3%;
- марганец — 0,4-0,65%;
- кремний — 0,05-0,17%;
- мышьяк менее 0,08%;
- серы не более 0,05;
- фосфор менее 0,04%.

Углерод определяет твёрдость, прочность, пластичность, показатели свариваемости, физико-механические свойства стали. Сера и фосфор – вредные примеси.
Легирующие элементы в структуре этого сплава, которые влияют на его характеристики – это марганец, хром, медь и никель.
Физические и механические свойства
Сталь Ст3 это самая используемая марка металла, применяемая в строительстве и в машиностроении. Низкая цена в сочетании с физико-механическими показателями, которые определили популярность этого материала.
Перечислим механические показатели Ст3:
- предел текучести 205-255 МПа;
- временное сопротивление разрыву 370-490 МПа;
- относительное удлинение 22-26%;
- ударная вязкость при температуре:
- 20 0С составляет 108 Дж/см2;
- 20 0С равняется 49 Дж/см2;
- твёрдость HB 10-1: 131 МПа.
Прочностные показатели предел текучести и относительное удлинение – зависят от толщины и формы проката. Чем больше толщина металлопроката, тем ниже значение показателя, самые низкие показатели у труб, высокие показатели у листов, толщиной 5-10 мм.
Чем больше толщина металлопроката, тем ниже значение показателя, самые низкие показатели у труб, высокие показатели у листов, толщиной 5-10 мм.
Плотность Ст3 составляет 7850 кг/м3. Сплав относится к хорошо свариваемым материалам.
Маркировка Ст3
Классифицируются низкоуглеродистые стали по составу степени расселения. Раскисление – это процесс удаления из расплава кислорода, являющегося вредной примесью. Он ухудшает механические и другие свойства материала.
По степени раскисления сплав бывает трёх видов:
- спокойная обозначается «сп»;
- полуспокойная – маркировка «пс»;
- кипящая – «кп».
Проведём расшифровку материала Ст3Гпс. Буквы «Ст» обозначают сталь. Цифра «3» – это процентное содержание углерода, чем больше цифра, тем больший процент углерода содержится в металле. Буква Г — пишется, если процент содержания марганца в 0,8% и более. ПС – полуспокойная.
Разновидности сплава Ст3
Спокойная сталь раскисляется с использованием марганца, кремния и алюминия. Это дорогой и высококачественный материал. За счёт однородной структуры спокойный металл пластичнее и коррозионно устойчивее. Применяется для изготовления несущих ответственных конструкций, узлов машин, механизмов, которые работают при отрицательных температурах и динамических нагрузках.
Это дорогой и высококачественный материал. За счёт однородной структуры спокойный металл пластичнее и коррозионно устойчивее. Применяется для изготовления несущих ответственных конструкций, узлов машин, механизмов, которые работают при отрицательных температурах и динамических нагрузках.
Полуспокойная сталь раскисляется марганцем и алюминием. Показатели прочности и пластичности у этого материала близки к спокойной стали, но уступают ей. Применяется при возведении несущих металлоконструкций, где требования к прочностным показателям ниже, чем у конструкций из спокойного металла. Преимуществом этого сплава – его стоимость дешевле.
Кипящая сталь самая дешёвая, раскисляется только марганцем. При заливке этого расплава в слябы происходит активное кипение – выделяются содержащиеся в сплаве газы. В разных частях слитка может иметь неоднородные свойства. Кипящая металл хрупкий, плохо сваривается и подвержена коррозии. Применяется для изготовления конструкций, к которым не предъявляются высокие требования.
Применение Ст3
Из спокойной стали производят: лист, уголок, швеллер, арматуру, двутавровую балку и другой металлопрокат, который используют для изготовления:
- трубопроводной арматуры, труб, фасонных изделий;
- мостовых кранов, несущих железнодорожных металлоконструкций, каркасов зданий, внутрицеховых металлоконструкций, железнодорожных и автомобильных мостов;
- ёмкостей для хранения воды и нефтепродуктов, железнодорожных вагонов, цистерн для перевозки нефтепродуктов;
- кузовов автомобилей, корпусов судов;
- других ответственные конструкции, применяемых во всех отраслях промышленности, работающих при низких температурах окружающего воздуха, в условиях динамических знакопеременных нагрузок.
Полуспокойная сталь используется для тех же металлоконструкций и деталей, что и спокойная, но при условии, что эти изделия не будут работать при температурах ниже -10 0С.
Кипящая сталь. Применяется для малонагруженных, второстепенных, ненагруженных металлоконструкций, которые работают при постоянных нагрузках. Из неё изготавливают заборы, заземление, кронштейны, листовую обшивку, другие элементы зданий и металлоконструкций.
Из неё изготавливают заборы, заземление, кронштейны, листовую обшивку, другие элементы зданий и металлоконструкций.
Характеристики меди и реакция металла с азотной кислотой
Похоже, вы зашли на наш сайт из
Германия .
Пожалуйста, перейдите на наш региональный сайт для получения более актуальных цен, сведений о продуктах и специальных предложениях.
Выбрать другую страну
Стабильный металл Vs. Сильный окислитель
[Депозитные фотографии]
Медь — один из старейших известных металлов, который использовался людьми с древних времен. На латыни медь известна как cuprum, а ее атомный номер — 29. В периодической таблице Менделеева медь находится в четвертом периоде, в первой группе.
В периодической таблице Менделеева медь находится в четвертом периоде, в первой группе.
Физические и химические свойства меди
Встречающаяся в природе медь представляет собой тяжелый металл розово-красного цвета с пластичной и мягкой структурой. Температура кипения составляет более 1000 градусов по Цельсию. Купрум является хорошим проводником электричества и тепла и плавится при температуре 1084 градусов по Цельсию. Плотность металла 8,9.г/см3, а в природе встречается в основном виде.
Согласно электронной формуле атома меди он имеет 4 уровня. На 4-s валентной орбитали находится один электрон. При химическом взаимодействии с другими веществами от атома отщепляется от одной до трех отрицательно заряженных частиц (электронов), в результате чего образуются соединения меди со степенью окисления +3, +2, +1. Максимальную стабильность проявляют двухвалентные производные меди.
[Депозитные фотографии]
Медь — вещество с низкой способностью к взаимодействию. Различают две основные степени окисления металла, проявляющиеся в соединениях: +1 и +2. Вещества, у которых эти значения изменяются до +3, встречаются редко. Медь взаимодействует с углекислым газом, воздухом, соляной кислотой и другими соединениями при очень высоких температурах. На поверхности металла образуется защитная оксидная пленка. Этот металл защищает медь от дальнейшего окисления, делает ее стабильной и придает металлу низкую активность.
Различают две основные степени окисления металла, проявляющиеся в соединениях: +1 и +2. Вещества, у которых эти значения изменяются до +3, встречаются редко. Медь взаимодействует с углекислым газом, воздухом, соляной кислотой и другими соединениями при очень высоких температурах. На поверхности металла образуется защитная оксидная пленка. Этот металл защищает медь от дальнейшего окисления, делает ее стабильной и придает металлу низкую активность.
Металл взаимодействует с простыми веществами – галогенами, селеном, серой. Металл способен образовывать двойные соли или комплексные соединения. Ядовиты почти все комплексные соединения этого элемента, кроме оксидов. Вещества, образованные одновалентной медью, легко окисляются до двухвалентных эквивалентов.
В химических реакциях медь выступает как малоактивный металл. Металл не растворяется в воде в обычных условиях. В сухом воздухе металл не подвергается коррозии, но при нагревании поверхность меди покрывается черным налетом окиси. Химическая стабильность элемента проявляется в его стойкости к воздействию углерода, сухих газов, ряда органических соединений, спиртов и фенольных смол. Для меди характерны сложные реакции, при которых выделяются окрашенные соединения. Медь имеет сходство с металлами щелочной группы, так как образует одновалентные производные.
Химическая стабильность элемента проявляется в его стойкости к воздействию углерода, сухих газов, ряда органических соединений, спиртов и фенольных смол. Для меди характерны сложные реакции, при которых выделяются окрашенные соединения. Медь имеет сходство с металлами щелочной группы, так как образует одновалентные производные.
Медь — реакция с азотной кислотой
Медь растворяется в азотной кислоте. Эта реакция происходит потому, что металл окисляется сильным реагентом.
Молекула азотной кислоты
[Депозитные фотографии]
Азотная кислота (разбавленная и концентрированная) проявляет окислительные свойства, с растворением меди. При реакции металла с разбавленной кислотой образуются нитрат меди и двухвалентный оксид азота в соотношении 75% и 25%. Уравнение реакции
8HNO₃ + 3Cu → 3Cu(NO3)₂ + 2NO + 4H₂O
В процессе реакции принимают участие 1 моль меди и 3 моля концентрированной азотной кислоты. При растворении меди раствор сильно нагревается, происходит термический распад окислителя и выделяется дополнительное количество оксида азота. Уравнение реакции
При растворении меди раствор сильно нагревается, происходит термический распад окислителя и выделяется дополнительное количество оксида азота. Уравнение реакции
4HNO₃ + Cu → Cu(NO3) + 2NO₂ + 2H₂O
Этот способ растворения меди имеет свои недостатки – при реакции меди с азотной кислотой выделяется большое количество оксида азота. Для улавливания или нейтрализации оксида азота требуется специальное оборудование, поэтому этот процесс слишком дорог. Растворение меди в азотной кислоте считается завершенным, когда перестают образовываться летучие оксиды азота. Температура реакции составляет от 60 до 70 градусов Цельсия. Следующий этап – слив раствора из химического реактора. На дне реактора остаются куски меди, не вступившие в реакцию. В полученную жидкость добавляют воду, и ее фильтруют. Нажмите здесь, чтобы узнать о свойствах меди во взаимодействии с другими веществами.
Реакция азотной кислоты и меди, проиллюстрированная экспериментом
Всю реакцию азотной кислоты и меди можно проследить с помощью опыта: поместите кусок меди в концентрированную азотную кислоту. Выделяется коричневый газ – сначала медленно, затем интенсивнее. Раствор становится зеленым. Если в процессе реакции добавить много меди, раствор постепенно станет синим. Реакция меди с азотной кислотой протекает с выделением тепла и ядовитого газа, имеющего едкий запах.
Выделяется коричневый газ – сначала медленно, затем интенсивнее. Раствор становится зеленым. Если в процессе реакции добавить много меди, раствор постепенно станет синим. Реакция меди с азотной кислотой протекает с выделением тепла и ядовитого газа, имеющего едкий запах.
Реакция меди и концентрированной азотной кислоты является окислительно-восстановительной реакцией. Восстановитель – металл, окислитель – азотная кислота. Уравнение реакции
Cu + 4HNO₃ = Cu(NO3)₂ + 2NO₂↑ + 2H₂O
Реакция экзотермическая, поэтому при самопроизвольном нагревании смеси она ускоряется.
Реакция меди с азотной кислотой начинается при комнатной температуре. Металл покрывается пузырьками, которые начинают подниматься на поверхность и наполняют пробирку коричневым газом – NO₂ (ядовитый ядовитый диоксид азота с едким запахом). Этот газ в 1,5 раза тяжелее воздуха.
Реакция меди с азотной кислотой протекает в две стадии: на первой стадии кислота окисляет медь до оксида меди с выделением диоксида азота; на второй стадии оксид меди реагирует с новыми порциями кислоты, образуя нитрат меди Cu(NO₃)₂. Смесь нагревается, и реакция ускоряется.
Смесь нагревается, и реакция ускоряется.
Образец тригидрата нитрата меди(II)
[Википедия]
В результате металл растворяется, и образуется раствор нитрата меди. Нитрат меди придает раствору зеленый или синий цвет (это будет зависеть от количества используемой воды).
У нас есть еще статьи по химии для вас:
- Эксперимент «Горячий лед».
Как сделать горячий лед в домашних условиях - Удивительный трюк с антигравитационной водой
Отличный простой эксперимент, который удивит и детей, и взрослых
Вы можете провести десятки химических опытов дома!
Трансмутация
Учить больше
Попробуй это
В их стихии
News Story
Химики Нью-Йоркского университета делятся своими фаворитами в честь 150-летия периодической таблицы
Читаете это с мобильного телефона? Ваш телефон содержит не менее 30 различных природных элементов, включая литий. Или, может быть, вы пьете сельтерскую воду — соединение двух элементов (углерода и кислорода в виде углекислого газа), растворенное в двух других элементах (водород и кислород в виде воды).
Или, может быть, вы пьете сельтерскую воду — соединение двух элементов (углерода и кислорода в виде углекислого газа), растворенное в двух других элементах (водород и кислород в виде воды).
Химические элементы, из которых состоит все вокруг нас, празднуют каждый день, но 2019 год особенный, потому что он отмечает 150-летие периодической таблицы. Разработанный русским ученым Дмитрием Менделеевым в 1869 году (с участием многих других ученых до и после Менделеева), знакомый плакат на стенах кабинета химии начинался как новый способ сортировки и классификации элементов.
В периодической таблице Менделеева он организовал 63 элемента, известных в 1869 г.по их атомному весу, группируя те, которые имеют схожие свойства. Он также предусмотрительно оставил на столе свободные места, чтобы предвидеть элементы, которые еще не были обнаружены.
Менделеев был на верном пути — за последующие полтора века ученые добавили много новых элементов в пробелы в таблице, доведя сегодня число элементов до 118. Как отметило ранее в этом году Американское химическое общество, «изменения в периодической таблице продолжаются и по сей день и, вероятно, продолжат удивлять нас в будущем. Совсем недавно, в 2016 году, четыре последних пробела в периоде 7 — элементы 113, 115, 117 и 118 — были официально заполнены». Как и многие элементы, два из новейших названы в честь мест, где проводились исследования по созданию элементов: московий и теннессин.
Как отметило ранее в этом году Американское химическое общество, «изменения в периодической таблице продолжаются и по сей день и, вероятно, продолжат удивлять нас в будущем. Совсем недавно, в 2016 году, четыре последних пробела в периоде 7 — элементы 113, 115, 117 и 118 — были официально заполнены». Как и многие элементы, два из новейших названы в честь мест, где проводились исследования по созданию элементов: московий и теннессин.
В честь 150-летия таблицы Менделеева журнал NYU News попросил группу химиков Нью-Йоркского университета назвать свои любимые элементы и рассказать нам, почему они их любят. От лития (№ 3) до галлия (№ 31) — вот их выбор.
Литий
Литий — мой самый любимый элемент в наши дни. Это один из самых легких элементов, и он невероятно преображает. Все наши сотовые телефоны и компьютеры оснащены литий-ионными аккумуляторами, а Нобелевская премия по химии в этом году была присуждена за разработку литий-ионных аккумуляторов.
В моей лаборатории мы хорошо знакомы с этим элементом, поскольку разрабатываем методы, которые позволяют нам заглянуть внутрь батарей, чтобы определить, хорошо ли они работают, и получить подсказки о том, как улучшить батареи, продлить срок их службы и обеспечить их безопасность. .
.
Углерод
Дирк Траунер, Дженис Катлер, профессор химии
Мне нравится углерод, потому что правила, по которым связываются атомы углерода, очень просты, но структуры, которые можно создать с их помощью (и несколькими более легкими и тяжелыми второстепенными актерами), такой разнообразный. После одной лекции студенты могут предложить молекулы, которые никогда раньше не создавались и о которых даже не думали, но которые, скорее всего, стабильны. Вы можете поставить ферму (и свою карьеру) на углерод!
Азот
Нед Симан, Маргарет и Герман Сокол Профессор химии
Азот
Азот. Это элемент, который присущ двум семантофоретическим молекулам [которые несут информацию] биологии, нуклеиновым кислотам и белкам. Без азота биология в основном состоит из сахара и жира.
Кремний
Кит Верпель, Маргарет и Герман Сокол Профессор медицинской химии
Кремний
Кремний. Он есть почти во всем: в камнях, песке, компьютерах, в этих маленьких пакетиках, которые вы найдете внутри обуви. Этот элемент больше всего похож на углерод, но он настолько не похож на углерод, что приводит к неожиданному химическому поведению, которое может оказаться действительно полезным. И просто для протокола: нет, я не думаю, что может существовать жизнь в том виде, в каком мы ее знаем, на основе кремния вместо углерода.
Этот элемент больше всего похож на углерод, но он настолько не похож на углерод, что приводит к неожиданному химическому поведению, которое может оказаться действительно полезным. И просто для протокола: нет, я не думаю, что может существовать жизнь в том виде, в каком мы ее знаем, на основе кремния вместо углерода.
Кальций
Марк Уолтерс, доцент кафедры химии
Кальций
Сейчас мой любимый элемент — кальций. Это вещество нашей геосферы в виде компонента известняковых и гипсовых минералов и нашей биосферы в виде костей, зубов, ракушек и даже яичной скорлупы. Это дает нам основу и структуру. Но не только мы… Как компонент портландцемента и облицовочного гипса (гипсокартон), он также служит для изготовления оболочек и жилья для людей.
Это компонент мела, который до появления маркеров сухого стирания служил для улучшения структуры наших идей и выражений, произнесенных или безмолвно набросанных на чистом листе.
Железо
Энди Гамильтон, профессор химии и президент Нью-Йоркского университета
Железо
Большинство химиков-органиков обычно говорят, что их любимым элементом является углерод из-за его роли в качестве основного строительного элемента жизни. Но для меня больше всего интересен элемент железа (Fe). Железо — это элемент, который даже в биологических условиях может иметь доступ к нескольким степеням окисления для выполнения ряда критических функций.
Но для меня больше всего интересен элемент железа (Fe). Железо — это элемент, который даже в биологических условиях может иметь доступ к нескольким степеням окисления для выполнения ряда критических функций.
В состоянии Fe 2+ его можно найти (в окружении моей любимой молекулы — порфиринового кольца) в гемоглобине. Эта замечательная комбинация Fe 2+ и порфирина придает крови ярко-красный цвет, а также способность Fe 2+ связываться с кислородом (O 2 ) и транспортировать его по телу. Опасные эффекты угарного газа (СО) связаны с его способностью еще более прочно связываться с Fe 2+ в гемоглобине и препятствовать доступу к живительной молекуле кислорода.
Железо совершает циклы между состояниями Fe 2+ и Fe 3+ в цитохромных белках, одной из важнейших ролей которых в жизни является перенос электронов по клетке. Смертельный яд цианид (CN — ) связывается с Fe 2+ в цитохроме точно так же, как O 2 или CO в гемоглобине, блокируя этот цикл и полностью разрушая пути управления энергией в живых клетках.
Наконец, железо получает доступ к Fe 4+ и Fe 5+ состояния в окислительном ферменте цитохроме Р450. Этот белок действует в печени как природный отбеливатель, часто очищая все нежелательные беспорядки, которые находятся внутри живых организмов, включая нас!
Медь
Джеймс Кэнэри, профессор и заведующий кафедрой химии
Медь
Я фанат элемента меди. Он не только красив, когда блестит, но и демонстрирует удивительно разнообразную химию. Он был обнаружен 11 000 лет назад и назван в честь Кипра. Медный век (энеолит) на Ближнем Востоке — один из моих любимых периодов в истории. Это необходимый элемент для всего живого на земле. В своей естественной металлической форме он обладает высокой проводимостью и пластичностью, что делает его идеальным материалом для проводов.
В ходе нашего исследования мы обнаружили, что он может заставить молекулу, имеющую хиральность, подобную резиновой перчатке, выворачиваться наизнанку, что приводит к противоположной хиральности. Точно так же, как когда вы выворачиваете инсайт из резиновой перчатки для левой руки, и он подходит к вашей правой руке, мы можем сделать то же самое с молекулами.
Точно так же, как когда вы выворачиваете инсайт из резиновой перчатки для левой руки, и он подходит к вашей правой руке, мы можем сделать то же самое с молекулами.
Если элемент теряет один электрон, он приобретает один положительный заряд, образуя медь(I). Бесцветная медь (I) является ключевым игроком в живых организмах для захвата, хранения и транспортировки кислорода в клетке. В крови человека эту роль выполняет железо, но медь(I) очень часто встречается в такой роли у многих организмов. Медь(I) также используется в органической химии для некоторых реакций, которые удивительны с точки зрения того, что они делают, и их эффективности.
Если металлическая медь теряет два электрона, она остается с двумя положительными зарядами на каждый атом меди, медь(II). Соединения меди (II) обычно имеют синий цвет. Он любит растворяться в воде, и реакции, связанные с присоединением/диссоциацией к/от меди (II), могут быть очень быстрыми. Медь (III) также известна, но она очень реакционноспособна и ее нелегко наблюдать.
Меня поразило то, что медь(0), медь(I) и медь(II) настолько отличаются друг от друга, что кажутся разными элементами. Все в них отличается — их внешний вид, их стабильность и их реактивность.
Галлий
Майк Уорд, Джулиус Сильвер, Рослин С. Сильвер и Энид Сильвер Уинслоу, профессор химии
Галлий
Моим любимым элементом должен быть галлий — атомный номер 31, простое число, окруженный алюминием, германием, индием и цинком в периодической таблице, и более редкий, чем золото. Его предсказал в 1871 году не кто иной, как Дмитрий Менделеев, назвавший его «экаалюминием». Затем он был обнаружен в 1875 году Полом Эмилем Лекоком де Буабодраном, который назвал его в честь «галлии», что на латыни означает Галлия, иначе известная как Франция, его родная страна.
Чем так интересен галлий? Он плавится при температуре около 30 ° C (86 ° F), что немного выше комнатной температуры. Это свойство было ключом к дешевому салонному трюку, когда галлий, выкованный в ложки для чайного сервиза, неожиданно плавился при использовании! Отсюда его появление на обложке книги «Исчезающая ложка: и другие правдивые рассказы о безумии, любви и истории мира из Периодической таблицы элементов » Сэма Кина.
