При какой температуре плавится бронза: Температура плавления бронзы и литье бронзы в домашних условиях
Содержание
кипения, какая зависимость сопротивления, рекристаллизации, график
Содержание:
- 1 Необходимая температура для плавления меди
- 2 Как изменяется металл под термическим воздействием
- 3 Отжиг меди
- 4 Видео: Плавление меди в микроволновке
Медные заготовки
Сегодня медь является одним из самых востребованных металлов. Высокий спрос объясняется отличительными характеристиками, присущими этому металлу. Медь проводит электроток лучше любых других металлов, кроме серебра, благодаря этому ее используют в производстве кабелей и электропроводов. Температура плавления меди не высокая, металл пластичный и легко поддается обработке, благодаря этому качеству стало возможным ее применение в строительстве в качестве водопроводных тр. Этот металл имеет высокое сопротивление к внешним раздражающим факторам, поэтому долговечен и может быть использован несколько раз, после переплавки. Это качество меди высоко ценят экологи, поскольку при повторной обработке металла тратится значительно меньшее количество энергии, чем при добыче и обработки руды, к тому же сохраняются земные недра. Добыча медной руды не проходит бесследно, на месте отработанных рудников появляются токсичные озера, наиболее известное во всем мире такое озеро – Беркли-Пит в штате Монтана в США.
Добыча медной руды не проходит бесследно, на месте отработанных рудников появляются токсичные озера, наиболее известное во всем мире такое озеро – Беркли-Пит в штате Монтана в США.
Необходимая температура для плавления меди
Медь не является легкоплавким металлом
Люди нашли применение меди еще в древние времена, тогда ее добывали в виде самородков. Ввиду низкой температуры, необходимой для осуществления процесса плавления ее стали широко применять для изготовления орудий труда и охоты, самородки можно плавить на костре. В наши дни технология получения металла мало чем отличается от придуманной в древние времена, совершенствуются лишь печи, увеличена скорость обжига и объемы обработки. Здесь возникает уместный вопрос — какая температура плавления меди? Ответ на него можно найти в любом учебнике по физике и химии – медь начинает плавиться при температуре нагрева до 1083 оС.
Кипение меди уменьшает ее прочность
В процессе термического воздействия на металл происходит разрушение его кристаллической решетки, это достигается при определенной температуре, которая в течение некоторого времени остается постоянной. В этот момент и происходит плавка металла. Когда процесс разрушения кристаллов полностью завершен, температура металла снова начинает подниматься, и он переходит в жидкую форму и начинает кипеть. Температура плавления меди значительно ниже, чем та, при которой металл кипит. Процесс кипения начинается с появлением пузырьков, по аналогии с водой. На этом этапе любой металл, в том числе и медь, начинает терять свои характеристики, в основном это отражается на прочности и упругости. Температура кипения меди составляет 2560 оС. Во время остывания металла происходит похожая картина, как и при нагреве – сначала температура опускается до определенного градуса, в этот момент происходит затвердевание, которое длится некоторое время, затем продолжается остывание до обычного состояния.
В этот момент и происходит плавка металла. Когда процесс разрушения кристаллов полностью завершен, температура металла снова начинает подниматься, и он переходит в жидкую форму и начинает кипеть. Температура плавления меди значительно ниже, чем та, при которой металл кипит. Процесс кипения начинается с появлением пузырьков, по аналогии с водой. На этом этапе любой металл, в том числе и медь, начинает терять свои характеристики, в основном это отражается на прочности и упругости. Температура кипения меди составляет 2560 оС. Во время остывания металла происходит похожая картина, как и при нагреве – сначала температура опускается до определенного градуса, в этот момент происходит затвердевание, которое длится некоторое время, затем продолжается остывание до обычного состояния.
Как изменяется металл под термическим воздействием
Любой нагрев меди влечет за собой изменение ее характеристик, наиболее значимой является величина ее удельного сопротивления. Медь является проводником электрического тока, при этом металл оказывает сопротивление движению носителям заряда. Отношение площади сечения проводника к оказываемому движению и называется удельным сопротивлением.
Отношение площади сечения проводника к оказываемому движению и называется удельным сопротивлением.
Термо обработка медной трубы
Так вот, эта величина для чистой меди составляет 0,0172 ОМ мм2/м при 20 оС. Этот показатель может измениться после термической обработки, а также вследствие добавления в состав различных примесей и добавок. Здесь наблюдается обратная зависимость сопротивления меди от температуры – чем выше была температура обработки металла, тем ниже будет ее сопротивление электрическому току. Для обеспечения наилучших электролитических характеристик медной проволоки, ее обрабатывают при 500 оС.
Во время термической обработки можно не только придавать металлу нужную форму и размер, но и создавать различные сплавы. Самыми распространёнными медными сплавами является бронза и латунь. Бронза получается путем смешивания меди с оловом, а латунь – с цинком. Добавление алюминия и стали увеличивает прочность материала, а добавление никеля повышает антикоррозийные свойства. Но стоит заметить, что любая примесь снижает главное свойство – электропроводность, поэтому для изготовления жил электрокабеля используют чистый состав металла.
Но стоит заметить, что любая примесь снижает главное свойство – электропроводность, поэтому для изготовления жил электрокабеля используют чистый состав металла.
Отжиг меди
Под отжигом меди следует понимать процесс ее нагрева с целью дальнейшей обработки и приданию необходимых форм изделию. В ходе отжига металл становится более пластичным и мягким, поддающимся различным трансформациям. При отжиге меди температура достигает 550 оС, она приобретает темно-красный оттенок. После нагрева желательно быстро производить ковку и оправлять изделие на охлаждение.
Оджиг позволяет деформировать без повреждений любое изделие из меди
Если подвергать материал медленному, естественному охлаждению, то возможно образование наклепа, поэтому чаще применяют мгновенное охлаждение путем помещения заготовки в холодную воду. Если превысить допустимую величину нагрева, металл может стать более хрупким и ломким.
Во время отжига осуществляется процесс рекристаллизации меди, в ходе которого образуются новые зерна или кристаллы металла, которые не искажены решеткой и отделены от прежних зерен угловыми границами.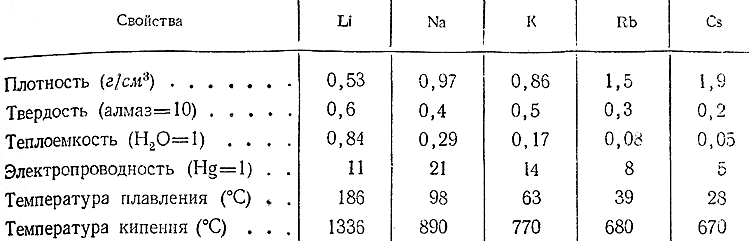 Новые зерна по размеру могут сильно отличаться от предшественников, при их образовании высвобождается большое количество энергии, увеличивается плотность и появляется наклеп. Рекристаллизация осуществляется только после деформации изделия, и только после достижения ее определенного уровня. Для меди критический уровень деформации составляет 5%, если он не достигнут процесс формирования новых зерен не начнется. Температура рекристаллизации меди составляет 270 оС. Следует отметить, что при этой температуре процесс роста кристаллов только начинается, но он достаточно медленный, поэтому для достижения необходимого результата медь необходимо нагреть до 500 оС, тогда времени для остывания хватит для завершения процесса рекристаллизации.
Новые зерна по размеру могут сильно отличаться от предшественников, при их образовании высвобождается большое количество энергии, увеличивается плотность и появляется наклеп. Рекристаллизация осуществляется только после деформации изделия, и только после достижения ее определенного уровня. Для меди критический уровень деформации составляет 5%, если он не достигнут процесс формирования новых зерен не начнется. Температура рекристаллизации меди составляет 270 оС. Следует отметить, что при этой температуре процесс роста кристаллов только начинается, но он достаточно медленный, поэтому для достижения необходимого результата медь необходимо нагреть до 500 оС, тогда времени для остывания хватит для завершения процесса рекристаллизации.
Видео: Плавление меди в микроволновке
Чтобы качественно сварить бронзу, алюминий и медь
В состав бронзы входят, помимо меди и алюминия, цинк, марганец, кремний и олово. Категория бронзы определяется содержанием добавок при сплаве. Оловянная бронза имеет в составе от восьми до десяти процентов олова, от двух до четырёх процентов цинка. Остальное приходится на долю меди.
Категория бронзы определяется содержанием добавок при сплаве. Оловянная бронза имеет в составе от восьми до десяти процентов олова, от двух до четырёх процентов цинка. Остальное приходится на долю меди.
К специальным бронзам относятся:
• кремнистые,
• марганцовые,
• железомарганцевые,
• алюминиевые.
Сварить бронзу можно не только металлическими, но и угольными электродами. Накануне сварки каждую бронзовую детальнадо подогреть от двухсот до пятисот пятидесяти градусов по Цельсию. Причём с сильным подогревом нужно сваривать детали, обладающие сложной конфигурацией. Если речь вести о простых деталях, то для них подойдёт предварительный подогрев с меньшей температурой.
Необходимостью сварка бронзы становится в следующих случаях:
1. При состыковке фрагментов изделий, которым присуща сложная форма.
2. Реставрации изношенных либо поломанных деталей.
3. Исправление дефекта отливок.
Подобные изделия определяются как сварнолитые. Выполнить сварку бронзы можно в полувертикальном или нижнем положении. Заделывая сквозной дефект, сваривая стыковой шов, необходимо использовать подкладки. Они помогут избежать протекания металла. Подкладки изготавливаются:
Выполнить сварку бронзы можно в полувертикальном или нижнем положении. Заделывая сквозной дефект, сваривая стыковой шов, необходимо использовать подкладки. Они помогут избежать протекания металла. Подкладки изготавливаются:
• из огнеупорной глины,
• асбеста,
• стальных листов.
Форму непременно надо соотносить с конфигурацией детали изнутри, в том месте, где производится сварка.
Для сварки оловянной бронзы
Сварить оловянную бронзу можно с применением угольных электродов. Для присадочного материала нужно взять отлитый вкокиль пруток. Он должен иметь в качестве составляющих:
1. 0,25 процента фосфора.
2. От трёх до четырёх процентов кремния.
3. 95-96 процентов меди.
На роль флюса годится борный шлак либо прокалённая бура. Чтобы сварить никелевую, свинцовую, цинковую, оловянную бронзу, потребуются электроды ОБ-5. Заварив детали, их надо для постепенного охлаждения укрыть асбестом. Это снизит остаточное напряжение, предотвратит появление трещин.
Специальные бронзы
Когда свариваешь специальную бронзу с использованием угольного электрода, присадочным металлом нужно выбрать прутки, идентичные по составу с главным металлом. Сваривая кремнистую бронзу, для флюса лучше всего взять прокалённую буру. Фосфористым бронзам рекомендуется бронборный шлак.
Алюминиевые бронзы требуют в качестве флюса тот же, который используется при сварке алюминиевых сплавов и самого алюминия. Для специальных бронз, при сварке с помощью металлического электрода, состав стержня подбирается с учётом состава главного металла. Сваривая фосфористую бронзу, лучше задействовать стержень с таким составом:
1. Не больше 0,75 процента примеси.
2. От девяти до одиннадцати процентов олова.
3. 0,5-1,0 процента фосфора.
4. Остальная часть – медь.
Алюминиевая бронза при сварке предполагает использование прутка, имеющего в составе:
• марганца от 1,5 до 2,5 процента;
• равное количество с главным металлом алюминия;
• медь, железо как остальная часть.
Сварку бронзы с применением металлического электрода лучше выполнить с постоянным током обратной полярности. Сила тока берётся с таким расчётом: на один миллиметр электродного диаметра потребуется 40 ампер. Алюминий используется при производстве деталей не только в своём чистом виде (99,5 процента), но и в разного рода сплавах с кремнием, медью, магнием, марганцем.
Снаружи как алюминий, так и сплавы с ним имеют плёнку окиси с температурой плавления приблизительно 2050 градусов. При нагреве алюминий подвержен весьма сильному окислению. Плёнка тугоплавкой окиси, которая расположена на поверхности заготовки, создаёт препятствие для сплавления присадочного металла с главным.
Чтобы соединение вышло надёжным, при сварке требуется удаление плёнки оксида. Этой цели можно добиться как химическим, так и механическим способом. Последний далеко не всегда даёт хороший результат. Его предпочтительней использовать, сваривая металл с определённой толщиной.
Надо учитывать, что окись алюминия может быть удалена концом присадочного материала. Химическая же очистка производится с помощью покрытий либо флюсов, гарантируя качественное удаление окиси алюминия. Окись алюминия полностью должна быть удалена по причине своей тяжести, превышающей вес алюминиевого сплава либо самого алюминия.
Химическая же очистка производится с помощью покрытий либо флюсов, гарантируя качественное удаление окиси алюминия. Окись алюминия полностью должна быть удалена по причине своей тяжести, превышающей вес алюминиевого сплава либо самого алюминия.
Нередко окись, располагаясь плёнкой вдоль швов, уменьшает надёжность сварной состыковки. Чтобы избежать ожогов, сварку алюминия в форме листа осуществляют на подкладках. Допускается использование металлических и угольных электродов, среды защитных газов.
Применяя угольные электроды
Если для сварки приготовлен угольный электрод, то на присадочный металл пойдут литые прутки или проволока, имеющие один и тот же состав с главным металлом. Из трёх возможных марок флюсов больше подходит АФ-4А. Такой флюс надо использовать, сваривая незначительной толщины металл. Сгодится он и при устранении дефектов в литой детали из сплавов алюминия и тонкими стенами.
При существенной толщине главного металла неплохого качества можно добиться, используя флюс №2 и №1. Его наносят накануне нагрева на поверхность, подлежащую сварке. Это может быть:
Его наносят накануне нагрева на поверхность, подлежащую сварке. Это может быть:
1. Состыковка шин электролизного цеха.
2. Монтаж иных электрических линий.
Алюминиевые шины сваривают обычно встык на графитовой либо алюминиевой подкладке. Графитовые пластины, обладающие вырезами против швов, ставят по бокам шин. Вырезы дают возможность удалить за границы рабочего сечения конец и начало шва.
Металлический электрод для сварки
Электродный стержень должен быть сделан из материала, обладающего с главным металлом одинаковым составом. Нужно нанести покрытие на стержень. Его состав хорошо известен, и необходимо соблюдать общепринятое процентное соотношение. Покрытие должно получиться толщиной до одного миллиметра.
Подогрев в специальных печах означает необходимость замера температуры термопарой. Речь идёт о подогреве древесными опилками либо термокарандашами в горне. Температура бывает достаточной уже при тлении опилок. Сварка осуществляется при применении постоянного тока обратной полярности. Сила его берётся в границе от тридцати до тридцати шести ампер на миллиметр диаметра электрода.
Сила его берётся в границе от тридцати до тридцати шести ампер на миллиметр диаметра электрода.
Детали из алюминиевых сплавов и алюминия надо хорошо очистить от остатка шлака и флюса. Именно эти остатки способствуют возникновению коррозии металла. Чтобы достигнуть этой цели, необходимо:
• деталь после завершения сварки промыть горячей водой;
• поверхность шва протереть волосяной щёткой;
• погрузить деталь на пять минут в 2-процентный раствор с хромовой кислотой, которая нагрета до восьмидесяти градусов.
Завершив эту процедуру, детали нужно опять промыть горячей водой и просушить.
В среде защитного газа
Защитным газом служит аргон. Сварка выполняется с использованием специального держателя и вольфрамового электрода. Задействованный в данном случае алюминиевый сплав и алюминий необходимо хорошо очистить.
Нельзя допустить в аргоне:
1. Содержания кислорода свыше 0,03 процента.
2. Наличия влаги.
3. Присутствие азота больше 0,3 процента.
Сваривая в аргоновой среде, флюс использовать не надо. В результате отпадает необходимость очистки после сварки от шлаков и флюса, что является трудоёмкой операцией. Сварка в среде аргона допускает также нахлесточные соединения, которые запрещены при сварке, подразумевающей использование флюса. Запрещение обосновывается тем, что практически невозможно стопроцентно удалить шлаки и остаток флюса. В итоге может появиться коррозия, разрушающая нахлесточное сварное соединение.
Уменьшая окисную плёнку
С дуговой сваркой покрытым электродом мы имеем дело только с двумя разновидностями цветного металла:
• медными сплавами и медью;
• алюминиевыми сплавами и алюминием.
Главные преимущества конструкций из сплава с алюминием многократно проверены практикой и заключаются в следующем:
1. В высокой устойчивости к коррозии.
2. Высокой удельной прочности.
3. В малой плотности.
По этим причинам конструкции распространены повсеместно. Для сварной конструкции применяется деформируемый сплавиз алюминия. При деформации и нагреве он не поддаётся растрескиванию. Основной же проблемой сварки алюминиевых сплавов и алюминия стала его значительная химическая активность:
При деформации и нагреве он не поддаётся растрескиванию. Основной же проблемой сварки алюминиевых сплавов и алюминия стала его значительная химическая активность:
• на поверхности алюминия появляется окисная плёнка, чья температура плавления составляет 2050 градусов по Цельсию;
• она не плавится в ходе сварки;
• потягивает металл устойчивой оболочкой;
• затрудняет формирование сварочной ванны.
Кусочки плёнки, попав в шов, уменьшают качество сварного соединения и срок его службы. Выполняя сварку, необходимо провести меры для разрушения, а потом удаления плёнки. Эта мера обеспечит защиту металла от нового окисления. Из-за немалой химической прочности окисной плёнки восстановить из окисла алюминий при сварке нельзя. Невозможно на практике связать её в прочное соединение со щелочью либо сильной кислотой.
Влияние шлака на сварку алюминия базируется на смывании расплавленным шлаком окисной плёнки, которая подверглась разрушению. Немалую роль играет процесс растворения. Готовя деталь из сплава с алюминием для предстоящей сварки, нужно удалить с кромки поверхностное загрязнение. Применяется для этой цели органический растворитель. Возможно использование травления по такой технологии:
Готовя деталь из сплава с алюминием для предстоящей сварки, нужно удалить с кромки поверхностное загрязнение. Применяется для этой цели органический растворитель. Возможно использование травления по такой технологии:
1. Промывка холодной водой.
2. Сушка с помощью сжатого воздуха.
3. Обезжиривание растворителем.
4. Пассивирование две минуты в тридцатипроцентном растворе с водой HNO3.
5. Травление одну-две минуты в NaOH, концентрированной щелочи.
Сварка даёт возможность применить с хорошей отдачей нахлесточные либо стыковые соединения. Снижая включения в швеокисной плёнки, допустимо применение флюсов, которые наносятся на торцы деталей накануне сварки. Они представляют собой дисперсную взвесь фторидов, находящихся в спирте.
Не разделывая кромки, допустимо сваривание с одного бока детали, имеющего толщину кромки до шести миллиметров. С двух боков эта толщина может доходить до десяти миллиметров. Разделка выполняется V-образно:
• с притуплением в 0,25 от толщины кромки;
• углом раскрытия кромки до шестидесяти-семидесяти градусов.
Соблюдение всех требований неизменно даёт положительный результат.
Электроды для алюминиевых сплавов
При сварке алюминиевого сплава самыми распространёнными типами электродов считаются: ОЗА-1, ЭЮ-1, АФ-4А, ОЗА-2. Последняя разновидность рассчитана для наплавки и заварки дефектов после литья. Стержень электрода выполняется с использованием сварочной проволоки, нанесением на неё покрытия, представляющего собой смесь фтористой и хлористой соли. Толщина его не больше 0,3 – 0,5 миллиметров на сторону.
Сварка осуществляется с применением постоянного тока обратной полярности. На силе тока останавливаются с учётом диаметра электрода и положения шва. Работа с электродом 03А-1:
1. Угол загиба 170 градусов.
2. Прочность шва 72 Мпа.
Выполнять сварку предпочтительней с предшествующим подогревом детали до 250 – 400 градусов по Цельсию (принимаетсяво внимание толщина кромки). Алюминий обладает значительной теплопроводностью, кромки разогреваются дугой чрезвычайно медленно. На каждый килограмм наплавленного металла расходуется два килограмма электродов.
На каждый килограмм наплавленного металла расходуется два килограмма электродов.
Существенны потери на разбрызгивание и угар электродного металла. Сваривая электродом ОЗА-2, надо иметь в виду, что угол загиба выходит меньше, а шов получится прочнее — 86 Мпа. Такое наблюдается из-за легирования кремнием швов.
Медные сплавы и медь
Применение медных сплавов и меди обусловлено антикоррозийной стойкостью в агрессивной среде, высокой тепло- и электропроводностью. Большая чистота металла означает повышение подобных свойств. Как теплопроводность, так и электропроводность меди быстро меняется и при малом присутствии примеси (до одного процента). Нагреваясь, медь вступает в реакцию с водородом, углеродом, серой, кислородом. Инертность она проявляет при сварке к азоту в каждом еётемпературном диапазоне.
При низкой температуре, похожей на температуру кристаллизации, водород и кислород почти не растворяются в меди. Неудовлетворительная защита и не существенное раскисление вызывает у меди трещины либо водородную «болезнь». Она проявляется в замедленном образовании трещин. В связи с этим необходимо:
Она проявляется в замедленном образовании трещин. В связи с этим необходимо:
• накануне работы два часа прокаливания сварочных электродов при температуре от 250 до 300 градусов по Цельсию;
• основной металл должен быть с низким содержанием газа;
Когда же речь заходит о сваривании чистой меди, то предпочтительней применять иные способы, в том числе сварку в защитном газе плавящимся либо не плавящимся электродом. Сплав меди с цинком, латунь, тоже отличается плохой свариваемостью по причине выгорания цинка.
Специфика бронз
Бронза сваривается при сопоставлении с чистой медью лучше. Бронзы различаются видом легирующего компонента. Хромистые и кремнистые бронзы можно сварить легче других. Кремнистыми бронзами существенно утрачена как электропроводность, так и теплопроводность, зато в значительной мере присуща износостойкость и устойчивость к коррозии.
Для хромистых бронз характерна при отличной свариваемости тепло- и электропроводность уровня чистой меди. Неплохой свариваемостью с жаропрочностью и превосходной устойчивостью к коррозии обладают марганцовистые бронзы. Оловянистые и алюминиевые бронзы из-за выгорания легко плавящегося легирующего материала свариваются неудовлетворительно.
Неплохой свариваемостью с жаропрочностью и превосходной устойчивостью к коррозии обладают марганцовистые бронзы. Оловянистые и алюминиевые бронзы из-за выгорания легко плавящегося легирующего материала свариваются неудовлетворительно.
Из электродов, что уже прошли проверку практикой, лучшими стали Комсомолец-100, ОЗБ-2М, АНЦ/СЭМ-3. Последняя разновидность рассчитана на наплавку бронз и сварку. Все другие – на сварку, наплавку чистой меди, а на её основе – низколегированного сплава. Сваривают медные сплавы и медь, используя постоянный ток обратной полярности.
Деталь, обладающую толщиной до десяти миллиметров, подвергают сварке с аналогичной без предварительного подогрева и разделки кромки. Сила тока подбирается с учётом диаметра электрода. Процесс сварки нужно осуществлять двух- либо односторонним швом:
• на графитовой ткани;
• либо на графитовой подкладке, высушенной и ровной.
Сваривают короткой дугой, чуть-чуть на подъём либо в нижнем положении, с незначительным поперечным колебанием электрода, находящегося в перпендикулярном положении к изделию.
Деталь, имеющую толщину 10 – 25 миллиметров, сначала нагревают до двухсот-четырёхсот градусов по Цельсию. Причём должна быть обеспечена электропроводность сварного шва в пределе шестидесяти процентов в сравнении с электропроводностью чистой меди. Границей прочности наплавленного материала становится 200 МПа. Электроды всех типов расходуются интенсивно. Затрачивается на каждый килограмм наплавленного металла 1,6-1,75 килограмма электродов. Зато результат соответствует технологическому стандарту.
Кремниевая ювелирная бронза красная в гранулах цена, описание, видео и фото как выглядит
Описание
Характеристики
Оплата и Доставка
Гарантия
Размер частиц
Прочее
Отзывы (0)
Кремниевая ювелирная бронза красная в гранулах цена 3500руб/кг
(гранулы сплава медь-олово-кремний, сплав медно-оловянно-кремниевый)
Минимальная партия на продажу 50гр.
Чистота 99,99%
Марка MELT BR12M производство Италия
Химический состав: Медь-88%; Олово-11%; Кремний-1%.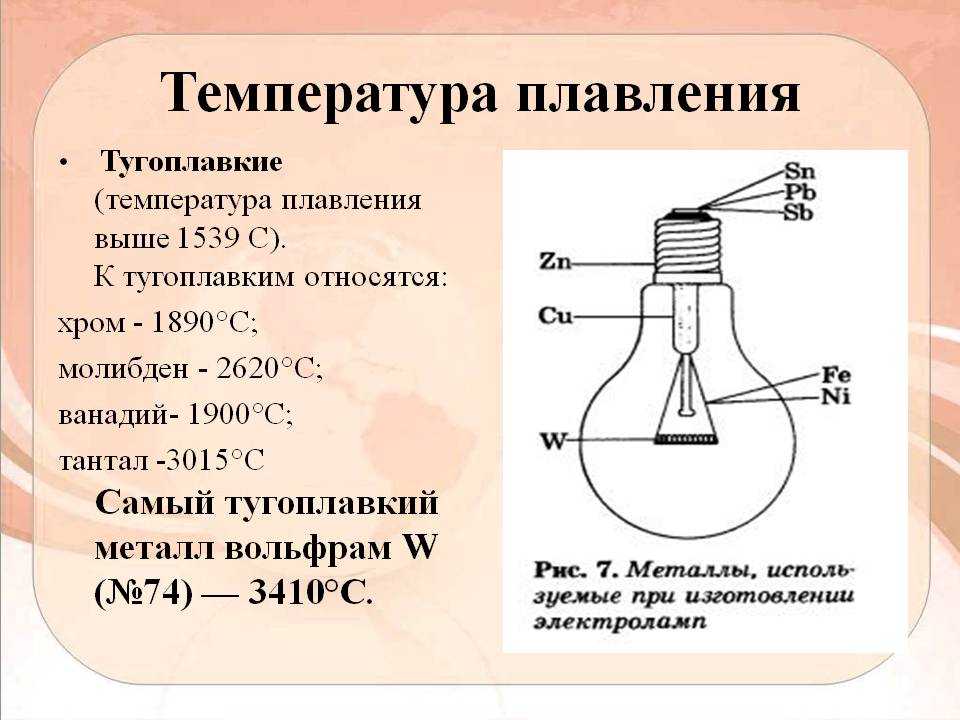 Сплав особо чистой бескислородной электролитической меди 99,999% с оловом 99,99% и кремнием 99,99%. Сплав дегазирован и обработан антиокислителями. Добавка кремния улучшает проливаемость для сложных, филигранных форм.
Сплав особо чистой бескислородной электролитической меди 99,999% с оловом 99,99% и кремнием 99,99%. Сплав дегазирован и обработан антиокислителями. Добавка кремния улучшает проливаемость для сложных, филигранных форм.
Плотность 8,67гр/см3
Солидус-1005С; Ликвидус-1007С
Температура опоки: Центробежная-500С; Вакуумная с литьем в атмосфере-600С; Вакуумная с литьем под давлением-650С
Цвет: светло-коричневый
Используется для любого типа литья, включая литье с камнями
Инструкция по применению
Тигель перед применением необходимо прогреть. Используйте только борную кислоту для защитного покрытия поверхности расплава, особенно при плавке без использования защитных газов или вакууме. Температура пролива должна быть примерно на 50С выше температуры плавления легированного сплава. Размывку опоки рекомендуется проводить через три минуты после заливки металла. В случае литья с камнями размывку следует начинать после остывания опоки до 100С.
Важно: не допускать излишнего нагрева сплава, соблюдайте рекомендованный температурный режим. При нагретом тигеле использовать полную мощь печи на 100%. Когда металл начнет плавится уменьшить мощность до 40%. Когда металл расплавился уменьшить мощность до 20%
Видео как выглядит кремниевая бронза ювелирная:
| Минимальный вес | 50 г. |
| Синонимы | сплав медь-олово-кремний |
| Формула | CuSnSi марка BR12M |
| Чистота | 99,99% |
| Минимальная партия на продажу | 0,1кг (100гр) |
| Насыпная плотность | 8,67гр/см3 |
| ГОСТ или ТУ | производство Италия |
Работаем с физическими и юридическими лицами
Гарантия возврата денежных средств
Способы оплаты:
- Безналичный расчет для юридических лиц.
 Предоставим полный пакет учредительных документов. Выставим счет, заключим договор. Бюджетным организациями предоставим отсрочку платежа в случае необходимости.
Предоставим полный пакет учредительных документов. Выставим счет, заключим договор. Бюджетным организациями предоставим отсрочку платежа в случае необходимости. - Банковской картой через сайт: Visa, MasterCard , Maestro, МИР, AmericanExpress и т.д.
- Электронные способы оплаты через сайт: Сбербанк Онлайн, Яндекс Деньги, QIWI, WebMoney и т.д.
- Наличными курьеру
- Наличными на складе по факту покупки
- Оплата через PayPal
- Наложенным платежом Почта России
Быстро организуем доставку по Москве, регионам России, странам СНГ и дальнего зарубежья.
В среднем в зависимости от транспортных компаний, стоимость доставки следующая:
Москва от 490руб до 990руб
Регионы России-1300руб
Страны СНГ-3500руб
Дальнее зарубежье-4900руб
Виды доставок и транспортные компании:
1) Доставка через транспортные компании: Деловые Линии, ПЭК, СДЭК, и т.д. Срок доставки от 2х дней
2) Курьерская экспресс доставка: Курьер экспресс, Пони экспресс, Достависта и т. д. Срок доставки от 1 дня
д. Срок доставки от 1 дня
Друзья. Если по какой-либо причине, объективной ли, субъективной ли, вас не устроило или не устроит качество купленного у нас товар, мы быстро, без долгих разбирательств и бюрократических проволочек вернем вам деньги обратно. Может вы проснулись не в духе, может чай не выпили, может погода повлияла, но если вы вдруг решили вернуть товар обратно, то ничего не нужно выдумывать, просто сообщите нам об этом любым удобным вам способом. Максимум на возврат средств уйдет 1-2 дня, обычно это происходит день в день после возврата товара. Таким образом, мы гарантируем быстрый возврат уплаченных вами средств.
Далее
1) Мы гарантируем что наши цены одни из самых дешевых на рынке. Сообщите пожалуйста если нашли дешевле и мы тут же снизим цену.
2) Мы гарантируем, что товары выложенные у нас на сайте, всегда в наличии на нашем складе, т.е. мы не тратим время на поиски или перекупку у другого поставщика.
3) Мы гарантируем быструю доставку товара. Так как товары представленные на нашем сайте всегда в наличии, то остается лишь транспортной компании забрать у нас груз
4) Мы гарантируем что заявленные на сайте характеристики соответствуют фактическим.
гранулы
Акции, скидки, распродажа
Отправить заявку или заказать обратный звонок
Купить продукцию: [email protected] или (495) 923-81-68
Сертификаты
Специалисты компании
Справочник
Схема проезда
Гарантии на покупку
Всегда в наличии
Продукция в интернет-магазине, всегда в наличии на нашем складе. Смело оплачивайте.
Точное соответствие
Заявленные на сайте характеристики продукции соответствуют фактическим.
Вернем деньги
Если не устроит качество или просто передумаете-быстро вернем деньги, без долгих процедур
Принимаю Условия подписки
Название — бронза — Большая Энциклопедия Нефти и Газа, статья, страница 2
Cтраница 2
В отдельных случаях помимо чистой меди в качестве проводникового материала применяются ее сплавы с небольшим содержанием олова, кремния, фосфора, бериллия, хрома, магния, кадмия и пр.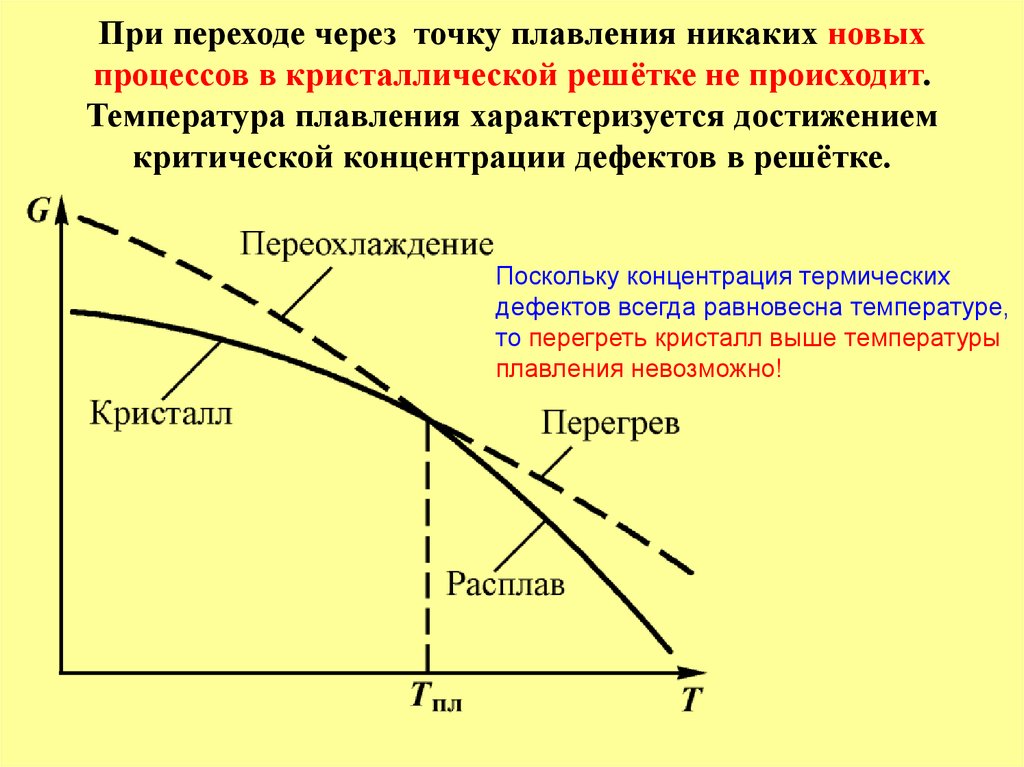 Такие сплавы, носящие в практике название бронз, при правильно подобранном составе имеют значительно более высокие механические свойства, чем медь; так, предел прочности при растяжении бронз может доходить до 80 — 135 кГ / мм.
Такие сплавы, носящие в практике название бронз, при правильно подобранном составе имеют значительно более высокие механические свойства, чем медь; так, предел прочности при растяжении бронз может доходить до 80 — 135 кГ / мм.
[16]
В отдельных случаях, помимо чистой меди, в качестве проводникового материала применяются ее сплавы с небольшим содержанием олова, бериллия, хрома, магния, цинка, кадмия, кремния, фосфора и пр. Такие сплавы, носящие на практике обычно название бронз, при правильно подобранном составе имеют значительно более высокие механические свойства, чем медь; так, прочность на разрыв бронз может доходить до 80 — 100 кПмм2 и даже более. Однако удельное сопротивление бронз, конечно, больше, чем чистой меди. Весьма сказывается использование в качестве присадки к меди кадмия; эта присадка при сравнительно малом уменьшении электропроводности дает значительное повышение механической прочности и твердости. Кадмиевая бронза применяется для контактных проводов и коллекторных пластин особо ответственного назначения. Еще большей механической прочностью обладает берилл и евая бронза.
Еще большей механической прочностью обладает берилл и евая бронза.
[17]
В отдельных случаях помимо чистой меди в качестве проводникового материала применяются ее сплавы с небольшим содержанием олова, бериллия, хрома, магния, цинка, кадмия, кремния, фосфора и пр. Такие сплавы, носящие на практике обычно название бронз, при правильно подобранном составе имеют значительно более высокие механические свойства, чем медь; так, прочность на разрыв бронз может доходить до 80 — 100 кг.мм. и даже более. Однако удельное сопротивление бронз, конечно, больше, чем чистой меди. Весьма удачным оказывается использование в качестве присадки к меди кадмия; эта присадка при сравнительно малом уменьшении электропроводности дает значительное повышение механической прочности и твердости. Кадмиевая бронза применяется для контактных проводов и коллекторных пластин особо ответственного назначения. Еще большей механической прочностью обладает бериллиевая бронза.
[18]
Заварка трещин в цилиндрах компрессоров и паровых машин производится автогенной сваркой после предварительного прогрева цилиндра. В качестве электродов применяют сплав, носящий название бронзы Тобина.
В качестве электродов применяют сплав, носящий название бронзы Тобина.
[19]
Заварка трещин производится автогенной сваркой после предварительного прогрева цилиндра. В качестве электродов применяется сплав, носящей название бронзы Тобина. При подготовке шва под заварку вырубают канавку вдоль всей трещины и ввептывают по краям ка-наики в шахматном порядке несколько стальных шпилек. В качестве флюса при сварке применяется бура с борной кислотой.
[20]
Бронзами называются медные сплавы, в которых основными легирующими элементами являются алюминий, олово, марганец, кремний и другие. В зависимости от преобладания легирующего элемента определяется и название бронзы. Бронзы делятся на две основные группы — оловянные и безоловянные.
[21]
Безоловянными или специальными бронзами называют медные сплавы ( двойные или многокомпонентные), содержащие в качестве легирующих элементов А. Ni, Si, Mn, Fe, Cd, Be, Cr и др. Название бронзы определяется по содержащимся в ней легирующим компонентам.
Название бронзы определяется по содержащимся в ней легирующим компонентам.
[22]
Заварка трещин производится автогенной сваркой после предварительного прогрева цилиндра. В качестве электродов применяется сплав, носящий название бронзы Тобина. При подготовке шва под заварку вырубают канавку вдоль всей трещины и ввертывают по краям канавки в шахматном порядке несколько стальных шпилек. В качестве флюса при сварке применяется бура с борной кислотой.
[23]
Такая двойная температура плавления SnCu3 указывает, что это соединение плавится с разложением. Диморфизмом соединения SnCu4 объясняется способность бронзы к закалке. Сплав SnCu4 представляется почти совершенно белым и известен под названием зеркальной бронзы, так как служит для приготовления отражательных зеркал.
[24]
В частности, у ( NaxW) O3 х — 0 3 — 1 0, причем состав, отвечающий х — 1 0, никогда не достигается. При х — 0 9 соединение имеет желтый цвет, по которому это соединение получило название бронзы. Когда дс — 0 8, соединение окрашено в оранжевый цвет, а при дс-0 6 — 0 7 — в красный.
Когда дс — 0 8, соединение окрашено в оранжевый цвет, а при дс-0 6 — 0 7 — в красный.
[25]
В течение многих лет считалось, что вольфрамовые бронзы являются единственными соединениями подобного типа, но сейчас идентифицировано много родственных им соединений. Подобие может быть трех видов. Во-первых, соединения могут иметь ту же структуру и свойства, но содержать вместо W другие элементы. Во-вторых, свойствами бронз могут обладать другие соединения с иным составом и структурой. В-третьих, известно несколько соединений, кристаллизующихся в структуре вольфрамовых бронз, но во всех других отношениях ведущих себя совершенно по-иному. Название бронзы, не являющееся специфичным для окислов вольфрама, условно. Его следует оставить в химической литературе для описания некоторых свойств окислов металлов и нельзя применять для описания фаз, имеющих свои специфические структуры.
[26]
Причину разногласия определяли тем, что кривые плоскости сплавов не обладают гпахптшт ами, которые наиболее ясно определяют состав определенных соединений, а представляют лишь особые переходные точки, что обусловливается ( Байков): 1) тем, что соединение SnCu4 образует с медью твердые растворы, и 2) тем, что соединение SnCu3 плавится с разложением, подобно солям с кристаллизационной водой. Наиболее точно кривая плавкости для системы Си Sn изучена Гейкоком и Невиллем. На основании их данных следует, что существуют два соединения; одно, имеющее состав SnCu4, видно резко выраженной угловой точкой для сплава, содержащего точно 32 % Sn и 68 % Си, и другое с большим содержанием олова, характеризуемое тоже особой — переходной точкой — но состав, ей отвечающий, не может быть определен на основании кривой, так как оно плавится с разложением. Это второе соединение есть очевидно SnCu3, существование которого доказано по электропроводности ( Матисен) и электродвижущей силе ( Лори, Гершкович) и было выделено Ле-Шателье из сплавов, богатых оловом, при действии на них соляной кислотой, в виде кристаллического порошка, и для которого еще Риш показал, что из всех медно-оловянных сплавов только SnCu3 и SnCu4 не дают явлений ликвации. Наблюдения Байкова над плавлением и микроструктурой этих сплавов показали, что сплав SnCu4 весь застывает при постоянной температуре и дает тело совершенно однородное.
Наиболее точно кривая плавкости для системы Си Sn изучена Гейкоком и Невиллем. На основании их данных следует, что существуют два соединения; одно, имеющее состав SnCu4, видно резко выраженной угловой точкой для сплава, содержащего точно 32 % Sn и 68 % Си, и другое с большим содержанием олова, характеризуемое тоже особой — переходной точкой — но состав, ей отвечающий, не может быть определен на основании кривой, так как оно плавится с разложением. Это второе соединение есть очевидно SnCu3, существование которого доказано по электропроводности ( Матисен) и электродвижущей силе ( Лори, Гершкович) и было выделено Ле-Шателье из сплавов, богатых оловом, при действии на них соляной кислотой, в виде кристаллического порошка, и для которого еще Риш показал, что из всех медно-оловянных сплавов только SnCu3 и SnCu4 не дают явлений ликвации. Наблюдения Байкова над плавлением и микроструктурой этих сплавов показали, что сплав SnCu4 весь застывает при постоянной температуре и дает тело совершенно однородное. Такая двойная температура плавления SnCu3 указывает, что это соединение плавится с разложением. Диморфизмом соединения SnCu4 объясняется способность бронзы к закалке. Сплав SnCu4 представляется почти совершенно белым и известен под названием зеркальной бронзы, так как служит для приготовления отражательных зеркал.
Такая двойная температура плавления SnCu3 указывает, что это соединение плавится с разложением. Диморфизмом соединения SnCu4 объясняется способность бронзы к закалке. Сплав SnCu4 представляется почти совершенно белым и известен под названием зеркальной бронзы, так как служит для приготовления отражательных зеркал.
[27]
Страницы:
1
2
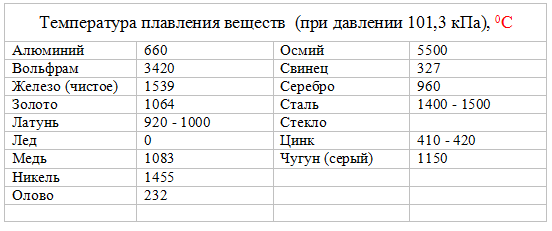
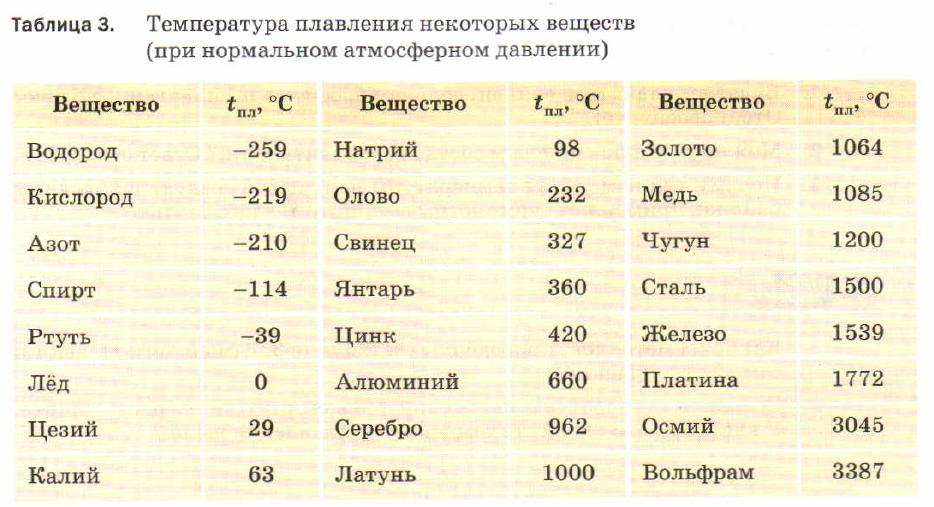
Температура плавления металлов: таблица и понятие
При сварке происходит воздействие высокой температуры на детали, поэтому очень важно придавать значение температуре плавления металлов, учитывая её в процессе работы, так как данные показатели играют немаловажную роль в параметрах тока. В горелке, при сгорании газа в момент действия электрической дуги, создается тепловая мощь для того, чтобы подвергнуть разрушению кристаллическую решетку металла. Характеристикам плавления металлов уделяют внимание при подборе материала для сооружения узлов, подвергающихся силе трения или же конструкций из металла, которые испытывают воздействие температур.
Что такое температура плавления?
Чтобы узнать при какой температуре плавится металл, в лабораторных условиях, точку старта в начале процесса плавления вычисляют до сотой градусной доли. При этом данный показатель не находится в зависимости от усилия при давлении на деталь.
При создании определенного давления в условиях вакуума, заготовки из металла имеют одинаковую температуру плавления. Данное явление можно объяснить накоплением энергии внутри вещества, при которой разрушаются связи между молекулами.
Литий (180°C)
Этот удивительный металл, открыли только в начале XIX века. Литий (Lithium, элемент №3) довольно легкоплавкий – жидкий метал температуры всего 180°C можно помешивать даже деревянной ложечкой.
Литий отличается очень малой плотностью – вдвое легче воды! Металл относится к группе щелочных и довольно активен химически (поэтому его так долго не могли открыть).
В современном мире литий широко используется для создания удивительных сплавов – твёрдых, лёгких и жаропрочных.
Без лития не обходится ни одна современная электронная штучка. Ведь литий является ключевым компонентом компактных и ёмких аккумуляторов. А ещё, именно литий придаёт замечательный алый цвет фейерверкам.
Разница между температурой плавления и кипения
Температурой плавления металлов называют точку перехода твердокристаллического вещества в жидкое состояние. В составе расплава у молекул нет собственного места расположения, они удерживаются за счет силы притяжения, поэтому в разжиженном состоянии сохраняется объем, но теряется форма.
В процессе кипения происходит потеря молекулярного объема, а молекулы вяло взаимодействуют друг с другом, двигаясь хаотично в разных направлениях, отставая от поверхности. Температурой кипения называется процесс, при котором уровень давления металлического пара уравновешивается с давлением внешней среды.
Калий (63,5°C)
Близкий родственник натрия – калий. Элемент №19 (Kalium) также бурно реагирует с водой, образуя щёлочь, и также легкоплавок – 63,5°C. А вот съедобных соединений калия почти нет, и в этом он полная противоположность натрию. Хотя в ограниченно малых количествах организму всё-таки необходим (микроэлемент).
А вот съедобных соединений калия почти нет, и в этом он полная противоположность натрию. Хотя в ограниченно малых количествах организму всё-таки необходим (микроэлемент).
В чистом виде калий практического применения не имеет. Но его многочисленные соединения с древних времён известны как удобрения, моющие средства, важные компоненты многих химических процессов.
Температура плавления различных металлов
Согласно знаниям из раздела физики, процесс превращения твердого вещества в жидкое имеется лишь у тел с кристаллической решеткой. Температура плавления металлов и сплавов возникает в различном диапазоне значений. Но, с точностью высчитать пограничную температуру фазовых состояний у сплавов весьма проблематично. У чистых элементов имеет значимость каждый градус, если это составы с легкой плавкостью.
Железо
Температура плавления железных составов должна быть высокой. Если элемент обладает технической чистотой, то он плавится при температуре 1 539 °C. В составе его вещества присутствуют включения серы, поэтому для её извлечения необходимо жидкое состояние. Также очищенное железо получается в процессе электролиза солей металла.
Также очищенное железо получается в процессе электролиза солей металла.
Чугун
Чугун считается самым лучшим материалом для плавления. Он имеет хорошие показатели жидкой текучести и усадки, поэтому его эффективно использовать в процессе литья. Ниже будут приведены показатели температурного кипения чугуна:
Серая разновидность чугуна, у которой температурный режим доходит до отметки 1 260 °C. А при разливе его в формы, увеличивается до 1 400 °C.
Белая разновидность чугуна, у которого температура поднимается до 1 350 °C.
Одним из немаловажных моментов является то, что температура, которой обладает чугун, на 400 единиц меньше той же стали. Поэтому процесс обработки данного материала менее энергозатратен.
Сталь, температура плавления
Средняя температура плавления стали составляет 1400 °C.
Сталью называется железосодержащий сплав с включением углерода. Её основной характеристикой является прочность. Это достигается за счет того, что она долгое время сохраняет параметры объема и формы.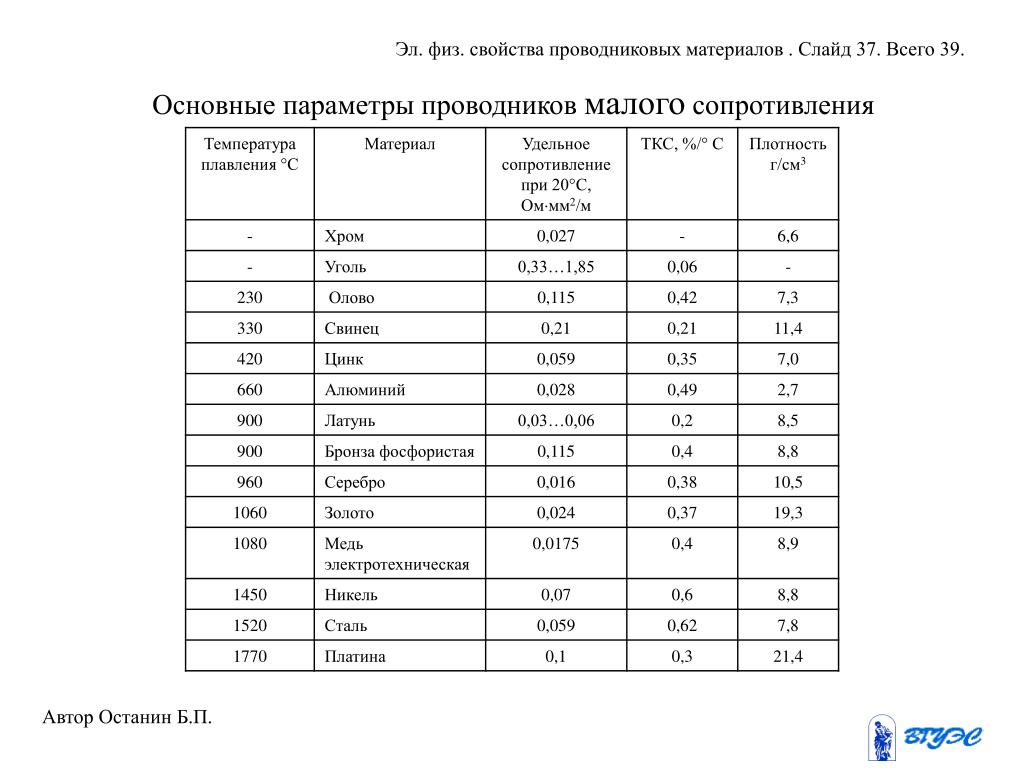 При этом расположение молекул в веществе находится в сбалансированном состоянии. Именно поэтому достигается равновесие между силой притяжения и силой отталкивания.
При этом расположение молекул в веществе находится в сбалансированном состоянии. Именно поэтому достигается равновесие между силой притяжения и силой отталкивания.
Диапазон плавления стали выше, чем у чугуна, поэтому она более энергозатратна.
Нержавеющая сталь
Температура плавления нержавеющей стали колеблется в среднем диапазоне между чугуном и сталью. Нержавеющей сталью называется вещество из легированной стали, обладающее антикоррозийными свойствами за счет содержания хрома в своем составе от 11% процентов и больше.
Показатели температуры плавления нержавейки составляют от 1 300 до 15 000 °C.
Алюминий и медь
Температура плавления алюминия составляет 6 600 °C, поэтому он зарекомендовал себя в качестве одного из среднеплавких металлов. Плавление чистых медных составов происходит при температуре 10 830 °C, а сплавов – 930 – 11 400 °C.
Серебро и золото
Серебро в чистом виде плавится при температуре 9 620 °C. При этом при температуре плавления серебра, оно может сравниться с температурой плавления в градусах со сплавами из меди.
Золото плавится при температуре в 10 640 °C.
Ртуть
Ртуть обладает самой низкой температурой плавления с отрицательным значением. Она составляет – 38,80 °C.
Олово (231°C)
Химический элемент, занимающий в периодической таблице юбилейное, пятидесятое место известен человечеству с древнейших времён. Первые капли олова (латинское наименование Stannum) первобытные люди заметили в своих кострах ещё за 4 тысячи лет до нашей эры. Немудрено – ведь олово плавится при температуре всего при 231°C. При этом дерево ещё только-только начинает обугливаться и робко гореть.
После застывания «слёзы», которыми плакал в огне красивый тяжёлый камень кассидерит, сохраняли форму, в которой им довелось застыть. Так появились первые металлические предметы кухонного быта.
Когда же удалось вытопить из зелёного малахита рыжую медь, оказалось, что смесь меди с оловом гораздо прочнее любого из металлов по отдельности. Тут-то цивилизация и начала бурно развиваться. Оружие, доспехи, посуда, инструменты – всё делали из прочной и красивой бронзы.
Таблица температур плавления
| Легкоплавкие металлы | |
| Литий | + 180 °C |
| Калий | + 63,60 °C |
| Индий | + 156,60 °C |
| Олово | + 2 320 °C |
| Таллий | + 3 040 °C |
| Кадмий | + 3 210 °C |
| Свинец | + 3 270 °C |
| Цинк | + 4 200 °C |
| Среднеплавкие металлы | |
| Магний | + 6 500 °C |
| Алюминий | + 6 600 °C |
| Барий | + 7 270 °C |
| Серебро | + 9 600 °C |
| Золото | +10 630 °C |
| Марганец | + 12 460 °C |
| Медь | + 10 830 °C |
| Никель | + 14 550 °C |
| Кобальт | + 14 950 °C |
| Железо | + 15 390 °C |
| Дюралей | + 6 500 °C |
| Латунь | + 950 – 10 500 °C |
| Чугун | + 1 100 – 13 000 °C |
| Тугоплавкие металлы | |
| Титан | + 16 800 °C |
| Платина | + 17 690 °C |
| Хром | + 19 070 °C |
| Цирконий | + 18 550 °C |
| Ванадий | + 19 100 °C |
| Иридий | + 24 470 °C |
| Молибден | + 26 230 °C |
| Тантал | + 30 170 °C |
| Вольфрам | + 34 200 °C |
Рубидий (39,31°C)
37-й элемент таблицы – рубидий (Rubidium) плавится всего при 39,31°C. Кусочек рубидия может растаять на блюдце как сливочное масло. Это лёгкий металл, его плотность лишь немного превышает плотность воды. Но реагирует с водой рубидий не менее бурно, чем его близкие родственники калий и натрий.
Кусочек рубидия может растаять на блюдце как сливочное масло. Это лёгкий металл, его плотность лишь немного превышает плотность воды. Но реагирует с водой рубидий не менее бурно, чем его близкие родственники калий и натрий.
Рубидий удивителен своими химическими свойствами. Сам по себе щелочной металл очень легко вступает в разнообразные химические реакции. Но при этом соли рубидия и его сплавы с другими металлами являются хорошими катализаторами реакций. То есть, значительно ускоряют процесс, при этом совершенно не расходуясь сами по себе. Это делает рубидий ценным материалом для химической промышленности и радиоэлектроники.
От чего зависит температура плавления?
У различных материалов различается, и температура их плавления, при которой происходит коренное перестраивание решетки до состояния жидкости. Металлические изделия и изделия из сплавов имеют следующие особенности:
- У различных материалов различается, и температура их плавления, при которой происходит коренное перестраивание решетки до состояния жидкости.
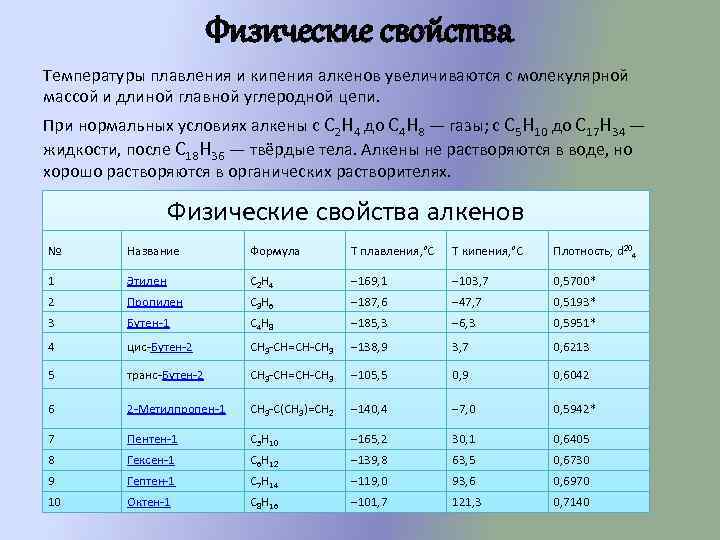 Металлические изделия и изделия из сплавов имеют следующие особенности:
Металлические изделия и изделия из сплавов имеют следующие особенности: - Они редко встречаются в натуральном виде, т.е. без примесей. Именно состав определяет, какой должна быть температура плавки. В пример можно взять олово, в которое добавляют включения серебра. Благодаря примесям материал начинает становится устойчивым к воздействию температуры.
- Существуют такие сплавы, которые из-за химического состава трансформируются в жидкое состояние, когда столбик термометра поднимается чуть выше отметки в + 1 500 °C. Есть и такие сплавы, которые «держатся», если их нагревать до 30 000 °C.
- Стоит учитывать тот факт, что одним из наиболее важных свойств веществ является их точка плавления. В качестве примера можно привести авиационную технику.
Натрий (97,8°C)
Натрий (Natrium, 11-й элемент) может расплавиться даже в кипятке – 97,8°C. Но мы бы не советовали позволить даже маленькому кусочку натрия упасть в воду (хотя бы и ледяную). Щелочной металл натрий очень активен химически и немедленно реагирует, отделяя от молекул воды водород и превращаясь в сильнейшую щелочь.
При этом выделяется много тепла, которое тут же поджигает освободившийся водород. Взрыв и пожар! Такие материалы как натрий хранят в керосине, что исключает их контакт с водой и влагой воздуха.
Как очень активный элемент, натрий в том или ином виде присутствует вокруг нас в огромных количествах. Взять хотя бы хлорид натрия – обычная поваренная соль.
Типы сплавов металлов
Типы металлических сплавов различаются на основе температуры плавления, поэтому выделяют следующие варианты сплава:
- Легкоплавкий (олово, цинк, свинец, висмут) с температурой плавления не больше 600 °C.
- Среднеплавкий (алюминий, магний, никель, железо) с температурой 600 – 1 600 °C.
- Тугоплавкий (молибден, вольфрам, титан) с температурой более 1 600 °C.
Далее расскажем немного о разновидностях сталей, о сплаве вуда и припоях.
Особенности углеродистой стали
В данном материале содержится примесь углерода, примерно 2,13 %. При этом он лишен легирующих добавок, но есть примеси кремния, марганца и магния.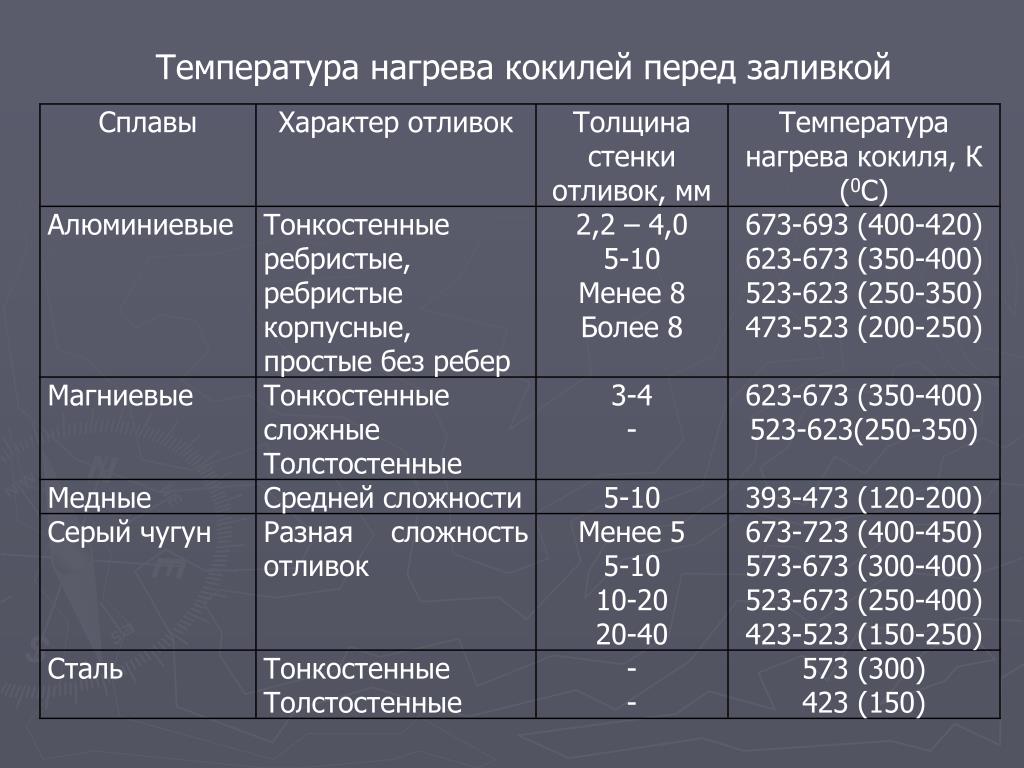
Особенности легированной стали
Помимо содержания углерода и железа в неё добавляют дополнительные элементы, улучшающие её свойства.
Особенности нержавейки
Нержавеющая сталь отлична от углеродистой из-за содержания элемента хрома в своем составе, благодаря свойствам которого она не подвержена окислению, а, следовательно, покрытию ржавчиной.
Особенности инструментальной стали
Также обладает углеродистым составом (0,8 – 0,9 %). Демонстрирует твердость, прочность, хорошо поддаются обработке. Используется в изготовлении инструментов, например, медицинских.
Сплав Вуда
Представляет собой материал, применяемый при паянии деталей для радиоприемников, а также в гальванической пластике, при работе в лабораторных условиях с ядохимикатами.
Сплавы для пайки
Другое их название – припои. Материалы для припоев бывают различными. Все зависит от того, что входит в состав материалов, которые необходимо соединить. К примеру, алюминий требует один сплав припоя, а вот медь уже совершенно другой.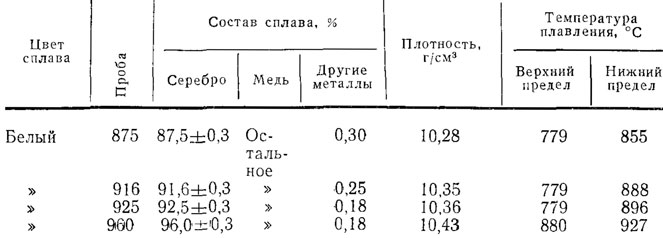
Индий (157°C)
В конце XIX века химикам удалось открыть и выделить в чистом виде элемент, занявший в периодической таблице клетку №49. Индий (Indium) – довольно тяжёлый (почти как железо) металл, плавящийся при 157°C.
Этот материал поразительно мягок и пластичен. Мягче этого металла только тальк! Невероятное свойство сделало индий незаменимым в радиоэлектронике. Тонкие индиевые полоски, нанесённые на стекло, хорошо проводят электрический ток – но при этом совершенно прозрачны. Так делают уже привычные нам плоские экраны на основе «жидких кристаллов» (LCD).
Физиологическое действие
Никель и его соединения токсичны и канцерогены.
Никель — основная причина аллергии (контактного дерматита) на металлы, контактирующие с кожей (украшения, часы, джинсовые заклепки). В 2008 году Американским обществом контактного дерматита никель был признан «Аллергеном года». В Евросоюзе ограничено содержание никеля в продукции, контактирующей с кожей человека.
В XX веке было установлено, что поджелудочная железа очень богата никелем. При введении вслед за инсулином никеля продлевается действие инсулина и тем самым повышается гипогликемическая активность. Никель оказывает влияние на ферментативные процессы, окисление аскорбиновой кислоты, ускоряет переход сульфгидрильных групп в дисульфидные. Никель может угнетать действие адреналина и снижать артериальное давление. Избыточное поступление никеля в организм вызывает витилиго. Депонируется никель в поджелудочной и околощитовидной железах.
При введении вслед за инсулином никеля продлевается действие инсулина и тем самым повышается гипогликемическая активность. Никель оказывает влияние на ферментативные процессы, окисление аскорбиновой кислоты, ускоряет переход сульфгидрильных групп в дисульфидные. Никель может угнетать действие адреналина и снижать артериальное давление. Избыточное поступление никеля в организм вызывает витилиго. Депонируется никель в поджелудочной и околощитовидной железах.
Цезий (28,5°C)
Очень мягкий серебристый металл буквально плавится в руках. При температуре 28,5°C цезий (Caesium) становится жидкостью и буквально утекает между пальцев. Но не вздумайте провести такой опыт! Из всех щелочных металлов элемент №55 самый химически активный (уступая лишь францию).
На открытом воздухе цезий моментально окисляется, образуя яркое пламя. А при попадании в воду просто взрывается. Цезий ухитряется поджечь даже лёд! Более того, образовавшийся при реакции с водой гидроксид цезия разъедает стекло – и потихоньку грызёт сосуды из золота и даже платины.
А вот в электронике такая активность цезия позволяет делать очень чувствительные фотоэлементы и часы поистине космической точности.
Галлий (26,79°C)
А вот серебристый металл галлий (Gallium – ещё до открытия элемента Д.И. Менделеев заранее оставил ему в таблице клеточку № 31) встречается гораздо чаще и нередко применяется просто для забав. Плавится он почти как цезий, при 26,79°C, но в остальном разительно отличается от своего «нервного» братца.
Внешне и по механическим свойствам галлий очень похож на алюминий. Лёгок, теплопроводен, в чистом виде довольно хрупок. Мгновенно образующаяся на воздухе плотная плёнка окислов так же хорошо защищает его от разрушения.
В чистом виде галлий практически не находит применения. А вот его соли и, особенно, легкоплавкие сплавы нашли широчайшее применение в ядерной физике, радиоэлектронике, измерительной технике.
Франций (27°C)
Элемент, занимающий 89-ю ячейку периодической таблицы – франций (Francium) – очень похож на цезий. Франций плавится при 27°C, но до этого неимоверно активный щелочной металл ещё требуется сберечь.
Франций плавится при 27°C, но до этого неимоверно активный щелочной металл ещё требуется сберечь.
Мало того, что франций бурно реагирует буквально со всем подряд – он ещё и очень радиоактивен! Буквально через полчаса от килограмма франция останется – хорошо если горстка – разнообразных сильно излучающих продуктов деления.
Впрочем, в таких количествах его никто никогда и не видел. Неудивительно, что в природе этот элемент один из самых редко встречающихся. Да и практического применения ему так и не нашлось.
Ртуть (-38,87°C)
Все мы хорошо знакомы со ртутью – даже сегодня, в век электроники, вряд ли найдётся хоть один человек, которому не измеряли бы температуру тела ртутным термометром. Но мало кто задумывается, что очень текучая тяжёлая серебристая жидкость – самый настоящий металл!
Да-да, элемент №80, Hydrargyrum, плавится на самом лютом морозе – температура кристаллизации ртути почти минус сорок градусов (-38,87°C).
Человечество знакомо со ртутью с древнейших времён. Ртуть находит широчайшее применение в технике, химии, металлургии. Этот элемент достоин отдельного, немаленького рассказа – а сегодня он гордо венчает наш рейтинг.
Ртуть находит широчайшее применение в технике, химии, металлургии. Этот элемент достоин отдельного, немаленького рассказа – а сегодня он гордо венчает наш рейтинг.
Добыча полезных ископаемых
Руд, в которых присутствует железо, существует несколько. Однако, в качестве сырья для производства железа в промышленности используют в основном следующие:
А также часто встречаются такие разновидности руды:
Существует еще минерал под названием мелантерит. Его используют преимущественно в фармацевтической промышленности. Из себя он представляет зелёного цвета хрупкие кристаллы, в которых присутствует стеклянный блеск. Из него производят лекарственные препараты, в составе которых имеется ферум.
Основным месторождением этого металла является Южная Америка, а именно Бразилия.
Как происходит
Плавление всех металлов происходит примерно одинаково – при помощи внешнего или внутреннего нагревания. Первый осуществляется в термической печи, для второго используют резистивный нагрев при пропускании электрического тока или индукционный нагрев в высокочастотном электромагнитном поле. Оба варианта воздействуют на металл примерно одинаково.
Оба варианта воздействуют на металл примерно одинаково.
При увеличении температуры увеличивается и амплитуда тепловых колебаний молекул, возникают структурные дефекты решетки, выражающиеся в росте дислокаций, перескоке атомов и других нарушениях. Это сопровождается разрывом межатомных связей и требует определенного количества энергии. В это же время происходит образование квази-жидкого слоя на поверхности тела. Период разрушения решетки и накопления дефектов называется плавлением.
Вольфрам
Самая высокая температура плавления – у металла вольфрама. Выше него по этому показателю стоит только неметалл углерод. Вольфрам представляет собой светло-серое блестящее вещество, очень плотное и тяжелое. Он кипит при 5555 °C, что почти приравнивается к температуре фотосферы Солнца.
При комнатных условиях он слабо реагирует с кислородом и не подвергается коррозии. Несмотря на свою тугоплавкость, он довольно пластичен и поддается ковке уже при нагревании до 1600 °C. Эти свойства вольфрама используют для нитей накаливания в лампах и кинескопах электродов для сварки. Большую часть добытого металла сплавляют со сталью, чтобы повысить ее прочность и твердость.
Большую часть добытого металла сплавляют со сталью, чтобы повысить ее прочность и твердость.
Широкое применение вольфрам имеет в военной сфере и технике. Он незаменим для изготовления боеприпасов, брони, двигателей и наиболее важных частей военного транспорта и самолетов. Из него также делают хирургические инструменты, ящики для хранения радиоактивных веществ.
Металлы и сплавы как литейный материал / Кустарь
Для литейных работ юного мастера пригодны будут главным образом легкоплавкие металлы и их сплавы. Температуру печи для плавки или горна трудно будет получить выше 1000°, поэтому брать для литья придется лишь металлы с более низкой температурой плавления. Для большинства работ наилучшими будут цинк, свинец и их сплавы, гарт, или типографский металл, из которого льют шрифт и матрицы для печатания, пепельницы, всевозможные подставки.
Вторым распространенным сплавом является баббит — металл, употребляющийся для заливки подшипников. В литейную мастерскую наших мастеров эти материалы будут попадать главным образом в виде различных обломков металла с неизвестным составом. Придется произвести сначала простейшую сортировку по внешним свойствам. Надо попробовать кусочки гнуть, ломать. Если куски легко ломаются, с крупнозернистым светлым изломом и блеском, то это будет гарт или баббит. Излом более темного цвета и мелкокристаллический и металл, труднее поддающийся излому, укажут на цинк. Гибкий, неломающийся кусок, легко расплющивающийся под молотком, темно-серого цвета, можно сразу признать за свинец. Таким образом производится приблизительная сортировка литейного металла.
Придется произвести сначала простейшую сортировку по внешним свойствам. Надо попробовать кусочки гнуть, ломать. Если куски легко ломаются, с крупнозернистым светлым изломом и блеском, то это будет гарт или баббит. Излом более темного цвета и мелкокристаллический и металл, труднее поддающийся излому, укажут на цинк. Гибкий, неломающийся кусок, легко расплющивающийся под молотком, темно-серого цвета, можно сразу признать за свинец. Таким образом производится приблизительная сортировка литейного металла.
Чистый цинк плавится при 419°, свинец — при 327°, а различные сплавы этих металлов при еще более низкой температуре. И цинк и его сплавы очень хорошо заполняют все мелкие детали формы. Цинк и его сплавы являются для юного мастера самым подходящим литейным металлом. Свинец хотя плавится легко, но хуже заполняет форму. Всё же это будут два самых подходящих металла, хотя в промышленном машиностроении главными литейными материалами являются чугун, сталь и бронза.
Сравнительно невелика температура плавления алюминия— 659°. Литье из алюминия требует большого уменья, так как при неподходящих условиях плавки он дает большое количество раковин в отливке. Но всё же отливка из него при некотором навыке хорошо удается. Там, где от литого изделия юному мастеру потребуется большая прочность, можно взять и более тугоплавкий металл — алюминий.
Литье из алюминия требует большого уменья, так как при неподходящих условиях плавки он дает большое количество раковин в отливке. Но всё же отливка из него при некотором навыке хорошо удается. Там, где от литого изделия юному мастеру потребуется большая прочность, можно взять и более тугоплавкий металл — алюминий.
Отличный литейный материал представляют собою различные бронзы, но они уже требуют гораздо более высоких температур, в пределах до 900°, которых труднее достигнуть.
При плавлении металлов необходимо соблюдать известные правила. Положим, что собираются плавить свинец и цинк. Свинец быстро расплавится, имея температуру плавления 327°; цинк же еще долго будет оставаться твердым, так как его температура плавления выше 419°. Что произойдет со свинцом при таком перегреве? Он начнет покрываться пленкой радужного цвета, а потом его поверхность окажется скрытой под слоем неплавящегося порошка. Свинец угорел от перегрева, окислился, соединившись с кислородом воздуха. Этот процесс, как известно, происходит и при обычной температуре, но при нагревании он идет гораздо быстрее. Таким образом, к тому времени, когда начнет плавиться цинк, останется очень мало металлического свинца. Сплав получится совсем не того состава, как предполагался, и потеряется большое количество свинца в виде угара. Ясно, что надо сначала плавить более тугоплавкий цинк и затем класть в него свинец.
Этот процесс, как известно, происходит и при обычной температуре, но при нагревании он идет гораздо быстрее. Таким образом, к тому времени, когда начнет плавиться цинк, останется очень мало металлического свинца. Сплав получится совсем не того состава, как предполагался, и потеряется большое количество свинца в виде угара. Ясно, что надо сначала плавить более тугоплавкий цинк и затем класть в него свинец.
То же самое произойдет, если сплавлять цинк с медью или латунью, разогревая сначала цинк. Цинк угорит к моменту расплавления меди. Значит, надо всегда сначала плавить металл с более высокой температурой плавления. Так как температура плавления сплавов обычно ниже температуры плавления наиболее тугоплавкого из составляющих сплав металлов, то иногда выгодно поступать наоборот: сперва расплавить более легкоплавкий металл, а затем — более тугоплавкий. Однако это допустимо лишь для металлов, не сильно окисляющихся, или при условии предохранения этих металлов от излишнего окисления. Но одним этим угара не избежать. Если правильно разогретый сплав долго держать на огне, опять образуется на поверхности жидкого металла пленка как следствие угара. Ясно, что опять обратится в окись более легкоплавкий металл и состав сплава изменится; значит, нельзя металл долго перегревать без надобности. Поэтому стараются всячески уменьшить угар металла, укладывая его компактной массой; мелкие куски, опилки, стружки сначала «пакетируют», плавят куски более или менее одинаковой величины, ведут нагрев при достаточной температуре, оберегают поверхность металла от соприкосновения с воздухом. Для этой цели юный мастер может брать буру или просто прикрывать поверхность металла слоем золы, которая всегда будет плавать наверху (благодаря своему меньшему удельному весу) и при выливании металла не помешает. При застывании металла происходит еще одно явление, вероятно также знакомое юным мастерам. Металл, застывая, уменьшается в объеме, причем это уменьшение происходит за счет внутренних, еще не застывших частиц металла.
Но одним этим угара не избежать. Если правильно разогретый сплав долго держать на огне, опять образуется на поверхности жидкого металла пленка как следствие угара. Ясно, что опять обратится в окись более легкоплавкий металл и состав сплава изменится; значит, нельзя металл долго перегревать без надобности. Поэтому стараются всячески уменьшить угар металла, укладывая его компактной массой; мелкие куски, опилки, стружки сначала «пакетируют», плавят куски более или менее одинаковой величины, ведут нагрев при достаточной температуре, оберегают поверхность металла от соприкосновения с воздухом. Для этой цели юный мастер может брать буру или просто прикрывать поверхность металла слоем золы, которая всегда будет плавать наверху (благодаря своему меньшему удельному весу) и при выливании металла не помешает. При застывании металла происходит еще одно явление, вероятно также знакомое юным мастерам. Металл, застывая, уменьшается в объеме, причем это уменьшение происходит за счет внутренних, еще не застывших частиц металла. На поверхности отливки или внутри нее образуется более или менее значительное воронкообразное углубление, так называемая усадочная раковина. Обычно форму делают так, чтобы усадочные раковины получились в тех местах отливки, которые впоследствии удаляются, стараясь по возможности предохранить самое изделие. Понятно, что усадочные раковины портят отливку и иногда могут сделать ее негодной.
На поверхности отливки или внутри нее образуется более или менее значительное воронкообразное углубление, так называемая усадочная раковина. Обычно форму делают так, чтобы усадочные раковины получились в тех местах отливки, которые впоследствии удаляются, стараясь по возможности предохранить самое изделие. Понятно, что усадочные раковины портят отливку и иногда могут сделать ее негодной.
После расплавления металл несколько перегревают, чтобы он был жиже и горячее и поэтому лучше заполнил бы детали формы и не застыл бы преждевременно от соприкосновения с более холодной формой.
Металла надо брать больше, чем требуется для самой вещи, чтобы он заполнил не только форму, но и литниковый канал. Ясно, что надо сначала рассчитать необходимое количество металла. Существуют таблицы, позволяющие точно определить вес отливки по весу модели. Приводим некоторые цифры из такой таблицы.
| Модель сделана из: | Предмет отливается из: | ||
|---|---|---|---|
| латуни | бронзы | цинка | |
| Ели и сосны | 15,8 | 16,6 | 13,5 |
| Липы | 15,1 | 15,5 | 12,9 |
| Березы | 11,9 | 12,3 | 10,2 |
| Дуба | 10,1 | 10,4 | 8,6 |
Вес модели надо умножить на соответствующее число таблицы.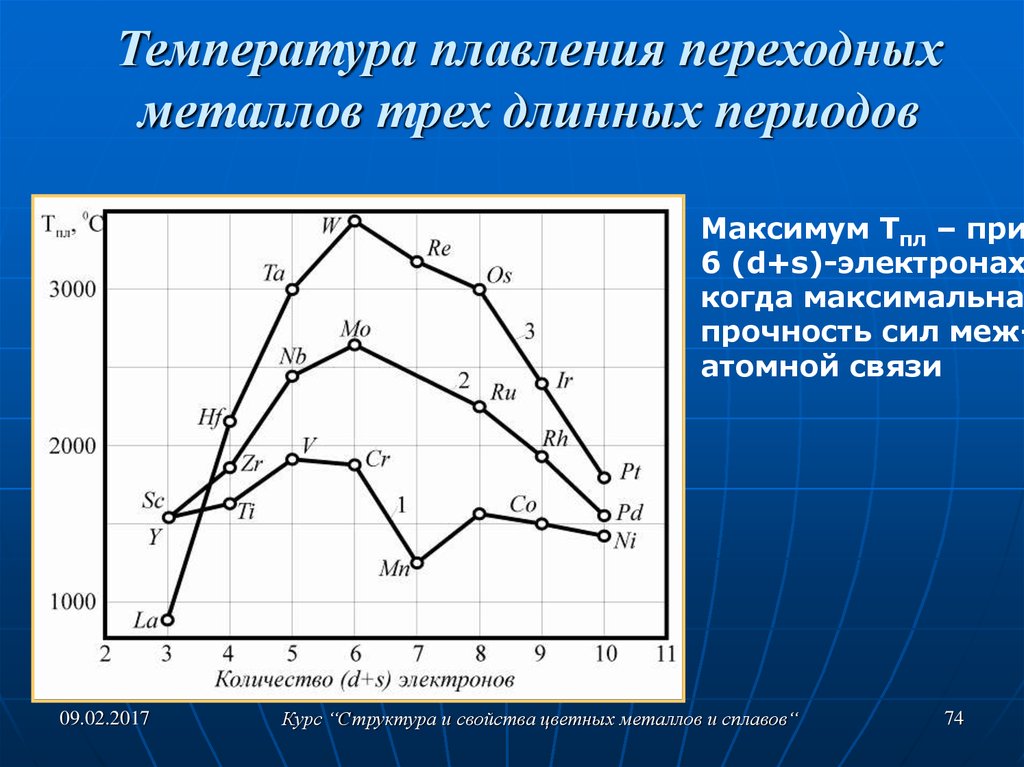 Нужно предупредить всё же, что этот способ будет справедлив лишь для сплошных литых деталей, не имеющих каких-либо пустот внутри, что часто делается для облегчения веса отливки или требуется самой конструкцией отливки. Для различных подсчетов прилагаем удельные веса материалов, могущих встретиться в работе:
Нужно предупредить всё же, что этот способ будет справедлив лишь для сплошных литых деталей, не имеющих каких-либо пустот внутри, что часто делается для облегчения веса отливки или требуется самой конструкцией отливки. Для различных подсчетов прилагаем удельные веса материалов, могущих встретиться в работе:
| Удельный вес латуни | 8,4—8,5 |
| Удельный вес цинка | 7,14 |
| Удельный вес бронзы | 7,4—8,9 |
| Удельный вес свинца | 11,40 |
| Удельный вес алюминия | 2,70 |
| Удельный вес баббита | 7,1 |
| Удельный вес песка сырого | 1,90—2,05 |
| Удельный вес земли глинистой | 2,0 |
| Удельный вес ели или сосны | 0,48—0,60 |
| Удельный вес липы | 0,45 |
| Удельный вес березы | 0,72 |
| Удельный вес дуба | 0,80 |
Этих данных достаточно для различных подсчетов при определении примерного веса будущей отливки и веса земли в опоке или том ящике, где делается форма. Если вес модели известен и будет изготовлена она из материала, удельный вес которого тоже известен, то составляют пропорцию:
Если вес модели известен и будет изготовлена она из материала, удельный вес которого тоже известен, то составляют пропорцию:
|
искомый вес отливки
вес модели
|
  = 
|
удельный вес металла
удельный вес дерева модели
|
Из этой пропорции находят с достаточной точностью нужную величину.
Автор: П.В. Леонтьев
Читайте еще:
- Металлы и сплавы как литейный материал
- Модели и инструменты литейщика
- Ковши и тигли
- Плавильный горн
- Муфельные и тигельные печи
- Формовка
- Заливка формы
- Примеры отливок
плавка алюминиевой бронзы в домашних условиях
Металлы и сплавы
- Температура плавления
- Чистый металл
- Смеси
- Пошаговая инструкция
- Подготовка инструмента
- Литейная форма
- Как улучшить качество продукции?
Бронза — первый сплав, который люди научились изготавливать тысячи лет назад. С тех пор изделия из бронзы пользуются большой популярностью. Сегодня современные мастера стараются адаптировать литейные технологии к домашним условиям, для этого необходимо знать химический состав и физические свойства бронзы, а также технические характеристики получаемых из нее сплавов, в том числе алюминиевой бронзы.
С тех пор изделия из бронзы пользуются большой популярностью. Сегодня современные мастера стараются адаптировать литейные технологии к домашним условиям, для этого необходимо знать химический состав и физические свойства бронзы, а также технические характеристики получаемых из нее сплавов, в том числе алюминиевой бронзы.
В данной статье рассказывается о таком важном показателе как температура плавления, а так же как поэтапно проводить процесс плавки и литья бронзы.
Температура плавления
Существует Таблица температур плавления различных видов бронзы. Прежде чем приступить непосредственно к плавке, необходимо понять, от чего зависит температура, при которой тот или иной металл начинает плавиться или полностью переходит в жидкое состояние. Бронза фактически представляет собой ряд различных сплавов , в состав которых в качестве основного компонента входит медь, а в качестве дополнительных (легирующих) элементов — другие.
Такими легирующими веществами могут быть алюминий, бериллий, олово, кремний и т.д. Вот только от химического состава бронзы зависят все физические свойства металла, в том числе и температура плавления. Чтобы расплавить медный сплав, нужно знать его химический состав , только так можно правильно определить температуру плавления в градусах Цельсия. Познакомимся с точками плавления.
Чистый металл
Хотя производить чистую медь крайне невыгодно, так как ее технические свойства во многом уступают специальным маркам, которые изготавливаются из этого металла в металлургической промышленности, тем не менее необходима температура плавления меди .
Почему? Дело в том, что те марки меди, которые используются в народном хозяйстве, имеют в своем составе ничтожно малое количество легирующих веществ, считающихся примесями. Так, из-за незначительности их количества температура плавления медных марок близка к температуре плавления чистой меди и составляет приблизительно 1084,5 градуса по Цельсию.
Как уже было сказано, температура плавления зависит от состава вещества, по этой причине температура плавления бронзы колеблется в пределах 900-1140 градусов Цельсия.
Смеси
Бронзовое олово снижает температуру плавления таких сплавов, она не превышает 900-950 градусов Цельсия .
Безоловянные, в том числе алюминиевые бронзы имеют более широкий диапазон температур, зависящих от химического состава медного сплава. Их температура плавления равна 9.0025 950-1080 градусов. Также необходимо учитывать, что бронза имеет высокую вязкость поэтому после окончательной плавки ее перегревают для обеспечения лучшего течения расплава. Рассмотрим процесс плавки и литья бронзы поэтапно.
Пошаговая инструкция
В кустарных условиях изготавливаются в основном мелкие изделия из бронзы, например, элементы декора. Более сложные детали требуют высокоточного литья, технологию которого очень сложно реализовать без специально приспособленного для этих целей помещения а также специальное оборудование . В некоторых случаях приходится прибегать к доводке отливки до нужного состояния с помощью правки в домашних условиях типа удаления лишнего расплавленного материала вручную, шлифовки и полировки изделия.
В некоторых случаях приходится прибегать к доводке отливки до нужного состояния с помощью правки в домашних условиях типа удаления лишнего расплавленного материала вручную, шлифовки и полировки изделия.
Перед началом плавки металла необходимо подготовить помещение и приобрести необходимые инструменты и оборудование . Главное требование к помещению – наличие хорошей вытяжной вентиляции, а также пол из негорючих материалов, таких как бетон, цемент или кирпич. При изготовлении небольших изделий эти требования соблюдать довольно просто, иначе придется использовать гараж.
Для того, чтобы сделать выплавку бронзы в домашних условиях, необходимо приобрести специальную муфельную печь с возможностью регулирования температуры, но можно обойтись и простой добычей, топливом для которой будет древесный уголь.
Подготовка инструмента
Начинающий литейщик должен приобрести или изготовить следующие инструменты самостоятельно.
- Тигель огнеупорный из тугоплавкого материала (например, из чугуна или стали) представляет собой специальный сосуд с носиком, куда помещаются куски расплавленного металла.
- Устройствами для извлечения тигля из печи, сводящими к минимуму риск ожогов, являются специальные крючки и щипцы.
- Форма для заливки расплавленного металла, которая изготавливается с использованием опоки и модели.
- Сама опока — два ящика, которые держат форму с наполнителем из формовочной смеси.
- Костюм сварщика или просто очень плотный фартук и рукавицы, назначение которых — защитить человека от летящих искр и брызг расплавленного металла.
Как только вы убедились в наличии всего вышеперечисленного, можно приступать непосредственно к плавке бронзы.
- Разогрейте духовку , установив температуру с помощью ручки. Температура зависит от химического состава бронзы, как мы обсуждали выше. Например, для алюминиевой бронзы эта температура составит 1040-1084 градуса Цельсия.

- Далее необходимо прогреть форму , это делается для того, чтобы расплавленный металл не замерз при попадании в холодную емкость. Форма помещается в печь, когда она прогреется до температуры 600 градусов, после термостат установлен на 900 градусов. Когда температура внутри духовки поднимется до 900 градусов, форму оставляют прогреваться на 3-4 часа, после чего ее осторожно вынимают с помощью специальных приспособлений и охлаждают до 500 градусов Цельсия.
- Ставят тигель с кусками бронзы , предназначенными для плавки, внутрь нагретой до нужной температуры плавки печи и доводят до полного плавления металла. После этого тигель оставляют для перегрева еще на 5 минут, чтобы добиться лучшего течения металла и лучшего качества отливки.
- Вытащите тигель из печи или пода с помощью крючков и щипцов и начните заполнять форму.
Давайте рассмотрим, как правильно оформить форму для получения продукции высокого качества. В литейных цехах эту форму изготавливают с использованием опоки , куда заливают смесь глины, песка и угольного порошка. Опока состоит из двух половинок, каждая из которых представляет собой ящик, куда будет заливаться формовочная смесь.
В литейных цехах эту форму изготавливают с использованием опоки , куда заливают смесь глины, песка и угольного порошка. Опока состоит из двух половинок, каждая из которых представляет собой ящик, куда будет заливаться формовочная смесь.
- Сначала берем первую коробку и начинаем заполнять ее смесью, наливая ее до половины, помещаем модель внутрь коробки.
- Затем продолжайте засыпать сыпучий материал, пока не заполните ящик до самого верха. В процессе работы требуется постоянно выравнивать и утрамбовывать формовочную смесь.
- Установите сверху второй ящик и продолжайте засыпать смесью глины, песка и угольного порошка.
- Во второй коробке необходимо предусмотреть литники — отверстия для заливки расплавленной бронзы в форму.
- Когда оба ящика заполнены доверху, их отделяют острым предметом. Одна половина модели в одном ящике, другая в другом.
- Аккуратно вынимают модель, снова соединяют оба ящика — образовавшаяся пустота и есть форма для заполнения.
Литейная форма
Расплавленный металл заливают из тигля тонкой струйкой в форму , следя за тем, чтобы струйка текла непрерывно. Если отливаемая деталь отличается сложностью контура , необходимо использовать специальную центрифугу , которая с помощью центробежной силы поможет расплаву правильно распределиться внутри формы, полностью заполняя ее.
Как улучшить качество продукции?
На самом деле по настоящему качественную вещь не получить в домашних условиях без доработки.
Вы также можете улучшить качество и внешний вид, изготовив форму из легкоплавкого материала . Для этого предварительно делают гипсовый слепок с модели, по которой будет изготовлена наша деталь, этот слепок должен состоять из двух частей, которые скрепляются между собой. В образовавшуюся полость заливают расплавленный в кипятке парафин или воск, а после его застывания удаляют гипсовую оболочку.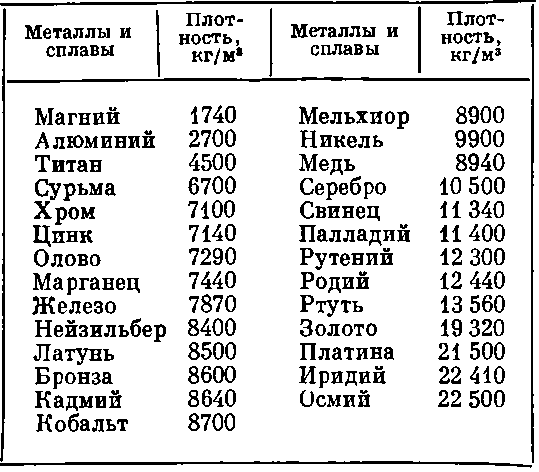
Далее полученную легкоплавкую модель помещают в специальную литейную массу, формируя отверстия для слива парафина и заливки расплавленной бронзы. После этого литейная масса помещается в кипящую воду, парафин плавится и легко выливается из формы.
Полученная форма имеет большую гладкость, из нее получаются более качественные изделия, чем из формы, изготовленной обычным способом.
В следующем видео показан процесс выплавки бронзы в домашних условиях.
Металл с высокой температурой плавления
Металл с высокой температурой плавления | Топ-10 металлов с высокими температурами плавления
4 комментария
админ
Просмотры сообщений:
19,542
Многие знают, что металл с самой низкой температурой плавления — это ртуть, которая является единственным металлом, который находится в жидком состоянии при комнатной температуре.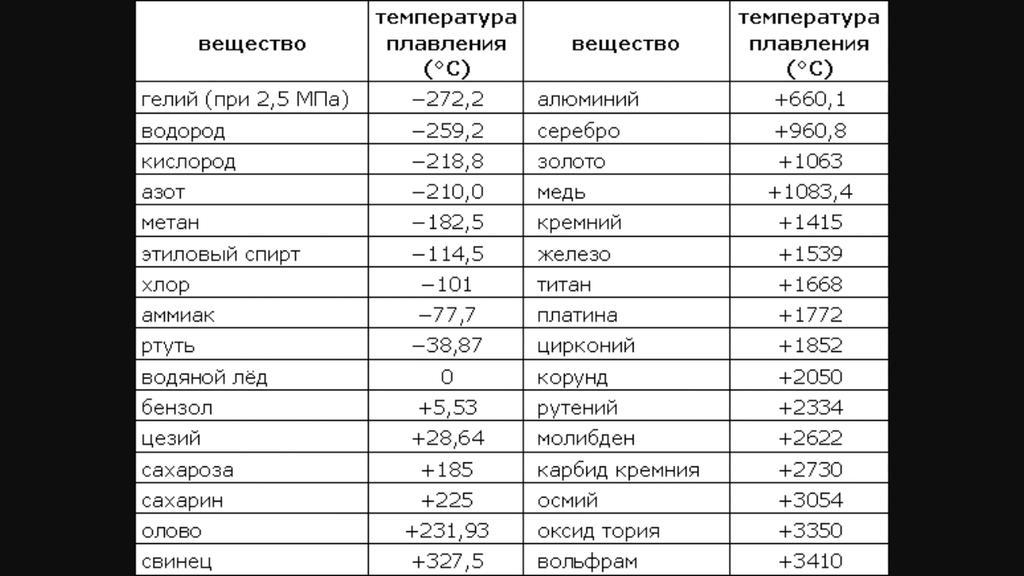 Но когда дело доходит до металла с высокой температурой плавления , вероятно, немногие знают ответ. Вот почему мы составили этот список металлов с высокой температурой плавления — 10 лучших.0003
Но когда дело доходит до металла с высокой температурой плавления , вероятно, немногие знают ответ. Вот почему мы составили этот список металлов с высокой температурой плавления — 10 лучших.0003
Металл с высокой температурой плавления
Металл с высокой температурой плавления — верхняя часть 1. Вольфрам (W)
Вольфрам — тугоплавкий металл с самой высокой температурой плавления (3420 °C) . Наиболее важным преимуществом вольфрама как тугоплавкого металла является то, что он обладает хорошей жаропрочностью и хорошей коррозионной стойкостью к расплавленному щелочному металлу и пару. Только когда температура вольфрама превышает 1000 ℃, происходит улетучивание оксида и образование оксидов в жидкой фазе.
Однако недостатком этого материала является то, что его трудно пластически обрабатывать при комнатной температуре. Тугоплавкие металлы, представленные вольфрамом, широко используются в металлургии, химической промышленности, электронике, светотехнике, машиностроении.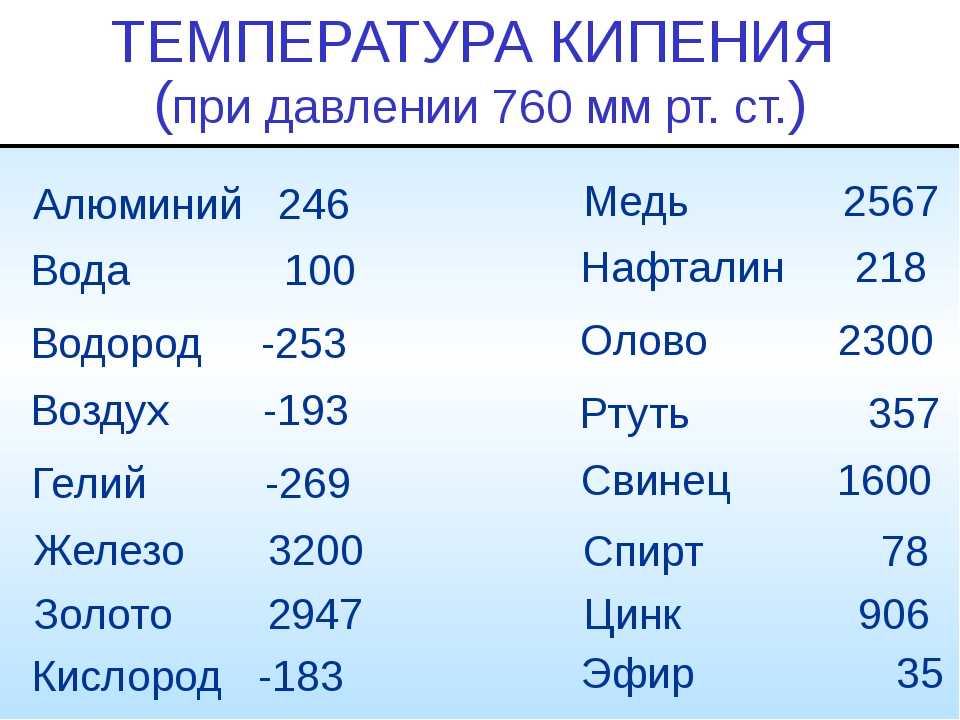
Вольфрам
Металл с высокой температурой плавления – Вверху 2. Рений (Re)
Рений представляет собой серебристо-белый металл со второй по величине температурой плавления ( 3180 °C ) после вольфрама и имеет самую высокую точка кипения. Коммерческий рений обычно представляет собой порошок, и его можно прессовать или спекать в твердое вещество высокой плотности в вакууме или водороде с плотностью более 90% металлического состояния.
Рениевые металлы обладают высокой пластичностью при отжиге, их можно сгибать и сворачивать. Блоки рения устойчивы к щелочам, серной кислоте, соляной кислоте, разбавленной азотной кислоте (азотная кислота неконцентрированная) и царской водке при стандартных температуре и давлении.
Рений
Мировое годовое производство рения колеблется от 40 до 50 тонн, в основном в Чили, США, Перу и Польше. Около 70% мирового рения используется для изготовления деталей из жаропрочных сплавов для реактивных двигателей. Еще одним важным применением рения являются платино-рениевые катализаторы, которые можно использовать для производства бессвинцового высокооктанового бензина.
Еще одним важным применением рения являются платино-рениевые катализаторы, которые можно использовать для производства бессвинцового высокооктанового бензина.
Металл с высокой температурой плавления – Топ 3. Тантал (Ta)
Тантал занимает третье место в нашем списке металлов с высокой температурой плавления. Он имеет температуру плавления 2966 °C .
Тантал можно вытягивать в тонкую фольгу благодаря его умеренной твердости и пластичности. Тантал имеет очень маленький коэффициент теплового расширения. Тантал обладает отличными химическими свойствами и обладает высокой устойчивостью к коррозии. Не реагирует на соляную кислоту, концентрированную азотную кислоту и «царскую водку» как в холодных, так и в горячих условиях.
Тантал
Тантал можно использовать для изготовления испарительных сосудов, а также электродов, выпрямителей и электролитических конденсаторов для электронных ламп. Тантал используется в медицине для изготовления тонких срезов или нитей для восстановления поврежденных тканей.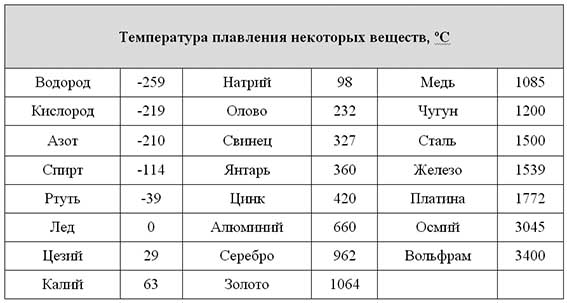
Тантал используется в конденсаторах для использования в военной технике. Половина производимого в мире тантала используется для изготовления танталовых конденсаторов. Американское агентство оборонной логистики, крупнейший владелец металла, однажды выкупило треть мировых запасов тантала.
Металл с высокой температурой плавления — Top 4. Молибден (Mo)
Молибден , как и вольфрам, является тугоплавким металлом. Он занимает 4-е место в нашем списке металлов с высокой температурой плавления. Его температура плавления составляет 2620 °C .
Молибден в основном используется в черной металлургии. Добавление молибдена в нержавеющую сталь может улучшить коррозионную стойкость стали. Добавление молибдена к чугуну может улучшить его прочность и износостойкость.
Молибден
Суперсплав на основе никеля, содержащий 18% молибдена , обладает высокой температурой плавления, низкой плотностью и малым коэффициентом теплового расширения.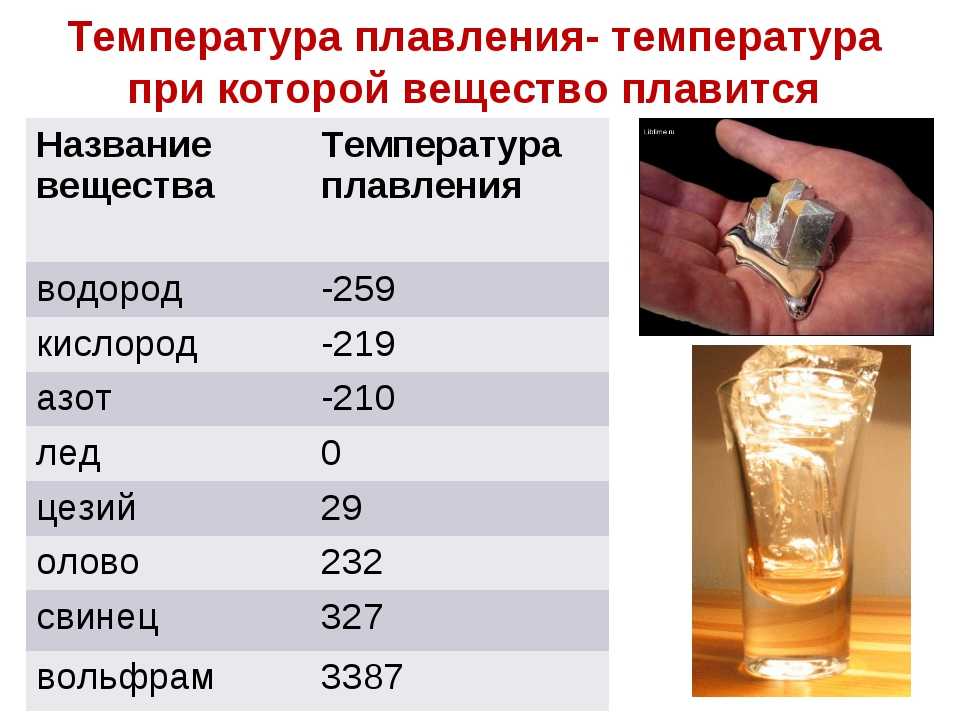 Молибден широко используется в электронных устройствах, таких как электронные лампы, транзисторы и выпрямители.
Молибден широко используется в электронных устройствах, таких как электронные лампы, транзисторы и выпрямители.
Металл с высокой температурой плавления – Top 5. Ниобий (Nb)
С температурой плавления 2468 °C , ниобий занимает 5-е место в нашем списке металлов с высокой температурой плавления.
Ниобий — редкий серебристо-серый, мягкий и ковкий металл с высокой температурой плавления . При комнатной температуре ниобий не реагирует с воздухом. Ниобий можно соединить с серой, азотом и углеродом непосредственно при высоких температурах. Ниобий не реагирует с неорганическими кислотами и основаниями, не растворяется в царской водке, но растворяется в плавиковой кислоте.
Ниобий
Содержание ниобия в земной коре составляет 20 ПП М, а распределение ресурсов ниобия относительно концентрированное.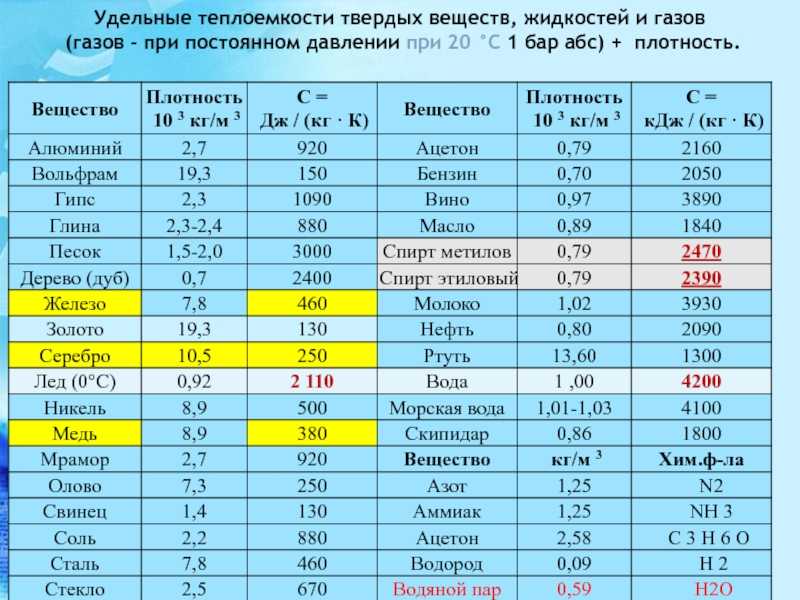 Благодаря хорошей сверхпроводимости, высокой температуре плавления, коррозионной стойкости и износостойкости ниобий широко используется в стали, сверхпроводящих материалах, аэрокосмической, атомной энергетике и других областях.
Благодаря хорошей сверхпроводимости, высокой температуре плавления, коррозионной стойкости и износостойкости ниобий широко используется в стали, сверхпроводящих материалах, аэрокосмической, атомной энергетике и других областях.
Металл с высокой температурой плавления — топ 6. Иридий (Ir)
Иридий занимает 9 место0025 6 место в нашем списке металлов с высокой температурой плавления . Его температура плавления составляет 2454 °C .
Иридий был открыт в 1803 году в нерастворимых примесях платины. Главный первооткрыватель, Смитсон Теннант, назвал его иридием в честь ириса из-за множества разноцветных солей.
Иридий
Иридий химически стабилен. Иридий – самый устойчивый к коррозии металл. Иридий химически устойчив к кислотам и нерастворим в них. Только губчатый иридий медленно растворяется в горячей царской водке.
Поскольку иридий очень устойчив к коррозии и высоким температурам, он очень подходит в качестве добавки к сплаву.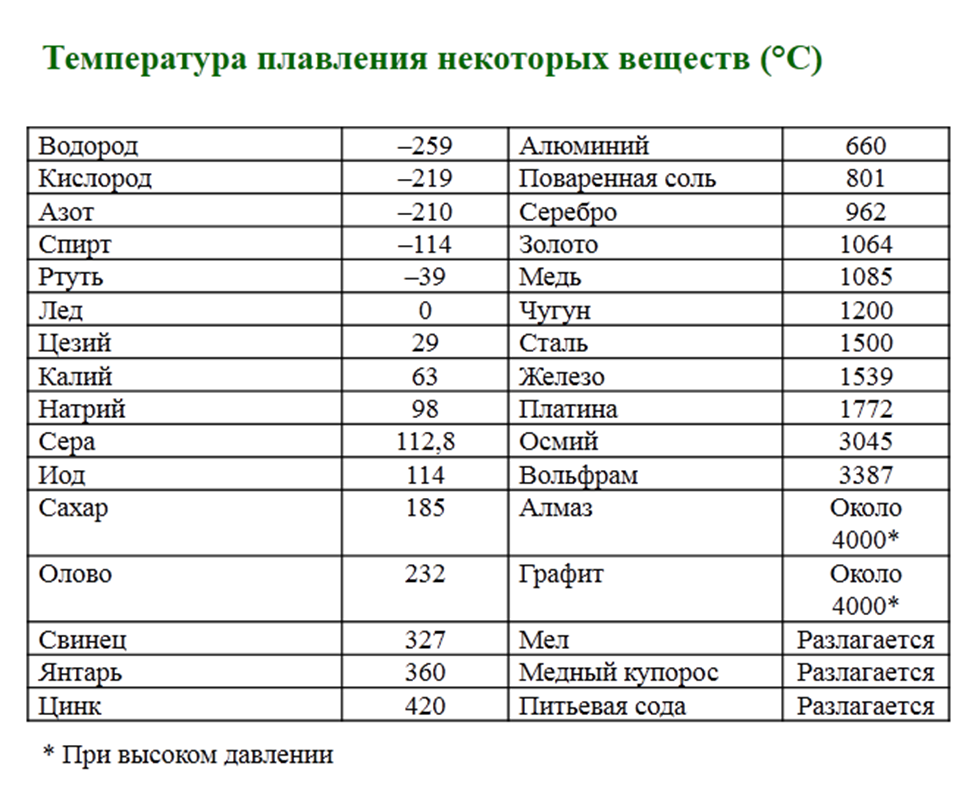 Некоторые из давно используемых деталей авиационных двигателей изготовлены из иридиевого сплава.
Некоторые из давно используемых деталей авиационных двигателей изготовлены из иридиевого сплава.
Металл с высокой температурой плавления — Top 7. Гафний (Hf)
Гафний — еще один металл с высокой температурой плавления, заслуживающий места в нашем списке. I имеет температуру плавления 2227 °C .
Гафний — блестящий серебристо-серый переходный металл. Гафний не взаимодействует с разбавленной соляной кислотой, разбавленной серной кислотой и сильным раствором щелочи, но может растворяться в плавиковой кислоте и царской водке.
Название элемента происходит от латинского названия города Копенгаген. В 1925 году шведский химик Эрвизи и голландский физик Костер получили чистую соль гафния, а затем восстановили ее металлическим натрием, чтобы получить чистый металлический гафний.
Гафний
Основным применением гафния является изготовление управляющих стержней для ядерных реакторов. Чистый гафний обладает пластичностью, простотой обработки, жаростойкостью и коррозионной стойкостью, что является важным материалом в атомной энергетике.
Чистый гафний обладает пластичностью, простотой обработки, жаростойкостью и коррозионной стойкостью, что является важным материалом в атомной энергетике.
Металл с высокой температурой плавления – Топ 8. Родий (Rh)
Родий занимает 8-е место в нашем списке металлов с высокой температурой плавления. Температура плавления этого тугоплавкого металла составляет 1960 °C .
Родий — серебристо-белый твердый металл с высокой отражательной способностью. Металлы родия обычно не образуют оксидов; расплавленный родий поглощает кислород, но при затвердевании кислород выделяется. Родий нерастворим в большинстве кислот, полностью нерастворим в азотной кислоте, мало растворим в царской водке.
Родий
Родий имеет высокую температуру плавления, высокую прочность, стабильные электротермические свойства, хорошую коррозионную стойкость, стойкость к высокотемпературному окислению и хорошую каталитическую активность. Поэтому родий широко используется в очистке выхлопных газов автомобилей, химической промышленности, аэрокосмической промышленности, производстве стекловолокна, электронной и электротехнической промышленности и других областях, известных как «промышленный витамин ».
Поэтому родий широко используется в очистке выхлопных газов автомобилей, химической промышленности, аэрокосмической промышленности, производстве стекловолокна, электронной и электротехнической промышленности и других областях, известных как «промышленный витамин ».
Металл с высокой температурой плавления – верхняя часть 9. Хром (Cr)
Хром занимает 8 место в нашем списке металлов с высокой температурой плавления. Это серебристо-белый блестящий металл с температурой плавления 1907 °C .
Чистый хром пластичен, тогда как содержащий примеси хром тверд и хрупок. Плотность хрома 7,20 г/см3 . Этот тугоплавкий металл не растворяется в воде, но растворяется в сильных щелочных растворах. Хром обладает высокой коррозионной стойкостью и очень медленно окисляется на воздухе даже при сильном нагревании. Следовательно, хромирование других металлов может защитить металл.
Хром
Содержание хрома в земной коре 0,01% , ранг 17 .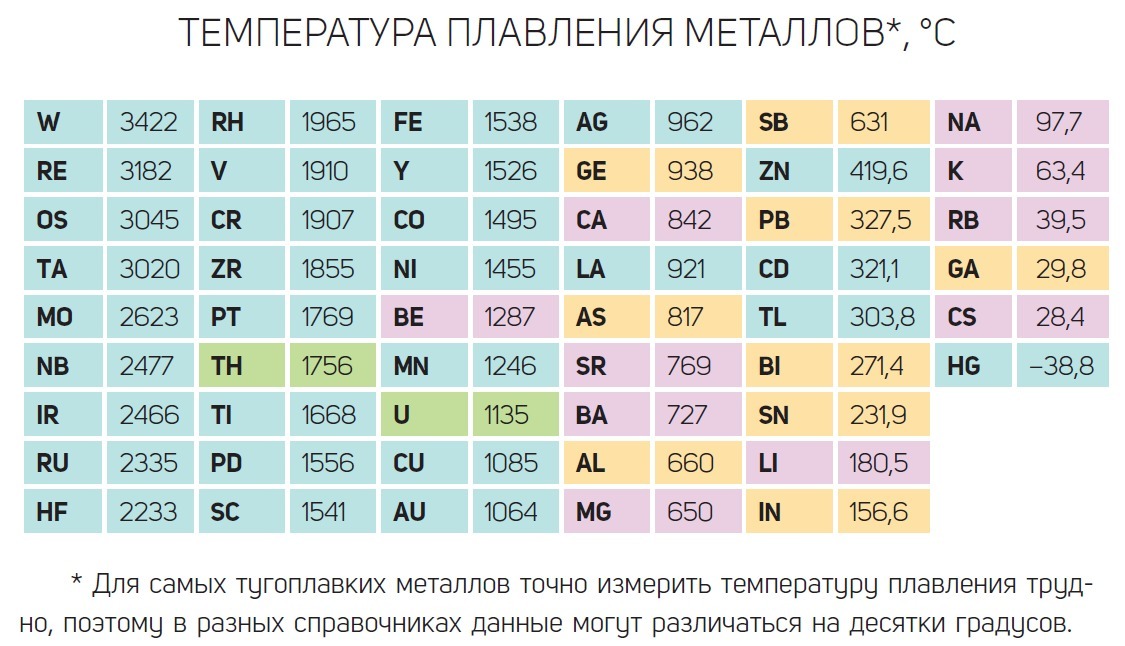 Свободного хрома в природе не существует, основной рудой, содержащей хром, является хромит. Хром широко используется в металлургии, химической промышленности, производстве чугуна, огнеупоров, высокоточной технологии и других областях.
Свободного хрома в природе не существует, основной рудой, содержащей хром, является хромит. Хром широко используется в металлургии, химической промышленности, производстве чугуна, огнеупоров, высокоточной технологии и других областях.
Металл с высокой температурой плавления — 10 лучших. Титан (Ti)
Наш список не полон без титана . Этот тугоплавкий металл имеет высокую температуру плавления 1668 °С . Титан представляет собой серебристо-белый переходный металл, характеризующийся легким весом, высокой прочностью, металлическим блеском и устойчивостью к коррозии влажным хлором.
Однако титан нельзя использовать в сухом газообразном хлоре. Даже если температура ниже 0 ℃ в сухом газообразном хлоре, произойдет бурная химическая реакция с образованием тетрахлорида титана, а затем разложение с образованием дихлорида титана или даже возгорание. Только при содержании воды в газообразном хлоре выше 0,5% можно титана быть надежно стабильным в нем.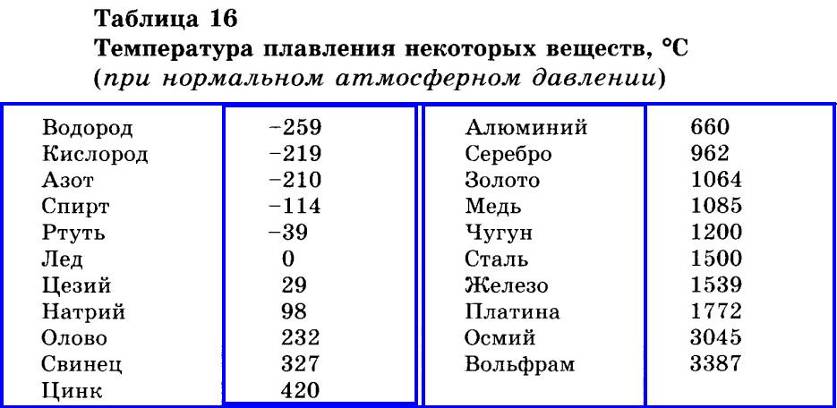
Титан
Титан можно сплавлять с другими элементами, такими как железо, алюминий, ванадий или молибден, для образования высокопрочных легких сплавов. Он имеет широкий спектр применений, включая аэрокосмическую, военную, автомобильную, сельскохозяйственную продукцию, медицину, кухонную утварь, спортивные товары, ювелирные изделия и мобильные телефоны.
Заключение
Спасибо, что прочитали наш список металлов с высокой температурой плавления , и мы надеемся, что он может быть вам полезен. Если вы хотите узнать больше о металле с высокой температурой плавления , вы можете посетить Advanced Refractory Metals для получения дополнительной информации. мы поставляем высококачественные тугоплавкие металлы для удовлетворения потребностей наших клиентов в исследованиях, разработках и производстве.
Похожие посты:
Распространенное использование молибденовых пластин
10 Важные применения индия
Преимущества и недостатки морских противовесов из вольфрамового сплава
Физические и химические свойства вольфрама
точка плавления — Что заставляет некоторые металлы плавиться при более высокой температуре?
Спросил
Изменено
2 года, 9 месяцев назад
Просмотрено
56 тысяч раз
$\begingroup$
Я смотрю на температуру плавления металлических элементов и замечаю, что все металлы с высокой температурой плавления сгруппированы в левом нижнем углу блока $\mathrm{d}$.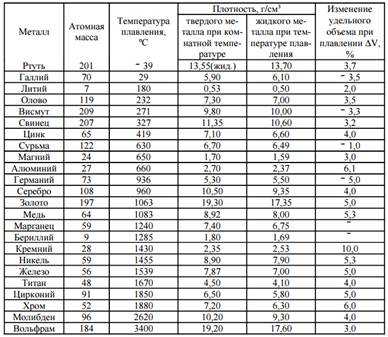 Если я возьму, например, периодическую таблицу с физическим состоянием, указанным в $\pu{2165 K}$:
Если я возьму, например, периодическую таблицу с физическим состоянием, указанным в $\pu{2165 K}$:
Я вижу, что (кроме бора и углерода) единственные элементы, остающиеся твердыми при этой температуре, образуют довольно четкий блок вокруг вольфрама (который плавится при $\pu{3695 K}$). Так что же заставляет эту группу металлов плавиться при такой высокой температуре?
- температура плавления
- металл
$\endgroup$
5
$\begingroup$
На некоторые факторы намекнули, но позвольте мне расположить их в порядке важности и упомянуть еще некоторые:
металлы обычно имеют высокую температуру плавления, потому что металлическая межатомная связь делокализованными электронами ($\ce{Li}$ имеет лишь несколько электронов для этого «электронного моря») между атомами ядра довольно эффективна в этих чистых твердые тела элементов по сравнению с альтернативными типами связи (ионная энергия связи $\pu{6-20 эВ/атом}$, ковалентная 1-7, металлическая 1-5, ван-дер-ваальсова значительно ниже).
 Также ионные решетки типа $\ce{NaCl}$ имеют более высокую решетку и энергию связи, у них слабая межатомная дальнодействующая связь, в отличие от большинства металлов. Они распадаются или легко растворяются, металлы податливы, но не ломаются, море электронов является причиной их способности к сварке.
Также ионные решетки типа $\ce{NaCl}$ имеют более высокую решетку и энергию связи, у них слабая межатомная дальнодействующая связь, в отличие от большинства металлов. Они распадаются или легко растворяются, металлы податливы, но не ломаются, море электронов является причиной их способности к сварке.кристаллическая структура и масса играют второстепенную роль среди отфильтрованных элементов (просто посмотрите кристаллическую структуру этих элементов), поскольку металлическая связь не является направленной, в отличие от ковалентной связи (орбитальная симметрия). Металлы часто имеют наполовину заполненные зоны $\mathrm{s}$ и $\mathrm{p}$ (более сильно делокализованные, чем $\mathrm{d}$ и $\mathrm{f}$) на краю Ферми (что означает высокую проводимость). ) и, следовательно, много делокализованных электронов, которые могут переходить в незанятые энергетические состояния, образуя самое большое электронное море с половиной или менее заполненных зон.
благородных металлов, таких как $\ce{Au,Ag}$, имеют полную $\mathrm{d}$-орбиталь, поэтому имеют низкую реакционную способность/электроотрицательность и часто используются в качестве контактных материалов (высокая проводимость из-за «очень жидкого» электронного моря, состоящего из только из $\mathrm{s}$-орбитальных электронов.
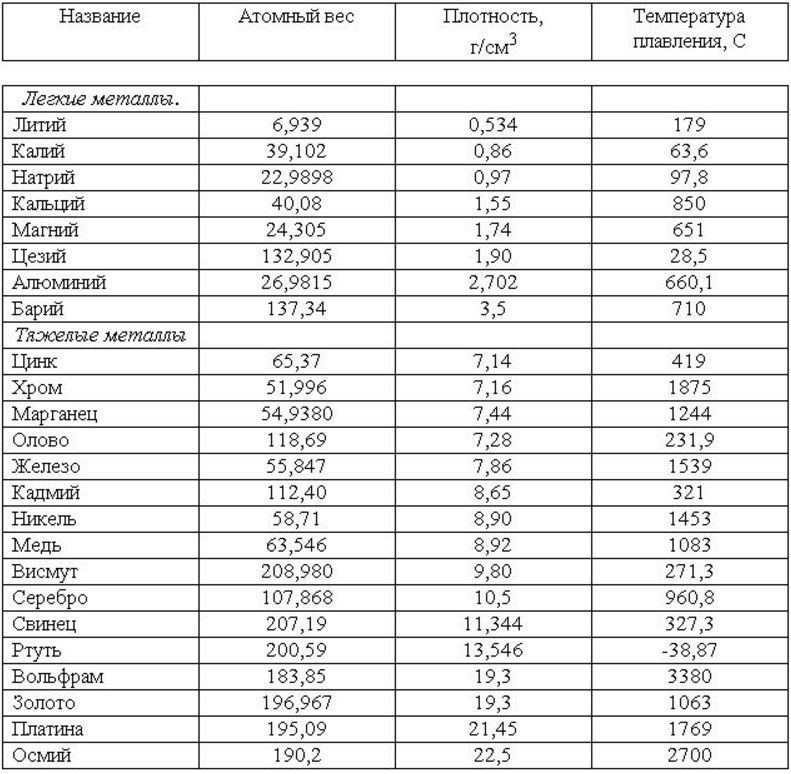 В отличие от вольфрама с половиной или менее занятыми $\mathrm{d}$-орбиталями они не обнаруживают межатомных $\mathrm{d-d}$-связей за счет делокализованных $\mathrm{d}$ -электронов, и что более важно, наполовину заполненная $\mathrm{d}$-орбиталь вносит в энергетическую зону 5 электронов, тогда как $\mathrm{s}$ только 1, $\mathrm{p}$ только 3, электронное море больше среди $\mathrm{d}$-группы.
В отличие от вольфрама с половиной или менее занятыми $\mathrm{d}$-орбиталями они не обнаруживают межатомных $\mathrm{d-d}$-связей за счет делокализованных $\mathrm{d}$ -электронов, и что более важно, наполовину заполненная $\mathrm{d}$-орбиталь вносит в энергетическую зону 5 электронов, тогда как $\mathrm{s}$ только 1, $\mathrm{p}$ только 3, электронное море больше среди $\mathrm{d}$-группы.«упаковка» атомов ядра в решетке (межатомное расстояние) среди высоких атомов $Z$ (по сравнению с , например, $\ce{Li}$) более плотная (больше протонов, сильнее притяжение электронов оболочки , меньший межатомный радиус), означает более сильную межатомную связь, передаваемую электронным морем:
Здесь видно, что в каждой серии ($\ce{Li,\ Na,\ K}$) температуры плавления увеличиваются до максимума, а затем уменьшаются с увеличением атомного номера (отсутствуют незанятые энергетические состояния для делокализованных $\ mathrm{d}$-электронов), большее электронное море здесь является более сильным фактором, чем чуть более плотная упаковка.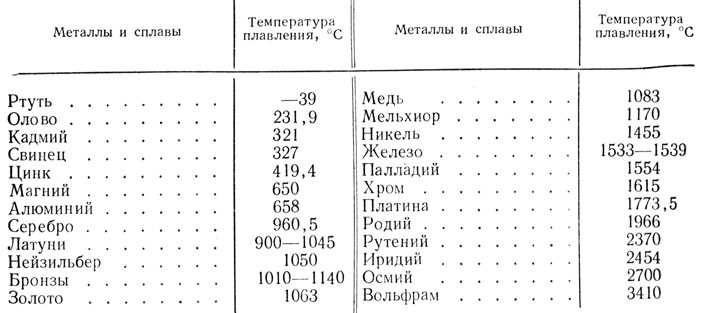
- Бор как полуметалл проявляет металлическую и ковалентную связь, углерод имеет сильную направленную ковалентную связь и способен образовывать сеть связей, в отличие от других неметаллических элементов, проявляющих ковалентную внутримолекулярную связь, e.g. , в двухатомных молекулах, но не в сильной межмолекулярной связи в макромолекулах из-за отсутствия неспаренных электронов.
Таким образом, существуют более серьезные тенденции для температур плавления, объясняющие высокие температуры плавления $\mathrm{d}$-металлов, а также некоторые незначительные исключения из этого правила, такие как $\ce{Mn}$.
$\endgroup$
1
$\begingroup$
Думаю, здесь играют роль два свойства: скорость атомов и стабильность структуры решетки.
Напомним, что температура является мерой средней кинетической энергии молекул, поэтому $v \propto \sqrt{\frac{T}{m}}$, или для достижения той же скорости $T \propto m$.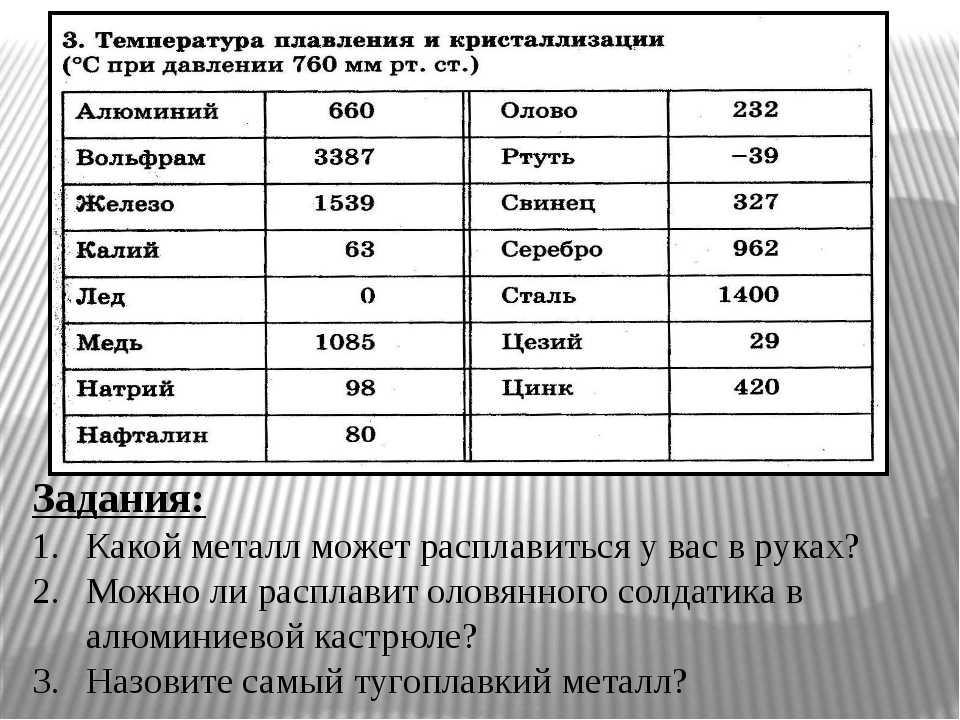 Таким образом, при одинаковой температуре два более тяжелых атома будут двигаться друг относительно друга медленнее, чем две более легкие молекулы, что дает им больше времени для взаимодействия.
Таким образом, при одинаковой температуре два более тяжелых атома будут двигаться друг относительно друга медленнее, чем две более легкие молекулы, что дает им больше времени для взаимодействия.
Теперь вспомним, что в твердом теле молекулы удерживаются в решетке межмолекулярными силами, а в жидкости атомы обладают достаточной энергией, чтобы силы между ними уже не были достаточно сильны, чтобы удерживать атомы в решетке. Таким образом, чем большую стабильность приобретают атомы вещества, находясь в твердом, кристаллическом расположении, тем выше будет его температура плавления. Теперь, почему металлы в этой области приобретают большую стабильность в своей твердой форме? Я совершенно уверен, что ответ связан с полнотой орбиталей и полуорбиталей. Я не уверен в деталях делокализованного электронного облака в металлах, но я думаю, вполне вероятно, что оно позволяет этим металлам каким-то образом заполнять или освобождать свои неполные орбитали.
$\endgroup$
2
Твой ответ
Зарегистрируйтесь или войдите в систему
Зарегистрируйтесь с помощью Google
Зарегистрироваться через Facebook
Зарегистрируйтесь, используя адрес электронной почты и пароль
Опубликовать как гость
Электронная почта
Требуется, но не отображается
Опубликовать как гость
Электронная почта
Требуется, но не отображается
Нажимая «Опубликовать свой ответ», вы соглашаетесь с нашими условиями обслуживания, политикой конфиденциальности и политикой использования файлов cookie
.
Belmont Легкоплавкие эвтектические и неэвтектические сплавы (плавкие сплавы)
Belmont Легкоплавкие эвтектические и неэвтектические сплавы (плавкие сплавы)
Содержит сплавы с радиационной защитой 158°F, 203°F, сплавы для гибки труб и низкотемпературные припои. Эвтектика: температура плавления от 117° до 281°F. Неэвтектика: температура плавления от 107° до 338°F. Металл меллотта, роза, металл Вуда и другие. Проволока из легкоплавкого сплава.
Легкоплавкие или легкоплавкие сплавы (также известные как эвтектические и неэвтектические сплавы) обычно представляют собой сплавы, плавящиеся при температуре ниже 450 град. F. (233 град. С). Наиболее полезными являются сплавы, содержащие высокие проценты висмута в сочетании со свинцом, оловом, кадмием, индием и другими металлами. Низкая температура плавления и уникальные характеристики роста/усадки этих сплавов приводят к большему разнообразию полезных применений, чем почти любая другая система сплавов.
Области применения:
От применения для защиты от радиационной терапии до создания патронов для удерживания деталей во время механической обработки, от использования в качестве наполнителя при гибке труб или труб до создания плавких элементов в автоматических пожарных спринклерах. тихое, но глубокое влияние на нашу жизнь.
Формы:
Торт, слиток, брусок, дробь, проволока, палка, полоса и нестандартные формы
Подробнее
Показаны все 21 результат
Сортировка по умолчаниюСортировать по популярностиСортировать по последнимПо алфавиту A..ZПо алфавиту Z..A
1 (833) 4-СПЛАВЫ Отправить запрос предложенийОтправить запрос предложенийКупить сейчас
1 (833) 4-СПЛАВЫ Отправить запрос предложенийОтправить запрос предложенийКупить сейчас
1 (833) 4-СПЛАВЫ Отправить запрос предложенийОтправить запрос предложенийКупить сейчас
1 (833) 4-СПЛАВЫ Отправить запрос предложенийОтправить запрос предложенийКупить сейчас
1 (833) 4-СПЛАВЫ Отправить запрос предложенийОтправить запрос предложенийКупить сейчас
1 (833) 4-СПЛАВЫ Отправить запрос предложенийОтправить запрос предложенийКупить сейчас
1 (833) 4-СПЛАВЫ Отправить запрос предложенийОтправить запрос предложенийКупить сейчас
1 (833) 4-СПЛАВЫ Отправить запрос предложенияОтправить запрос предложения
1 (833) 4-СПЛАВЫ Отправить запрос предложенияОтправить запрос предложения
1 (833) 4-СПЛАВЫ Отправить запрос предложенийОтправить запрос цен
1 (833) 4-СПЛАВЫ Отправить запрос предложенияОтправить запрос предложения
1 (833) 4-СПЛАВЫ Отправить запрос предложенияОтправить запрос предложения
СВЯЗАННЫЕ СООБЩЕНИЯ
Преимущества эвтектических сплавов по сравнению с неэвтектическими сплавами для легкоплавких материалов
Эвтектические сплавы и неэвтектические сплавы являются категориями при обсуждении легкоплавких сплавов. Легкоплавкие сплавы требуют более низких температур для плавления, от 40 до 300 градусов по Фаренгейту. Это свойство позволяет плавить сплавы при более низких температурах, не повреждая и не воздействуя на другие близлежащие материалы или поверхности, которые легкоплавкий сплав…
Легкоплавкие сплавы требуют более низких температур для плавления, от 40 до 300 градусов по Фаренгейту. Это свойство позволяет плавить сплавы при более низких температурах, не повреждая и не воздействуя на другие близлежащие материалы или поверхности, которые легкоплавкий сплав…
Читать далее
Применение индийсодержащих легкоплавких сплавов
Легкоплавкие сплавы обычно используются в производственном процессе для облегчения создания изделий или помещаются внутрь изделий для выполнения определенных функций. Эти сплавы плавятся и текут при очень низких температурах в зависимости от состава основных металлов и металлов-присадок. Обычный низкоплавкий недрагоценный металл может состоять из висмута с более высокой…
Читать далее
Различные свойства легкоплавких сплавов
Соединение металлических деталей припоем, легкое сгибание труб для обхода углов и компонентов, а также системы блокировки линз — все это основано на использовании легкоплавких сплавов.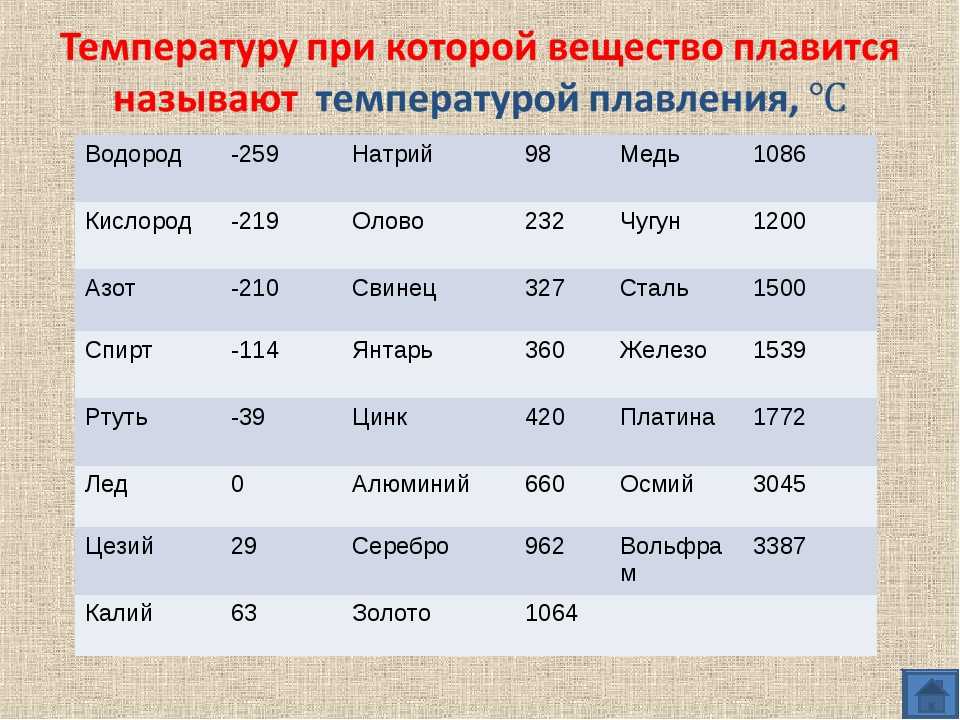 Этот тип металла позволяет изготавливать и отливать изделия, детали и узлы при более низких температурах. Эта функция идеальна, когда требуются более низкие температуры для…
Этот тип металла позволяет изготавливать и отливать изделия, детали и узлы при более низких температурах. Эта функция идеальна, когда требуются более низкие температуры для…
Читать далее
Легкоплавкие сплавы на основе висмута в интересах художественного литья
На протяжении всей истории художественное литье использовалось для создания прекрасных произведений искусства, для воссоздания предыдущих произведений искусства, которые могли быть повреждены или испортились из-за возраста, или при массовом производстве произведений искусства. Метод художественного литья предполагает использование форм из дерева, камня, гипса или силиконовой резины и какого-либо гибкого материала, например…
Читать далее
Легкоплавкие сплавы, содержащие индий: характеристики и применение
Часто, думая о металлических сплавах, мы учитываем прочность и долговечность металла, чтобы выдерживать ряд нагрузок, напряжений и экстремальных температур. Тем не менее, существует ряд производственных применений, где сплав должен иметь низкую плавкость. Легкоплавкий сплав, также называемый легкоплавким, может принимать жидкий или…
Тем не менее, существует ряд производственных применений, где сплав должен иметь низкую плавкость. Легкоплавкий сплав, также называемый легкоплавким, может принимать жидкий или…
Читать далее
Приложения, использующие легкоплавкие сплавы
Легкоплавкие сплавы считаются легкоплавкими, так как плавятся при температуре ниже 300 градусов, часто комбинируются с другими металлами с целью повышения тех или иных свойств. Например, висмут часто комбинируют с оловом и/или серебром для создания нетоксичных бессвинцовых припоев. Применение и использование низкоплавких сплавов Легкоплавкие сплавы могут быть…
Читать далее
Характеристики легкоплавких сплавов
Производители по всему миру полагаются на качественные материалы для создания целого ряда деталей, оборудования и продуктов для предприятий и потребителей. В процессе сборки различные материалы могут быть соединены вместе для обеспечения герметичности, отлиты в форме до заданной формы или согнуты в новом направлении без разрушения. Легкоплавкий…
В процессе сборки различные материалы могут быть соединены вместе для обеспечения герметичности, отлиты в форме до заданной формы или согнуты в новом направлении без разрушения. Легкоплавкий…
Читать далее
Низкая температура плавления жидкого металла
Низкая температура плавления легкоплавких сплавов позволяет использовать их в самых разных областях. Температура плавления алюминия составляет 1220 градусов по Фаренгейту. Углеродистая сталь плавится где-то между 2600 и 2800 градусов по Фаренгейту, и температура должна подняться до 6150 градусов по Фаренгейту, чтобы расплавить вольфрам. Специализированные печи необходимы для…
Читать далее
Основы висмута
Этот белый элемент является неотъемлемой частью многих сплавов Пурпурно-серебряный, кристаллический висмут использовался с первых дней сплавов, хотя в то время его часто ошибочно принимали за свинец.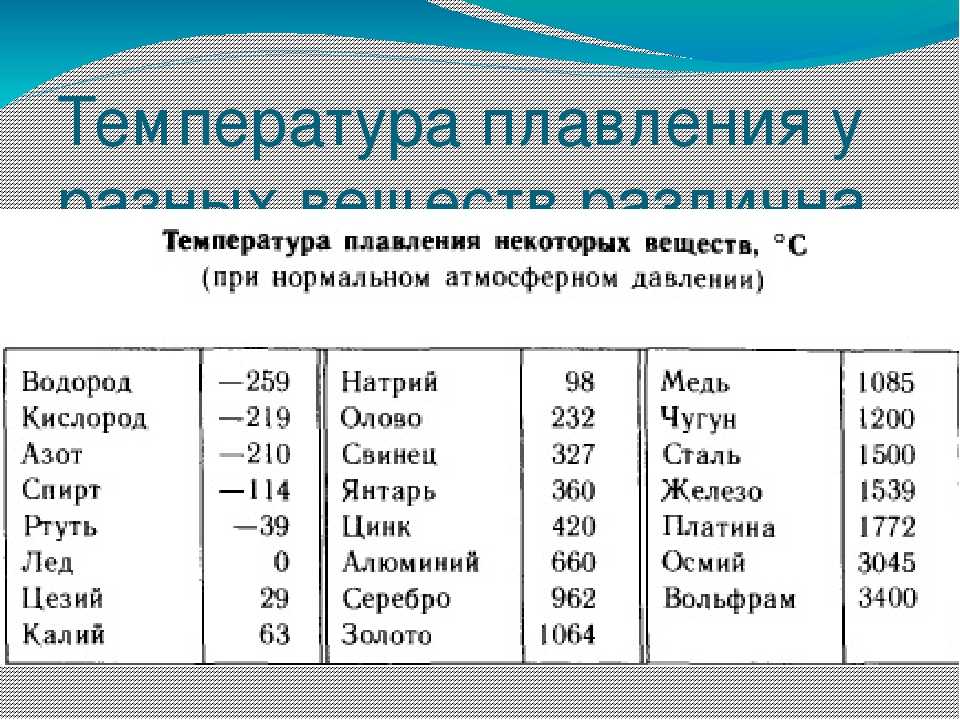 Это самый естественный диамагнитный элемент, что означает, что он отталкивает и север, и юг, и у него одно из самых низких значений…
Это самый естественный диамагнитный элемент, что означает, что он отталкивает и север, и юг, и у него одно из самых низких значений…
Читать далее
Свяжитесь с нами
Металл, плавящийся в горячей воде
Пока я держу серебристую металлическую проволоку в дымящейся горячей воде, капли жидкого металла формируются и падают в блестящую лужу на дне стакана.
То, что было толстой сплошной проволокой, теперь превратилось в лужу расплавленного металла. Никаких паяльников, пламени или факелов, только чашка с горячей водой.
Поскольку жидкий металл имеет температуру всего 144° по Фаренгейту (62° по Цельсию), мы можем залить его в пластиковые формы, предназначенные для изготовления свечей или мыла.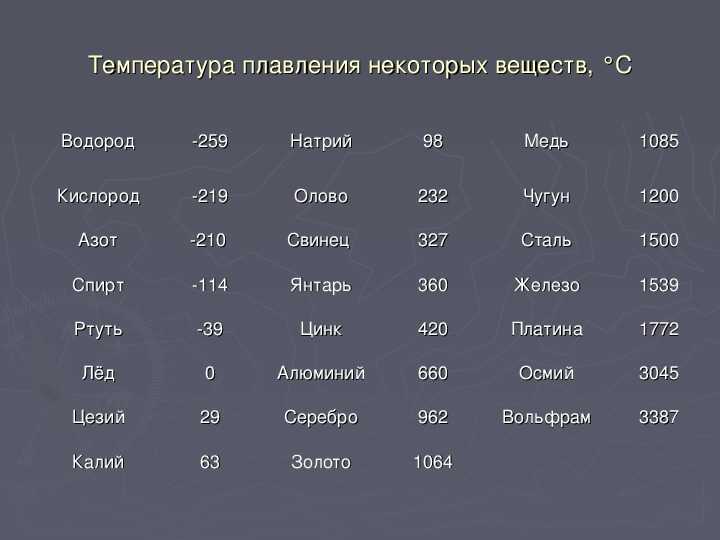
На картинке ниже около фута провода находится рядом с линейкой. Провод поставляется в толстой виниловой трубке, поэтому на картинке он выглядит больше, чем его реальная толщина 1/8 дюйма. Несколько дюймов были расплавлены и вылиты в пластиковую форму. Белая скрепка с пластиковым покрытием была вставлена в форму до того, как металл затвердел, просто для развлечения.
Металл очень хорошо подходит для заполнения всех закоулков и углов в форме, что позволяет точно воспроизводить такие мелкие предметы, как отпечатки пальцев. Ниже приведены некоторые изделия, которые мы отливали из металла, используя только горячую воду.
Что это за штука?
Металл представляет собой смесь висмута, олова и индия. Мы называем его Field’s Metal .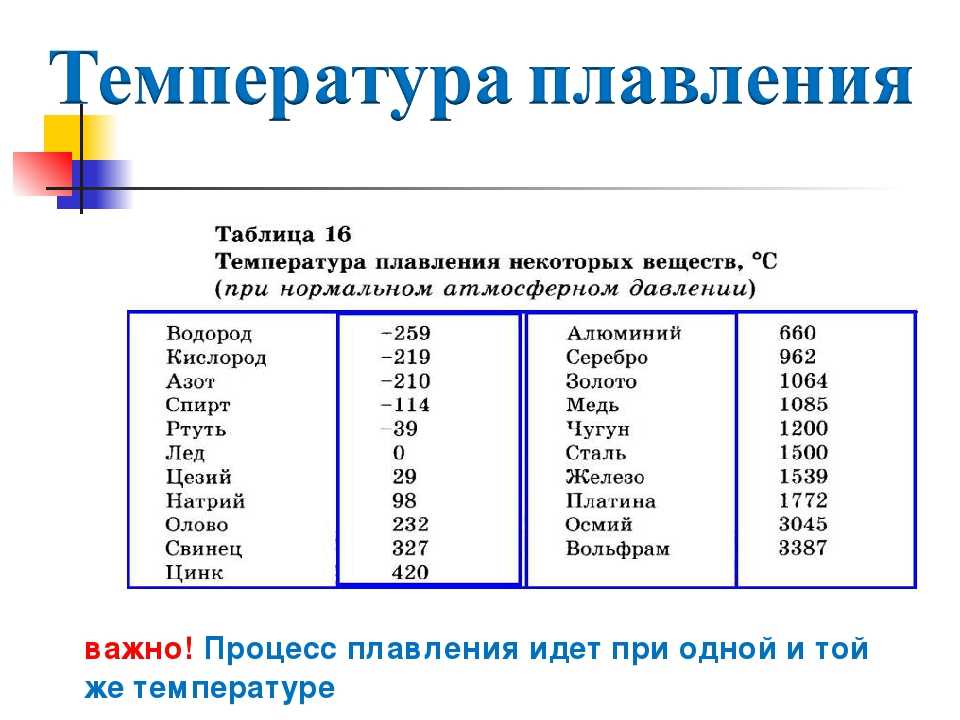 Индий — это металл, внешне похожий на серебро, но примерно в два раза дороже. Он имеет особое применение в научной аппаратуре благодаря своим интересным свойствам, таким как способность прилипать к стеклу. Это позволяет вам «припаивать» вещи прямо к стеклу и делать хорошее уплотнение металла к стеклу для работы с вакуумом.
Индий — это металл, внешне похожий на серебро, но примерно в два раза дороже. Он имеет особое применение в научной аппаратуре благодаря своим интересным свойствам, таким как способность прилипать к стеклу. Это позволяет вам «припаивать» вещи прямо к стеклу и делать хорошее уплотнение металла к стеклу для работы с вакуумом.
Есть много сплавов, которые плавятся при низких температурах. Они называются легкоплавкими сплавами . Возможно, вы слышали об известном экземпляре под названием Wood’s Metal . Металл Вуда представляет собой смесь 50% висмута, 25% свинца, 12,5% олова и 12,5% кадмия. Он плавится при температуре 158° по Фаренгейту (70° по Цельсию).
Кадмий и свинец являются токсичными металлами. Благодаря использованию нетоксичных металлов, таких как индий, олово и висмут, металл Филда можно безопасно использовать в качестве игрушки. Он плавится и при более низкой температуре.
Индий не является бытовым материалом, и его трудно найти. Коммерческие поставщики обычно имеют минимальные заказы в диапазоне десяти фунтов или более, в результате чего минимальная стоимость достигает нескольких сотен долларов.
По этой причине мы изготовили партию металла Филда, отлили из него провода и сделали его доступным для экспериментаторов в нашем каталоге в доступных количествах.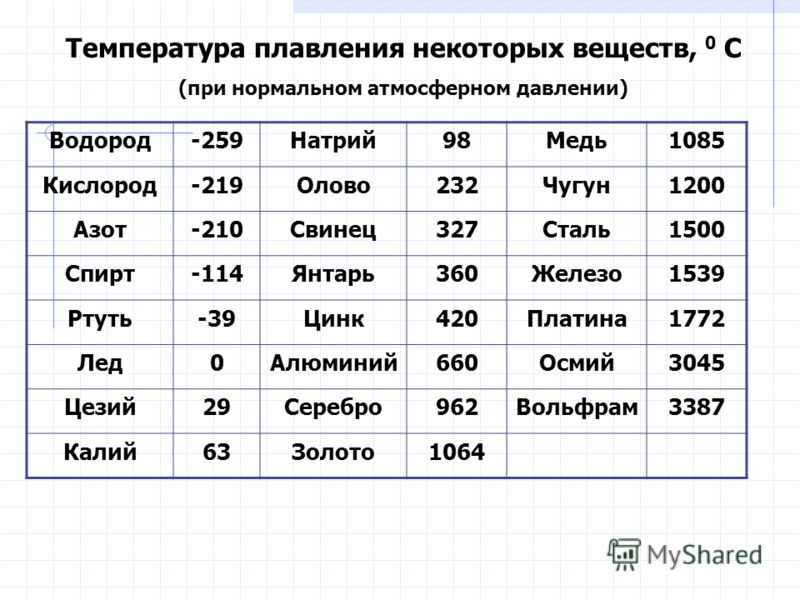
Легкоплавкие сплавы используются в некоторых довольно распространенных изделиях. Они используются в спринклерных системах пожаротушения в офисных зданиях, где металл плавится, если температура становится слишком высокой, и позволяет воде разбрызгиваться. Они также используются во всплывающих таймерах в индюках. Кусок твердого металла удерживает пластиковый флажок на пружине. Когда температура подходящая, металл плавится, и пружина выдвигает флаг на обозрение.
Как это сделать?
Температура плавления сплава часто сильно отличается от температуры плавления чистых металлов, из которых он изготовлен.
Висмут плавится при 519,8° F (271,3° C).
Олово плавится при 447,8° F (231,8° C).
Свинец плавится при температуре 620,6° F (327,5° C).
Индий плавится при 312,8° F (156,6° C).
Чистые вещества имеют высокую температуру плавления. Чистое вещество – это либо элемент, либо химическое соединение. Смеси плавятся в диапазоне температур.
Эвтектический сплав имеет высокую температуру плавления. Это означает, что это химическое соединение, в котором элементы связаны друг с другом в строгих пропорциях, а не простая смесь элементов.
В смеси элементов некоторые из них будут реагировать вместе, образуя соединения.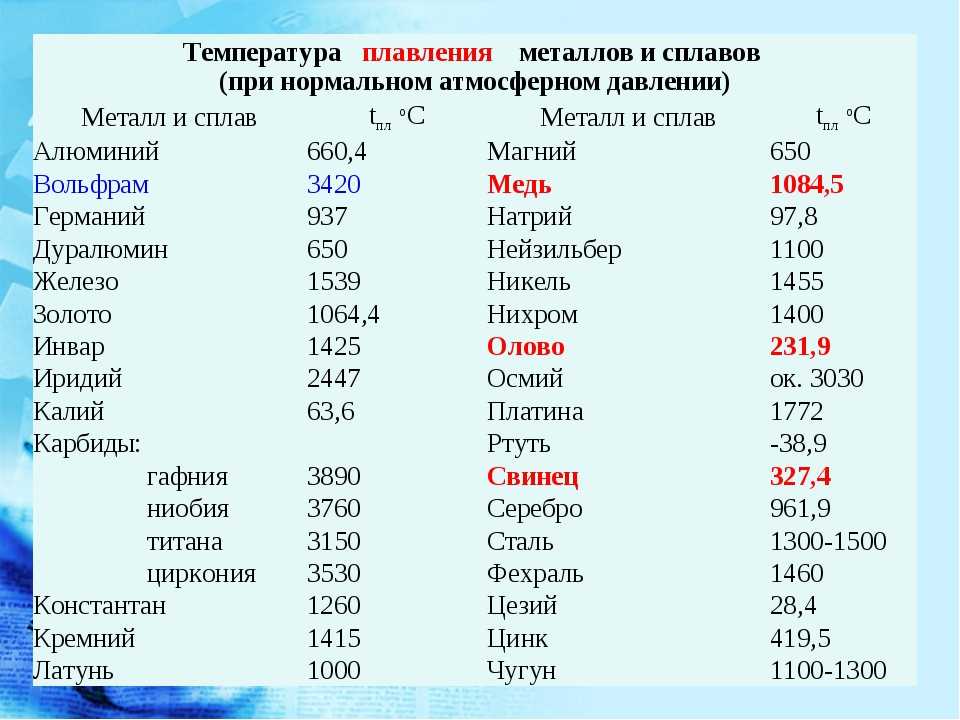 Соединения состоят из точных пропорций одного атома к другому, таких как один к одному, два к одному, три к двум и т. д. Любой избыток одного элемента над другим не будет реагировать и останется в смеси как чистый элемент.
Соединения состоят из точных пропорций одного атома к другому, таких как один к одному, два к одному, три к двум и т. д. Любой избыток одного элемента над другим не будет реагировать и останется в смеси как чистый элемент.
Поэтому смеси имеют более широкую температуру плавления. Один химикат плавится при одной температуре, а другой плавится при более высокой температуре. Только когда все они растают, вы получите настоящую жидкость.
Что заставляет вещество плавиться при данной температуре, так это то, насколько сильно молекулы материала связываются друг с другом. Иногда два элемента объединяются, образуя соединение, которое прочно связывается между собой. Это повысит температуру плавления. В других случаях образовавшееся соединение не связывается с собой так легко, как это делают чистые элементы. Это соединение будет иметь более низкую температуру плавления, чем любой из чистых элементов. Соединения не ограничиваются двумя элементами. Иногда многие элементы объединяются в одно соединение.
Это соединение будет иметь более низкую температуру плавления, чем любой из чистых элементов. Соединения не ограничиваются двумя элементами. Иногда многие элементы объединяются в одно соединение.
В электронике одним из предпочтительных припоев является эвтектическая смесь свинца и олова. По весу там всего около 63% олова и 37% свинца. Он плавится при температуре 361° по Фаренгейту (183° по Цельсию).
Атомный вес свинца 207,2.
Атомный вес олова 118,71.
Если бы на каждые три атома олова приходился один атом свинца, соотношение было бы:
207,2
------------------ = 36,78% свинца
207,2 + 3 х 118,71
а также
3 х 118,71
------------------ = 63,22% олова
207,2 + 3 х 118,71
Таким образом, химическая формула соединения PbSn 3 .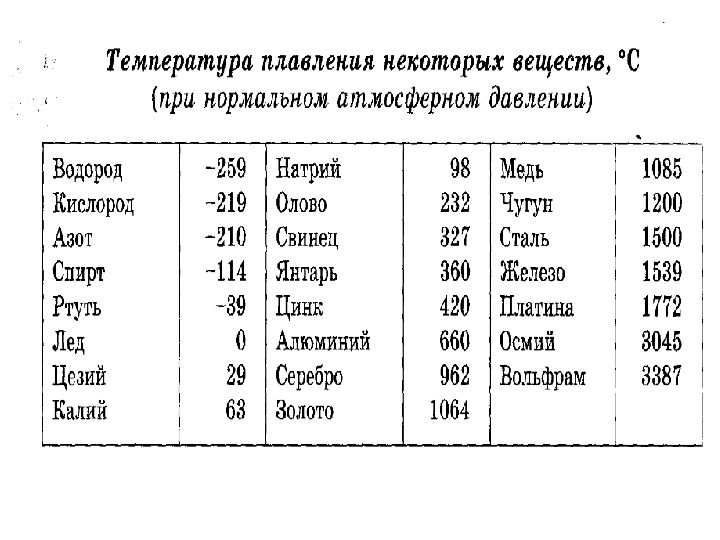
Другой эвтектический сплав представляет собой смесь свинца и сурьмы. На каждый атом сурьмы приходится четыре атома свинца. Точки плавления:
Свинец (Pb): 327° Цельсия
Сурьма (Sb): 630° Цельсия
Сплав (SbPb 4 ): 246° Цельсия
В эвтектическом сплаве магния и свинца есть два атома магния на каждый атом свинца:
Свинец (Pb): 327° Цельсия
Магний (Mg): 651° Цельсия
Сплав (PbMg 2 ): 530° Цельсия
Сделайте свой собственный легкоплавкий сплав
Легкоплавкий сплав можно сделать из висмута, свинца и олова.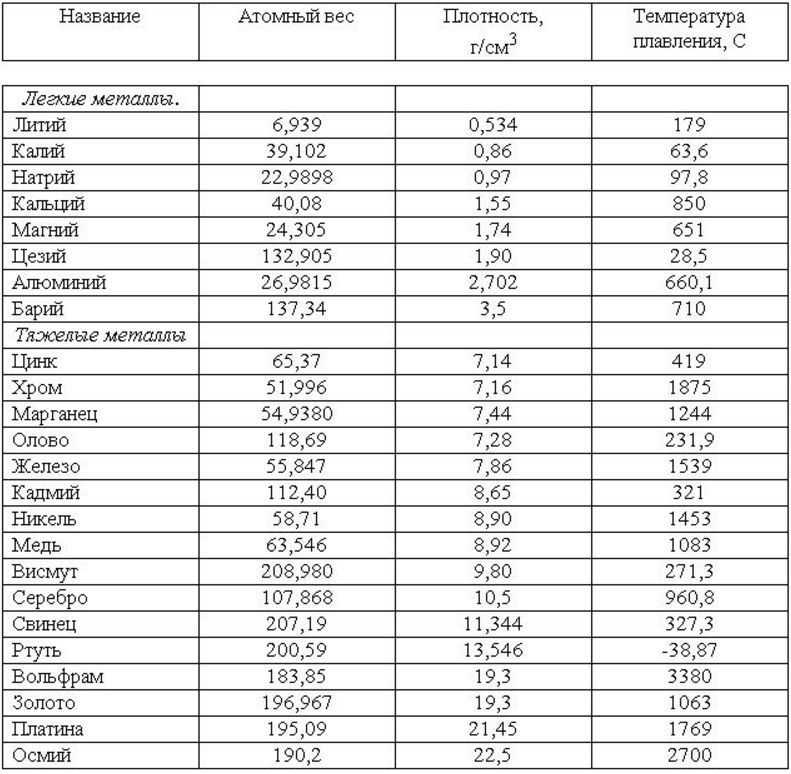
Свинец токсичен, поэтому с этим сплавом следует обращаться осторожно, его нельзя использовать рядом с едой и нельзя рассматривать как игрушку. Вместо этого для игрушек используйте Металл Филда.
Висмут можно найти в магазинах спортивных товаров в виде дроби для использования в ружьях. Предпочтительнее использовать свинцовую дробь, потому что она не токсична и не загрязняет воду, в которую стреляют охотники на уток.
Поскольку некоторым из наших читателей было трудно найти висмут (особенно за пределами США), мы поставляем его в нашем каталоге.
Свинец и олово нетрудно найти по отдельности, но особенно легко их найти вместе в виде припоя.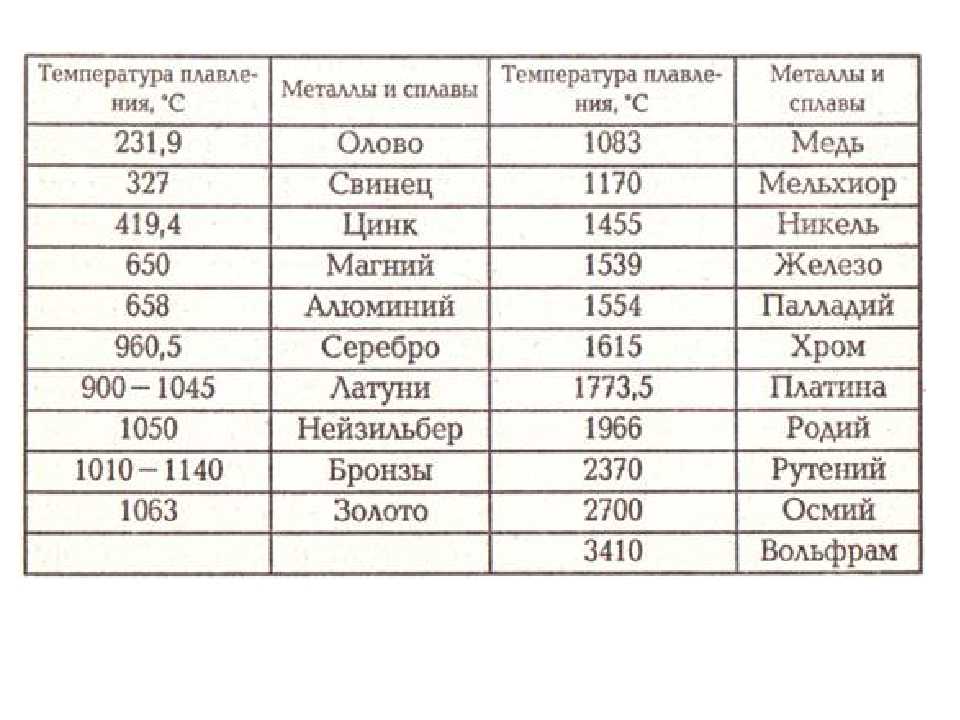
Для наших целей мы будем использовать немного менее распространенную форму припоя. Припой обычно производится в эвтектических пропорциях или в почти эвтектической форме 60% олова, 40% свинца. Но некоторые припои доступны в противоположном соотношении — 60% свинца и 40% олова. Это форма, которая нам нужна (если вы не можете получить свинец и олово по отдельности).
Эвтектическая форма сплава висмут-свинец-олово содержит 52,53% висмута, 32,55% свинца и 14,92% олова по весу. Соединение представляет собой Bi 8 Pb 5 Sn 4 .
Если у вас есть отдельные металлы, вы можете взвесить их и расплавить вместе, и вы получите сплав, который плавится при 203° по Фаренгейту (95° по Цельсию).
Если у вас есть оловянно-свинцовый припой 40/60, вы можете взвесить равные части припоя и висмута и расплавить их вместе. Это дает вам смесь, которая не является эвтектической, поэтому температура плавления находится в диапазоне от 203 ° F (9от 5°C) до 219°F (103,8°C). Это все еще будет таять в почти кипящей воде.
Металлы с высокой температурой плавления
Что такое температура плавления?
Температура плавления вещества – это температура, при которой оно переходит из твердого состояния в жидкое.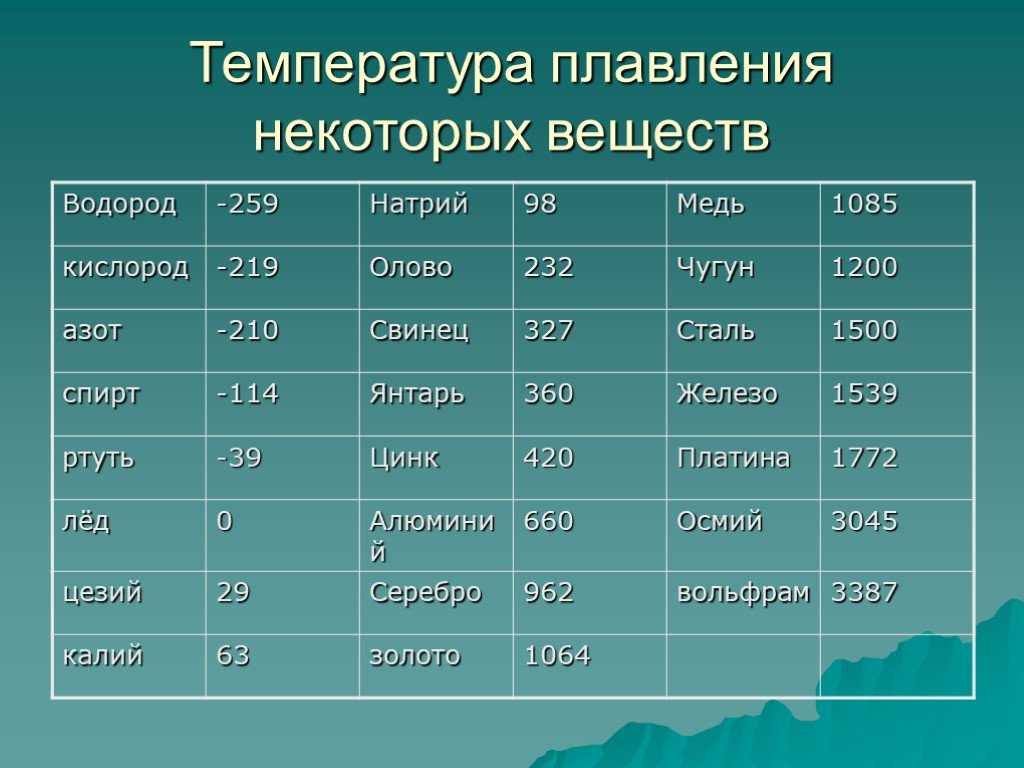
Металлы имеют высокую температуру плавления, поскольку они существуют в кристаллической твердой форме. Металлы с высокой температурой плавления имеют сильные межмолекулярные силы между атомами.
Силы электростатического притяжения между ионами металлов и свободными электронами создают прочные металлические связи, причем более прочные связи приводят к более высоким температурам плавления.
Температура плавления тугоплавких металлов
Существует два общепринятых определения тугоплавких металлов.
- Тугоплавкий металл – это металл с температурой плавления выше 2200 °С.
- Все металлы с температурой плавления выше 1850 °C считаются тугоплавкими металлами.
Используя более широкое определение, следующие 14 металлов классифицируются как тугоплавкие металлы.
Металл | Точка плавления | Приложения |
Вольфрам (Вт) | 3420 °С | Нити накала лампочек, сварочные электроды, нагревательные элементы печей |
Рений (Re) | 3180 °С | Детали реактивных двигателей, легирование, нити накаливания, рентгеновские аппараты |
Тантал (Та) | 2966 °С | Лопасти турбин двигателей, медицинские приборы, военные, полупроводники |
Молибден (Mo) | 2620 °С | Покрытия, солнечные элементы, инструментальная и быстрорежущая сталь |
Ниобий (Nb) | 2468 °С | Сверхпроводники, легирование стали, инструментальные стали, натриевые лампы |
Хром (Cr) | 1907 °С | Легирование, покрытие, катализатор |
Гафний (Hf) | 2227 °С | Стержни управления ядерными реакторами, легирование, микропроцессоры |
Иридий (Ir) | 2454 °С | Отвердитель, легирование (особенно осмием), наконечники ручек, подшипники компаса |
Осмий (Os) | 3050 °С | Легирование, иглы, кончики ручек |
Родий (Rh) | 1960 °С | Легирование, катализатор, украшения |
Рутений (Ру) | 2310 °С | Солнечные элементы, легирование (особенно платиной и палладием), ювелирные изделия |
Титан (Ti) | 1668 °С | Легирование, самолеты, корабли, гребные валы, теплообменники |
Ванадий (V) | 1910 °С | Легирование (особенно сталью и титаном) |
Цирконий (Zr) | 1855 °С | Реакторы ядерные, магниты (легированные ниобием), химическая промышленность |
Тугоплавкие металлы имеют узкоспециализированные применения, такие как освещение, инструменты, смазочные материалы и стержни для ядерных реакций. Они не могут быть отлиты в формы и могут быть обработаны только с использованием порошковой металлургии.
Они не могут быть отлиты в формы и могут быть обработаны только с использованием порошковой металлургии.
Лютеций, лавренций и протактиний также имеют высокие температуры плавления. Но они очень радиоактивны или имеют очень ограниченное применение и обычно не используются.
Для сравнения, температура плавления стали колеблется в пределах 1370-1510 °C (в зависимости от конкретного сплава). Сталь, конечно же, не тугоплавкий металл, а сплав на основе железа, который иногда смешивают с указанными выше тугоплавкими металлами.
Другие распространенные металлы с высокой температурой плавления
Следующие четыре металла являются наиболее часто используемыми металлами с высокой температурой плавления ниже 1850 °C (не тугоплавкие металлы):
- Палладий (Pd)
- Скандий (Sc)
- Железо (Fe)
- Иттрий (Y)
Палладий (Pd)
Палладий — блестящий серебристо-белый металл, плавящийся при 1555 °C и имеющий плотность 12,02 г/см 3 .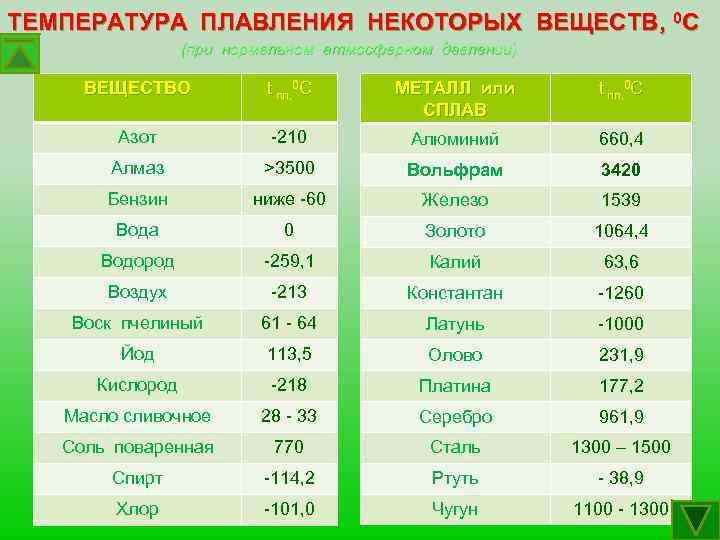 Металл обладает высокой коррозионной стойкостью на воздухе, но может потускнеть во влажном воздухе, содержащем серу. Он не играет никакой биологической роли и не токсичен.
Металл обладает высокой коррозионной стойкостью на воздухе, но может потускнеть во влажном воздухе, содержащем серу. Он не играет никакой биологической роли и не токсичен.
Металл получают как побочный продукт при рафинировании медных и никелевых руд. Он чрезвычайно пластичен, и его легко можно превратить в тонкий лист, который можно использовать в декоративных целях или в качестве украшений.
Чаще всего используется в производстве автомобильных каталитических нейтрализаторов. Он также широко используется для обесцвечивания золота при изготовлении украшений из белого золота. Другие популярные применения включают стоматологию, керамические конденсаторы, изготовление электрических контактов и хирургических инструментов.
Скандий (Sc)
Скандий — серебристо-белый металл с температурой плавления 1541 °C и плотностью 3,0 г/см 3 . Это мягкий металл, который медленно меняет цвет на желтоватый или розоватый при воздействии воздуха из-за образования оксида скандия (Sc 2 O 3 ) на поверхности. Он не имеет известной биологической роли, но считается канцерогеном.
Он не имеет известной биологической роли, но считается канцерогеном.
Скандий является основным элементом тортвейтита, очень ценного коллекционного минерала, найденного в Скандинавии. Скандий считается редкоземельным элементом, поскольку он имеет химические свойства, сходные с другими редкоземельными элементами, и встречается в тех же рудах.
Скандий повышает температуру рекристаллизации алюминия более чем до 600 °C. Это намного выше температурного диапазона термообрабатываемых алюминиевых сплавов. Это мощный легирующий элемент, который значительно улучшает механические и физические характеристики алюминиевого сплава. Эти сплавы набирают популярность в авиационной и транспортной отраслях.
Железо (Fe)
Железо – металл серебристо-серого цвета с температурой плавления 1535 °C и плотностью 7,87 г/см 3 . Это пластичный, мягкий металл, относительно хороший проводник тепла и электричества. В чистом виде он очень реакционноспособен и легко окисляется на воздухе с образованием красно-коричневых оксидов железа (или ржавчины). Он имеет известные биологические роли и жизненно важен для функционирования живых организмов. Считается нетоксичным.
Он имеет известные биологические роли и жизненно важен для функционирования живых организмов. Считается нетоксичным.
Железо получают путем плавки/восстановления железной руды (гематита и магнетита) в чугун, содержащий большое количество углерода и других примесей, в доменных печах при температуре около 2000 °C с последующим удалением этих примесей.
Железо (вместе с его сплавами) является наиболее распространенным промышленным металлом в мире. Большая часть производимого железа используется для производства различных видов стали. Добавление никеля, хрома, ванадия и вольфрама улучшает коррозионную стойкость, а добавление углерода в количестве 3-5% масс. позволяет получить недорогой сплав для труб и других неконструкционных применений.
Иттрий (Y)
Иттрий — серебристо-белый металл, плавящийся при 1525 °C и имеющий плотность 4,47 г/см 3 . Он в меру мягкий и пластичный. Он не имеет известной биологической роли, но может быть очень токсичным для людей и животных.