Ржавеет медь: Коррозия меди
Содержание
Какие металлы ржавеют? — Официальный блог компании «ПЕРХИМ»
Автор Анна Фомина На чтение 6 мин Просмотров 2.8к. Опубликовано
Содержание
- Что такое ржавчина?
- Что такое коррозия?
- Что такое редукция?
- Что такое окисление?
- Ржавеют ли медь, железо и алюминий?
- Ржавеет ли медь?
- Ржавеет ли железо?
- Как предотвратить ржавление металлов
Что такое ржавчина?
Ржавчина, обычно называемая окислением, возникает, когда железо или металлические сплавы, содержащие железо, такие как сталь, подвергаются воздействию кислорода и воды в течение длительного периода времени.
Ржавчина образуется, когда железо подвергается процессу окисления, но не все окисления образуют ржавчину. Как уже говорилось выше, ржаветь может только железо или сплавы, содержащие железо, но и другие металлы могут подвергаться коррозии аналогичным образом.
Что такое коррозия?
Коррозия возникает, когда элемент, легко теряющий свои электроны (например, некоторые металлы), соединяется с элементом, который поглощает дополнительные электроны (кислород), а затем вступает в контакт с раствором электролита (водой). Работа воды в процессе коррозии заключается в ускорении потока электронов от металла к кислороду.
Этот процесс называется окислительно -восстановительной реакцией и на самом деле представляет собой два химических процесса, которые происходят одновременно: восстановление (редукция) и окисление.
Что такое редукция?
Редукция – это название химической реакции, которая происходит, когда молекула получает электрон. Это роль кислорода в коррозии металлов.
Что такое окисление?
Окисление – это противоположная восстановлению реакция, которая происходит, когда молекула теряет электрон. Это роль воздействия металла в коррозии металла. Ржавчина и патина меди странного зеленого цвета – видимые результаты того, что металлы теряют свои электроны в воздухе.
Ржавеют ли медь, железо и алюминий?
Технически ржаветь может только железо и сплавы, содержащие железо. Другие металлы, включая драгоценные металлы, такие как золото и серебро, могут подвергаться аналогичной коррозии.
Что отличает определенные металлы, так это время, необходимое для того, чтобы они начали ржаветь или подвергаться коррозии.
Вот несколько примеров о том, как наиболее распространенные металлы противостоят ржавчине и коррозии.
В ассортименте нашей компании есть эффективный удалитель ржавчины с металлов «РжавоМед-У»
Ржавеет ли медь?
Медь не ржавеет, однако, корродирует. Медь имеет естественный коричневый цвет и при коррозии приобретает ярко-зеленый оттенок. Хотя некоторые считают, что реакция меди скорее потускнение, чем окисление, металл по-прежнему подвергается аналогичному процессу «ржавления».
В естественной среде медь крайне несклонна к коррозии. Тип коррозии, которая в конечном итоге приводит к поломке медных питьевых труб, называется эрозионной коррозией, и она возникает только из-за воздействия текущей турбулентной воды в течение длительного периода времени. Обычно видимая на старых монетах знаменитая красивая зеленая «патина» может полностью сформироваться за 20 лет.
Обычно видимая на старых монетах знаменитая красивая зеленая «патина» может полностью сформироваться за 20 лет.
Это один из немногих природных металлов, который не добывается из руды (хотя он может быть получен другими способами), пригодный для непосредственного использования в естественной среде. Этот, а также тот факт, что медь очень мягкая и с ней легко работать, повлекли за собой то, что медь стала одним из первых металлов, с которыми работали люди в истории человечества.
Фактически, медь имела такое большое значение, что у нас действительно есть период в истории, называемый медным веком.
Медь обладает высокой проводимостью к теплу и электричеству, поэтому ее часто используют в электропроводке.
Медь также имеет очень низкую реакционную способность. Известный инструмент в химии, который представляет собой последовательность металлов, упорядоченную от самой высокой до самой низкой реакционной способности до кислот, воды, извлечения металлов из их руд и других реакций.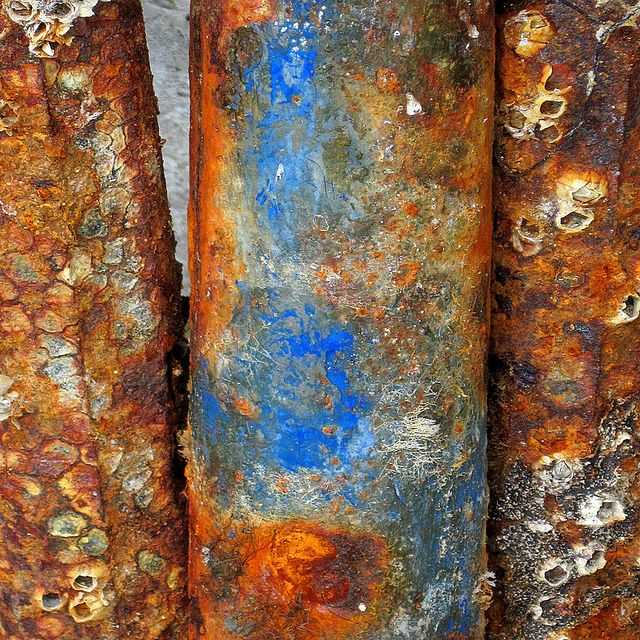 Из-за её низкой реакционной способности специальный сплав меди (90% меди и 10% никеля) используется для деталей лодок, которые в дальнейшем подвергаются воздействию морской воды, или в качестве труб для транспортировки питьевой воды. Если вы осмотритесь в своем доме или здании, то заметите, что во многих ваших приборах используются медные трубы для подачи и отвода воды.
Из-за её низкой реакционной способности специальный сплав меди (90% меди и 10% никеля) используется для деталей лодок, которые в дальнейшем подвергаются воздействию морской воды, или в качестве труб для транспортировки питьевой воды. Если вы осмотритесь в своем доме или здании, то заметите, что во многих ваших приборах используются медные трубы для подачи и отвода воды.
По данным Министерства жилищного строительства и городского развития России, средний срок службы медной водопроводной трубы составляет 50-70 лет.
Ржавеет ли железо?
Да. Помните, что технически ржаветь может только железо и сплавы, содержащие железо.
По сравнению с коррозией других металлов, железо относительно быстро ржавеет, особенно если оно подвергается воздействию воды и кислорода. Фактически, когда железо подвергается воздействию воды и кислорода, оно может начать ржаветь в течение нескольких часов.
Железо также быстро ржавеет при воздействии высоких температур. Экстремальные температуры могут изменить химический состав металла, что делает его чрезвычайно склонным к рекомбинации с кислородом в окружающей среде.
Экстремальные температуры могут изменить химический состав металла, что делает его чрезвычайно склонным к рекомбинации с кислородом в окружающей среде.
Алюминий производится в 3 этапа:
Этап 1. Добыча полезных ископаемых
Этап 2. Обработка
Этап 3. Электролитическое восстановление (при котором образуется сам алюминий)
Алюминий получают из минерала боксита. Бокситы чаще всего встречаются в субтропических местах, таких как Африка, Западная Индия, Южная Америка и Австралия, хотя есть небольшие месторождения и в других местах, например, в Европе. Австралия является крупнейшим производителем бокситов. На его долю приходится около 23% мировой добычи.
Затем этот боксит перерабатывается в оксид алюминия, который состоит только из атомов алюминия и кислорода, связанных вместе.
Затем через оксид алюминия пропускается электрический ток, который отделяет различные компоненты друг от друга. Пузырьки кислорода образуются на одном конце, а капли чистого расплавленного алюминия собираются на другом.
Около 4-5 тонн боксита перерабатывается в 2 тонны оксида алюминия, что дает 1 тонну чистого алюминия.
Алюминий корродирует намного медленнее, чем другие металлы, такие как железо. Причина того, что алюминий не так легко подвергается коррозии, как другие металлы, заключается в его особой реакции с водой.
Обычно, когда вода вступает в контакт с металлом, она побуждает металл еще быстрее отдавать свои электроны окружающему его кислороду.
Однако у алюминия особая реакция на воду. Когда вода соприкасается с алюминием, атомы алюминия и кислорода (содержащиеся в металле, а не кислород в окружающем его воздухе) перемещаются дальше друг от друга.
Они окажутся почти на 50% дальше друг от друга, чем были в начале. Эта реакция удаления меняет молекулярную структуру алюминия настолько, что он становится химически инертным, а это означает, что он не так легко подвергается коррозии.
Как предотвратить ржавление металлов
Ржавчина – это естественная химическая реакция. Несмотря на то, что некоторые металлы ржавеют быстрее других, это не должно вас сдерживать от использования этих металлов для определенных целей. Есть много способов предотвратить ржавчину металлов, например, металлические краски и покрытия, защитные барьеры, барьерные пленки, а также многочисленные антикоррозионные растворы и лужение. В каждом методе используются разные соединения и материалы для создания защитного барьера между металлом и элементами, вызывающими ржавчину и коррозию.
Несмотря на то, что некоторые металлы ржавеют быстрее других, это не должно вас сдерживать от использования этих металлов для определенных целей. Есть много способов предотвратить ржавчину металлов, например, металлические краски и покрытия, защитные барьеры, барьерные пленки, а также многочисленные антикоррозионные растворы и лужение. В каждом методе используются разные соединения и материалы для создания защитного барьера между металлом и элементами, вызывающими ржавчину и коррозию.
В ассортименте нашей компании есть эффективный удалитель ржавчины с металлов «РжавоМед-У»
Защита от ржавчины — MEL Chemistry
Реагенты
Медная проволока
Железный гвоздь
Гексацианоферрат(III) калия
Магниевая полоска
Хлорид натрия
Феноловый красный
Безопасность
- Перед началом опыта наденьте защитные перчатки и очки.

- Проводите эксперимент на подносе.
Общие правила безопасности
- Не допускайте попадания химических реагентов в глаза или рот.
- Не допускайте к месту проведения экспериментов людей без защитных очков, а также маленьких детей и животных.
- Храните экспериментальный набор в месте, недоступном для детей младше 10 лет.
- Помойте или очистите всё оборудование и оснастку после использования.
- Убедитесь, что все контейнеры с реагентами плотно закрыты и хранятся по правилам после использования.
- Убедитесь, что все одноразовые контейнеры правильно утилизированы.
- Используйте только оборудование и реактивы, поставляемые в наборе или рекомендуемые текущими инструкциями.

- Если вы использовали контейнер для еды или посуду для проведения экспериментов, немедленно выбросьте их. Они больше не пригодны для хранения пищи.
Информация о первой помощи
- В случае попадания реагентов в глаза тщательно промойте глаза водой, при необходимости держа глаз открытым. Немедленно обратитесь к врачу.
- В случае проглатывания реагентов промойте рот водой, выпейте немного чистой воды. Не вызывайте рвоту. Немедленно обратитесь к врачу.
- В случае вдыхания реагентов выведите пострадавшего на свежий воздух.
- В случае контакта с кожей или ожогов промывайте поврежденную зону большим количеством воды в течение 10 минут или дольше.
- В случае сомнений немедленно обратитесь к врачу.
 Возьмите с собой химический реагент и контейнер от него.
Возьмите с собой химический реагент и контейнер от него. - В случае травм всегда обращайтесь к врачу.
Рекомендации для родителей
- Неправильное использование химических реагентов может вызвать травму и нанести вред здоровью. Проводите только указанные в инструкции эксперименты.
- Данный набор опытов предназначен только для детей 10 лет и старше.
- Способности детей существенно различаются даже внутри возрастной группы. Поэтому родители, проводящие эксперименты вместе с детьми, должны по своему усмотрению решить, какие опыты подходят для их детей и будут безопасны для них.
- Родители должны обсудить правила безопасности с ребенком или детьми перед началом проведения экспериментов. Особое внимание следует уделить безопасному обращению с кислотами, щелочами и горючими жидкостями.

- Перед началом экспериментов очистите место проведения опытов от предметов, которые могут вам помешать. Следует избегать хранения пищевых продуктов рядом с местом проведения опытов. Место проведения опытов должно хорошо вентилироваться и находиться близко к водопроводному крану или другому источнику воды. Для проведения экспериментов потребуется устойчивый стол.
- Вещества в одноразовой упаковке должны быть использованы полностью или утилизированы после проведения одного эксперимента, т.е. после открытия упаковки.
Часто задаваемые вопросы
А другой металл может защитить железо?
Конечно! Но, чтобы соответствовать роли защитника, металл должен соответствовать определенным критериям.
Все металлы по-разному готовы делиться своими электронами. Одни отдают их очень неохотно, а другие делятся с удовольствием. Более щедрый металл может отдать свои электроны другому и таким образом защитить его от коррозии. Ученые создали электрохимический ряд активности металлов, в котором все металлы расположены в зависимости от их готовности отдавать электроны:
Более щедрый металл может отдать свои электроны другому и таким образом защитить его от коррозии. Ученые создали электрохимический ряд активности металлов, в котором все металлы расположены в зависимости от их готовности отдавать электроны:
Cs → Na → Mg → Al → Zn → Fe → Sn → Pb → Cu → Ag
Чем левее металл, тем он щедрее. Поэтому спасти железо Fe от коррозии могут только те металлы, которые стоят слева от него в ряду активности. Помимо магния Mg, защитить железо могут алюминий Al и цинк Zn. А могут ли помочь железу самые крайние слева металлы, такие как натрий Na и цезий Cs? Увы, они слишком щедрые! Вместо того чтобы спокойно отдавать электроны воде и другому металлу, натрий и цезий слишком быстро отдают электроны воде, выделяя при этом большое количество тепла и воспламеняющийся газ водород.
Медь, из которой сделана проволока, — это тоже металл. Она передает железу электроны от магния, но достаточно ли этого для спасения железа? Может ли медь защитить железо своими силами?
В электрохимическом ряду активности металлов (о нем можно прочитать выше) медь расположена правее железа Fe, а значит, она не станет делиться электронами. Даже наоборот: медь будет забирать электроны у железа, ускоряя его коррозию.
Даже наоборот: медь будет забирать электроны у железа, ускоряя его коррозию.
Если электроны переходят по проволоке от одного металла к другому, можно ли сказать, что по проволоке течет электрический ток?
Да, именно так и работают электрические батарейки! Кстати, эта тема подробно рассмотрена в наборе Химия и электричество.
Другие эксперименты
Батарейка из лимона
Волшебная бумага
Трансмутация
Разноцветное пламя
Пошаговая инструкция
Ржавчина — это особый «симптом» постепенного разрушения металла (коррозии). В соленой воде коррозия протекает намного быстрее — потому-то мы и добавляем NaCl. Однако этого недостаточно, чтобы ржавление гвоздей стало заметным за короткий промежуток времени.
В соленой воде коррозия протекает намного быстрее — потому-то мы и добавляем NaCl. Однако этого недостаточно, чтобы ржавление гвоздей стало заметным за короткий промежуток времени.
Чтобы сделать этот процесс наглядным, добавим гексацианоферрат(III) калия K3[Fe(CN)6] и феноловый красный. Они выявят даже слабые следы ржавчины и образуют с ними яркоокрашенные соединения.
Когда кислород O2 забирает у железа Fe электроны, образуется ржавчина. Железо не прочь поделиться своими электронами, но некоторые металлы делают это более охотно. Так, магний с легкостью отдает железу электроны, и те переходят от полоски к гвоздю по мостику из меди Cu.
Одиночный железный гвоздь ржавеет в воде, а K3[Fe(CN)6] это быстро выявляет и покрывает его синими наростами, похожими на водоросли. При этом гвоздь, соединенный с магнием, сияет как новый. Почему так?
Железо, оказавшееся с кислородом один на один, теряет электроны. А вот в гвозде, соединенном с полоской, железо сохраняет металлическую форму, принимая по медной проволоке электроны от магния. Чтобы убедиться в этом, перережьте проволоку и посмотрите, справится ли железо без электронов магния.
А вот в гвозде, соединенном с полоской, железо сохраняет металлическую форму, принимая по медной проволоке электроны от магния. Чтобы убедиться в этом, перережьте проволоку и посмотрите, справится ли железо без электронов магния.
Утилизация
Пожалуйста, утилизируйте химические отходы эксперимента в соответствии с нормами вашего региона. Остальные твердые отходы утилизируйте вместе с бытовым мусором. Растворы слейте в раковину и затем тщательно промойте ее водой.
Что произошло
Почему гвоздь покрыт синим осадком? И почему раствор во второй половине чашки Петри становится красным?
Коррозия протекает очень медленно, и процесс разрушения металла не отследить невооруженным глазом. Поэтому мы используем два вещества: гексацианоферрат(III) калия K3[Fe(CN)6] и феноловый красный.
С ними процесс коррозии становится более наглядным. Химические уравнения для коррозии железа Fe и магния Mg очень похожи. Железо Fe окисляется до Fe2+, в то время как молекулы кислорода O2 и воды H2O превращаются в ионы OH−:
2Fe − 4e− → 2Fe2+
O2 + 2H2O + 4e− → 4OH−
А вот уравнение коррозии магния:
2Mg − 4e− → 2Mg2+
O2 + 2H2O + 4e− → 4OH−
Гексацианоферрат(III) калия K3[Fe(CN)6] сразу же взаимодействует с ионами железа Fe2+. Вместе они образуют очень яркое соединение, известное как «берлинская лазурь» KFe[Fe(CN)6]. Это соединение прекрасно видно, даже если его совсем немного.
Fe2+ + K3[Fe(CN)6] → KFe[Fe(CN)6] + 2K+
В отличие от гексацианоферрата(III) калия, феноловый красный меняет окраску с желтой на красную (не запутайтесь!) не в присутствии ионов металла, а при наличии другого продукта коррозии металла — ионов OH−.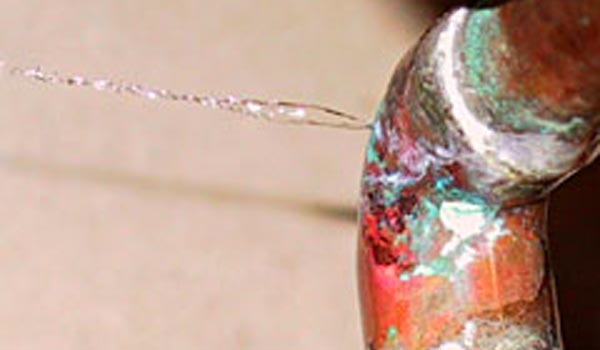 Поэтому при коррозии магния Mg, раствор становится красным. Вы можете спросить: «Почему же тогда феноловый красный не меняет окраску в первой половинке чашке Петри? Ведь при окислении железа Fe так же образуются ионы OH−». Интересно, что феноловый красный меняет цвет в первой половинке чашки Петри, но мы этого не видим, из-за яркой берлинской лазури, которая перекрывает феноловый красный. Чтобы это проверить, можете провести опыт без K3[Fe(CN)6].
Поэтому при коррозии магния Mg, раствор становится красным. Вы можете спросить: «Почему же тогда феноловый красный не меняет окраску в первой половинке чашке Петри? Ведь при окислении железа Fe так же образуются ионы OH−». Интересно, что феноловый красный меняет цвет в первой половинке чашки Петри, но мы этого не видим, из-за яркой берлинской лазури, которая перекрывает феноловый красный. Чтобы это проверить, можете провести опыт без K3[Fe(CN)6].
Как защитить от коррозии целый корабль?
В опыте «Защита от ржавчины» вы защитили от коррозии маленькие кусочки магния и железа. Но как защитить от коррозии целый океанский лайнер? Конечно же, с помощью огромного количества магния! Кстати, обычно так и делают…
Защитные пластины из алюминиевого Al, цинкового Zn или магниевого Mg сплава прикрепляются к корпусу корабля, сделанного из сплава железа Fe. Эти пластины называют «анодами-протекторами» — они отдают электроны корпусу корабля и подвергаются коррозии вместо него. Так корабль какое-то время остается в безопасности. Как только эти пластины уменьшаются больше, чем наполовину, их заменяют на новые.
Так корабль какое-то время остается в безопасности. Как только эти пластины уменьшаются больше, чем наполовину, их заменяют на новые.
Но электроны могут перемещаться между металлами не только за счет щедрости одного металла и жадности другого. В опыте «Электричество против железа» показано, как электроны могут перемещаться с помощью батареек. Поэтому существует и другой способ защиты судна: нужно подключить батарейки к корпусу корабля и к металлической пластине. Пластина, подсоединенная к положительно заряженному «+» концу батарейки, будет ржаветь, а корпус корабля, подсоединенный к отрицательно-заряженному «–» концу батарейки, будет надежно защищен от коррозии.
СИР 12 — Древо
- Статья
- Обсуждение
- Предложения
- Версии
Изменить
Статья из энциклопедии «Древо»: drevo-info.ru
Библия. Ветхий Завет. Книга Премудрости Иисуса, сына Сирахова. Глава 12
| Скрыть русский перевод | Скрыть церковнославянский перевод
Главы: 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 21 22 23 24 25 26 27 28 29 30 31 32 33 34 35 36 37 38 39 40 41 42 43 44 45 46 47 48 49 50 51
1 Если ты делаешь добро, знай, кому делаешь, и будет благодарность за твои благодеяния. | 1 Аще добро твориши, разумей, кому твориши, и будет благодать благим твоим. |
| 2 Делай добро благочестивому, и получишь воздаяние, и если не от него, то от Всевышнего. | 2 Добро сотвори благочестивому, и обрящеши воздаяние, и аще не от него, то от вышняго. |
| 3 Нет добра для того, кто постоянно занимается злом и кто не подает милостыни. | 3 Не будет добро прилежащему во злых и не подающему милостыни. |
| 4 Давай благочестивому, и не помогай грешнику. | 4 Даждь благочестивому и не заступай грешника. |
| 5 Делай добро смиренному, и не давай нечестивому: запирай от него хлеб и не давай ему, чтобы он чрез то не превозмог тебя; | 5 Добро сотвори смиренному и не даждь нечестивому: возбрани хлебы твоя и не даждь ему, да не теми тя преможет: |
6 ибо ты получил бы сугубое зло за все добро, которое сделал бы ему; ибо и Всевышний ненавидит грешников и нечестивым воздает отмщением. | 6 сугуба бо зла обрящеши во всех благих, яже аще сотвориши ему: яко и вышний возненавиде грешники и нечестивым воздаст месть. |
| 7 Давай доброму, и не помогай грешнику. | 7 Даждь благому и не заступай грешника. |
| 8 Друг не познается в счастье, и враг не скроется в несчастье. | 8 Не познан будет во благих друг и не скрыется во злых враг. |
| 9 При счастье человека враги его в печали, а в несчастье его и друг разойдется с ним. | 9 Егда во благих будет муж, врази его во печали суть, во злых же его и друг разлучится. |
| 10 Не верь врагу твоему вовек, ибо, как ржавеет медь, так и злоба его: | 10 Не ими веры врагу твоему во веки: якоже бо медь ржавеет, тако и злоба его: |
| 11 хотя бы он смирился и ходил согнувшись, будь внимателен душею твоею и остерегайся его, и будешь пред ним, как чистое зеркало, и узнаешь, что он не до конца очистился от ржавчины; | 11 и аще смирится и пойдет поникнув, настави душу твою и хранися от него, и будеши ему яко очищено зерцало, и уразумееши, яко не до конца оторжаве: |
12 не ставь его подле себя, чтобы он, низринув тебя, не стал на твое место; не сажай его по правую сторону себя, чтобы он когда-нибудь не стал домогаться твоего седалища, и ты наконец поймешь слова мои и со скорбью вспомнишь о наставлениях моих. | 12 не постави его при себе, да не когда изринув тя станет на месте твоем: не посади его одесную себе, да не поищет когда седалища твоего, и на последок уразумееши словеса моя и о глаголех моих умилишися. |
| 13 Кто пожалеет об ужаленном заклинателе змей и обо всех, приближающихся к диким зверям? Так и о сближающемся с грешником и приобщающемся грехам его: | 13 Кто помилует обаянника змием усекнена и всех приступающих ко зверем? такожде ходящаго с мужем грешником и примешающагося грехом его: |
| 14 на время он останется с тобою, но, если ты поколеблешься, он не устоит. | 14 час с тобою пребудет, и аще уклонишися, не стерпит. |
15 Устами своими враг усладит тебя, но в сердце своем замышляет ввергнуть тебя в яму: глазами своими враг будет плакать, а когда найдет случай, не насытится кровью. | 15 Устнама своима усладит враг, и много пошепчет и речет добро глаголя: очима своима прослезится, а сердцем своим усоветует вринути тя в ров, и егда обрящет время, не насытится крове. |
| 16 Если встретится с тобою несчастье, ты найдешь его там прежде себя, | 16 Аще срящут тя злая, ту обрящеши его первее себе, |
| 17 и он, как будто желая помочь, подставит тебе ногу: | 17 и яко помагаяй подсечет пяту твою: |
| 18 будет кивать головою и хлопать руками, многое будет шептать, и изменит лицо свое. | 18 покивает главою своею и восплещет рукама своима, и много пошепчет и изменит лице свое. |
| Скрыть русский перевод | Скрыть церковнославянский перевод
Главы: 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 21 22 23 24 25 26 27 28 29 30 31 32 33 34 35 36 37 38 39 40 41 42 43 44 45 46 47 48 49 50 51
Редакция текста от: 30. 03.2008 14:23:19
03.2008 14:23:19
Дорогой читатель, если ты видишь, что эта статья недостаточна или плохо написана,
значит ты знаешь хоть немного больше, — помоги нам, поделись своим знанием.
Или же, если ты не удовлетворишься представленной здесь информацией и пойдешь искать дальше, пожалуйста,
вернись потом сюда и поделись найденным, и пришедшие после тебя будут тебе благодарны.
«СИР 12» еще можно поискать:
полнотекстовый поиск в Древе:
Яндекс —
Google
в других энциклопедиях:
Яндекс —
Википедия —
Mail.ru —
в поисковых системах:
Искомое.ru —
Яндекс —
Google
Медь ржавеет? — Подробное объяснение
Медь имеет атомный номер 29 и относится к d-блоку периодической таблицы. Это розовато-оранжевый блестящий металл. Он податлив, пластичен и хорошо проводит тепло и электричество.
Он также является важным микроэлементом для большинства живых организмов. Медь находит свое применение в различных отраслях промышленности, таких как строительство, электроника и т. д., а также в декоративных предметах.
д., а также в декоративных предметах.
В этой статье мы проверим, ржавеет ли медь так же, как железо.
Медь ржавеет? Нет, медь не ржавеет. Однако он подвергается окислению или коррозии. В отличие от ржавчины, медь образует на своей поверхности голубовато-зеленый цветной слой, известный как патина после коррозии, что приводит к потускнению ее блестящей поверхности. Поскольку медь восприимчива к потере электронов, она подвергается окислению при воздействии воздуха и влажной среды и со временем подвергается коррозии.
На самом деле ржавление представляет собой тип реакции окисления, которая происходит, в частности, с железом и его металлическими сплавами, когда они подвергаются воздействию воздуха и воды, например, во влажной среде.
Приводит к образованию на поверхности красноватого или желтовато-коричневого налета, известного как ржавчина. Итак, технически ржавление — это свойство, присущее только железу и родственным соединениям.
Медь не ржавеет. Тем не менее, он подвергается коррозии, что является еще одним типом реакции окисления. Это электрохимический процесс, который происходит, когда медь вступает в контакт с другим электроотрицательным элементом, который имеет сильное стремление получить электрон, например кислородом, или раствором электролита, например водой.
Тем не менее, он подвергается коррозии, что является еще одним типом реакции окисления. Это электрохимический процесс, который происходит, когда медь вступает в контакт с другим электроотрицательным элементом, который имеет сильное стремление получить электрон, например кислородом, или раствором электролита, например водой.
Коррозия меди отличается от ржавчины железа, поскольку ржавчина, образующаяся на поверхности железных предметов, разрушает и ослабляет металл, а также подвергает внутренние поверхности дальнейшему разрушению из-за ржавчины, поскольку верхний слой со временем отслаивается.
С другой стороны, слой патины, образующийся на поверхности меди, действует как защитное покрытие, прилипая к предмету и предотвращая дальнейшее повреждение металла.
Ржавчина также делает поверхность металла неприглядной, однако слой патины придает изделию эстетический вид.
Сколько времени требуется для коррозии меди?
Медь является одним из немногих металлов, встречающихся в природе почти в чистом виде. Влияние коррозии на медь в естественной среде практически не заметно.
Влияние коррозии на медь в естественной среде практически не заметно.
Однако воздействие усиливается в экстремальных условиях, таких как соленая вода, сера, аммиак, окисляющие кислоты и т. д. При благоприятных условиях коррозия меди занимает до 20 лет.
На самом деле медь является одним из наименее реакционноспособных металлов. Он занимает четвертое место в ряду реакционной способности после золота, серебра и платины, которые являются благородными металлами.
Собственно, благодаря низкой реакционной способности меди ее мельхиоровый сплав (90 % меди и 10 % никеля) пригоден для изготовления различных деталей водных лодок и кораблей.
Вы видели голубовато-зеленый налет на старых монетах, это из-за потускнения меди. Водопроводные трубы из меди со временем подвергаются эрозионному разрушению из-за турбулентного потока воды.
А знаете ли вы, что статуя свободы на самом деле сделана из меди? Теперь вы знаете причину его голубовато-зеленого цвета.
Этот слой почти такой же толщины, как исходный медный слой, и предотвращает дальнейшее окисление внутренних атомов меди, помогая сохранить это наследие.
Почему медь тускнеет?
Медь имеет электронную конфигурацию [Ar] 3d10 4s1.
Это показывает, что атом меди находится на расстоянии одного электрона от достижения стабильности. Именно из-за этого дополнительного электрона медь реагирует с электроотрицательными атомами, такими как кислород.
Эта реакция вызывает окисление меди, в результате чего она образует оксид меди, а также вызывает через некоторое время образование патины голубовато-зеленого цвета на поверхности медных изделий.
Слой патины служит защитным покрытием для меди, покрывая внутренние атомы меди и предохраняя их от дальнейшего окисления.
Эта реакция еще больше ускоряется во влажных условиях, когда присутствующая в воздухе влага служит катализатором реакции. Вот почему всегда рекомендуется сушить медные изделия или украшения каждый раз, когда они соприкасаются с водой.
Существуют и другие факторы, ответственные за потускнение меди, такие как:
• Тепло : Процесс коррозии ускоряется при высоких температурах, которые легко доступны в наши дни из-за изменения климата.
• Кислотная среда : Низкий уровень pH также действует как ускоритель реакции. Кислотные дожди и сернистые газы, присутствующие в атмосфере из-за высокого уровня загрязнения, также делают медные изделия восприимчивыми к коррозии.
• Чистящие химикаты : Они воздействуют на внешний слой меди, делая его восприимчивым к коррозии.
Почему медь становится зеленой, синей или черной?
Изменение цвета при потускнении меди происходит из-за образования различных оксидов меди при контакте с кислородом в присутствии влаги.
Различные оксиды образуются за счет наличия атомов меди из изделия и атомов кислорода из атмосферы.
Красный цвет, появляющийся на поверхности меди, обусловлен образованием оксида меди (I). Он медленно меняется на темно-коричневый или черноватый, что на самом деле является оксидом меди (II).
На более поздних стадиях покрытие приобретает голубовато-зеленый цвет, известный также как патина, из-за образования более сложных оксидов меди.
Корродирует ли медь в воде?
Да. Медь подвергается коррозии в воде в присутствии растворенного кислорода или без него.
Коррозия, возникающая в отсутствие растворенного кислорода, известна как бескислородная коррозия.
При этом типе коррозии газообразный водород выделяется в результате реакции между атомами меди и молекулами воды.
Теоретически коррозия происходит под водой, когда давление водорода и концентрация ионов меди низки.
Реакция протекает следующим образом:
Cu + h3O —–> CuOH + ½ h3
Однако, будучи зависимой от давления, реакция меняется на противоположную при увеличении давления водорода и снова приводит к образованию ионов меди.
Химия коррозии меди
Как обсуждалось в предыдущем разделе, существует несколько стадий коррозии меди, которые приводят к образованию различных продуктов. Условия образования этих продуктов также различаются.
В этом разделе попробуем понять химию коррозии меди.
Когда атомы кислорода впервые вступают в контакт с атомами меди, они приводят к образованию оксида меди(I) красного цвета в соответствии со следующей реакцией: s)
По мере дальнейшего развития реакции оксид меди (I) вступает в реакцию с большим количеством атомов кислорода, что приводит к образованию оксида меди (II) черного цвета.
2Cu2O(т) + O2 (г) —-> 4CuO(т)
Дальнейшие реакции протекают из-за присутствия в воздухе различных примесей. Различные уравнения реакций приведены ниже:
2CuO (т) + CO2 (г) + h3O (ж) —-> Cu2CO3(OH)2 (т)
3CuO (т) + 2CO2 (г) + h3O (ж) —-> Cu2 (CO3)2(OH)2 (т)
4CuO (т) + SO3 (г) + 3h3O (ж) —–> Cu4SO4(OH)6 (т)
Эти сложные оксиды меди ответственны за голубовато-зеленый слой патины, покрывающий медные конструкции и защищающий их от дальнейшей коррозии.
Лучшие способы очистки меди
На рынке доступны различные чистящие средства для очистки изделий из меди. Кроме того, поскольку медь использовалась людьми с доисторических времен, также доступны многие бытовые решения.
Их всех объединяет то, что они слабокислые, из-за чего образуют соли меди, которые можно смыть водой, придав вашему изделию новый вид.
Ниже приведены несколько признанных решений для очистки изделий из меди.
• Очистители меди, приобретаемые на рынке : На рынке имеется ряд продуктов в виде паст или кремов, которые очищают медные изделия, не повреждая их поверхность.
• Вустерширский соус : Этот кислый соус может очистить потускневшую поверхность меди, придав ей блестящий вид.
• Тамариндовая паста : Она также обладает кислотными свойствами, благодаря чему может использоваться в качестве чистящего средства для изделий из меди.
• Лимонный сок плюс пищевая сода : Лимон является кислым по своей природе, а пищевая сода помогает отчистить потускневшую поверхность, тем самым профессионально очищая медные изделия.
• Белый уксус и соль : 1½ чайной ложки соли, смешанные в чашке белого уксуса, служат отличным очистителем для меди.
Как предотвратить коррозию меди
Медь естественным образом окисляется во влажных условиях, что приводит к потускнению ее поверхности. Однако существуют определенные способы защиты изделий из меди от коррозии.
Некоторые из них перечислены ниже:
• Смазка : Образует защитный слой вокруг внешней поверхности, сводя к минимуму воздействие влаги. Любая бытовая смазка, например вазелин, может помочь предотвратить коррозию меди.
• Герметик для краски : Герметик не пропускает воздух к медным изделиям. Это может быть эффективным решением в случае с объектами отображения, которые не обрабатываются регулярно.
• Очистка : Самое простое, но самое эффективное решение для предотвращения коррозии. Регулярная чистка медных изделий и поддержание их в сухом состоянии — отличный способ предотвратить потускнение.
Заключение
Медь не ржавеет, как железо. Однако он подвергается другому типу реакции окисления, называемой коррозией.
Коррозия меди отличается от ржавчины тем, что проржавевшие железные предметы становятся слабыми и хрупкими. Слой ржавчины продолжает отслаиваться, обнажая внутренние слои и еще больше ухудшая качество объекта. С другой стороны, коррозия меди образует защитное покрытие на поверхности, которое предотвращает дальнейшее повреждение внутренних атомов.
Медь является одним из наименее реакционноспособных металлов, коррозия которого занимает много времени.
Основной причиной реакции меди с атомами кислорода является наличие одного 4s-электрона, который может быть легко удален электроотрицательным атомом, что делает атом меди стабильным.
Различное изменение цвета при коррозии меди связано с образованием различных оксидов меди.
Медь ржавеет, подвергается коррозии или окисляется?
Медь — это металл, который существует уже тысячи лет. Вы можете найти его на монетах, трубах, кабелях для электропроводки и даже декоративных элементах. Это популярный выбор по многим причинам, но многие люди могут задаться вопросом, способна ли медь ржаветь.
Медь не ржавеет, так как не содержит железа и поэтому не способна образовывать ржавчину. Подобно другим материалам, таким как латунь, которые также не содержат железа, медь может подвергаться окислению и коррозии, но не образует ржавчины.
Хотя ржавчина и коррозия не обязательно эквивалентны, в этой статье мы обсудим, как определенные факторы окружающей среды и другие элементы могут вызвать коррозию меди, а также ее окисление. Мы подробно рассмотрим, почему медь не ржавеет, как на нее влияет окружающая среда, а также как успешно обслуживать и очищать материалы, изготовленные из меди.
Если вы хотите узнать больше, продолжайте читать.
Содержание
Почему медь не ржавеет
Как сказано выше, медь просто не ржавеет, потому что не содержит железа. Металлы могут ржаветь только в том случае, если в них есть железо. Материалы, содержащие железо внутри, ржавеют при контакте с кислородом и водой.
Металлы могут ржаветь только в том случае, если в них есть железо. Материалы, содержащие железо внутри, ржавеют при контакте с кислородом и водой.
Хотя медь не содержит железа, она содержит элементы, которые делают ее способной к окислению и коррозии. Многие путают образование ржавчины и коррозии как одно и то же, но это разные вещи, и в основном это сводится к химии.
Во-первых, давайте разберем разницу между ржавчиной и коррозией.
Коррозия – это постепенное разрушение металлов в результате химической реакции, вызванной окружающей средой, которой подвергается материал. Ржавчина на самом деле является формой коррозии, но при возникновении ржавчины происходит окисление железа, также ржавчина не может возникнуть, если в этих материалах нет железа.
Ниже мы рассмотрим, как и почему медь может подвергаться коррозии и окислению, а также как можно лечить зараженную область.
Медь и коррозия
Коррозия возникает на меди при контакте с водой.
Когда вода встречается с медью, на поверхности может образоваться голубовато-зеленый налет, называемый патиной. В то время как визуально многим людям нравится вид яркой патины на таких поверхностях, как крыши и старинный декор, они, безусловно, являются плюсами и минусами коррозии меди.
В то время как визуально многим людям нравится вид яркой патины на таких поверхностях, как крыши и старинный декор, они, безусловно, являются плюсами и минусами коррозии меди.
Например, при образовании патины на поверхности меди металл теряет электроны. Тем не менее, патина также может служить положительным моментом, поскольку накопленная грязь может защитить медную поверхность от повреждения в результате окисления.
Медь и окисление
Окисление происходит при контакте поверхности металла с воздухом.
Подобно патине, которая образуется при коррозии, патина яркого цвета также может образовываться, когда медь подвергается воздействию воздуха. Это, в свою очередь, также защищает металл от будущей коррозии, что положительно сказывается на медной поверхности в долгосрочной перспективе.
Тем не менее, окисление также может сделать медь непригодной для использования и даже опасной. Например, при использовании для приготовления пищи медной поверхности, когда окисление на этой поверхности уже произошло, это может быть потенциально ядовитым при контакте с кислыми продуктами.
Вероятно, одна из самых известных уличных скульптур, Статуя Свободы, сделана из меди и покрыта зеленой патиной.
Таким образом, несмотря на то, что окисление и коррозия могут оказывать негативное воздействие на некоторые поверхности, медь может по-прежнему иметь культовый и красивый вид, даже когда она окружена и подвергается воздействию внешних факторов. В отличие от ржавчины, которая создает красно-коричневую чешуйчатость на поверхности, она может надолго повредить металл.
Надеюсь, теперь вы лучше понимаете, почему медь может не ржаветь, но как такие факторы, как окисление и коррозия, все же могут иметь место. Ниже мы рассмотрим некоторые способы обработки меди, на которую повлияли внешние элементы.
Как обрабатывать потускневшую медь
Как уже говорилось выше, мы обсуждали, как окисление и коррозия могут повлиять на внешний вид и долговечность меди. Ниже мы рассмотрим несколько способов, с помощью которых можно успешно обрабатывать поверхность меди, потускневшую от других элементов, таких как вода и воздух.
Полироль для меди
Полироль для меди легко удалит обесцвечивание, потускнение и восстановит блеск. Хотя некоторые из них могут рекламироваться как полироль для латуни или меди, вы можете использовать большинство из этих продуктов для большинства металлов. 9№ 0003
Средство для полировки и очистки латуни и меди Weiman — отличный выбор, который легко поможет вам достичь желаемых результатов. Этот продукт также обещает нетоксичную, устойчивую к царапинам формулу на водной основе, которая не повредит поверхность ваших медных материалов.
Рекомендуется наносить полироль на чистую мягкую ткань и смывать продукт после тщательной полировки. Наконец, высушите и отполируйте чистой тканью, чтобы получить блестящую поверхность.
Лимонный сок и соль
Если вы ищете способ использовать бытовые средства для очистки медных материалов, это решение может быть для вас.
Вы можете легко удалить любой вид потускнения меди на поверхности всего за несколько простых шагов. Выжмите лимон в миску, затем посыпьте солью. Рекомендуется использовать соотношение 75:25, в три раза больше лимона и соли.
Выжмите лимон в миску, затем посыпьте солью. Рекомендуется использовать соотношение 75:25, в три раза больше лимона и соли.
После того, как вы перемешали смесь до полного исчезновения соли, окуните в смесь мягкую ткань и приложите к медной поверхности. Если у вас нет лимонов под рукой, вы также можете использовать апельсиновый сок, так как он тоже кислый.
Заключение
В этой статье мы рассмотрели, что медь не подвержена ржавчине, потому что это металл, который не содержит железа.
Мы рассмотрели, что, хотя медь не ржавеет, мы коснулись того, как медь все еще может окисляться и подвергаться коррозии. Это происходит, когда такие металлы, как медь, вступают в контакт с водой и кислородом. Это может повлиять на общий внешний вид поверхности, а также на другие факторы, такие как прочность и долговечность.
Мы также рассмотрели несколько способов обработки и очистки потускневшей меди. Надеюсь, теперь вы лучше понимаете, как работает медь и как добиться наилучших результатов.
Con-Lux 9B-4D Медная ржавчина Точно подходит для краски и аэрозольной краски
Звоните 1-973-863-2639
Con-Lux
$
9,99
70% заказов отправляются в течение 2 рабочих дней.
Для гарантированной доставки в течение 1 рабочего дня выберите «Плата за ускоренное производство» во время оформления заказа.
Выберите тип краски / область применения
Спрей, OEM, бутылки и ручки
Краска для дома и стен
Специальная краска
Спрей, OEM, флаконы и ручки
Краска для дома и стен
Специальная краска
Выберите тип краски/нанесение
с помощью одной из кнопок выше
Вам нужно выбрать, прежде чем вы сможете добавить это в корзину.
Удовлетворение гарантировано
Если вас не устроит цвет краски, мы переделаем его бесплатно! Нажмите здесь, чтобы узнать подробности.
Описание
Как быстро я получу краску, соответствующую Con-Lux 9B-4D Copper Rust?
Вся краска изготавливается на заказ. В то время как большинство заказов доставляются в течение 48 часов, время изготовления краски, соответствующей Con-Lux 9B-4D Copper Rust, зависит от типа необходимой краски. Краски для внутренних и наружных работ обычно доставляются в течение 1–3 дней, в то время как доставка индивидуальной аэрозольной краски обычно занимает 3–5 дней. Время доставки зависит от вашего местоположения и выбранного вами способа доставки. Если вам нужно срочно, выберите «Ускоренное производство» во время оформления заказа. Большинство срочных производственных заказов доставляются в течение 24 часов в рабочие дни. Пожалуйста, свяжитесь с MyPerfectColor, если вас беспокоит конкретный крайний срок. Мы делаем все возможное, чтобы вы получили краску вовремя. Узнайте больше о сроках поставки краски на MyPerfectColor.
В то время как большинство заказов доставляются в течение 48 часов, время изготовления краски, соответствующей Con-Lux 9B-4D Copper Rust, зависит от типа необходимой краски. Краски для внутренних и наружных работ обычно доставляются в течение 1–3 дней, в то время как доставка индивидуальной аэрозольной краски обычно занимает 3–5 дней. Время доставки зависит от вашего местоположения и выбранного вами способа доставки. Если вам нужно срочно, выберите «Ускоренное производство» во время оформления заказа. Большинство срочных производственных заказов доставляются в течение 24 часов в рабочие дни. Пожалуйста, свяжитесь с MyPerfectColor, если вас беспокоит конкретный крайний срок. Мы делаем все возможное, чтобы вы получили краску вовремя. Узнайте больше о сроках поставки краски на MyPerfectColor.
Какие значения RGB, HEX и LRV для Con-Lux 9B-4D Медная ржавчина?
Значения RGB для Con-Lux 9B-4D Copper Rust: 152, 97, 92, а шестнадцатеричный код — #98615C. LRV для Con-Lux 9B-4D Copper Rust составляет 16,00. LRV означает значение отражения света и измеряет процент света, который отражает цвет. Узнайте больше о значениях коэффициента отражения света и использовании кодов RGB и Hex для краски.
LRV означает значение отражения света и измеряет процент света, который отражает цвет. Узнайте больше о значениях коэффициента отражения света и использовании кодов RGB и Hex для краски.
Какой тип краски используется для изготовления аэрозольной краски, соответствующей Con-Lux 9B-4D Copper Rust? И сколько аэрозольных баллончиков мне нужно?
MyPerfectColor использует акриловую эмаль, которая представляет собой быстросохнущее прочное покрытие, подходящее для внутренних и наружных работ. Индивидуальная аэрозольная краска MyPerfectColor, соответствующая Con-Lux 9B-4D Copper Rust, позволяет легко получить профессиональную гладкую поверхность любого цвета с любым блеском. Он хорошо прилипает к большинству поверхностей, включая металл, пластик, порошковые покрытия, шкафы и загрунтованное или ранее окрашенное дерево.
Спрей MyPerfectColor 11 унций покроет около 20 квадратных футов за один слой. Имейте в виду, что трудно оценить потребность в аэрозольной краске, так как покрытие сильно зависит от того, как она наносится. Узнайте больше о том, как работает аэрозольная краска, на MyPerfectColor.
Узнайте больше о том, как работает аэрозольная краска, на MyPerfectColor.
Что такое угол оттенка и цветность для Con-Lux 9B-4D Copper Rust?
Угол оттенка для Con-Lux 9B-4D Copper Rust составляет 29,85, а цветность — 24,75. Угол оттенка представляет положение оттенка цвета вокруг цветового круга. Цветность представляет интенсивность оттенка. Узнайте больше о просмотре цветов по оттенку.
Как MyPerfectColor может соответствовать Con-Lux 9B-4D Copper Rust?
В архиве MyPerfectColor есть оригинальный образец Con-Lux 9B-4D Copper Rust. Это позволяет нам сделать краску и убедиться, что она соответствует оригиналу.
Обратите внимание: если ваш материал не новый, краска может не подойти для подкрашивания, так как ваш материал состарился и, вероятно, отличается от того, что был новым. Узнайте больше о нашей точности подбора цветов. Если вам нужно средство для подкраски, отправьте нам часть, и мы сможем создать решение для подкрашивания, точно соответствующее текущему цвету и блеску ваших конкретных материалов.
Узнайте больше о нашей услуге подбора цветов.
Нужна ли грунтовка для Con-Lux 9B-4D Copper Rust?
Необходимость грунтовки под Con-Lux 9B-4D Copper Rust зависит от типа краски, окрашиваемой поверхности и места ее расположения. Ознакомьтесь с нашей таблицей выбора праймера, чтобы узнать, какой праймер вам может понадобиться, и узнать больше о том, когда вам может понадобиться праймер. Большинство людей не используют грунтовку для подкрашивания краски, но грунтовка может улучшить адгезию и обычно рекомендуется для наружных работ.
Как преобразовать Con-Lux 9B-4D Copper Rust в другую компанию?
Пока можем предоставить Con-Lux 9B-4D Медная ржавчина в краске, мы не предоставляем никакой информации о кроссовере. Мы обнаружили, что каждая компания по производству красок предлагает свой собственный уникальный набор цветов, и цвет редко имеет точный эквивалент в другом бренде.
Однако под цветным изображением на цветной странице есть ссылка «Исследовать цвета». При нажатии на эту ссылку отображаются цвета с похожими значениями, и вы можете искать любые цвета нужного вам бренда.
При нажатии на эту ссылку отображаются цвета с похожими значениями, и вы можете искать любые цвета нужного вам бренда.
Имейте в виду, что это просто показывает похожие цвета на основе значений цвета, которые мы сохранили в нашей базе данных. Это не означает, что это то же самое или дает какое-либо приближение о том, насколько близок цвет. Вы можете поиграть с ползунками Hue, Lightness и Chroma, чтобы расширить выбор.
Подходящие цвета краски Con-Lux
MyPerfectColor может сочетаться со всеми цветами краски Con-Lux, чтобы вы могли найти и наслаждаться любимыми цветами. MyPerfectColor использует свои экспертные возможности для воссоздания оригинального цвета Con-Lux путем сопоставления с оригинальными каталогами цветов Con-Lux и образцами. MyPerfectColor не использует Con-Lux Paint.
Цвета, показанные на этом веб-сайте, являются компьютерной имитацией цветов Con-Lux Color и могут не соответствовать стандартам Con-Lux Color. Обратитесь к публикациям Con-Lux, чтобы получить точный цвет.
