Ржавление железа признаки: Признаки химических реакций — урок. Химия, 8 класс.
Содержание
Признаки химических реакций | Образовательная социальная сеть
Урок-лабораторная работа в 8 классе
«Признаки химических реакций»
ХОД УРОКА:
В природе с момента ее зарожденья
Всегда с веществами идут превращенья.
Про эти природные измененья
Мы с вами сказали бы: “Это явленья!”
Явленья бывают различными,
Рассмотрим химические и физические.
Должны научиться мы их наблюдать,
А самое главное их различать!
ДЕМОНСТРАЦИОННЫЙ ЭКСПЕРИМЕНТ: ГОРЕНИЕ БУМАГИ И РЖАВЫЙ ГВОЗДЬ.
УЧИТЕЛЬ. Какие явления, происходящие с веществами, вам известны? Какие явления называются физическими? Приведите примеры физических явлений.
УЧЕНИК. Физическими явлениями называются изменения, при которых новые вещества не образуются. Переход воды в пар при нагревании, вытягивание кусочка меди в проволоку относятся к физическим явлениям.
УЧИТЕЛЬ. Какие изменения происходят с веществами при физических явлениях?
УЧЕНИК. При физических явлениях происходит изменение агрегатного состояния вещества, формы, размера тел. Физические явления — это явления: происходящие с веществами с сохранением их молекул, при которых данные вещества не превращаются в другие, а обычно изменяется только агрегатное состояние;
Физические явления — это явления: происходящие с веществами с сохранением их молекул, при которых данные вещества не превращаются в другие, а обычно изменяется только агрегатное состояние;
УЧИТЕЛЬ. Какие явления называются химическими? Приведите примеры химических явлений.
УЧЕНИК. Химическими называются явления, при которых исходные вещества (реагенты) превращаются в другие вещества (продукты реакции). К таким явлениям относятся: ржавление железа, скисание молока и множество других.
Химические явления — это явления, происходящие с веществами с разрушением молекул , в результате которых из одних веществ образуются другие.
А теперь попробуем применить полученные знания для выполнения следующего задания: укажите, о каких явлениях, физических или химических, идет речь в высказываниях поэтов:
• Унылая пора! Очей очарованье!
Приятна мне твоя прощальная краса –
Люблю я пышное природы увяданье,
В багрец и золото одетые леса!
А.С.Пушкин
• И трещат сухие сучья,
Разгораясь жарко,
Освещая тьму ночную
Далеко и ярко!
И. Суриков
Суриков
• В декабре, в декабре
Все деревья в серебре,
Нашу речку, словно в сказке,
За ночь вымостил мороз…
С.Я.Маршак
•…А если медь в печи нагреть,
То станет тяжелее медь
С окалиною вместе.
Не верите – так взвесьте…
Е.Ефимовский
• Что за звездочки резные
На пальто и на платке?
Все сквозные, вырезные,
А возьмешь – вода в руке?
Е.Благинина
При изучении химии нас конечно же будут интересовать явления химические. Ежеминутно в мире протекает миллионы химических реакций – в нашем желудке, когда мы едим, в выпекающемся пироге или в двигателе автомобиля. Но как определить происходит химическая реакция или нет?
При химических процессах происходит превращение одних веществ в другие, которые обладают новыми свойствами, которыми не обладали исходные вещества. Эти превращения сопровождаются яркими и наглядными изменениями. Эти наглядные изменения называются признаки.
На ваших столах имеются инструкции по выполнению лабораторной работы и необходимый набор реактивов. Перед выполнением опытов я напоминаю о необходимости соблюдения правил техники безопасности:
Перед выполнением опытов я напоминаю о необходимости соблюдения правил техники безопасности:
- При выполнении опытов следует соблюдать осторожность.
2) Не разбрызгивайте и не разливайте реактивы.
3) Работу выполняйте только над подносом.
4) Не направляйте пробирку на себя или на соседа.
5) Свое рабочее место оставляйте чистым.
Лабораторные опыты:
1) Взаимодействие мела с серной кислотой.
На кусочек мела капните 2-3 капли раствора серной кислоты. Что вы наблюдаете? Что является признаком данной реакции?
Давайте составим уравнение этого превращения.
CaCO3 + h3SO4 = CaSO4 + h3О + СO2↑
Почему дрожжевое тесто «пыхтит» в кастрюле? А когда его обминают, то появляется писк? Это тоже признак того, что протекает химическая реакция. При брожении дрожжей образуется углекислый газ, происходит образование нового вещества.
- Взаимодействие хлорида бария с сульфатом натрия.

В пробирку с хлоридом бария добавьте 2-3 капли раствора сульфата натрия. Что вы наблюдаете? Что является признаком данной реакции?
Давайте составим уравнение этого превращения.
BaCl2 + Na2SO4 = BaSO4 + 2 NaCl
- Взаимодействие FeCl3 c KCNS.
В пробирку с хлоридом железа (III) добавьте 2 капли роданида калия KCNS. Что вы наблюдаете? Что является признаком данной реакции?
Давайте составим уравнение этого превращения.
FeCl3 + 3KNCS = Fe(CNS)3 + 3KCl
- Взаимодействие гидроксида натрия с фенолфталеином.
В пробирку с гидроксидом натрия добавьте 2 капли фенолфталеина. Что вы наблюдаете? Что является признаком данной реакции?
ПРИЗНАКИ ХИМИЧЕСКИХ РЕАКЦИЙ:
- Выделение газа
- Образование осадка
- Изменение окраски
- Появление запаха
- Выделение или поглощение энергии (в виде света или тепла).
ВИРТУАЛЬНАЯ ЛАБОРАТОРИЯ.
ДОМАШНЕЕ ЗАДАНИЕ:
- Физическое или химическое явление?
• кипение воды;
• образование на деревьях инея;
• скисание молока;
• ржавление гвоздя;
• таяние льда;
• горение бенгальских огней;
• гниение растений;
• приготовление сахарного сиропа;
• приготовление сахарной пудры из сахара;
• горение свечи;
- почернение медной пластинки при нагревании;
- измельчение сахара в ступке.

2) Физические явления — это явления:
А) происходящие с веществами в разные времена года;
Б) происходящие с веществами с разрушением молекул;
В) при которых данные вещества не превращаются в другие, а обычно изменяется только их агрегатное состояние;
Г) в результате которых из одних веществ образуются другие.
3) Признаком химических реакций не является:
А) появление запаха;
Б) изменение объёма;
В) изменение цвета;
Г) выделение света и тепла.
- В крепко заваренный свежий чай в стакане опустите кусочек лимона или несколько кристаллов лимонной кислоты. Что наблюдаете?
5) Немного лимонной кислоты на кончике чайной ложки растворите в воде, а затем добавьте в полученный раствор столько же пищевой (питьевой) соды. Что наблюдаете?
Лабораторная работа по химии
Ученика(цы) 8 класса
_________________________________________________________
ФИО
ПРИЗНАКИ ХИМИЧЕСКИХ РЕАКЦИЙ
В природе с момента ее зарожденья
Всегда с веществами идут превращенья.
Про эти природные измененья
Мы с вами сказали бы: “Это явленья!”
Явленья бывают различными,
Рассмотрим химические и физические.
Должны научиться мы их наблюдать,
А самое главное их различать!
Физические явления — это явления, происходящие с веществами с сохранением их молекул, при которых данные вещества не превращаются в другие, а обычно изменяется только их агрегатное состояние.
Химические явления — это явления, в результате которых из одних веществ образуются другие.
ЗАДАНИЕ: укажите, о каких явлениях, физических или химических, идет речь в высказываниях поэтов:
• Унылая пора! Очей очарованье!
Приятна мне твоя прощальная краса –
Люблю я пышное природы увяданье,
В багрец и золото одетые леса! (А.С.Пушкин)
• И трещат сухие сучья,
Разгораясь жарко,
Освещая тьму ночную
Далеко и ярко! (И.Суриков)
• В декабре, в декабре
Все деревья в серебре,
Нашу речку, словно в сказке,
За ночь вымостил мороз. .. (С.Я.Маршак)
.. (С.Я.Маршак)
•…А если медь в печи нагреть,
То станет тяжелее медь
С окалиною вместе.
Не верите – так взвесьте… (Е.Ефимовский)
• Что за звездочки резные
На пальто и на платке?
Все сквозные, вырезные,
А возьмешь – вода в руке? (Е.Благинина)
При химических процессах происходит превращение одних веществ в другие, которые обладают новыми свойствами, которыми не обладали исходные вещества. Эти превращения сопровождаются яркими и наглядными изменениями. Эти наглядные изменения называются признаки химических реакций.
ПРИ ВЫПОЛНЕНИИ ЛАБОРАТОРНОЙ РАБОТЫ ПОМНИ О СЛЕДУЮЩИХ ПРАВИЛАХ:
- При выполнении опытов следует соблюдать осторожность.
2) Не разбрызгивайте и не разливайте реактивы.
3) Работу выполняйте только над подносом.
4) Не направляйте пробирку на себя или на соседа.
5) Свое рабочее место оставляйте чистым.
I. Взаимодействие мела с серной кислотой.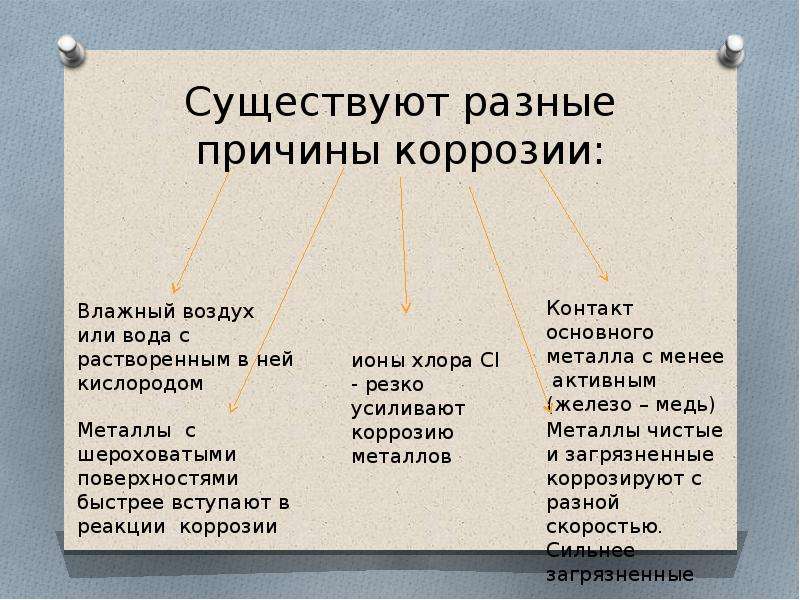
На кусочек мела капните 2-3 капли раствора серной кислоты. Что вы наблюдаете? Что является признаком данной реакции?
Уравнение реакции:
Признаком реакции является:_____________________________
II. Взаимодействие хлорида бария с сульфатом натрия.
В пробирку с хлоридом бария добавьте 2-3 капли раствора сульфата натрия. Что вы наблюдаете? Что является признаком данной реакции?
Уравнение реакции:
Признаком реакции является:_____________________________
III. Взаимодействие FeCl3 c KCNS.
В пробирку с хлоридом железа (III) добавьте 2 капли роданида калия KCNS. Что вы наблюдаете? Что является признаком данной реакции
Уравнение реакции:
Признаком реакции является:_____________________________
IV. Взаимодействие гидроксида натрия с фенолфталеином.
В пробирку с гидроксидом натрия добавьте 2 капли фенолфталеина. Что вы наблюдаете? Что является признаком данной реакции?
Признаком реакции является:_____________________________
ПРИЗНАКИ ХИМИЧЕСКИХ РЕАКЦИЙ
1)
2)
3)
4)
5)
ДОМАШНЕЕ ЗАДАНИЕ:
- Физическое или химическое явление?
• кипение воды;
• образование на деревьях инея;
• скисание молока;
• ржавление гвоздя;
• таяние льда;
• горение бенгальских огней;
• гниение растений;
• приготовление сахарного сиропа;
• приготовление сахарной пудры из сахара;
• горение свечи;
- почернение медной пластинки при нагревании;
- измельчение сахара в ступке.

2) Физические явления — это явления:
А) происходящие с веществами в разные времена года;
Б) происходящие с веществами с разрушением молекул;
В) при которых данные вещества не превращаются в другие, а обычно изменяется только их агрегатное состояние;
Г) в результате которых из одних веществ образуются другие.
3) Признаком химических реакций не является:
А) появление запаха;
Б) изменение объёма;
В) изменение цвета;
Г) выделение света и тепла.
4) В крепко заваренный свежий чай в стакане опустите кусочек лимона или несколько кристаллов лимонной кислоты. Что наблюдаете?
5) Немного лимонной кислоты на кончике чайной ложки растворите в воде, а затем добавьте в полученный раствор столько же пищевой (питьевой) соды. Что наблюдаете?
Урок 10. Признаки химических реакций – HIMI4KA
Архив уроков › Химия 8 класс
В уроке 10 «Признаки химических реакций» из курса «Химия для чайников» рассмотрим, что из себя представляют физические и химические явления; выясним, что такое химическая реакция, а также признаки и условия протекания химических реакций.
Давайте внимательно посмотрим вокруг себя. Мы уже знаем, что весь окружающий нас мир состоит из различных веществ: органических и неорганических, простых и сложных, твердых, жидких и газообразных. Остаются ли эти вещества в природе неизменными? Нет, в природе происходят различные изменения, которые называются явлениями. В зависимости от того, какие изменения происходят с веществами, различают явления физические и химические. Эти два рода явлений можно отличить друг от друга.
Содержание
- Физические явления
- Химические явления (реакции)
- Признаки химических реакций
- Условия протекания химических реакций
Физические явления
Нальем воду в колбу и нагреем ее до кипения. Каждый из вас знает, что при кипении вода превращается в пар, т. е. переходит в другое агрегатное состояние. Однако несложно доказать, что вода и пар — это одно и то же вещество. Подумайте, как это можно сделать.
Нагреем тонкую стеклянную трубку в пламени спиртовки. Стекло станет мягким, и мы легко изменим форму трубки, но стекло как вещество остается тем же.
Стекло станет мягким, и мы легко изменим форму трубки, но стекло как вещество остается тем же.
Эти явления физические. При физических явлениях не происходит образования новых веществ. Изменяется только агрегатное состояние веществ, их форма, а состав веществ остается прежним (рис. 48).
Например, вода — это вещество, которое в природе образует не только реки, моря, но и ледники, и облака. Ледники тают, облака роняют капли воды, вода испаряется, т. е. происходит изменение ее агрегатного состояния, но состав молекул остается неизменным.
Сгибание проволоки, дробление соли, плавление металлов (рис. 49), образование мраморной крошки, перемалывание зерна в муку, превращение воды в пар при кипячении — все это физические явления. Они осуществляются в результате деятельности человека. У веществ при этом изменяется только форма или агрегатное состояние.
Физическими называются явления, при которых изменяется только форма или агрегатное состояние веществ.
Химические явления (реакции)
Всегда ли вещества остаются неизменными? Нагреем красную медную проволоку в пламени спиртовки. Проволока покрывается черным налетом, который можно легко соскоблить ножом в виде черного порошка. Это уже новое вещество, в которое превратилась медь. Оно отличается от меди по цвету и плотности. В этом опыте мы наблюдаем химическое явление, которое происходит благодаря химической реакции.
Химические реакции — это явления, при которых происходит превращение одних веществ в другие.
Природа — это огромная лаборатория, в которой непрерывно происходит образование новых веществ. Горные породы и минералы под воздействием солнца, воды, углекислого газа и других веществ постепенно разрушаются и превращаются в новые вещества. В зеленых растениях из углекислого газа и воды образуются глюкоза и крахмал.
Человек превращает взятые из природы вещества (природный газ, нефть, руды) в необходимые ему бензин, резину, пластмассы, волокна, металлы.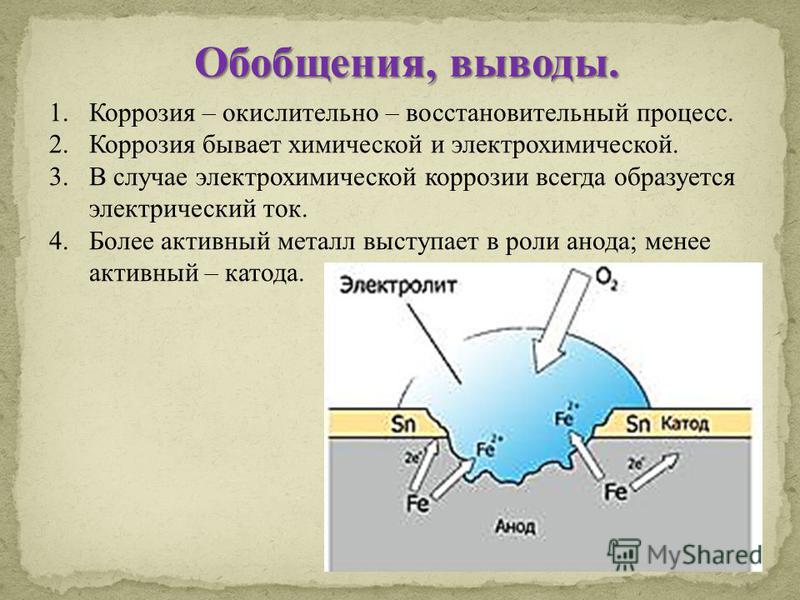 Часто в результате множества превращений получаются новые вещества, которых нет в природе. При всех этих явлениях происходит разрушение исходных веществ и образование новых веществ.
Часто в результате множества превращений получаются новые вещества, которых нет в природе. При всех этих явлениях происходит разрушение исходных веществ и образование новых веществ.
Например, в результате сгорания магния образуется новое вещество MgO (рис. 50). При сгорании метана получаются два вещества: углекислый газ CO2 и вода H2O. Из одного сложного вещества HgO в результате его разложения образуются два новых — ртуть Hg и кислород O2 (рис. 51).
Ржавление железа (рис. 52), кипячение воды, горение лучины, распространение запаха — какие из этих явлений можно отнести к химическим реакциям? По каким признакам можно судить, что химическая реакция произошла?
Признаки химических реакций
Проведем несколько химических реакций. Нагреем в пробирке зеленый порошок малахита (рис. 53) — минерала, в состав которого входят атомы меди, углерода, водорода и кислорода. Порошок малахита начинает «кипеть» из-за выделяющегося газа. Поднесем к отверстию пробирки спичку, она гаснет — это выделяющийся углекислый газ препятствует ее горению. На стенках пробирки заметны капельки воды, на дне остается черный порошок соединения меди (CuO). Наблюдения доказывают, что образуются новые вещества с другими свойствами. Прекратим нагревание. Сразу прекращается выделение углекислого газа — реакция больше не протекает.
Поднесем к отверстию пробирки спичку, она гаснет — это выделяющийся углекислый газ препятствует ее горению. На стенках пробирки заметны капельки воды, на дне остается черный порошок соединения меди (CuO). Наблюдения доказывают, что образуются новые вещества с другими свойствами. Прекратим нагревание. Сразу прекращается выделение углекислого газа — реакция больше не протекает.
Существуют и другие признаки химических реакций. Например, при горении магния излучается яркий свет и выделяется много теплоты (см. рис. 50).
На заметку: Раньше вспышка магния использовалась для освещения объекта во время фотографирования.
При сливании некоторых растворов наблюдается выпадение осадка (рис. 54). Некоторые осадки можно растворить при помощи других веществ. Например, при сливании растворов соды и известковой воды образуется белый осадок, который легко растворяется в уксусе.
При сгорании спички ощущается резкий запах. Какие еще признаки химических реакций наблюдаются при горении спички?
Изменения, происходящие с веществами, свидетельствуют о протекании химических реакций и являются признаками химических реакций.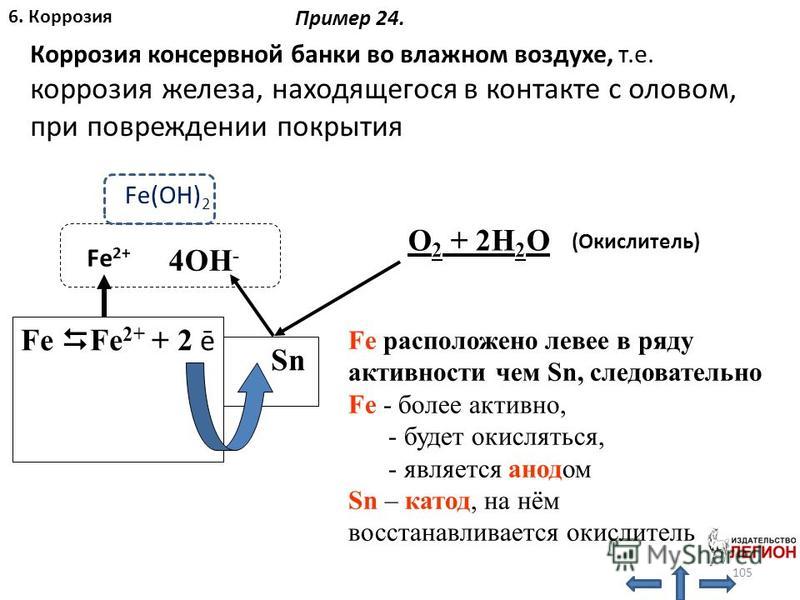
Признаки химических реакций:
• Выделение газа.
• Образование или исчезновение осадка.
• Изменение цвета.
• Появление запаха.
• Излучение света.
• Выделение или поглощение теплоты.
Большинство веществ не могут взаимодействовать друг с другом самопроизвольно. Для протекания многих химических реакций необходимо создавать определенные условия.
Условия протекания химических реакций
Необходимое и главное условие для протекания большинства реакций между различными веществами — это их соприкосновение. Для обеспечения лучшего контакта вещества измельчают, переводят в газообразное состояние. Многие вещества лучше реагируют друг с другом, если они растворены в воде.
Во многих случаях этого недостаточно, поэтому реагирующие вещества нагревают. Деревянная лучинка, смесь железа и серы, медь могут долгое время сохраняться при комнатной температуре, реакции начинаются только при их нагревании.
Мало знать, как начать химическую реакцию, надо еще знать, при каких условиях она будет протекать дальше. Почему необходимо все время нагревать сахар, чтобы добиться его полного сгорания, а деревянную лучинку зажигают один раз и она продолжает гореть?
Если при образовании новых веществ выделяется много теплоты, то ее бывает достаточно, чтобы нагревались новые порции вещества и реакция продолжалась. Во многих случаях реакции, начавшись, продолжаются за счет теплоты, выделяемой в этих реакциях, не требуя дополнительной энергии. Примером является горение угля. Другие реакции, например разложение сахара, требуют постоянной затраты энергии на ее продолжение.
В некоторых случаях для начала химического процесса необходимо освещение. Одной из таких реакций, требующих постоянного освещения, является известная вам реакция фотосинтеза.
Таким образом, окружающий нас мир состоит из множества веществ, которые вступают в различные химические реакции. Изучая химические реакции, человек познает сущность процессов, протекающих в живой и неживой природе. Полученные знания помогают более эффективно использовать вещества для получения больших урожаев, выращивания животных, борьбы с различными болезнями. Человечество учится бережно и грамотно относиться к окружающему нас миру.
Полученные знания помогают более эффективно использовать вещества для получения больших урожаев, выращивания животных, борьбы с различными болезнями. Человечество учится бережно и грамотно относиться к окружающему нас миру.
Краткие выводы урока:
- Химические реакции — это явления превращения одних веществ в другие.
- О протекании химических реакций судят по выделению газа, выпадению или исчезновению осадка, изменению цвета, появлению запаха, поглощению или выделению теплоты и излучению света.
- Необходимым условием протекания большинства химических реакций является соприкосновение реагирующих веществ.
Надеюсь урок 10 «Признаки химических реакций» был понятным и познавательным. Если у вас возникли вопросы, пишите их в комментарии.
Урок 11. Химические уравнения →
← Урок 9. Молярная масса и молярный объем
Признаки ржавчины (и причины их возникновения)
Первоначально эта статья была опубликована в марте 2018 года. Ржавчина — одна из неприятных, но неизбежных проблем, связанных с владением автомобилем.
Ржавчина — одна из неприятных, но неизбежных проблем, связанных с владением автомобилем.
Понимание процесса ржавчины, проблемных областей и способов устранения неполадок имеет решающее значение для устранения ржавчины до того, как она станет серьезной проблемой. В этой первой статье мы обсудим виды ржавчины и причины их возникновения.
Типы ржавчины
Ржавчина — это непрофессиональное название «окисление» или разрушение металлов на основе железа. При достаточном времени и воздействии элементов большинство типов железа и стали полностью превращаются в оксид железа в процессе ржавчины. Поскольку эти металлы обычно используются в автомобилях, водителям следует опасаться трех основных типов ржавчины:
1) Поверхностная ржавчина
Первые признаки поверхностной ржавчины обычно появляются на краске. Этот тип ржавчины охотится на небольшие забоины, трещины и царапины. По мере износа прозрачного покрытия ваша краска также становится уязвимой к износу и истиранию. Как только вода проникает в незащищенный металл, он окисляется. Чистое железо и алюминий не окисляются так агрессивно, но сталь имеет примеси в металле, которые ускоряют процесс ржавчины.
Как только вода проникает в незащищенный металл, он окисляется. Чистое железо и алюминий не окисляются так агрессивно, но сталь имеет примеси в металле, которые ускоряют процесс ржавчины.
2) Окалина Ржавчина
Сталь ржавеет с различной скоростью в зависимости от нескольких переменных: компонентов сплава, толщины, окружающей среды, в которой находится сталь, и типа термообработки, которой подвергается сталь. Окалина относится к оксидам железа, которые образуются на кованых или обработанных металлах в результате операций мельницы (обычно в результате высокотемпературной прокатки или обработки в печи). Эти химические процессы портят поверхность и снижают прочность металла, делая его более уязвимым к окислению. Со временем вода может вступить в реакцию с химическими веществами, используемыми при термической обработке, что приведет к образованию накипи. Чешуя обычно твердая, но ломкая и шелушащаяся.
3) Проникающая ржавчина
После длительного воздействия элементов окисленная сталь обычно разлагается до хрупкого оксида железа, что приводит к образованию отверстий в металлических листах. Автопроизводители делают все возможное, чтобы предотвратить этот серьезный тип коррозии, и многие автомобили теперь имеют толстое покрытие на днище, которое химически изолирует сталь от окислителей. Но эти провалы и покрытия со временем стираются, особенно на обочине дороги, где соль и другие элементы вызывают чрезмерный износ металла. Проникающую ржавчину обычно можно предотвратить, если ее обнаружить и вылечить достаточно рано.
Автопроизводители делают все возможное, чтобы предотвратить этот серьезный тип коррозии, и многие автомобили теперь имеют толстое покрытие на днище, которое химически изолирует сталь от окислителей. Но эти провалы и покрытия со временем стираются, особенно на обочине дороги, где соль и другие элементы вызывают чрезмерный износ металла. Проникающую ржавчину обычно можно предотвратить, если ее обнаружить и вылечить достаточно рано.
В V&F
Если не принять меры, пятно ржавчины может быстро вырасти, пока не вызовет структурную проблему. Во многих штатах автомобиль с ржавчиной на кузове не пройдет техосмотр, независимо от того, где расположены пятна и насколько они серьезны.
С 1988 года наш семейный сервисный центр предоставляет высококачественные услуги по ремонту автомобилей в Агаваме, Фидинг-Хиллз, Саутвике, Уэст-Спрингфилде и прилегающих районах Массачусетса. Если ваш автомобиль нуждается в обслуживании или ремонте в зимний сезон, позвоните нам по телефону (413) 314-2280 или запишитесь на прием онлайн.
Распространенные признаки ржавчины и их причины
Если она есть в вашем автомобиле, вы, вероятно, недовольны ею. При отсутствии лечения пятно ржавчины может быстро вырасти и вызвать серьезные структурные проблемы. Во многих штатах автомобиль с ржавчиной на кузове даже не пройдет техосмотр, независимо от того, где расположены пятна и насколько они малы.
Вот почему лучше сразу решать проблему, как только вы ее обнаружите. Понимание процесса ржавчины, хронически проблемных областей и способов решения проблем имеет решающее значение для устранения ржавчины до того, как она станет серьезной проблемой. В этой первой статье мы обсудим виды ржавчины и причины их возникновения.
Что такое ржавчина
Ржавчина — это непрофессиональное название «окисление» или распад металлов на основе железа. При достаточном времени и воздействии элементов большинство типов железа и стали полностью превращаются в оксид железа в процессе ржавчины. К сожалению, в автомобилях чаще всего используются окисляющиеся металлы. Есть три основных типа ржавчины, о которых следует беспокоиться водителям.
К сожалению, в автомобилях чаще всего используются окисляющиеся металлы. Есть три основных типа ржавчины, о которых следует беспокоиться водителям.
Поверхностная ржавчина
Первые признаки поверхностной ржавчины обычно появляются на краске. Этот тип ржавчины охотится на небольшие забоины, трещины и царапины. По мере износа прозрачного покрытия краска также становится уязвимой к износу и истиранию. Как только вода проникает в незащищенный металл, он окисляется. Чистое железо и алюминий не окисляются так агрессивно, но сталь имеет примеси в металле, которые ускоряют процесс ржавчины.
Окалина Ржавчина
Незащищенная сталь ржавеет с разной скоростью в зависимости от нескольких переменных: компонентов сплава, толщины, среды, в которой находится сталь, и типа термообработки, которой подвергается сталь. Окалина относится к оксидам железа, которые образуются на кованых или обработанных металлах в результате операций мельницы (обычно в результате высокотемпературной прокатки или обработки в печи).
