Виды электроды: Виды сварочных электродов. Какие марки применять в конкретном случае
Содержание
Виды электродов таблица — краткое описание, применение
Электроды описание — виды электродов, применение, характеристики
Для удобства предлагаем для клиентов описание видов электродов. В таблице Вы найдете все электроды, которые производятся на заводе сварочных электродов ООО Ватра. У нас Вы можете купить электроды оптом и в розницу по самым низким ценам.
Купить электроды в розницу можно в фирменных магазинах «Эксперт — все для сварки и стройки», по РБ в филиалах (Барановичи, Брест, Витебск, Гомель, Гродно, Могилев, Полоцк, Солигорск и др.) и у партнеров в РФ.
Электроды сварочные собственного производства
| ||||
|
Марка электрода |
Тип Электрода по ГОСТ 9467-45 Гост 9466-75 |
Диаметр, мм |
Род сварочного тока |
Назначение |
|
Электроды для сварки углеродистых сталей рядовых и ответственных конструкций
| ||||
|
МР-3 |
Э46 |
2.  5; 3.0; 4.0 5; 3.0; 4.0
|
Переменный и постоянный обратной полярности |
Рутиловое покрытие. Электроды предназначены для сварки черных металлов. Область применения- строительство и машиностроение. Электроды позволяют выполнять сварку на низких токах, а для электродов малого диаметра-от источников питания, включенных в бытовую сеть. Обеспечивают легкое отделение шлака и хорошее повторное зажигание, равномерное горение дуги в процессе сварки. |
|
ОЗС-12 |
Э46 |
2.5; 3.0; 4.0 |
Переменный и постоянный прямой и обратной полярности | |
|
АНО-21 |
Э46 |
2.5; 3.0; 4.0 |
Постоянный ток любой полярности, переменный от трансформатора с напряжением холостого хода не менее 50В |
Для сварки конструкций из низкоуглеродистых сталей малых толщин марок Ст3, 10, 20 и др.  Электроды обеспечивают легкое зажигание дуги, мелкочешуйчатое формирование металла шва, легкую или самопроизвольную отделяемость шлаковой корки. Они могут применяться для сварки водопроводных труб, газопроводов малого давления. Электроды обеспечивают легкое зажигание дуги, мелкочешуйчатое формирование металла шва, легкую или самопроизвольную отделяемость шлаковой корки. Они могут применяться для сварки водопроводных труб, газопроводов малого давления.
|
|
АНО-36 |
Э46 |
2.5; 3.0; 4.0 |
Переменный и постоянный обратной полярности |
Рутил-целллюлозное покрытие. Предназначены для сварки рядовых и ответственных конструкций из углеродистых сталей, во всех пространственных положениях шва. Также используется для сварки потолочных и вертикальных швов. Для сварки черных металлов. |
|
Электроды для сварки углеродистых сталей особо ответственных конструкций
| ||||
|
УОНИ 13/55 |
Э50А |
2.5; 3.0; 4.0 |
Постоянный ток обратной полярности |
Для сварки ответственных конструкций из углеродистых и низколегированных сталей, когда к металлу сварных швов предъявляются повышенные требования по пластичности, ударной вязкости.  Сварка во всех пространственных положениях, кроме вертикального. Свариваемая поверхность должна быть тщательно очищена от окисов, ржавчины, жиров, влаги, краски и других загрязнений. Сварка во всех пространственных положениях, кроме вертикального. Свариваемая поверхность должна быть тщательно очищена от окисов, ржавчины, жиров, влаги, краски и других загрязнений.
|
|
УОНИ 13/45 |
Э42А |
2.5; 3.0; 4.0 |
Постоянный ток обратной полярности | |
|
ТМУ-21У |
Э50А |
2.5; 3.0; 4.0 |
Постоянный ток обратной полярности | |
|
Электроды наплавочные
| ||||
|
Т-590 |
Э-120Х6С2ГР3 |
2.5; 3.0; 4.0 |
Постоянный ток обратной полярности |
Предназначены для наплавки деталей из стали |
|
ЭН-60 |
Э-70Х3СМТ |
2.  5; 3.0; 4.0 5; 3.0; 4.0
|
Постоянный ток обратной полярности | |
|
Электроды для сварки серого, высокопрочного и ковкого чугуна
| ||||
|
ЦЧ-4В |
ГОСТ 9466-75 |
3.0; 4.0; 5.0 |
Постоянный ток обратной полярности |
Предназначены для холодной сварки или заварки деталей из высокопрочного чугуна. |
|
МНЧ-2 |
ГОСТ 9466-75 |
3.0; 4.0; 5.0 |
Постоянный ток обратной полярности | |
|
Электроды для сварки изделий из коррозионностойких хромоникелевых сталей (электроды для нержавейки)
| ||||
|
ЦЛ-11 |
Э-08Х20Н9Г2Б |
3.  0; 4.0; 5.0 0; 4.0; 5.0
|
Постоянный ток обратной полярности |
Электроды используются для сварки коррозионно- стойких нержавеющих сталей. Сварка во всех пространственных положениях. |
|
ОЗЛ-8 |
Э-07Х20Н9 |
3.0; 4.0; 5.0 |
Постоянный ток обратной полярности | |
|
НЖ-13 |
Э-09Х19Н10Г2М2Б |
3.0; 4.0; 5.0 |
Постоянный ток обратной полярности | |
|
Электроды для сварки разнородных сталей (нержавейка+сталь)
| ||||
|
ОЗЛ-6 |
Э-10Х25Н13Г2 |
3.0; 4.0 |
Постоянный ток обратной полярности |
Данные электроды используются для сварки разнородных жаропростойких сталей.  Сварка во всех пространственных положениях. Сварка во всех пространственных положениях.
|
|
ОЗЛ-9А |
Э-28Х24Н16Г6 |
3.0; 4.0 |
Постоянный ток обратной полярности | |
|
ОЗЛ-17У |
ГОСТ 9466-75 |
3.0; 4.0 |
Постоянный ток обратной полярности | |
|
ОЗЛ-25Б |
Э-10Х20Н70Г2М2Б2В |
3.0; 4.0 |
Постоянный ток обратной полярности | |
|
ЦТ-15 |
Э-08Х19Н10Г2Б |
3.0; 4.0 |
Постоянный ток обратной полярности | |
|
ЭА-395/9 |
Э-11Х15Н25М6АГ2 |
3.0; 4.0 |
Постоянный ток обратной полярности | |
|
ЭА-400/10У |
Э-07Х19Н11МГ2Ф |
3.  0; 4.0 0; 4.0
|
Постоянный ток обратной полярности | |
Виды электродов с покрытием и их применение
Главная |
Статьи |
Виды электродов с покрытием и их применение
Ассортимент плавящихся электродов с покрытием для ручной сварки довольно разнообразен. Все разновидности выпускаемой продукции имеют вид прутков. Все они обладают достоинствами и недостатками и подбираются в зависимости от условий работы и требуемого результата.
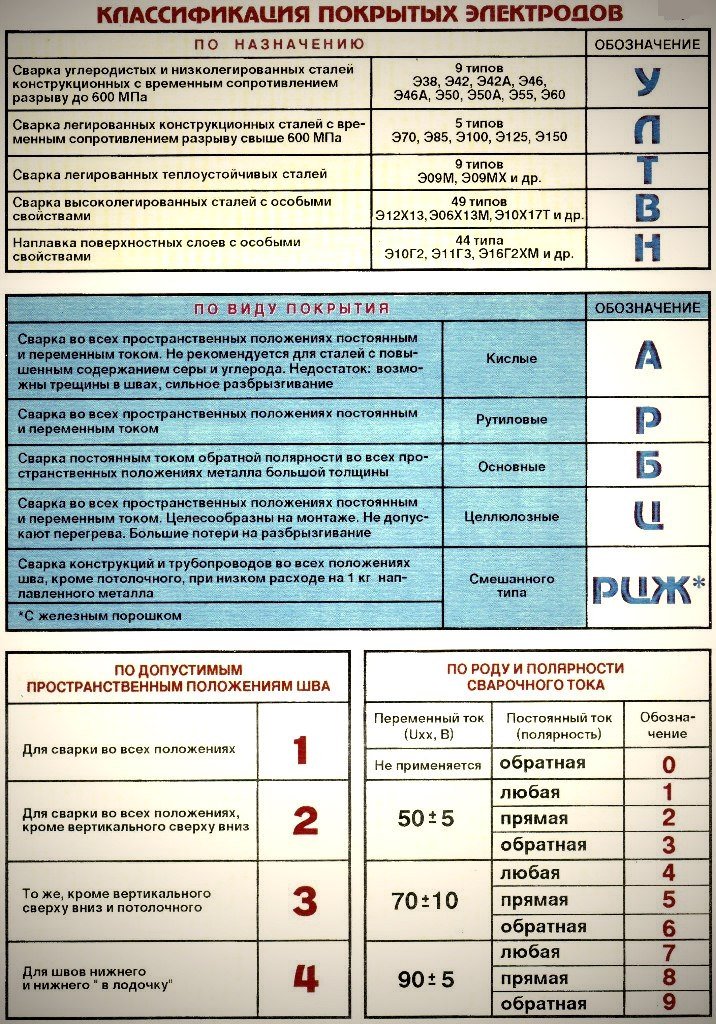
Согласно ГОСТу и ISO, электроды подразделяются по составу покрытия на несколько групп. По названию каждой группы можно определить, какие именно компоненты преобладают. Разбираясь в маркировке и обладая необходимыми знаниями, можно добиться высокого качества шва и прочности соединения.
ВИДЫ ПОКРЫТИЙ И ИХ МАРКИРОВКА
Кислые покрытия (А) состоят в основном из шлакообразующих оксидов железа, марганца, кремния, с небольшим включением оксида алюминия. Газообразующими добавками служат органические вещества, например, крахмал или целлюлоза, а связующим — жидкое стекло. Образующийся при плавлении шлак имеет характерные кислотные свойства, что и дало название этой группе.
Газообразующими добавками служат органические вещества, например, крахмал или целлюлоза, а связующим — жидкое стекло. Образующийся при плавлении шлак имеет характерные кислотные свойства, что и дало название этой группе.
Главными компонентами основных или щелочных покрытий (Б) являются мрамор и плавиковый шпат, в состав которых входят кальций и фтор. Для образования при сварке шлака вводятся рутил и кварцевый песок. При разложении мрамора выделяется углекислый газ, защищающий дугу и сварочную ванну от попадания воздуха. Для стабильности горения применяются добавки карбонатов и щелочных металлов. Этот вид покрытий называется основным, так как в результате плавления образуется шлак с ярко выраженными основными свойствами.
В составе целлюлозных покрытий (Ц) содержится более 50 % целлюлозы и других органических компонентов, служащих для газообразования. В процессе сварки выделяется окись углерода и водород.
Рутиловые покрытия (Р) на 50 % и более состоят из оксида титана — рутила, который является шлакообразующим веществом. В качестве добавок используются карбонаты, полевой шпат, каолин. Рутиловые составы могут применяться в смеси с любыми другими видами покрытий. Получающаяся в результате этого продукция маркируется двумя буквами в соответствии с компонентами: АР, РБ, РЦ. К рутилу также добавляют порошкообразное железо. Такое покрытие маркируется буквами РЖ.
В качестве добавок используются карбонаты, полевой шпат, каолин. Рутиловые составы могут применяться в смеси с любыми другими видами покрытий. Получающаяся в результате этого продукция маркируется двумя буквами в соответствии с компонентами: АР, РБ, РЦ. К рутилу также добавляют порошкообразное железо. Такое покрытие маркируется буквами РЖ.
ПРЕИМУЩЕСТВА ЭЛЕКТРОДОВ С ПОКРЫТИЕМ И ИХ ПРИМЕНЕНИЕ
Электроды с кислым покрытием (А) не имеют в составе дорогостоящих компонентов. Они характеризуются стабильным горением дуги и подходят для сварки как постоянным, так и переменным током. Кислое покрытие обладает стойкостью к увлажнению и прочностью к механическому воздействию. К недостаткам продукции этого вида относят разбрызгивание металла и повышенное выделение токсинов, вызывающих силикоз. Образующийся шов имеет невысокую пластичность и склонность к старению. По механическим характеристикам он сопоставим с марками кипящей стали невысокой прочности. Этот вид электродов не подходит для сварки высоколегированной стали и стали с высоким содержанием углерода и серы. Они применяются для конструкций с невысокой нагрузкой.
Они применяются для конструкций с невысокой нагрузкой.
Электроды с щелочным покрытием (Б) позволяют получить шов, сопоставимый по свойствам со спокойной сталью с повышенными механическими характеристиками и пластичностью. При необходимости в покрытие можно добавлять легирующие компоненты для придания соединению особых свойств. Электродами удобно работать в любом пространственном положении. Лучше всего основные электроды подходят для сварки постоянным током. Для работы с аппаратами на переменном токе выпускается продукция с сильными стабилизирующими компонентами. Без них постоянной дуги добиться сложно. Основные покрытия гигроскопичны, поэтому эти электроды требуют соблюдения правил хранения. В их состав входят дорогостоящие компоненты, что отражается на цене. Электроды применяются при сварке ответственных конструкций, для получения жестких соединений. Они подходят для работы с углеродистой и легированной сталью.
Электроды с целлюлозным покрытием (Ц) характеризуются стабильностью дуги и подходят для работы на любом токе и во всех пространственных положениях. Этот вид продукции предпочтителен для сваривания тонколистовых деталей. При этом нужно учесть, что покрытие не обеспечивает достаточной защиты от воздуха и отличается высоким влагопоглощением. Металл при сварке сильно разбрызгивается. Электроды с целлюлозным покрытием востребованы для работ на газонефтепроводах.
Этот вид продукции предпочтителен для сваривания тонколистовых деталей. При этом нужно учесть, что покрытие не обеспечивает достаточной защиты от воздуха и отличается высоким влагопоглощением. Металл при сварке сильно разбрызгивается. Электроды с целлюлозным покрытием востребованы для работ на газонефтепроводах.
Рутиловое покрытие (Р) не выделяет токсичных веществ и поддерживает стабильную дугу при любом токе. Металл при сварке не разбрызгивается, а шов образует плавный переход к свариваемым деталям. Прочность соединения выше, чем при работе с кислым электродом, но и стоит рутиловая продукция дороже. Применяют ее для сварки низколегированной стали. Для повышения прочности шва без излишних затрат для работы используют электроды с кисло-рутиловым покрытием (АР).
Газовый электрод, электрод из металлической соли и т. д.
Наука > Химия > Электрохимия > Типы электродов
В этой статье мы изучим различные типы электродов, их представление, написание клеточных реакций и нахождение ЭДС. клетки.
клетки.
Есть
четыре типа электродов
- Газовые электроды
- Электроды на основе малорастворимых солей металлов
- Металло-ионные электроды
- Редокс-электроды
Газовые электроды:
Газовый электрод состоит из газа (например, h3, Cl2, O2), находящегося в контакте с раствором, содержащим ионы, образующиеся из газа, напр. Н+, Cl-, ОН-. Потенциал газового электрода зависит от концентрации его ионов в растворе и давления газа.
Газовый электрод состоит из газа, барботируемого вокруг инертной металлической проволоки (платинированный платиновый электрод), погруженной в раствор, содержащий ионы, с которыми газ необратим. Платина используется в качестве проводника и для адсорбции газа. например Стандартный водородный электрод.
Примеры газовых электродов:
Стандартный водородный электрод (SHE):
SHE is
представлен как
Pt| H 2(г) (1 атм.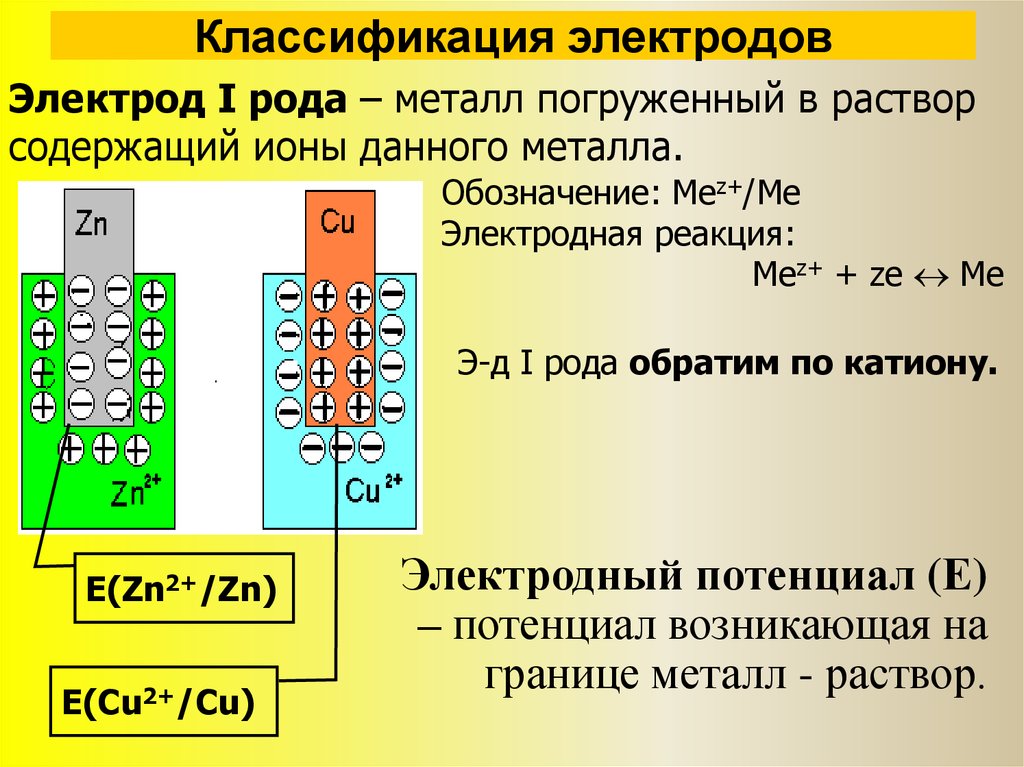 )| H + (водный)
)| H + (водный)
(1 м)
Половинка
клеточные реакции:
H 2(g) → 2H + (водн.) + 2e –
(окисление) (L.H.S.)
2H + (водн.) + 2e – → H 2(g)
(уменьшение) (правая сторона)
Потенциалу электрода произвольно присваивается нуль. Этот
электрод катионный электрод.
Электрод для газообразного хлора:
Этот
электрод — анионный электрод. Хлоргазовый электрод представлен
как,
Pt| Cl 2(г) (1 атм.)| Cl – (водный)
(1 м)
Половинка
клеточные реакции:
2Cl – (водн.) → Cl 2(г) + 2e –
(окисление) (Л.В.С.)
Cl 2(г) + 2e – → 2Cl – (водн.)
(восстановление) (R.H.S.)
Кислородный электрод:
Кислородный газ
электрод представлен как,
Pt | O 2(г) (1 атм)| ОН – (водный)
(1M)
Половинка
реакция клетки
4OH – → 2H 2 O+ O 2(g) + 4e –
(окисление) (Л. В.С.)
В.С.)
2H 2 O + O 2(g) + 4e – →
4OH – (восстановление) (R.H.S.)
Электрод на основе малорастворимой соли металла:
Реверсивный
анионный электрод также называют металл-умеренно растворимой солью металла.
электрод. В этом электроде металл, малорастворимая соль металла в
равновесие с раствором, содержащим тот же анион, что и труднорастворимый
соль. например Каломельный электрод.
Металлоионные электроды:
В этом случае металлическая полоса находится в контакте с раствором водорастворимого солевого катиона того же металла.
напр. Zn (с) |
Zn ++ (водный)
В
в электрохимической ячейке электрод с более высоким потенциалом окисления подвергается
окисления и действует как анод или отрицательный электрод и электрод, имеющий
меньший потенциал окисления подвергается восстановлению и действует как катод или
положительный электрод.
Примеры электродов металл-ионы металла:
Zn (s) | Zn ++ (водный)
Zn (s) → Zn ++ (водн.) +
2e – (Окисление)
Zn ++ (водн.) + 2e – → Zn (s)
(Сокращение)
Cu (s) | Cu ++ (водн.)
Cu (тв.) → Cu ++ (водн.) +
2e – (Окисление)
Cu ++ (водн.) + 2e – → Cu (s)
(Уменьшение)
Окислительно-восстановительный электрод:
В этих
электродов инертный металл типа Pt погружают в раствор, содержащий ионы
активный металл в двух различных степенях окисления.
Пл | Fe 2+ , Fe 3+
Fe 2+ → Fe 3+
e – (Окисление)
Fe +++ + e –
→ Fe ++ (восстановление)
Pt | Сн 2+ , Сн 4+
Sn 2+ → Sn 4+ +
2e – (Окисление)
Sn 4+ + 2e – →
Sn 2+ (Редукция)
Запись клеточной реакции и нахождение Э. Д.С. ячейки:
Д.С. ячейки:
Окислительно-восстановительный потенциал:
Потенциал, возникающий благодаря способности ионов терять или приобретать электроны, образуя более высокую или более низкую стабильную степень окисления, называется окислительно-восстановительным потенциалом.
Редокс
потенциал зависит от соотношения концентраций двух типов ионов.
Пт | Fe 2+ (водн.) (1M), Fe 3+ (водн.) (1M) E 2 ox =
– 0,771 В
Представление ячеек, содержащих стандарт и эталон
электроды:
А ячейка
состоит из контакта цинкового стержня с 1-молярным раствором иона цинка и насыщенного
каломельный электрод.
Zn (с) | Zn 2+ (1M) || KCl (водный) (насыщенный) |
Hg 2 Cl 2(s) |Hg (л) , тел +
Ячейка состоит из SHE и насыщенного каломельного электрода
Pt | H 2(г) (1 атм)| H + (водный)
(1М) || KCl (водн. ) (насыщенный)|Hg 2 Cl 2(тв) | рт.ст. (л)
) (насыщенный)|Hg 2 Cl 2(тв) | рт.ст. (л)
,Pt +
Реакции ячеек:
Шаги для записи реакции ячейки гальванического элемента:
- Представьте данный гальванический элемент со стандартным соглашением.
- Электрод в левой части изображения показывает, что он является анодом и на этом электроде происходит окисление. Напишите для него реакцию полуклеточного окисления полуклеточную реакцию.
- Электрод в правой части изображения показывает, что он является катодом и на этом электроде происходит восстановление. Напишите для него полуклеточную реакцию восстановления полуклеточной реакции.
- Баланс выше двух реакций для электронов для реакции окисления и восстановления.
- Добавьте две реакции и получите чистую (общую) клеточную реакцию.
Шаг
– 1: Представьте ячейку условно:
Pb (s) | Pb 2+ (водн. ) (1M)
) (1M)
|| Ag + (водн.) (1M)| Ag (s) +
Шаг
– 2: Напишите реакцию полуэлемента слева: Pb(s) находится в левой части изображения.
что это анод, и окисление происходит на Pb(s) электроде.
Pb (т) → Pb 2+ (водн.)
+ 2e – (Окисление) … (1)
Шаг
– 3: Напишите реакцию правой половины ячейки: Ag (s) находится в правой части представления
показывает, что это катод и восстановление происходит при Ag (с)
электрод.
Ag + (водный) + e –
→ Ag (s) (Сокращение) … (2)
Шаг
– 4: Сбалансируйте электроны двух вышеуказанных реакций половинной ячейки:
Умножьте уравнение (2) на 2, чтобы сбалансировать электроны.
2Ag + (водный) + 2e –
→ 2Ag (s) (Сокращение) … (2)
Шаг
– 5: Складывая уравнения (1) и (3), получаем
общая реакция.
Pb (т) + Ag + (водн.)
→ Pb 2+ (водн.) + Ag (s)
Действия по нахождению ЭДС. гальванического элемента:
- Представление данного гальванического элемента в соответствии со стандартными условными обозначениями.
- Электрод в левой части изображения показывает, что он является анодом и на этом электроде происходит окисление.
- Электрод в правой части изображения показывает, что он является катодом и на этом электроде происходит восстановление.
- Получите стандартные значения потенциала окисления из электродвижущего ряда для материала катода и анода.
- Используйте следующую формулу для расчета Э.Д.С. клетки.
E o Ячейка = E o (вол/катод)
– E o (вол/анод)
ИЛИ
E o Ячейка = E o (вол/катод) +
E или (красный/анод)
Чтобы найти э. д.с. Daniel Cell:
д.с. Daniel Cell:
Шаг
– 1: представить ячейку условно
Шаг
– 2: Определите анод и катод: Pb(s) является
в левой части изображения видно, что это анод и окисление
происходит на Pb(s) электроде. Ag(s) находится на правой стороне
изображении видно, что это катод и восстановление происходит при
Ag(s) электрод.
Шаг
– 3: Получить значения потенциала окисления или
восстановительный потенциал для электродов из электрохимической серии
E o (ox/Zn) = 0,76 В и EE o (ox/Cu)
=-0,34 В
Шаг
– 4: рассчитать ЭДС ячейки:
E o Cell = E o (вол/катод)
– E (окс/анод)
E o Ячейка = E o (ox/Zn)
– E o (ox/Cu)
E o Ячейка
= 0,76 – (- 0,34)
E o Ячейка =
0,76 +0,34
E O Cell = 1,1 В
Предыдущая тема: Электроды справки
Следующая тема: Теория Nersnt of Electrode Потенциал
Следующая Отделение:
наука> Химикация> Электрохма
. Типы электродов
Типы электродов
Сколько типов электродов у нас есть?
15 января 2021 г. 15 января 2021 г.
| 10:06
Электрод является жизненно важным компонентом электрохимических элементов. Это точка, в которой ток входит и выходит из электролита. Точка, в которой ток покидает электроды, называется катодом. Точка, куда входит ток, называется анодом. Эти электроды доступны в различных типах, например:
Газовые электроды:
Газовый электрод включает различные газы, такие как h3, Cl2 и O2, в контакте с раствором, содержащим ионы, получаемые из газа, такого как H+, Cl-, OH -. Потенциал газового электрода зависит от интенсивности его ионов в растворе и силы газа. Газовый электрод барботирует газ вокруг инертной металлической проволоки, включенной в раствор, содержащий ионы, с которыми газ постоянен.
Электрод на основе малорастворимой соли металла:
Электрод на основе малорастворимой соли металла также известен как обратимый анионный электрод. В электроде этого типа металл и труднорастворимая соль металла находятся в равных пропорциях с раствором, содержащим тот же анион, что и труднорастворимая соль.
В электроде этого типа металл и труднорастворимая соль металла находятся в равных пропорциях с раствором, содержащим тот же анион, что и труднорастворимая соль.
Электроды металл-металл-ион:
В этом случае кусок металла помещают в раствор водорастворимого катиона, несущего соль соответствующего металла. В электрохимической ячейке электрод с более высоким окислительным потенциалом подвергается окислению и служит анодом/отрицательным электродом. Электрод с более низким потенциалом окисления испытывает потери и действует как катод/положительный электрод.
Каломельный электрод:
Исходный электрод, содержащий молекулы ртути и хлорида ртути. Он изготовлен из жидкой элементарной ртути и твердой пасты Hg2Cl2, соединенной со стержнем, покрытым насыщенным раствором KCl. Необходимо использовать насыщенный раствор, так как это обеспечивает действие хлорида калия и минимальное напряжение, более похожее на стандартный водородный электрод, т. е. СВЭ. Этот насыщенный раствор позволяет осуществить перенос ионов хлора.
Серебряно-хлоридный электрод:
Электрод этого типа прессует соль в растворе, который связывается с результатом электрода. Этот электрод содержит твердое серебро и осажденную соль AgCl. Это обычно используемый электрод сравнения, потому что он разумен и не очень токсичен. Электрод из хлорида серебра-серебра изготавливается с использованием нити из твердого серебра и путем кодирования его в AgCl. Затем его помещают в пробирку с раствором AgCl и KCl. Это позволяет ионам образовываться по мере движения электронов в систему электродов и из нее.
pH-электрод:
Пожалуй, самый полезный и надежный способ определения pH — использование стеклянного электрода. рН-электрод зависит от ионного обмена в гидратированных слоях, построенных снаружи стеклянного электрода. Стекло состоит из силикатной сетки, в которой ионы металла координированы с частицей кислорода, и именно ионы металла взаимодействуют с H+. Стеклянный электрод действует как батарея, напряжение которой зависит от движения H+ в растворе, в котором он находится.
Ионоселективные электроды:
Ионоселективный электрод реагирует на действие селективного иона. Предположим, что некоторые из атомов несвободны и сохраняются в виде компактной структуры или необъяснимого осадка. В этом случае эти электроды обеспечат гораздо более низкие показания, чем метод, который идентифицирует все присутствующие ионы. Обычно используются ионоселективные электроды K+, Ca2+ и NO-3. Возможно, что электрод является ионоселективным, но он не будет ионоселективным.
Газочувствительные электроды:
Они обычно используются для определения интенсивности газа путем его взаимодействия с тонким слоем, окружающим ион-чувствительный электрод, обычно pH-электрод. Диоксид серы, диоксид углерода и аммиак можно измерить по их растворению в тонком слое, окружающем pH-электрод и содержащем результирующий pH покрытия.
Кислородный электрод Кларка:
Этот электрод состоит из платинового катода и серебряного анода, включенных в один и тот же раствор насыщенного хлорида калия и изолированных от исследуемого раствора кислородно-пористой пленкой.
