Химическая коррозия и электрохимическая коррозия: Чем химическая коррозия отличается от электрохимической?
Содержание
Чем химическая коррозия отличается от электрохимической?
От латинского слова corrosio, означающего «разъедание», образовано всем известное понятие коррозии, означающим самопроизвольное разрушение материала при взаимодействии с контактирующей с ним средой.
Влиянию коррозии подвержены не только металлы, но и полимеры (старение полимеров), керамика и даже деревянные материалы.
Контактирующая с веществами окружающая среда вносит свою специфику во взаимодействие с ними, по типу взаимодействия выделяют многочисленные разновидности процессов разрушения, включая электрохимическую коррозию металлоконструкций или химическую коррозию.
Реакции корродирования обусловлены возникновением окислительно-восстановительных реакций вещества с контактирующей с ним средой, необходимых для перехода вещества в наиболее устойчивое термодинамическое состояние.
Классификация процессов корродирования
Многообразие сред и условий протекания коррозионных процессов не позволяет создать всеобъемлющую и единую систему классификации встречающихся коррозий.
Основными критериями разделения коррозионных разновидностей в настоящее время являются:
- Степень агрессивности среды, в которой происходит процесс коррозионного разрушения;
- Условия протекания коррозионных реакций;
- Локальность коррозионных изменений, связанная с корродированием отдельных участков;
- Характер разрушений рабочей поверхности металлоконструкции;
- Механизм процесса корродирования, согласно которому принято выделять:
- химическую и
- электрохимическую коррозии.
Чем химическая коррозия отличается от электрохимической?
Коррозия химическая и электрохимическая принципиально отличаются друг от друга по виду взаимодействия вещества с контактирующей средой, длительности процесса и по конечному результату взаимодействия.
- Химическая коррозия происходит в обезвоженной среде, то есть при полном отсутствии влаги. Результатом коррозии химической для металлоконструкций являются образовавшиеся оксиды металлов.
 Оксиды создают пленку толщиной не более двух периодов кристаллической решетки, но этого оказывается достаточно, чтобы изолировать основной металл от кислорода контактирующей среды и воспрепятствовать дальнейшему окислению.
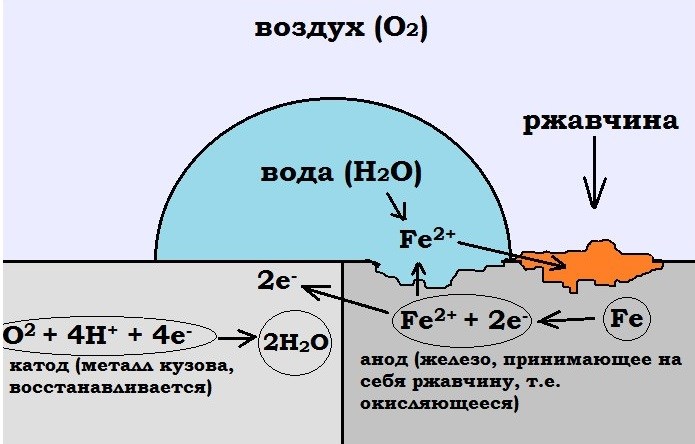
Оксиды создают пленку толщиной не более двух периодов кристаллической решетки, но этого оказывается достаточно, чтобы изолировать основной металл от кислорода контактирующей среды и воспрепятствовать дальнейшему окислению. - Реакции электрохимической коррозии обязательно происходят в электролитной среде и относятся к анодно-катодным взаимодействиям. Это могут быть водные растворы, а также иная среда, содержащая влагу, например, обыкновенная атмосфера. Ионы металла поверхностного слоя материала, имеющие положительный заряд, отрываются молекулами воды, в результате основной металл обретает избыточное количество оставшихся электронов и заряжается отрицательно. Слой воды, граничащий с металлом, за счет приобретенных ионов, отданных металлом, заряжается положительно. Граничный слой воды с металлом приобретает скачок потенциала, обусловленный разностью зарядов. Примером электрохимических реакций корродирования являются разрушающие факторы для металлоконструкций, эксплуатируемых в воде или в сырой атмосфере, при воздействии охлаждающих эмульсий и жидкостей, используемых при мехобработке металлов, образование накипи при использовании магниевых анодов в электрических бойлерах.

Немного подробнее об электрохимическом корродировании металлоконструкций
Электрохимическая коррозия металлов – самый распространенный вид коррозионного разрушения, представляющий собой разрушение металлов в электролитных средах, с созданием в системе направленного движения электронов и ионов.
На поверхности и в граничном со средой слое металла одновременно происходят анодная и катодная реакции, в ходе которых происходят:
- Анодное окисление метала;
- Катодное восстановление водорода или кислорода.
Это важно! Не следует относить к электрохимической коррозии корродирование однородных материалов, например, всем известное ржавление железа. Для протекания электрохимических коррозионных разрушений всегда необходимо присутствие электролита. Ими могут оказаться дождевая вода, конденсат, с которыми происходит соприкосновение структурных элементов материала или двух различных контактирующих веществ, имеющих различные по величине окислительно-восстановительные потенциалы.
Основные методы защиты металлов от электрохимических коррозионных разрушений
Защита металлоконструкций базируется на целенаправленных воздействиях, частично снижающих или полностью предотвращающих активность факторов, провоцирующих развитие коррозионных процессов. Защитные мероприятия однозначно разделены на три категории:
- Воздействие на конструкционный материал, которое на практике чаще всего выражается нанесением защитных и изолирующих покрытий;
- Воздействие на контактирующую с металлоконструкцией среду, на практике это методы ингибирования воды или ее деаэрации;
- Комбинированные мероприятия.
Наиболее доступные и широко применяемые из методов защиты:
- Легирование металла, основанное на внедрении в сплав компонентов на основе вольфрама, хрома или никеля, провоцирующих образование устойчивых оксидных пленок, тем самым вызывающих пассивность конструкционного металла к коррозионному разрушению;
- Покрытия конструкционного металла;
- Электрохимическая защита от коррозии, базирующаяся на использовании торможения коррозионных реакций путем присоединения к защищаемой металлоконструкции элементов с более высоким значением отрицательного потенциала электрода;
- Подщелачивание коррозионной среды или ее деаэрация с целью снижения концентрации водородных ионов.
Коррозия металлов — что это такое? Виды и примеры
Коротко о главном
Коррозия металлов или ржавление в химии — это явление, которое возникает из-за взаимодействия металлической пластинки с веществами окружающей среды (кислородом воздуха или кислотами, с которыми может реагировать металлическое изделие).
Обычно окисляются металлы, включая железо, которые находятся левее водорода в ряду напряжений.
Чаще всего встречаются химическая и электрохимическая коррозии. Чтобы понять, чем они отличаются друг от друга, давайте сравним их по нескольким критериям в таблице ниже.
Таблица 1. Сравнение химической и электрохимической коррозии металлов | ||
|---|---|---|
Признаки сравнения | Химическая коррозия | Электрохимическая коррозия |
Определение | Разрушение металлов в из-за взаимодействия с газами или растворами, которые не проводят электрический ток | Разрушение металла, при котором возникает электрический ток в воде или среде другого электролита |
Агрессивные реагенты | O2, пары H2O, CO2, SO2, Cl2 | Растворы электролитов |
Примеры | 3Fe + 2O2 → Fe3O4 | 4Fe + 3O2 + 6H2O = 4 Fe(OH)3 При контакте железа с цинком коррозии подвергается цинк: А (+) на цинке: Zn0 — 2e— = Zn2+. К (–) на железе: 2H+ + 2e— = H2. |
Защитить металл от коррозии можно по-разному: покрытием защитными материалами, электрохимическими методами, шлифованием и т. д. Далее — подробно обо всем этом.
Практикующий детский психолог Екатерина Мурашова
Бесплатный курс для современных мам и пап от Екатерины Мурашовой. Запишитесь и участвуйте в розыгрыше 8 уроков
Что такое коррозия
Коррозия — это самопроизвольное разрушение элементов, чаще всего металлов, под действием химического или физико-химического влияния окружающей среды.
Иными словами, из-за химического воздействия железо начинает ржаветь. Это весьма сложный процесс, который состоит из несколько этапов. Но суммарное уравнение коррозии выглядит так:
4Fe + 6H2O (влага) + 3O2 (воздух) = 4Fe(OH)3.
Часто под коррозией понимают химическую реакцию между материалом и средой либо между их компонентами, которая протекает на границе раздела фаз. Обычно это окисление металла. Например:
Обычно это окисление металла. Например:
3Fe + 2О2 = Fe3O4;
Fe + H2SO4 = FeSО4 + Н2.
Некоторые металлы, даже активные, покрываются плотной оксидной пленкой при коррозии. Это одна из их характерных черт. Оксидная пленка не дает окислителям проникнуть в более глубокий слой и поэтому защищает металл от коррозии. Алюминий обычно устойчив при контакте с воздухом и водой, даже горячей. Тем не менее, если поверхность алюминия покрыть ртутью, то образуется амальгама. Она разрушает оксидную пленку, и алюминий начинает быстро превращаться в белые хлопья метагидроксида алюминия:
Коррозии подвергаются и многие малоактивные металлы. Например, поверхность медного изделия покрывается патиной — зеленоватым налетом. Это происходит потому, что на ней образуются смеси основных солей.
Виды коррозии металлов
Химическая коррозия
Химическая коррозия — это процесс разрушения металла, который связан с реакцией между металлом и коррозионной средой.
Химическая коррозия протекает без воздействия электрического тока, и в результате этой реакции металлы окисляются. Этот вид коррозии можно разделить на два подвида:
Их них более распространенной считают газовую коррозию. Она протекает во время прямого контакта твердого тела с активным газом воздуха. Чаще всего это кислород. В результате на поверхности тела образуется пленка продуктов химической реакции между веществом и газом. Дальше эта пленка мешает контакту корродирующего материала с газом. При высоких температурах газовая коррозия развивается интенсивно. Возникшая при этом пленка называется окалиной, которая со временем становится толще.
Важную роль в процессе коррозии играет состав газовой среды. Но для каждого металла он индивидуален и изменяется с переменой температур.
Электрохимическая коррозия
Электрохимическая коррозия — это разрушение металла, которое протекает при его взаимодействии с окружающей средой электролита.
Этот вид коррозии считают наиболее распространенным. Самым важным происхождением электрохимической коррозии является то, что металл неустойчив в окружающей среде с точки зрения термодинамики. Вот несколько ярких примеров этой реакции: ржавчина в трубопроводе, на обшивке днища морского судна и на различных металлоконструкциях в атмосфере.
Самым важным происхождением электрохимической коррозии является то, что металл неустойчив в окружающей среде с точки зрения термодинамики. Вот несколько ярких примеров этой реакции: ржавчина в трубопроводе, на обшивке днища морского судна и на различных металлоконструкциях в атмосфере.
В механизме электрохимической коррозии обычно выделяют два направления: гомогенное и гетерогенное. Разберем их подробнее в таблице ниже.
Гомогенный механизм электрохимической коррозии | Гетерогенный механизм электрохимической коррозии |
|---|---|
Поверхность металла рассматривается как однородный слой. | У твердых металлов поверхность неоднородна из-за структуры сплава, в котором атомы по-разному расположены в кристаллической решетке. |
Растворение металла происходит из-за термодинамической возможности для катодного или анодного процессов. | Неоднородность можно наблюдать при наличии в сплаве каких-либо включений. |
Скорость, с которой протекает электрохимическая коррозия, зависит от времени протекания процесса. |
В электрохимической коррозии протекает одновременно два процесса на аноде и на катоде, которые зависят друг от друга. Растворение основного металла происходит только на анодах. Анодный процесс заключается в том, что ионы металла отрываются и переходят в раствор:
Fe → Fe2+ + 2e.
В результате происходит реакция окисления металла. В данном случае анод заряжается отрицательно.
При катодном процессе избыточные электроны переходят в молекулы или атомы электролита, которые, в свою очередь, восстанавливаются. На катоде идет реакция восстановления. Он носит заряд положительного электрода.
O2 + 2H2O + 4e → 4OH—
2H+ + 2e → H2
Торможение одного процесса приводит к торможению и другого процесса.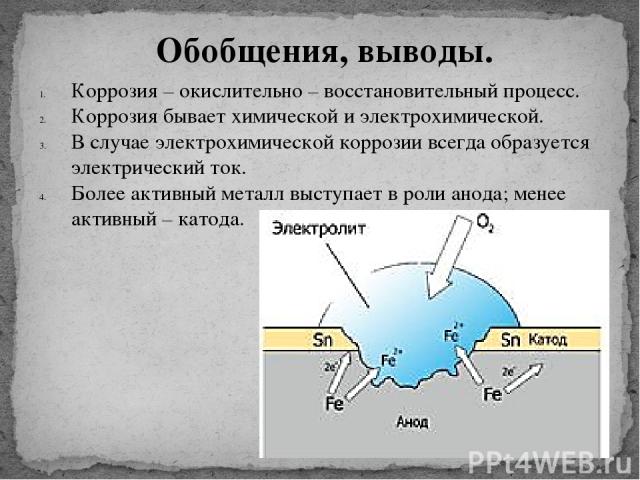 Окисление металла может происходить только в анодном процессе.
Окисление металла может происходить только в анодном процессе.
Учёба без слёз (бесплатный гайд для родителей)
Пошаговый гайд от Екатерины Мурашовой о том, как перестать делать уроки за ребёнка и выстроить здоровые отношения с учёбой.
Как защитить металлы от коррозии
От коррозии можно и нужно защищаться. Чтобы уберечь металлы от этой реакции, их покрывают защитными материалами, обрабатывают электрохимическими методами, шлифованием и т. д. Рассмотрим все эти способы подробнее.
Способ № 1. Защитные покрытия.
Для защиты от коррозии металлические изделия покрывают другим металлом, т. е. производят никелирование, хромирование, цинкование, лужение и т. д. Еще один вариант защиты — покрыть поверхность металла специальными лаками, красками, эмалями.
Способ № 2. Легирование.
Легирование — это введение добавок, которые образуют защитный слой на поверхности металла. Например, при легировании железа хромом и никелем получают нержавеющую сталь.
Способ № 3. Протекторная защита.
Протекторная защита — это способ уберечь металл от коррозии, при котором металлическое изделие соединяют с более активным металлом. Этот второй металл в итоге и разрушается в первую очередь.
Способ № 4. Электрохимическая защита.
Чтобы защитить металлы от электрохимической коррозии, нейтрализуют ток, который возникает при ней. Это делают с помощью постоянного тока, который пропускают в обратном направлении.
Способ № 5. Изменение состава среды путем добавления ингибиторов.
Для защиты от коррозии используют специальные средства, которые ее замедляют — ингибиторы. Они изменяют состояние поверхности металла — образуют труднорастворимые соединения с катионами металла. Защитные слои, образованные ингибиторами, всегда тоньше наносимых покрытий.
Способ № 6. Замена корродирующего металла на другие материалы: керамику и пластмассу.
Способ № 7. Шлифование поверхностей изделия.
Шлифование поверхностей изделия.
Проверьте себя
Что такое коррозия?
Где в повседневной жизни можно встретить ржавление железа и других металлов? Приведите примеры.
Гидроксид железа Fe(OH)3 называют:
а ржавчина;
б) окалина;
в) патина.
Что является причиной возникновения коррозии?
Чем отличаются химический и электрохимический типы коррозии?
Что такое коррозионная среда?
Узнайте все о коррозии металлов и разберитесь в других темах за 9 класс на онлайн-курсах по химии в Skysmart! Наши преподаватели помогут выяснить, где скрываются пробелы в знаниях, и восполнить их. Никаких скучных задач и сухих лекций — только интерактивные упражнения, опыты и теория простым языком. Все это поможет разобраться даже в тех темах, которые не давались в школе. Ждем на бесплатном вводном уроке!
Коррозия металлов и способы защиты от неё
Коррозия – разрушение поверхности сталей и сплавов под воздействием различных физико-химических факторов – наносит огромный ущерб деталям и металлоконструкциям. Ежегодно этот невидимый враг «съедает» около 13 млн. т металла. Для сравнения – металлургическая промышленность стран Евросоюза в прошлом, 2014 году произвела всего на 0,5 млн. тонн больше. И это только – прямые потери. А длительная эксплуатация стальных изделий без их эффективной защиты от коррозии вообще невозможна.
Ежегодно этот невидимый враг «съедает» около 13 млн. т металла. Для сравнения – металлургическая промышленность стран Евросоюза в прошлом, 2014 году произвела всего на 0,5 млн. тонн больше. И это только – прямые потери. А длительная эксплуатация стальных изделий без их эффективной защиты от коррозии вообще невозможна.
Что такое коррозия и её разновидности
Основной причиной интенсивного окисления поверхности металлов (что и является основной причиной коррозии) являются:
- Повышенная влажность окружающей среды.
- Наличие блуждающих токов.
- Неблагоприятный состав атмосферы.
Соответственно этому различают химическую, трибохимическую и электрохимическую природу коррозии. Именно они в совокупности своего влияния и разрушают основную массу металла.
Химическая коррозия
Такой вид коррозии обусловлен активным окислением поверхности металла во влажной среде. Безусловным лидером тут является сталь (исключая нержавеющую). Железо, являясь основным компонентом стали, при взаимодействии с кислородом образует три вида окислов: FeO, Fe2O3 и Fe3O4. Основная неприятность заключается в том, что определённому диапазону внешних температур соответствует свой окисел, поэтому практическая защита стали от коррозии наблюдается только при температурах выше 10000С, когда толстая плёнка высокотемпературного оксида FeO сама начинает предохранять металл от последующего образования ржавчины. Это процесс называется воронением, и активно применяется в технике для защиты поверхности стальных изделий. Но это – частный случай, и таким способом активно защищать металл от коррозии в большинстве случаев невозможно.
Безусловным лидером тут является сталь (исключая нержавеющую). Железо, являясь основным компонентом стали, при взаимодействии с кислородом образует три вида окислов: FeO, Fe2O3 и Fe3O4. Основная неприятность заключается в том, что определённому диапазону внешних температур соответствует свой окисел, поэтому практическая защита стали от коррозии наблюдается только при температурах выше 10000С, когда толстая плёнка высокотемпературного оксида FeO сама начинает предохранять металл от последующего образования ржавчины. Это процесс называется воронением, и активно применяется в технике для защиты поверхности стальных изделий. Но это – частный случай, и таким способом активно защищать металл от коррозии в большинстве случаев невозможно.
Химическая коррозия активизируется при повышенных температурах. Склонность металлов к химическому окислению определяется значением их кислородного потенциала – способности к участию в окислительно-восстановительных реакциях.Сталь – ещё не самый худший вариант: интенсивнее её окисляются, в частности, свинец, кобальт, никель.
Электрохимическая коррозия
Эта разновидность коррозии более коварна: разрушение металла в данном случае происходит при совокупном влиянии воды и почвы на стальную поверхность (например, подземных трубопроводов). Влажный грунт, являясь слабощёлочной средой, способствует образованию и перемещению в почве блуждающих электрических токов. Они являются следствием ионизации частиц металла в кислородсодержащей среде, и инициирует перенос катионов металла с поверхности вовне. Борьба с такой коррозией усложняется труднодоступностью диагностирования состояния грунта в месте прокладки стальной коммуникации.
Электрохимическая коррозия возникает при окислении контактных устройств линий электропередач при увеличении зазоров между элементами электрической цепи. Помимо их разрушения, в данном случае резко увеличивается энергопотребление устройств.
Трибохимическая коррозия
Данному виду подвержены металлообрабатывающие инструменты, которые работают в режимах повышенных температур и давлений. Антикоррозионное покрытие резцов, пуансонов, фильер и пр. невозможно, поскольку от детали требуется высокая поверхностная твёрдость. Между тем, при скоростном резании, холодном прессовании и других энергоёмких процессах обработки металлов начинают происходить механохимические реакции, интенсивность которых возрастает с увеличением температуры на контактной поверхности «инструмент-заготовка». Образующаяся при этом окись железа Fe2O3 отличается повышенной твёрдостью, и поэтому начинает интенсивно разрушать поверхность инструмента.
Методы борьбы с коррозией
Выбор подходящего способа защиты поверхности от образования ржавчины определяется условиями, в которых работает данная деталь или конструкция. Наиболее эффективны следующие методы:
- Нанесение поверхностных атмосферостойких покрытий;
- Поверхностная металлизация;
- Легирование металла элементами, обладающими большей стойкостью к участию в окислительно-восстановительных реакциях;
- Изменение химического состава окружающей среды.

Механические поверхностные покрытия
Поверхностная защита металла может быть выполнена его окрашиванием либо нанесением поверхностных плёнок, по своему составу нейтральных к воздействию кислорода. В быту, а также при обработке сравнительно больших площадей (главным образом, подземных трубопроводов) применяется окраска. Среди наиболее стойких красок – эмали и краски, содержащие алюминий. В первом случае эффект достигается перекрытием доступа кислороду к стальной поверхности, а во втором – нанесением алюминия на поверхность, который, являясь химически инертным металлом, предохраняет сталь от коррозионного разрушения.
Положительными особенностями данного способа защиты являются лёгкость его реализации и сравнительно небольшие финансовые затраты, поскольку процесс достаточно просто механизируется. Вместе с тем долговечность такого способа защиты невелика, поскольку, не обладая большой степенью сродства с основным металлом, такие покрытия через некоторое время начинают механически разрушаться.
Химические поверхностные покрытия
Коррозионная защита в данном случае происходит вследствие образования на поверхности обрабатываемого металла химической плёнки, состоящей из компонентов, стойких к воздействию кислорода, давлений, температур и влажности. Например, углеродистые стали обрабатывают фосфатированием. Процесс может выполняться как в холодном, так и в горячем состоянии, и заключается в формировании на поверхности металла слоя из фосфатных солей марганца и цинка. Аналогом фосфатированию выступает оксалатирование – процесс обработки металла солями щавелевой кислоты. Применением именно таких технологий повышают стойкость металлов от трибохимической коррозии.
Недостатком данных методов является трудоёмкость и сложность их применения, требующая наличия специального оборудования. Кроме того, конечная поверхность изменяет свой цвет, что не всегда приемлемо по эстетическим соображениям.
Легирование и металлизация
В отличие от предыдущих способов, здесь конечным результатом является образование слоя металла, химически инертного к воздействию кислорода. К числу таких металлов относятся те, которые на линии кислородной активности находятся возможно дальше от водорода. По мере возрастания эффективности этот ряд выглядит так: хром→медь→цинк→серебро→алюминий→платина. Различие в технологиях получения таких антикоррозионных слоёв состоит в способе их нанесения. При металлизации на поверхность направляется ионизированный дуговой поток мелкодисперсного напыляемого металла, а легирование реализуется в процессе выплавки металла, как следствие протекания металлургических реакций между основным металлом и вводимыми легирующими добавками.
К числу таких металлов относятся те, которые на линии кислородной активности находятся возможно дальше от водорода. По мере возрастания эффективности этот ряд выглядит так: хром→медь→цинк→серебро→алюминий→платина. Различие в технологиях получения таких антикоррозионных слоёв состоит в способе их нанесения. При металлизации на поверхность направляется ионизированный дуговой поток мелкодисперсного напыляемого металла, а легирование реализуется в процессе выплавки металла, как следствие протекания металлургических реакций между основным металлом и вводимыми легирующими добавками.
Изменение состава окружающей среды
В некоторых случаях существенного снижения коррозии удаётся добиться изменением состава атмосферы, в которой работает защищаемая металлоконструкция. Это может быть вакуумирование (для сравнительно небольших объектов), или работа в среде инертных газов (аргон, неон, ксенон). Данный метод весьма эффективен, однако требует дополнительного оборудования — защитных камер, костюмов для обслуживающего персонала и т. д. Используется он главным образом, в научно-исследовательских лабораториях и опытных производствах, где специально поддерживается необходимый микроклимат.
д. Используется он главным образом, в научно-исследовательских лабораториях и опытных производствах, где специально поддерживается необходимый микроклимат.
Кто нам мешает, тот нам поможет
В завершение укажем и на довольно необычный способ коррозионной защиты: с помощью самих окислов железа, точнее, одного из них — закиси-окиси Fe3O4. Данное вещество образуется при температурах 250…5000С и по своим механическим свойствам представляет собой высоковязкую технологическую смазку. Присутствуя на поверхности заготовки, Fe3O4 перекрывает доступ кислороду воздуха при полугорячей деформации металлов и сплавов, и тем самым блокирует процесс зарождения трибохимической коррозии. Это явление используется при скоростной высадке труднодеформируемых металлов и сплавов. Эффективность данного способа обусловлена тем, что при каждом технологическом цикле контактные поверхности обновляются, а потому стабильность процесса регулируется автоматически.
Основные виды коррозии металлов
ОСНОВНЫЕ ВИДЫ КОРРОЗИИ
Коррозией металлов называется их разрушение вследствие химического или электрохимического взаимодействия с окружающей средой. По механизму протекания процесса различают два ее типа: химическую и электрохимическую.
По механизму протекания процесса различают два ее типа: химическую и электрохимическую.
Химическая коррозия протекает в средах, не проводящих электрический ток, например, при высокотемпературном нагреве стали для горячей обработки давлением или термической обработки. При этом на поверхности металла образуются различные химические соединения – оксиды, сульфиды и другие – в виде пленки.
В отдельных случаях образовавшиеся при химической коррозии пленки, особенно сплошные, предохраняют металл от дальнейшей коррозии. Например, алюминий, олово, свинец, никель и хром способны к образованию на поверхности металлов плотных защитных пленок. пленки же на стали и чугуне непрочны, способны к растрескиванию и проникновению коррозии вглубь металла.
Электрохимическая коррозия обычно сопровождается протеканием электрического тока. Примерами могут служить ржавление металлических конструкций и изделий в атмосфере, корпусов судов и стальной арматуры гидросооружений в речной и морской воде и т.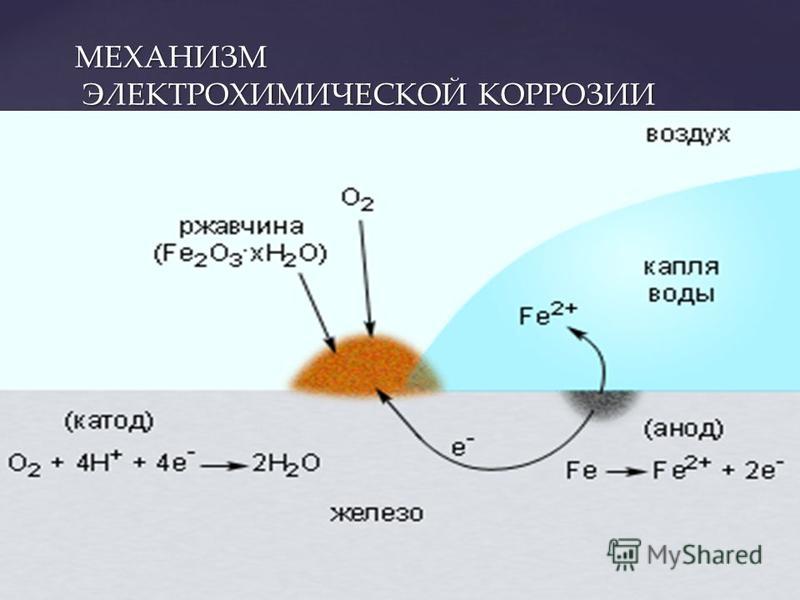 п.
п.
Детальное рассмотрение механизмов химической и электрохимической коррозии показывает, что резкого различия между ними не существует. В ряде случаев возможен постепенный переход химической коррозии в электрохимическую и, наоборот, механизм коррозии металлов в растворах электролитов может иметь двоякий характер.
Коррозия по условиям протекания бывает следующая. Газовая – коррозия металла в газах при высоких температурах. Коррозия в неэлектролитах (например, коррозия стали в бензине). Атмосферная коррозия различных металлических конструкций на воздухе. Коррозия в электролитах – в проводящих электрический ток жидких средах. Почвенная (например, коррозия подземных трубопроводов). Коррозия внешним током или электрокоррозия (например, повреждение подземной трубы блуждающими токами). Контактная – электрохимическое разрушение металлов, происходящее в результате контакта различных металлов в электролите (например, коррозия деталей из алюминиевых сплавов, соприкасающихся с деталями из меди). Структурная – связанная со структурной неоднородностью металлов; например, ускорение коррозионного процесса чугуна в растворе серной кислоты в результате имеющихся в нем включений графита. Коррозия под напряжением, изменяющимся по значению и знаку, что часто вызывает понижение предела выносливости металла. Коррозия при трении; например, разрушение шейки вала при вращении в морской воде. Щелевая, протекающая в узких щелях и зазорах между отдельными деталями. Биокоррозия – коррозия металлов под воздействием продуктов, выделяемых микроорганизмами, и пота рук человека. По характеру коррозионных процессов и месту их распределения различают сплошную, местную и межкристаллитную коррозию. Сплошная характеризуется тем, что металлическое изделие разрушается почти равномерно и коррозия охватывает всю его поверхность. Сравнительно легко поддается контролю и оценке.
Структурная – связанная со структурной неоднородностью металлов; например, ускорение коррозионного процесса чугуна в растворе серной кислоты в результате имеющихся в нем включений графита. Коррозия под напряжением, изменяющимся по значению и знаку, что часто вызывает понижение предела выносливости металла. Коррозия при трении; например, разрушение шейки вала при вращении в морской воде. Щелевая, протекающая в узких щелях и зазорах между отдельными деталями. Биокоррозия – коррозия металлов под воздействием продуктов, выделяемых микроорганизмами, и пота рук человека. По характеру коррозионных процессов и месту их распределения различают сплошную, местную и межкристаллитную коррозию. Сплошная характеризуется тем, что металлическое изделие разрушается почти равномерно и коррозия охватывает всю его поверхность. Сравнительно легко поддается контролю и оценке.
Местная коррозия обычно бывает сосредоточенна на отдельных участках поверхности изделия. Это более опасный вид коррозии, так как распространяется на значительную глубину, а следовательно, приводит к потере работоспособности изделий. Чаще всего этот вид коррозии наблюдается в местах механических повреждений поверхности изделий. При межкристаллитной коррозии процесс разрушения начинается с поверхности изделия и распространяется вглубь его, в основном по границам зерен, что вызывает хрупкость металла и значительное снижение его несущей способности. Этот часто встречающийся на практике вид коррозии является весьма опасным и обычно имеет место при термической обработке металлов или сварке. Степень коррозийной стойкости сталей существенно зависит от содержания углерода. Так, с уменьшением содержания углерода в легированной хромоникелевой стали марки Х18Н9 до 0.015% практически устраняется склонность ее к межкристаллитной коррозии.
Чаще всего этот вид коррозии наблюдается в местах механических повреждений поверхности изделий. При межкристаллитной коррозии процесс разрушения начинается с поверхности изделия и распространяется вглубь его, в основном по границам зерен, что вызывает хрупкость металла и значительное снижение его несущей способности. Этот часто встречающийся на практике вид коррозии является весьма опасным и обычно имеет место при термической обработке металлов или сварке. Степень коррозийной стойкости сталей существенно зависит от содержания углерода. Так, с уменьшением содержания углерода в легированной хромоникелевой стали марки Х18Н9 до 0.015% практически устраняется склонность ее к межкристаллитной коррозии.
МЕТОДЫ ЗАЩИТЫ ОТ КОРРОЗИИ, ИХ ЭФФЕКТИВНОСТЬ
Существуют многочисленные способы защитить металл от разрушений или ржавчины. Выбор того или иного способа определяется конкретными условиями работы и хранения металлических изделий. Наиболее широко применяются: легирование сталей, нанесение металлических покрытий, электрохимическая защита.
Легирование эффективнее всего в условиях воздействия механических напряжений и коррозийной среды. Легирование позволяет предотвратить и коррозийное растрескивание изделий.
Так, например, к группе сталей с особыми химическими свойствами относят коррозионно-стойкие стали. Их получают путем введения в углеродистые и низколегированные стали значительных добавок хрома или хрома и никеля. При содержании хрома 13, 17 и 25% хромистые стали являются не только коррозионно-, но и жаростойкими. Хромоникелевые стали обладают большей коррозионной стойкостью, чем хромистые, и находят широкое применение в химической промышленности.
Металлические покрытия наносят на поверхность изделия тонким слоем металла, обладающего достаточной стойкостью в данной среде. Такое покрытие придает также поверхностным слоям металлоизделий требуемую твердость, износостойкость. Различают два типа покрытий – анодное и катодное. Для железоуглеродистых сплавов таким анодным покрытием может служить покрытие из цинка и кадмия. В воде и во влажном воздухе цинк покрывается слоем основной углекислой соли белого цвета, защищающим его от дальнейшего разрушения. Широкое применение получили цинковые покрытия для защиты арматуры, труб и резервуаров от действия воды и горячих жидкостей.
В воде и во влажном воздухе цинк покрывается слоем основной углекислой соли белого цвета, защищающим его от дальнейшего разрушения. Широкое применение получили цинковые покрытия для защиты арматуры, труб и резервуаров от действия воды и горячих жидкостей.
Металлические покрытия наносят различными способами. Наиболее часто применяется горячий метод, гальванизация и металлизация.
При горячем методе изделие погружают в расплавленный металл, который смачивает его поверхность и покрывает тонким слоем. Затем изделие вынимают из ванны и охлаждают. Таким методом изделие покрывают слоем олова или цинка. Лужение применяют при изготовлении белой жести, при устройстве покрытий на внутренних поверхностях пищевых котлов и других изделий. Цинкованием предохраняют от коррозии, например, кровельное железо, водопроводные трубы.
При гальваническом способе металлические изделия помещают в гальваническую ванну. Под действием электрического тока на поверхности изделия происходит катодное осаждение пленки защитного металла. Толщину покрытия можно регулировать в широких пределах. Покрытия получают также распылением расплавленного металла с помощью специальных металлизационных пистолетов и напылением на его поверхность защищаемого металла. Этот вид защиты используют для крупногабаритных конструкций: ж/д мостов и т. д. В качестве защитного металла используют алюминий, цинк, хром, коррозионно-стойкие стали.
Толщину покрытия можно регулировать в широких пределах. Покрытия получают также распылением расплавленного металла с помощью специальных металлизационных пистолетов и напылением на его поверхность защищаемого металла. Этот вид защиты используют для крупногабаритных конструкций: ж/д мостов и т. д. В качестве защитного металла используют алюминий, цинк, хром, коррозионно-стойкие стали.
Неметаллические покрытия выполняются из лаков, красок, эмалей и др. веществ и изолируют изделие от воздействия внешней среды. Они легко наносятся на изделие, хорошо закрывают поры, не изменяют свойств металла и являются относительно дешевыми. При хранении и перевозке металлические изделия покрывают специальными смазочными материалами, минеральными маслами и жирами. Для защиты изделий, работающих в высокоагрессивных средах, применяют пластмассовые покрытия из винипласта, поливинилхлорида.
Химические покрытия – защитные оксидные и иные пленки – создаются при воздействии на металл сильных химических реагентов. Широко применяются также оксидирование и фосфатирование металлоизделий.
Широко применяются также оксидирование и фосфатирование металлоизделий.
Оксидирование – создание на поверхности изделия оксидной пленки, обладающей большой коррозийной стойкостью. Наиболее широко применяется для защиты от коррозии изделий из алюминия и его сплавов.
Фосфатирование стальных изделий заключается в создании поверхностного слоя из фосфатов марганца и железа. Фосфатные покрытия используются в дальнейшем в качестве подслоя, часто в сочетании со смазочными материалами, для уменьшения трения при обработке металлов давлением, волочением, для хорошей приработки трущихся деталей машин.
В отдельных случаях прибегают к защите металлов от коррозии при помощи протекторов. Сущность протекторной защиты заключается в том, что к поверхности защищаемого изделия прикрепляют протекторы – куски металла. Образуется гальваническая пара, в которой анод – протектор, катод – изделие. В результате протектор разрушается, защищая изделие. Таким образом защищают, например, подводные металлические части кораблей, прикрепляя к ним пластины цинка.
НАРОДНОХОЗЯЙСТВЕННОЕ ЗНАЧЕНИЕ БОРЬБЫ С КОРРОЗИЕЙ
Потери от коррозии можно разделить на прямые и косвенные. Прямые потери – это стоимость заменяемых изделий, затраты на защитные мероприятия и безвозвратные потери металла вследствие коррозии. По подсчетам специалистов, таковые в мировом масштабе составляют в настоящее время около 10…15% от объема производства стали. Косвенные – потери продукта в результате утечек, снижение производительности агрегата, загрязнение продуктами коррозии целевого продукта и т.п.
Значительная часть мощности предприятий черной металлургии затрачивается на восполнение потерь металла вследствие коррозии. Однако это далеко не полностью отражает действительный ущерб, связанный с выходом из строя изделий из металла. Значительные потери обусловлены авариями оборудования, его простоями, потерями и отходами в металлообработке, нарушениями качества продукции и в конечном счете повышением ее себестоимости и снижением производительности труда. Поэтому экономия металла, повышение качества исходного сырья и металлоизделий, уменьшение коррозионных потерь – непременное условие повышения эффективности производства и качества продукции, которое должно обеспечиваться в государственном масштабе.
Типы и виды коррозий металла — Короли Воды и Пара на vc.ru
173
просмотров
Коррозии металла
Сегодня мы с вами разберемся, узнаем многое про типы и виды коррозии металла. Изучим тему, узнав, откуда и из-за чего берётся коррозия на металле.
Откуда берётся, коррозия металла
Коррозия появляется из-за воздействия на него окружающей среды. Учёные выяснили, что это саморазрушение металлов и сплавов в ходе химических и физико-химических и электрохимических процессов. Так же есть практически аналогичный процесс, это разрушение металла методом физического воздействия, не надо его путать с коррозией, этот процесс называют: «эрозия» или же «износ».
Также стоит сказать, что на появление ржавчины сильнее всего содействует влажная среда. На появление ржавчины, как и на все химические процессы, влияет температура окружающей среды, даже если температура воздуха будет различаться всего на 5-10 градусов, то разница в скорости уже будет видна. Таким образом, появляется ржавчина, она бывает разных видов и ниже мы расскажем именно про это.
Таким образом, появляется ржавчина, она бывает разных видов и ниже мы расскажем именно про это.
Типы и виды коррозии
Коррозию в основном различают на четыре основных типа, а именно: электрохимическая, химическая, водородная и кислородная.
Электрохимическая коррозия
Электрохимической коррозией называют разрушение металла, вследствие взаимодействия с коррозионной средой гальванических элементов. Для появления электрохимической коррозии обязательна наличие электролита, с которыми будут соприкасаться электроды и другие элементы. Если процесс проходит в воде и в нем растворены соли, то процесс идет намного быстрее.
Водородная и кислородная коррозия
Когда случается Восстановление ионов Н3О+ или же молекулы воды Н2О, это называют коррозией с водородной деполяризацией или же проще водородной коррозией. Такую коррозию чаще всего называют ржавчиной. Коррозия такого типа возникает во влажных местах либо же в водопроводных трубах (при скоплении конденсата). Каждый из нас видел коррозии такого типа, если не дома, то на улице уж точно.
Каждый из нас видел коррозии такого типа, если не дома, то на улице уж точно.
Также коррозия может возникать, не только при прикосновении нескольких разных металлов. Элементы коррозии могут возникать и в случаи, если металл один. Если структура металла неоднородна, то она возникает также, так случается чаще ведь сейчас практически всегда в любом металле есть примеси в виде других металлов, это делается для экономии.
Химическая коррозия (при воздействии пара)
Химической коррозией считается ржавчина возникшая из-за касания и взаимодействия металла с средой которая полна активной коррозией, в отличии от электрохимической, процесс не идет совместно с электрохимическими реакциями и стоит на границе фаз. В отличии от остальных в этом виде есть и другие типы. Например жидкостная коррозия, газовая коррозия, атмосферная коррозия и так далее.
- Газовая коррозия (при воздействии пара) – Это коррозия, которая возникает из-за взаимодействия с активными газами, которые находятся в среде, где находится, металл.
 Для хода газовой коррозии обязательна высокая температура среды. Такими газами могут быть: Кислород, пары воды, пары серы и другие.
Для хода газовой коррозии обязательна высокая температура среды. Такими газами могут быть: Кислород, пары воды, пары серы и другие. - Жидкостная коррозия – Ржавчина этого типа может появится из-за соприкосновения с активными жидкостями, например нефть, керосин, бензин или почти со всеми маслами.
Защита от появления коррозии
Вы, наверное, задаетесь вопросом: «Если есть такое множество видов коррозии и если ржавчина может возникнуть практически везде, то мы не придумали как защитить металлы?» И это логичный вопрос, ведь люди постоянно придумывают, как облегчить свою жизнь. Наш ответ да, люди всё таки придумали, как защищать металлы от коррозии, и этих методов великое множество, ниже мы расскажем про нескольких из них.
Металлическое покрытие
Это самый простой метод защиты, металл, покрывают защитным слоем, другого уже заведомо обработанного металлом, уж простите за тавтологию. Таким тонким слоем можно защитить металл от возникновения ржавчины, таких покрытии есть великое множество, например анодное покрытие и катодное покрытие. К сожалению, покрытие такого типа не защищает от коррозии, которая возникает водородным методом, то есть от пара, от воды и так далее.
К сожалению, покрытие такого типа не защищает от коррозии, которая возникает водородным методом, то есть от пара, от воды и так далее.
Химическое покрытие
Так же есть неметаллические покрытия для защиты металлов от ржавчины, химическое покрытие один из этих методов защиты, вот несколько из этих покрытий:
- Оксидирование;
- Фосфатирование;
- Азотирование;
- Воронение стали;
- Цементация.
Электрохимическая защита
В этом случае защита создаётся при помощи постоянного обеспечения током. Так же есть и другой метод электрохимической защиты, его называют Протекторной, при этой схеме К поверхности прицепляются другие куски металла уже обеспеченным защитой и это называют протектором.
Наши специалисты проконсультируют Вас и помогут в правильном подборе оборудования в паровые и пароконденсатные системы, во избежание появления коррозий.
Если у Вас остались вопросы, мы будем рады Вам помочь. С нами можно связаться любым удобным способом:
По почте: [email protected]
По телефону: +7 (343) 288-35-54 или WhatsApp
Подписывайтесь на наш Телеграм канал, там всегда много полезного и интересного.
Коррозия металлов и её виды
Химические и физико-химические реакции, возникающие в момент взаимодействия окружающей среды с металлами и сплавами, в большинстве случаев приводят к их самопроизвольному разрушению. Процесс саморазрушения имеет собственный термин – «коррозия». Результатом коррозии является существенное ухудшение свойств металла, вследствие чего изделия из него быстро выходят из строя. Каждый металл обладает свойствами, позволяющими ему сопротивляться разрушению. Коррозийная стойкость или, как ее еще называют, химическое сопротивление материала, является одним из главных критериев, по которым осуществляется отбор металлов и сплавов для изготовления тех или иных изделий.
В зависимости от интенсивности и длительности коррозийного процесса металл может быть подвергнут как частичному, так и полному разрушению. Взаимодействие коррозийной среды и металла приводят к образованию на поверхности металла таких явлений, как окалина, оксидная пленка и ржавчина. Данные явления отличаются друг от друга не только внешним видом, но еще и степенью адгезии с поверхностью металлов. Так, например, в процессе окисления такого металла, как алюминий, его поверхность покрывает пленка оксидов, отличающаяся высокой прочностью. Благодаря этой пленке разрушительные процессы купируются и не проникают вовнутрь. Если говорить о ржавчине, то результатом ее воздействия является образование рыхлого слоя. Процесс коррозии в данном случае очень быстро проникает во внутреннюю структуру металла, что способствует его скорейшему разрушению.
Взаимодействие коррозийной среды и металла приводят к образованию на поверхности металла таких явлений, как окалина, оксидная пленка и ржавчина. Данные явления отличаются друг от друга не только внешним видом, но еще и степенью адгезии с поверхностью металлов. Так, например, в процессе окисления такого металла, как алюминий, его поверхность покрывает пленка оксидов, отличающаяся высокой прочностью. Благодаря этой пленке разрушительные процессы купируются и не проникают вовнутрь. Если говорить о ржавчине, то результатом ее воздействия является образование рыхлого слоя. Процесс коррозии в данном случае очень быстро проникает во внутреннюю структуру металла, что способствует его скорейшему разрушению.
Показатели, по которым осуществляется классификация коррозийных процессов:
-
вид коррозийной среды; -
условия и механизм протекания; -
характер коррозийных разрушений; -
вид дополнительных воздействий на металл.
По механизму коррозийного процесса различают как химическую, так и электрохимическую коррозию металлов и сплавов.
Химическая коррозия – это взаимодействие металлов с коррозийной средой, в процессе которого наблюдается единовременное осуществление окисления металла и восстановление окислительного компонента среды. Взаимодействующие между собой продукты не разделены пространственно.
Электрохимическая коррозия – это взаимодействие металлов с коррозийно-активной средой, представляющей собой раствор электролита. Процесс ионизации атомов металла, а также процесс восстановления окислительного компонента данной коррозийной среды протекают в разных актах. Электродный потенциал раствора электролита оказывает существенное влияние на скорость этих процессов.
В зависимости от типа агрессивной среды существует несколько видов коррозии
Атмосферная коррозия представляет собой саморазрушение металлов в воздушной атмосфере, либо в газовой атмосфере, отличающейся повышенной влажностью.
Газовая коррозия – это коррозия металлов, происходящая в газовой среде, содержание влаги в которой минимально. Отсутствие влаги в газовой среде не единственное условие, способствующее саморазрушению металла. Также коррозия возможна и при высоких температурах. Наиболее часто встречается данный вид коррозии в нефтехимической и химической промышленности.
Радиационная коррозия представляет собой саморазрушение металла под воздействием на него радиоактивного излучения разной степени интенсивности.
Подземная коррозия – это коррозия, происходящая в почвах и различных грунтах.
Контактная коррозия представляет вид коррозии, образованию которого способствует контакт нескольких металлов, отличающихся друг от друга стационарными потенциалами в конкретном электролите.
Биокоррозия – это коррозия металлов, происходящая под воздействием различных микроорганизмов и их жизнедеятельности.
Коррозия током (внешним и блуждающим) – еще один вид коррозии металлов. Если на металл воздействует ток от внешнего источника, то это коррозия внешним током. Если же воздействие осуществляется посредством блуждающего тока, то это коррозия блуждающего тока.
Коррозийная кавитация представляет собой процесс саморазрушения металлов, возникновению которого способствует как ударное, так и коррозионное воздействие внешней среды.
Коррозия под напряжением представляет собой коррозию металла, причиной появления которой является взаимодействие коррозийно-активной среды и напряжений механического типа. Данный вид коррозии представляет существенную опасность для конструкций из металла, которые подвергаются сильнейшим механическим нагрузкам.
Фреттинг-коррозия — вид коррозии металлов, к которой приводит совокупность вибрации и воздействие коррозийной среды. Чтобы минимизировать вероятность возникновения коррозии при трении и вибрации, необходимо внимательно подходить к выбору конструкционного материала. Также необходимо применять специальные покрытия и по возможности снизить коэффициент трения.
Также необходимо применять специальные покрытия и по возможности снизить коэффициент трения.
По характеру разрушений коррозия разделяется на сплошную и избирательную
Сплошная коррозия полностью покрывает поверхность металла. Если скорость разрушений на всей поверхности одинакова, то это равномерная коррозия. Если разрушение металла на различных его участках происходит с разной скоростью, то коррозия называется неравномерной.
Избирательная коррозия подразумевает разрушение одного из компонентов сплава или же одной структурной составляющей.
Местная коррозия, проявляющаяся в виде отдельно разбросанных по поверхности металла пятен, представляет собой углубления разной толщины. Разрушения могут представлять собой раковины или точки.
Подповерхностная коррозия образуется непосредственно на поверхности металла, после чего активно проникает вглубь. Данный вид коррозии сопровождается расслоением изделий из металла.
Данный вид коррозии сопровождается расслоением изделий из металла.
Межкристаллитная коррозия проявляется в разрушении металла по границам зерен. По внешнему виду металла ее достаточно сложно определить. Однако очень быстро меняются показатели прочности и пластичности металла. Изделия из него становятся хрупкими. Наиболее опасен этот вид коррозии для хромистых и хромоникелевых видов стали, а также для алюминиевых и никелевых сплавов.
Щелевая коррозия образуется на тех участках металлов и сплавов, которые находятся в резьбовых креплениях, различных зазорах и под всевозможными прокладками.
16.8: Электрохимическая коррозия — Химия LibreTexts
- Последнее обновление
- Сохранить как PDF
- Идентификатор страницы
- 265
- Стивен Лоуэр
- Университет Саймона Фрейзера
Цели обучения
Убедитесь, что вы полностью поняли следующие основные идеи. Особенно важно, чтобы вы знали точное значение всех выделенных терминов в контексте этой темы.
Особенно важно, чтобы вы знали точное значение всех выделенных терминов в контексте этой темы.
- Электрохимическая коррозия металлов происходит, когда электроны от атомов на поверхности металла переносятся на подходящий акцептор электронов или деполяризатор . Вода должна присутствовать, чтобы служить средой для переноса ионов.
- Наиболее распространенными деполяризаторами являются кислород, кислоты и катионы менее активных металлов.
- Поскольку электроны проходят через сам металлический объект, анодная и катодная области (две половины электрохимической ячейки) могут находиться далеко друг от друга.
- Анодные области имеют тенденцию развиваться в местах, где металл находится под напряжением или защищен от кислорода.
- Контакт с другим металлом, прямой или косвенный, может привести к коррозии более активного металла.
- Коррозию стали можно подавить с помощью цинкования , то есть путем покрытия ее цинком, более активным металлом, растворение которого оставляет на металле отрицательный заряд, препятствующий дальнейшему растворению Fe 2+ .

- Катодная защита с использованием внешнего источника напряжения широко применяется для защиты подземных сооружений, таких как резервуары, трубопроводы и опоры. Источником может быть расходуемый анод из цинка или алюминия, сетевой или фотогальванический источник питания.
Коррозию можно определить как разрушение материалов в результате химических процессов. Из них наиболее важной на сегодняшний день является электрохимическая коррозия металлов, при которой процесс окисления М → М + + е – облегчается наличием подходящего акцептора электронов, иногда называемого в науке о коррозии как деполяризатор.
В некотором смысле коррозию можно рассматривать как самопроизвольный возврат металлов в их руды; огромное количество энергии, затраченной на добычу, очистку и производство металлов в полезные предметы, рассеивается множеством различных путей. Экономические аспекты коррозии намного значительнее, чем думает большинство людей; предполагаемая стоимость коррозии только в США составляла 276 миллиардов долларов в год. Из них около 121 миллиарда долларов было потрачено на борьбу с коррозией, а разница в 155 миллиардов долларов осталась чистыми потерями для экономики. Коммунальные услуги, особенно системы питьевого водоснабжения и канализации, испытывают наибольшее экономическое воздействие, а автомобили и транспорт занимают второе место.
Из них около 121 миллиарда долларов было потрачено на борьбу с коррозией, а разница в 155 миллиардов долларов осталась чистыми потерями для экономики. Коммунальные услуги, особенно системы питьевого водоснабжения и канализации, испытывают наибольшее экономическое воздействие, а автомобили и транспорт занимают второе место.
Ячейки коррозии и реакции
Особенностью большинства процессов коррозии является то, что стадии окисления и восстановления происходят в разных местах металла. Это возможно, потому что металлы являются проводящими, поэтому электроны могут течь через металл от анодных к катодным областям (рисунок \(\PageIndex{1}\)). Присутствие воды необходимо для переноса ионов к металлу и от него, но тонкой пленки адсорбированной влаги может быть достаточно.
Рисунок \(\PageIndex{1}\): Коррозия — это двухэтапный процесс. Рисунок \(\PageIndex{1}\): Электрохимическая коррозия железа. Коррозия часто начинается в месте (1), где металл находится под напряжением (на изгибе или сварке) или изолирован от воздуха (где соединяются два куска металла или под слабо прилипшей пленкой краски). Ионы металла растворяются в пленке влаги, а электроны мигрируют в другое место (2), где они поглощаются 9{–}} \rightarrow \ce{M(s)} \label{1.7.2c}\]
Ионы металла растворяются в пленке влаги, а электроны мигрируют в другое место (2), где они поглощаются 9{–}} \rightarrow \ce{M(s)} \label{1.7.2c}\]
, где \(\ce{M}\) — металл.
То, какие части металла служат анодами и катодами, может зависеть от многих факторов, как видно из обычно наблюдаемых неравномерных картин коррозии. Атомы в областях, подвергшихся напряжению, которые могут быть получены путем формовки или механической обработки, часто имеют более высокую свободную энергию и, таким образом, имеют тенденцию становиться анодными.
Рисунок \(\PageIndex{2}\): Схематическая диаграмма коррозионных ячеек на железе. (CC BY-NSA-NC; анонимно по запросу)
Если одна часть металлического предмета защищена от атмосферы так, что недостаточно \(\ce{O2}\) для создания или поддержания оксидной пленки, эта «защищенная» область часто будет местом, где коррозия наиболее активна. активный. Тот факт, что такие места обычно скрыты от глаз, объясняет большую часть трудностей в обнаружении коррозии и борьбе с ней.
Рисунок \(\PageIndex{3}\): Точечная коррозия Большинство металлов покрыты тонкой оксидной пленкой, препятствующей анодному растворению. Когда коррозия действительно возникает, иногда в металле образуются узкие отверстия или ямки. Дно этих ямок, как правило, лишено кислорода, что способствует дальнейшему прорастанию ямок в металл. (CC BY 3.0 непортированная; Стивен Лоуэр)
В отличие от анодных участков, которые, как правило, локализованы в определенных областях поверхности, катодная часть процесса может происходить практически где угодно. Поскольку оксиды металлов обычно являются полупроводниками, большинство оксидных покрытий не препятствуют потоку электронов к поверхности, поэтому почти любая область, которая подвергается воздействию \(\ce{O2}\) или какого-либо другого акцептора электронов, может действовать как катод. Тенденция мест, лишенных кислорода, к анодированию является причиной многих широко наблюдаемых моделей коррозии.
Ржавые автомобили и пятна в ванных комнатах
Любой, кто владел старым автомобилем, видел коррозию на стыках между частями кузова и под лакокрасочным покрытием. Вы также заметите, что как только начинается коррозия, она имеет тенденцию питаться сама собой. Одна из причин этого заключается в том, что одним из продуктов реакции восстановления O 2 является гидроксид-ион. Высокий уровень pH, создаваемый в этих катодных областях, имеет тенденцию разрушать защитную оксидную пленку и может даже смягчить или ослабить пленки краски, так что эти участки могут стать анодными. Большее поступление электронов способствует более интенсивному катодному действию, что порождает еще больше анодных участков и т.д.
Вы также заметите, что как только начинается коррозия, она имеет тенденцию питаться сама собой. Одна из причин этого заключается в том, что одним из продуктов реакции восстановления O 2 является гидроксид-ион. Высокий уровень pH, создаваемый в этих катодных областях, имеет тенденцию разрушать защитную оксидную пленку и может даже смягчить или ослабить пленки краски, так что эти участки могут стать анодными. Большее поступление электронов способствует более интенсивному катодному действию, что порождает еще больше анодных участков и т.д.
Рисунок \(\PageIndex{4}\): Ржавая машина. Сильно проржавевшие половицы автомобиля Chrysler New Yorker 1990 года выпуска. Автомобиль был поврежден до такой степени, что управлять им стало небезопасно. Под ржавым участком между двумя отверстиями находились две тормозные магистрали (общественное достояние; Bige1977 через Википедию).
Очень распространенной причиной коррозии является контакт двух разнородных металлов, что может произойти вблизи крепежных деталей или сварных швов. В месте соединения собирается влага, действующая как электролит и образующая ячейку, в которой два металла служат электродами. Влага и токопроводящие соли на внешних поверхностях образуют внешний токопроводящий путь, эффективно замыкая элемент накоротко и вызывая очень быструю коррозию; Вот почему автомобили так быстро ржавеют в тех местах, где дороги посыпают солью, чтобы растопить лед. 9{3+}}\) соли, выпадающие в осадок в виде зеленоватых пятен.
В месте соединения собирается влага, действующая как электролит и образующая ячейку, в которой два металла служат электродами. Влага и токопроводящие соли на внешних поверхностях образуют внешний токопроводящий путь, эффективно замыкая элемент накоротко и вызывая очень быструю коррозию; Вот почему автомобили так быстро ржавеют в тех местах, где дороги посыпают солью, чтобы растопить лед. 9{3+}}\) соли, выпадающие в осадок в виде зеленоватых пятен.
Контроль коррозии
Поскольку для возникновения коррозии должны иметь место как катодная, так и анодная стадии, предотвращение любой из них остановит коррозию. Наиболее очевидная стратегия — остановить оба процесса, покрыв объект краской или другим защитным покрытием. Даже если это будет сделано, вероятно, будут места, где покрытие сломано или не проникает, особенно если есть отверстия или резьба. Более сложный подход состоит в том, чтобы нанести на металл небольшой отрицательный заряд, что затруднит протекание реакции: 9{-}}.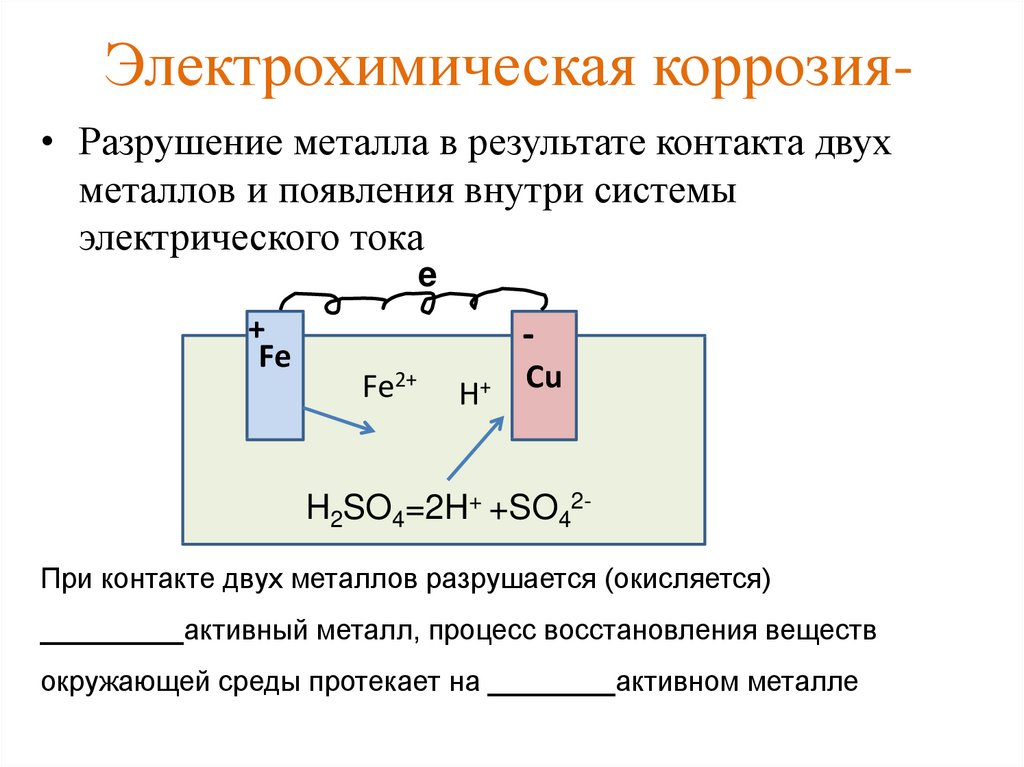 \]
\]
Метод защиты 1: расходуемые покрытия
Одним из способов создания этого отрицательного заряда является нанесение покрытия из более активного металла. Таким образом, очень распространенным способом защиты стали от коррозии является покрытие ее тонким слоем цинка; этот процесс известен как цинкование. Цинковое покрытие, будучи менее благородным, чем железо, склонно к избирательной коррозии. Растворение этого жертвенного покрытия оставляет после себя электроны, которые концентрируются в железе, делая его катодным и, таким образом, препятствуя его растворению.
Рисунок \(\PageIndex{5}\): Жертвенные покрытия (CC BY 3.0 Unported; Стивен Лоуэр)
Эффект покрытия железа менее активным металлом дает интересный контраст. Хорошим примером является обычная луженая банка (справа). Пока оловянное покрытие остается неповрежденным, все в порядке, но воздействие влажной атмосферы даже на крошечную часть нижележащего железа вызывает коррозию. Электроны, выпущенные из железа, перетекают в олово, делая железо более анодным, так что теперь олово активно способствует коррозии железа! Вы, наверное, замечали, как быстро разлагаются жестяные банки, оставленные на открытом воздухе.
Метод защиты 2: катодная защита
Более сложная стратегия заключается в поддержании постоянного отрицательного электрического заряда на металле, чтобы предотвратить его растворение в виде положительных ионов. Поскольку вся поверхность принудительно переходит в катодное состояние, этот метод известен как катодная защита . Источником электронов может быть внешний источник питания постоянного тока (обычно используемый для защиты нефтепроводов и других заглубленных конструкций), или это может быть коррозия другого, более активного металла, такого как кусок цинка или алюминия, зарытый в землю поблизости. , как показано на иллюстрации заглубленного резервуара для хранения пропана ниже.
Рисунок \(\PageIndex{6}\): Катодная защита (CC BY 3.0, непортированная; Стивен Лоуэр)
Эта страница под названием 16.8: Электрохимическая коррозия распространяется под лицензией CC BY 3.0 и была создана, изменена и/или курирована Стивеном Лоуэром с помощью исходного контента, который был отредактирован в соответствии со стилем и стандартами платформы LibreTexts; подробная история редактирования доступна по запросу.
- Наверх
- Была ли эта статья полезной?
- Тип изделия
- Раздел или Страница
- Автор
- Стивен Лоуэр
- Лицензия
- СС BY
- Версия лицензии
- 3,0
- Показать страницу TOC
- нет на странице
- Теги
- катодная защита
- коррозия
- коррозионная стойкость
- ржавчина
- Жертвенные покрытия
- источник@http://www.
 chem1.com/acad/webtext/virtualtextbook.html
chem1.com/acad/webtext/virtualtextbook.html
Электрохимия коррозии: 6 электрохимических реакций
Коррозия — это электрохимический метод разрушения материалов. Во многих случаях — и особенно когда присутствуют жидкости — это связано с химией. Во время коррозии электроны из отдельных участков поверхности металла перетекают в альтернативные участки через атмосферу, способную проводить ионы. Это простая химия коррозии, но деталей совсем нет. То же самое касается воздействия.
Реклама
На самом деле экономические последствия коррозии намного больше, чем многие думают. Согласно отчету CC Technologies Laboratories Inc. за 2001 год, стоимость коррозии только в США составляла 276 миллиардов долларов в год. Из них 121 миллиард долларов был потрачен на борьбу с коррозией, а остальные 155 миллиардов долларов были понесены в качестве чистого убытка для экономики. Коммунальные услуги, особенно водопроводные и канализационные системы, испытывают наибольшее экономическое воздействие, за ними следуют автомобили и транспорт.
Поскольку коррозия металлов представляет собой непрерывный электрохимический процесс, крайне важно знать основную природу электрохимических реакций, чтобы должным образом подавлять коррозию и уменьшать ее воздействие на конструкции. В этой статье мы обсудим механизмы коррозии, подробно рассмотрев:
Реклама
- Электрохимические реакции
- Ячейка Даниэля
- Анодный метод
- Закон Фарадея
- Катодный метод
0003 Воздействие на площадь поверхности
Что такое электрохимия коррозии?
Коррозия в водной среде и в атмосферных условиях представляет собой электрохимический процесс, при котором электроны переносятся между металлической поверхностью и жидким раствором электролита, что приводит к ухудшению состояния подложки. Коррозия возникает из-за сильной склонности металлов к электрохимическим реакциям с кислородом, водой и другими веществами в атмосфере. В этом контексте термин «анод» используется для объяснения той части поверхности металла, которая действительно подвергается коррозии, тогда как термин «катод» используется для объяснения поверхности металла, которая поглощает электроны, образующиеся в результате реакции коррозии. Улик Р. Эванс, пионер объяснения коррозии как электрохимического процесса, сказал, что ее можно описать как разрушение электрохимическими или химическими факторами. Таким образом, электрохимия коррозии — это просто электрохимический метод, с помощью которого мы можем понять механизмы коррозии.
Улик Р. Эванс, пионер объяснения коррозии как электрохимического процесса, сказал, что ее можно описать как разрушение электрохимическими или химическими факторами. Таким образом, электрохимия коррозии — это просто электрохимический метод, с помощью которого мы можем понять механизмы коррозии.
Электрохимические реакции
Электрохимическая реакция определяется как реакция с переносом электронов. Это также реакция, которая включает окисление и восстановление. Тот факт, что коррозия состоит как минимум из одной химической реакции и одной реакции восстановления, не совсем очевиден, потому что обе реакции обычно сочетаются в одном куске металла (например, в цинке), как схематично показано ниже.
Рис. 1. Электрохимические реакции при коррозии Zn в безвоздушной HCl.
Реклама
На рисунке 1 кусочек цинка, погруженный в раствор кислоты, подвергается коррозии. В какой-то момент на поверхности Zn превращается в ионы Zn, теряя электроны. Эти электроны проходят через твердый проводящий металл к альтернативным местам на поверхности металла, где ионы водорода (H) восстанавливаются до газообразного водорода в соответствии со следующим уравнением:
Эти электроны проходят через твердый проводящий металл к альтернативным местам на поверхности металла, где ионы водорода (H) восстанавливаются до газообразного водорода в соответствии со следующим уравнением:
Эти уравнения иллюстрируют характер электрохимической реакции в цинке. На протяжении всей такой реакции передаются электроны, или, если рассматривать ее по-другому, реакция окисления происходит в сочетании с реакцией восстановления.
Следовательно, в электрохимии анодные и катодные реакции протекают одновременно и с одинаковыми скоростями. Однако коррозия происходит исключительно в областях, которые функционируют как аноды.
Ячейка Даниэля и электрохимическая коррозия
Доктрина электрохимических реакций используется в ячейке Даниэля, во время которых металлы меди и цинка погружаются в растворы их индивидуальных сульфатов. Ячейка Даниэля была первой разумной и надежной батареей, поддерживавшей несколько разрядов. Электрические инновации го века, такие как телеграф.
Электрические инновации го века, такие как телеграф.
В ячейке Даниэля электроны передаются от корродирующего цинка к меди по электропроводящему пути в виде электрического тока. (Узнайте о похожей коррозионной ячейке в статье «Введение в ячейку Александра».) Цинк теряет электроны быстрее, чем медь, а это означает, что раствор цинка и меди в растворах их солей вызовет поток электронов через внешний провод, который ведет к из цинка в медь по следующим реакциям:
Разница в коррозионном потенциале между двумя металлами обычно вызывает сценарий, называемый гальванической коррозией, названной в честь ее первооткрывателя Луиджи Гальвани.
Такая ситуация характерна для ячеек с естественной коррозией, где используется электролит, дополняющий ячейку для коррозии. Проводимость жидкой атмосферы, такой как почва, бетон или вода, обычно связана с ее коррозионной активностью.
Сокращенное описание в следующем уравнении действительно для каждой конфигурации ячейки Daniell.
Это уравнение идентифицирует цинковый электрод как анод, поскольку он отрицателен в случае спонтанной реакции, а медный электрод является катодом из-за его положительного заряда.
Анодный метод и коррозия
Теперь мы более подробно рассмотрим, что происходит на аноде после возникновения коррозии (анодный метод). Например, реакция коррозии железа (Fe), которая включает восстановление ионов водорода до газообразного водорода, согласуется с электрохимической реакцией цинка в хлористом водороде (HCl). Эта реакция выделения водорода происходит в различных металлах и кислотах и может включать соляную, серную, хлорную, плавиковую, муравьиную и альтернативные кислоты. Отдельные анодные реакции для железа, никеля и алюминия перечислены ниже:
Мы можем записать общую анодную реакцию, происходящую во время коррозии, рассмотрев приведенные выше уравнения как: с валентным зарядом n+ и, следовательно, с высвобождением «n» электронов. Ценность n, конечно, полностью зависит от характера металла. Некоторые металлы, такие как серебро, являются одновалентными, в то время как многовалентное железо, титан и уран обладают положительным зарядом до +6. Это уравнение является общим и применимо ко всем без исключения реакциям коррозии.
Ценность n, конечно, полностью зависит от характера металла. Некоторые металлы, такие как серебро, являются одновалентными, в то время как многовалентное железо, титан и уран обладают положительным зарядом до +6. Это уравнение является общим и применимо ко всем без исключения реакциям коррозии.
Закон Фарадея и электрохимия коррозии
Если бы ток, генерируемый одной из анодных реакций, описанных ранее, был известен, можно было бы преобразовать этот ток в аналогичную скорость потери массы или скорости проникновения коррозии, используя полезное соотношение, открытое Майклом Фарадеем. . (См. Преобразование скорости коррозии: простые способы преобразования данных между распространенными единицами измерения коррозии, чтобы узнать о скорости коррозии.) Эмпирические законы электролиза Фарадея связывают ток электрохимической реакции с количеством молей реагирующего элемента. Предположим, что заряд, необходимый для такой реакции, составляет один электрон на молекулу, как в случае гальваники или коррозионного воздействия серебра, это может быть показано как:
Согласно закону Фарадея, для реакции с одним молем серебра потребуется один моль электронов или одно число электронов Авогадро (6,022 x 10 23 ). Заряд, переносимый одним молем электронов, известен как один Фарадей (F). Один Фарадей равен 96 485 Кл/(моль электронов). Объединение основных представлений Фарадея с конкретными электрохимическими реакциями общепризнанной стехиометрии дает нам следующее уравнение:
Заряд, переносимый одним молем электронов, известен как один Фарадей (F). Один Фарадей равен 96 485 Кл/(моль электронов). Объединение основных представлений Фарадея с конкретными электрохимическими реакциями общепризнанной стехиометрии дает нам следующее уравнение:
Где:
N — число молей и Δ N — изменение этого количества
n — число электронов на молекулу реагирующего вещества
I — общий ток в амперах (А)
t – период электрохимического метода в секундах (с)
Катодный метод
Когда ионы водорода (H) восстанавливаются до своего атомарного типа, они обычно смешиваются, как показано ранее, с образованием газообразного водорода в результате реакции с электронами на катодной поверхности. Это восстановление ионов водорода на катодной поверхности может нарушить баланс между кислыми ионами водорода (H+) и образующими основания ионами гидроксила (OH-), делая раствор менее кислым, более щелочным или щелочным в этой области.
В нейтральной воде анодная коррозия некоторых металлов, таких как алюминий (Al), цинк (Zn) или магний (Mg), создает достаточно энергии для непосредственного отделения воды, как показано в следующем уравнении и на рисунке:
Рис. 2. Электрохимические реакции Mg при коррозии в нейтральной воде.
Изменение концентрации ионов H или увеличение содержания ионов гидроксила (OH) может быть выявлено путем измерения уровня pH для обнаружения поверхностей, на которых происходят катодные реакции. В процессе коррозии может происходить множество катодных реакций. Среди них:
Кислородное восстановление
Кислородное восстановление является обычной катодной реакцией, поскольку кислород присутствует в атмосфере и в растворах, подвергающихся воздействию окружающей среды. Хотя и нечасто, восстановление ионов металла и осаждение металла вызывают серьезные проблемы с коррозией, например: осаждение ионов меди, которые образуются перед водяным контуром, на внутренней алюминиевой поверхности радиатора. Поэтому, как правило, следует избегать использования медного трубопровода в контуре на водной основе, где также присутствует алюминий.
Поэтому, как правило, следует избегать использования медного трубопровода в контуре на водной основе, где также присутствует алюминий.
Все реакции коррозии представляют собой просто комбинации одной или многих из вышеперечисленных катодных реакций в сочетании с анодной реакцией. Таким образом, каждый случай жидкостной коррозии в большинстве случаев может быть сведен к этим уравнениям либо по отдельности, либо в комбинации. Учитывайте коррозию Zn (цинка) водой или влажным воздухом. Умножая реакцию окисления цинка на 2 и суммируя ее с реакцией восстановления кислорода, можно получить следующее уравнение:
Продуктами этой реакции являются Zn 2+ и OH — , которые сразу превращаются в нерастворимый Zn(OH) 2 . Аналогичным образом, коррозия Zn сульфатом меди, представленная в следующем уравнении, представляет собой просто суммирование реакции окисления Zn и реакции осаждения металла с участием ионов меди (II):
может иметь место реакция восстановления. Например, при коррозии Zn в концентрированном растворе соляной кислоты, содержащем растворенный кислород, возможны две катодные реакции. Один представляет собой выделение H, а другой — восстановление кислорода. Поскольку есть две катодные реакции или методы, которые потребляют электроны, общая скорость коррозии цинка завышена. Таким образом, он обычно более агрессивен, чем кислоты, не содержащие воздуха, и удаление кислорода из растворов кислот обычно может сделать эти растворы менее коррозионно-активными. Это типичный метод снижения коррозионной активности во многих условиях. Кислород можно удалить химическим или механическим путем.
Например, при коррозии Zn в концентрированном растворе соляной кислоты, содержащем растворенный кислород, возможны две катодные реакции. Один представляет собой выделение H, а другой — восстановление кислорода. Поскольку есть две катодные реакции или методы, которые потребляют электроны, общая скорость коррозии цинка завышена. Таким образом, он обычно более агрессивен, чем кислоты, не содержащие воздуха, и удаление кислорода из растворов кислот обычно может сделать эти растворы менее коррозионно-активными. Это типичный метод снижения коррозионной активности во многих условиях. Кислород можно удалить химическим или механическим путем.
Воздействие на площадь поверхности
При коррозии куска металла электроны, образующиеся в анодных областях, проходят через металл, реагируя на катодные области, которые в равной степени подвержены воздействию окружающей среды, где они восстанавливают электрический баланс системы. Сам факт отсутствия суммарного накопления зарядов на коррозионной поверхности имеет жизненно важное значение для понимания большинства процессов коррозии и способов их смягчения. Однако равенство между анодным и катодным токами, выраженное в следующем уравнении, не означает, что плотности тока для этих токов равны:
Однако равенство между анодным и катодным токами, выраженное в следующем уравнении, не означает, что плотности тока для этих токов равны:
Взяв относительные анодные (S a ) и катодные (S c ) площади поверхности (и связанные с ними плотности тока ia см ), это уравнение может быть выражено через плотности тока.
Важность отношения площади поверхности (S c /S a) в приведенном выше уравнении особенно важна, когда речь идет о нескольких разновидностях локальной коррозии, таких как точечная коррозия и коррозионное растрескивание под напряжением. (Дополнительную информацию о коррозионном растрескивании под напряжением см. в разделе Что вызывает коррозионное растрескивание под напряжением в трубопроводах?) Это также имеет большое значение для возникновения коррозии в разнородных металлах.
Легко понять, что результат определенного количества анодного тока, сфокусированного на небольшом участке поверхности металла, будет намного больше, чем когда такое же количество тока рассеивается на гораздо большей площади.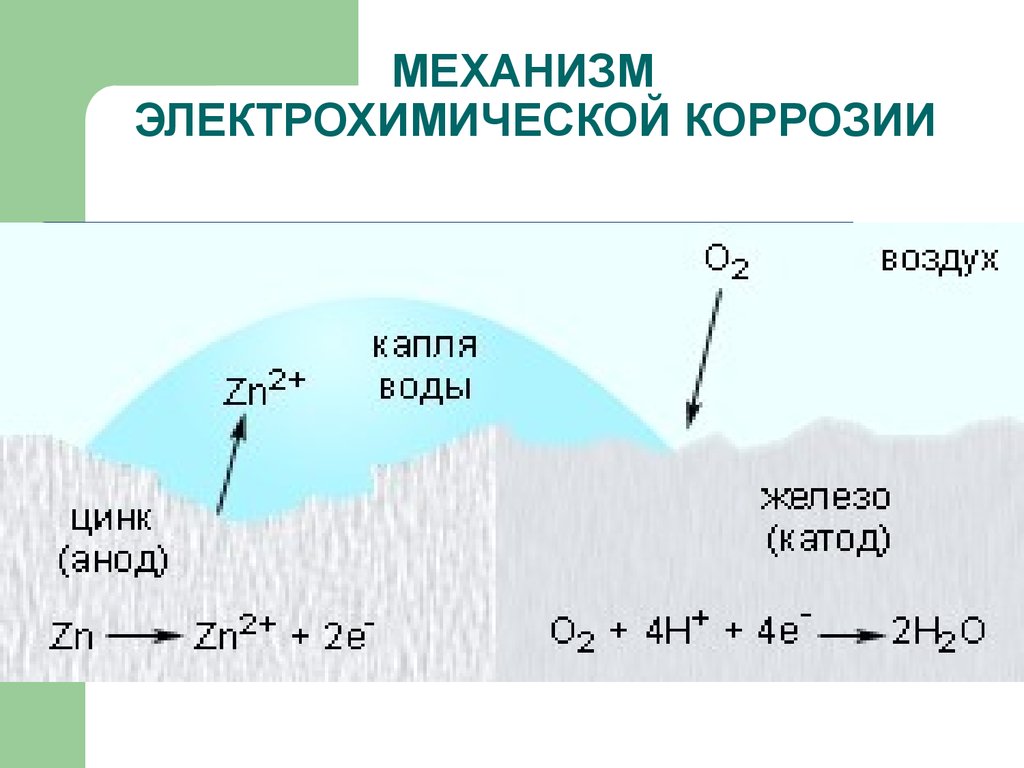 Это важная проблема усиления анодного тока, когда S c /S a больше единицы, и фактор подавления, когда он меньше единицы.
Это важная проблема усиления анодного тока, когда S c /S a больше единицы, и фактор подавления, когда он меньше единицы.
Причину плотности тока можно увидеть при соединении двух разнородных металлов (здесь это Cu и Fe), что схематично показано на рисунке 3 ниже.
Рис. 3. Области, затронутые разнородными металлами, где «а» показывает заклепки из стали на медных пластинах, а «б» показывает заклепки из меди на стальных пластинах.
Когда стальные заклепки являются частью медных пластин, коррозия катодных медных пластин будет низкой, а коррозия малых заклепок из анодной стали будет высокой. С другой стороны, если медные заклепки соединяют стальные пластины, коррозия меди будет высокой, а коррозия стальных пластин едва заметна.
Ключ к пониманию предотвращения коррозии
В этой статье мы рассмотрели коррозию как электрохимическое явление, при котором материалы/конструкции разрушаются. Подробно рассмотрены электрохимические реакции коррозии с помощью ячейки Даниэля, анодного метода, катодного метода, законов Фарадея и эффектов площади поверхности. Поскольку мы можем предотвратить коррозию, если хорошо понимаем электрохимию коррозии, производители и пользователи продуктов коррозии должны быть внимательны к электрохимическим механизмам коррозии.
Подробно рассмотрены электрохимические реакции коррозии с помощью ячейки Даниэля, анодного метода, катодного метода, законов Фарадея и эффектов площади поверхности. Поскольку мы можем предотвратить коррозию, если хорошо понимаем электрохимию коррозии, производители и пользователи продуктов коррозии должны быть внимательны к электрохимическим механизмам коррозии.
Реклама
Связанные термины
- Электрохимическая реакция
- Закон Фарадея
- Анод
- Катод
- Окисление
- Сокращение
- Гальваническая коррозия
- Площадь воздействия
- Дэниел Сотовый
- Валентность
Поделиться этой статьей
Электрохимические испытания на коррозию | Анализ электрохимической коррозии
Описание метода
Вся коррозия представляет собой электрохимический процесс реакций окисления и восстановления. Когда происходит коррозия, электроны высвобождаются металлом (окисление) и приобретаются элементами (восстановление) в корродирующем растворе. Поскольку в реакции коррозии присутствует поток электронов (ток), его можно измерять и контролировать с помощью электроники. Таким образом, контролируемые электрохимические экспериментальные методы могут быть использованы для характеристики коррозионных свойств металлов и металлических компонентов в сочетании с различными растворами электролитов. Характеристики коррозии уникальны для каждой системы металл/раствор.
Когда происходит коррозия, электроны высвобождаются металлом (окисление) и приобретаются элементами (восстановление) в корродирующем растворе. Поскольку в реакции коррозии присутствует поток электронов (ток), его можно измерять и контролировать с помощью электроники. Таким образом, контролируемые электрохимические экспериментальные методы могут быть использованы для характеристики коррозионных свойств металлов и металлических компонентов в сочетании с различными растворами электролитов. Характеристики коррозии уникальны для каждой системы металл/раствор.
В практике тестирования используется поляризационная ячейка, состоящая из раствора электролита, электрода сравнения, противоэлектрода(ов) и исследуемого металлического образца, соединенного с держателем образца. (Образец называется рабочим электродом.) Электроды подключены к электронному прибору, называемому потенциостатом. Рабочий электрод, электрод сравнения и счетный электрод помещаются в раствор электролита, обычно раствор, который наиболее точно соответствует реальной среде применения испытуемого материала. В растворе между различными электродами создается электрохимический потенциал (напряжение). Потенциал коррозии (E CORR ) измеряется потенциостатом как разность энергий между рабочим электродом и электродом сравнения.
В растворе между различными электродами создается электрохимический потенциал (напряжение). Потенциал коррозии (E CORR ) измеряется потенциостатом как разность энергий между рабочим электродом и электродом сравнения.
Эксперименты по электрохимической коррозии измеряют и/или контролируют потенциал и ток реакций окисления/восстановления. Можно провести несколько типов экспериментов, манипулируя этими двумя переменными и измеряя их.
В большинстве экспериментов к рабочему электроду прикладывается потенциал и измеряется результирующий ток. Потенциостатический эксперимент прикладывает постоянный потенциал к рабочему электроду в течение определенного периода времени. Измеренный ток отображается в зависимости от времени.
Для потенциодинамических экспериментов приложенный потенциал увеличивается со временем, в то время как ток постоянно контролируется. Ток (или плотность тока) отображается в зависимости от потенциала. После сканирования потенциала до заданной плотности тока или потенциала, сканирование потенциала может быть реверсировано, в то время как ток продолжает измеряться. Подобное потенциодинамическое сканирование называется обратной поляризацией или циклической поляризацией.
Подобное потенциодинамическое сканирование называется обратной поляризацией или циклической поляризацией.
Также возможно контролировать ток и измерять результирующий потенциал. Эксперименты, в которых накладывается ток, а не потенциал, называются гальванодинамическими или гальваностатическими. Гальванодинамические методы отображают изменение потенциала в зависимости от контролируемого тока. Гальваностатические тесты поддерживают постоянный ток и отображают изменение потенциала в зависимости от времени.
Аналитическая информация
Потенциодинамические эксперименты могут предоставить различные данные, связанные с точечной, щелевой коррозией и пассивацией для определенных комбинаций образец/раствор. По мере увеличения потенциала точечная коррозия начинается при определенном значении, известном как потенциал пробоя (E B , самый низкий потенциал, при котором возникает точечная коррозия). Поскольку питтинговая коррозия связана с увеличением скорости окисления, E B определяется соответствующим увеличением измеренного тока. Увеличение Е B ассоциируется с более высокой стойкостью к точечной коррозии. По мере уменьшения потенциала при обратном сканировании происходит уменьшение тока. Однако для обратного сканирования наблюдается гистерезис и прослеживается петля гистерезиса. Образец репассивируется при потенциале, при котором обратное сканирование пересекает прямое сканирование. Потенциал репассивации, или защитный потенциал (E P ), возникает при более низком потенциале, чем E B . Отличие Е В и E P относится к восприимчивости к щелевой коррозии; чем больше гистерезис на поляризационной кривой, тем больше подверженность щелевой коррозии.
Поскольку питтинговая коррозия связана с увеличением скорости окисления, E B определяется соответствующим увеличением измеренного тока. Увеличение Е B ассоциируется с более высокой стойкостью к точечной коррозии. По мере уменьшения потенциала при обратном сканировании происходит уменьшение тока. Однако для обратного сканирования наблюдается гистерезис и прослеживается петля гистерезиса. Образец репассивируется при потенциале, при котором обратное сканирование пересекает прямое сканирование. Потенциал репассивации, или защитный потенциал (E P ), возникает при более низком потенциале, чем E B . Отличие Е В и E P относится к восприимчивости к щелевой коррозии; чем больше гистерезис на поляризационной кривой, тем больше подверженность щелевой коррозии.
Эксперименты по электрохимической коррозии также можно использовать для определения скорости коррозии (график Тафеля), активных/пассивных характеристик для конкретной системы образец/раствор, скорости пассивации, а также анодной и катодной защиты.
Типичные области применения
- Анализ готовых медицинских изделий на восприимчивость к точечной и щелевой коррозии
- Сравнение сырья (сортировка) по коррозионным характеристикам
- Оценка влияния пассивации или модификации поверхности на коррозионное поведение
- Оценка/Сравнение влияния обработки на коррозионные свойства
- Оценка комбинаций биметаллов на гальваническую коррозию
Требования к образцам
Образцы для испытаний на электрохимическую коррозию должны быть электрическими проводниками и должны быть достаточно малы, чтобы поместиться в поляризационной ячейке. Компоненты можно тестировать как целиком, так и в виде небольшой секции. Металлические купоны изготавливаются специально для некоторых испытаний.
Металлические купоны изготавливаются специально для некоторых испытаний.
Chem1 Электрохимическая коррозия
Коррозию можно определить как разрушение материалов в результате химических процессов. Из них на сегодняшний день наиболее важной является электрохимическая коррозия металлов, при которой процесс окисления M → M n + + n e n – облегчается наличием подходящего акцептора электронов, иногда упоминается в науке о коррозии как деполяризатор .
В некотором смысле коррозию можно рассматривать как самопроизвольный возврат металлов в их руды; огромное количество энергии, затраченной на добычу, очистку и производство металлов в полезные предметы, рассеивается множеством различных путей.
Хорошим справочником по этой теме является Corrosion and Corrosion Control: An Introduction to Corrosion Science and Engineering (4th Ed), R.W. Revie и H.H. Uhlig.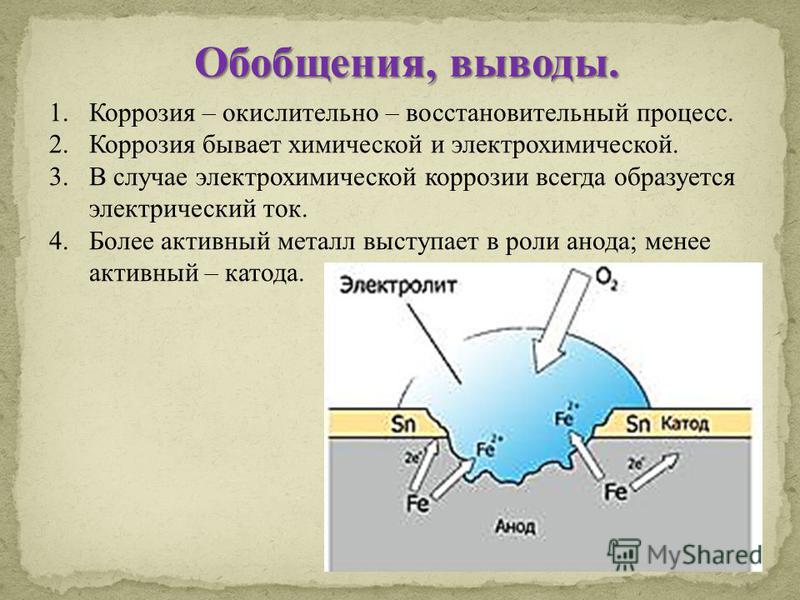 Ограниченные части его можно увидеть на этом сайте Google Книги.
Ограниченные части его можно увидеть на этом сайте Google Книги.
Экономические аспекты коррозии намного значительнее, чем думает большинство людей; согласно отчету за 2001 год, стоимость коррозии только в США составляла 276 миллиардов долларов в год. Из них около 121 миллиарда долларов было потрачено на борьбу с коррозией, а разница в 155 миллиардов долларов осталась чистым убытком для экономики.
Коммунальные услуги, особенно системы питьевого водоснабжения и канализации, испытывают наибольшее экономическое воздействие,
с автомобилями и транспортом, занимающим второе место.
На этом снимке показана внутренняя часть торгового центра Algo Center в Эллиот-Лейк, Онтарио, после того, как в июне 2012 года часть парковки на крыше обрушилась на первый этаж, в результате чего погибли два человека. Основной причиной обрушения этой и очень большого количества других парковочных конструкций в холодном климате было попадание дорожной соли в настил, что привело к электрохимической коррозии стальных арматурных стержней, заделанных в бетон. Однако настоящей причиной был человеческий фактор ; Проблемы с протечками с настила крыши возникали почти с момента постройки здания в 1970-х годах, но стоимость надлежащей обработки этих утечек (например, нанесение защитного покрытия на настил) удержала владельцев торговых центров от этих инвестиций. (Подробнее здесь)
Однако настоящей причиной был человеческий фактор ; Проблемы с протечками с настила крыши возникали почти с момента постройки здания в 1970-х годах, но стоимость надлежащей обработки этих утечек (например, нанесение защитного покрытия на настил) удержала владельцев торговых центров от этих инвестиций. (Подробнее здесь)
1 Коррозионные клетки и реакции
Особенностью большинства процессов коррозии является то, что стадии окисления и восстановления происходят в разных местах металла. Это возможно, потому что металлы являются проводящими, поэтому электроны могут течь через металл от анодных к катодным областям. Присутствие воды необходимо для переноса ионов к металлу и от него, но тонкой пленки адсорбированной влаги может быть достаточно.
Коррозионную систему можно рассматривать как короткозамкнутую электрохимическую ячейку, в которой анодный процесс выглядит примерно так: Катодные шаги могут быть любыми из
O 2 + 2 H 2 O + 4 E — → 4 OH —
H + + E –4 + + E –9 № ½ ½ ½ ½ ½ ½ ½ ½ ½ ½ . 2 (г)
2 (г)
M 2+ + 2 e – → M (s)
где M – металл.
Коррозия часто начинается в месте ( 1 ), где металл находится под напряжением (на изгибе или сварке) или изолирован от воздуха (где соединяются два куска металла или под слабо прилипшей пленкой краски). ионы металлов растворяются в пленке влаги, а электроны мигрируют в другое место ( 2 ), где их поглощает деполяризатор . Кислород является наиболее распространенным деполяризатором; полученные ионы гидроксида реагируют с Fe 2+ с образованием смеси водных оксидов железа, известной как ржавчина .
Какие части металла служат анодами, а какие катодами, может зависеть от многих факторов, как видно из обычно наблюдаемых неравномерных картин коррозии. Атомы в областях, подвергшихся напряжению, которые могут быть получены путем формовки или механической обработки, часто имеют более высокую свободную энергию и, таким образом, имеют тенденцию становиться анодными.
[ссылка]
Если одна часть металлического предмета защищена от атмосферы так, что недостаточно O 2 для создания или поддержания оксидной пленки, эта «защищенная» область часто будет местом, где коррозия наиболее активна. Тот факт, что такие места обычно скрыты от глаз, объясняет большую часть трудностей в обнаружении коррозии и борьбе с ней.
Большинство металлов покрыты тонкой оксидной пленкой, препятствующей анодному растворению. Когда коррозия все-таки происходит, она иногда выдалбливает узкую дыру или яма в металле. Дно этих ямок, как правило, лишено кислорода, что способствует дальнейшему прорастанию ямок в металл.
Тенденция мест, лишенных кислорода, к анодированию является причиной многих широко наблюдаемых моделей коррозии
В отличие от анодных участков, которые, как правило, локализованы в определенных областях поверхности, катодная часть процесса может происходить практически где угодно. Поскольку оксиды металлов обычно являются полупроводниками, большинство оксидных покрытий не препятствуют потоку электронов к поверхности, поэтому почти любая область, которая подвергается воздействию O 2 или какой-либо другой акцептор электронов может выступать в качестве катода.
Поскольку оксиды металлов обычно являются полупроводниками, большинство оксидных покрытий не препятствуют потоку электронов к поверхности, поэтому почти любая область, которая подвергается воздействию O 2 или какой-либо другой акцептор электронов может выступать в качестве катода.
Любой, кто владел старым автомобилем, видел коррозию на стыках между деталями кузова и под лакокрасочным покрытием. Вы также заметите, что как только начинается коррозия, она имеет тенденцию питаться сама собой. Одна из причин этого заключается в том, что одним из продуктов реакции восстановления O 2 является гидроксид-ион. Высокий уровень pH, создаваемый в этих катодных областях, имеет тенденцию разрушать защитную оксидную пленку и может даже смягчить или ослабить пленки краски, так что эти участки могут стать анодными. Большее поступление электронов способствует более интенсивному катодному действию, что порождает еще больше анодных участков и т.д.
Очень распространенной причиной коррозии является контакт двух разнородных металлов, что может произойти вблизи крепежных деталей или сварных швов. В месте соединения собирается влага, действующая как электролит и образующая ячейку, в которой два металла служат электродами. Влага и токопроводящие соли на внешних поверхностях образуют внешний токопроводящий путь, эффективно замыкая элемент накоротко и вызывая очень быструю коррозию; Вот почему автомобили так быстро ржавеют в тех местах, где дороги посыпают солью, чтобы растопить лед.
В месте соединения собирается влага, действующая как электролит и образующая ячейку, в которой два металла служат электродами. Влага и токопроводящие соли на внешних поверхностях образуют внешний токопроводящий путь, эффективно замыкая элемент накоротко и вызывая очень быструю коррозию; Вот почему автомобили так быстро ржавеют в тех местах, где дороги посыпают солью, чтобы растопить лед.
Коррозия разнородных металлов может возникнуть, даже если два металла изначально не находились в прямом контакте. Например, в домах, где для водопровода используются медные трубы, в воде всегда присутствует небольшое количество растворенного Cu 2+ . Когда эта вода сталкивается со стальными трубами или хромированным e- сливом раковины в ванной комнате, более благородная медь оседает на другом металле, создавая новую ячейку коррозии металлов в контакте. В случае хромированной фурнитуры для ванных комнат это приводит к образованию Cr 9.0051 3+ соли, выпадающие в осадок в виде зеленоватых пятен.
2 Контроль коррозии
Поскольку для возникновения коррозии должны иметь место как катодная, так и анодная стадии, предотвращение любой из них остановит коррозию. Наиболее очевидная стратегия — остановить оба процесса, покрыв объект краской или другим защитным покрытием. Даже если это будет сделано, вероятно, будут места, где покрытие сломано или не проникает, особенно если есть отверстия или резьба.
Более сложный подход состоит в том, чтобы нанести на металл небольшой отрицательный заряд, что затруднит протекание реакции M → M 2+ + 2 e – .
видео по электрохимической коррозии:
Химия ржавчины и коррозии (Джейсон Гуди, 12½ м)
Коррозия и разложение инфраструктуры (GeoChannel, 43 м)
Эффект покрытия железа менее активным металлом дает интересный контраст. Хорошим примером является обычная луженая банка (справа). Пока оловянное покрытие остается неповрежденным, все в порядке, но воздействие влажной атмосферы даже на крошечную часть нижележащего железа вызывает коррозию. Электроны, выпущенные из железа, перетекают в олово, делая железо более анодным, так что теперь олово активно способствует коррозии железа! Вы, наверное, замечали, как быстро разлагаются жестяные банки, оставленные на открытом воздухе.
Электроны, выпущенные из железа, перетекают в олово, делая железо более анодным, так что теперь олово активно способствует коррозии железа! Вы, наверное, замечали, как быстро разлагаются жестяные банки, оставленные на открытом воздухе.
Более изощренная стратегия заключается в поддержании постоянного отрицательного
электрический заряд на металле, так что его растворение в виде положительных ионов
ингибируется. Так как вся поверхность вдавлена в катодную
состоянии, этот метод известен как катодная защита .
Источником электронов может быть внешний источник питания постоянного тока.
(обычно используется для защиты нефтепроводов и других заглубленных сооружений),
или это может быть коррозия другого, просто куска более активного металла, такого как цинк или алюминий, закопанного в землю поблизости.
3 Галерея ужасов коррозии
Разъедание ногтя
Ногти погружают в агар, который образует влажный твердый гель. Агар также содержит фенолфталеин и гексацианожелезо (III).
Агар также содержит фенолфталеин и гексацианожелезо (III).
Fe(CN6) – образует темно-синий цвет («берлинская лазурь») в присутствии Fe2+. Синие цвета явно связаны с теми участками ногтя, которые подверглись нагрузке, что способствует анодному высвобождению Fe2+ из металла. Розовым цветом показаны катодные области, которые стали щелочными в результате реакции.
O2 + 2 h3O + 4e– → 4 OH–
Это ясно показывает разделение анодных и катодных процессов в коррозии.
Внутренняя часть водопроводной магистрали
Если вы живете в старой части города, где водопроводу 50-100 лет, вода, которую вы пьете, вполне могла пройти по трубе в таком состоянии! Подобная сильная коррозия чаще встречается в районах с кислой водой. Такая вода происходит от горного снеготаяния и стока, а свою кислотность обычно приобретает от растворенного атмосферного углекислого газа.
Воды рек, озер и особенно подземные воды из колодцев обычно достаточно долго контактировали с карбонатсодержащими отложениями, чтобы быть нейтрализованными.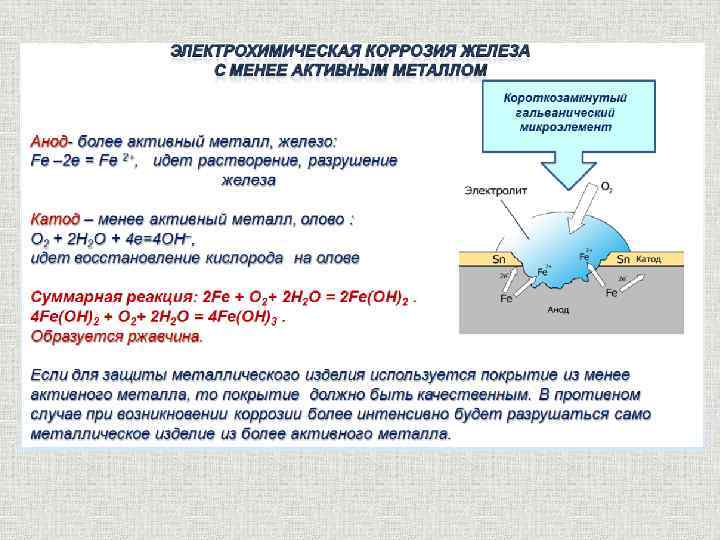 Администраторы водопроводных сооружений любят делать воду слегка щелочной и слегка перенасыщенной карбонатом кальция, чтобы сохранить тонкий слой твердого карбоната на внутренней части трубы, который защищает ее от коррозии.
Администраторы водопроводных сооружений любят делать воду слегка щелочной и слегка перенасыщенной карбонатом кальция, чтобы сохранить тонкий слой твердого карбоната на внутренней части трубы, который защищает ее от коррозии.
Стальные арматурные стержни, встроенные в бетон
Все большие бетонные конструкции содержат стальные арматурные стержни («арматурные стержни»), которые помогают обеспечить целостность конструкции при различных условиях нагрузки и особенно во время землетрясений. Проникновение воды, даже в виде тумана или дымки, может привести к серьезным коррозионным повреждениям, как видно на этом изображении этой колонны, поддерживающей эстакаду.\\
Коррозия металлических соединений
На рисунке показаны два элемента стальной конструкции, соединенные чугунными фланцами, скрепленными болтами. По какой-то причине одна из частей стала более анодированной, чем другая, что привело к обширной коррозии верхней части.
Коррозия, вызванная почвенными бактериями перенос электронов на O2. Он также окисляет серу, образуя серную кислоту. Образовавшийся химический коктейль проел дыру в трубе.
Эти оцинкованные болты использовались для соединения деревянных балок. Последующее перемещение балок из-за различных условий нагрузки привело к истиранию цинкового покрытия. Недостаток кислорода вблизи центров болтов также, вероятно, способствовал коррозии, препятствуя образованию защитной оксидной пленки.
Коррозия из-за недостатка кислорода
Эти оцинкованные болты использовались для соединения деревянных балок. Последующее перемещение балок из-за различных условий нагрузки привело к истиранию цинкового покрытия. Недостаток кислорода вблизи центров болтов также, вероятно, способствовал коррозии, препятствуя образованию защитной оксидной пленки.
Точечная коррозия поверхности
Питтинговая коррозия имеет тенденцию образовывать узкие, но глубокие отверстия («ямки») на поверхности, которые трудно обнаружить, особенно когда они покрыты продуктами коррозии.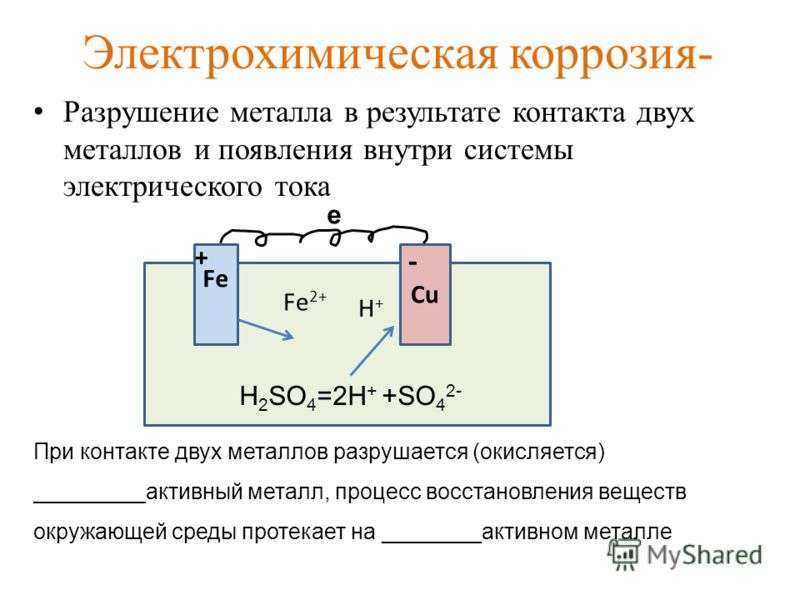 Как только яма образуется, она имеет тенденцию копаться глубже из-за более медленной диффузии кислорода в узкое дно ямы.
Как только яма образуется, она имеет тенденцию копаться глубже из-за более медленной диффузии кислорода в узкое дно ямы.
Нержавеющая сталь не полностью защищена от коррозии
Стальные сплавы, содержащие 13–26 весовых процентов хрома, образуют тонкий, хорошо прилипающий поверхностный слой Cr 2 O 3 при воздействии воздуха, в результате чего они становятся пассивированными и устойчивыми к коррозии. Но для того, чтобы сохранить это сопротивление, кислород должен оставаться доступным на поверхности.
Если это условие не соблюдается, пассивирующая пленка может разрушиться, как это произошло с этим фланцем, подвергшимся обширной точечной коррозии. Ионы хлорида также могут разрушить защитную пленку, хотя существуют специальные марки нержавеющей стали для использования в морских условиях, которые более устойчивы к этому эффекту.
Особую осторожность следует соблюдать при соединении нержавеющих сталей с другими конструкциями. Чрезмерное затягивание гаек на этом кронштейне могло повредить пленку Cr 2 O 3 ; использование крепежных винтов и гаек, отличных от SS, гарантировало бы обычную гальваническую коррозию.
Чрезмерное затягивание гаек на этом кронштейне могло повредить пленку Cr 2 O 3 ; использование крепежных винтов и гаек, отличных от SS, гарантировало бы обычную гальваническую коррозию.
Что вы должны уметь делать
Убедитесь, что вы полностью понимаете следующие основные понятия, представленные выше.
- Электрохимическая коррозия металлов происходит, когда электроны от атомов на поверхности металла переносятся на подходящий акцептор электронов или деполяризатор . Вода должна присутствовать, чтобы служить средой для переноса ионов.
- Наиболее распространенными деполяризаторами являются кислород, кислоты и катионы менее активных металлов.
- Поскольку электроны проходят через сам металлический объект, анодная и катодная области (две половины электрохимической ячейки) могут находиться далеко друг от друга.
- Анодные области имеют тенденцию развиваться в местах, где металл находится под напряжением или защищен от кислорода.

- Контакт с другим металлом, прямой или косвенный, может привести к коррозии более активного металла.
- Коррозию стали можно подавить с помощью цинкования , т. е. путем покрытия ее цинком, более активным металлом, растворение которого оставляет на металле отрицательный заряд, препятствующий дальнейшему растворению Fe 2+ .
- Катодная защита с использованием внешнего источника напряжения широко применяется для защиты подземных сооружений, таких как резервуары, трубопроводы и опоры. Источником может быть расходуемый анод из цинка или алюминия, сетевой или фотогальванический источник питания.
Каталожные номера
Превосходный иллюстрированный учебник по коррозии и катодной защите
Хорошие схематические иллюстрации различных причин коррозии
Обзор различных форм коррозии (с фотографиями)
Проблемы коррозии, связанные с железобетоном
Почему нержавеющая сталь является нержавеющей?
Концептуальная карта
Коррозия металлов
Теория коррозии металлов
Коррозия определяется как воздействие на материал в результате
химическая, часто электрохимическая реакция с окружающей средой.
Согласно этому определению, термин коррозия может применяться ко всем
материалов, в том числе неметаллов. Но на практике слово коррозия в основном используется в
сочетание с металлическими материалами.
Почему металлы ржавеют? Помимо золота, платины и некоторых других,
металлы не встречаются в природе в чистом виде. Они обычно
химически связанные с другими веществами в рудах, такими как сульфиды, оксиды и т. д.
Энергия должна быть затрачена (например, в доменной печи) для извлечения металлов из
сульфиды, оксиды и др. для получения чистых металлов.
Чистые металлы содержат больше связанной энергии, т.
более высокое энергетическое состояние, чем то, что встречается в природе в виде сульфидов или оксидов.
Энергетическое состояние металла в различных формах
Поскольку весь материал во Вселенной стремится вернуться к своему низшему
энергетическое состояние, чистые металлы также стремятся вернуться в свое самое низкое энергетическое состояние.
которые они имели в виде сульфидов или оксидов. Один из способов, которыми металлы могут
возврат к низкому энергетическому уровню происходит за счет коррозии. Продукты коррозии из
металлы часто представляют собой сульфиды или оксиды.
Химическая и электрохимическая коррозия
Химическая коррозия может рассматриваться как окисление и возникает под действием
сухих газов, часто при высоких температурах. С другой стороны, происходит электрохимическая коррозия.
электродными реакциями, часто во влажной среде, т. е. влажной коррозией.
Все металлы в сухом воздухе покрыты очень тонким слоем оксида,
около 100 (10 -2 м) толщ. Этот слой образован химическим
коррозия кислородом воздуха. При очень высоких температурах реакция
с кислородом в воздухе может продолжаться без ограничений, и металл быстро превратится в
оксид.
Окисление металла при различных температурах
При комнатной температуре реакция прекращается, когда слой становится тонким. Эти
Эти
тонкие слои оксида могут защитить металл от продолжительного воздействия, т.е. в
водный раствор. На самом деле это и есть эти слои оксида
и/или продукты коррозии, образующиеся на поверхности металла, защищающего
металл от продолжающегося воздействия в гораздо большей степени, чем коррозия
сопротивление самого металла.
Эти слои оксида могут быть более или менее прочными в
вода, например. Мы знаем, что обычная углеродистая сталь быстрее корродирует в воде.
чем нержавеющая сталь. Разница зависит от состава и
проницаемость их соответственно оксидных слоев. Следующее описание
явление коррозии будет иметь дело только с электрохимической коррозией, т.е.
мокрая коррозия.
Ячейки коррозии
Как корродируют металлы в жидкостях? Проиллюстрируем это,
с использованием явления коррозии, называемого биметаллической коррозией или гальванической коррозией.
Биметаллическая коррозионная ячейка может, например. состоит из стальной пластины и медной пластины
находящиеся в электрическом контакте друг с другом и погруженные в водный раствор
(электролит).
Электролит содержит растворенный кислород воздуха
и растворенная соль. Если лампа подключена между стальной пластиной и
медная пластина, она загорится. Это указывает на то, что ток течет между
металлические пластины. Медь будет положительным электродом, а сталь
быть отрицательным электродом.
Ток течет через лампу от медной пластины к стальной пластине
Движущей силой тока является разность электрических
потенциал между медью и сталью. Цепь должна быть замкнута и
следовательно, ток будет течь в жидкости (электролите) от стальной пластины.
к медной пластине. Течение тока происходит по положительно заряженным
атомы железа (ионы железа) покидают стальную пластину, и стальная пластина подвергается коррозии.
Поверхность металла, подверженная коррозии, называется анодом. Кислород
и вода потребляются на поверхности медной пластины и ионы гидроксила
(OH-), которые заряжены отрицательно. Отрицательные гидроксильные ионы
«нейтрализовать» положительно заряженные атомы железа. Ионы железа и гидроксила образуют
Ионы железа и гидроксила образуют
гидроксид железа (ржавчина).
В коррозионной ячейке, описанной выше, металлическая медь
называется катодом. Обе металлические пластины называются электродами.
определение анода и катода дано ниже.
Анод : Электрод, от которого течет положительный ток
в электролит.
Катод : Электрод, через который проходит положительная электрическая
ток уходит из электролита.
Когда положительные атомы железа переходят в раствор со стальной пластины,
электроны остаются в металле и переносятся в противоположном направлении, к
положительный ток.
Предпосылки для
образования биметаллической ячейки являются:
1. Электролит
2. Анод
3. Катод
4. Окислительная среда, такая как растворенный кислород (O 2 ) или ионы водорода.
(Н + ).
Потенциал электрода — серия Galvanic
В приведенном выше примере
было показано, что движущая сила течения тока и, следовательно,
коррозия — это разность электродных потенциалов.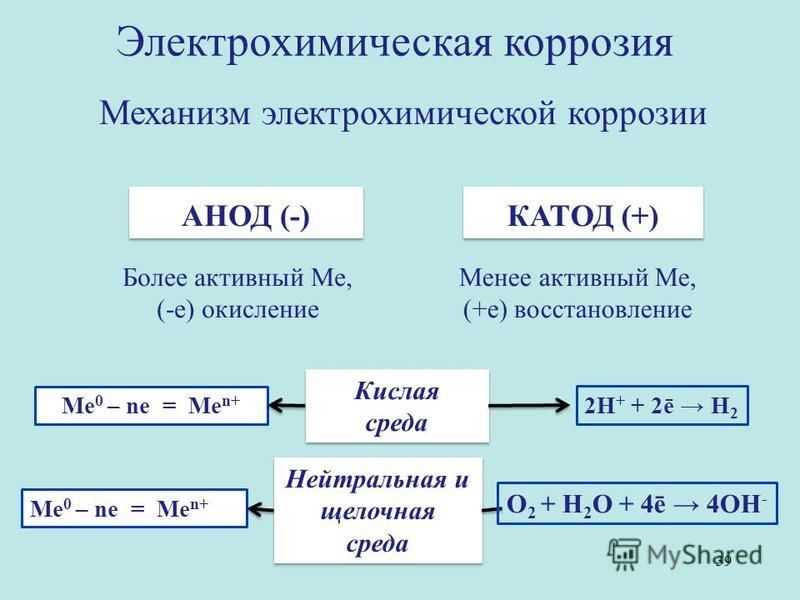 Электродный потенциал
Электродный потенциал
металл указывает на склонность металла к растворению и коррозии.
в определенном электролите.
Упоминается также «благородство» металла. Чем благороднее
металла, чем выше потенциал, тем меньше склонность к
растворяться в электролите.
Электродные потенциалы различных металлов могут быть указаны в
относительно друг друга в гальваническом ряду для разных электролитов.
гальванический ряд различных металлов в морской воде показан ниже.
Золото | +0,42 |
| Серебро | +0,19 |
Нержавеющая сталь (AISI 304), пассивное состояние | +0,09 |
| Медь | +0,02 |
| Олово | -0,26 |
Нержавеющая сталь (AISI 304), активное состояние | -0,29 |
| Свинец | -0,31 |
| Сталь | -0,46 |
| Кадмий | -0,49 |
| Алюминий | -0,51 |
| Оцинкованная сталь | -0,81 |
| Цинк | -0,86 |
| Магний | -1,36 |
Учитывая сталь-медь
Например, из приведенной выше таблицы следует, что медь имеет более высокий потенциал (соответствует
благороднее), чем обычная углеродистая сталь. Сталь будет анодом и будет корродировать,
Сталь будет анодом и будет корродировать,
тогда как медь будет катодом и не будет подвергаться коррозии.
Коррозия в микроячейках
сталь-медь
пример показал, как происходит коррозия, когда два различных материала
связаны в водном растворе. Как происходит коррозия на поверхности
из одного металла? Когда поверхность металла исследуют под микроскопом,
будет видно, что это не единый однородный металл. Различия в
структура и размер зерна возникают на поверхности. Химический состав может
различаются и могут присутствовать различные примеси.
Если электродный потенциал измеряется на внешнем
однородной поверхности, будет обнаружено, что она значительно различается только в областях
доли квадратного миллиметра. Итак, катоды и аноды, возможно, небольшие, но
достаточно большие, чтобы вызвать коррозию, могут образовываться на одной и той же металлической поверхности.
При анодной и катодной реакциях образовалась коррозионная микроячейка.
описано ниже.
Анодная часть поверхности корродирована
В случае низкого рН катодная реакция будет: 2e — +
2H + → H 2 . Поверхность катода может быть
Поверхность катода может быть
примеси, такие как оксидные включения, прирост графита или более благородная фаза.
Вернуться к: Джером Крюгер Улик Р. Эванс, британский ученый, которого считают «отцом науки о коррозии», сказал, что «коррозия в значительной степени представляет собой электрохимическое явление, [которое] можно определить как разрушение электрохимическими или химическими агентами …». Коррозия в водной среде и в атмосферной среде (которая также включает тонкие водные слои) является электрохимическим процессом, поскольку коррозия включает перенос электронов между металлической поверхностью и водным раствором электролита. Хотя в последние годы термин «коррозия» применялся ко всем видам материалов во всех средах, в этой статье будет рассматриваться только электрохимия коррозии металлов и сплавов в водных растворах при температуре окружающей среды. Протекающая в таких условиях электрохимическая коррозия является крупным разрушительным процессом, приводящим к таким дорогостоящим, неприглядным и разрушительным последствиям, как образование ржавчины и других продуктов коррозии, образование зияющих дыр или трещин в самолетах, автомобилях, лодках, водосточных желобах, экранах. , сантехника и многие другие предметы, сделанные из любого металла, кроме золота. Такие системы, как ядерные реакторы с кипящей водой, использующие водные растворы, также являются примерами электрохимической коррозии, но не будут рассматриваться. В этой статье также не будет рассматриваться неэлектрохимический процесс, называемый высокотемпературным окислением, деструктивный процесс, представляющий собой воздействие на металл или сплав высоких температур в газовой среде (обычно включая кислород или газы с серосодержащими соединениями), где более толстые слои образуются продукты коррозии. Однако следует отметить, что если процесс высокотемпературного окисления приводит к образованию солевых слоев, плавящихся при используемых высоких температурах, то разница в электродном потенциале между фазами или неоднородности в сплаве могут привести к горячей коррозии, имеющей электрохимические особенности. аналогично пленкам конденсированной воды, участвующим в атмосферной коррозии. Этот технологически важный коррозионный процесс приводит к выходу из строя таких устройств, как газовые турбины, теплообменники и многих других, работающих при высоких температурах. Последствия коррозииКоррозия имеет много серьезных последствий для экономики, здоровья, безопасности, технологий и культуры для нашего общества. Экономические эффекты Исследования в ряде стран пытались определить национальную стоимость коррозии. Самым обширным из этих исследований было исследование, проведенное в Соединенных Штатах в 1976 году, которое показало, что общие ежегодные затраты на металлическую коррозию для экономики США составляют 70 миллиардов долларов, или 4,2% валового национального продукта. Чтобы почувствовать серьезность этой потери, мы можем сравнить ее с другим экономическим воздействием, которое всех беспокоит — импортом иностранной сырой нефти, который стоил 45 миллиардов долларов в 1919 году.77. Влияние на здоровье В последние годы все чаще используются металлические протезы в организме, такие как штифты, пластины, тазобедренные суставы, кардиостимуляторы и другие имплантаты. Были разработаны новые сплавы и улучшенные методы имплантации, но коррозия продолжает создавать проблемы. Защитные эффекты Еще более серьезной проблемой является коррозия конструкций, которая может привести к тяжелым травмам или даже гибели людей. На безопасность влияет коррозия, способствующая выходу из строя мостов, самолетов, автомобилей, газопроводов и т. д. всего комплекса металлических конструкций и устройств, из которых состоит современный мир. Технологические эффекты Экономические последствия коррозии сказываются на технологии. Культурные предметы Международную обеспокоенность вызвало сообщение о серьезном ухудшении художественно и культурно значимых позолоченных бронзовых статуй в Венеции, Италия. Коррозионные процессы ускорят износ драгоценных артефактов, таких как те, что находятся в Венеции, из-за сильно загрязненной окружающей среды, которая сейчас распространена в большинстве стран мира. Точно так же в музеях мира консерваторы и реставраторы трудятся, чтобы защитить культурные ценности от разрушительного действия коррозии или удалить ее следы с художественных или культурно важных артефактов. Электрохимия коррозииОдна и та же металлическая поверхность, подверженная воздействию водного электролита, обычно имеет места для окисления (или анодной химической реакции), в результате которого в металле образуются электроны, и для восстановления (или катодной реакции), в результате которого электроны, образующиеся в результате анодной реакции, потребляются. Эти «участки» вместе составляют «коррозионную ячейку».
Места, где протекают анодные и катодные реакции, аноды и катоды коррозионной ячейки, определяются многими факторами: (i) они не обязательно закреплены на месте; (ii) они могут быть смежными или далеко друг от друга, так что, например, если два металла находятся в контакте, один металл может быть анодом, а другой катодом, что приводит к гальванической коррозии более анодного металла; (iii) могут существовать поверхностные колебания концентрации кислорода в окружающей среде, что приводит к установлению анода на тех участках, которые подвергаются воздействию среды с более низким содержанием кислорода дифференциальная аэрационная коррозия; (iv) или аналогичным образом, изменения концентрации ионов металлов или других веществ в окружающей среде, возникающие из-за пространственной ориентации корродирующего металла и гравитации; или, наконец, (v) вариации однородности поверхности металла из-за наличия включений, различных фаз, границ зерен, нарушения металла и других причин могут привести к образованию анодных и катодных участков. Процесс, происходящий на анодных участках, представляет собой растворение металла в виде ионов металлов в электролите или превращение этих ионов в нерастворимые продукты коррозии, такие как ржавчина. Это разрушительный процесс, называемый коррозией. Поток электронов между корродирующими анодами и некорродирующими катодами образует коррозионный ток, величина которого определяется скоростью образования электронов анодной реакцией и их потребления катодной реакцией. Скорости производства и потребления электронов, конечно, должны быть равными, иначе произойдет накопление заряда. Движущая сила, склонность к коррозииДвижущая сила необходима для движения электронов между анодами и катодами. Этой движущей силой является разница потенциалов между анодным и катодным участками. Это различие существует потому, что с каждой реакцией окисления или восстановления связан потенциал, определяемый тенденцией к самопроизвольному протеканию реакции. Потенциал является мерой этой тенденции. Электрохимические равновесия: окисление и восстановление Поскольку большинство коррозионных реакций, протекающих в присутствии жидкости, такой как вода, являются не химическими, а электрохимическими, использование химических равновесий для изучения водной коррозии имеет минимальное значение. Полезным способом изучения связи потенциала с коррозией является использование диаграммы электрохимического равновесия, называемой «диаграммой Пурбэ», разработанной М. Пурбэ (доступно на WWW). большое значение для коррозионных процессов.
Упрощенная диаграмма Пурбе для железа показана на рисунке 2. На графике изображен потенциал железа, измеренный относительно стандартного водородного электрода сравнения. Диаграмма Пурбэ позволяет определить с помощью измерений потенциала и pH, находится ли металлическая поверхность в зоне невосприимчивости, где склонность к коррозии нулевая, (ii) в области, где склонность к коррозии высока, или (iii) в районе, где все еще может существовать тенденция к коррозии, но также существует тенденция к образованию защитной или пассивной пленки. Кинетика, скорость коррозииХотя необходимо определить склонность к коррозии путем измерения потенциалов, недостаточно установить, будет ли данный металл или сплав подвергаться коррозии при заданном наборе условий окружающей среды. Потому что, хотя склонность к коррозии может быть высокой, скорость коррозии может быть очень низкой, и, таким образом, коррозия может не представлять проблемы. Скорость коррозии определяется путем подачи тока для получения поляризационной кривой (степень изменения потенциала в зависимости от величины приложенного тока) для металлической поверхности, скорость коррозии которой определяется. Когда потенциал металлической поверхности поляризуется приложением тока в положительном направлении, говорят, что он анодно поляризован; отрицательное направление означает, что он катодно поляризован. Степень поляризации является мерой того, насколько скорости анодных и катодных реакций замедляются под воздействием различных факторов окружающей среды (концентрация ионов металлов, растворенного кислорода и т.
На рис. 3 показаны анодные и катодные поляризационные кривые, представляющие анодные реакции (например, растворение металла) или катодные реакции (например, восстановление кислорода или выделение водорода). На рисунке 3 потенциал «Е» изображен как функция логарифма плотности тока «i». Когда коррозионные реакции контролируются активационной поляризацией, как это часто наблюдается, поведение поляризации будет представлять собой прямую линию на этом графике, следующую за Уравнение Тафеля (см. Части экстраполяции, показанные на рис. 3, дают диаграммы (диаграммы Эванса), показанные на рис. 4. Относительные значения «наклонов» анодных или катодных поляризационных кривых определяют, анодная, катодная или обе реакции контролируют скорость реакции. процесс коррозии. Диаграммы Эванса широко используются учеными и инженерами-коррозионистами для оценки влияния различных факторов на скорость коррозии. Пассивность и срыв пассивности Поскольку как движущая сила (склонность к коррозии), так и кинетические (скорость коррозии) соображения имеют решающее значение при определении степени коррозии поверхности металла, решающим фактором, контролирующим скорость, является существование явления пассивности для некоторых металлов и сплавов. таких как нержавеющая сталь и титан. До сих пор существуют серьезные разногласия по поводу того, какой процесс отвечает за существование феномена пассивности, хотя было проведено множество исследований, чтобы лучше понять его. Чтобы быть эффективной, пассивная пленка должна обеспечивать защитный барьер, который удерживает ток коррозии на металлической поверхности на достаточно низком уровне, чтобы свести к минимуму степень коррозионного повреждения. Эффективная пленка — это та, которая противостоит разрушению (называемому разрушением) пассивной пленки. Процессы разрушения приводят к формам локальной коррозии, которые являются одними из основных источников коррозионных разрушений, точечной, щелевой, межкристаллитной коррозии и коррозии под напряжением (см. ниже). Они вызывают разрушение пассивной пленки и, таким образом, подвергают дискретные оголенные участки поверхности металла воздействию окружающей среды, где вероятность атаки очень высока. С процессом разрушения пассивной пленки конкурирует процесс репассивации пассивной пленки. Таким образом, эффективным сплавом для сопротивления локальной коррозии будет сплав, поверхность которого не только образует пассивирующую пленку, которая противостоит процессу, ведущему к разрушению, но также способна репассивировать с достаточно высокой скоростью, так что, как только произойдет разрушение, воздействие коррозионного экология минимальна. Виды коррозииТолько что описанный процесс разрушения и восстановления пассивности связан со многими, но не со всеми различными типами коррозии. Питтинговая коррозия Возникновение ямки происходит, когда электрохимическое или химическое разрушение подвергает небольшой локальный участок на поверхности металла воздействию повреждающих частиц, таких как ионы хлорида. Места, где зарождаются ямки, до конца не изучены, но некоторые из них могут быть связаны с царапинами, неоднородностями состава поверхности (включениями) или местами, где существуют вариации окружающей среды. Ямка растет, если высокая плотность тока область инициирования пробоя чрезвычайно мала , участвующая в процессе репассивации, не препятствует образованию большой локальной концентрации ионов металла, образующихся при растворении в точке инициирования. Если скорость репассивации недостаточна для подавления роста ямок, возникают два новых условия. Во-первых, ионы металлов, образующиеся в процессе распада, осаждаются в виде твердых продуктов коррозии (таких как Fe(OH) 2 , Приложение, Уравнение [7]), которые обычно закрывают устье карьера. Ямка представляет собой анод электрохимической коррозионной ячейки, а катод ячейки представляет собой поверхность без изъязвлений. Поскольку площадь поверхности язвы составляет очень малую часть площади катодной поверхности, весь ток анодной коррозии течет на чрезвычайно малую площадь поверхности очага возникновения пробоя. Таким образом, плотность анодного тока становится очень высокой, и проникновение в металлическую конструкцию, имеющую лишь несколько ямок, может быть быстрым. Щелевая коррозия
Щелевая коррозия возникает, когда часть металлической поверхности экранирована таким образом, что экранированная часть имеет ограниченный доступ к окружающей среде. Такие окружающие среды содержат вещества, вызывающие коррозию, обычно ионы хлора. Типичным примером щелевой коррозии является щель, образованная в области между двумя металлическими поверхностями, находящимися в тесном контакте с прокладкой или другой металлической поверхностью. Среда, которая в конечном итоге образуется в щели, аналогична среде, образующейся под осажденным продуктом коррозии, покрывающим ямку (рис. 5). Точно так же электрохимическая коррозионная ячейка образуется из пары между неэкранированной поверхностью и внутренней частью щели, подвергаемой воздействию среды с более низкой концентрацией кислорода по сравнению с окружающей средой. Эта комбинация анода коррозионной ячейки и существования в кислой среде с высоким содержанием хлоридов, где репассивация затруднена, делает внутреннюю часть щели подверженной коррозионному воздействию. Коррозионное растрескивание под напряжением, водородное повреждение и коррозионная усталость Коррозионное растрескивание под напряжением (SCC) представляет собой форму локализованной коррозии, которая приводит к образованию трещин в металлах под одновременным действием корродирующего и растягивающего напряжения. Электрохимическая ячейка между внешней и внутренней средами трещины аналогична описанной выше для трещины. Из-за необходимости приложения напряжения разрушение пассивного слоя на поверхности металла в SCC обычно приписывают механическим причинам, но многие предполагают, что электрохимия является важным фактором, поскольку она контролирует скорость восстановления пассивного слоя, разрушенного SCC. механическое напряжение. Коррозионная усталость в чем-то похожа на SCC. Он в основном отличается от SCC тем, что включает ситуации, когда напряжение применяется циклически, а не как статическое устойчивое растягивающее напряжение. Межкристаллитная коррозия За исключением металлических стекол, металлы, используемые в практических устройствах, состоят из мелких кристаллов (зерен), поверхности которых соединяются с поверхностями других зерен, образуя границы зерен. Такие границы или небольшие области, примыкающие к этим границам, могут при определенных условиях быть значительно более реакционноспособными (будучи более анодными), чем внутренности зерен. Возникающая при этом коррозия называется межкристаллитной коррозией. Это может привести к потере прочности металлической детали или образованию мусора (выпавших зерен). Равномерная коррозия Равномерная коррозия возникает из-за участков, не обязательно зафиксированных в определенном месте, которые распределены по поверхности металла, где происходят анодные и катодные реакции. Гальваническая (и термогальваническая) коррозия Два металла, имеющие разные потенциалы в проводящем электролите, приводят к тому, что более анодный металл обычно подвергается гальванической коррозии. Из-за электрического контакта между двумя разными металлами гальваническая коррозия отличается от других форм коррозии, описанных ранее, тем, что анодный и катодный участки коррозионной ячейки находятся отдельно на двух связанных разных металлах, составляющих коррозионную ячейку, в то время как для других форм коррозии коррозии, катоды и аноды существуют на поверхности одного и того же металла. Значение разности потенциалов между двумя разнородными металлами обычно получают из списка стандартных равновесных потенциалов для различных металлов (для реакций типа, приведенного в Приложении, уравнение [1]). Селективное выщелачивание Когда один компонент сплава избирательно удаляется коррозией из-за различий потенциалов между различными компонентами сплава — ситуация аналогична гальванической коррозии связанных разнородных металлов. Эрозионная коррозия Эрозионная коррозия возникает в результате разрушения защитно-пассивных пленок эрозионными или абразивными процессами. После удаления защитной или пассивной пленки в водном электролите происходят электрохимические процессы описанных выше видов коррозии. Защита от коррозииТолько что описанные типы электрохимической коррозии можно предотвратить или контролировать, используя современное понимание принципов, лежащих в основе коррозионных процессов. Это понимание стало основой для разработки ряда мер по предотвращению коррозии.
Три меры по борьбе с коррозией основаны на электрохимической движущей силе, как показано на диаграмме Пурбе, приведенной на рисунке 6: (i) Катодная защита предложена Британскому Адмиралтейству для защиты от коррозии кораблей с медной обшивкой сэром Хамфри Дэви в 1824 г. (Доступно на WWW) обеспечивает контроль над коррозией, превращая защищаемую конструкцию в катод коррозионной ячейки, переводя потенциал конструкции в область невосприимчивости диаграммы Пурбе или близко к ней; (ii) Анодная защита превращает защищаемую конструкцию в анод, а приложенный ток переводит потенциал конструкции в пассивную область диаграммы Пурбе; и (iii) Модификация окружающей среды путем изменения pH, чтобы привести защищаемую структуру в зону иммунитета или пассивации. Другие меры, используемые для контроля процессов электрохимической коррозии, включают следующее: (i) Коррозионно-стойкие сплавы разрабатываются как устойчивые к коррозии и содержат такие компоненты, как хром, которые образуют более эффективные защитные пленки, устойчивые к разрушению и быстро восстанавливающие пассивацию. ПриложениеРеакции коррозии Ниже приведены некоторые примеры анодных и катодных реакций, протекающих одновременно на поверхности металла в «коррозионной ячейке». Типичное анодное окисление, при котором образуется растворенный ионный продукт, например, для металлического железа, представляет собой: [1] Примерами катодного восстановления, участвующего в процессе коррозии, являются: [2] [3] [4] Катодная реакция, представленная уравнением [2], иллюстрирует коррозию в естественных условиях, где коррозия происходит при почти нейтральных значениях рН. [5] В результате этой реакции образуются ионы Н + , концентрация которых при определенных условиях может стать большой, если ионы Н + не могут легко выйти из ограниченного объема. [6] или для реакции с образованием нерастворимого гидроксида (сумма реакций [1] и [2]): [7] Уравнение Тафеля Уравнение Тафеля представляет собой раннее (1905 г. «а» и «b» — характеристические константы электродной системы. График электродного потенциала в зависимости от логарифма плотности тока называется «графиком Тафеля», а полученная прямая линия — «линии Тафеля». «b» представляет собой «наклон Тафеля», который дает информацию о механизме реакции, а «a» точка пересечения дает информацию о константе скорости (и плотности тока обмена) реакции. Связанные статьи Анодирование Библиография
|





 Это происходит из-за подавляющей склонности металлов к электрохимическим реакциям с кислородом, водой и другими веществами в водной среде. К счастью, большинство полезных металлов вступают в реакцию с окружающей средой, образуя более или менее защитные пленки продуктов реакции коррозии, которые не позволяют металлам переходить в раствор в виде ионов.
Это происходит из-за подавляющей склонности металлов к электрохимическим реакциям с кислородом, водой и другими веществами в водной среде. К счастью, большинство полезных металлов вступают в реакцию с окружающей средой, образуя более или менее защитные пленки продуктов реакции коррозии, которые не позволяют металлам переходить в раствор в виде ионов.

 Примеры включают отказы из-за разорванных соединений в кардиостимуляторах, воспаление, вызванное продуктами коррозии в тканях вокруг имплантатов, и разрушение протезов, несущих нагрузку. Примером последнего является использование металлических тазобедренных суставов, которые могут облегчить некоторые проблемы артрита тазобедренного сустава. В последние годы ситуация улучшилась, так что тазобедренные суставы, которые сначала использовались только у людей старше 60 лет, теперь используются у более молодых людей, потому что они служат дольше.
Примеры включают отказы из-за разорванных соединений в кардиостимуляторах, воспаление, вызванное продуктами коррозии в тканях вокруг имплантатов, и разрушение протезов, несущих нагрузку. Примером последнего является использование металлических тазобедренных суставов, которые могут облегчить некоторые проблемы артрита тазобедренного сустава. В последние годы ситуация улучшилась, так что тазобедренные суставы, которые сначала использовались только у людей старше 60 лет, теперь используются у более молодых людей, потому что они служат дольше. В значительной степени развитие новых технологий сдерживается проблемами коррозии, потому что материалы должны выдерживать, во многих случаях одновременно, более высокие температуры, более высокое давление и более агрессивные среды. Проблемы с коррозией, которые легче решить, затрагивают солнечные энергетические системы, которые требуют, чтобы сплавы выдерживали горячую циркулирующую жидкость-теплоноситель в течение длительных периодов времени, и геотермальные системы, которые требуют, чтобы материалы выдерживали высококонцентрированные растворы коррозионно-активных солей при высоких температурах и давлениях. Другой пример, бурение на нефть в море и на суше, включает в себя преодоление таких проблем коррозии, как сульфидная коррозия под напряжением, микробиологическая коррозия и широкий спектр трудностей, связанных с работой в высококоррозионной морской среде. Во многих из этих случаев коррозия является ограничивающим фактором, препятствующим разработке экономически или даже технологически работоспособных систем.
В значительной степени развитие новых технологий сдерживается проблемами коррозии, потому что материалы должны выдерживать, во многих случаях одновременно, более высокие температуры, более высокое давление и более агрессивные среды. Проблемы с коррозией, которые легче решить, затрагивают солнечные энергетические системы, которые требуют, чтобы сплавы выдерживали горячую циркулирующую жидкость-теплоноситель в течение длительных периодов времени, и геотермальные системы, которые требуют, чтобы материалы выдерживали высококонцентрированные растворы коррозионно-активных солей при высоких температурах и давлениях. Другой пример, бурение на нефть в море и на суше, включает в себя преодоление таких проблем коррозии, как сульфидная коррозия под напряжением, микробиологическая коррозия и широкий спектр трудностей, связанных с работой в высококоррозионной морской среде. Во многих из этих случаев коррозия является ограничивающим фактором, препятствующим разработке экономически или даже технологически работоспособных систем.
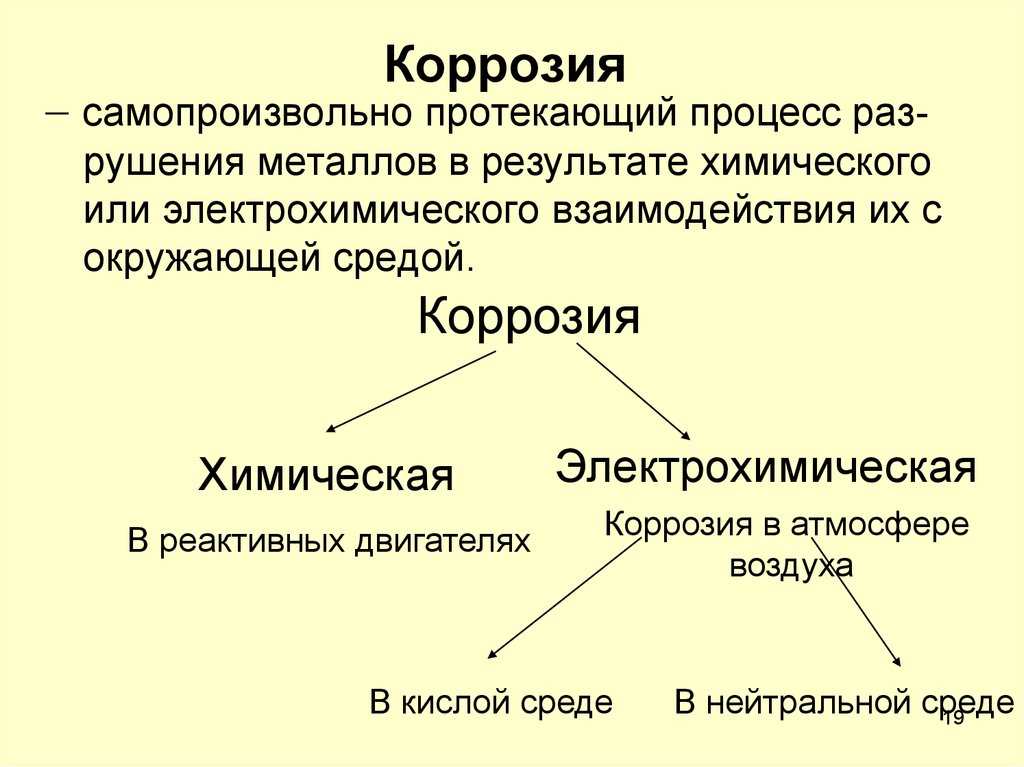 Анодная реакция представляет собой растворение металла с образованием либо растворимых ионных продуктов, либо нерастворимого соединения металла, обычно оксида. Возможны несколько катодных реакций в зависимости от того, какие восстанавливаемые частицы присутствуют в растворе. Типичными реакциями являются восстановление растворенного газообразного кислорода или восстановление растворителя (воды) с получением газообразного водорода. Примеры таких реакций приведены в Приложении. Поскольку эти анодная и катодная реакции происходят одновременно на поверхности металла, они создают электрохимическую ячейку типа, показанного на рисунке 1.
Анодная реакция представляет собой растворение металла с образованием либо растворимых ионных продуктов, либо нерастворимого соединения металла, обычно оксида. Возможны несколько катодных реакций в зависимости от того, какие восстанавливаемые частицы присутствуют в растворе. Типичными реакциями являются восстановление растворенного газообразного кислорода или восстановление растворителя (воды) с получением газообразного водорода. Примеры таких реакций приведены в Приложении. Поскольку эти анодная и катодная реакции происходят одновременно на поверхности металла, они создают электрохимическую ячейку типа, показанного на рисунке 1.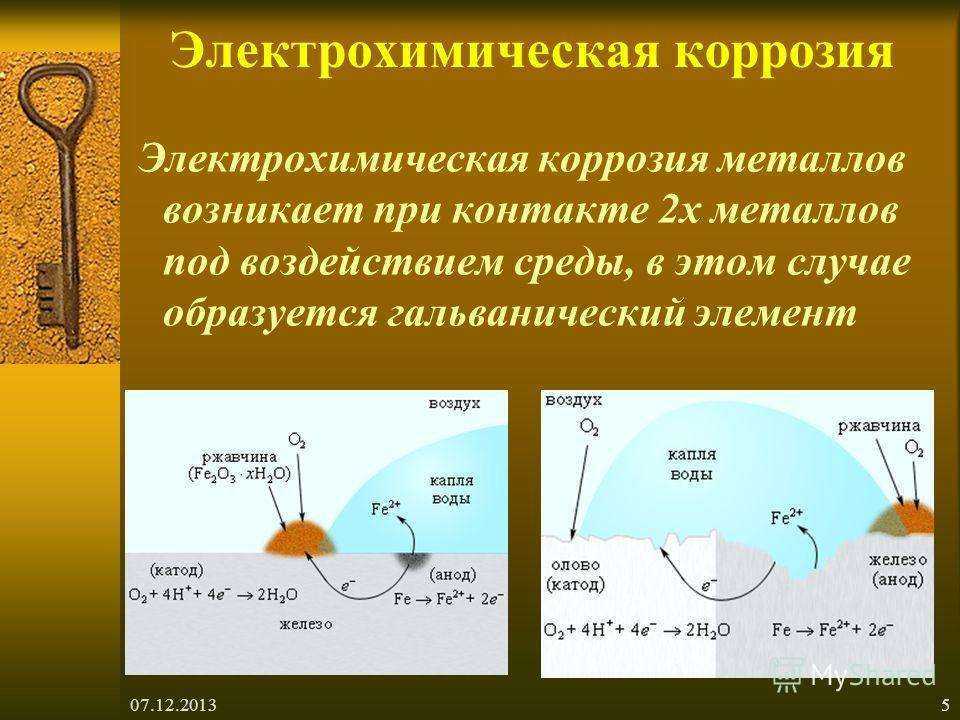

 Такая пленка может резко повлиять на скорость коррозии, а в некоторых случаях практически остановить ее (см. Пассивность и пробой). Линии (a) и (b) на рисунке 2 представляют восстановление кислорода (приложение, уравнения [2] или [3]) и выделение водорода (приложение, уравнение [4]) соответственно. Они являются мерой концентрации кислорода или водорода в растворе и показывают изменение потенциала в зависимости от pH для растворов, находящихся в равновесии с одной атмосферой кислорода или водорода. Линии, проведенные параллельно (а), но ниже, показывают изменение потенциала в зависимости от рН для раствора, содержащего меньшее количество кислорода, чем представлено (а). Таким образом, потенциал образца может дать некоторое представление о концентрации кислорода в окружающей среде. Различия в концентрации кислорода между разными участками металла приводят к Дифференциальная аэрационная коррозия упомянутая выше. С помощью диаграммы Пурбе путем измерения потенциала и рН можно получить некоторое представление о склонности металла находиться в невосприимчивом, пассивном или коррозионном режиме, а также оценить влияние ограниченного или легкого доступа кислорода на его состояние.
Такая пленка может резко повлиять на скорость коррозии, а в некоторых случаях практически остановить ее (см. Пассивность и пробой). Линии (a) и (b) на рисунке 2 представляют восстановление кислорода (приложение, уравнения [2] или [3]) и выделение водорода (приложение, уравнение [4]) соответственно. Они являются мерой концентрации кислорода или водорода в растворе и показывают изменение потенциала в зависимости от pH для растворов, находящихся в равновесии с одной атмосферой кислорода или водорода. Линии, проведенные параллельно (а), но ниже, показывают изменение потенциала в зависимости от рН для раствора, содержащего меньшее количество кислорода, чем представлено (а). Таким образом, потенциал образца может дать некоторое представление о концентрации кислорода в окружающей среде. Различия в концентрации кислорода между разными участками металла приводят к Дифференциальная аэрационная коррозия упомянутая выше. С помощью диаграммы Пурбе путем измерения потенциала и рН можно получить некоторое представление о склонности металла находиться в невосприимчивом, пассивном или коррозионном режиме, а также оценить влияние ограниченного или легкого доступа кислорода на его состояние. коррозионный процесс.
коррозионный процесс.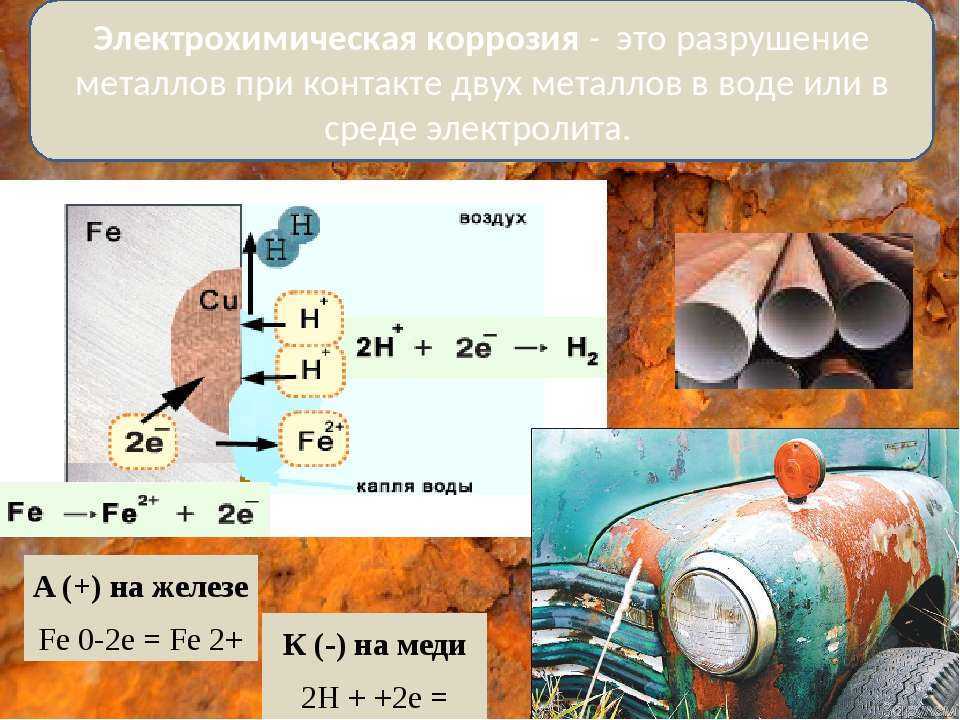 д. в растворе) и/или поверхностных процессов (адсорбция, пленкообразование, легкость нанесения). высвобождение электронов и др.) факторы. Первая называется концентрационной поляризацией, вторая — активационной поляризацией. Изменение потенциала в зависимости от тока (поляризационная кривая) позволяет изучить влияние процессов концентрации и активации на скорость, с которой анодные или катодные реакции могут отдавать или принимать электроны. Следовательно, измерения поляризации могут таким образом определить скорость реакций, участвующих в процессе коррозии — скорость коррозии.
д. в растворе) и/или поверхностных процессов (адсорбция, пленкообразование, легкость нанесения). высвобождение электронов и др.) факторы. Первая называется концентрационной поляризацией, вторая — активационной поляризацией. Изменение потенциала в зависимости от тока (поляризационная кривая) позволяет изучить влияние процессов концентрации и активации на скорость, с которой анодные или катодные реакции могут отдавать или принимать электроны. Следовательно, измерения поляризации могут таким образом определить скорость реакций, участвующих в процессе коррозии — скорость коррозии. Экстраполяция анодных и катодных кривых дает диаграммы Эванса (см. рис. 4).
Экстраполяция анодных и катодных кривых дает диаграммы Эванса (см. рис. 4).  также Приложение). На этом рисунке «Е о,а » и «Е о,с » — равновесные потенциалы рассматриваемых реакций (анодных или катодных). «Линии Тафеля» характеризуются «наклоном» линейной части поляризационной кривой и их «пересечением» при экстраполяции к равновесному потенциалу. «Пересечение» пропорционально логарифму плотности тока обмена «i o » (то есть выражает собственную скорость электродной реакции). Значения этих характеристических констант в уравнении Тафеля зависят от рассматриваемого металла и окружающей среды. Анодный и катодный линейные участки поляризационных кривых можно экстраполировать на коррозионный потенциал «Е корр », где в идеальных условиях они должны пересекаться. Величиной тока в месте их пересечения будет скорость коррозии «i корр », выраженная в плотности тока. Значения плотностей тока обмена для катодной и анодные реакции оказывают сильное влияние на скорость коррозии. Это показано на примере использования двух значений «i o,c » (но для простоты предполагается, что «E o,c » постоянная): чем больше «i o,c » чем больше скорость коррозии, «i корр.
также Приложение). На этом рисунке «Е о,а » и «Е о,с » — равновесные потенциалы рассматриваемых реакций (анодных или катодных). «Линии Тафеля» характеризуются «наклоном» линейной части поляризационной кривой и их «пересечением» при экстраполяции к равновесному потенциалу. «Пересечение» пропорционально логарифму плотности тока обмена «i o » (то есть выражает собственную скорость электродной реакции). Значения этих характеристических констант в уравнении Тафеля зависят от рассматриваемого металла и окружающей среды. Анодный и катодный линейные участки поляризационных кривых можно экстраполировать на коррозионный потенциал «Е корр », где в идеальных условиях они должны пересекаться. Величиной тока в месте их пересечения будет скорость коррозии «i корр », выраженная в плотности тока. Значения плотностей тока обмена для катодной и анодные реакции оказывают сильное влияние на скорость коррозии. Это показано на примере использования двух значений «i o,c » (но для простоты предполагается, что «E o,c » постоянная): чем больше «i o,c » чем больше скорость коррозии, «i корр.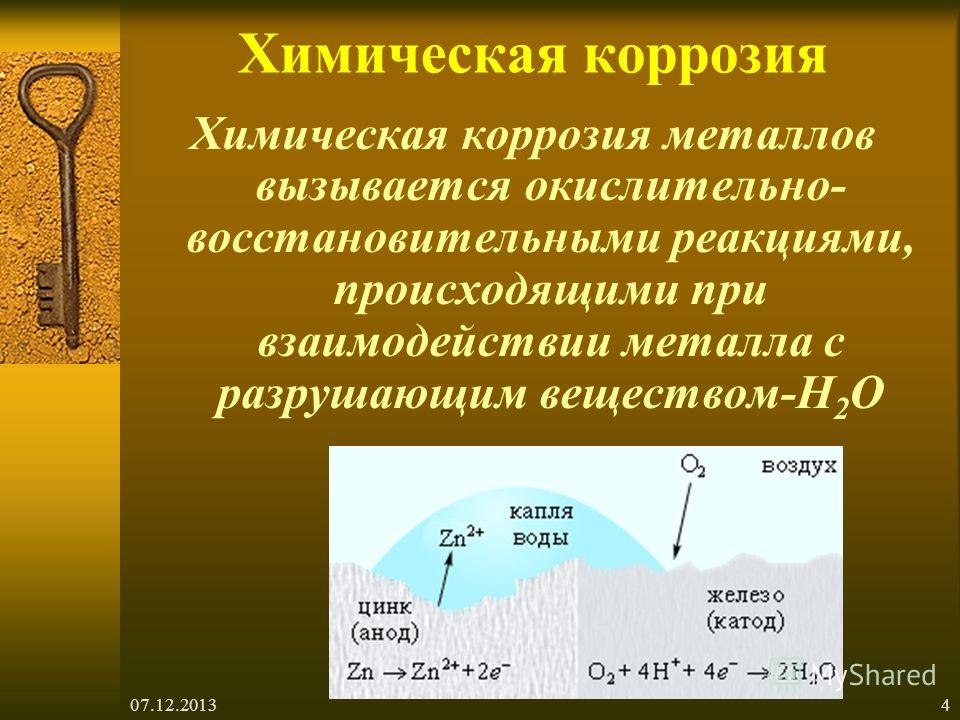 » (см. рисунок 3).
» (см. рисунок 3). Для целей данного обсуждения достаточно охарактеризовать пассивность как условия, существующие на поверхности металла из-за наличия защитной пленки, природа которой является источником разногласий, которая заметно снижает скорость коррозии, даже если активна. коррозии можно было бы ожидать из соображений движущей силы (склонности к коррозии).
Для целей данного обсуждения достаточно охарактеризовать пассивность как условия, существующие на поверхности металла из-за наличия защитной пленки, природа которой является источником разногласий, которая заметно снижает скорость коррозии, даже если активна. коррозии можно было бы ожидать из соображений движущей силы (склонности к коррозии). Многие предложенные механизмы химического распада основаны на двух моделях, каждая из которых имеет множество вариаций. Это (i) модели вытеснения адсорбированных ионов и (ii) модели миграции или проникновения ионов. Существует два типа процессов разрушения: электрохимическое разрушение, при котором многие исследования показали, что разрушение происходит при потенциале выше определенного «потенциала пробоя», и механическое разрушение, которое происходит, когда пассивная пленка разрывается в результате напряжения или абразивного износа. Следует отметить, что во всех механизмах разрушения задействованы повреждающие виды. К сожалению, одним из основных видов, вызывающих нарушение пассивности, является ион хлорида, повреждающий вид, широко распространенный в природе.
Многие предложенные механизмы химического распада основаны на двух моделях, каждая из которых имеет множество вариаций. Это (i) модели вытеснения адсорбированных ионов и (ii) модели миграции или проникновения ионов. Существует два типа процессов разрушения: электрохимическое разрушение, при котором многие исследования показали, что разрушение происходит при потенциале выше определенного «потенциала пробоя», и механическое разрушение, которое происходит, когда пассивная пленка разрывается в результате напряжения или абразивного износа. Следует отметить, что во всех механизмах разрушения задействованы повреждающие виды. К сожалению, одним из основных видов, вызывающих нарушение пассивности, является ион хлорида, повреждающий вид, широко распространенный в природе.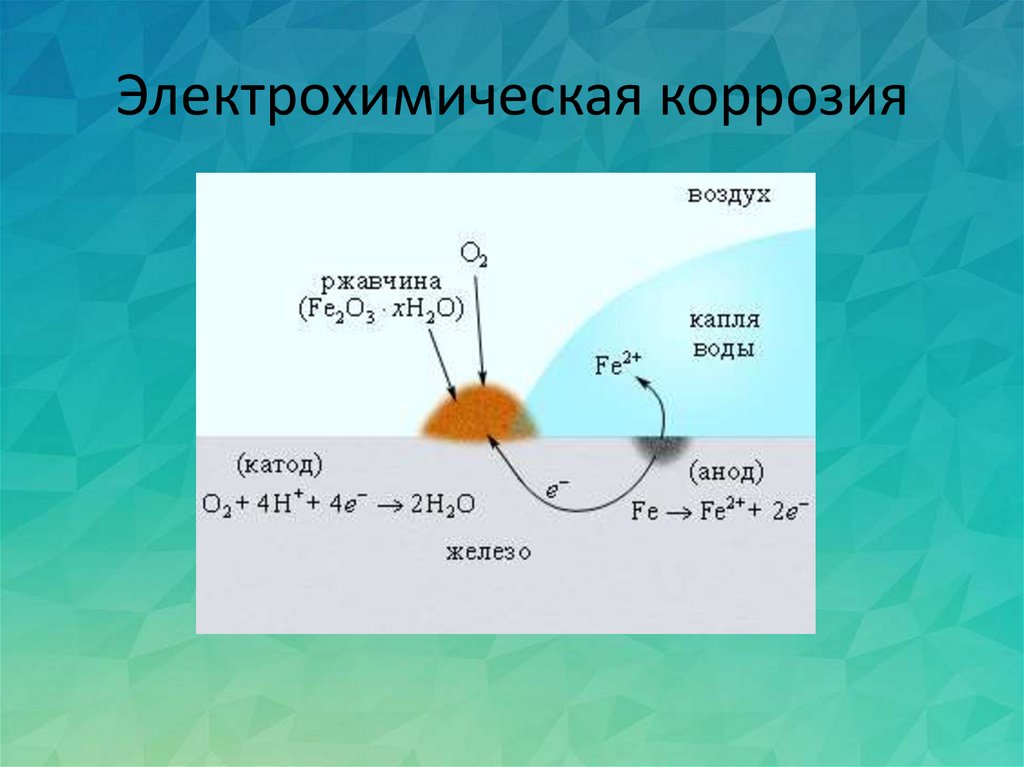
 Это покрытие улавливает раствор в ямке и позволяет накапливать положительные ионы водорода в результате реакции гидролиза (Приложение, уравнение [5]). Затем хлорид или другие повреждающие отрицательные ионы диффундируют в яму, чтобы поддерживать нейтральность заряда. Следовательно, репассивация значительно затрудняется, поскольку раствор в яме очень кислый, содержит большую концентрацию повреждающих ионов и ионов металлов и низкую концентрацию кислорода. Тем самым скорость роста ямок ускоряется.
Это покрытие улавливает раствор в ямке и позволяет накапливать положительные ионы водорода в результате реакции гидролиза (Приложение, уравнение [5]). Затем хлорид или другие повреждающие отрицательные ионы диффундируют в яму, чтобы поддерживать нейтральность заряда. Следовательно, репассивация значительно затрудняется, поскольку раствор в яме очень кислый, содержит большую концентрацию повреждающих ионов и ионов металлов и низкую концентрацию кислорода. Тем самым скорость роста ямок ускоряется. 5. Идеализированная картина среды, развивающейся в щели коррозионной ячейкой, создаваемой на железе анодом в щели и катодом вне щели.
5. Идеализированная картина среды, развивающейся в щели коррозионной ячейкой, создаваемой на железе анодом в щели и катодом вне щели. 