Латунь встречается в природе в виде: Латунь в природе встречается в виде
Содержание
Получение и химические реакции меди
Нахождение в природе.
Медь встречается главным образом в виде сульфидных соединений. Наиболее важные минералы — медный блеск Cu2S, медный колчедан (халькопирит) CuFeS2 и борнит Cu3FeS2 входят в состав так называемых полиметаллических сульфидных руд. Реже встречаются кислородсодержащие соединения: малахит (основной карбонат меди) СuСО3 • Сu(ОН)2, азурит 2СuСО3 • Сu(ОН)2 и куприт СuO2.
Физические свойства.
Медь — металл красного цвета, плавится при температуре 1083°С, кипит при 2877°С. Чистая медь довольно мягка, легко поддается прокатке и вытягиванию. Примеси увеличивают твердость меди. Медь отличается очень высокой электро- и теплопроводностью. Примеси мышьяка и сурьмы значительно уменьшают электропроводность меди. Медь образует различные сплавы (латуни, бронзы и др.).
Химические свойства.
Медь относится к числу малоактивных металлов. На холоду она очень слабо взаимодействует с кислородом воздуха, покрываясь пленкой оксида, которая препятствует дальнейшему окислению меди. При нагревании медь окисляется полностью:
На холоду она очень слабо взаимодействует с кислородом воздуха, покрываясь пленкой оксида, которая препятствует дальнейшему окислению меди. При нагревании медь окисляется полностью:
2Cu + O2 = 2СuО
Сухой хлор на холоду не взаимодействует с медью, однако в присутствии влаги реакция проходит довольно энергично:
Сu + Сl2 = СuС12.
При нагревании медь довольно энергично взаимодействует с серой:
Си + S = CuS.
Медь может растворятся только в кислотах-окислителях. В концентрированной серной кислоте она растворяется только при нагреваний, a в азотной — и на холоду:
Сu+ 2H2SO4 = CuSO4 + SO2 + 2Н2O,
ЗСu + 8HNO3(Разбавл.) = 3Cu(NO3)2 + 2NO + 4Н2O,
Сu + 4HNO3(Конц .) = Cu(NO3)2+ 2NO + 2Н2O.
Получение.
Процесс получения меди состоит из нескольких стадий. Сначала сульфидную руду обжигают. При этом часть меди превращается в оксид:
При этом часть меди превращается в оксид:
4CuFeS2 + 13O2 = 4CuO + 2Fe203 + 8SO2.
Затем проводят плавку на штейн и получают сульфид меди (I). При этом к огарку прибавляют кокс и песок для образования шлака:
2CuO + FeS + С + SiO2 = Cu2S + FeSi03 + СО
или
CuO + FeO + CuS + С + SiO2 = Cu2S + FeSiO3+ CO.
Далее штейн подвергают конвертерной плавке:
9Cu2 S + 3O2 = 2Cu2 O + 2SO2 ,
2CuO2 + Cu2 S = 6Cu + SO2 .
Получаемая медь называется черновой.
Очищают медь рафинированием. Электролитом служит раствор сульфата меди, анодом — медные болванки ,катодом — пластинка чистой меди. При пропускании электрического тока через электролит медь анода растворяется, а на катоде выделяется чистая медь.
Оксид меди
Обладает основными свойствами. Он может взаимодействовать с кислотами и кислотными оксидами:
CuO + H2SО4 = CuSО4 + Н2О,
CuO + SО3 = CuSО4.
Оксид меди не растворим в воде. При нагревании оксида меди и присутствии восстановителя довольно легко происходит его восстановление:
CuO + Н2 = Сu + Н2O,
СuО + СО = Сu + СO2.
Оксид меди получают окислением меди при нагревании или прокаливанием гидроксида меди:
2Сu + O2 = 2СuО,
Cu(OH)2 = CuO + Н2O.
Оксид меди встречается в природе в продуктах выветривания некоторых медных руд. Он используется в производстве стекла и эмалей как зеленый и синий красители (медно-рубиновое стекло), как окислитель в органическом анализе и в медицине.
Гидроксид меди
Гидроксид меди Сu(ОН)2. Выпадает в виде осадка при действии на растворы солей меди (II) растворов щелочей (но не аммиака):
CuSO4 + 2NaOH = Cu(OH)2↓ + Na2SO4.
При действии аммиака на соли меди (II) сначала выпадает гидроксид меди, который очень легко растворяется в избытке аммиака с образованием аммиаката меди:
Cu(OH)2 + 4NH4OH = [Cu(NH3)4](OH)2 + 4Н2O
или
Cu(OH)2 + 4NH3 = [Cu(NH3)4](OH)2.
Аммиакат меди окрашен в интенсивный сине-фиолетовый цвет, Поэтому он позволяет обнаружить малые количества ионов меди (П) в растворе. Эта реакция применяется в аналитической химии.
Гидроксид меди обладает очень слабо выраженными амфотерными свойствами. В кислотах он растворяется легко, в концентрированных растворах щелочей — с большим трудом. В первом случае образуются соли меди, во втором — гидроксокупраты:
Сu(ОH)2 + 2NaOH = Na2[Cu(OH)4].
Гидроксид меди может восстанавливаться до гемиоксида меди при нагревании С различными не очень сильными восстановителями: альдегидами, сахарами, гидразином, гидроксиламином и др.:
2Cu(OH)2 + R—СНО → Cu2O + R—COOH + 2H2O.
Гемиоксид, или оксид меди (I)
Гемиоксид, или оксид меди (I), Си20. Обладает только основными свойствами. Часть солей меди (I) хорошо растворима, но довольно неустойчива и легко окисляется кислородом воздуха. Устойчивыми соединениями меди (I) являются, как правило, либо нерастворимые соединения (Cu2S, Cu2O, Cu2I2), либо комплексные соединения (Cu(NH3)+2 и др.). Гемиоксид меди применяется для изготовления купроксных выпрямителей переменного тока.
Устойчивыми соединениями меди (I) являются, как правило, либо нерастворимые соединения (Cu2S, Cu2O, Cu2I2), либо комплексные соединения (Cu(NH3)+2 и др.). Гемиоксид меди применяется для изготовления купроксных выпрямителей переменного тока.
При растворении гемиоксида меди в кислородсодержащих кислотах, например серной, образуются соли меди (II) и медь:
Cu2O + H2SO4 = CuSO4 + Сu + Н2O,
а при растворении в галогеноводородных кислотах — соли меди (I):
Cu20 + 2НС1 = 2СuС1 + Н2O.
Многие соли меди (II) хорошо растворимы в воде, но подвержены гидролизу, поэтому в растворе всегда должен быть небольшой избыток кислоты. Нерастворимыми солями меди (II) являются сульфид CuS, карбонат (основной карбонат) СuСO3• Сu(ОН)2 • 0,5Н2О, оксалат СuС2O4 и фосфат Сu3(РO4)2.
Под действием восстановителей соли меди (II) в кислом растворе могут восстанавливаться до солей меди (I):
2CuSO4 + 4KI = 2K2SO4 + Cu2I2 + I2
Аммиачные растворы солей меди (I) могут взаимодействовать с ацетиленом, образуя ацетиленид меди;
СН≡СН + 2CuCl = Cu2C2 + 2НС1.
Литература [3]
Где найти латунь
Главная » Разное » Где найти латунь
Где найти латунь? | Металл Трейдинг
Латунь сегодня является одним из распространенных сплавов. Она известна и используется веками и впервые была получен в Индии в начале железного века. На нашем континенте она использовалась уже в древние времена, однако известность и популярность приобрела только в средние века, когда стала скульптурным материалом. На протяжении тысячелетий процесс совершенствовался, и эксперименты с пропорциями приводили к открытию все более новых применений для этого металлического сплава.
Характеристики и разновидности
В дополнение к меди и алюминию латунь является одним из желательных цветных металлов благодаря применению и большим возможностям обработки. Наиболее популярные типы лома, которые могут быть проданы:
- желтый лом — встречается в натуральном желто-золотом цвете. Этот тип можно найти в кулерах, сантехническом оборудовании и монтажных деталях;
- латунный лом, то есть покрытый поверхностным слоем никеля или цинка. Часто используется в гидравлических и охлаждающих устройствах;
- латунные и латунно-медные кулеры — используются в автомобилях, тракторах и сельскохозяйственных машинах, в устройствах и промышленных установках;
- несортированный металлолом также допускает смеси различных марок.
Латунь состоит из меди и цинка (40-45%) и других металлических добавок: алюминия, олова, свинца, марганца, железа и хрома. Основной цвет идет от эффекта присутствия цинка в ее составе, что придает характерный оранжево-желтый цвет. После добавления 1% марганца латунь может стать шоколадно-коричневой. Плавится данный металл при 1000 градусах Цельсия в зависимости от состава отдельного сплава. К тому же она отличается от бронзы прочностью, потому что содержит цинк (он и придает большую прочность).
После добавления 1% марганца латунь может стать шоколадно-коричневой. Плавится данный металл при 1000 градусах Цельсия в зависимости от состава отдельного сплава. К тому же она отличается от бронзы прочностью, потому что содержит цинк (он и придает большую прочность).
Что не примут?
Пункты приема обычно принимают все виды лома, которые подпадают под категории, перечисленные выше. Независимо от того, отходы это или сантехнические компоненты, вы можете привезти их на сдачу или заказать вывоз металлолома.
При этом лом следует, по возможности, отделять в соответствии с вышеуказанной классификацией, кроме того, металлолом должен быть свободен от любых загрязнений, то есть пластмасс, других отходов, лишних вкраплений и т. д.
В случае большого количества латунного лома важно, чтобы во время сбора в пункте мешки были отделены. Также мы принимаем автомобильные радиаторы из латуни. Они классифицируются в зависимости от преимущества данного сырья по составу на те, которые представляют собой смесь латуни и меди, и те, которые состоят из алюминия. Однако они не должны быть загрязнены другими металлами.
Однако они не должны быть загрязнены другими металлами.
В случае каких-либо сомнений относительно классификации металлолома и других отходов обслуживающий персонал пункта сбора оказывает профессиональную помощь.
Медь, бронза, латунь оптом и в розницу в Москве
МЕТАЛЛСЕРВИС производит продажу высококачественного цветного металла и недорого поставляет востребованные виды проката во все регионы России. В ассортименте компании представлены изделия из меди, алюминия, никеля, латуни, нихрома, цинка. Эта продукция востребована в строительстве, электротехнике, электронике, энергетике, машиностроении. Она используется при сварке, из нее производятся электроды, нагревательные элементы, радиодетали и детали машин, отделочные и конструкционные материалы.
Преимуществами цветного проката являются:
- снижение веса конструкций;
- простота обработки;
- эстетичность поверхности;
- пластичность и гибкость;
- коррозионная стойкость;
- хорошая теплопроводность и малая окисляемость.

Поверхность большинства изделий хорошо поддается полировке и шлифовке, поэтому они используются при внутренней и внешней отделке зданий, для изготовления различной декоративной продукции.
Виды цветного проката
Наиболее широко в промышленности используются сплавы меди и алюминия: латунь, бронза, дюраль и др. Из меди изготавливаются листовой и трубный прокат, проволока и прутки, сварочные электроды. Из более дешевого алюминия выпускаются листы и плиты, уголок, круглые и профильные трубы, швеллеры.
Сортамент цветного металла на металлобазе очень разнообразен. Покупателям предлагается листовой и сортовой прокат всех видов, изготовленный в соответствии с требованиями ГОСТов. При необходимости принимаются заказы на производство нестандартной и специальной продукции, а также проката повышенной прочности и точности.
Чтобы купить оптом цветной металлопрокат на выгодных условиях, свяжитесь с офисом компании в Москве по указанным телефонам или оформите заказ на сайте. При подаче заявки уточните маркировку сплава и размеры продукции. Стоимость доставки в зависимости от региона и массогабаритных характеристик товара рассчитывается онлайн на соответствующей странице сайта.
При подаче заявки уточните маркировку сплава и размеры продукции. Стоимость доставки в зависимости от региона и массогабаритных характеристик товара рассчитывается онлайн на соответствующей странице сайта.
Вопрос: Как отличить латунь от меди? — Хобби и рукоделие
Для того чтоб эффективно собирать и дороже сдавать металлолом необходимо уметь отличить металлы друг от друга. Отличить цветной металл от черного достаточно просто, это можно сделать при помощи магнита. Но бывает, чтоб различить металлолом нужно учесть ряд нюансов. Чермет не всегда может быть ржавым и большим, когда визуально понятно, что это обычный железный металлолом. Железо часто покрывают различными красками или другими металлами, что может сбить с толку. Но железо или чермет даже с другой расцветкой обладают ярко выраженными магнитными свойствами и хорошо магнитятся, иногда конечно встречаются легированные стали которые магнит не берет, но они попадаются редко и детали из этого металла имеют большие размеры. Также железо и прочий чермет довольно тяжелые и крепкие, гнуть, ломать изделия из железа довольно тяжело. Цветные металлы или цветмет отличаются тем, что не магнитятся, но цветмет в некоторых случаях нужно уметь отличить от обычного железного металлолома, а так же от другого цветного металла. Металлов которые нужно уметь различить не так уж и много. В основном кроме обычного железа встречаются алюминий, свинец, латунь, бронза и медь..
Также железо и прочий чермет довольно тяжелые и крепкие, гнуть, ломать изделия из железа довольно тяжело. Цветные металлы или цветмет отличаются тем, что не магнитятся, но цветмет в некоторых случаях нужно уметь отличить от обычного железного металлолома, а так же от другого цветного металла. Металлов которые нужно уметь различить не так уж и много. В основном кроме обычного железа встречаются алюминий, свинец, латунь, бронза и медь..
Алюминий металл очень легкий и мягкий, отличить его можно по весу. Следует учесть, что алюминиевые сплавы и детали от техники обычно тяжелее простого алюминия, а банки из алюминия идут в металлолом отдельно, самый ценный это алюминий электротехнический..
Свинец встречается в виде рыболовных грузил, грузов от шиномонтажа, а так же в обмотке бронированного электрокабеля, есть так же пломбы и пули из свинца. Свинец металл очень тяжелый и мягкий, окислившись имеет серый цвет, свежий свинец хорошо блестит..
Латунь и бронза это сплавы меди и принимаются на приемке по одной цене. Имеют желтый цвет и отличить бронзу от латуни довольно сложно, но можно собирать их вместе. Латунь может быть луженая и чтоб увидеть желтый блеск металла его нужно протереть напильником. Так же латунь в сантехнике часто покрывается другими металлами и ее необходимо царапнуть напильником, чтоб убедится, что это действительно латунь и не спутать ее с силумином..
Имеют желтый цвет и отличить бронзу от латуни довольно сложно, но можно собирать их вместе. Латунь может быть луженая и чтоб увидеть желтый блеск металла его нужно протереть напильником. Так же латунь в сантехнике часто покрывается другими металлами и ее необходимо царапнуть напильником, чтоб убедится, что это действительно латунь и не спутать ее с силумином..
Касательно меди, то отличить медь довольно просто, но все равно нужно знать некоторую информацию о меди. Медь имеет характерный красноватый оттенок, это мягкий и пластичный металл. С разобранных приборов медь блестит, но со временем медь окисляется, темнеет или становится зеленого цвета, ее нужно проверить магнитом и напильником, чтоб увидеть характерный медный блеск. В электроприборах так же встречается луженая медь, которая покрыта защитным составом для защиты от окисления, такую медь можно спутать с обычным металлом..
Надеюсь видео о том как различать и сортировать металлолом окажется полезным и познавательным, принесет кому-то практическую пользу. Всем желаю удачного сбора и поиска металлолома. Всем приятного просмотра! Спасибо за просмотр!
Всем желаю удачного сбора и поиска металлолома. Всем приятного просмотра! Спасибо за просмотр!
особенности заработка на сдаче лома
Сдача металлолома — это замечательная возможность избавиться от ненужных вещей и заработать хорошую сумму денег. Все металлы делятся на черные и цветные. К черным относится железо и все сплавы с ним, к цветным — остальное. Наиболее популярными вариантами из второй группы являются медь, алюминий, бронза, латунь и т.д. Люди с большим опытом находят даже драгоценные составы: серебро, золото, платину.
Почему цветной металлолом дороже?
Стоимость цветных металлов значительно выше, чем черных. Это связано с тем, что они менее распространены, поэтому являются более ценными. Хорошая электро- и теплопроводность, устойчивость к различным температурам и многие другие положительные свойства делают их незаменимыми в производстве. Они просто необходимы при создании бытовой и любой другой техники. Однако лом цветных металлов надо искать правильно. При всей распространенности он представлен в отдельных предметах в минимальном количестве.
При всей распространенности он представлен в отдельных предметах в минимальном количестве.
Также ценность цветного лома обусловлена тем, что на его переработку затрачивается намного меньше ресурсов, чем на добычу. Именно по этой причине сдача цветмета всячески поддерживается государством. Эта область серьезно контролируется: принимать материалы могут только пункты, имеющие соответствующие лицензии.
На стоимость лома влияют и другие факторы. Материалы с краской или другими покрытиями стоят дешевле. Обязательно учитывается и радиационный фон изделия: он должен находиться в пределах нормы. Перед сдачей рекомендуется поделить металлы по видам, убрать с них грязь. Чем чище и аккуратнее лом, тем больше за него можно выручить денег.
Где искать цветные металлы?
При ремонте или демонтаже дома или работе с техникой можно найти немало хороших материалов. Кто-то делает это целенаправленно, кто-то просто пользуется случаем. В любой ситуации надо обращать внимание на предметы, которые находятся под руками. Некоторые варианты металлов часто встречаются в быту.
Некоторые варианты металлов часто встречаются в быту.
- Медь. Этот металл красно-желтого цвета является одним из самых дорогих. Он используется для изготовления монет, кухонной утвари (сковородки, кастрюли), труб в системах кондиционеров, проводов и т.д. Осторожнее следует быть с различными кабелями. Пункты приема не берут такую продукцию, поскольку она запрещена законом. Это способ борьбы с мародерством, которое некоторое время активно процветало в данной сфере.
- Алюминий. Сам материал и его сплавы встречаются не так редко. Он есть в посуде, мебели, инструментах для сада/огорода, оконных профилях, водостоках и т.д. Стоимость зависит от особенностей сплава.
- Латунь. Прежде чем выбросить старую сантехнику, трубы и запорную арматуру, следует осмотреть все изделия на предмет латунных элементов. Они могут встретиться с большой вероятностью. Также из латуни изготавливают некоторые части радиаторов, дверную и мебельную фурнитуру, ключи.
- Свинец.
 Материал содержится в аккумуляторах и кабелях. Чтобы не прогадать с последними, заранее стоит ознакомиться со списком запрещенных для приема изделий. Каждый пункт имеет такой список в свободном доступе.
Материал содержится в аккумуляторах и кабелях. Чтобы не прогадать с последними, заранее стоит ознакомиться со списком запрещенных для приема изделий. Каждый пункт имеет такой список в свободном доступе. - Драгоценные металлы. Они могут содержаться также в аккумуляторах, химической аппаратуре, электронагревателях и т.д.
Если надо сдать лом и отходы цветных металлов, рекомендуется обращаться в компании, которые имеют современное оборудование. Это не только весы, но и приборы, высчитывающие дополнительные примеси в материале. Благодаря таким устройствам можно точно высчитать массу чистого вещества. Если же приемщик оценивает лом со своей точки зрения, такая оценка обычно не в пользу клиента. Но при выборе проверенной компании с хорошей репутацией подобных проблем возникнуть не может.
Пункт приема латуни в Москве
Латунь широко применяется в сантехническом оборудовании и в радиаторах, поэтому часто после ремонта остается много лома, который можно выгодно сдать в пункт приема. Цена на этот сплав достаточно высока, поэтому пренебрегать дополнительной возможностью заработать не стоит. Фирма «ХотЛом» принимает металлолом в любых количествах, поэтому чтобы заработать не нужно копить большие объемы лома, а можно сдать его с выгодой.
Цена на этот сплав достаточно высока, поэтому пренебрегать дополнительной возможностью заработать не стоит. Фирма «ХотЛом» принимает металлолом в любых количествах, поэтому чтобы заработать не нужно копить большие объемы лома, а можно сдать его с выгодой.
Какой лом латуни мы принимаем?
Компания «ХотЛом» предлагает возможность сдать в любом количестве, любой лом латуни. В наш пункт приема можно утилизировать даже стружку латуни, которую зачастую производители просто выкидывают. Мы принимаем следующие виды латунных изделий:
- Гильзы;
- Куски металла, проволоку и провода из латуни;
- Обломки технических приборов;
- Водопроводные изделия;
- Автомобильные радиаторы;
- Радиаторы отопления;
- Отходы с латунных производств.
Почему с нами выгодно работать?
- Наша компания работает на рынке уже много лет;
- Свой автомобильный парк, поэтому при необходимости мы выезжаем на объект и осуществляем вывоз лома из любой точки Москвы.

- Расчет с клиентом производим на месте, наличными средствами или иными способами, как удобно вам.
- Мы гарантируем выгодные цены на металлолом.
Фирма «ХотЛом» принимает сплавы латуни и любые изделия из этого металла во всех пунктах приема. Мы работаем в четырех районах Москвы, но при необходимости вывезем лом и из другой части города. Для консультации и справки, обращайтесь по контактам. Фирма работает без выходных, поэтому сдать на утилизацию металл на лом можно в любой день.
Мы осуществляем прием латуни в Москве, Люберцах, Химках, Балашихе, Мытищах, Долгорудном, Королёве, Красногорске, Одинцово и в других регионах (спрашивайте у менеджеров).
Какие виды латуни можно продать на свалке металлолома?
При уборке квартиры, подвала, чердака или гаража вы наверняка встретите большое количество металлолома, который вместо того, чтобы оставаться на долгие годы, можно продать по привлекательной цене на свалке. Некоторые типы металлов, хотя они, казалось бы, сгорают до обычного железа, позволят вам заработать действительно хорошие деньги — например, латунь, которая является чрезвычайно востребованным сырьем во многих отраслях промышленности. Познакомьтесь с ее свойствами и узнайте, какие виды латуни можно продать в магазине.
Познакомьтесь с ее свойствами и узнайте, какие виды латуни можно продать в магазине.
Что такое латунь и каковы ее свойства?
Латунь, смесь меди и цинка, является одним из наиболее распространенных металлических сплавов с широким промышленным применением. Он имеет характерный золотисто-желтый цвет, который во многом зависит от процентного содержания цинка (обычно до 45%) и используемых легирующих добавок, наиболее популярными из которых являются: свинец, марганец, олово, железо, алюминий и хром. Латунь — очень необходимый сплав из-за своих свойств.Его плотность выше, чем у стали, и достигает 9 кг / дм3, а температура плавления, в зависимости от состава сплава, составляет около 1000 ° C. Благодаря этому он используется, среди прочего, в отопительных установках или при производстве деталей автомобилей, подверженных воздействию высоких рабочих температур.
Однофазная и двухфазная латунь
Однофазная латунь содержит не более 30% цинка, что демонстрирует отличные пластические свойства, что позволяет обрабатывать ее в стандартных условиях. Чем выше процентное содержание Zn, тем тверже становится латунь и меньше поддается холодной обработке. В свою очередь, двухфазные латуни характеризуются более высоким содержанием цинка, что делает их менее пластичными, но в то же время гораздо более прочными. Этот тип латуни часто используется для производства листов, труб или стержней, а также винтов и фитингов. В промышленности также используются легированные и литейные латуни. Первые применимы, т. Е. в производстве подшипников благодаря хорошим свойствам скольжения и высокой коррозионной стойкости.В свою очередь, литейные латуни представляют собой многокомпонентные сплавы, чаще всего обогащенные такими металлами, как марганец, кремний или свинец.
Чем выше процентное содержание Zn, тем тверже становится латунь и меньше поддается холодной обработке. В свою очередь, двухфазные латуни характеризуются более высоким содержанием цинка, что делает их менее пластичными, но в то же время гораздо более прочными. Этот тип латуни часто используется для производства листов, труб или стержней, а также винтов и фитингов. В промышленности также используются легированные и литейные латуни. Первые применимы, т. Е. в производстве подшипников благодаря хорошим свойствам скольжения и высокой коррозионной стойкости.В свою очередь, литейные латуни представляют собой многокомпонентные сплавы, чаще всего обогащенные такими металлами, как марганец, кремний или свинец.
Покупка латуни — что в ней продать?
Помимо меди и алюминия, латунь является одним из наиболее востребованных цветных металлов из-за ее широкого применения и широких возможностей обработки. Неудивительно, что почти каждый покупаемый лом в Польше также принимает латунь в различных формах. Наиболее популярные виды, которые можно продать в покупку:в том числе:
Наиболее популярные виды, которые можно продать в покупку:в том числе:
- лом желтой латуни — доступен в натуральном золотисто-желтом цвете. Этот вид латуни встречается, среди прочего, в: охладители, сантехнические устройства и установочные элементы, фурнитура или декоративные элементы,
- лом беленой латуни — т.е. латунь, покрытая верхним слоем никеля или цинка. Очень часто используется в гидравлических и охлаждающих устройствах,
- латунных и латунно-медных охладителях — охладителях, используемых в автомобилях, тракторах и сельскохозяйственных машинах, а также в устройствах и промышленных установках,
- несортированная латунь — покупка лома также принимает смешанную латунь, присутствует у разных видов.В этом типе сплавов сложно определить цвет и оттенок, ареолы
- , волосы и стружки — то есть всевозможные отходы постпроизводства латуни, что является побочным эффектом механической обработки.
,
Закупка латуни и цветных металлов — Познань
В нашу закупку лома принимаются все виды лома латуни, включенные в вышеупомянутые категории. Независимо от того, есть ли у вас отходы после производства, элементы гидравлической системы, арматура, охладители или декоративные элементы, вы можете в любой момент привезти их в нашу штаб-квартиру в Познани или заказать экспорт лома в больших количествах — мы приедем к вам с нашим собственный транспорт и предлагаем выгодную цену на лом, предназначенный для продажи на месте покупки.Свяжитесь с нами сегодня и ознакомьтесь с нашим текущим прайс-листом на латунный лом.
Независимо от того, есть ли у вас отходы после производства, элементы гидравлической системы, арматура, охладители или декоративные элементы, вы можете в любой момент привезти их в нашу штаб-квартиру в Познани или заказать экспорт лома в больших количествах — мы приедем к вам с нашим собственный транспорт и предлагаем выгодную цену на лом, предназначенный для продажи на месте покупки.Свяжитесь с нами сегодня и ознакомьтесь с нашим текущим прайс-листом на латунный лом.
.90 000 как узнать, сколько это стоит и где мы найдем?
Медь в химическом отношении, отмеченная символом Cu, является чрезвычайно характерным и популярным металлом с красноватым цветом и металлическим блеском. В природе на его долю приходится только 1% всех встречающихся соединений.
Что такое медь?
Медь — это металл, который выделяется среди лучших проводников электричества и тепла. В большинстве языков (купфер, кобре, медь) номенклатура происходит от латыни. «Купрум» или «Кипрская руда». Как уже было сказано, у меди много преимуществ:
«Купрум» или «Кипрская руда». Как уже было сказано, у меди много преимуществ:
- отлично проводит тепло
- отлично проводит электричество
- устойчиво к коррозии
- легко легируется
Кроме того, это еще:
- легко подключается
- немагнитный
- перерабатывается
- прочный
- растягивается
- просто красиво
Где найти медь?
При добыче меди ее получают из рудных минералов, присутствие которых было обнаружено у 160 видов.Однако известно, что этот вопрос задает каждый энтузиаст, занимающийся самоделкой и переработкой, и чтобы прояснить для людей, которые ищут медь, с точки зрения заработка. Итак, ниже представлены наиболее популярные варианты:
Лом электроники
Ни в коем случае не буду преувеличивать, если скажу, что 90% электронного лома — это медь. Начиная с компьютеров, заканчивая бытовой техникой, заканчивая RTV. Различные типы двигателей, установок и др.
Почему в электронном ломе так много меди?
Все благодаря уже упомянутой хорошей электропроводности.Мы используем медь для изготовления различных типов кабелей, коммуникационных и токопроводящих систем и электрических установок.
Кабели и провода старые
Пожалуй, самый ценный и популярный источник добычи меди — это кабели. Мы не раз принимаем участие в демонтаже старых электроустановок, и в них может быть золотая проволока, называемая медной. Поэтому стоит подумать об участии в модернизации или сносе построек.
Сколько стоит медь?
Стоимость меди во многом зависит от региона и текущего спроса.Однако мы можем взять средние значения, которые приводим ниже.
| Millber | 19,90 PLN / кг |
|---|---|
| Luminous, new energy | 19,30 PLN / кг |
| Шт. | 17,10 PLN / кг |
| Unsort, луч, жареный | 16,80 зл / кг |
| Электрозола | 16,20 зл / кг |
| печи с белеными трубами | 15,50 зл / кг |
| Щепа | 15,50 зл / кг |
Как распознать медь?
Большая часть ответа находится в первом абзаце, но позвольте мне напомнить вам об этом. Все дело в электропроводности и отсутствии намагниченности. По этой причине мы чаще всего будем видеть его в корпусе электропроводки, а для того, чтобы убедиться, стоит проверить его с помощью высокопрочного магнита, потому что он не магнитный.
Все дело в электропроводности и отсутствии намагниченности. По этой причине мы чаще всего будем видеть его в корпусе электропроводки, а для того, чтобы убедиться, стоит проверить его с помощью высокопрочного магнита, потому что он не магнитный.
Цвет и блеск — два наиболее важных фактора, определяющих его. Сравнивая ее с металлами, с которыми ее часто путают, например, с латунью и бронзой, медь имеет коричневатый оттенок с немного деревенским оттенком.Стоит знать, что он единственный чистый, истинный сам по себе. А латунь, например, представляет собой смесь.
.90 000 металлов, выбрасывать которые не стоит
Наша цивилизация производит огромное количество отходов. Управление ими становится все более и более проблематичным, поскольку в мире постепенно становится недостаточно места для их хранения. Кроме того, многие предметы, которые попадают в пресловутый мусор, сделаны из сырья, мировые ресурсы которого постоянно сокращаются.
Итак, прежде чем выбросить предмет в корзину, подумайте, можно ли его просто использовать повторно. И мы не предлагаем использовать его самостоятельно, а отдать специалистам. Например — закупка металлолома. Вы не только принесете пользу окружающей среде, но и получите финансовую выгоду от переработки.
И мы не предлагаем использовать его самостоятельно, а отдать специалистам. Например — закупка металлолома. Вы не только принесете пользу окружающей среде, но и получите финансовую выгоду от переработки.
Уточняйте цену при закупке лома
Как простой смертный может зарабатывать на жизнь объедками? Это действительно проще, чем вы думаете. Все, что вам нужно сделать, это пойти на свалку металлолома. Там вы можете легко вернуть медные кабели, утилизировать цветные металлы и в то же время немного поправить свой бюджет.Вместо того, чтобы выбрасывать — просто найдите поблизости металлический магазин и доставьте туда ненужный мусор.
Медь до 20 злотых за килограмм
Знаете ли вы, что покупка меди может принести вам до 20 злотых за каждый килограмм этого ценного сырья? На это стоит обратить внимание, ведь этого элемента вокруг нас огромное количество. Узнайте, как распознать медь и где ее найти.
Стоит знать, что медь можно найти практически в каждом электронном устройстве. Смартфон, компьютер, плита, телевизор есть — буквально все! Это связано с тем, что медь обладает отличными проводящими свойствами, что позволяет создавать точные электрические цепи. Почему стоит поискать покупку меди? Довольно неплохие деньги — один из аргументов. Также стоит помнить, что мировые ресурсы этого сырья стремительно сокращаются. Ведь он довольно интенсивно использовался для производства электронных устройств с конца 19 века. Так что давайте подумаем о планете и сделаем что-нибудь для ее защиты!
Смартфон, компьютер, плита, телевизор есть — буквально все! Это связано с тем, что медь обладает отличными проводящими свойствами, что позволяет создавать точные электрические цепи. Почему стоит поискать покупку меди? Довольно неплохие деньги — один из аргументов. Также стоит помнить, что мировые ресурсы этого сырья стремительно сокращаются. Ведь он довольно интенсивно использовался для производства электронных устройств с конца 19 века. Так что давайте подумаем о планете и сделаем что-нибудь для ее защиты!
Что на самом деле происходит с медью после того, как ее отправят на пункт переработки? Сначала металлолом помещается в специальную печь.Именно там все сырье плавится под воздействием температуры. Следующим этапом является так называемое восстановление меди с последующим ее разливом — в виде заготовок или прутков. Вид обработки меди, очевидно, зависит от качества поставляемого сырья. В худшем состоянии помещают в раствор серной кислоты, который позволяет очистить. Не знаете, как распознать медь? Это металл с характерным красным отливом. Однако с изношенными, более старыми медными элементами стоит обратить внимание на то, что они могут иметь зеленый цвет.Пример — медные кровли, покрытые патиной.
Однако с изношенными, более старыми медными элементами стоит обратить внимание на то, что они могут иметь зеленый цвет.Пример — медные кровли, покрытые патиной.
Элементы из латуни на сумму более 10 зл.
Латунь — еще один элемент, который можно найти в окружающем нас мире. Он особенно ценится за отличную теплопроводность. Вот почему его так охотно выбирают для производства, например, радиаторов. Кроме того, этот материал чрезвычайно устойчив к температурам — не только высоким, но и низким — он не крошится даже при экстремально низких температурах.
Алюминий тоже окупается
Другой металл, из которого можно изготовить, — это алюминий. Самый простой пример — это, конечно, алюминиевые банки, которые можно найти в любом продуктовом магазине. И хотя их сбор может иметь для вас немного отрицательный оттенок, мы все же призываем вас внести свой вклад в развитие планеты. Вы, наверное, задаетесь вопросом, как распознать алюминий. Это серебристый металл, который легко гнется даже в руках. Как выглядит переработка алюминия? Кратко объясним.
Как выглядит переработка алюминия? Кратко объясним.
Алюминийсодержащие отходы сначала поступают на сортировочную установку. Здесь происходит их очищение. Специальные пескоструйные аппараты позволяют удалять такие элементы, как
.
Переработке подлежат только поверхности, очищенные таким образом. Подготовленные таким образом отходы затем режутся на стружку, которая в свою очередь поступает на специальный пресс. И в таком виде их отправляют на сталелитейные и литейные заводы. Подготовленный таким образом материал теперь можно преобразовать в другие алюминиевые элементы, такие как жестяные банки или даже автомобильные диски
.
Металлические детали, которые также можно продать при покупке
Закупка цветных металлов позволяет легко принять любое количество элементов из металла.Независимо от того, являются ли они автомобильными деталями, такими как детали двигателя, детали кузова или даже диски, но также и все другие отходы. Например, при покупке подойдут и все мебельные комплектующие или различные украшения из металла. Также проверьте свой гараж на предмет неиспользованных инструментов — вы обязательно найдете такие, которые можно легко купить из цветных металлов. За изделия из жести можно получить неплохие деньги. Как распознать олово? Это металл серебристого цвета с голубоватым оттенком.Обычно его используют как соединитель для других элементов.
Например, при покупке подойдут и все мебельные комплектующие или различные украшения из металла. Также проверьте свой гараж на предмет неиспользованных инструментов — вы обязательно найдете такие, которые можно легко купить из цветных металлов. За изделия из жести можно получить неплохие деньги. Как распознать олово? Это металл серебристого цвета с голубоватым оттенком.Обычно его используют как соединитель для других элементов.
.
Латунь — свойства, применение, состав, типы
Латунь — это сплав меди и цинка, который, в том числе, используется в для создания дверной фурнитуры или фурнитуры, но не только! Хотите узнать о его применении, свойствах, составе и типах? Приглашаем к прочтению!
Что такое латунь?
Среди наиболее часто используемых металлических сплавов выделяется латунь. Он состоит преимущественно из меди и максимум 40% цинка.Более того, он также может быть обогащен различными типами легирующих добавок, например оловом, марганцем, железом, свинцом, алюминием, хромом и кремнием. Латунь плавится при температуре около 1000 ° C, но точная температура зависит от конкретного химического состава.
Латунь плавится при температуре около 1000 ° C, но точная температура зависит от конкретного химического состава.
Пример использования латуни доступен в магазине EBMiA: Болты, гайки, шайбы, винты
Свойства латуни
Латунь можно узнать по характерному желто-золотистому цвету, конечный цвет которого зависит от содержания цинка в составе.Когда он составляет около 45%, он приобретает более оранжево-желтый оттенок. Чем его меньше, тем больше цвет напоминает естественный цвет меди. Его плотность колеблется от 8,4 до 8,7 кг / дм 3 , что делает его немного тяжелее стали.
Плотность латуни
При работе с латунью, помимо температуры плавления, важным аспектом является ее плотность. Поскольку известно, что этот материал плавится при температуре от 850 ° С до 950 ° С, стоит также упомянуть, что удельная теплоемкость металла составляет 0,377 кДж * кг -1 * К-1 при термическом воздействии 20 ° С. С.Плотность латуни колеблется в пределах 8300-8700 кг / м 3 .
С.Плотность латуни колеблется в пределах 8300-8700 кг / м 3 .
Типы и состав латуни
α Однофазная латунь — их состав содержит максимум 30% цинка. Этот вид отличается большой пластичностью уже при комнатной температуре, а это значит, что их обрабатывают без предварительного нагрева. Также стоит отметить, что как прочность, так и твердость этих латуни возрастают с увеличением содержания цинка. Однофазные альфа-латуни используются для производства снарядов для боеприпасов.
Двухфазная латунь — их свойства являются связующим звеном между свойствами α и β латуни. Когда в них увеличивается содержание цинка, их прочность и твердость возрастают, но их пластичность снижается. Двухфазная латунь подходит, например, для для производства лент, труб, листов, прутков, поковок, винтов или экструдированных изделий. Однако следует учитывать, что двухфазные бюстгальтеры обладают меньшей коррозионной стойкостью по сравнению с однофазными бюстгальтерами.
Литая латунь — это обычно двухфазные и многокомпонентные сплавы.Среди добавок, которыми дополняют литейные латуни, наиболее распространены алюминий, свинец, железо, кремний и марганец.
Латунь из сплава — показывает отличную устойчивость к образованию ржавчины. Некоторые из них хорошо подходят для производства подшипников, поскольку обладают очень хорошими свойствами скольжения. Легированная латунь также отлично подходит для механической обработки.
Использование латуни
Латунь используется, в частности, в промышленном секторе, поскольку она имеет действительно отличные функциональные и технологические свойства.Они могут иметь немного разные свойства, а значит, и их применение — это зависит от химического состава. Некоторые сплавы будут более подвержены механической обработке, в то время как другие будут иметь лучшие пластические свойства.
Примеры использования латуни доступны в магазине EBMiA: Болты, гайки, шайбы, винты
В том числе используется латунь для производства арматуры, а также компонентов машин в автомобилестроении, судостроении, химической и электротехнической промышленности. Более того, он также широко используется для изготовления декоративных элементов в металлообрабатывающей промышленности.Сегодня все чаще вместо свинца используется добавка мышьяка, и эта комбинация хорошо работает при производстве элементов, контактирующих с питьевой водой, а также монет, дверных ручек, перил и замков. .
Более того, он также широко используется для изготовления декоративных элементов в металлообрабатывающей промышленности.Сегодня все чаще вместо свинца используется добавка мышьяка, и эта комбинация хорошо работает при производстве элементов, контактирующих с питьевой водой, а также монет, дверных ручек, перил и замков. .
В следующих статьях мы описали:
Сварка латуни
Типы, состав, свойства, применение бронзы
Чугун — виды, сварка, применение, свойства
Медь — что это такое , свойства, заявка
.
Виды и преимущества латунных издели
Изделия из латуни славятся своей долговечностью и износостойкостью при бережном уходе и правильном покрытии. Зачастую покрытием является нанесение верхнего защитного слоя непосредственно на сам металл. Выбор защитного слоя зависит напрямую от условий использования изделия. Если говорить о сооружениях или сантехнике, то материалами для покрытия в этом случае выступают цинк, алюминий, хром, никель и др. Также защитный слой может нести декоративную функцию, если речь идет об изделиях для интерьеров или предметах роскоши. Для этого латунные изделия производители могут посеребрить или позолотить способом напыления.
Зачастую покрытием является нанесение верхнего защитного слоя непосредственно на сам металл. Выбор защитного слоя зависит напрямую от условий использования изделия. Если говорить о сооружениях или сантехнике, то материалами для покрытия в этом случае выступают цинк, алюминий, хром, никель и др. Также защитный слой может нести декоративную функцию, если речь идет об изделиях для интерьеров или предметах роскоши. Для этого латунные изделия производители могут посеребрить или позолотить способом напыления.
Ржавеет ли латунь — нет, не ржавеет. Важным преимуществом латуни (даже классического сплава без примесей и добавок) среди других металлов является то, что она не ржавеет, а лишь темнеет, теряет зеркальный блеск, окисляется. Поэтому этот металл широко применялся и применяется до сих пор для изготовления смесителей, тазов, ванн, пуговиц, посуды, орденов, медалей, статуэток, подсвечников, рамок для больших зеркал или картин, основ для стеклянных столов, разнообразных украшений и др.
Новосвердловская металлургическая компания осуществляет продажу и доставку различных сплавов, черных и цветных металлов по Уралу, а также во всех города России и страны СНГ. Компания реализует продукцию от ответственных заводов-производителей, что дает возможность купить латунный прокат по выгодным ценам.
Компания реализует продукцию от ответственных заводов-производителей, что дает возможность купить латунный прокат по выгодным ценам.
Технология получения
В природе латунь не встречается.
Исходником-шихтой для ее производства служит сырье трех видов:
- Первичное. Добыча медных, цинковых, других руд ведется на природных месторождениях.
- Медный, цинковый, другой металлический лом, пригодный к переработке (вторсырье). Аккумулируется на пунктах приема.
- Отходы собственного производственного цикла меткомбинатов.
Традиционные способы получения предусматривают использование печей для выплавки меди и ее сплавов. Обычно это электро-индукционные агрегаты, снабженные магнитопроводом и работающие на низких частотах.
Микроструктура отшлифованного и протравленного латунного сплава под 400-кратным увеличением
Процесс получения сплава:
- Раскаленную медь помещают в печь.
- Следом загружают кусковой цинк.
- Плавка проходит при 875-945°С.

- В специальные латуни добавляют легирующие добавки.
- Массу перемешивают до однородности, разливают по формам.
На выходе получаются плоские либо круглые латунные слитки. У выплавленных изделий разная твердость, степень закалки и старения.
Процесс плавки
Для того чтобы латунь быстрее перешла в жидкое состояние, лучше помещать ее в тигель в измельченном виде. Следует иметь в виду: чем меньше будут такие куски, помещенные в тигель, тем быстрее начнется процесс плавления.
После того как вы наполните тигель измельченным металлом, необходимо установить сосуд в печь и начать ее нагрев до температуры плавления латуни. Если для плавки латуни вы используете заводскую муфельную печь, то следить за процессами, протекающими в тигле, можно через специальное окошко. В том случае, если вы самостоятельно изготовили печь простейшей конструкции, вам понадобится крышка из огнеупорного материала, которой будет закрываться емкость для плавления латуни.
Плавку в компактной печке заводского изготовления можно производить прямо на кухне.
Тигель извлекается из печи только тогда, когда весь металл, который в него помещен, полностью расплавился. Для вынимания емкости с латунью следует пользоваться специальными щипцами и делать это максимально аккуратно. На поверхности латуни, подвергнутой плавлению, всегда присутствует пленка, которую в обязательном порядке надо убрать. Выполнить такую операцию совсем несложно, если взять для этого обычную стальную проволоку.
Для литья изделия из латуни вы должны подготовить форму, благодаря которой металл, переходя из жидкого расплавленного состояния в твердое, примет требуемые очертания. Заливка латуни в такую форму выполняется только после того, как удалена пленка, о которой говорилось выше. Затем вам останется только дождаться, когда латунь, залитая в форму, полностью перейдет в твердое состояние и остынет.
В домашних условиях можно использовать и более упрощенный вариант плавильной печи, применяя в качестве нагревательных элементов газовую горелку. Подвергнуть латунь плавлению таким образом можно, надежно закрепив газовую горелку под сосудом для плавки в вертикальном положении.
При этом важно следить за тем, чтобы пламя, которое выдает горелка, равномерно охватывало всю нижнюю часть сосуда.
Процесс плавки пойдет быстрее, если использовать вторую горелку.
Используя такое простое приспособление, следует иметь в виду, что латунь, которая будет плавиться в тигле, подвергается значительному окислению. Чтобы минимизировать последствия этого процесса, который негативно отражается на характеристиках сплава, можно использовать обычный древесный уголь.
Таким образом, существует несколько способов, позволяющих эффективно расплавить латунь в домашних условиях. Выбирая один из них в зависимости от своих предпочтений и финансовых возможностей, вы сможете изготавливать из латуни методом литья изделия различного назначения.
Подготовка
Печь для плавки выкладывают из огнеупорного кирпича (лучше использовать марки с повышенной способностью). Ее необходимо надежно закрепить термостойким раствором, и некоторые мастера предпринимают меры, чтобы обезопасить ее от теплового воздействия – обмазывают снаружи специальными составами. Рекомендованное место возведения должно хорошо проветриваться, но при этом надежно укрыто от природных воздействий. Поэтому в мастерской устанавливают достаточно мощную вентиляцию, или размещают ее во дворе под навесом.
Рекомендованное место возведения должно хорошо проветриваться, но при этом надежно укрыто от природных воздействий. Поэтому в мастерской устанавливают достаточно мощную вентиляцию, или размещают ее во дворе под навесом.
Нагревательным элементом служат индукционные трубки из керамики. Мощность источника энергии – не менее 30 КВт, с максимально возможным КПД, изготовление – только из качественных деталей. Дополнительные приспособления – тигель, щипцы с закругленными краями и длинной ручкой, ложку для разливания расплавленного металла лучше купить фабричные. Однако некоторые умельцы предпочитают вместо графитовой емкости делать свой собственный тигель из шамота с дополнительным защитным слоем – это может быть жидкое стекло с добавлением талька или раствор силиката калия.
При интенсивной работе с металлом длительность любого такого приспособления будет небольшой.
Шамот выдержит больше расплавлений, чем графит, но с покупным и возиться не придется.
Области применения
Использование латуни охватывает самые разнообразные сферы человеческой деятельности. Так, золотистый цвет сплава обусловил его использование в бижутерии и в различных декоративных элементах. Также его используют в котельном деле, при производстве военного снаряжения и амуниции, при изготовлении проволок и труб конденсаторов, электрических терминалов и денежных монет.
Так, золотистый цвет сплава обусловил его использование в бижутерии и в различных декоративных элементах. Также его используют в котельном деле, при производстве военного снаряжения и амуниции, при изготовлении проволок и труб конденсаторов, электрических терминалов и денежных монет.
Благодаря устойчивости к разрушению в соленой воде металл используется при изготовлении снаряжения различных морских судов, а его акустические свойства позволяют делать духовые инструменты: трубы и аккордеоны. Благодаря бактерицидным свойствам, сплав используется для изготовления дверных ручек в больницах и госпиталях.
Если говорить о применении в качестве декора, то следует выделить производство ламп, светильников, карнизов и некоторых ювелирных изделий. Такого рода вещи производятся в основном в странах восточной Европы, на территории стран СНГ, а также во многих арабских и некоторых государствах Азии.
Благодаря легкости механической обработки, высокой износостойкости и невысокой цене, материал используется для изготовления разнообразных вентилей. Из-за высокой сопротивляемости коррозии и кавитации используется латунь для изготовления винтов судов. Также материал использует при производстве некоторых деталей современных компьютеров.
Из-за высокой сопротивляемости коррозии и кавитации используется латунь для изготовления винтов судов. Также материал использует при производстве некоторых деталей современных компьютеров.
Характеристика сплава
Латунь представляет собой макроскопический материал с однородной структурой. В его состав, как правило, включены металлические составляющие. От самого вещества он отличается своими свойствами, которые обеспечивает структурой фаз (микроструктурой или кристаллической структурой). Так, тепло- и электропроводность, которая характерна для металлов, в любом случае является также и свойством металлического сплава. Однако наряду с этим физические параметры могут меняться, если определенная фаза становится преобладающей.
Например, если рассматривать латунь, то повышение содержания цинка оказывает нелинейное воздействие на свойства этого материала и его марку. В меди цинк может растворяться до 39 процентов. Если эта величина достигнута, то состав обретает особую структуру и пластичность, но его прочность заметно снижается. Если же долю цинка увеличить, то возникает иная кристаллическая фаза, характеризующаяся увеличением прочностных характеристик и снижением пластичности.
Если же долю цинка увеличить, то возникает иная кристаллическая фаза, характеризующаяся увеличением прочностных характеристик и снижением пластичности.
Такой особенностью обладает любой металлический сплав. В общем, все сплавы на основе меди делятся на бронзы, латуни и припои. Бронзы собой представляют составы из олова и меди, алюминия и бериллия. У припоев может быть очень непростой состав. Однако если рассматриваемый материал можно с легкостью отличить от припоя, то с бронзой все несколько сложнее.
Они имеют очень сходный внешний вид, но совершенно разные свойства:
- Во-первых, бронза имеет крупнозернистую структуру, характеризуется долговечностью и высокой стойкостью к воздействию коррозии: детали из этого сплава можно использовать даже на улице. Ковкость этой разновидности сплава гораздо ниже, нежели у латуни.
- Во-вторых, это сочетание цинка и меди является более пластичным материалом, его можно обрабатывать с помощью холодной ковки. Но именно высокая степень пластичности обуславливает быстрый износ этого сплава, потому изделия из латуни можно применять лишь в качестве декоративных элементов.

В основном материал применяется в ювелирном деле. Для производства крупных деталей декора — предметы интерьера, украшения для лестниц (кованые) – рекомендуется применять бронзу.
Требования техники безопасности
- Расплавление латуни желательно проводить на открытом воздухе под навесом. Если рабочее место находится в помещении, организуют хорошую вентиляцию;
- В непосредственной близости от печи не должно быть легковоспламеняемых предметов, взрывопожароопасных жидкостей, баллонов с газом;
- В доступном месте возле рабочего стола необходимо иметь огнетушитель, большую емкость с водой;
- Работу проводят в спецодежде из хлопчатобумажной ткани, обувь должна быть из плотной кожи;
- Органы зрения защищают очками, органы дыхания – респиратором;
- На подходе к рабочему месту, столам с литейными формами не должно быть посторонних предметов, проводов, за которые можно зацепиться;
- Заливая расплавленный металл в форму, нужно стараться избегать брызг;
- В помещении должна быть аптечка с наличием всего необходимого для оказания первой медицинской помощи.

Влияние составных элементов
Для расширения спектра использования латуни и улучшения ее свойств, в сплав добавляют легирующие компоненты. Каждый составной элемент оказывает определенное воздействие:
- кремний понижает значение твердости, делает материал менее прочным, но устойчивым к износам при длительном трении;
- марганец повышает прочность и сопротивляемость коррозии;
- олово, алюминий и железо в небольших пропорциях присоединяют к сплаву вместе с марганцем для улучшения значений прочности;
- свинец почти перестали добавлять в качестве легирующего элемента, он снижает механические свойства сплава, ухудшает пластичность, упругость;
- никель повышает сопротивляемость коррозии и дает возможность использовать металл в щелочных средах;
- алюминий, оксид алюминия создает защитное покрытие на поверхности металла, которое не дает окислительным процессам оказывать разрушительное воздействие;
- олово является легким металлом, его добавление способствует улучшению параметров прочности и устойчивости к коррозии.

Сплав с оловом широко применяют для создания комплектующих деталей для кораблей, которые постоянно работают в условиях морской воды.
Самые прочные металлы на Земле
Первое качество, с которым ассоциируется у нас металл, это прочность. На самом деле прочность определяется несколькими свойствами, учитывая которые именно сталь и ее сплавы находятся в списке самых прочных металлов.
Что же такое прочность? Это способность материала выдерживать внешние нагрузки, при этом не разрушаясь. При оценке прочности металла учитывается много параметров и качеств: насколько хорошо металл сопротивляется разрыву, как он противостоит сжатию, каков порог перехода от упругого к пластическому состоянию, когда деформация материала становится необратимой, какова способность материала сопротивляться распространению трещин и т.п.
Прочные сплавы и природные металлы
Сплавы представляют собой комбинации разных металлов. Потребность получить самые разные качественные характеристики металлов, среди которых и прочность, привела к появлению различных сплавов. Одним из важных в этом смысле сплавов является сталь, которая представляет собой комбинацию железа и углерода. Итак, какие же металлы принято считать самыми прочными на Земле?
Потребность получить самые разные качественные характеристики металлов, среди которых и прочность, привела к появлению различных сплавов. Одним из важных в этом смысле сплавов является сталь, которая представляет собой комбинацию железа и углерода. Итак, какие же металлы принято считать самыми прочными на Земле?
Поскольку для определения прочности металла необходимо учесть очень много факторов, трудно однозначным образом упорядочить металлы от самого «крепкого» до самого «слабого». В зависимости от того, какое свойство считается наиболее важным в каждом конкретном случае, и будет складываться расстановка сил прочности среди металлов.
Сталь и ее сплавы
Сталь — это прочный сплав железа и углерода, с добавками других элементов, таких как кремний, марганец, ванадий, ниобий и пр. Благодаря различным системам легирования стали можно получать совершенно разный комплекс свойств новых сплавов.
Так, высокоуглеродистая сталь — это сплав железа с высоким содержанием углерода — получается прочной, относительно дешевой, долговечной, она хорошо поддается обработке. Из недостатков стоит отметить низкую прокаливаемость и низкую теплостойкость, что делает углеродистую сталь уязвимой в агрессивной среде.
Из недостатков стоит отметить низкую прокаливаемость и низкую теплостойкость, что делает углеродистую сталь уязвимой в агрессивной среде.
Сферы применения: из углеродистой стали изготавливают различные инструменты, детали машин и сложных механизмов, элементы металлоконструкций. Важным условием применения таких изделий является неагрессивная среда.
Сплав стали, железа и никеля – один из наиболее прочных сплавов. Существует несколько его разновидностей, но в целом легирование углеродистой стали никелем увеличивает предел текучести до 1420 МПа и при этом показатель предела прочности на разрыв доходит до 1460 МПа.
Сферы применения: сплавы на никелевой основе используют в конструкциях некоторых типов мощных атомных реакторов в качестве защитных высокотемпературных оболочек для предохранения от коррозии урановых стержней.
Нержавеющая сталь – коррозионностойкий сплав стали, хрома и марганца с пределом текучести до 1560 МПа и пределом прочности на разрыв до 1600 МПа. Как и все виды стали, этот сплав обладает высокой ударопрочностью и имеет средний балл по шкале Мооса.
Как и все виды стали, этот сплав обладает высокой ударопрочностью и имеет средний балл по шкале Мооса.
Сферы применения: благодаря своим антикоррозийным свойствам нержавеющую сталь широко применяют в самых разных областях – нефтехимической промышленности, машиностроении, строительстве, электроэнергетике, кораблестроении, пищевой промышленности и для изготовления бытовых приборов.
Особо твердые сплавы
Сплавы на основе карбидов вольфрама, титана, тантала обладают твердостью, которой позавидует любой молот Тора.
Титан – это наиболее растиражированный в средствах массовой информации и кинематографе природный металл, который принято ассоциировать с суперпрочностью. Его удельная прочность почти вдвое выше, чем аналогичная характеристика легированных сталей. Он обладает самым высоким отношением прочности на разрыв к плотности из всех металлов. По этому показателю он обошел вольфрам, вот только по шкале твердости Мооса титан ему уступает. Тем не менее, титановые сплавы прочны и легки.
Тем не менее, титановые сплавы прочны и легки.
Сферы применения: титан и его сплавы часто используются в аэрокосмической промышленности. Из него делают элементы обшивки космических кораблей, топливные баки, детали реактивных двигателей. Активно используют его и в морском судостроении, строительстве трубопроводов для агрессивных сред и в качестве конструкционного материала.
Вольфрам с его самой высокой прочностью на растяжение среди всех встречающихся в природе металлов часто комбинируют со сталью и другими металлами для создания еще более прочных сплавов. К недостаткам вольфрама можно отнести его хрупкость и способность к разрушению при ударе.
Сферы применения: вольфрам применяют в металлургии для производства легированных сталей и различных сплавов, в электротехнической индустрии для изготовления элементов осветительных приборов, в машино- и авиастроении, в космической отрасли и химпроме. Сплав вольфрама и углерода (карбид вольфрама) используют для производства инструментов с режущими краями, таких как ножи и дисковые пилы, а также износостойких рабочих элементов горношахтного оборудования и прокатных валков.
Тантал обладает сразу тремя достоинствами – прочностью, плотностью и устойчивостью к коррозии. Он состоит в группе тугоплавких металлов, как и выше описанный вольфрам.
Сферы применения: тантал используется в производстве электроники и сверхмощных конденсаторов для персональных компьютеров, смартфонов, камер и для электронных устройств в автомобилях.
Инновационные сплавы
Существует ряд сплавов, которые появились совсем недавно, но уже успели завоевать признание благодаря своим «сверхкачествам» и активно используются в аэрокосмической сфере и медицине.
Алюминид титана – сплав титана и алюминия, который выдерживает высокие температуры и обладает антикоррозийными свойствами, но при этом он довольно хрупкий и недостаточно пластичный. Тем не менее, он нашел свое применение в производстве специальных защитных покрытий.
Сплав титана с золотом – еще один уникальный материал, который был разработан несколько лет назад группой ученых из университетов США. Основная задача, которая стояла перед учеными, создать материал крепче титана, который можно было бы применять в медицине для производства протезов, совместимых с биотканью. Дело в том, что титановые протезы, несмотря на свою прочность, изнашиваются относительно быстро, их приходится менять каждые 10 лет. А вот сплав титана с золотом оказался вчетверо более прочным, чем те сплавы, что сейчас используются в производстве протезов.
Основная задача, которая стояла перед учеными, создать материал крепче титана, который можно было бы применять в медицине для производства протезов, совместимых с биотканью. Дело в том, что титановые протезы, несмотря на свою прочность, изнашиваются относительно быстро, их приходится менять каждые 10 лет. А вот сплав титана с золотом оказался вчетверо более прочным, чем те сплавы, что сейчас используются в производстве протезов.
Как отличить медь от латуни, бронзы, алюминия
Главная » Металлы и сплавы » Медь
Просмотров 1.1к. Опубликовано Обновлено
Содержание
- 1 Основные свойства и параметры меди
- 2 Отличия меди от латуни
- 3 Отличия меди от бронзы
- 4 Отличия меди от алюминия
Медь, как металл обладает выраженной пластичностью. Цвет меди имеет золотисто розовый оттенок с присутствием характерного металлического блеска. В качестве элемента периодической системы он имеет обозначение Cu. Название происходит от латинского Cuprum, что связано с именем острова Кипр. Имеются научные доказательства того, что в древние времена именно там находились рудники, где добывали, а затем выплавляли этот металл.
В качестве элемента периодической системы он имеет обозначение Cu. Название происходит от латинского Cuprum, что связано с именем острова Кипр. Имеются научные доказательства того, что в древние времена именно там находились рудники, где добывали, а затем выплавляли этот металл.
Древняя культура связана с изготовлением из нее украшений, посуды, иных предметов обихода. Но главным достижением древней металлургии было обстоятельство, при котором получили бронзу – сплав на ее основе.
Содержание
- Основные свойства и параметры меди
- Отличия меди от латуни
- Отличия меди от бронзы
- Отличия меди от алюминия
Основные свойства и параметры меди
Характерны следующие моменты:
- В контакте с кислородом воздуха способна образовывать оксидную пленку, что обусловлено появлением желтовато-красного оттенка. Этим можно ответить на вопрос, какого цвета медь. Если на свет посмотреть тонкую пластинку, то она будет зеленовато-голубого оттенка.

- В чистом виде обладает достаточно выраженной мягкостью и пластичностью. Ее легко прокатать и вытянуть. С добавлением примесей твердость повышается.
- Широта применения обусловлено ее способностью отличной электропроводности.
- Обладает хорошими показателями теплопроводности. По этой характеристике ее опережает лишь серебро.
- Для нее характерна высокая плотность, температура плавления и кипения.
- С добавлением примесей свойства теплопроводности и электропроводности падают.
- Стойкость по отношению к процессам, связанным с коррозией. В воде, например, железо будет окисляться значительно быстрее.
- Материал легко протянуть в довольно тонкую проволоку.
- Металл обладает диамагнетическими свойствами.
В химическом плане активность незначительная по своей величине. Если воздух сухой, то окисления не произойдет. Процесс проходит только на воздухе с достаточным содержанием влаги. Не поддается действию кислот без окислительных свойств. С химических позиций отличается выраженной амфотерностью. В зависимости от условий ее характеристики отличаются и принимают характер кислоты или основания.
С химических позиций отличается выраженной амфотерностью. В зависимости от условий ее характеристики отличаются и принимают характер кислоты или основания.
Отличия меди от латуни
Нередко возникает вопрос о том, как отличить медь от латуни. Латунь представляет собой сплав, где в 30% содержится цинк. В половине случаев для производства латуни проводят использование технического цинка, где его присутствует только 50%. Остальная часть состоит из свинца и других примесей. Для того чтобы различить эти представители, надо знать их характеристики. В связи с этим уместен вопрос, как определить медь?
Для отличия латуни от меди требуется выполнение ряда действий, с помощью которых можно распознать медь в домашних условиях:
- Чистят предмет, который необходимо проверить. Для удаления загрязнений используют водный раствор уксуса. Таким способом происходит удаление и окислов.

- Лучше определение проводить при белом свете. Медные изделия характеризуются красно-коричневым цветом. Латунная поверхность переливается несколькими цветами. Это связано с присутствием в ее составе нескольких представителей.
- Медные предметы мягкие и удар о твердую поверхность сопровождает приглушенность звука. У латуни этого нет. Звук более звонкий по своим характеристикам.
- Предметы способны содержать пометки в виде литеры «М» или «Л». По этому признаку эти два вида также могут отличаться.
- Узнать, что перед вами конкретно, можно и по области применения изделия. Медные изделия встретишь довольно редко, зато она повсеместно используется для производства проводов.
Перечисленными способами и проводят определение меди прямо дома.
Отличия меди от бронзы
Эти два вида имеют сходство по цвету. Поэтому иногда бывает необходимость провести разграничения. Это сделать не так сложно, если знать особенности бронзового состава. Узнать, что конкретно перед вами, можно по следующим характеристикам.
- Вещи из более пластичного материала характеризуются присутствием красновато-коричневого цвета. А вот для бронзы характерен желто-розовый оттенок. Даже по этому признаку можно отличить медь от бронзы.
- Отличить изделия можно и по характеру их взаимодействия с солевым раствором. Если им пролить медный предмет, то будет наблюдаться изменение цвета. Цвет у бронзы останется неизменным. Это также является характерным отличием.
- Оба вида отличаются свойствами эластичности. Если медная проволока легко сгибается одной рукой, то согнуть бронзовое изделие весьма проблематично.
- Медные вещи подвержены процессу естественного патинирования. При длительном взаимодействии с воздухом они покрываются зеленоватым налетом. У бронзовых изделий такой особенности не наблюдается.
Отличия меди от алюминия
Нередко актуальным становится вопрос, как отличать медь от алюминия.
По свойствам электропроводности она в 1,5 раза превышает этот показатель у алюминия. Такие предметы по прочности превосходят алюминиевые предметы. Если несколько раз согнуть алюминиевую проволоку, она сломается, а рыжая катанка останется невредимой. Можно даже отличить эти виды по весу. Изделия из алюминия гораздо легче. Температура плавления у алюминия гораздо меньше. Если при температуре 660 градусов он начинает плавиться, то такой температуры явно недостаточно для расплавления меди.
Такие предметы по прочности превосходят алюминиевые предметы. Если несколько раз согнуть алюминиевую проволоку, она сломается, а рыжая катанка останется невредимой. Можно даже отличить эти виды по весу. Изделия из алюминия гораздо легче. Температура плавления у алюминия гораздо меньше. Если при температуре 660 градусов он начинает плавиться, то такой температуры явно недостаточно для расплавления меди.
Рыжий провод легко спаять и контакт при этом будет весьма надежным. А вот обычным способом спаять алюминиевый провод весьма проблематично.
Он является представителем более молодым в плане его получения. В чистом виде он в природе не встречается, а, взаимодействуя с кислородом воздуха, способен образовывать стойкое соединение. Получать его стали лишь в 1825 году, в то время, как медь выплавляли уже в древние времена. Поскольку он гораздо легче, его активно используют при производстве самолетов. Поэтому он и получил название «крылатого металла». Добавляя в алюминий медь, получают сплав, имеющий название дюралюминий, для которого присущи более высокие характеристики прочности.
Латунь
Для использования в других целях см. Латунь (значения).
Латунь астролябия
Латунь кафедра с орлом. Приписывается Aert van Tricht, Лимбург (Нидерланды), c. 1500
Латунь является сплав из медь и цинк в пропорциях, которые можно изменять для достижения различных механических и электрических свойств.[1] Это замещающий сплав: атомы двух составляющих могут заменять друг друга в пределах одной и той же кристаллической структуры.
Латунь похожа на бронза, еще один сплав, содержащий медь, в котором используется банка вместо цинка;[2] как бронза, так и латунь могут включать небольшие пропорции ряда других элементы включая мышьяк, вести, фосфор, алюминий, марганец, и кремний. Различие между двумя сплавами в значительной степени историческое,[3] и современная практика в музеях и археология все чаще избегает обоих терминов для исторических объектов в пользу более общего «медный сплав «. [4]
[4]
Латунь долгое время была популярным материалом для украшения из-за ее яркого золотого внешнего вида, например за выдвижной ящик и дверные ручки. Он также широко используется для всех видов посуды из-за многих свойств, таких как низкая температура плавления, пригодность для обработки (как с ручными инструментами, так и с современными превращение и фрезерование машин), долговечность, электрические и теплопроводность. Он по-прежнему широко используется в приложениях с низким трение и требуется коррозионная стойкость, например замки, петли, шестерни, подшипники, боеприпасы оболочки, молнии, сантехника, шланговые соединения, клапаны, и электрические вилки и розетки. Он широко используется для музыкальные инструменты Такие как рога и колокола, а также используется как заменитель меди в производстве бижутерия, модное ювелирное украшение и другие бижутерия. Состав латуни, обычно 66 процентов меди и 34 процентов цинка, делает ее подходящей заменой ювелирным изделиям на основе меди, поскольку она демонстрирует большую устойчивость к коррозии. Латунь часто используется в ситуациях, когда важно, чтобы искры не подвергаться ударам, например, в приспособлениях и инструментах, используемых вблизи легковоспламеняющихся или взрывоопасных материалов.[5]
Латунь часто используется в ситуациях, когда важно, чтобы искры не подвергаться ударам, например, в приспособлениях и инструментах, используемых вблизи легковоспламеняющихся или взрывоопасных материалов.[5]
Содержание
- 1 Характеристики
- 2 Ведущий контент
- 3 Коррозионно-стойкая латунь для тяжелых условий эксплуатации
- 4 Использование в музыкальных инструментах
- 5 Бактерицидные и противомикробные препараты
- 6 Растрескивание сезона
- 7 Типы
- 8 История
- 8.1 Ранние медно-цинковые сплавы
- 8.2 Римский мир
- 8.3 Средневековый период
- 8.4 Африка
- 8.5 Ренессанс и постсредневековая Европа
- 9 Смотрите также
- 10 Рекомендации
- 11 Библиография
- 12 внешняя ссылка
Характеристики
Микроструктура проката и отожженный латунь (увеличение 400 ×)
Латунь имеет более высокую пластичность, чем бронза или цинк. Относительно низкий температура плавления из латуни (от 900 до 940 ° C, от 1650 до 1720 ° F, в зависимости от состава) и его характеристики текучести делают этот материал относительно легким для литья. Изменяя пропорции меди и цинка, можно изменять свойства латуни, что позволяет использовать твердые и мягкие латуни. В плотность из латуни от 8,4 до 8,73 г / см3 (От 0,303 до 0,315 фунта / куб. Дюйм).[6]
Изменяя пропорции меди и цинка, можно изменять свойства латуни, что позволяет использовать твердые и мягкие латуни. В плотность из латуни от 8,4 до 8,73 г / см3 (От 0,303 до 0,315 фунта / куб. Дюйм).[6]
Сегодня почти 90% всех латунных сплавов перерабатываются.[7] Потому что латунь не ферромагнитный, его можно отделить от лома черных металлов, пропустив его рядом с мощным магнитом. Лом латуни собирается и транспортируется в литейный цех, где плавится и перерабатывается в заготовки. Заготовки нагревают и экструдируют до желаемой формы и размера. Общая мягкость латуни означает, что ее часто можно обрабатывать без использования смазочно-охлаждающая жидкость, хотя есть исключения.[8]
Алюминий делает латунь более прочной и устойчивой к коррозии. Алюминий также создает очень полезный твердый слой оксид алюминия (Al2О3) на тонкой, прозрачной и самовосстанавливающейся поверхности. Олово обладает аналогичным действием и находит свое применение, особенно в морская вода аппликации (морские латуни). Из комбинации железа, алюминия, кремния и марганца получается латунь. носить — и устойчивый к разрыву.[9] Примечательно, что добавление всего лишь 1% железа к латунному сплаву приведет к получению сплава с заметным магнитным притяжением.[10]
Из комбинации железа, алюминия, кремния и марганца получается латунь. носить — и устойчивый к разрыву.[9] Примечательно, что добавление всего лишь 1% железа к латунному сплаву приведет к получению сплава с заметным магнитным притяжением.[10]
Бинарная фазовая диаграмма
Латунь будет ржаветь при наличии влаги, хлориды, ацетаты, аммиак, и некоторые кислоты. Это часто случается, когда медь реагирует с серой с образованием коричневого, а затем и черного поверхностного слоя. сульфид меди которые, если регулярно подвергаться воздействию слабокислой воды, такой как городская дождевая вода, могут затем окисляться на воздухе с образованием патина зелено-синего сульфат меди[требуется разъяснение ]. В зависимости от того, как образовался сульфидный / сульфатный слой, этот слой может защитить нижележащую латунь от дальнейшего повреждения.[11]
Хотя медь и цинк имеют большую разницу в электрический потенциал, полученный латунный сплав не подвергается интернализации гальваническая коррозия из-за отсутствия в смеси агрессивной среды. Однако, если латунь находится в контакте с более благородным металлом, таким как серебро или золото, в такой среде, латунь подвергнется гальванической коррозии; и наоборот, если латунь контактирует с менее благородным металлом, таким как цинк или железо, менее благородный металл подвергнется коррозии, а латунь будет защищена.
Однако, если латунь находится в контакте с более благородным металлом, таким как серебро или золото, в такой среде, латунь подвергнется гальванической коррозии; и наоборот, если латунь контактирует с менее благородным металлом, таким как цинк или железо, менее благородный металл подвергнется коррозии, а латунь будет защищена.
Ведущий контент
Чтобы улучшить обрабатываемость латуни, вести часто добавляют в концентрации около 2%. Поскольку свинец имеет меньшее температура плавления чем другие составляющие латуни, она имеет тенденцию мигрировать в границы зерен в виде глобул по мере остывания после литья. Рисунок, который глобулы образуют на поверхности латуни, увеличивает доступную площадь поверхности свинца, что, в свою очередь, влияет на степень выщелачивания. Кроме того, при резке свинцовые шарики могут размазываться по поверхности. Эти эффекты могут привести к значительному вымыванию свинца из латуни со сравнительно низким содержанием свинца.[12]
В октябре 1999 года генеральный прокурор штата Калифорния подал в суд на 13 основных производителей и дистрибьюторов по поводу содержания свинца. В лабораторных испытаниях исследователи штата обнаружили, что средний латунный ключ, новый или старый, превышает Предложение 65 Калифорнии лимиты в среднем в 19 раз, при условии работы два раза в день.[13] В апреле 2001 года производители согласились снизить содержание свинца до 1,5% или столкнуться с требованием предупреждать потребителей о содержании свинца. Клавиши, покрытые другими металлами, не подвержены оседанию и могут продолжать использовать латунные сплавы с более высоким процентным содержанием свинца.[14][15]
В лабораторных испытаниях исследователи штата обнаружили, что средний латунный ключ, новый или старый, превышает Предложение 65 Калифорнии лимиты в среднем в 19 раз, при условии работы два раза в день.[13] В апреле 2001 года производители согласились снизить содержание свинца до 1,5% или столкнуться с требованием предупреждать потребителей о содержании свинца. Клавиши, покрытые другими металлами, не подвержены оседанию и могут продолжать использовать латунные сплавы с более высоким процентным содержанием свинца.[14][15]
Также в Калифорнии должны использоваться бессвинцовые материалы для «каждого компонента, который контактирует со смачиваемой поверхностью труб и трубопроводная арматура, сантехническая арматура и арматура ». 1 января 2010 года максимальное количество свинца в« бессвинцовой латуни »в Калифорнии было снижено с 4% до 0,25%.[16][17]
Коррозионно-стойкая латунь для тяжелых условий эксплуатации
Кран для отбора проб из латуни с ручкой из нержавеющей стали
Устойчивый к децинкификации (DZR или DR) латунь, иногда обозначаемая как CR (коррозия стойкие) латуни, используются там, где существует большой риск коррозии и где обычные латуни не соответствуют стандартам. Применения с высокими температурами воды, хлориды наличие или отклонение качества воды (Мягкая вода ) играть роль. DZR-латунь отлично подходит для воды котел системы. Этот латунный сплав необходимо производить с особой тщательностью, уделяя особое внимание сбалансированному составу и надлежащим производственным температурам и параметрам, чтобы избежать долговременных отказов.[18][19]
Применения с высокими температурами воды, хлориды наличие или отклонение качества воды (Мягкая вода ) играть роль. DZR-латунь отлично подходит для воды котел системы. Этот латунный сплав необходимо производить с особой тщательностью, уделяя особое внимание сбалансированному составу и надлежащим производственным температурам и параметрам, чтобы избежать долговременных отказов.[18][19]
Примером латуни DZR является латунь C352, содержащая около 30% цинка, 61-63% меди, 1,7-2,8% свинца и 0,02-0,15% мышьяка. Свинец и мышьяк значительно подавляют потерю цинка.[20]
«Красные латуни», семейство сплавов с высоким содержанием меди и обычно менее 15% цинка, более устойчивы к потере цинка. Один из металлов, называемых «красной латунью», состоит из 85% меди, 5% олова, 5% свинца и 5% цинка. Медный сплав C23000, также известный как «красная латунь», содержит 84–86% меди, по 0,05% железа и свинца, а остальное — цинк.[21]
Еще один такой материал — бронза, из семейства красных латуней. Сплавы из бронзы содержат примерно 88% меди, 8-10% олова и 2-4% цинка. Свинец может быть добавлен для облегчения обработки или для подшипниковых сплавов.[22]
Сплавы из бронзы содержат примерно 88% меди, 8-10% олова и 2-4% цинка. Свинец может быть добавлен для облегчения обработки или для подшипниковых сплавов.[22]
«Морская латунь» для использования в морской воде содержит 40% цинка, но также 1% олова. Добавление олова подавляет выщелачивание цинка.[23]
В NSF International требуется латунь с содержанием цинка более 15%, используется в трубопроводная и сантехническая арматура, чтобы быть устойчивым к децинкификации.[24]
Использование в музыкальных инструментах
Коллекция медных духовых инструментов
Высота пластичность и удобоукладываемость, относительно хорошая устойчивость к коррозия, и традиционно приписывают акустический свойства латуни, сделали ее обычным металлом выбора для строительства музыкальные инструменты чей акустический резонаторы состоят из длинных, относительно узких трубок, часто свернутых или свернутых в спираль для компактности; серебро и его сплавы, и даже золото, использовались по тем же причинам, но латунь является наиболее экономичным выбором.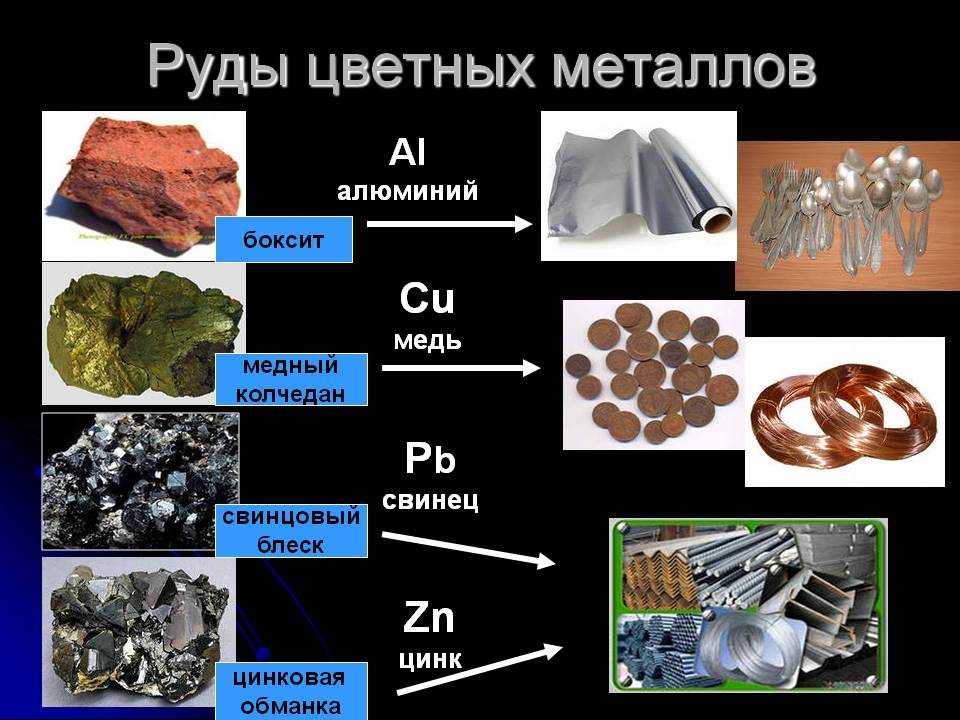 Все вместе известные как латунные инструменты к ним относятся тромбон, туба, труба, корнет, баритон рог, эуфониум, тенор рог, и валторна, и многие другие «рога «, многие в семьях разного размера, например саксофон.
Все вместе известные как латунные инструменты к ним относятся тромбон, туба, труба, корнет, баритон рог, эуфониум, тенор рог, и валторна, и многие другие «рога «, многие в семьях разного размера, например саксофон.
Другой духовые инструменты могут быть изготовлены из латуни или других металлов, и действительно, большинство современных студенческих моделей флейты и пикколо сделаны из латуни, обычно мельхиор сплав похожий на нейзильбер /Немецкое серебро. Кларнеты, особенно низкие кларнеты, такие как контрабас и субконтрабас, иногда изготавливаются из металла из-за ограниченных запасов плотных, мелкозернистых тропических лиственных пород, традиционно предпочитаемых для небольших деревянные духовые. По той же причине некоторые низкие кларнеты, фаготы и контрафаготы имеют гибридную конструкцию с длинными прямыми деревянными секциями и изогнутыми стыками, шейкой и / или металлическим колоколом. Использование металла также позволяет избежать риска воздействия на деревянные инструменты изменений температуры или влажности, которые могут вызвать внезапное растрескивание. Хотя саксофоны и саррузофоны классифицируются как деревянные духовые инструменты, они обычно изготавливаются из латуни по тем же причинам, а также потому, что их широкие конические отверстия и тонкостенные корпуса легче и эффективнее изготавливать путем формовки листового металла, чем путем обработки дерева.
Хотя саксофоны и саррузофоны классифицируются как деревянные духовые инструменты, они обычно изготавливаются из латуни по тем же причинам, а также потому, что их широкие конические отверстия и тонкостенные корпуса легче и эффективнее изготавливать путем формовки листового металла, чем путем обработки дерева.
Основа самых современных деревянные духовые, включая инструменты с деревянным корпусом, также обычно изготавливают из сплава, такого как нейзильбер /Немецкое серебро. Такие сплавы жестче и долговечнее, чем латунь, из которой изготавливаются корпуса инструментов, но их можно обрабатывать простыми ручными инструментами — благо для быстрого ремонта. В мундштуки обоих латунные инструменты и, реже, деревянный духовой инструменты часто делают из латуни, среди других металлов.
Сразу после латунные инструменты, наиболее заметное использование духовых инструментов в музыке ударные инструменты, в первую очередь тарелки, гонги, и оркестровые (трубчатые) колокола (большая «церковь» колокола обычно сделаны из бронза ). Маленький колокольчики и «колокольчик «также обычно изготавливаются из латуни.
Маленький колокольчики и «колокольчик «также обычно изготавливаются из латуни.
В гармоника это бесплатный язычковый аэрофон, также часто из латуни. В органные трубы из семейства тростниковых, латунные полосы (называемые язычками) используются в качестве тростей, которые бьются о шалот (или проткнуть лук-шалот «насквозь» в случае «свободного» тростника). Хотя не входит в состав латунной секции, малые барабаны также иногда делают из латуни. Некоторые части на электрогитары также сделаны из латуни, особенно из инерционных блоков на тремоло-системах из-за ее тональных свойств, а для гайки и седла струнных — как из-за тональных свойств, так и из-за низкого трения.[25]
Бактерицидные и противомикробные препараты
Основная статья: Антимикробные сенсорные поверхности из медного сплава
Смотрите также: Антимикробные свойства меди и Медные сплавы в аквакультуре
В бактерицидный свойства латуни наблюдались веками, особенно в морской среде, где она предотвращает биообрастание. В зависимости от типа и концентрации патогены и среда, в которой они находятся, латунь убивает их микроорганизмы в течение нескольких минут или часов после контакта.[26][27][28]
В зависимости от типа и концентрации патогены и среда, в которой они находятся, латунь убивает их микроорганизмы в течение нескольких минут или часов после контакта.[26][27][28]
Большое количество независимых исследований[26][27][28][29][30][31][32] подтверждают этот противомикробный эффект даже против устойчивых к антибиотикам бактерий, таких как MRSA и VRSA. Механизмы антимикробного действия меди и ее сплавов, включая латунь, являются предметом интенсивных и постоянных исследований.[27][33][34]
Растрескивание сезона
Трещины в латуни, вызванные аммиак атака
Латунь подвержена коррозионное растрескивание под напряжением,[35] особенно из аммиак или вещества, содержащие или выделяющие аммиак. Проблема иногда известна как сезонные трещины после того, как он был впервые обнаружен в латуни патроны используется для винтовка боеприпасы в 1920-е годы в Британская индийская армия. Проблема была вызвана высоким остаточные напряжения от холодной штамповки корпусов во время производства, а также от химического воздействия следов аммиака в атмосфере. Картриджи хранились в стойлах, и в жаркие летние месяцы концентрация аммиака повышалась, что приводило к появлению хрупких трещин. Проблема была решена отжиг гильзы и хранение картриджей в другом месте.
Проблема была вызвана высоким остаточные напряжения от холодной штамповки корпусов во время производства, а также от химического воздействия следов аммиака в атмосфере. Картриджи хранились в стойлах, и в жаркие летние месяцы концентрация аммиака повышалась, что приводило к появлению хрупких трещин. Проблема была решена отжиг гильзы и хранение картриджей в другом месте.
Типы
| Учебный класс | Массовая доля (%) | Примечания | |
|---|---|---|---|
| Медь | Цинк | ||
| Альфа-латунь | > 65 | < 35 | Латунь Alpha податлива, может обрабатываться в холодном состоянии и используется при прессовании, ковке и т. Д. Они содержат только одну фазу, с гранецентрированная кубическая Кристальная структура. Благодаря высокому содержанию меди эти латуни имеют более золотистый оттенок, чем другие. Альфа-фаза — это замена Твердый раствор цинка в меди. По свойствам он близок к меди, прочен, прочен и довольно трудно поддается обработке. Наилучшая формуемость — с 32% цинка. Сюда относятся коррозионно-стойкие красные латуни с содержанием цинка не более 15%. Наилучшая формуемость — с 32% цинка. Сюда относятся коррозионно-стойкие красные латуни с содержанием цинка не более 15%. |
| Альфа-бета латунь | 55–65 | 35–45 | Также называемый дуплексные латуни, они подходят для горячей обработки. Они содержат как α, так и β ‘фазы; β’-фаза упорядочена объемно-центрированный кубический, с атомами цинка в центре кубиков, он тверже и прочнее, чем α. Латунь альфа-бета обычно подвергается горячей обработке. Более высокое содержание цинка означает, что эти латуни ярче, чем альфа-латуни. При 45% цинка сплав имеет самую высокую прочность. |
| Бета-латуни[нужна цитата ] | 50–55 | 45–50 | Бета-латунь можно обрабатывать только горячим способом, она тверже, прочнее и подходит для литья. Высокое содержание цинка и низкое содержание меди означает, что это одни из самых ярких и наименее золотистых из обычных латуни. |
| Гамма-латуни | 33–39 | 61–67 | Есть также гамма-латуни Ag-Zn и Au-Zn, Ag 30–50%, Au 41%. [36] Гамма-фаза представляет собой кубическую решетку. интерметаллид, Cu5Zn8. [36] Гамма-фаза представляет собой кубическую решетку. интерметаллид, Cu5Zn8. |
| Белая латунь | < 50 | > 50 | Они слишком хрупкие для обычного использования. Термин может также относиться к определенным типам нейзильбер сплавы, а также сплавы Cu-Zn-Sn с высоким содержанием (обычно 40% +) олова и / или цинка, а также преимущественно цинковые литейные сплавы с добавками меди. Они практически не имеют желтой окраски, а имеют гораздо более серебристый вид. |
Другими фазами, кроме α, β и γ, являются ε, гексагональный интерметаллид CuZn.3, η — твердый раствор меди в цинке.
| Название сплава | Массовая доля (%) | Другой | Примечания | |||
|---|---|---|---|---|---|---|
| Медь | Цинк | Банка | Свинец | |||
| Абиссинское золото | 90 | 10 | ||||
| Адмиралтейская латунь | 69 | 30 | 1 | Олово тормозит потеря цинка во многих средах. | ||
| Сплав Айха | 60.66 | 36.58 | 1.02 | 1,74% железа | Разработан для использования в морских условиях благодаря своей коррозионной стойкости, твердости и прочности. Типичным применением является защита днищ судов, но более современные методы катодной защиты сделали его менее распространенным. Его внешний вид напоминает золото.[37] | |
| Алюминиевая латунь | 77.5 | 20.5 | 2% алюминия | Алюминий улучшает коррозионную стойкость. Применяется для труб теплообменника и конденсатора.[38] | ||
| Мышьяковая латунь | Мышьяк; часто алюминий | Используется для котла топки. | ||||
| Картридж латунный (C260) | 70 | 30 | — | ≤ 0.07[39] | Хороший холодная обработка характеристики. Используется для ящиков для боеприпасов, сантехники и оборудования. | |
| Обычная латунь | 63 | 37 | Также называемый заклепка латунь. Дешево и стандартно для холодной обработки. Дешево и стандартно для холодной обработки. | |||
| Латунь DZR | Мышьяк | Стойкая к децинкификации латунь с небольшим содержанием мышьяка. | ||||
| Дельта металл | 55 | 41–43 | 1–3% железа, остальное — различные другие металлы. | Используемые пропорции делают материал более твердым и подходящим для клапанов и подшипников. | ||
| Свободная обработка латуни (C360) | 61.5 | 35.5 | 3 | 0,35% железа | Также называется латунь 360 или C360. Высокая обрабатываемость. Содержание свинца 2,5–3,7%[39] | |
| Позолота металла | 95 | 5 | Самый мягкий тип латуни, доступный на рынке. Золочение обычно используется для «курток» патронов; например., цельнометаллическая оболочка пули. Почти красного цвета. | |||
| Высокая латунь | 65 | 35 | Имеет высокий предел прочности и используется для пружины, винты, и заклепки. | |||
| Свинцовая латунь | > 0 | Альфа-бета латунь с добавлением вести для улучшения обрабатываемости. | ||||
| Бессвинцовая латунь | < 0.25 | Согласно Закону собрания Калифорнии, закон AB 1953 года содержит «не более 0,25% свинца».[16] Предыдущий верхний предел составлял 4%. | ||||
| Низкая латунь | 80 | 20 | Светло-золотистый цвет, очень пластичный; используется для гибких металлических шлангов и металлических мехи. | |||
| Марганцевая латунь | 70 | 29 | 1.3% марганец | Наиболее часто используется при изготовлении золотой доллар монеты в США.[40] | ||
| Muntz metal | 60 | 40 | Следы железа | Используется в качестве подкладки на лодках. | ||
| Морская латунь | 59 | 40 | 1 | Подобно адмиралтейской латуни. Также известен как бронза Тобина. [41] [41] | ||
| Никелевая латунь | 70 | 24.5 | 5,5% никеля | Используется для изготовления монет фунта в фунт стерлингов валюта. Также основная составляющая биметаллического Монета в один евро и центральная часть монеты Два евро. | ||
| Северное золото | 89 | 5 | 1 | 5% алюминия | Используется в 10, 20 и 50 центов евро монеты. | |
| Орихалк | 75-80 | 15-20 | След | Следы никеля и железа | Определяется из 39 слитков, извлеченных из древнего кораблекрушения в Гела, Сицилия. | |
| Металл принца | 75 | 25 | Тип альфа-латуни. Из-за желтого цвета он используется как имитация золота.[42] Также называемый Металл принца Руперта, сплав назван в честь Принц Руперт Рейнский. | |||
| Красная латунь, розовая латунь (C230) | 85 | 5 | 5 | 5 | Оба американских термина для сплава медь-цинк-олово, известного как бронза, и сплав, который считается как латунь, так и бронза. [43][44] Красная латунь — также альтернативное название для медный сплав C23000, который состоит из 14–16% цинка, минимум 0,05% железа и минимум 0,07% свинца,[39] а остальное медь.[45] Это также может относиться к унция металла, еще один сплав медь-цинк-олово. [43][44] Красная латунь — также альтернативное название для медный сплав C23000, который состоит из 14–16% цинка, минимум 0,05% железа и минимум 0,07% свинца,[39] а остальное медь.[45] Это также может относиться к унция металла, еще один сплав медь-цинк-олово. | |
| Богатая низкая латунь, Томпак | 5–20 | Часто используется в ювелирных изделиях. | ||||
| Кремний томбак | 80 | 16 | 4% кремний | Используется как альтернатива для деталей из литой стали. | ||
| Тонваль латунь | > 0 | Также называется CW617N, CZ122 или OT58. Не рекомендуется использовать в морской воде, так как она подвержена децинкификации.[46][47] | ||||
| Желтая латунь | 67 | 33 | Американский термин для обозначения 33% цинковой латуни. | |||
История
Основная статья: Изделия из бронзы и латуни.
Хотя формы латуни использовались с предыстория,[48] его истинная природа как медно-цинкового сплава не была понята до постсредневекового периода, потому что цинк пар который вступал в реакцию с медью, давая латунь, не был признан металл.[49] В Библия короля Якова делает много ссылок на «латунь»[50] перевести «nechosheth» (бронза или медь) с иврита на архаический английский. В Шекспировский английский использование слова «латунь» может означать любой бронзовый сплав или медь, что даже менее точное определение, чем современное.[нужна цитата ] Самые ранние латуни могли быть натуральными сплавами, изготовленными плавка медь с высоким содержанием цинка руды.[51] Посредством Римский латунь того времени преднамеренно производилась из металлической меди и цинковых минералов с использованием цементация процесс, продукт которого был каламиновая латунь, и вариации этого метода продолжались до середины 19 века.[52] В конечном итоге он был заменен на спекание, прямое легирование меди и цинка, которое было введено в Европа в 16 веке. [51]
[51]
Латунь исторически иногда называют «желтой медью».[53][54]
Ранние медно-цинковые сплавы
В Западная Азия и Восточное Средиземноморье ранние медно-цинковые сплавы теперь известны в небольшом количестве из ряда памятников 3-го тысячелетия до нашей эры в Эгейское море, Ирак, то Объединенные Арабские Эмираты, Калмыкия, Туркменистан и Грузия и из памятников 2-го тысячелетия до нашей эры в Западная Индия, Узбекистан, Иран, Сирия, Ирак и Ханаан.[55] Однако отдельные примеры медно-цинкового сплавы известны в Китай с еще 5-го тысячелетия до нашей эры.[56]
Состав этих ранних изделий из «латуни» сильно варьируется, и в большинстве из них содержание цинка составляет от 5 до 15 мас.%, Что ниже, чем в латуни, полученной путем цементации.[57] Это могут быть «природные сплавы «произведены путем плавки богатых цинком медных руд в редокс условия. Многие имеют такое же содержание олова, что и современная бронза. артефакты и возможно, что некоторые медно-цинковые сплавы возникли случайно и, возможно, даже не отличаются от меди.[57] Однако большое количество известных в настоящее время медно-цинковых сплавов позволяет предположить, что по крайней мере некоторые из них были изготовлены намеренно, и многие из них имеют содержание цинка более 12 мас.%, Что привело бы к характерному золотистому цвету.[57][58]
артефакты и возможно, что некоторые медно-цинковые сплавы возникли случайно и, возможно, даже не отличаются от меди.[57] Однако большое количество известных в настоящее время медно-цинковых сплавов позволяет предположить, что по крайней мере некоторые из них были изготовлены намеренно, и многие из них имеют содержание цинка более 12 мас.%, Что привело бы к характерному золотистому цвету.[57][58]
К VIII – VII векам до нашей эры. Ассирийский клинопись Таблички упоминают об использовании «меди гор», и это может относиться к «натуральной» латуни.[59] «Орейхалкон» (горная медь),[60] то Древнегреческий перевод этого термина, позже был адаптирован к латинский аурихалк Значение «золотая медь» стало стандартным термином для латуни.[61] В 4 веке до нашей эры. Платон знал Орихалкос такой же редкий и почти такой же ценный, как золото[62] и Плиний описывает, как аурихалк пришел из Киприот рудные месторождения, истощенные к I веку нашей эры. [63]Рентгеновская флуоресценция анализ 39 орихалк слитки, извлеченные из кораблекрушения 2600-летней давности у Сицилии, обнаружили, что они представляют собой сплав, состоящий из 75–80 процентов меди, 15–20 процентов цинка и небольшого процента никеля, свинца и железа.[64][65]
[63]Рентгеновская флуоресценция анализ 39 орихалк слитки, извлеченные из кораблекрушения 2600-летней давности у Сицилии, обнаружили, что они представляют собой сплав, состоящий из 75–80 процентов меди, 15–20 процентов цинка и небольшого процента никеля, свинца и железа.[64][65]
Римский мир
7-го века персидский кувшин из латуни с медной вставкой
Во второй половине первого тысячелетия до нашей эры использование латуни распространилось на обширную географическую территорию от Британия[66] и Испания[67] на западе в Иран, и Индия на востоке.[68] Похоже, этому способствовал экспорт и влияние Средний Восток и восточное Средиземноморье, где было освоено целенаправленное производство латуни из металлической меди и цинковых руд.[69] Писатель IV века до н.э. Теопомп, цитируется Страбон, описывает, как нагревают землю от Андейра в индюк произвел «капельки фальшивого серебра», вероятно, металлического цинка, который можно было использовать для превращения меди в орейхалкос. [70] В I веке до нашей эры греческий Диоскорид кажется, признал связь между цинком минералы и латунь, описывающие, как Кадмия (оксид цинка ) был найден на стенах печи используется для нагрева цинковой руды или меди и поясняет, что затем ее можно использовать для изготовления латуни.[71]
[70] В I веке до нашей эры греческий Диоскорид кажется, признал связь между цинком минералы и латунь, описывающие, как Кадмия (оксид цинка ) был найден на стенах печи используется для нагрева цинковой руды или меди и поясняет, что затем ее можно использовать для изготовления латуни.[71]
К первому веку до нашей эры латуни было достаточно, чтобы использовать ее в качестве чеканка в Фригия и Вифиния,[72] и после Августа денежная реформа 23 г. до н.э. он также использовался для изготовления римских dupondii и сестерции.[73] Равномерное использование латуни для чеканки монет и военной техники по всей Римский мир может указывать на степень участия государства в отрасли,[74][75] а латунь, кажется, даже намеренно бойкотировалась Еврейский общины в Палестине из-за его связи с римской властью.[76]
Латунь была произведена в процессе цементации, при котором медная и цинковая руда нагреваются до тех пор, пока не образуется пар цинка, который вступает в реакцию с медью. Есть хорошие археологические свидетельства этого процесса и тигли использовались для производства латуни путем цементирования, были найдены на Римский период сайты в том числе Ксантен[77] и Нидда[78] в Германия, Лион в Франция[79] и на ряде сайтов в Великобритании.[80] Они различаются по размеру от крошечного желудя до большого. амфоры как и сосуды, но все они имеют повышенный уровень цинка внутри и закрыты крышками.[79] Они не проявляют никаких признаков шлак или металл гранулы предполагая, что минералы цинка нагревали с образованием паров цинка, которые реагировали с металлической медью в твердотельная реакция. Ткань этих тиглей пористая и, вероятно, предназначена для предотвращения повышения давления, и во многих из них есть небольшие отверстия в крышках, которые могут быть предназначены для сброса давления.[79] или добавить дополнительные минералы цинка ближе к концу процесса. Диоскорид упомянул, что минералы цинка использовались как для обработки, так и для отделки латуни, возможно, предполагая вторичные добавки.
Есть хорошие археологические свидетельства этого процесса и тигли использовались для производства латуни путем цементирования, были найдены на Римский период сайты в том числе Ксантен[77] и Нидда[78] в Германия, Лион в Франция[79] и на ряде сайтов в Великобритании.[80] Они различаются по размеру от крошечного желудя до большого. амфоры как и сосуды, но все они имеют повышенный уровень цинка внутри и закрыты крышками.[79] Они не проявляют никаких признаков шлак или металл гранулы предполагая, что минералы цинка нагревали с образованием паров цинка, которые реагировали с металлической медью в твердотельная реакция. Ткань этих тиглей пористая и, вероятно, предназначена для предотвращения повышения давления, и во многих из них есть небольшие отверстия в крышках, которые могут быть предназначены для сброса давления.[79] или добавить дополнительные минералы цинка ближе к концу процесса. Диоскорид упомянул, что минералы цинка использовались как для обработки, так и для отделки латуни, возможно, предполагая вторичные добавки. [81]
[81]
В латуни, изготовленной в раннеримский период, по-видимому, содержание цинка составляло от 20% до 28%.[81] Высокое содержание цинка в монетах и изделиях из латуни снизилось после первого века нашей эры, и было высказано предположение, что это отражает потерю цинка во время переработка отходов и, таким образом, прекращается производство новой латуни.[73] Однако теперь считается, что это, вероятно, было преднамеренное изменение состава.[82] и в целом использование латуни увеличивается за этот период, составляя около 40% от всех медные сплавы использовался в римском мире к 4 веку нашей эры.[83]
Средневековый период
Крещение Христа в 12 веке купель в церкви Святого Варфоломея, Льеж
Мало что известно о производстве латуни в течение столетий сразу после распада Римская империя. Нарушение торговли оловом на бронзу из западная Европа возможно, способствовали росту популярности латуни на востоке, и к VI – VII векам нашей эры более 90% медный сплав артефакты из Египет были изготовлены из латуни. [84] Однако использовались и другие сплавы, такие как бронза с низким содержанием олова, и они варьируются в зависимости от местных культурных традиций, назначения металла и доступа к цинку, особенно между Исламский и византийский Мир.[85] И наоборот, использование настоящей латуни, похоже, сократилось в Западной Европе в этот период в пользу бронза и другие смешанные сплавы[86] но около 1000 латунных артефактов найдено в Скандинавский могилы в Шотландия,[87] латунь использовалась в производстве монет в Нортумбрия[88] и есть археологические и исторические свидетельства производства каламиновая латунь в Германии[77] и Низкие страны,[89] районы, богатые каламин руда.
[84] Однако использовались и другие сплавы, такие как бронза с низким содержанием олова, и они варьируются в зависимости от местных культурных традиций, назначения металла и доступа к цинку, особенно между Исламский и византийский Мир.[85] И наоборот, использование настоящей латуни, похоже, сократилось в Западной Европе в этот период в пользу бронза и другие смешанные сплавы[86] но около 1000 латунных артефактов найдено в Скандинавский могилы в Шотландия,[87] латунь использовалась в производстве монет в Нортумбрия[88] и есть археологические и исторические свидетельства производства каламиновая латунь в Германии[77] и Низкие страны,[89] районы, богатые каламин руда.
Эти места останутся важными центрами производства латуни на протяжении всего средневековый период,[90] особенно Dinant. Латунные предметы по-прежнему известны как Dinanderie На французском. В купель в церкви Святого Варфоломея, Льеж в современном Бельгия (до 1117 г. ) — выдающийся шедевр Романский латунное литье, хотя также часто описывается как бронза. Металл начала 12 века Глостерский подсвечник необычен даже по средневековым стандартам, поскольку представляет собой смесь меди, цинка, олова, свинца, никель, утюг, сурьма и мышьяк с необычно большим количеством серебро, варьируясь от 22,5% в основании до 5,76% в поддоне под свечой. Пропорции этой смеси позволяют предположить, что подсвечник был сделан из клада старых монет, вероятно, позднеримских.[91]Латтен это термин для обозначения декоративных бордюров и подобных предметов, вырезанных из листового металла, будь то из латуни или бронзы. Акваманилы как правило, изготавливались из латуни как в европейском, так и в исламском мире.
) — выдающийся шедевр Романский латунное литье, хотя также часто описывается как бронза. Металл начала 12 века Глостерский подсвечник необычен даже по средневековым стандартам, поскольку представляет собой смесь меди, цинка, олова, свинца, никель, утюг, сурьма и мышьяк с необычно большим количеством серебро, варьируясь от 22,5% в основании до 5,76% в поддоне под свечой. Пропорции этой смеси позволяют предположить, что подсвечник был сделан из клада старых монет, вероятно, позднеримских.[91]Латтен это термин для обозначения декоративных бордюров и подобных предметов, вырезанных из листового металла, будь то из латуни или бронзы. Акваманилы как правило, изготавливались из латуни как в европейском, так и в исламском мире.
Латунь акваманил из Нижняя Саксония, Германия, гр. 1250
Процесс цементирования продолжался, но литературные источники из Европы и Исламский мир похоже, описывают варианты более высокотемпературного жидкого процесса, который происходил в тиглях с открытым верхом. [92] Исламская цементация, похоже, использовала оксид цинка, известный как Tutiya или же тутти вместо цинковых руд для производства латуни, в результате чего получается металл с более низкой утюг примеси.[93] Ряд исламских писателей и 13 век Итальянский Марко Поло опишите, как это было получено сублимация из цинковых руд и конденсированный на глина или железные прутья, археологические образцы которых были обнаружены в Куш в Иране.[94] Затем его можно было использовать для изготовления латуни или в лечебных целях. В 10 веке Йемен аль-Хамдани описал, как распространяется аль-иглимия Вероятно, оксид цинка, на поверхности расплавленной меди образовывались пары тутия, которые затем вступали в реакцию с металлом.[95] Иранский писатель 13 века аль-Кашани описывает более сложный процесс, посредством которого Tutiya был смешан с изюм и осторожно обжаривают перед добавлением на поверхность расплавленного металла. В этот момент была добавлена временная крышка, предположительно, чтобы минимизировать утечку паров цинка.
[92] Исламская цементация, похоже, использовала оксид цинка, известный как Tutiya или же тутти вместо цинковых руд для производства латуни, в результате чего получается металл с более низкой утюг примеси.[93] Ряд исламских писателей и 13 век Итальянский Марко Поло опишите, как это было получено сублимация из цинковых руд и конденсированный на глина или железные прутья, археологические образцы которых были обнаружены в Куш в Иране.[94] Затем его можно было использовать для изготовления латуни или в лечебных целях. В 10 веке Йемен аль-Хамдани описал, как распространяется аль-иглимия Вероятно, оксид цинка, на поверхности расплавленной меди образовывались пары тутия, которые затем вступали в реакцию с металлом.[95] Иранский писатель 13 века аль-Кашани описывает более сложный процесс, посредством которого Tutiya был смешан с изюм и осторожно обжаривают перед добавлением на поверхность расплавленного металла. В этот момент была добавлена временная крышка, предположительно, чтобы минимизировать утечку паров цинка. [96]
[96]
В Европе имел место аналогичный жидкий процесс в тиглях с открытым верхом, который, вероятно, был менее эффективен, чем римский процесс и использование термина «тутти». Альбертус Магнус в 13 веке предполагает влияние исламских технологий.[97] 12 век Немецкий монах Теофил описали, как предварительно нагретые тигли наполнялись на одну шестую порошкообразным каламином и уголь затем доливают медью и древесным углем перед расплавлением, перемешивают и снова заливают. Конечный продукт был В ролях, потом снова растопил каламином. Было высказано предположение, что это второе плавление могло происходить при более низкой температуре, чтобы позволить больше цинка быть поглощен.[98] Альбертус Магнус заметил, что «сила» как каламина, так и тутти могла испариться и описал, как добавление порошка стекло можно было создать пленку, чтобы привязать его к металлу.[99] Немецкие тигли для изготовления латуни известны из Дортмунд датируется 10 веком нашей эры и с Soest и Schwerte в Вестфалия датируемые примерно 13 веком, подтверждают рассказ Феофила, поскольку они открыты, хотя керамика диски от Soest, возможно, служили свободными крышками, которые могли использоваться для уменьшения содержания цинка. испарение, и внутри есть шлак в результате жидкого процесса.[100]
испарение, и внутри есть шлак в результате жидкого процесса.[100]
Африка
12 век »Бронзовая голова от Ифе «, фактически из» цинк-латуни с высоким содержанием свинца «
Некоторые из самых известных объектов в Африканское искусство являются потерянный воск отливки Западной Африки, в основном из того, что сейчас Нигерия, произведенный первым Королевство Ифе а затем Бенинская Империя. Хотя обычно их называют «бронзой», Бенинские бронзы, сейчас в основном в британский музей и другие западные коллекции, а также большие портретные головы, такие как Бронзовая голова от Ифе из «цинк-латуни с высоким содержанием свинца» и Бронзовая голова королевы Идии, оба они также Британский музей, лучше охарактеризовать как латунь, хотя и с переменным составом.[101] Работа из латуни и бронзы по-прежнему имела важное значение в Бенин искусство и другие западноафриканские традиции, такие как Акан золотые весы, где металл считался более ценным материалом, чем в Европе.
Ренессанс и постсредневековая Европа
В эпоха Возрождения увидел важные изменения как в теории, так и в практике изготовления латуни в Европе. К 15 веку появились свидетельства возобновления использования тиглей для цементации с крышкой в Цвикау в Германии.[102] Эти большие тигли были способны производить около 20 кг латуни.[103] В салоне остались следы шлака и куски металла. Их нерегулярный состав предполагает, что это был более низкотемпературный, не совсем жидкий процесс.[104] В крышках тиглей были небольшие отверстия, которые были заблокированы глиняными пробками ближе к концу процесса, предположительно для максимального увеличения содержания цинка. поглощение на завершающих этапах.[105] Затем из треугольных тиглей плавили латунь для Кастинг.[106]
К 15 веку появились свидетельства возобновления использования тиглей для цементации с крышкой в Цвикау в Германии.[102] Эти большие тигли были способны производить около 20 кг латуни.[103] В салоне остались следы шлака и куски металла. Их нерегулярный состав предполагает, что это был более низкотемпературный, не совсем жидкий процесс.[104] В крышках тиглей были небольшие отверстия, которые были заблокированы глиняными пробками ближе к концу процесса, предположительно для максимального увеличения содержания цинка. поглощение на завершающих этапах.[105] Затем из треугольных тиглей плавили латунь для Кастинг.[106]
Технические писатели XVI века, такие как Бирингуччо, Ercker и Агрикола описал различные методы изготовления латуни с цементацией и приблизился к пониманию истинной природы процесса, отметив, что медь становилась тяжелее, когда она превращалась в латунь, и что она становилась более золотистой, когда добавлялось дополнительное количество каламина. [107] Металлический цинк также становился все более распространенным явлением. К 1513 г. металлический цинк слитки из Индии и Китая прибывали в Лондон и гранулы цинка, конденсированные в печь дымоходы в Раммельсберг в Германии использовались для изготовления латуни для цементации примерно с 1550 года.[108]
[107] Металлический цинк также становился все более распространенным явлением. К 1513 г. металлический цинк слитки из Индии и Китая прибывали в Лондон и гранулы цинка, конденсированные в печь дымоходы в Раммельсберг в Германии использовались для изготовления латуни для цементации примерно с 1550 года.[108]
В конце концов было обнаружено, что металлический цинк может быть легированный с медью для изготовления латуни, процесс, известный как спелтинг,[109] а к 1657 году немецкий химик Иоганн Глаубер признали, что каламин — это «не что иное, как неплавящийся цинк», а цинк — «наполовину спелый металл».[110] Однако некоторые более ранние латуни с высоким содержанием цинка и низким содержанием железа, такие как латунный мемориал Вайтмана 1530 года бляшка из Англии, возможно, был получен путем легирования меди с цинк и включать следы кадмий аналогичны тем, что содержатся в некоторых цинковых слитках из Китая.[109]
Однако от процесса цементирования не отказались, и уже в начале 19 века есть описания твердое состояние цементация в купольной печи при температуре около 900–950 ° C и продолжительностью до 10 часов. [111] Европейская латунная промышленность продолжала процветать и в постсредневековый период, чему способствовали такие инновации, как введение в 16 веке гидравлических молотов для производства аккумуляторы.[112] К 1559 г. германский город Аахен только мог произвести 300000 cwt латуни в год.[112] После нескольких неудачных попыток в XVI и XVII веках латунная промышленность также была основана в Англии, воспользовавшись обильными поставками дешевой меди. плавил в новом каменный уголь уволенный отражательная печь.[113] В 1723 г. Бристоль латунный производитель Неемия Защитник запатентовал использование гранулированный медь, полученная путем заливки расплавленного металла в холодную воду.[114] Это увеличило площадь поверхности медь, помогающая ей реагировать, и содержание цинка до 33% масс.[115]
[111] Европейская латунная промышленность продолжала процветать и в постсредневековый период, чему способствовали такие инновации, как введение в 16 веке гидравлических молотов для производства аккумуляторы.[112] К 1559 г. германский город Аахен только мог произвести 300000 cwt латуни в год.[112] После нескольких неудачных попыток в XVI и XVII веках латунная промышленность также была основана в Англии, воспользовавшись обильными поставками дешевой меди. плавил в новом каменный уголь уволенный отражательная печь.[113] В 1723 г. Бристоль латунный производитель Неемия Защитник запатентовал использование гранулированный медь, полученная путем заливки расплавленного металла в холодную воду.[114] Это увеличило площадь поверхности медь, помогающая ей реагировать, и содержание цинка до 33% масс.[115]
В 1738 году сын Неемии Уильям Чемпион запатентовал технологию для первого промышленного масштаба дистилляция металлического цинка, известного как дистилляция по убыванию или «английский процесс». [116][117] Этот местный цинк использовался при спектировании и позволил лучше контролировать содержание цинка в латуни и производство медных сплавов с высоким содержанием цинка, которые было бы трудно или невозможно производить с помощью цементации, для использования в дорогостоящих объектах, таких как научные инструменты, часы, латунь кнопки и бижутерия.[118] Однако Champion продолжал использовать более дешевый метод цементации каламином для производства латуни с низким содержанием цинка.[118] и археологические остатки цементирующих печей в форме улья были обнаружены на его работах в Warmley.[119] К середине-концу 18 века разработки более дешевой дистилляции цинка, такие как Джон-Жак Дони горизонтальные печи в Бельгии и снижение тарифов на цинк[120] а также спрос на коррозия Устойчивые сплавы с высоким содержанием цинка повысили популярность спелтинга, и в результате от цементирования в основном отказались к середине 19 века.
[116][117] Этот местный цинк использовался при спектировании и позволил лучше контролировать содержание цинка в латуни и производство медных сплавов с высоким содержанием цинка, которые было бы трудно или невозможно производить с помощью цементации, для использования в дорогостоящих объектах, таких как научные инструменты, часы, латунь кнопки и бижутерия.[118] Однако Champion продолжал использовать более дешевый метод цементации каламином для производства латуни с низким содержанием цинка.[118] и археологические остатки цементирующих печей в форме улья были обнаружены на его работах в Warmley.[119] К середине-концу 18 века разработки более дешевой дистилляции цинка, такие как Джон-Жак Дони горизонтальные печи в Бельгии и снижение тарифов на цинк[120] а также спрос на коррозия Устойчивые сплавы с высоким содержанием цинка повысили популярность спелтинга, и в результате от цементирования в основном отказались к середине 19 века. День 1991, стр. 192–3; Крэддок и Экштейн 2003 г., стр. 228
День 1991, стр. 192–3; Крэддок и Экштейн 2003 г., стр. 228
Библиография
- Бейли, Дж. (1990) «Производство латуни в древности с особым упором на римскую Британию» в Craddock, P.T. (ред.) 2000 лет цинку и латуни Лондон: Британский музей
- Крэддок, П. и Экштейн, К. (2003) «Производство латуни в древности путем прямого восстановления» в Craddock, P.T. и Ланг, Дж. (ред.) Горное дело и производство металлов сквозь века Лондон: Британский музей
- Дэй, Дж. (1990) «Латунь и цинк в Европе от средневековья до XIX века» в Craddock, P.T. (ред.) 2000 лет цинку и латуни Лондон: Британский музей
- Дэй, Дж. (1991) «Производство меди, цинка и латуни» в Дэй, Дж. И Тайлекоте, Р. Ф. (редакторы) Промышленная революция в металлах Лондон: Институт металлов
- Мартинон Торрес, М .; Ререн, Т. (2002). «Агрикола и Цвиккау: теория и практика производства латуни эпохи Возрождения в Юго-Восточной Германии». Историческая металлургия. 36 (2): 95–111.

- Ререн, Т. и Мартинон Торрес, М. (2008) «Naturam ars imitation: европейское медное производство между ремеслом и наукой» в Мартинон-Торрес, М. и Ререн, Т. (ред.) Археология, история и наука, объединяющие подходы к древним материалам: Left Coast Press
внешняя ссылка
- Brass.org
- [1]
- детали машин
- Производитель латунных деталей Индия
6.7A: Сплавы замещения — Химия LibreTexts
- Последнее обновление
- Сохранить как PDF
- Идентификатор страницы
- 2594
Когда расплавленный металл смешивается с другим веществом, существует два механизма, которые могут вызвать образование сплава: (1) атомный обмен или (2) межузельный механизм . Относительный размер каждого элемента в смеси играет основную роль в определении того, какой механизм будет реализован.
Относительный размер каждого элемента в смеси играет основную роль в определении того, какой механизм будет реализован.
Когда атомы относительно близки по размеру, обычно применяется метод обмена атомами, при котором некоторые из атомов, составляющих металлические кристаллы, замещаются атомами другой составляющей. Это называется замещающим сплавом . Примеры сплавов замещения включают бронзу и латунь, в которых некоторые атомы меди замещены либо атомами олова, либо атомами цинка.
Рисунок \(\PageIndex{1}\): Различные атомные механизмы образования сплавов, демонстрирующие структуры чистого металла, замещения и внедрения. (CCO; Hbf878 через Википедию)
Почему возникают сплавы замещения: соединение
Связь между двумя металлами лучше всего описывается как комбинация металлического «обмена электронами» и ковалентной связи, одно не может происходить без другого и доли одного к другим изменениям в зависимости от вовлеченных составляющих. Металлы разделяют свои электроны по всей своей структуре, этот поток электронов является причиной многих характеристик, связанных с металлами, включая их способность действовать как проводники. Различное количество и сила ковалентных связей могут меняться в зависимости от различных конкретных металлов и того, как они смешиваются. Ковалентная связь отвечает за кристаллическую структуру, а также за температуру плавления и различные другие физические свойства.
Различное количество и сила ковалентных связей могут меняться в зависимости от различных конкретных металлов и того, как они смешиваются. Ковалентная связь отвечает за кристаллическую структуру, а также за температуру плавления и различные другие физические свойства.
Рисунок \(\PageIndex{2}\): Примеры металлических сплавов замещения. В зависимости от конкретного типа сплава замещения они могут иметь несколько кристаллических структур. Две из возможных структур включают Face Center Cubic (слева) и Cubic Center Cubic (справа). Структура металлического сплава не ограничивается этими двумя структурами, но вместе они составляют большую часть обычных сплавов.
По мере увеличения сходства электронной структуры металлов, входящих в состав сплава, металлические характеристики сплава снижаются. Чистые металлы полезны, но их применение часто ограничивается свойствами каждого отдельного металла. Сплавы допускают смеси металлов, обладающие повышенной стойкостью к окислению, повышенной прочностью, электропроводностью и температурой плавления; Практически любым свойством можно управлять, регулируя концентрацию сплава. Примером может служить латунная дверная фурнитура, она прочная и устойчива к коррозии лучше, чем чистый цинк или медь, два основных металла, из которых состоит латунный сплав. Комбинация также имеет низкую температуру плавления, что позволяет легко отливать ее во множество различных форм и размеров. (1) Есть много других аспектов сплавов замещения, которые можно было бы изучить более подробно, но основная концепция заключается в том, что каждый отдельный металл в сплаве придают конечному продукту его химические и физические свойства.
Примером может служить латунная дверная фурнитура, она прочная и устойчива к коррозии лучше, чем чистый цинк или медь, два основных металла, из которых состоит латунный сплав. Комбинация также имеет низкую температуру плавления, что позволяет легко отливать ее во множество различных форм и размеров. (1) Есть много других аспектов сплавов замещения, которые можно было бы изучить более подробно, но основная концепция заключается в том, что каждый отдельный металл в сплаве придают конечному продукту его химические и физические свойства.
Сплавы замещения сыграли важную роль в развитии человеческого общества и культуры, какими мы их знаем сегодня. Сам бронзовый век назван в честь сплава замещения, состоящего из олова в металлическом растворе меди. Древние бронзы очень загрязнены или даже неправильно маркированы, содержат большое количество цинка и мышьяка, а также множество примесей. Эти многочисленные замещающие сплавы позволили создать более прочные инструменты и оружие, они позволили повысить производительность как в мастерской, так и на поле боя. Потребность в сырье, таком как олово и медь, для производства бронзы также стимулировала рост торговли, поскольку их руды редко встречаются вместе. Нынешнее химическое понимание сплавов замещения не было бы таким глубоким, если бы не полезность сплавов для человека.
Потребность в сырье, таком как олово и медь, для производства бронзы также стимулировала рост торговли, поскольку их руды редко встречаются вместе. Нынешнее химическое понимание сплавов замещения не было бы таким глубоким, если бы не полезность сплавов для человека.
Резюме
Сплав представляет собой смесь металлов, которая имеет объемные металлические свойства, отличные от свойств составляющих ее элементов. Сплавы могут быть образованы путем замены одного атома металла на другой такого же размера в решетке (сплавы замещения), путем вставки меньших атомов в отверстия в решетке металла (сплавы внедрения) или комбинацией того и другого. Хотя элементный состав большинства сплавов может варьироваться в широких пределах, некоторые металлы соединяются только в фиксированных пропорциях, образуя интерметаллические соединения.0028
Ссылки
- Смоллман Р.Э., Нган А.Х.В. и Смоллман Р.Э. (2007). Металлургия и современные материалы . Амстердам: Баттерворт Хайнеманн.

- Ван, Ф.Э.. (2005). Теория соединения металлов и сплавов . Амстердам: Эльзевир.
- Дикинсон, ОТПК (1994). Эгейский бронзовый век . Кембриджская мировая археология. Кембридж: Издательство Кембриджского университета.
Проблемы
- Встречаются ли сплавы замещающих металлов в природе на поверхности земли?
- Какие две характеристики металла необходимы для образования сплава замещения?
- Могут ли кислород или азот быть частью кристаллической структуры сплава замещения?
Растворы
- Нет, окисляющая природа земной атмосферы, а также потребность в определенных и концентрированных металлах не позволяют им встречаться в природе.
- Похожие радиусы и аналогичная электроотрицательность.
- Только металлические элементы могут образовывать необходимые металлические связи, позволяющие образовывать сплавы.
6. 7A: Substitutional Alloys распространяется по незадекларированной лицензии, автором, ремиксом и/или куратором является LibreTexts.
7A: Substitutional Alloys распространяется по незадекларированной лицензии, автором, ремиксом и/или куратором является LibreTexts.
- Наверх
- Была ли эта статья полезной?
- Тип изделия
- Раздел или Страница
- Показать страницу TOC
- № на стр.
- Теги
- замещающий сплав
Факты о никеле | Dartmouth Toxic Metals
Что такое никель?
Никель — металл серебристо-белого цвета, естественным образом встречающийся в земной коре. Никель занимает 24-е место в мире по распространенности и является переходным металлом, то есть занимает середину периодической таблицы элементов. Это указывает на то, что он обладает химическими свойствами, которые позволяют ему образовывать несколько химических соединений, некоторые из которых токсичны. Чистый никель тверд, но пластичен и по этой причине используется в качестве упрочняющего компонента в металлических сплавах. Он также является отличным проводником как тепла, так и электричества.
Никель занимает 24-е место в мире по распространенности и является переходным металлом, то есть занимает середину периодической таблицы элементов. Это указывает на то, что он обладает химическими свойствами, которые позволяют ему образовывать несколько химических соединений, некоторые из которых токсичны. Чистый никель тверд, но пластичен и по этой причине используется в качестве упрочняющего компонента в металлических сплавах. Он также является отличным проводником как тепла, так и электричества.
Этот элемент был случайно открыт в 1751 году бароном Акселем Фредериком Кронштедтом, который извлек его из минерала под названием никколит. Намереваясь извлечь медь, усилия барона привели к получению белого вещества, а не красноватого, как он ожидал. Он назвал новый металл «купферникель», немецкое слово, которое примерно переводится как «дьявольская медь».
Где можно найти никель?
Никель встречается повсюду в окружающей среде, но обычно только в следовых количествах. Например, концентрация никеля в питьевой воде на всей территории Соединенных Штатов составляет в среднем 2 части на миллиард (ppb), то есть на каждый миллиард частей воды приходится 2 части никеля (2 микрограмма на литр).
Например, концентрация никеля в питьевой воде на всей территории Соединенных Штатов составляет в среднем 2 части на миллиард (ppb), то есть на каждый миллиард частей воды приходится 2 части никеля (2 микрограмма на литр).
Этот металл также повсеместно присутствует в почве и может быть обнаружен в более высоких концентрациях в ряде минеральных руд, включая сульфиды, оксиды и силикаты никеля. Большая часть никеля в почве настолько тесно связана с другими минералами, что сопротивляется прямому поглощению растениями и животными и не может легко повлиять на здоровье человека или экосистемы.
Никель, обнаруженный в земной коре, имеет многочисленные природные источники. Никель можно найти как в гидротермальных жилах — каналах, по которым проходит вода, нагретая в глубинных слоях земли, так и в поверхностных отложениях, образовавшихся в результате эрозии и выветривания горных пород. Извержения вулканов выделяют большое количество никеля в потоки лавы, что позволяет предположить, что внутренние области земли содержат более высокие концентрации металла, чем земная кора. Было обнаружено, что метеориты содержат концентрированные залежи никеля, связанного с железом, а высокие концентрации никеля можно найти в морских конкрециях, которые представляют собой плотные отложения полезных ископаемых на дне океана.
Было обнаружено, что метеориты содержат концентрированные залежи никеля, связанного с железом, а высокие концентрации никеля можно найти в морских конкрециях, которые представляют собой плотные отложения полезных ископаемых на дне океана.
Следы никеля также присутствуют в воздухе — наследие промышленных операций, таких как переработка металлов, нефтяные и угольные электростанции и мусоросжигательные заводы. Обследование 111 городов США в 1982 году показало, что концентрация никеля в атмосфере колеблется от 1 до 86 нанограммов (миллиардных долей грамма) на кубический метр (10 кубических футов). Чтобы представить это в перспективе, Агентство по охране окружающей среды США рекомендует людям избегать вдыхания воздуха, содержащего более 50 микрограммов (миллионных долей грамма) никеля на кубический метр, что более чем в пятьсот раз превышает самую высокую измеренную концентрацию в атмосфере. в городе США.
В процессе очистки и сжигания руд, содержащих никель, образуются летучие формы никеля, такие как карбонил никеля и никелевая пыль. Эти соединения могут быть токсичными при непосредственном вдыхании в высоких концентрациях в течение длительного периода времени, и рабочие в этих отраслях должны быть защищены от воздействия этих соединений, чтобы сохранить свое здоровье.
Эти соединения могут быть токсичными при непосредственном вдыхании в высоких концентрациях в течение длительного периода времени, и рабочие в этих отраслях должны быть защищены от воздействия этих соединений, чтобы сохранить свое здоровье.
Каково использование никеля?
Никель был излюбленным компонентом монет, потому что он яркий и хорошо полируется, а также потому, что он легче меди, серебра и других металлов, обычно используемых в монетах. В 1850 году Швейцария стала первой современной страной, которая официально использовала никель для чеканки монет. США вскоре последовали этому примеру в 1850-х и 60-х годах, когда они ввели никель в свои пенни и пятицентовые монеты, чтобы сделать их легче. Хотя пятицентовая монета США содержала только 25 процентов никеля, она быстро стала известна как «никель». Первая монета из чистого никеля была выпущена Швейцарией в 1881 году; Австрия и Венгрия последовали их примеру в 189 г.3.
Поскольку никель не легко окисляется или ржавеет, в 1850-х годах этот металл был адаптирован в качестве материала для гальванического покрытия. Гальваника – это процесс, при котором ионы металла в химическом растворе притягиваются к твердому металлическому электроду. Когда ионы связываются с поверхностью металла, они образуют однородное тонкое покрытие. Гальваническое покрытие металлической поверхности никелем может образовать слой, защищающий от коррозии. Когда электрохимия никеля стала лучше изучена, его адаптировали для использования в батареях. Сегодня соединения никеля и кадмия используются для производства перезаряжаемых никель-кадмиевых (Ni-Cd) аккумуляторов.
Гальваника – это процесс, при котором ионы металла в химическом растворе притягиваются к твердому металлическому электроду. Когда ионы связываются с поверхностью металла, они образуют однородное тонкое покрытие. Гальваническое покрытие металлической поверхности никелем может образовать слой, защищающий от коррозии. Когда электрохимия никеля стала лучше изучена, его адаптировали для использования в батареях. Сегодня соединения никеля и кадмия используются для производства перезаряжаемых никель-кадмиевых (Ni-Cd) аккумуляторов.
Сегодня никель больше всего используется в сталелитейной промышленности, которая использует примерно две трети ежегодно производимого в мире никеля. Металл обладает необычными свойствами: он твердый — прочный, способный выдерживать разрушение под действием больших усилий — и пластичный — способный поддаваться или изгибаться до того, как сломается или треснет. Кроме того, никель химически подобен железу, но обладает особенно хорошей стойкостью к окислению. Из-за своего сходства с железом никель может легко заменить железо в стальных сплавах или смесях. Добавление никеля в сталь повышает ее прочность, пластичность, устойчивость к ржавчине и ее ценность.
Добавление никеля в сталь повышает ее прочность, пластичность, устойчивость к ржавчине и ее ценность.
Так называемые нержавеющие стали, которые содержат хром и от 5 до 25 процентов никеля, используются в самых разных областях. Коррозионно-стойкие свойства этой стали делают ее идеальной для использования в столовых приборах, смесителях, раковинах, уличном оборудовании, моторизованных транспортных средствах и кухонной одежде. Высокопрочные конструкционные стали с содержанием никеля используются в автомобильной, аэрокосмической и строительной отраслях. Практически любая тяжелая промышленность, производящая механические устройства, на каком-то этапе производственного процесса использует конструкционную или нержавеющую сталь.
Другие сплавы цветных металлов включают медно-никелевые сплавы, обычно содержащие около 65 процентов никеля, и медно-никелевые сплавы, которые обычно содержат около 10 процентов никеля. Их использование включает морское оборудование и оборудование для обработки неорганических кислот и щелочей. Никель-хромовые сплавы, содержащие от 40 до 70 процентов никеля, используются в агрессивных химических средах и при высоких температурах, таких как нагревательные элементы и детали реактивных двигателей, столовые приборы из нержавеющей стали и кухонная утварь. Никель-медно-цинковые сплавы, широко известные как никель-серебро, используются в декоративных целях, в том числе в ювелирных изделиях, из-за тонкой полировки, которую они могут достичь.
Никель-хромовые сплавы, содержащие от 40 до 70 процентов никеля, используются в агрессивных химических средах и при высоких температурах, таких как нагревательные элементы и детали реактивных двигателей, столовые приборы из нержавеющей стали и кухонная утварь. Никель-медно-цинковые сплавы, широко известные как никель-серебро, используются в декоративных целях, в том числе в ювелирных изделиях, из-за тонкой полировки, которую они могут достичь.
Нужен ли никель для здоровья?
Было показано, что никель является важным микроэлементом для нескольких видов животных и, вероятно, необходим для человека. Тем не менее, у людей нет известных заболеваний, связанных с дефицитом никеля, и вполне вероятно, что мы получаем весь необходимый нам никель из его повсеместного присутствия в пище и воде.
Опасен ли никель для здоровья?
Хотя чистый никель может легко реагировать с другими элементами с образованием различных химических соединений, большинство форм никеля не представляют угрозы для здоровья человека. Люди неосознанно ежедневно потребляют в среднем 170 микрограммов никеля, что немного меньше массы одной песчинки. Следовые количества никеля присутствуют в воздухе, которым мы дышим, и в предметах домашнего обихода, от кранов до шампуней. Эти количества не имеют известного влияния на здоровье человека или экосистемы.
Люди неосознанно ежедневно потребляют в среднем 170 микрограммов никеля, что немного меньше массы одной песчинки. Следовые количества никеля присутствуют в воздухе, которым мы дышим, и в предметах домашнего обихода, от кранов до шампуней. Эти количества не имеют известного влияния на здоровье человека или экосистемы.
В организме человека развились механизмы метаболизма — выделения и выведения — небольших количеств никеля. Водорастворимые формы никеля, вдыхаемые в виде частиц пыли в воздухе, растворяются в кровотоке, а никель также попадает в кровоток через кожу после контакта с никельсодержащими продуктами. Большая часть никеля в кровотоке удаляется почками и выводится из организма с мочой. Проглоченный никель проходит через желудочно-кишечный тракт, но не всасывается.
Было показано, что большие дозы никеля, такие как случайное проглатывание, имеют более неблагоприятные последствия для здоровья, начиная от болей в животе и заканчивая сердечной недостаточностью. Однако эти эффекты возникали после воздействия уровней, в 50 000–100 000 раз превышающих уровни, обычно встречающиеся в пищевых продуктах или питьевой воде, и являются явно редкими случаями. Количества, обнаруженные в этих исследованиях, даже превышают количества, обнаруженные в твердых никелевых отходах на полигонах опасных отходов.
Однако эти эффекты возникали после воздействия уровней, в 50 000–100 000 раз превышающих уровни, обычно встречающиеся в пищевых продуктах или питьевой воде, и являются явно редкими случаями. Количества, обнаруженные в этих исследованиях, даже превышают количества, обнаруженные в твердых никелевых отходах на полигонах опасных отходов.
Другие исследования показали, что работники, вдыхающие никелевую пыль на предприятиях по переработке и рафинированию металлов, а также работники, вдыхающие никельсодержащие пары при сварке нержавеющей стали, могут иметь более серьезные последствия для здоровья. Исследования в течение 1960-е годы показали ранние признаки того, что соединения никеля, такие как карбонил никеля, могут вызывать опухоли легких у лабораторных крыс. Более поздние исследования, проведенные в 1980-х годах Агентством по охране окружающей среды США (EPA), показали, что длительное воздействие пыли никелевых заводов, карбонила никеля или субсульфида никеля, всех прямых побочных продуктов рафинирования никеля и обработки металлов, может вызывать рак. Это привело к принятию федеральных правил, ограничивающих воздействие определенных соединений никеля на рабочем месте и в окружающей среде. При вдыхании в определенных формах и в течение достаточно длительного периода времени никель действительно канцерогенен для человека. Современные методы промышленной гигиены помогли обуздать эти нежелательные осложнения для здоровья, вызванные никелем, за счет снижения уровня никелевой пыли в воздухе на рабочем месте и предоставления защитного оборудования, которое снижает воздействие.
Это привело к принятию федеральных правил, ограничивающих воздействие определенных соединений никеля на рабочем месте и в окружающей среде. При вдыхании в определенных формах и в течение достаточно длительного периода времени никель действительно канцерогенен для человека. Современные методы промышленной гигиены помогли обуздать эти нежелательные осложнения для здоровья, вызванные никелем, за счет снижения уровня никелевой пыли в воздухе на рабочем месте и предоставления защитного оборудования, которое снижает воздействие.
К счастью для большинства людей, такое хроническое воздействие никеля встречается редко. Самая распространенная проблема со здоровьем, связанная с никелем, с которой сталкиваются люди, — это аллергическая реакция, возникающая в результате частого обращения с никельсодержащими продуктами. Доля населения, генетически предрасположенного к кожным аллергическим реакциям на никель (5-10%), аналогична другим металлам.
Как у людей развивается аллергическая реакция на никель?
Наиболее распространенным заболеванием, с которым сталкиваются люди, соприкасающиеся с никелем, является кожная сыпь, называемая контактным дерматитом. Это состояние может быть вызвано непосредственным прикосновением к никельсодержащим предметам, распространенным в большинстве домашних хозяйств. Монеты, сантехника, некоторые шампуни и моющие средства, пигменты и украшения могут содержать небольшое количество никеля, который может впитываться через кожу.
Это состояние может быть вызвано непосредственным прикосновением к никельсодержащим предметам, распространенным в большинстве домашних хозяйств. Монеты, сантехника, некоторые шампуни и моющие средства, пигменты и украшения могут содержать небольшое количество никеля, который может впитываться через кожу.
Со временем прямой контакт кожи с этими предметами может вызвать у человека чувствительность к металлу и аллергическую реакцию на никель. Например, ношение серег из металла, содержащего никель, может повысить чувствительность человека к этому элементу. Ученые считают, что никель в украшениях растворяется в поту, впитавшемся в кожу. Затем металл может связываться с одним из естественных белков организма. Этот никель-белковый комплекс может не распознаваться иммунной системой, и это может запускать сигналы к защитным механизмам организма, чтобы реагировать на комплекс, как если бы он был проникающим антигеном.
Наиболее частым результатом такой реакции является кожная сыпь в месте контакта. В более острых случаях сообщалось о приступах астмы. Как только человек становится сенсибилизированным к этому веществу, даже попадание никеля с пищей может вызвать аллергические симптомы. По этой причине аллергологи рекомендуют тем, кто страдает тяжелой аллергией на никель, снизить потребление никеля с пищей, избегая определенных продуктов, показанных в таблице ниже.
В более острых случаях сообщалось о приступах астмы. Как только человек становится сенсибилизированным к этому веществу, даже попадание никеля с пищей может вызвать аллергические симптомы. По этой причине аллергологи рекомендуют тем, кто страдает тяжелой аллергией на никель, снизить потребление никеля с пищей, избегая определенных продуктов, показанных в таблице ниже.
Как никель вредит живым существам?
сельдь, ростки, спаржа, арахис, грибы, ревень, кукуруза, какао, помидоры, капуста, устрицы, фасоль, лук, шпинат, горох, груши, изюм, чай, разрыхлитель, цельнозерновая мука, продукты, приготовленные в никелевой посуде, все консервы
Подобно большинству факторов окружающей среды, токсическое действие любого металла связано с тем, как он попадает в организм, или, говоря языком токсикологии, с путем его воздействия. Никель имеет три основных пути воздействия. Его можно вдыхать, проглатывать или всасывать через кожу. При вдыхании никеля газообразные соединения никеля, такие как субсульфид никеля или мелкие частицы никелевой пыли (в частности, частицы PM-2,5 — менее 2,5 микрометров в диаметре) оседают глубоко в легких. В случае ингаляционного воздействия ученые обнаружили, что форма никеля и его растворимость являются ключевым определяющим фактором в результирующих механизмах токсичности. Водорастворимые соединения никеля могут всасываться легкими в кровоток и в конечном итоге удаляться почками. Однако плохо растворимые соединения никеля со временем могут накапливаться в легких и вызывать такие осложнения, как легочный фиброз, накопление рубцовой ткани в легких, а также бронхит и рак легких. Механизм, который позволяет никелю вызывать или способствовать развитию рака, до сих пор очень плохо изучен.
В случае ингаляционного воздействия ученые обнаружили, что форма никеля и его растворимость являются ключевым определяющим фактором в результирующих механизмах токсичности. Водорастворимые соединения никеля могут всасываться легкими в кровоток и в конечном итоге удаляться почками. Однако плохо растворимые соединения никеля со временем могут накапливаться в легких и вызывать такие осложнения, как легочный фиброз, накопление рубцовой ткани в легких, а также бронхит и рак легких. Механизм, который позволяет никелю вызывать или способствовать развитию рака, до сих пор очень плохо изучен.
Представляет ли воздействие никеля на рабочем месте риск для здоровья?
Некоторые формы никеля являются канцерогенными или вызывают рак, но эти формы вряд ли можно встретить за пределами промышленных предприятий, таких как заводы по обработке металлов, особенно там, где перерабатывается никелевая руда и где производится нержавеющая сталь. Другими рабочими, которые могут подвергаться воздействию этих форм никеля, являются сварщики, гальваники, производители аккумуляторов, ювелиры, маляры, производители красок и лаков.
Работники металлургической промышленности, которые ежедневно подвергались воздействию никелевой пыли в виде карбонила никеля или субсульфида никеля, чаще болели раком носа, придаточных пазух носа и легких. Ингаляционное воздействие никелевой пыли также может привести к хроническому бронхиту, острому респираторному дистресс-синдрому и легочному фиброзу. Уровни никелевой пыли и соединений никеля в воздухе на промышленных предприятиях по переработке никелевых руд и сплавов до 1980-х годов были от 100 000 до 1 миллиона раз выше, чем типичные фоновые уровни, обнаруживаемые в воздухе на всей территории Соединенных Штатов. С тех пор Агентство по охране окружающей среды США определило, что пыль никелевых заводов, субсульфид никеля и карбонил никеля являются канцерогенами для человека в этих профессиональных условиях.
Управление по охране труда и здоровья (OSHA) разрабатывает и обеспечивает соблюдение федеральных правил, касающихся никеля и других токсичных веществ, для защиты работников от подобных вредных воздействий. OSHA определило, что уровень никеля в воздухе на рабочем месте не может превышать 1 микрограмм на кубический метр. Эта политика помогла снизить воздействие никелевой пыли на работников металлургической промышленности.
OSHA определило, что уровень никеля в воздухе на рабочем месте не может превышать 1 микрограмм на кубический метр. Эта политика помогла снизить воздействие никелевой пыли на работников металлургической промышленности.
Красота МЕДИ и ЛАТУНИ — Рабочее серебро
серьги из меди и стерлингового серебра и кольцо из латуни и стерлингового серебра
МЕДЬ и ЛАТУНЬ – прекрасные альтернативные металлы для изготовления украшений! Цена драгоценных металлов может быть непомерно высокой для изготовления ювелирных изделий, но не менее важны прекрасные качества меди и латуни (сплав меди и цинка). Медь имеет мягкий характер, легко текстурируется и формуется. Латунь имеет более твердый характер и может с силой поддержать Медь. Латунь также можно отжигать, что облегчает текстурирование и форму. Латунь также можно использовать в качестве украшения вместо золота (но она тускнеет).
Когда приходит осень, я всегда хочу делать и носить украшения из меди. Я не знаю, потому ли это, что он напоминает мне о ярких листьях, оранжевых тыквах или луне урожая, но в это время года медь кажется мне подходящей. С ним легко работать и он экономичен, что также делает его привлекательным выбором для крупных изделий. Как будто этого было недостаточно, со временем на нем появляется богатая, глубокая патина, которая только добавляет ему красоты.
С ним легко работать и он экономичен, что также делает его привлекательным выбором для крупных изделий. Как будто этого было недостаточно, со временем на нем появляется богатая, глубокая патина, которая только добавляет ему красоты.
медные завитки
Медь была хорошо известна древним. Впервые он был использован около 8000 г. до н.э. в естественной или нативной форме. Его выплавляли из сульфидных руд около 5000 г. до н.э., отливали в форму около 4000 г. до н.э. и сплав с оловом для создания бронзы около 3500 г. до н.э. Сегодня медь используется в электропроводке, кровле и водопроводе, а также в машинах. И, конечно же, он используется в декоративно-прикладном искусстве, например, в ювелирном деле.
Медь также необходима для всей жизни на Земле и естественным образом содержится во многих продуктах, включая какао, зеленые оливки и авокадо, и это лишь некоторые из моих любимых продуктов! Он уступает только серебру по электропроводности, а также является биостатическим, что означает, что на нем не могут расти бактерии и другие микроорганизмы. Медные браслеты часто носят люди, страдающие артритом, чтобы облегчить боль в суставах, а некоторые компрессионные изделия производятся с использованием медных волокон! Есть ли что-то, что медь не может сделать?
Медные браслеты часто носят люди, страдающие артритом, чтобы облегчить боль в суставах, а некоторые компрессионные изделия производятся с использованием медных волокон! Есть ли что-то, что медь не может сделать?
текстурированный медный лист
Медь и латунь производятся в различных продуктах, которые подходят для изготовления ювелирных изделий. Листовая медь и латунь доступны в различных размерах, которые можно использовать для подвесок, серег, браслетов и колец. Вы можете получить текстурированный медный лист с различными узорами, но я предпочитаю классическую чеканную текстуру. Кроме того, когда вас что-то раздражает, нет ничего лучше, чем несколько раз разбить лист металла молотком! Вы также можете приобрести медную и латунную проволоку круглого, квадратного и узорчатого сечения для любого проекта, который вы задумали. Для завершения ваших проектов также доступны медная рамка, медные трубки и припой для медной проволоки. Совет от одного из наших многочисленных знающих клиентов: когда медный припой потечет, не выключайте пламя сразу — оставьте его еще немного, и он станет такого же красивого ярко-медного цвета, как и остальная часть вашего изделия. Медь очень мягкая, и ей можно легко придать любую форму. Как и в случае с любым другим металлом, он затвердевает по мере того, как вы его формируете, поэтому вам может потребоваться периодически отжигать его. Когда вы закончите, медь и латунь можно отправить в тумблер для окончательной полировки, что также укрепит их.
Медь очень мягкая, и ей можно легко придать любую форму. Как и в случае с любым другим металлом, он затвердевает по мере того, как вы его формируете, поэтому вам может потребоваться периодически отжигать его. Когда вы закончите, медь и латунь можно отправить в тумблер для окончательной полировки, что также укрепит их.
Только помните, сначала стакан, затем патина и, наконец, закрепка камня.
медная рамка
Итак, что можно сделать с медью, чтобы сделать ее более интересной? Что ж, как упоминалось ранее, мне нравится бить по нему молотком с шариковым бойком. Однако, как и в случае с серебром, вы можете создавать всевозможные текстуры с помощью различных молотков и инструментов. Он может пройти через прокатный стан вместе с тканью, листьями, прокатными пластинами и т. д., чтобы создать интересные текстуры. Попробуйте разные патины. Отделку verdigris можно создать с помощью нашатырного спирта, соли и/или уксуса. В Интернете есть много информации о медянке, но будьте осторожны, если вы используете аммиак. Убедитесь, что вы работаете в хорошо проветриваемом помещении и носите защитное снаряжение. Silver Black отлично подходит для выделения текстурированных областей. Нанесите его на изделие, а затем отполируйте области, которые вы не хотите затемнять. Вы также можете использовать пламя своего факела, чтобы сделать разноцветные узоры на меди. Или оставьте свою медь простой и дайте ей естественным образом развить прекрасную патину. Если вы хотите сохранить отделку меди в ее нынешнем виде, используйте воск Renaissance Wax для ее герметизации и защиты.
Убедитесь, что вы работаете в хорошо проветриваемом помещении и носите защитное снаряжение. Silver Black отлично подходит для выделения текстурированных областей. Нанесите его на изделие, а затем отполируйте области, которые вы не хотите затемнять. Вы также можете использовать пламя своего факела, чтобы сделать разноцветные узоры на меди. Или оставьте свою медь простой и дайте ей естественным образом развить прекрасную патину. Если вы хотите сохранить отделку меди в ее нынешнем виде, используйте воск Renaissance Wax для ее герметизации и защиты.
Медь с патиной Verdigris
Попробуйте смешать медь и латунь с другими металлами, такими как серебро и латунь, для получения интересных эффектов. Смешанные металлы сейчас очень популярны, и на то есть веские причины. Вы можете создать стиль стимпанк, особенно если используете холодные соединения. Вы также можете спаять металлы слоями, чтобы создать эффект 3D-эффекта. И, конечно же, вы можете текстурировать и патинировать эти слои, чтобы создать впечатляющие многокомпонентные изделия.
Подвеска из стерлингового серебра и меди
Хризаколл
Лазурит
Вы также можете установить камни в медь (помните медный безель?). Есть много камней, которые эффектно смотрятся с медью, например, бирюза, хризаколла и малахит, которые на самом деле получают свой цвет от меди. Лазурит — еще один камень, который потрясающе смотрится с медью. Медь оранжевого цвета и темно-синий лазурит располагаются напротив друг друга на цветовом круге , что создает очень динамичный эффект. Если вы хотите попробовать что-то действительно необычное, сочетайте медь с фиолетовыми камнями, такими как аметист и чароит. Медь также отлично смотрится с гранатами и черными камнями, например с ониксом. И, конечно же, все идет с прозрачным кварцем. Также попробуйте агаты и яшмы, чтобы придать им красивый, землистый вид.
Итак, добавьте в свою жизнь немного меди и отпразднуйте осень во всей ее яркой красоте!
Металлы, которые не ржавеют — и те, которые ржавеют
Вы, вероятно, знаете, что ржавчина — это шелушащаяся красноватая коррозия на металлических поверхностях. Термин «ржавчина» на самом деле относится к окислению железа — проще говоря, это комбинация железа и кислорода. Любой металл, содержащий железо, может ржаветь, в то время как другие металлы реагируют на кислород по-другому.
Термин «ржавчина» на самом деле относится к окислению железа — проще говоря, это комбинация железа и кислорода. Любой металл, содержащий железо, может ржаветь, в то время как другие металлы реагируют на кислород по-другому.
Ржавчина может разрушить металлические предметы и сделать их бесполезными, требуя дорогостоящей и трудоемкой замены. Самый простой способ избежать ржавчины — выбрать правильный металл.
Только железо может ржаветь. Это означает, что другие металлы, не содержащие железа, не подвержены коррозии. Это делает их идеальными для размещения на открытом воздухе, так как они прослужат гораздо дольше в естественных условиях. Узнайте, какие металлы не ржавеют, а какие ржавеют.
Какие металлы не ржавеют?
Ржавчина — это химическая реакция, поэтому для образования ржавчины должны быть задействованы правильные элементы. Ржавчина может возникнуть только при наличии молекул железа, кислорода и воды. Любая другая реакция по определению не является ржавчиной. Металлы с небольшим содержанием железа или без него, также известные как цветные металлы, не будут ржаветь, хотя они могут реагировать на кислород другими способами. Обычные металлы, которые не ржавеют, включают:
Металлы с небольшим содержанием железа или без него, также известные как цветные металлы, не будут ржаветь, хотя они могут реагировать на кислород другими способами. Обычные металлы, которые не ржавеют, включают:
Алюминий
Нержавеющая сталь
Бронза
Медь
9
9
Алюминий устойчив к коррозии. Причина этого проста — алюминий не содержит железа. Алюминий — самостоятельный элемент в периодической таблице, а это значит, что он не содержит ничего, кроме самого себя. Во время производства производитель может добавлять небольшое количество магния, кремния, меди или других элементов, чтобы сделать конечный продукт более прочным. Свойства алюминия делают его практичным выбором для наружных электрических шкафов или других металлических предметов на открытом воздухе.
Почему нержавеющая сталь не ржавеет?
Обычная сталь представляет собой комбинацию железа и углерода, а также небольшого количества других элементов. Нержавеющая сталь немного отличается. Хотя сталь содержит железо, нержавеющая сталь также содержит элемент хром, обладающий высокой коррозионной стойкостью.
Нержавеющая сталь немного отличается. Хотя сталь содержит железо, нержавеющая сталь также содержит элемент хром, обладающий высокой коррозионной стойкостью.
Хром защищает сталь от ржавчины, поскольку хром соединяется с кислородом раньше, чем железо. Поскольку железо никогда не соединяется с кислородом, ржавчина никогда не образуется. Кроме того, нержавеющая сталь популярна, потому что она противостоит росту бактерий и остается стабильной при экстремальных температурах.
Почему бронза не ржавеет?
Бронза не ржавеет благодаря минимальному содержанию железа. Имейте в виду, однако, что бронза может реагировать на кислород другими способами. Бронза не встречается в природе, как чистый алюминий или железо. Вместо этого бронза представляет собой смесь меди и олова. Эта композитная структура делает его более устойчивым к коррозии, но не полностью невосприимчивым. Он прочнее, чем сама по себе медь, но со временем может испортиться.
Почему медь не ржавеет?
Медь никогда не ржавеет по той же причине, что и бронза — в ней слишком мало железа. Хотя медь не ржавеет, со временем на ее поверхности может образовываться зеленая пленка или патина. Однако эта патина не будет отслаиваться, как ржавчина. Вместо этого он создает ровное толстое покрытие поверх самой меди. Многие люди на самом деле предпочитают внешний вид окисленной меди ее первоначальному состоянию.
Хотя медь не ржавеет, со временем на ее поверхности может образовываться зеленая пленка или патина. Однако эта патина не будет отслаиваться, как ржавчина. Вместо этого он создает ровное толстое покрытие поверх самой меди. Многие люди на самом деле предпочитают внешний вид окисленной меди ее первоначальному состоянию.
Только подумайте о Статуе Свободы. Ее медная кожа изначально выглядела коричневой, но со временем она стала зеленой из-за окисления меди. Эта зеленая пленка такая же толстая, как и исходный слой меди, и фактически помогает Lady Liberty противостоять атмосферным воздействиям. Вы также можете увидеть тот же эффект на старых пенни, которые могут начать выглядеть зелеными.
Металлы, которые ржавеют
Любой металл, содержащий значительное количество железа, также известный как «черные металлы», может ржаветь. Металлы, которые будут ржаветь, включают:
Сталь
Чугун
Кованое железо
Почему сталь ржавеет?
Поскольку сталь представляет собой смесь железа и углерода, она обязательно заржавеет. Что отличает сталь от нержавеющей стали, так это элемент хром — хром образует защитный экран от ржавчины, что делает нержавеющую сталь более устойчивой к коррозии. Чем больше содержание хрома, тем лучше. Обычная сталь не имеет такой защиты от коррозии.
Что отличает сталь от нержавеющей стали, так это элемент хром — хром образует защитный экран от ржавчины, что делает нержавеющую сталь более устойчивой к коррозии. Чем больше содержание хрома, тем лучше. Обычная сталь не имеет такой защиты от коррозии.
Почему чугун или кованое железо ржавеют?
Любая форма железа может ржаветь под воздействием кислорода и молекул воды. Чугун представляет собой комбинацию железа, углерода и кремния. Хотя он известен своей износостойкостью, он может ржаветь. С другой стороны, кованое железо содержит лишь следовые количества углерода. Это почти чистое железо, поэтому может образоваться ржавчина.
Железные предметы можно защитить от ржавчины, регулярно крася и удаляя пятна ржавчины проволочной щеткой. Вы также должны держать железные предметы как можно более сухими — протирайте чугунные кастрюли и сковородки полотенцем после мытья, а не дайте им высохнуть на воздухе. Кроме того, мойте их сразу, а не оставляйте их замачиваться. Железо требует гораздо большего внимания и обслуживания, чем другие металлы, когда речь идет о предотвращении коррозии.
Железо требует гораздо большего внимания и обслуживания, чем другие металлы, когда речь идет о предотвращении коррозии.
Практическое применение
Возможно, вы помните, как взрослый напоминал вам занести велосипед в гараж перед ливнем, иначе он промокнет и может заржаветь. Однако некоторые металлические предметы, такие как наружные электрические шкафы, должны постоянно оставаться снаружи. Металлические предметы, размещенные на открытом воздухе, должны выдерживать естественные условия, включая дождь и влажность.
Если бы эти предметы были восприимчивы к ржавчине, их пришлось бы заменять слишком часто. Это было бы дорого и отнимало много времени, но также представляло бы угрозу безопасности. Электрический корпус, разрушающийся из-за ржавчины, может быть очень опасным.
Для таких применений популярны алюминий и нержавеющая сталь. Алюминий не ржавеет, поэтому его можно безопасно использовать на открытом воздухе. Он также имеет другие ценные характеристики, такие как:
Он достаточно прочен, чтобы выдерживать сильные удары.

Может рассеивать тепло для безопасного контроля температуры.
Легкий по сравнению с другими металлами.
Как и алюминий, нержавеющая сталь часто используется для наружных металлических предметов. Нержавеющая сталь обладает впечатляющей температурной стабильностью. Он одновременно пожаробезопасен и устойчив к низким температурам. Если металлический предмет должен выдерживать экстремальные климатические условия — например, в пустыне, где температура может резко повышаться и понижаться за короткие промежутки времени, — нержавеющая сталь является одним из самых безопасных вариантов.
Узнайте больше о металлических корпусах для наружного применения
Корпуса APX предлагают корпуса, сертифицированные Национальной ассоциацией производителей электрооборудования (NEMA). Они созданы, чтобы противостоять любым условиям — дождю, снегу, льду, огню, грязи, пыли, бактериям и экстремальным температурам. Вы можете настроить корпус в соответствии с вашими потребностями. APX Enclosures предлагает электрические шкафы для самых разных отраслей, от гражданского строительства до телекоммуникаций.
APX Enclosures предлагает электрические шкафы для самых разных отраслей, от гражданского строительства до телекоммуникаций.
Узнайте, какие металлы лучше всего подходят для наружного применения. Если вам нужен прочный, устойчивый к коррозии и стабильный электрический корпус, свяжитесь с APX Enclosures уже сегодня.
Коррозия закладных материалов
Коррозия арматурной стали и других закладных металлов является основной причиной разрушения бетона. При коррозии стали образующаяся ржавчина занимает больший объем, чем сама сталь. Это расширение создает растягивающие напряжения в бетоне, что в конечном итоге может привести к растрескиванию, расслаиванию и отслаиванию.
Сталь подвергается коррозии, потому что это не природный материал. Скорее, железная руда плавится и очищается для производства стали. Производственные этапы, которые превращают железную руду в сталь, добавляют металлу энергии.
Сталь, как и большинство металлов, за исключением золота и платины, термодинамически нестабильна в нормальных атмосферных условиях, высвобождает энергию и возвращается в свое естественное состояние — оксид железа или ржавчину. Этот процесс называется коррозией.
Этот процесс называется коррозией.
Для возникновения коррозии должны присутствовать следующие элементы:
- Должно быть не менее двух металлов (или два места на одном металле) с разными уровнями энергии
- электролит
- металлическое соединение
В армированном бетоне арматурный стержень может иметь множество отдельных областей с разными энергетическими уровнями. Бетон действует как электролит, а металлическое соединение обеспечивается проволочными стяжками, опорами стульев или самой арматурой.
Коррозия представляет собой электрохимический процесс, связанный с потоком зарядов (электронов и ионов). На активных участках стержня, называемых анодами, атомы железа теряют электроны и перемещаются в окружающий бетон в виде ионов двухвалентного железа. Этот процесс называется реакцией полуэлементного окисления или анодной реакцией и представляется как:
2Fe → 2Fe 2+ + 4e —
Электроны остаются в стержне и направляются к участкам, называемым катодами, где они соединяются с водой и кислородом в бетоне. Реакция на катоде называется реакцией восстановления. Обычная реакция восстановления:
Реакция на катоде называется реакцией восстановления. Обычная реакция восстановления:
2H 2 O + O 2 + 4E — → 4OH —
333333333333023 гг. к этим катодным участкам, где они объединяются, образуя гидроксиды железа или ржавчину:
2Fe 2+ + 4OH — → 2Fe(OH)
Этот исходный осажденный гидроксид имеет тенденцию в дальнейшем реагировать с кислородом с образованием высших оксидов. Увеличение объема по мере дальнейшего взаимодействия продуктов реакции с растворенным кислородом приводит к внутреннему напряжению в бетоне, которого может быть достаточно, чтобы вызвать растрескивание и отслоение бетонного покрытия.
Коррозию залитых в бетон металлов можно значительно уменьшить, укладывая бетон без трещин с низкой проницаемостью и достаточным бетонным покрытием. Бетон с низкой проницаемостью может быть получен за счет уменьшения соотношения воды и вяжущих материалов в бетоне и использования пуццоланов и шлака. Пуццоланы и шлак также повышают удельное сопротивление бетона, тем самым снижая скорость коррозии даже после ее начала. АКИ 318-11, 9Требования строительных норм и правил 0024 к конструкционному бетону содержит минимальные требования к бетонному покрытию, которые помогут защитить встроенные металлы от коррозионно-активных материалов. Дополнительные меры по снижению коррозии стальной арматуры в бетоне включают применение антикоррозионных добавок, покрытие арматуры (например, эпоксидной смолой), нанесение герметиков и мембран на поверхность бетона. Герметики и мембраны, если они используются, необходимо периодически наносить повторно.
Пуццоланы и шлак также повышают удельное сопротивление бетона, тем самым снижая скорость коррозии даже после ее начала. АКИ 318-11, 9Требования строительных норм и правил 0024 к конструкционному бетону содержит минимальные требования к бетонному покрытию, которые помогут защитить встроенные металлы от коррозионно-активных материалов. Дополнительные меры по снижению коррозии стальной арматуры в бетоне включают применение антикоррозионных добавок, покрытие арматуры (например, эпоксидной смолой), нанесение герметиков и мембран на поверхность бетона. Герметики и мембраны, если они используются, необходимо периодически наносить повторно.
Бетон и пассивный слой
Хотя сталь имеет естественную склонность к коррозии, щелочная среда бетона (pH от 12 до 13) обеспечивает защиту стали от коррозии. При высоком pH на стали образуется тонкий оксидный слой, препятствующий растворению атомов металла. Эта пассивная пленка на самом деле не останавливает коррозию; снижает скорость коррозии до незначительного уровня. Для стали в бетоне скорость пассивной коррозии обычно составляет 0,1 мкм в год. Без пассивной пленки скорость коррозии стали бы как минимум в 1000 раз выше (ACI222 2001).
Для стали в бетоне скорость пассивной коррозии обычно составляет 0,1 мкм в год. Без пассивной пленки скорость коррозии стали бы как минимум в 1000 раз выше (ACI222 2001).
Благодаря присущей бетону защите, арматурная сталь не подвергается коррозии в большинстве бетонных элементов и конструкций. Однако при разрушении пассивного слоя может возникнуть коррозия. Разрушение пассивного слоя происходит при снижении щелочности бетона или при повышении концентрации хлоридов в бетоне до определенного уровня.
Роль ионов хлора
Воздействие ионов хлора на железобетон является основной причиной преждевременной коррозии стальной арматуры. Проникновение ионов хлора, присутствующих в солях против обледенения и морской воде, в железобетон может вызвать коррозию стали, если кислород и влага также доступны для поддержания реакции. Растворенные в воде хлориды могут проникать сквозь прочный бетон или достигать стали через трещины. Хлорсодержащие примеси также могут вызывать коррозию.
Никакой другой загрязнитель не упоминается в литературе так широко, как причина коррозии металлов в бетоне, чем ионы хлорида. Механизм, с помощью которого хлориды вызывают коррозию, не совсем понятен, но наиболее популярная теория состоит в том, что ионы хлорида проникают через защитную оксидную пленку легче, чем другие ионы, делая сталь уязвимой для коррозии.
Риск коррозии возрастает по мере увеличения содержания хлоридов в бетоне. Когда содержание хлоридов на поверхности стали превышает определенный предел, называемый пороговым значением, возникает коррозия, если также доступны вода и кислород. Исследования Федерального управления автомобильных дорог (FHWA) показали, что пороговое значение в 0,20 процента общего (кислоторастворимого) хлорида от веса цемента может вызвать коррозию арматурной стали в мостовых настилах (Clear 19).76). Однако только водорастворимые хлориды способствуют коррозии; некоторые растворимые в кислоте хлориды могут быть связаны внутри агрегатов и, следовательно, не могут способствовать коррозии. Работа в FHWA (Clear 1973) показала, что коэффициент преобразования кислоторастворимых хлоридов в водорастворимые может варьироваться от 0,35 до 0,90, в зависимости от компонентов и истории бетона. Произвольно было выбрано значение 0,75, в результате чего предел водорастворимых хлоридов составил 0,15 процента от массы цемента.
Работа в FHWA (Clear 1973) показала, что коэффициент преобразования кислоторастворимых хлоридов в водорастворимые может варьироваться от 0,35 до 0,90, в зависимости от компонентов и истории бетона. Произвольно было выбрано значение 0,75, в результате чего предел водорастворимых хлоридов составил 0,15 процента от массы цемента.
Хотя хлориды напрямую ответственны за инициирование коррозии, они, по-видимому, играют лишь косвенную роль в скорости коррозии после ее инициирования. Основными факторами, контролирующими скорость, являются наличие кислорода, удельное электрическое сопротивление и относительная влажность бетона, а также pH и температура.
Карбонизация
Карбонизация происходит, когда углекислый газ из воздуха проникает в бетон и реагирует с гидроксидами, такими как гидроксид кальция, с образованием карбонатов. В реакции с гидроксидом кальция образуется карбонат кальция:
Ca(OH) 2 + CO 2 → CaCO 3 + H 2 O
Эта реакция снижает pH пористого раствора до уровня 8,5, при котором пассивная пленка на стали не стабильно.
Карбонизация обычно является медленным процессом. Было подсчитано, что в высококачественном бетоне карбонизация будет происходить со скоростью до 0,04 дюйма в год. Количество карбонизации значительно увеличивается в бетоне с высоким водоцементным отношением, низким содержанием цемента, коротким периодом отверждения, низкой прочностью и высокопроницаемой или пористой массой.
Карбонизация сильно зависит от относительной влажности бетона. Самые высокие показатели карбонизации возникают, когда относительная влажность поддерживается в пределах от 50 до 75 процентов. Ниже 25 процентов относительной влажности степень карбонизации считается незначительной. При относительной влажности выше 75 процентов влага в порах ограничивает проникновение CO2. Коррозия, вызванная карбонизацией, часто возникает на участках фасадов зданий, которые подвергаются воздействию осадков, затенены от солнечного света и имеют низкое бетонное покрытие поверх арматурной стали.
Карбонизация бетона также снижает количество ионов хлора, необходимых для ускорения коррозии. В новом бетоне с pH от 12 до 13 требуется от 7000 до 8000 частей на миллион хлоридов, чтобы начать коррозию закладной стали. Однако, если pH снижается до диапазона от 10 до 11, пороговое значение хлоридов для коррозии значительно ниже — на уровне 100 частей на миллион или ниже. Однако, как и ионы хлора, карбонизация разрушает пассивную пленку арматуры, но не влияет на скорость коррозии.
В новом бетоне с pH от 12 до 13 требуется от 7000 до 8000 частей на миллион хлоридов, чтобы начать коррозию закладной стали. Однако, если pH снижается до диапазона от 10 до 11, пороговое значение хлоридов для коррозии значительно ниже — на уровне 100 частей на миллион или ниже. Однако, как и ионы хлора, карбонизация разрушает пассивную пленку арматуры, но не влияет на скорость коррозии.
Пример карбонизации фасада здания.
Коррозия разнородных металлов
Когда два разных металла, таких как алюминий и сталь, соприкасаются внутри бетона, может возникнуть коррозия, поскольку каждый металл имеет уникальный электрохимический потенциал. Знакомый тип коррозии разнородных металлов происходит в обычной батарейке для фонарика. Цинковый корпус и угольный стержень представляют собой два металла, а влажная паста действует как электролит. Когда углерод и цинк соединены проводом, течет ток. В железобетоне коррозия разнородных металлов может возникать на балконах, где встроенные алюминиевые перила соприкасаются с арматурной сталью. Ниже приведен список металлов в порядке электрохимической активности:
Ниже приведен список металлов в порядке электрохимической активности:
1. Цинк 5. Никель 9. Медная
2. Алюминий 6. Олово 10. Бронзовая
3. Сталь 7. Стенд 11. Недоверной сталь
4. Железо 8. Латунь 12. Золото
Когда металлы соприкасаются в активном электролите, коррозирует менее активный металл (меньший номер) в ряду.
Каталожные номера
Комитет МСА 222, Защита металлов в бетоне от коррозии , ACI 222R-01, Американский институт бетона, Фармингтон-Хиллз, Мичиган, 2001 г., 41 страница.
Комитет ACI 318, Требования строительных норм и правил к конструкционному бетону , ACI 318-05, Американский институт бетона, Фармингтон-Хиллз, Мичиган, 2005 г., 443 страницы.
Клир, К.С., и Хэй, Р.Э., «Время до коррозии арматурной стали в бетонной плите, т. 1: влияние параметров состава и конструкции смеси», FHWA-RD-73-32, Федеральное управление автомобильных дорог, Вашингтон , округ Колумбия, 19 апреля73, 103 страницы.
Clear KC, «Время до коррозии арматурной стали в бетонных плитах», Федеральное управление автомобильных дорог, PB 258 446, Vol. 3, апрель 1976 г.
PCA, Типы и причины разрушения бетона, Ассоциация портландцемента, Скоки, Иллинойс, 2002 г., 16 страниц.
Почему латунь обесцвечивается на воздухе?
Нам всем нравится видеть красивую латунную посуду, сияющие талии для пуджи и изысканные предметы декора, украшающие наш дом. Но уход за антиквариатом и сохранение его красоты иногда может стать проблемой. Например, вспомните, когда вы впервые заметили, что ваше любимое латунное кашпо или латунный сосуд теряют свой естественный цвет и блеск. Изменение цвета латуни является обычным явлением, но каковы основные причины этого? Давайте обсудим это в сегодняшней записи блога.
Что вызывает обесцвечивание латуни?
Латунь — это сплав, который обычно состоит из 33% цинка и 67% меди. Если вы долго держите свои латунные изделия на открытом воздухе, медь, присутствующая в сплаве (первоначально тускло-золотисто-желтая), через некоторое время может стать слегка зеленой или коричнево-зеленой. Зеленый оттенок известен как медь-медь, а коричневато-зеленое окисление часто называют патиной.
Зеленый оттенок известен как медь-медь, а коричневато-зеленое окисление часто называют патиной.
Существует множество причин, по которым ваше изделие может изменить цвет из-за воздействия влаги или даже после длительного использования в течение десятилетий. Читайте вперед, чтобы узнать больше!
Отсутствие очистки изделий из латуни
Неправильная очистка изделий из латуни часто является частой причиной обесцвечивания поверхности. Защита латуни от пыли и влаги является обязательным условием, и существует так много способов сделать это. Например, вы можете использовать зубную щетку для регулярной аккуратной чистки мелких и более деликатных предметов, чтобы избежать скопления пыли.
Если вы выполняете влажную уборку, обязательно используйте мягкие моющие средства для мытья посуды или натуральные моющие средства, такие как мякоть тамаринда. Тщательно удалите все мыло и остатки при очистке и хорошо высушите, желательно на ярком солнце.
Статуя Вишну из латуни
Если на вашем старинном или старинном латунном изделии есть признаки коррозии, лучше обратиться к опытному консерватору. Если ваш объект имеет уникальную отделку и поверхность, только профессионал знает, какие чистящие средства лучше всего использовать, сохраняя при этом естественную патину.
Потертости или вмятины
Хрупкие латунные предметы с мелкими деталями можно легко повредить при грубом обращении, что приведет к вмятинам или потертостям. Латунь Изменение цвета частый результат накопления влаги и грязи в крошечных трещинах латуни. Поэтому деликатное обращение и чистка необходимы для сохранения долговечности и блеска вашего антиквариата.
Активная коррозия
Если вы заметили зеленые порошкообразные пятна, быстро распространяющиеся по предмету из латуни или бронзы, это называется активной коррозией или болезнью бронзы. Восковые или ярко-зеленые пятна также являются символами активной коррозии. Эти области часто являются слабыми местами на деталях и могут легко сломаться / треснуть или отколоться, если не использовать их с осторожностью.
Эти области часто являются слабыми местами на деталях и могут легко сломаться / треснуть или отколоться, если не использовать их с осторожностью.
Изменение цвета латуни в основном происходит из-за присутствия соли в воздухе. Однако иногда это также происходит из-за неправильной чистки или обращения с предметом. Это состояние активной коррозии еще больше усугубляется высокой влажностью, грязью и пылью, поскольку они удерживают влагу на поверхности латуни.
Поэтому очень важно обращаться с ними деликатно и следить за тем, чтобы область была высушена, а предмет хранился вдали от влаги.
Безопасное обесцвечивание или окисление
Безопасное обесцвечивание или окисление латуни на предмете из латуни выглядит темно-коричневым или красновато-коричневым, и его можно увидеть на совершенно чистом и сухом предмете. Такое окисление полезно для изделия и действует как защитный барьер. Черноватая или коричневатая коррозия часто наблюдается на меди и возникает, когда объект подвергается воздействию воздуха. Его можно безопасно удалить с помощью мякоти тамаринда или мягких моющих средств.
Его можно безопасно удалить с помощью мякоти тамаринда или мягких моющих средств.
Медная Панчапатра с Утрани
Патина — это то же самое, что оксидирование?
Патиной называют старение некоторых металлов, дерева и даже изделий из кожи. Это форма окисления, которая происходит естественным образом после того, как вы использовали предмет в течение многих лет, и объект подвергается воздействию изменения климата. Патина возникает в результате выветривания, окисления или того и другого и изменяет внешний вид ваших латунных материалов.
Латунная ложка Teertha
Как только ваш продукт вступает в контакт с такими атмосферными факторами, как ветер, лед, вода, резкое повышение или понижение температуры, начинается процесс окисления.
В конечном итоге это приводит к образованию патины – потускнения на поверхности латуни. В дополнение ко всему этому, патина также является результатом старения, износа или даже полировки. Весь процесс называется патинированием.
Вы можете задаться вопросом безопасно ли использовать кастрюли или посуду из патинированной латуни? Ответ будет ДА, если процесс патинирования естественен и начинается со слабого латунного обесцвечивания и затемняется с годами. Тем не менее, если ваш предмет имеет заметное значение для семейных традиций или наследства, вы должны быть осторожны, чтобы устранить ущерб и предотвратить его дальнейшее ухудшение.
Цените свои антикварные изделия из латуни на всю жизнь!
Очарование предметов из латуни поистине непревзойденно! Хотя изменение цвета латуни является обычным явлением после нескольких лет использования красивых кухонных принадлежностей или предметов первой необходимости для пуджи , , вы можете сохранить их красоту и сияние с помощью простых советов по очистке и уходу, упомянутых в нашем блоге.
Мы надеемся, что это руководство помогло вам сохранить семейный антиквариат с большой любовью и заботой.
