Латунь защита от коррозии: Латунь. Серия «Материалы в коммунальном хозяйстве», часть 1 || ГЕРЦ
Содержание
Латунь. Серия «Материалы в коммунальном хозяйстве», часть 1 || ГЕРЦ
В нашей новой серии «Материалы для оборудования коммунальных систем» мы представляем Вам один из наиболее распространенных материалов — латунь. Этот очень древний материал, который, по достоверным источникам, был известен уже за 3000 лет до нашей эры, и сегодня является наиболее распространённым в технике материалом.
Латунь обладает многими преимуществами:
— высокими прочностными характеристиками;
— хорошей коррозионной стойкостью;
— хорошими свойствами для механической обработки;
— возможностью нанесения гальванических покрытий;
— хорошей пластической деформацией.
Повторное использование без потери качества
Старые изделия из латуни после использования и после переплавки перерабатываются в новые латунные изделия. Это относится и к стружке, полученной в процессе обработки. При этом не происходит потери качества даже при многократных процессах переработки. Помимо своей долговечности латунь отвечает требованиям стабильности свойств.
Помимо своей долговечности латунь отвечает требованиям стабильности свойств.
Сплавы для различных областей применения
Латунь — это сплав, получаемый из меди (Cu) и цинка (Zn), таким образом, химический символ и точное техническое обозначение этого материала CuZn.
| Медь | не менее 50% |
| Цинк | до 44%, сплав с содержанием цинка до 30% называется томпак. В необработанном виде его распознают по красному цвету поверхности и «латунного» цвета обрезной кромке |
| Свинец | до 3%, улучшает обрабатываемость резанием |
| Никель | (нейзильбер) улучшает прочностные свойства и коррозионную стойкость |
| Алюминий | улучшает прочность, способность работать на скольжение, а также коррозионную стойкость |
| Марганец | улучшает коррозионную стойкость и прочность |
| Олово | образует поверхностный слой, предохраняющий от коррозии, улучшает прочность и способность работать на скольжение |
| Мышьяк | 0,1-0,2% добавка служит в качестве ингибитора, препятствующего выщелачиванию цинка |
Помимо меди и цинка к легирующим добавкам относятся свинец и мышьяк.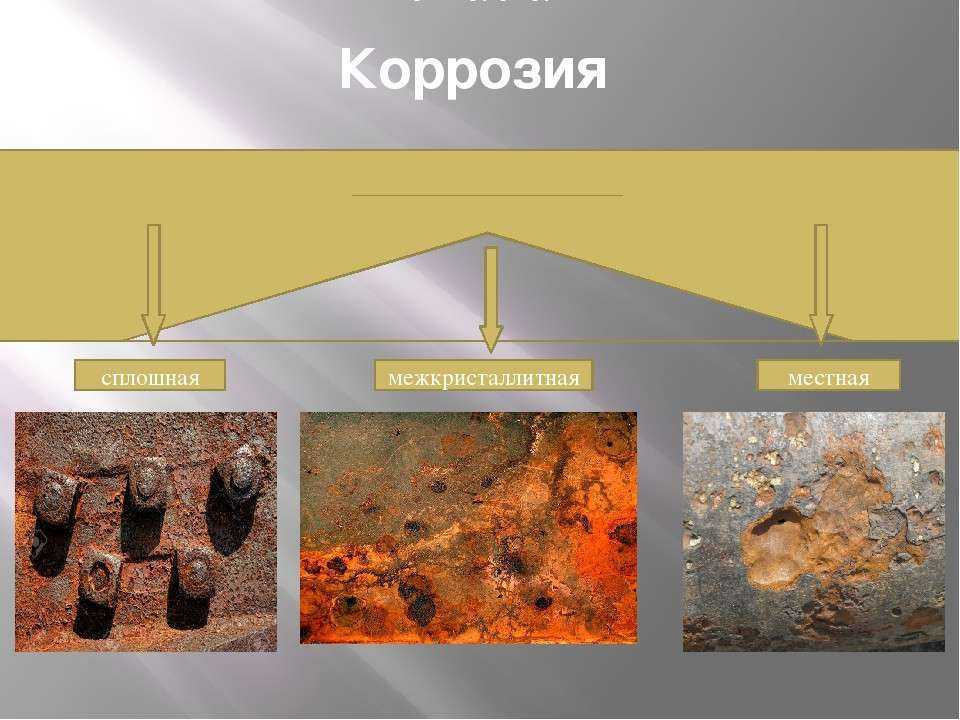 Их процентное содержание слегка варьируется, так как в сплавах могут содержаться и другие обязательные добавочные элементы. Бывает, что доля дополнительного элемента составляет более 1%, или он оказывает особое влияние на свойства сплава.
Их процентное содержание слегка варьируется, так как в сплавах могут содержаться и другие обязательные добавочные элементы. Бывает, что доля дополнительного элемента составляет более 1%, или он оказывает особое влияние на свойства сплава.
Латунь, устойчивая к выщелачиванию цинка, для хозяйственно-питьевого водоснабжения
Выщелачивание цинка – это избирательная коррозия медно-цинковых сплавов, или латуней с содержанием цинка более 20%. Предпосылкой этого процесса является повышенное содержание хлоридов (например, в морской воде, но возможно и во внутреннем санитарно-техническом оборудовании зданий), как правило, в мягкой воде.
В этом случае рекомендуется использование конструктивных элементов из устойчивой к выщелачиванию цинка латуни. Выщелачивание цинка можно эффективно предупредить уже на стадии проектирования питьевого водоснабжения. Базой для этого является подбор используемых материалов на основании анализа воды.
DR-латунь (dezincification resistant) является альтернативой известной стандартной латуни в случаях критического состояния воды. В отопительных системах эти обстоятельства не важны. Правильно спроектированная и обслуживаемая отопительная система практически не содержит кислорода, и благодаря этому коррозионные процессы не наблюдаются.
Считается, что латунь, устойчивая к выщелачиванию цинка, обладает хорошей устойчивостью к органическим веществам и нейтральным или щелочным соединениям. Обрабатываемость резанием и формуемость у DR-латуней похожи, способность к пайке (твердой и мягкой) такая же, как и у других латунных сплавов. При несоблюдении режима пайки, например, при слишком продолжительном времени пайки, структура может пострадать.
Вся трубопроводная арматура ГЕРЦ изготовлена из DR-латуни.
Дополнительно выпускается арматура ГЕРЦ для питьевого водоснабжения с гигиенически безопасными уплотнениями, соответствующая требованиям закона о качестве и гигиене продуктов питания.
Многочисленные факторы, такие как минимальные осаждения, трещины и поры в облицовке и недостаточный доступ кислорода способствуют выщелачиванию цинка. Одной добавки ингибиторов в расплав латуни недостаточно, чтобы исключить выщелачивание цинка. Только комбинация состава материала, определенного метода изготовления и термообработки гарантируют стойкость к выщелачиванию цинка, что подтверждает успешное прохождение тестирований ISO. Выщелачивание цинка появляется в виде поверхностной коррозии или локально ограниченного образования продуктов коррозии в виде наростов. Вначале медь и цинк переходят в раствор, и более благородная медь осаждается на поверхности, образуя губчатый пористый осадок. Проще говоря, при выщелачивании цинка медь и цинк растворяются. Структура металла становится пористой. Губчатые медные наросты, не содержащие цинка, нестойкие, неплотные и, как следствие, быстро разрушаются. Цинк остается в растворе или осаждается в виде солей на поверхности. Относительная форма сохраняется, однако прочность быстро снижается. Выщелачивание цинка продвигается очень быстро, и вскоре проникает вглубь материала. Это может привести к быстрому разрушению материала.
Выщелачивание цинка продвигается очень быстро, и вскоре проникает вглубь материала. Это может привести к быстрому разрушению материала.
Пример композиции типичного латунного сплава, применяемого в системах питьевого водоснабжения с 2003 г. иллюстрирует жесткие требования металлургии (Постановление о качестве питьевой воды, DIN 50930 часть 6):
| Легирующие добавки | в % |
| Медь | 61,5-64,5 |
| Цинк | остальное |
| Свинец | 1,5-2,2 |
| Мышьяк | 0,15 |
| Алюминий | 0,3-0,7 |
| Железо | 0,3 |
| Марганец | 0,15 |
| Никель | 0,25 |
| Олово | 0,4 |
Помимо меди, цинка и свинца этот сплав содержит также мышьяк (As). Благодаря добавке мышьяка в качестве ингибитора, а также вследствие особой технологии и термообработки получается структура материала, устойчивая к выщелачиванию цинка. Хотя содержание мышьяка всего лишь 0,1…0,2%, оно всегда указывается, так как его влияние на свойства латуни значительно.
Хотя содержание мышьяка всего лишь 0,1…0,2%, оно всегда указывается, так как его влияние на свойства латуни значительно.
Формы коррозии
В нормальных условиях латунь обладает хорошей коррозионной стойкостью в воде и в воздухе. Однако, при определенных обстоятельствах, помимо уже упомянутого выщелачивания цинка, могут встречаться и другие формы коррозии.
Коррозия из-за внутренних напряжений
У многих материалов, как, впрочем, и у готовых деталей из латуни, иногда наблюдаются трещины, которые могут привести к разрушению данных изделий. Этот вид коррозии, обусловленный механическими напряжениями в материалах, называется коррозией из-за внутренних напряжений, которая у латуни почти исключительно вызвана присутствием аммиака или его соединений в воде или водяном паре.
Чтобы избежать коррозии из-за внутренних напряжений, необходимо устранить напряжение растяжения материала, которое может возникнуть в результате термообработки. Поэтому необходимо, насколько это возможно, использовать материалы, свободные от внутренних напряжений. Другой хорошей защитой от коррозии под напряжением является исключение контакта с агрессивными средами. Часто инициирующим фактором является насыщенная аммиаком атмосфера. В сельском хозяйстве (на фермах) часто возникает атмосфера с присутствием аммиака.
Другой хорошей защитой от коррозии под напряжением является исключение контакта с агрессивными средами. Часто инициирующим фактором является насыщенная аммиаком атмосфера. В сельском хозяйстве (на фермах) часто возникает атмосфера с присутствием аммиака.
Латунь в сфере коммунального хозяйства, напротив, широко распространена и не создаёт никаких проблем. Латунь, как и другие материалы, необходимо транспортировать и хранить в сухом состоянии.
Питтинговая коррозия имеет вид точечных отверстий, диаметр которых меньше их глубины, и образуется при нарушении защитного слоя меди.
Контактная коррозия
Сплавы меди и цинка обладают относительно инертным равновесным потенциалом, то есть, эти сплавы редко коррозируют. Неблагородные металлы, вступающие в контакт с латунью, подвергаются коррозии в местах контакта, где затем может осаждаться электролитическая медь.
Опубликовано журнал HERZ NEWS, выпуск февраль 2007
Как протекает коррозия меди в воде, щелочи, кислоте.
 Меры защиты.
Меры защиты.
Содержание
- 1 Коррозийные свойства
- 2 Влияние воды
- 3 Влияние кислоты и щелочи
- 4 Нахождение в почве и влажном воздухе
Коррозия меди не так известна как коррозийные воздействия на железо. Однако механизмы воздействия на структуру металла схожи. Это спонтанное разрушение при воздействии различного типа агрессивных сред. Однозначно сравнивать понятие ржавчина с коррозией меди нельзя. Коррозия любого металла связана с термодинамической неустойчивостью при влиянии активных элементов, которые находятся в воздухе. Скорость коррозии меди непосредственно будет зависеть от температурных колебаний. Если увеличить ее на 100 градусов, то темп возрастает в 2-3 раза. Далее рассмотрим, как протекает коррозия медных сплавов и как защитить их от окисления в различных средах размещения.
Содержание
- Коррозийные свойства
- Влияние воды
- Влияние кислоты и щелочи
- Нахождение в почве и влажном воздухе
Коррозийные свойства
В связи с отсутствием у меди химической активности, при контакте с водой, влажным воздухом ее коррозия практически не возникает. Находясь в сухом воздухе, у металла может образовываться небольшая оксидная пленка толщиной до 50 нм. Если изделие лужено, то пленка почти не образовывается. Качественное покрытие из олова способно надежно защитить от влаги, перепадов температуры. При этом продолжительность эксплуатации такого предмета может составлять до 100 лет без потери первоначальных свойств. С течением времени цвет не будет изменяться. Применение луженных поверхностей давно показало себя с лучшей стороны. Примером могут стать купола множества храмов.
Находясь в сухом воздухе, у металла может образовываться небольшая оксидная пленка толщиной до 50 нм. Если изделие лужено, то пленка почти не образовывается. Качественное покрытие из олова способно надежно защитить от влаги, перепадов температуры. При этом продолжительность эксплуатации такого предмета может составлять до 100 лет без потери первоначальных свойств. С течением времени цвет не будет изменяться. Применение луженных поверхностей давно показало себя с лучшей стороны. Примером могут стать купола множества храмов.
В связи с высоким порогом коррозийной стойкости медь активно применяется во многих химических и электрохимических производствах. К примеру, процесс обмеднения металла помогает решить множество задач при обработке. В одной из прошлых статей, мы рассматривали процедуру в домашних условиях, рекомендуем ознакомиться.
Влияние воды
Коррозия меди в воде и скорость протекания процесса будет зависеть от наличия оксидной пленки и объема растворенного в ней кислорода. Как правило, протекает ударный или точечный процесс. При этом скорость будет тем быстрее, чем большее количество кислорода содержится в воде. Также негативно будет влиять жидкость с содержанием ионов хлора и низким уровнем pH.
Как правило, протекает ударный или точечный процесс. При этом скорость будет тем быстрее, чем большее количество кислорода содержится в воде. Также негативно будет влиять жидкость с содержанием ионов хлора и низким уровнем pH.
В общем сопротивление поверхности коррозийным воздействиям достаточно высоко, чему способствует наличие оксидной пленки, не позволяющая разрушающим элементом проникать в структуру металла. Слой оксида будет возникать при нахождении металла более 2 месяцев постоянного пребывания в воде. Оксидное покрытие может быть двух типов:
- · Карбонат – зеленого оттенка. Принято считать наиболее прочным.
- · Сульфат – темного цвета. Обладает рыхлой структурой и меньшей прочностью.
Металл часто используется при производстве различных трубопроводов. Однако, если протекающая по ним жидкость имеет контакт с алюминием, цинком, железом, то она значительно ускоряет их коррозию. Чтобы это предотвратить и защитить медь от коррозии опять же проводится лужение оловом.
Влияние кислоты и щелочи
Коррозия меди в кислых средах менее выявлена. Наиболее сильным будет влияние азотной и серной кислоты. Если поместить в концентрат этих кислот, то она способна полностью растворяться. Эти особенности учитывают, выбирая сплавы, для элементов и трубопроводов в нефтегазовой промышленности.
В щелочной среде эффект вообще не наблюдается, так как щелочь позволяет восстановиться меди с 2-валентного до 1-валентного состояния. При этом стоит вспомнить, что она сама является щелочным металлом.
Защита от окисления и коррозии при влиянии кислот осуществляется ингибиторами – веществами, замедляющими химическую реакцию. Можно выделить следующие типы:
- · Экранирующий – формируют защитные плетки и исключают возможность контакта с кислотами.
- · Окислительный – происходит образование оксида, вступающего в реакции с кислотами, тем самым препятствуя их проникновению к структуре металла.
- · Катодный – предназначен для повышения перенапряжения катодов раствора благодаря чему химические реакции снижают свою интенсивность.

Как правило, коррозию меди в кислых средах предотвращают экранирующим типом ингибиторов. Наиболее распространен бензотриазол, который совместно с соляными образованиями меди формирует защитную оболочку, замедляя скорость коррозии или практически полностью ее прекращая.
Нахождение в почве и влажном воздухе
Коррозия меди в почве, в основном, вызывается влиянием кислот, которые содержатся в грунте. Если сравнить с воздействием воды, то кислород в грунте значительно меньше окисляет металлические элементы. К наиболее опасным в почве относятся микроорганизмы, вернее, их выделения. Зачастую они способны выделять сероводород, разрушающий металл. Так, медь длительно пролежавшая в почве способна полностью разложиться.
Во влажном воздухе процесс протекает не стремительно. Необходимо длительное время. В сухом климате можно вообще не наблюдать разрушительных влияний. Объясняется это тем, что во влажном воздухе высока концентрация углекислого газа, сульфидов, хлоридов, вызывающих коррозию и разрушительных для защитной пленки.
Длительное пребывание на влажном воздухе способно вызывать образование слоя патины. Так называется зеленый налет на меди. Она представляет собой оксиды солей, которые на начальном этапе темно-коричневого цвета, а затем поверхность начинает зеленеть. Особенностью патины является то, что ее невозможно растворить в воде и на нее не действует повышенная влажность воздуха. Она имеет нейтральные свойства к самой меди, что позволяет ей защищать поверхность от пагубного влияния окружающей среды. Кроме этого современные методы создания искусственной патины позволяют ее использовать в предметах искусства и при реставрации.
Посмотрите личный опыт борьбы с коррозийными очагами с помощью ингибиторов.
Взаимодействие оцинкованных покрытий с другими металлами
Когда два разнородных металла вступают в контакт, и присутствует электролит, такой как влага, то возникает вероятность биметаллической коррозии у более электроотрицательного или анодного металла, как определено в электрохимическом ряду, который корродирует в первую очередь, предотвращая коррозию другого металла.
Биметаллический эффект является основой для защиты, которую цинковое покрытие (горячее цинкование) обеспечивает для малых зон незащищённой стали, если покрытие повреждено. Цинковые покрытия корродируют в первую очередь, защищая металл, который ниже его в электрохимическом ряду. Степень биметаллической коррозии будет зависеть от числа таких факторов, как контактируют металлы, соотношение площадей контактирующих металлов и условий эксплуатации. Как правило уровень биметаллической коррозии будет увеличиваться с увеличением разницы потенциалов между двумя металлами, например, как далеко расположены друг от друга два металла в гальваническом ряду напряжений. Однако потенциал может изменяться вследствие образования оксидного слоя и не может быть использован для определения степени возникновения биметаллической коррозии, так как другие факторы, которые приведены ниже, также важны. Соотношение площадей контактирующих металлов имеет существенное значение, и в идеале соотношение металлов анод-катод должно быть высоким. Если соотношение уменьшается, то могут возникнуть проблемы вследствие высокого уровня восстановления кислорода, которое может привести к увеличению коррозии анодного металла. Воздействующие условия имеют большое значение, т.к. для биметаллической коррозии электролит должен связать два имеющихся металла. В результате, в сухой окружающей среде (внутри помещения) вероятность биметаллической коррозии очень низкая, в то время как во внешних атмосферных условиях вероятность увеличивается, вследствие наличия влаги в виде дождя и конденсации. Наиболее худшими условиями является погружение в раствор, где электролит постоянно соединяет два металла. Обычно любая возможность биметаллической коррозии может быть ослаблена электрической изоляцией двух металлов друг от друга. Для болтовых соединения могут быть обеспечены при использовании неопреновых или пластиковых шайб, в то время как для перекрытых поверхностей это может быть достигнуто использованием пластиковых прокладок или окрашиванием одной из поверхностей подходящей системы лакокрасочного покрытия.
Если соотношение уменьшается, то могут возникнуть проблемы вследствие высокого уровня восстановления кислорода, которое может привести к увеличению коррозии анодного металла. Воздействующие условия имеют большое значение, т.к. для биметаллической коррозии электролит должен связать два имеющихся металла. В результате, в сухой окружающей среде (внутри помещения) вероятность биметаллической коррозии очень низкая, в то время как во внешних атмосферных условиях вероятность увеличивается, вследствие наличия влаги в виде дождя и конденсации. Наиболее худшими условиями является погружение в раствор, где электролит постоянно соединяет два металла. Обычно любая возможность биметаллической коррозии может быть ослаблена электрической изоляцией двух металлов друг от друга. Для болтовых соединения могут быть обеспечены при использовании неопреновых или пластиковых шайб, в то время как для перекрытых поверхностей это может быть достигнуто использованием пластиковых прокладок или окрашиванием одной из поверхностей подходящей системы лакокрасочного покрытия. Обычно горячеоцинованная сталь хорошо функционирует в контакте с наиболее распространенными конструкционными металлами, когда в атмосферных условиях, обеспечивается высокое отношение площадей оцинкованной стали к другому металлу. И наоборот, в условиях погружения эффект биметаллической коррозии существенно увеличивается, и обычно требуется изоляция.
Обычно горячеоцинованная сталь хорошо функционирует в контакте с наиболее распространенными конструкционными металлами, когда в атмосферных условиях, обеспечивается высокое отношение площадей оцинкованной стали к другому металлу. И наоборот, в условиях погружения эффект биметаллической коррозии существенно увеличивается, и обычно требуется изоляция.
Медь и латунь
Если установка требует, чтобы контакт между гальванизированными материалами и медью или латунью в сырой или влажной окружающей среде, может произойти быстрая коррозия цинка. Даже сточные воды могут содержать достаточное количество растворенной меди, чтобы вызвать быструю коррозию.
Если использование меди или латуни в контакте с гальванизированными покрытиями неизбежно, должны быть приняты меры предосторожности, чтобы предотвратить электрический контакт между этими двумя металлами. Поверхность разъема должна быть изолирована непроводящими прокладками; соединения должны быть выполнены с изолирующим крепежом и уплотняющей втулкой. Это должно гарантировать, что вода повторно не распространиться и потоки воды от гальванизированной поверхности к медной или латунной не реверсирует.
Это должно гарантировать, что вода повторно не распространиться и потоки воды от гальванизированной поверхности к медной или латунной не реверсирует.
Алюминиевая и нержавеющая сталь
В умеренных атмосферных условиях умеренной влажности, контакт между оцинкованной поверхностью и алюминия или нержавеющей стали, вряд ли вызовет существенную инкрементную коррозию. Тем не менее, при очень влажных условиях, оцинкованной поверхности может потребоваться электрическая изоляция от алюминия или нержавеющей стали.
Нержавеющая сталь
Когда гальванизированные болты используются на нержавеющей стали, цинк первоначально жертвует собой, пока защитный слой ржавчины не разовьется на нержавеющей стали. Как только этот слой ржавчины разовьется, он формирует слой изоляции, который предотвращает дальнейшую защиту цинка. Цинковое покрытие должно быть достаточно толстым, чтобы продлить защиту от ржавчины в течение несколько лет. У гальванизированных болтов выполненных горячим методом хватает цинкового покрытия, чтобы продлить защиту с минимальной потерей в эксплуатации покрытия.
Металл Воздействие атмосферы Погруженное состояние
Сельская местность Промышленные/городские районы Прибрежная зона Пресная вода Морская вода
Аллюминий а а-б а-б б б-в
Латунь б б а-в б-в в-г
Бронза б б б-в б-в в-г
Литейный чугун б б б-в б-в в-г
Медь б б-в б-в б-в в-г
Свинец а а-в а-б а-в а-в
Нержавеющая сталь а-б а-б а-б б б-в
a — Цинковое покрытие будет испытывать или дополнительную коррозию, или только незначительную. дополни- тельную коррозию, которая обычно допускается при эксплуатации.
Б — Цинковое покрытие будет испытывать незначительную или умеренную дополнительную коррозию, которая может быть допустимой в некоторых случаях эксплуатации.
В — Цинковое покрытие будет испытывать сильную дополнительную коррозию, необходимы защитные меры.
Г — Цинковое покрытие будет испытывать сильную дополнительную коррозию, контакта рекомендуется избегать.
Руководство, связанное с конкретным применением, касающимся оцинкованных стальных изделий в контакте с указанным металлом или сплавом.
а) Алюминий – Вероятность увеличения биметаллической коррозии вследствие атмосферного кон- такта с алюминием относительно низкая. Применение оцинкованной стали и алюминия, используемые в сочетании друг с другом, является плакирование алюминием. В этом случае рекомендуется изоляция вследствие большой площади поверхности алюминиевых пластин.
б) Медь – Вследствие большого потенциала, установившегося при контакте между сталью с цинковым покрытием, и медью и медьсодержащими сплавами, рекомендуется применение электроизоляции (даже в атмосферных условиях). При конструировании рекомендуется избегать стока воды с меди на оцинкованные изделия, так как малые количества меди, растворенной в воде, могут откладываться на изделии, что приведет к биметаллической коррозии.
в) Свинец – Вероятность биметаллической коррозии со свинцом в атмосферной среде низкая и нет информации о проблемах, касающихся, например, применения свинцовой гидроизоляции оцинкованных изделий и использование свинца в опорах с цинковым покрытием.
г) Нержавеющая сталь – Применение нержавеющей стали с оцинкованной сталью используется в виде гаек и болтов в атмосферных условиях. Учитывая низкий потенциал для биметаллической коррозии и малую площадь поверхности крепежных изделий из нержавеющей стали, биметаллическая коррозия обычно отсутствует, практика показывает необходимость сохранения изоляции, используя изолирующие шайбы. Практический опыт показывает, что там, где отношение площади поверхности цинка к площади другого металла большое, и указана категория «а» или «а – б», дополнительная коррозия как результат контакта будет незначительной или будет отсутствовать. Если соотношение площадей поверхностей уменьшено или выше, может потребоваться изоляция.
Коррозия металлов в кислотах
Коррозия металла в кислотах – это его разрушение при взаимодействии с концентрированными или разведенными кислотами. Часто такие разрушения встречаются на химических производствах и других сферах деятельности человека. Слабые кислотные растворы могут создавать даже некоторые продукты питания, и непокрытый металл, соприкасающийся с ними, будет коррозировать. То, как себя поведет металлический предмет при контакте с кислотой, зависит от его способности пассивироваться. Процесс коррозии металлов в кислотах проходит с выделением водорода.
Слабые кислотные растворы могут создавать даже некоторые продукты питания, и непокрытый металл, соприкасающийся с ними, будет коррозировать. То, как себя поведет металлический предмет при контакте с кислотой, зависит от его способности пассивироваться. Процесс коррозии металлов в кислотах проходит с выделением водорода.
Рассмотрим более подробно случаи коррозии металла в кислотах разного происхождения.
Коррозия металлов в соляной кислоте
Соляная кислота является очень агрессивной по отношению к металлам. В большей степени это обуславливается содержанием в ней ионов Cl—. Даже коррозионно-стойкие стали подвергаются разрушению, когда концентрация кислоты выше среднего. Если же раствор достаточно сильно разбавлен, такие стали коррозии не подвергаются.
Коррозия никеля в серной кислоте не протекает даже в случаях, когда достигается температура кипения. В присутствии трехвалентного железа, хлоридов, других окислителей никель и его сплавы начинают разрушаться.
Низколегированная аустенитная сталь при комнатной температуре и концентрации соляной кислоты в 0,2 – 1% подвергается коррозии со скоростью 24 г/(м2•сут).
Коррозия металлов в органических кислотах
Самой сильной среди органических кислот является уксусная. В яблочной, бензойной, пикриновой, олеиновой, винной, стеариновой кислотах даже при больших температурах (выше 100°С) коррозионно-стойкие стали отличаются высокой устойчивостью. При контакте металлов с муравьиной кислотой образуются питтинги (особенно при увеличении температуры). Глубина их даже больше, чем в уксусной кислоте.
В органических кислотах высокой устойчивостью обладает алюминий, т.к. на его поверхности присутствует защитная пленка труднорастворимых окислов.
Щавелевая, себациновая, лимонная и молочная кислоты вызывают коррозию сталей только при больших концентрациях. В них устойчивы хромистые стали с добавками молибдена.
Коррозия металлов в азотной кислоте
Азотная кислота обладает агрессивным воздействием по отношению ко многим металлам. Малоуглеродистые стали не обладают достаточной устойчивостью в растворах азотной кислоты. Кроме того, при повышении концентрации HNO3 до 35 – 40% (при данных концентрациях сталь переходит в пассивное состояние) коррозия малоуглеродистых сталей в азотной кислоте увеличивается. При концентрации азотной кислоты близкой к 100% пассивное состояние нарушается. Азотная кислота является окислителем. При коррозии железа катодными деполяризаторами являются молекулы азотной кислоты и нитрат-ионы. Устойчивость в азотной кислоте хромистых сталей повышается, если в их состав вводить никель и молибден. Коррозионное разрушение сталей в азотной кислоте происходит по границам зерен. На алюминий слабое влияние оказывают пары азотной кислоты или растворы с концентрацией более 80%. При нормальной температуре алюминий обладает высокой коррозионной стойкостью в азотной кислоте. Скорость коррозии алюминия в азотной кислоте возрастает при постоянном перемешивании и присутствии в растворе хлорид-ионов.
Малоуглеродистые стали не обладают достаточной устойчивостью в растворах азотной кислоты. Кроме того, при повышении концентрации HNO3 до 35 – 40% (при данных концентрациях сталь переходит в пассивное состояние) коррозия малоуглеродистых сталей в азотной кислоте увеличивается. При концентрации азотной кислоты близкой к 100% пассивное состояние нарушается. Азотная кислота является окислителем. При коррозии железа катодными деполяризаторами являются молекулы азотной кислоты и нитрат-ионы. Устойчивость в азотной кислоте хромистых сталей повышается, если в их состав вводить никель и молибден. Коррозионное разрушение сталей в азотной кислоте происходит по границам зерен. На алюминий слабое влияние оказывают пары азотной кислоты или растворы с концентрацией более 80%. При нормальной температуре алюминий обладает высокой коррозионной стойкостью в азотной кислоте. Скорость коррозии алюминия в азотной кислоте возрастает при постоянном перемешивании и присутствии в растворе хлорид-ионов.
Коррозия металлов в серной кислоте
При концентрации серной кислоты около 50 – 55% поверхность железа переходит в пассивное состояние. Далее с повышением температуры и концентрации серной кислоты поверхность железа становится активной (наблюдается коррозия железа в серной кислоте).
В растворах серной кислоты, как и в других кислотах, на скорость коррозии железа большое влияние оказывает природа анионов. Это связано с торможением катодного и анодного процессов и их адсорбцией на поверхности металла.
Я.М. Колотыркин развил представления, что на анодное растворение железа оказывают влияние анионы. Это связано с образование комплекса:
Fe + H2O ↔ Fe(OH—)адс. + H+;
Fe(OH—)адс ↔ Fe(OH)адс + e—;
Fe(OH)адс + HSO4— →FeSO4 + H2O + e—;
Fe(OH)адс + SO42- → FeSO4 + OH— + e—;
FeSO4 = Fe2+ + SO42-.
Из вышеперечисленных уравнений понятно, что скорость анодного процесса возрастает с увеличением концентрации ионов HSO4— и SO42-. С поверхности железа сульфат ионы вытесняются хлорид ионами, но до определенной концентрации ионов хлора, скорость протекания анодного процесса замедляется.
В 95 – 98% серной кислоте при нормальной температуре хорошей устойчивостью обладают хромистые стали (с содержанием хрома около 17%) с небольшой добавкой молибдена или без него. В таких условиях (при большой концентрации серной кислоты) стоек также алюминий и углеродистые стали. Чистый алюминий (99,5%) более устойчив в серной кислоте, чем его сплавы, в состав которых не входит медь. Скорость коррозии алюминия в серной кислоте (и его сплавов) при повышении температуры с 20°С до 98°С увеличивается с 8 до 24 г/(м2•сут). Коррозионно-стойкие стали в 5-ти или 20-% растворе при температуре кипения серной кислоты устойчивы только в присутствии ингибиторов коррозии.![]()
При обычной температуре в серной кислоте коррозия меди практически не наблюдается. А при повышении температуры до 100°С процесс разрушения интенсифицируется. В 25% растворе серной кислоты, повышенном давлении и температуре близкой к 200°С медь быстро разрушается.
Латунь не обладает коррозионной стойкостью в растворах серной кислоты любых концентраций даже при комнатной температуре. Устойчивость латуней к разрушению в серной кислоте можно только повысить введением в раствор 30% соли CuSO4•5H2O.
Коррозия металлов в фосфорной кислоте
Наибольшей стойкостью к коррозии в фосфорной кислоте отличаются молибденовые стали. Алюминий и его сплавы (в состав которых не входит медь, магний) устойчивы в фосфорной кислоте. При обычной температуре не поддаются также разрушениям хромоникелевые аустенитные стали (в растворах фосфорной кислоты любой концентрации). В концентрированной технической фосфорной кислоте при температуре не выше 50°С стойки малоуглеродистые стали. Если сталь с 17% хрома поместить в раствор фосфорной кислоты, концентрацией от 1 до 10%, то она будет обладать высокой устойчивостью даже при температуре кипения.
Если сталь с 17% хрома поместить в раствор фосфорной кислоты, концентрацией от 1 до 10%, то она будет обладать высокой устойчивостью даже при температуре кипения.
Медь практически не подвергается коррозии в фосфорной кислоте при температуре от 20 до 95°С. Но если в систему вводить окислитель и повышать температуру – скорость коррозии меди в фосфорной кислоте значительно увеличивается. Бронзы и латуни в фосфорной кислоте ведут себя аналогично.
Коррозия металлов во фтористоводородной кислоте
Чугун, малоуглеродистая сталь и железо во фтористоводородной кислоте быстро разрушаются. В 10-% фтористоводородной кислоте при нормальной температуре обладают хорошей устойчивостью хромистые стали (с содержанием хрома 17%). В 20-% кислоте при температуре до 50°С устойчивы аустенитные высоколегированные стали. Латуни не разрушаются в 40-60-% фтористоводородной кислоте при 20°С. Магниевые сплавы устойчивы при температурах до 65°С в 45-% растворе.
Почему латунь, бронза и медь зеленеют?
Возможно, у вас есть украшения из этих металлов, и вы заметили, что через некоторое время на них появляется зеленоватый налет, или что они могут окрашивать вашу кожу в зеленый цвет. А может быть, вы слышали, что Статуя Свободы сделана из меди и изначально была медного красно-коричнего цвета, но почему тогда сейчас она полностью зеленая? Ответ на этот вопрос довольно интересен.
А может быть, вы слышали, что Статуя Свободы сделана из меди и изначально была медного красно-коричнего цвета, но почему тогда сейчас она полностью зеленая? Ответ на этот вопрос довольно интересен.
Латунь и бронза содержат медь. Когда медь вступает в реакцию с кислородом, она окисляется и образует зеленовато-голубой слой, который защищает металл от дальнейшей коррозии. Любой металл, содержащий большое количество меди, может позеленеть.
Сколько времени требуется меди, чтобы позеленеть? Это очень относительно. В очень сухих условиях медь может зеленеть до 20 лет! Она также меняет цвет поэтапно. Сначала медь становится тусклой. Затем коричневой, затем темно-коричневой и, наконец, начнет зеленеть. С парами аммиака это может произойти всего за несколько часов.
На самом деле, этот зеленый слой имеет ряд преимуществ, и его часто намеренно оставляют.
Почему латунь, бронза и медь становятся зелеными
Проще говоря, наиболее распространенный оксид меди имеет зеленый цвет (да, есть несколько разных видов!).
Оксид меди — это что-то вроде «ржавчины», хотя ржавчина — это слово, которое используется для определения оксида железа. Это означает, что если нет железа, то нет и ржавчины. Но и то, и другое — это типы оксидов.
Когда вы видите зеленый слой на этих металлах, обычно его называют патиной, это значит, что произошла химическая реакции. Медь вступила в реакцию с кислородом, водой и углекислым газом в атмосфере.
Латунь — это сплав, который обычно состоит из 67% меди и 33% цинка. Бронза состоит из 88% меди и 12% олова.
Оба эти металла имеют очень высокое содержание меди, поэтому при окислении на них образуется одинаковый налет.
Для чего подходит оксид меди
Отделка патиной на самом деле довольно популярна для таких вещей, как латунные дверные ручки, медная кровля и другие виды декоративных изделий. Но помимо косметических, есть и практические причины, по которым вам может понадобиться такая отделка.
Во-первых, это добавляет защитный слой к металлу.
Оксид меди — интересное вещество. Он очень хорошо прилипает к основному металлу и довольно долговечен. Чем толще слой оксида меди, тем дольше металл сопротивляется дальнейшей коррозии.
Это совсем не похоже на оксид железа, который отслаивается, обнажая новый слой металла, который затем ржавеет, отслаивается и т.д. В результате ржавчина со временем может разъедать целые конструкции.
Вот что делает оксид меди таким крутым. Это окисление, которое предотвращает дальнейшее окисление.
Один из примеров — Статуя Свободы, построенная в 1886 году. Спустя более 130 лет воздействия стихий толщина слоя оксида меди составляет всего 0,005 дюйма! Это примерно толщина двух листов бумаги.
Для чего не подходит оксид меди
Есть много ситуаций, когда вам не нужен этот налет.
Например, вы, вероятно, не хотите, чтобы ваша кожа позеленела, если вы носите украшения с медью. Или вы просто предпочитаете яркий вид меди вместо тусклого зеленоватого цвета патины.
Оксид меди также не проводит электричество. Поскольку медь является популярным материалом для таких вещей, как провода и электрические соединения, окисление меди может стать настоящей головной болью.
Поскольку медь является популярным материалом для таких вещей, как провода и электрические соединения, окисление меди может стать настоящей головной болью.
Как сделать медь зеленой
Итак, медь (и металлы с большим содержанием меди) со временем зеленеет сама по себе под воздействием воздуха и воды. Но что если вы хотите ускорить этот процесс?
Вот один из способов быстрее покрыть патиной небольшие кусочки меди:
Прежде всего, тщательно очистите металл обезжиривателем. Любые масла в конечном итоге защитят металл от окисления и позеленения.
Наполните герметичную стеклянную банку на 1/4 объема нашатырным спиртом.
Подвесьте медь на нитке и банке прямо над аммиаком. Закройте банку. Пары аммиака создадут тонкую патину в течение нескольких часов. Если вы хотите получить более толстый патины, оставьте ее на более длительное время.
Чистка — очень важный этап, если вы хотите сделать все правильно с первого раза. Если медь не будет идеально чистой, патина не будет равномерной. Однако это не является серьезной проблемой, поскольку вы можете просто очистить медь и повторить процесс.
Однако это не является серьезной проблемой, поскольку вы можете просто очистить медь и повторить процесс.
Совет профессионала: Делайте это в хорошо проветриваемом помещении. Аммиак — довольно вредная штука.
Как удалить оксид меди
На самом деле его очень легко удалить, и для этого существует целый ряд способов.
Например, если вы пытаетесь удалить зеленый оксид с монет, вы можете просто замочить их на ночь в кислоте.
Кроме того, простая чистка и скрабирование помогут избавиться от патины. Существует также несколько чистящих средств (обычно содержащих кислоту), предназначенных специально для чистки медьсодержащих металлов. Вы также можете просто использовать абразивный диск, если медь имеет матовую поверхность.
Для очистки электрических соединений обычно используют проволочную щетку и сильное кислотное средство для очистки меди, которое быстро справляется с проблемой.
Оксид меди на самом деле очень опасен для посуды. Он токсичен, и нужно избегать его попадания в пищу. Медная посуда довольно популярна и за ней нужно регулярно ухаживать. Поскольку она обычно полированная, вам понадобятся специальные средства для чистки.
Медная посуда довольно популярна и за ней нужно регулярно ухаживать. Поскольку она обычно полированная, вам понадобятся специальные средства для чистки.
Если проблема заключается в небольшом потускнении, а не в зеленом окисле, использование бытовых кислот, таких как лимонный сок, и губки обычно удаляет проблемные участки без особых проблем. Неплохо было бы после этого отполировать медь ингибитором, поскольку кислоты могут вытравить металл и сделать его склонным к окислению в будущем.
Как предотвратить образование оксида меди
Самый простой способ предотвратить позеленение меди, латуни и бронзы — просто регулярно чистить их. При средних условиях для образования патины может потребоваться несколько недель.
Тем не менее, уход за изделием — это хлопотное дело. Поэтому, если вы не хотите помнить о необходимости чистить медь, есть несколько альтернатив.
Варианты с прозрачным покрытием наиболее популярны для таких изделий, как фурнитура и ювелирные украшения. Существуют сотни продуктов, предназначенных для защиты от потускнения или образования патины, чтобы медь выглядела блестящей.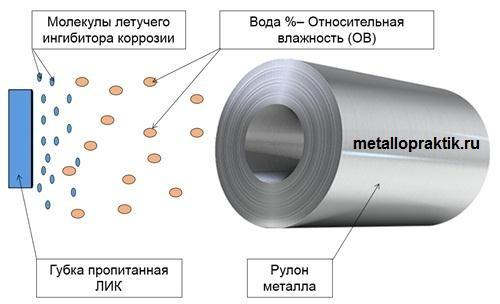
Прозрачный лак для ногтей также хорошо подходит для защиты меди. Этот способ более популярен для таких вещей, как ювелирные изделия.
Очень старомодный способ сохранения меди — полировка пчелиным воском, он очень хорошо защищает металл от влаги и кислорода.
Советуем вам прочитать статьи опубликованные в нашем блоге ранее: «Область применения и интересные факты о меди» и «Как резать лазером медь и другие светоотражающие металлы?».
Если вам понравилась статья, то ставьте лайк, делитесь ею со своими друзьями и оставляйте комментарии!
Статья о защите металлов — Химик
18 декабря 2019
Необходимость защиты металлов от коррозии возникла вместе с появлением первых металлических изделий.
В случае с металлами, говоря об их коррозии, имеют ввиду нежелательный процесс взаимодействия металла со средой. Физико-химическая сущность изменений, которые претерпевает металл при коррозии, является окисление металла.
По механизму процесса различают химическую и электрохимическую коррозию металла.
Химическая коррозия – это разрушение металла окислением его в окружающей среде без возникновения электрического тока в системе. Большой вред наносит разновидность химической коррозии — газовая коррозия. Металл реагирует с определенными газами, содержащимися в воздухе — кислородом, диоксидом углерода, диоксидом серы или сероводородом, образуя на поверхности металла оксид. Когда металл коррозирует, на его поверхности появляются маленькие углубления, и прочность металла уменьшается.
Наибольший вред наносит электрохимическая коррозия. В этом случае наряду с химическими процессами происходят и электрические процессы. Электрохимическую коррозию вызывают главным образом примеси других металлов и неметаллических веществ или неоднородность поверхности. Согласно теории электрохимической коррозии, в этих случаях при контакте металла с электролитом (электролитом может быть влага, адсорбированная из воздуха) на его поверхности возникают гальванические микроэлементы. При этом металл с более отрицательным потенциалом разрушается. Его ионы переходят в раствор, а электроны переходят к менее активному металлу. На скорость коррозии влияет и характер электролита. Чем выше его кислотность (то есть меньше pH), тем быстрее происходит коррозия. Также коррозия растет при повышении температуры.
При этом металл с более отрицательным потенциалом разрушается. Его ионы переходят в раствор, а электроны переходят к менее активному металлу. На скорость коррозии влияет и характер электролита. Чем выше его кислотность (то есть меньше pH), тем быстрее происходит коррозия. Также коррозия растет при повышении температуры.
Ещё в древние времена для защиты меди применялось горячее лужение, растительные масла, коррозионностойкие сплавы (оловянная бронза, латунь), для защиты железных и стальных изделий — полирование, воронение, лужение.
Основные методы антикоррозионной защиты
В начале 19 века был открыт электрохимический метод антикоррозионной защиты с помощью протекторов. В середине 19 в. была установлена принципиальная возможность получения металлических покрытий электролитическим способом. Наиболее интенсивно антикоррозионная защита развивается в связи с изобретением нержавеющих сталей, новых коррозионностойких сплавов, полимерных покрытий и др.
Система антикоррозионной защиты определяется условиями эксплуатации и механизмом коррозии металлов (электрохимическим или химическим). Все методы антикоррозионной защиты можно разделить на 2 основные группы: электрохимические, оказывающие влияние на потенциал металла и механические, изолирующие металл от воздействия окружающей среды созданием защитной плёнки и покрытий.
Все методы антикоррозионной защиты можно разделить на 2 основные группы: электрохимические, оказывающие влияние на потенциал металла и механические, изолирующие металл от воздействия окружающей среды созданием защитной плёнки и покрытий.
Применение различных методов защиты металлов от коррозии позволяет в какой-то степени свести к минимуму потери металла от коррозии.
Электрохимические методы защиты применяют для предотвращения коррозии морских судов, подземных и гидротехнических сооружений, а также химической аппаратуры, работающей с агрессивными электропроводными средами. Путём катодной или анодной поляризации от постороннего источника тока или присоединением к защищаемой конструкции протекторов потенциал металла смещается до значений, при которых сильно замедляется или полностью прекращается его коррозия.
Антикоррозионные защитные покрытия
Для антикоррозионной защиты широко применяют защитные покрытия. Они делятся на металлические (чистые металлы и их сплавы) и неметаллические. В зависимости от потенциала металла покрытия могут быть анодными и катодными по отношению к защитному металлу.
В зависимости от потенциала металла покрытия могут быть анодными и катодными по отношению к защитному металлу.
Неметаллические защитные покрытия — лакокрасочные, пластмассовые, каучуковые.
Всё больше распространяются пластмассовые покрытия из полиэтилена, полиизобутилена, фторопласта, найлона, поливинилхлорида и др., обладающих высокой водо-, кислото- и щёлочестойкостью. Многие пластмассы используют как футеровочный материал для химических аппаратов и гальванических ванн (винипласт, фаолит и др.). Для защиты деталей радиоаппаратуры служат заливочные полимерные компаунды. Эффективно защищают от действия кислот и др. реагентов покрытия на основе каучука (гуммирование).
Лакокрасочные покрытия имеют ряд преимуществ по сравнению с другими видами защитных покрытий:
- простота нанесения;
- возможность получения покрытия любого цвета;
- возможность обработки металлоконструкций больших габаритов и сложной конфигурации;
- экономичность по сравнению с другими видами защитных покрытий
- высокие защитные свойства;
- возможность восстановления в процессе эксплуатации.

Наиболее часто антикоррозионная защита заключается в нанесении на поверхность защищаемых конструкций слоев защитных покрытий на основе органических и неорганических материалов, в частности, лакокрасочных материалов.
Антикоррозионное защитное покрытие должно соответствовать следующим требованиям:
- повышать сопротивляемость конструкции внешнему вредному воздействию;
- должно подбираться с учетом специфики защищаемого материала;
- должно обеспечивать изоляцию материала от негативной среды.
Выбор антикоррозионного покрытия и схемы антикоррозионной защиты металла (включая марку ЛКМ, количество наносимых слоёв и общую толщину покрытия) осуществляется с учётом характеристики среды эксплуатации металлической конструкции, а также с учётом условий при нанесении антикоррозионного покрытия.
Лакокрасочные материалы для антикоррозионной защиты металлоконструкций
Существуют различные антикоррозийные материалы и покрытия, применение которых зависит от агрессивности окружающей среды и особенностей эксплуатации.
Одними из наиболее распространенных лакокрасочных материалов используемых для антикоррозионной защиты металлоконструкций являются материалы на основе эпоксидных смол.
Практически всегда эпоксидные лакокрасочные материалы двухупаковочные. Основой эпоксидных лакокрасочных материалов служат эпоксидные смолы, которые представляют собой линейные простые полиэфиры, молекулярные цепи которых имеют реакционно-способные эпоксидные группы на обеих концах и вторичные гидроксильные группы, расположенные вдоль всей цепи.
Образование пространственных полимеров (отверждение смол) происходит в результате сшивки линейных молекул при взаимодействии их с органическими азотосодержащими соединениями (отвердителями). В процессе реакции происходит отверждение смолы и превращение ее в нерастворимое, неплавкое соединение трехмерного строения без выделения побочных продуктов реакции, поэтому почти не происходит усадки покрытия.
Перспективные разработки — лакокрасочные материалы без растворителей
Одним из наиболее перспективных лакокрасочных материалов являются материалы, не содержащие растворителей. Их получают на основе жидких эпоксидных смол. Для снижения вязкости в них вводят активные разбавители, которые придают лакокрасочному материалу малярные свойства без использования летучих растворителей. Особенно важно использовать лакокрасочные материалы без растворителей при окрашивании различных цистерн и других замкнутых объемов. Это позволяет резко снизить токсичность, пожаро- и взрывоопасность окрашивания.
Их получают на основе жидких эпоксидных смол. Для снижения вязкости в них вводят активные разбавители, которые придают лакокрасочному материалу малярные свойства без использования летучих растворителей. Особенно важно использовать лакокрасочные материалы без растворителей при окрашивании различных цистерн и других замкнутых объемов. Это позволяет резко снизить токсичность, пожаро- и взрывоопасность окрашивания.
Эпоксидные материалы для наружной и внутренней защиты магистральных трубопроводов
Основное достоинство покрытий на основе эпоксидных смол — сочетание хороших физико-механических и электроизоляционных свойств. Покрытия на основе эпоксидных смол обладают хорошей адгезией к металлу, дереву и другим материалам, высокой твердостью и химической стойкостью, отличной водостойкостью; они устойчивы к воздействию нефти и нефтепродуктов и многих растворителей.
Хорошая стойкость к щелочам и кислотам, алифатическим и ароматическим углеводородам, маслам, топливу, воде позволяют использовать эпоксидные материалы для наружной и внутренней защиты магистральных трубопроводов. Используя их можно получить покрытия с одинаково хорошей твердостью, эластичностью и ударной прочностью.
Используя их можно получить покрытия с одинаково хорошей твердостью, эластичностью и ударной прочностью.
Поэтому антикоррозионные покрытия на основе эпоксидных смол с каждым годом становятся всё более востребованными в самых разных отраслях промышленности.
Испытания на коррозию
доказывают, что латунь свободной резки превосходит сталь с покрытием
Скачать PDF [677 KB]
- Введение
- Покрытия
- Программа испытаний CDA
- Результаты испытаний
- Резюме
- Ссылки
Введение
Изделия для винтовых станков, изготовленные из латуни Free Cutting, UNS C36000, могут быть значительно дешевле, чем идентичные детали, изготовленные из освинцованной стали AISI типа 12L14. Это возможно по трем причинам:
- Латунная стружка является ценным товаром, и автоматические винтовые станки обычно производят больше стружки, чем деталей по весу;
- можно обрабатывать намного быстрее, чем из свинцовистой стали (теоретически почти в пять раз быстрее), что приводит к значительному снижению производственных затрат;
- Изделия для латунных винтовых машин не требуют дорогостоящего гальванического покрытия для защиты от коррозии или сохранения их полезности или внешнего вида.

Детали из латуни
Детали из латуни могут стоить дешевле независимо от того, является ли фактором гальваническое покрытие; однако в последние годы экологические проблемы значительно повысили стоимость гальванического покрытия, и латунь становится все более выгодной, чем когда-либо прежде.
Коррозионная стойкость, безусловно, является важным фактором для компонентов автомобильных винтовых машин. Несмотря на воздействие коррозионных условий, детали должны продолжать функционировать, резьба и фитинги должны правильно подходить, а образ качества должен поддерживаться. Действительно ли естественная коррозионная стойкость латуни достаточна для длительного воздействия потенциально коррозионной среды под капотом? И если да, то как характеристики латуни соотносятся с изделиями из стали с обычным покрытием?
Эти вопросы были рассмотрены в ходе серии ускоренных испытаний на коррозию, проведенных для Ассоциации развития меди (CDA) Центром коррозионных технологий LaQue, Райтсвилл-Бич, Северная Каролина. Типичные изделия автомобильных винтовых машин из латуни и плакированной стали в Центре подвергались ускоренным коррозионным испытаниям. В данной публикации описаны результаты этих испытаний.
Типичные изделия автомобильных винтовых машин из латуни и плакированной стали в Центре подвергались ускоренным коррозионным испытаниям. В данной публикации описаны результаты этих испытаний.
Наверх
Покрытия
Наиболее распространенной системой покрытия автомобильных компонентов является гальваническое цинкование, состоящее из слоя чистого цинка средней толщиной около 0,00015 дюйма (0,004 мм). Покрытие обычно тоньше в углублениях, на резьбе и т. д. Цинк обладает достаточно хорошей атмосферной коррозионной стойкостью, но при толщине, используемой в деталях автомобильных винтовых машин, он выполняет не более чем косметическую функцию. Например, в сильно загрязненной промышленной атмосфере даже толстые гальванизированные покрытия толщиной 2 унции/фут2 (61,0 г/м2), 1,7 мил (0,04 мм) начинают ржаветь через 4 года, и они могут быть на 80% проржавевшими за 1 год. 0 лет. В аналогичных условиях тонкое гальванопокрытие на автомобильных компонентах прослужило бы менее одного года.
Для продления срока годности цинковые гальванические пластины обычно защищают хроматными конверсионными покрытиями, которые можно определить по цвету: от прозрачного до голубоватого или бледно-желтого для очень тонких покрытий; соломенно-желтый, зеленый, оливково-зеленый и коричневый для более толстых слоев.
Среди других популярных покрытий для изделий винтовых машин – электрофоретически наносимые полимеры (ЭКоатс), те или иные патентованные обработки и легированные гальванические покрытия. E-покрытия успешно использовались на панелях кузова в течение многих лет, и недавно было показано, что они обеспечивают 10-летнюю защиту от коррозии медных и латунных радиаторов.
Один автопроизводитель выпускает спецификацию на запатентованное покрытие JS-500, название которого предполагает, что оно способно выдерживать 500 часов при стандартном испытании в солевом тумане. Также были опробованы цинк-железо, цинк-кобальт и другие нетрадиционные покрытия. Их общей целью является обеспечение приемлемой степени защиты от коррозии при минимальных затратах.
Покрытия и коррозия
Независимо от того, какой процесс используется, важно понимать, что все покрытия имеют:
- конечной толщины, которая может быть или не быть одинаковой;
- несовершенства, которые у пластинщиков называют «праздниками», и ограниченный срок службы.
Когда покрытие на основе цинка разрушается и обнажается основной металл, гальваническое воздействие защищает небольшие открытые участки в течение ограниченного периода времени. Когда цинк израсходован, общая коррозия может продолжаться свободно.
Продукты коррозии цинка включают оксид, гидроксиды, карбонаты и другие соли. По отдельности или в смеси с оксидами и гидроксидами железа (ржавчина) они образуют объемистую массу, которая может мешать работе резьбы и муфты. По крайней мере, они склонны удерживать влагу и выглядят неприглядно.
Коррозионное поведение латуни
Латунь
не требует дополнительной защиты от коррозии, поскольку она по своей природе устойчива к агрессивным средам. Хотя латунь может быть менее устойчива к коррозии, чем другие медные сплавы, ее характеристики вполне соответствуют условиям, возникающим при применении под капотом.
Хотя латунь может быть менее устойчива к коррозии, чем другие медные сплавы, ее характеристики вполне соответствуют условиям, возникающим при применении под капотом.
Латунь тускнеет. На воздухе быстро образует коричневую или серо-зеленую защитную пленку продукта коррозии. Скорость образования пленки (скорость коррозии) вскоре уменьшается, поскольку кислород удаляется с поверхности металла.
При определенных условиях латунь также может обесцинковываться (терять цинковую составляющую своего состава). Децинкификация связана с погружением или застойными условиями воздействия, часто в кислых средах. При атмосферном воздействии эта форма коррозии обычно ограничивается поверхностным воздействием.
Наверх
Программа испытаний CDA
Наиболее важными коррозионными компонентами автомобильной среды являются хлориды, которые появляются в морской атмосфере и в дорожных брызгах, содержащих растворенные противогололедные соли. Таким образом, программа испытаний CDA основывалась на хлоридных средах. Испытания были разработаны для моделирования режимов воздействия как тумана, так и брызг. Поскольку не существует стандартного метода испытаний, специально предназначенного для проверки подкапотных условий, программа CDA использовала или адаптировала другие стандартные методы, которые разумно имитировали коррозионную среду, за исключением того, что условия были достаточно жесткими, чтобы получить результаты за относительно короткое время.
Испытания были разработаны для моделирования режимов воздействия как тумана, так и брызг. Поскольку не существует стандартного метода испытаний, специально предназначенного для проверки подкапотных условий, программа CDA использовала или адаптировала другие стандартные методы, которые разумно имитировали коррозионную среду, за исключением того, что условия были достаточно жесткими, чтобы получить результаты за относительно короткое время.
Тестовые материалы
Форма изделия часто влияет на его коррозионные свойства. Такие детали, как острые углы, углубления и резьба, подвержены коррозии раньше и быстрее, чем плоские поверхности, либо из-за того, что они задерживают воду, либо из-за того, что на них не нанесено достаточно толстое защитное покрытие. Очевидно, что разнообразие форм, представленных обычными изделиями винтовых машин, включает в себя большое количество потенциальных участков коррозии. Таким образом, вместо того, чтобы определить один образец для представления этой ситуации, в программе испытаний CDA использовались настоящие фитинги, сальниковые гайки и соединители шлангов, используемые в автомобилях текущего производства.
На рисунках 1 и 2 показан выбор винтовых машин из латуни и стали с покрытием в том виде, в каком они выглядели до воздействия соляного тумана. Стальные детали, показанные на фиг. 2a , 2b и 2c , соответственно, включают цилиндрическую часть с электрофорезным покрытием; примеры покрытий из чистого цинка, цинка плюс желтый (толстый) хромат и цинк плюс синий (тонкий) хромат; и две детали, покрытые системой General Motors JS-500. Некоторые детали из латуни показаны до и после сборки.
| Рисунок l . Выбор латунных винтовых деталей машин в том виде, в котором они были получены. | ||
НАЖМИТЕ НА ЛЮБОЕ ИЗОБРАЖЕНИЕ, ЧТОБЫ УВЕЛИЧИТЬ ИЗОБРАЖЕНИЕ
и . Электронное пальто Электронное пальто | б. Слева — 0,00015 дюйма Zn + дихромат синего Центр — 0,00015 дюйма Zn + желтый дихромат Справа — 0,00015 дюйма Zn пластина | с . Система JS-500 |
| Рисунок 2 . Выбор деталей шнековых машин из стали с покрытием. | ||
Для альтернативных испытаний погружением колючие латунные фитинги шланга были закрыты прозрачными виниловыми трубками для проверки наличия признаков щелевой коррозии.
Солевой спрей
Воздействие соляного тумана, знакомый ускоренный метод испытаний, обычно проводят в соответствии с ASTM B 117.2 В соответствии с этой стандартной процедурой образцы подвешивают в закрытом шкафу, где они подвергаются воздействию мелкодисперсного тумана 5% NaCl. раствор поддерживается на уровне 95 F (35 C) с начальным pH 7,1.
Данные можно записывать несколькими способами. В некоторых случаях образцы исследуют через установленные интервалы времени, чтобы контролировать ход коррозии, тем самым устанавливая коррозионную «жизнь» материала. Чаще, как в настоящей программе испытаний CDA, испытания в солевом тумане используются в качестве критерия «годен-не годен», основанного на заранее определенном периоде воздействия. Программа CDA требовала 96-часовой экспозиции.
В некоторых случаях образцы исследуют через установленные интервалы времени, чтобы контролировать ход коррозии, тем самым устанавливая коррозионную «жизнь» материала. Чаще, как в настоящей программе испытаний CDA, испытания в солевом тумане используются в качестве критерия «годен-не годен», основанного на заранее определенном периоде воздействия. Программа CDA требовала 96-часовой экспозиции.
Альтернативное погружение
В процессе эксплуатации автомобильные компоненты обычно попеременно смачиваются и высушиваются во время движения и стоянки автомобиля. Программа испытаний CDA стремилась воспроизвести эту среду в контролируемых, но ускоренных условиях.
Стандартная практика ASTM G 441 описывает испытание, при котором образцы поочередно погружают в раствор электролита на 10 минут, а затем дают стечь/высохнуть в течение 50 минут. Цикл влажный-сухой повторяется несколько сотен раз или до тех пор, пока визуальный осмотр не обнаружит начало коррозии. Образцы латуни и стали экспонировали в отдельных емкостях.
Альтернативное испытание погружением ASTM изначально было разработано для измерения стойкости алюминия и стали к коррозионному растрескиванию под напряжением хлоридов, но, поскольку испытание также в разумных пределах моделирует циклы смачивания и высыхания компонентов подкапотного пространства, оно было адаптировано к программе оценки CDA. Процедура требует тестовой температуры 80,6 F 1,8 F (27 C ± 1 C) и относительной влажности 45% ± 6%. Эти условия поддерживались в тестах CDA.
Агрессивная среда, указанная в ASTM G 44, представляет собой 3,5% (по весу) раствор NaCl реактивной чистоты, но в тестах CDA был использован раствор обычной каменной соли, наиболее распространенного состава для борьбы с обледенением дорог. Таким образом, в дополнение к хлориду коррозионная среда испытаний содержала некоторое количество сульфата и кальция плюс меньшее количество магния, Таблица 1 . Начальный рН раствора доводили до 7,1, как указано в процедуре ASTM. Детали визуально осматривали после 200, 500 и 1000 циклов, т. е. примерно через 33, 84 и 167 часов суммарного погружения.
е. примерно через 33, 84 и 167 часов суммарного погружения.
| Anions/Cations | Tank #1 (Steel Parts) | Tank #2 (Brass Parts) | ||
|---|---|---|---|---|
| Pre-test | Post-test | Pre-test | Post-test | |
| Хлорид | 22 600 | 23 700 | 21 500 | 22 800 |
| Натрий | 15 300 | Н/Д | 14 700 | нет данных |
| Сульфат | 178 | 441 | 161 | 388 |
| Кальций | 90 | 210 | 80 | 190 |
| Магний | 1,7 | нет данных | 1,7 | нет данных |
| Медь | нет данных | нет данных | нет данных | 0,16 |
Наверх
Результаты испытаний
Испытания в солевом тумане
Насколько хорошо изделия из оцинкованной стали и латуни должны выдерживать испытание в соляном тумане по ASTM B 11 7? Данные, опубликованные в одном справочнике по металлургическим покрытиям, позволяют предположить, что покрытия на основе цинка служат в восемь раз дольше, чем покрытия из медных сплавов, Таблица 2 .
| Цинк с гальваническим покрытием | |
|---|---|
| Обработка | Часы до белой коррозии |
| Без обработки | < 8 |
| Прозрачный хромат | 24-100 |
| Жёлтый переливающийся | 100-200 |
| Серо-оливковый | 100-500 |
| Медь и латунь | |
| Обработка | Часы до белой коррозии |
| Медь, необработанная | < 24 |
| Медно-светлый хромат | 24 |
| Тяжелый хромат меди | 50 |
| Латунь необработанная | 24 |
| Латунь-светлый хромат | 100 |
| Тяжелый хромат латуни | 150 |
Однако эти данные следует интерпретировать осторожно, потому что начало белой коррозии на хромированном цинке сигнализирует о приближающемся конце защиты для основной стали, а появление зеленой коррозии на латуни сигнализирует о начале того, что обычно только начинается. поверхностное воздействие и образование защитного слоя продуктов коррозии.
поверхностное воздействие и образование защитного слоя продуктов коррозии.
Коррозионное поведение, предсказанное в Таблица 2 , быстрое образование защитной пленки, именно то, что наблюдалось в тестах CDA. На рисунках 3 и 4 показан внешний вид испытательных образцов из латуни и стали после 96-часового воздействия соляного тумана. Изделия из латуни, Рисунок 3 , явно потускнели и содержат многочисленные участки, покрытые серо-зеленым продуктом коррозии. Продукт коррозии кажется тонким и липким даже в местах резьбы.
Стальные детали, Рисунок 4 , проявляют различные коррозионные свойства. Цилиндр Ecoated, показанный в модели . На рис. 4a показаны несколько областей, в которых защитное покрытие полностью разрушено, что привело к ржавчине нижележащей стали.
Электрогальванизированные детали, показанные на Рис. 4b , демонстрируют самый широкий диапазон реакции на воздействие солевого тумана. Цинковая пластина с желтым (толстым) хроматным покрытием в центре содержит только небольшие пятна видимых продуктов коррозии, но в остальном не повреждена. Чистая цинковая часть слева и цинк плюс синий (тонкий) хроматный участок справа демонстрируют признаки полного разрушения покрытия с обильным белым продуктом коррозии и отчетливыми участками красной ржавчины.
Цинковая пластина с желтым (толстым) хроматным покрытием в центре содержит только небольшие пятна видимых продуктов коррозии, но в остальном не повреждена. Чистая цинковая часть слева и цинк плюс синий (тонкий) хроматный участок справа демонстрируют признаки полного разрушения покрытия с обильным белым продуктом коррозии и отчетливыми участками красной ржавчины.
Детали с покрытием JS-500, показанные в Рисунок 4c , покрыты объемным белым продуктом коррозии, хотя признаков ржавчины нет. Покрытие продолжает защищать нижележащую сталь, но резьба может оказаться трудной для зацепления, а внешний вид деталей явно ухудшится.
| Рисунок 3 . Образцы из латуни после 96-часовое воздействие соляного тумана. | |
НАЖМИТЕ НА ЛЮБОЕ ИЗОБРАЖЕНИЕ, ЧТОБЫ УВЕЛИЧИТЬ ИЗОБРАЖЕНИЕ
а. Электронное пальто. Электронное пальто. | б. Слева — Цинковая пластина Центр — Цинковая пластина + желтый дихромат Справа — Цинк + синий дихромат. с . Система JS-500. |
|---|---|
| Рисунок 4 . Стальные испытательные детали после 96-часовое воздействие соляного тумана. | |
Реакции оцинкованных и хромированных деталей довольно хорошо согласуются с независимыми данными, приведенными в таблице 2 , и показывают, что при воздействии соляного тумана коррозионное поведение оцинкованной стали сильно зависит от толщины хроматное конверсионное покрытие. Данные в таблице также свидетельствуют о том, что стойкость толстохромированного цинка эквивалентна или даже превосходит стойкость непокрытой латуни. Программа испытаний CDA стремилась проверить этот момент, чтобы определить, будет ли такое поведение продолжаться в течение более длительного времени при поочередном погружении в раствор дорожной соли.
Альтернативные испытания погружением
Компоненты, исследованные после 200 чередующихся циклов погружения в 3,5% раствор каменной соли (приблизительно эквивалентно 1,5 дням совокупного погружения), продемонстрировали почти такую же реакцию, что и компоненты, подвергшиеся воздействию солевого тумана, рис. 5 и 6 . Латунные фитинги, показанные на рис. 5 , слегка потускнели, и имеются следы зелено-серого продукта коррозии, наблюдаемые ранее. Резьба, углубления и острые углы достаточно чистые, а под виниловым чехлом нет следов щелевой атаки.
| Рисунок 5 . Латунные детали после 200 циклов поочередного погружения в 3,5% раствор каменной соли. | |||
| НАЖМИТЕ НА ЛЮБОЕ ИЗОБРАЖЕНИЕ, ЧТОБЫ УВЕЛИЧИТЬ ИЗОБРАЖЕНИЕ | |||
и . Электронное пальто Электронное пальто | б . Цинковая пластина + желтая дихромат | с . Система JS-500 | д . Цинковая пластина |
| Рисунок 6 . Стальные испытуемые детали после 200 чередующихся циклов погружения в 3,5% раствор каменной соли. | |||
Цилиндр с покрытием E, показанный в Рис. 6a , показывает небольшие участки красной ржавчины на острых радиусах, но в остальном это не затрагивается. Это говорит о том, что экопокрытие, вероятно, неравномерно и плохо защищает углы.
Гайки с покрытием из чистого цинка и цинка плюс желтый хромат, 9 шт.0075 Рисунок 7b , примерно повторяйте поведение, наблюдаемое после воздействия соляного тумана. Незащищенная цинковая часть содержит несколько областей белого продукта коррозии цинка, в основном возле углов и на резьбе. Часть цинка плюс желтый (толстый) хромат остается довольно хорошо защищенной, хотя хромат, по-видимому, разрушился в углах, что привело к коррозии цинка. На данный момент нет признаков красной ржавчины ни на одной из оцинкованных деталей.
На данный момент нет признаков красной ржавчины ни на одной из оцинкованных деталей.
| Рисунок 7 . Латунные детали после 1000 чередующихся циклов погружения в 3,5% раствор каменной соли. | ||
НАЖМИТЕ НА ЛЮБОЕ ИЗОБРАЖЕНИЕ, ЧТОБЫ УВЕЛИЧИТЬ ИЗОБРАЖЕНИЕ
| и . Электронное покрытие b . Левая — Цинковая пластина Центр — Цинковая пластина + желтый дихромат Правая — Цинковая пластина + синий дихромат в . Система JS-500 | |
Рисунок 8 . Стальные образцы после 1000 циклов погружения в 3,5% раствор каменной соли. | |
Гайка с покрытием JS-500, показанная на рисунке , содержит большие пятна белых продуктов коррозии, но не красной ржавчины. Покрытие внешне не повреждено, хотя качество резьбовых участков вызывает сомнения. Однако после 1000 циклов (около одной недели) накопленного погружения становятся очевидными разительные различия между латунными и стальными деталями. Помимо появления нескольких пятен тонкого зелено-серого продукта коррозии, латунные винтовые станки, показанные на рис.0075 Рисунок 7 выглядят лишь немного иначе, чем раньше. Резьба функциональна, а участки под виниловыми трубками остаются яркими.
Напротив, стальные изделия с покрытием сильно корродированы, Рисунок 8 , с большими участками красной ржавчины, видимыми в большинстве случаев. Резьба забивается продуктами коррозии, и даже плоские поверхности покрываются объемным налетом. Любопытно, что гайка из цинка и синего хромата, Рис. 8b , в центре, осталась свободной от красной ржавчины, хотя покрытие заметно ухудшилось.
Тот факт, что аналогичные образцы продемонстрировали гораздо худшее поведение в менее суровых условиях, свидетельствует о том, что эффективность системы покрытия значительно варьируется от детали к детали.
Данные о потере массы подтверждают визуальные доказательства
Детали были зачищены и очищены, а затем взвешены для измерения потери массы в результате коррозии. Поскольку это не стандартные детали с одинаковой исходной массой, данные потери массы были преобразованы в процентные значения, указанные в таблице 3 9 .0076 . Латунные детали потеряли в среднем только около 0,13% массы в результате 1000 чередующихся циклов погружения в 3,5%-ный раствор дорожной соли.
| Ранг | Описание детали | Потеря массы в процентах |
|---|---|---|
| «Лучший» | Все детали из латуни | 0,07-0,26, ср. 0,13 0,13 |
| Сталь с покрытием E | 0,21 | |
| Цинк, 0,15 мил (0,004 мм) | 1,35 | |
| Цинк + синий хромат | 1,47 | |
| Дженерал Моторс JS-500 | 1,62 | |
| «Худший» | Цинк + желтый хромат | 2,37 |
За исключением детали с Е-покрытием, все испытательные образцы из стали потеряли примерно в 10 раз или более массу по сравнению с образцами из латуни . Деталь, покрытая цинком и желтым хроматом, которая довольно хорошо показала себя под воздействием соляного тумана и, по-видимому, сохраняла защитные свойства в течение нескольких сотен циклов «влажный-сухой», претерпела наибольшую процентную потерю массы из всех после 1000 циклов. Несмотря на плохой внешний вид, стальная деталь Ecoated потеряла относительно немного массы. Вероятно, это связано с тем, что коррозия была ограничена дискретными областями, где Е-покрытие разрушилось.
Наверх
Резюме
Воздействие условий ускоренной коррозии в соляном тумане и альтернативных средах погружения явно влияет как на латунь, так и на сталь с покрытием. После 96 часов воздействия соляного тумана покрытие из цинка плюс (толстое) желтого хромата, по-видимому, работает как минимум так же хорошо, как и голая латунь, которая довольно быстро начинает тускнеть. Другие покрытия, наносимые на стальные детали винтовых машин, менее удовлетворительны.
Однако по мере проведения испытаний присущая латуни коррозионная стойкость становится все более очевидной. Все покрытия на стальных деталях со временем разрушаются, а физическое состояние изделий значительно ухудшается.
Продукты коррозии накапливаются в виде неприглядных пятен, и детали остаются далекими от их первоначального внешнего вида. Резьба подвергается коррозии, возможно, до такой степени, что отсоединение соединений может оказаться затруднительным.
Продукты коррозии скапливаются в углублениях. Некоторых это может просто раздражать; для других это означает отсутствие качества.
Некоторых это может просто раздражать; для других это означает отсутствие качества.
Латунные детали тускнеют, и это происходит после очень небольшого воздействия. Но, как и у других металлов на основе меди, первоначальные продукты коррозии защищают от долговременного воздействия, а внешний вид деталей практически не изменяется. Резьбовые соединения по-прежнему легко отвинчиваются, а фитинги для шлангов сохраняют сцепление. Есть обесцвечивание, но общее ощущение качества остается.
Внешний вид, безусловно, важен на современном рынке, ориентированном на качество, но данные о потере массы, измеренные в этом кратком исследовании, доказывают, что коррозионная стойкость латуни не ограничивается поверхностным слоем. Прочное качество латуни гарантирует, что изделия не только сохранят свой внешний вид, но и продолжат выполнять свои функции.
И это истинная ценность латуни.
Наверх
Каталожные номера
- ASM International, Handbook of Corrosion Data, B.
 D.Craig, Ed., Metals Park, 1989, стр. 149 и далее.
D.Craig, Ed., Metals Park, 1989, стр. 149 и далее. - Американское общество по испытаниям и материалам, обозначение ASTM B 1 17-90: Стандартный метод испытаний в соляном тумане, Ежегодный сборник стандартов ASTM 1991 г., том 03.02 Износ и эрозия; Коррозия металла.
- Американское общество по испытаниям и материалам, обозначение ASTM G 44-88: Стандартная практика оценки стойкости металлов и сплавов к коррозионному растрескиванию под напряжением путем попеременного погружения в 3,5% раствор хлорида натрия, Ежегодный сборник стандартов ASTM 1991 г., том 03.02 Износ и эрозия; Коррозия металла.
- Эппенштейнер, Ф. В. и М. Р. Дженкинс, «Хроматные конверсионные покрытия», Руководство и справочник по отделке металлов, Metals and Plastics Publications, Inc., Хакенсак, Нью-Джерси, 1989, стр. 456-469.
Защита от коррозии и сопротивление: прозрачная органическая отделка
- Возможность обслуживания
- Основные системы покрытий
- Добавки
- Приложение
- Свойства покрытия
- Дополнительные соображения
Отличительные цвета меди и медных сплавов делают их ценными для архитектурных и потребительских предметов и предметов искусства. Их естественные металлические тона варьируются от красноватого до серебристого, а ряд других цветов можно получить путем химической или электрохимической обработки. Медь и ее сплавы чрезвычайно устойчивы к коррозии, но при воздействии атмосферы или обращении со временем образуется поверхностное обесцвечивание. Внешний вид этих металлов можно сохранить, нанеся на их поверхности тонкие прозрачные защитные покрытия. Эти покрытия представляют собой органические химические вещества, которые затвердевают при комнатной температуре или при выпекании и обычно наносятся в растворителе.
Их естественные металлические тона варьируются от красноватого до серебристого, а ряд других цветов можно получить путем химической или электрохимической обработки. Медь и ее сплавы чрезвычайно устойчивы к коррозии, но при воздействии атмосферы или обращении со временем образуется поверхностное обесцвечивание. Внешний вид этих металлов можно сохранить, нанеся на их поверхности тонкие прозрачные защитные покрытия. Эти покрытия представляют собой органические химические вещества, которые затвердевают при комнатной температуре или при выпекании и обычно наносятся в растворителе.
На рынке представлены сотни полезных прозрачных покрытий, составленных из многочисленных полимеров, растворителей и добавок. Пользователь выбирает из них покрытие, исходя из экономичности, предполагаемого срока службы, желаемой прозрачности и ожидаемых условий эксплуатации.
Многие производители покрытий предпочитают изготавливать покрытия по индивидуальному заказу и тесно сотрудничать с пользователем для решения его конкретных проблем. Существует также большое количество стандартных композиций, которые можно заказать по торговому наименованию и которые удовлетворят многие потребности.
Существует также большое количество стандартных композиций, которые можно заказать по торговому наименованию и которые удовлетворят многие потребности.
Из-за широкого спектра доступных составов здесь рассматриваются только общие характеристики различных систем и добавок. Результаты испытаний репрезентативных систем покрытия представлены для указания диапазона и типа свойств, которые могут быть получены. Но следует помнить, что эффективность отделки также зависит от состава основного металла и от процедур очистки и нанесения, используемых при нанесении покрытия.
По свойствам невозможно количественно предсказать, как долго и насколько хорошо покрытие будет защищать подложку. Чтобы ответить на этот вопрос, необходимо нанести покрытие на металл в заводских условиях и подвергнуть комбинацию воздействию окружающей среды, характерной для предполагаемого использования.
Наверх
Удобство обслуживания
Доступны покрытия
, которые могут защищать металлы на основе меди в течение многих лет в идеальных условиях. Однако обращение, влажность, загрязнение воздуха, солнечный свет и истирание — все это сокращает срок службы покрытия. Например, срок службы покрытия обычно невелик при наружном применении в городах с сильным загрязнением воздуха.
Однако обращение, влажность, загрязнение воздуха, солнечный свет и истирание — все это сокращает срок службы покрытия. Например, срок службы покрытия обычно невелик при наружном применении в городах с сильным загрязнением воздуха.
При выборе покрытия необходимо понимать, что максимальная устойчивость к одному типу условий эксплуатации может снизить устойчивость к другим. Кроме того, если ожидается, что срок службы изделия будет больше, чем любой разумно достижимый срок службы покрытия, необходимо выбрать покрытие, которое можно снять с помощью растворителя, чтобы можно было восстановить изделие, когда покрытие и внешний вид ухудшились до неприемлемого состояния. уровень.
Некоторые примеры характеристик покрытия указывают на диапазон пригодности органических покрытий для меди и ее сплавов.
Акриловый лак, высыхающий на воздухе, с ингибитором потускнения (бензотриазол*) более пяти лет защищает бронзовую табличку с именем на открытом воздухе в городских районах Нью-Джерси. Такое же покрытие в помещении на поручнях и других объектах, подверженных износу, вышло из строя менее чем за год.
Такое же покрытие в помещении на поручнях и других объектах, подверженных износу, вышло из строя менее чем за год.
Комбинация силиконовой грунтовки и акрилового верхнего слоя продемонстрировала превосходный внешний вид после более чем шести лет эксплуатации внутри помещений с умеренным истиранием или без него. Та же самая система значительно потемнела за один год открытого наружного воздействия, но показала хорошие результаты в течение более трех лет на закрытых дверях офисных зданий и церквей.
Нитроцеллюлозный лак разрушился менее чем через год при открытом внешнем воздействии. Уретановые лаки продержались около года в тех же условиях.
Обожженные алкидно-бутиловые и бутиловые покрытия хорошо выглядели после двух лет эксплуатации на открытом воздухе. Эпоксидные покрытия темнеют через четыре-шесть месяцев.
Силиконовые термореактивные покрытия сохраняют хорошие защитные свойства через 62 дня при 200 F или 100 часов при 300 F.
Отделка салона автомобиля из состаренной латуни защищена термореактивным эпоксидным прозрачным покрытием.
Медная крыша Дворца спорта в Мехико покрыта акриловым лаком воздушной сушки, содержащим ингибитор и органические поглотители ультрафиолета.
Сантехника из латуни в течение более пяти лет удовлетворительно защищена эпоксидным покрытием спекания.
Наверх
Основные системы покрытий
Нитроцеллюлоза . Нитроцеллюлозные покрытия являются наименее дорогими и наиболее распространенными покрытиями воздушной сушки для внутренних работ. Их модифицируют алкидными или акриловыми смолами. Нитроцеллюлозные покрытия используются для наружных работ; однако их обычно разбирают и заменяют с интервалом менее одного года. Они не обладают высокой устойчивостью к химическим веществам, но быстро сохнут и просты в использовании.
Акрил . Акриловые материалы, доступные в виде сушки на воздухе или в термореактивных композициях, являются относительно дорогими материалами. Модификации воздушной сушки популярны для наружных работ, в то время как термореактивные типы подходят для внутренних работ, требующих высокой устойчивости к нагреву и истиранию. Поскольку термореактивные покрытия не снимаются удобно, они не подходят для основных архитектурных применений.
Поскольку термореактивные покрытия не снимаются удобно, они не подходят для основных архитектурных применений.
Эпоксидные покрытия . Эпоксидные покрытия обладают отличной стойкостью к износу и химическим веществам. Они относительно дороги и доступны только в термореактивных или двухкомпонентных (активируемых катализатором) композициях с относительно коротким сроком годности. Они хороши для тяжелых условий эксплуатации внутри помещений, но быстро портятся и темнеют через несколько месяцев эксплуатации на открытом воздухе.
Силиконовые покрытия . Силиконы обеспечивают лучший потенциал для покрытий, которые должны работать при повышенных температурах. Используются тонкие пленки этих дорогостоящих покрытий, и может потребоваться защита вторым слоем более стойкого к истиранию лака. Добавляются вещества, поглощающие ультрафиолет, чтобы предотвратить потемнение силикона при внешнем воздействии.
Алкидные покрытия . При нанесении алкидных покрытий требуется медленная сушка или обжиг. Эти покрытия, модифицированные меламиновыми смолами, недороги и достаточно прочны для наружного применения. Устойчивость к химическим веществам обычно хорошая.
При нанесении алкидных покрытий требуется медленная сушка или обжиг. Эти покрытия, модифицированные меламиновыми смолами, недороги и достаточно прочны для наружного применения. Устойчивость к химическим веществам обычно хорошая.
Уретановые покрытия . Ухудшение цвета при внешнем воздействии было проблемой для уретановых покрытий. Стойкость к химическим веществам и истиранию хорошая даже для покрытий, высыхающих на воздухе.
Бутират ацетата целлюлозы . Обычно рассматриваемые для внутренних работ, покрытия из ацетата целлюлозы и бутирата высыхают на воздухе и имеют умеренные стоимость и свойства. Они имеют тенденцию темнеть при наружном применении.
Винил . Виниловые покрытия требуют стабилизации против разрушения ультрафиолетом. Обычно это относительно мягкие и гибкие покрытия.
Поливинилфторидная пленка (Tediars). Пленки Tedlar, нанесенные путем склеивания валиком с клеем, использовались для защиты листовой меди при наружных работах. Предполагается, что эти прозрачные пленки могут защищать правильно подготовленную подложку в течение двадцати и более лет.
Предполагается, что эти прозрачные пленки могут защищать правильно подготовленную подложку в течение двадцати и более лет.
Наверх
Добавки
Среди распространенных добавок для покрытий выделяют следующие типы:
Поглотители ультрафиолета . Поглотители ультрафиолета представляют собой органические соединения, которые иногда добавляют в покрытия для наружных работ, чтобы предотвратить потемнение и разрушение покрытия. В некоторых случаях они могут также взаимодействовать с подложкой и предотвращать потускнение.
Выравнивающие агенты . Выравнивающие агенты улучшают текучесть покрытий и тем самым улучшают внешний вид поверхности. Кроме того, снижается вероятность Dinholling или других дефектов.
Хелатирующие агенты . Бензотриазол и другие хелатирующие агенты взаимодействуют с медью и ее сплавами, предотвращая потускнение. Хелатирующие агенты предпочтительно впитываются на поверхности металлов и действуют как невидимый барьер для элементов или соединений, которые могут вызвать коррозию. Таким образом, они защищают металл от проникновения окислителей через покрытие и продолжают защищать даже после того, как в покрытии образовался незначительный дефект. Хелатирующие агенты могут быть включены в состав покрытия или применяться как часть процедуры предварительной обработки.
Таким образом, они защищают металл от проникновения окислителей через покрытие и продолжают защищать даже после того, как в покрытии образовался незначительный дефект. Хелатирующие агенты могут быть включены в состав покрытия или применяться как часть процедуры предварительной обработки.
Антиоксиданты . Антиоксиданты уменьшают деградацию покрытий при длительном и сильном воздействии. Примерами являются гидрохинон, N-пропилгаллат и модифицированные соединения фенола и крезола.
Наверх
Применение
Ни одно покрытие не может оправдать ожиданий, если оно нанесено на плохо подготовленную поверхность. На металлической поверхности не должно быть таких загрязнений, как грязь, масло, пыль, старая отделка и отпечатки пальцев. Покрытие должно быть выполнено с минимальной задержкой после очистки, и должны быть приняты меры предосторожности для предотвращения повторного загрязнения. Меры предосторожности включают работу в среде с низким содержанием пыли, работу в белых перчатках и нанесение на поверхность ингибиторов потускнения (хелатирующих агентов).
Не следует использовать обычную стальную вату для очистки, так как подушечки могут содержать химические вещества, окрашивающие медные металлы. Подходящими абразивами являются подушечки или круги из карбида кремния (Scotch-brite), подушечки из нержавеющей стали и порошкообразная пемза. Порошок пемзы растворяют в 5% растворе щавелевой кислоты и растирают тканью. Все остатки необходимо удалить, а поверхность вытереть насухо чистой тряпкой. Абразивы нельзя использовать на сильно полированных (зеркальных) поверхностях. Если для полировки перед нанесением покрытия использовались полировочные составы, детали необходимо обезжирить или очистить каким-либо другим способом, чтобы удалить любые остатки.
Обезжиривание обычно проводят растворителями, такими как бутилцеллозольв и трихлорэтилен. Чтобы предотвратить образование полос и пятен, может потребоваться протирание больших участков насухо безворсовыми салфетками. Свежепокрытые детали должны быть тщательно нейтрализованы и промыты горячей водой перед нанесением покрытия.
Зона распыления должна быть свободной от пыли и грязи, при умеренной температуре (от 50 до 900F), при низкой влажности (определенно менее 80% при использовании органических транспортных средств) и с хорошей вентиляцией.
Обычно наносится достаточное количество слоев для достижения общей толщины сухой пленки от 0,5 до 1,5 мил. Большая толщина обычно становится очевидной, и металл приобретает лакированный вид. Однако производитель покрытия может рекомендовать более тонкие покрытия для определенных областей применения.
Наверх
Свойства покрытия
Свойства ряда патентованных коммерческих покрытий представлены в таблице 1. Свойства покрытия иногда зависят от состава подложки (медь, латунь, нейзильбер и т.д.). Свойства, показанные в таблице 1, являются репрезентативными для нескольких различных подложек. Эта подборка иллюстрирует, что различия между покрытиями данной органической основы могут быть такими же большими, как и различия между основами. Различия возникают из-за того, что производители используют собственные рецептуры, комбинации полимеров и добавок.
Процедуры испытаний, использованные для компиляции свойств в Таблице 1, были следующими:
Твердость по карандашу — Твердость, при которой происходит переход от царапания покрытия к выкрашиванию грифеля. Шкала твердости от самой твердой до самой мягкой: 7H, 6H, 5H, 4H, 3H, 2H, H, HB, F.
Испытание на истирание по Таберу — Колесо CS 10 Calibrase с нагрузкой 500 грамм подвергали образцу испытанию до разрушения или до 500 циклов. Результаты представлены как потеря веса из-за истирания.
Гибкость — Изгиб был выполнен на 1/8 дюйма. до 11/2 дюйма. Коническая оправка Гарднера. Результаты представлены как отсутствие растрескивания (NC), мелкое растрескивание (FC), растрескивание (C) или сильное растрескивание (SC).
Сопротивление удару — Удар силой 28 дюймов-фунтов был выполнен на приборе для испытаний на удар Gardner. Результаты представлены как отсутствие звезд (NS), слабое звездообразование (SS), звездообразование (S) или широкое звездообразование (ES).
Устойчивость к химическим веществам — Образцы были визуально исследованы для выявления изменений после воздействия растворов в течение 24 часов. Использовались растворы 0,5% сульфида аммония, 1% детергента Tide и синтетического пота.
Наверх
Дополнительные соображения
Блестящая металлическая поверхность служит отличным фоном для наблюдения за дефектами покрытия и потускневшими пятнами. Следовательно, допустимость дефектов низкая, и прозрачные покрытия должны иметь высокую степень эффективности, чтобы работать удовлетворительно. Это не проблема для состаренных или цветных металлов. Проблема медных сплавов заключается в том, что потемнение подложки может происходить даже под неповрежденным покрытием из-за взаимодействия меди с остаточными растворителями. Это особая проблема при экспонировании на открытом воздухе, когда ультрафиолетовое излучение может стимулировать расщепление растворителей. При правильном выборе растворителей и добавок эту проблему можно свести к минимуму. Этиловый спирт и изопропиловый спирт вызывают значительное потускнение. Бензол, толуол, ксилол, бутилацетат и этилацетат намного лучше.
Этиловый спирт и изопропиловый спирт вызывают значительное потускнение. Бензол, толуол, ксилол, бутилацетат и этилацетат намного лучше.
Изменение цвета меди и ее сплавов также может происходить при температурах отверждения, обычно рекомендуемых для термореактивных покрытий. Целесообразно использовать низкие температуры отверждения и короткие графики отверждения, чтобы избежать такого обесцвечивания в процессе. Каталитическая активность меди иногда позволяет использовать более низкие температуры или более короткие графики отверждения.
Короткие графики обжига при высоких температурах являются обязательным требованием для операций по нанесению покрытия на рулоны. В этой области было проведено значительное количество исследований, и теперь доступны удовлетворительные рецептуры рулонного покрытия. Эти покрытия могут формироваться после отверждения и при этом сохранять хорошие защитные свойства. Использование пленки Tediar для покрытия рулонов является новой инновацией. Чрезвычайно долгий срок службы покрытий Tedlar при наружном применении обеспечивает экономию расходов на техническое обслуживание, что может оправдать дополнительные расходы на покрытие. Металл с тедиаровым покрытием также может быть сформирован.
Металл с тедиаровым покрытием также может быть сформирован.
Адгезия покрытий к меди и ее сплавам может быть проблемой. В этой области также ведутся серьезные исследования. Эта работа показала, что адгезия покрытий может быть улучшена за счет использования грунтовок или конверсионных покрытий. В операциях по нанесению рулонного покрытия растворы для предварительной обработки могут быть распылены и высушены перед нанесением покрытия. Однако известно, что предварительная обработка влияет на формуемость покрытия, и это должно быть проверено перед применением предварительной обработки. Предварительную обработку также можно использовать для защиты от потускнения под пленкой путем включения ингибиторов в растворы или повторного окисления поверхности.
Наверх
Бензотриазол : эффективный ингибитор коррозии для медных сплавов, Лист технических данных 108/9, Copper Development Association Inc., Нью-Йорк (1969)
Tediars является зарегистрированным товарным знаком Du Pont Co.
Ржавеет или подвергается коррозии латунь? (Металлы)
Латунь обычно используется в производстве таких вещей, как музыкальные инструменты, механические инструменты и предметы декора. Это популярный выбор по многим причинам, от разнообразия цветов до эстетически приятного внешнего вида. Но способна ли латунь ржаветь?
Латунь не ржавеет, так как не содержит железа и поэтому не может ржаветь. В зависимости от металла вероятность образования ржавчины выше или ниже в зависимости от элементов, обнаруженных внутри него.
В этой статье мы более подробно рассмотрим, почему латунь не ржавеет, как латунь реагирует на окружающую среду, а также как на нее влияет каждый элемент, содержащийся в латуни. Если вам интересно узнать больше об этих темах, продолжайте читать.
Содержание
Почему латунь не ржавеет?
Как сказано выше, латунь просто не ржавеет, потому что не содержит железа. Материалы, содержащие железо, будут ржаветь при контакте с такими факторами, как кислород и вода. Когда металл, такой как латунь, не содержит железа, он не может образовывать оксид железа, из-за чего металлы начинают ржаветь.
Когда металл, такой как латунь, не содержит железа, он не может образовывать оксид железа, из-за чего металлы начинают ржаветь.
Латунь — это металлический сплав, состоящий из меди и цинка. В зависимости от количества каждого элемента, содержащегося в каждом отдельном куске латуни, он может оказывать положительное или отрицательное влияние на материал. В то время как такие элементы, как медь и цинк, делают латунь прочной и долговечной, недостаток железа также препятствует возникновению ржавчины.
Хотя латунь может не ржаветь, это не означает, что она полностью устойчива к коррозии. Многие путают образование ржавчины и коррозии как одно и то же, но это разные вещи, и в основном это сводится к химии.
Коррозия — это постепенное разрушение металлов в результате химической реакции, вызванной окружающей средой, которой подвергается материал. Ржавчина на самом деле является формой коррозии, но при возникновении ржавчины происходит окисление железа, также ржавчина не может возникнуть, если в этих материалах нет железа.
Таким образом, хотя латунь может подвергаться коррозии в среде, в которой она находится, она все же не подвержена коррозии.
Теперь, когда вы лучше понимаете, почему латунь не ржавеет, ниже мы обсудим, как латунь реагирует в определенных средах и в определенных условиях.
Как реагирует латунь?
Надеюсь, теперь вы лучше понимаете, как латунь может подвергаться коррозии. Но что вызывает коррозию латуни и как с этим бороться?
Коррозия
Хотя металлы, не содержащие железа, не ржавеют, они все же подвержены риску коррозии при контакте с некоторыми элементами, такими как кислород и вода.
Обычно латунь подвергается коррозии, когда содержащиеся в ней элементы, такие как медь и олово, подвергаются воздействию воды. Это, в свою очередь, может изменить цвет латуни и образовать красноватые или розовые пятна на поверхности.
Материалы из латуни, такие как трубы и механические инструменты, которые регулярно подвергаются воздействию воды или окружены ею, более подвержены коррозии, чем латунные материалы, которые не подвержены коррозии. К счастью, существует множество способов обработки корродированной латуни, независимо от того, решите ли вы купить бытовой очиститель или создадите средство для удаления налета своими руками.
К счастью, существует множество способов обработки корродированной латуни, независимо от того, решите ли вы купить бытовой очиститель или создадите средство для удаления налета своими руками.
Хотя на таких поверхностях, как латунь, при контакте с водой может возникнуть коррозия, ниже мы рассмотрим, как кислород может вызывать окисление.
Окисление
Когда металлы встречаются с кислородом, на поверхности может образоваться окисление.
Хотя латунь легко подвергается коррозии, она также может окисляться. Подобно коррозии, окисление происходит, когда латунь или любой другой материал вступает в контакт с воздухом.
На самом деле у окисления есть свои плюсы и минусы, о которых многие люди могут не знать. Во-первых, хотя процесс окисления может плохо повлиять на внешний вид латуни, он создает защитное покрытие вокруг материала, которое помогает остановить дальнейшую коррозию.
Тем не менее, окисление также может быть чрезвычайно опасным, так как оно разрушает цинк, хранящийся в материале.
Цинк отвечает за прочность, которую удерживает латунь, поэтому, когда латунь отвечает за такие вещи, как скрепление трубы, болта или выполняет какую-либо соединительную функцию, это определенно может быть проблемой, когда цинк начинает разрушаться из-за к окислению.
Признаки окисления латуни очевидны, так как поверхность обычно становится черной, зеленой или синей. Вы можете обрабатывать окисленную латунь так же, как и корродированную латунь, если вы сразу после этого полностью высушите поверхность. Таким образом, вы не получите никакого вреда от воздействия воды.
Надеюсь, теперь вы лучше понимаете плюсы и минусы коррозии и окисления таких металлов, как латунь.
Какие элементы содержатся в латуни?
Каждый элемент из латуни повышает прочность, долговечность и другие положительные свойства материала. Ниже мы рассмотрим некоторые из наиболее часто встречающихся элементов в латуни и то, что они делают.
Медь
Современная латунь на 67 % состоит из меди и считается основным компонентом латуни. Медь оказывает много положительного воздействия на латунь и ее поверхности, например, создает неблагоприятные условия для размножения бактерий.
Медь оказывает много положительного воздействия на латунь и ее поверхности, например, создает неблагоприятные условия для размножения бактерий.
Хотя вероятность образования бактерий на материалах на основе меди меньше, это позволяет латуни быть идеальным кандидатом, когда речь идет о создании медицинского оборудования и внутренних приспособлений, таких как дверные ручки.
Цинк
Современная латунь на 33% состоит из цинка и помогает латуни придать ей прочность и долговечность, необходимые для выполнения работы.
Ранее мы обсуждали, насколько полезен цинк для латуни и как он помогает латуни сохранять свою прочность, когда латунь используется в производстве таких вещей, как трубы и болты. Хранение таких инструментов вместе и на месте очень полезно для долговечности вашей латуни, а также для обеспечения ее безопасности и там, где она должна быть.
Большое количество цинка также делает латунь очень пластичной, что способствует долговечности латуни в любых возможных условиях. Это показывает, насколько мощным элементом является цинк и насколько он полезен для латунных материалов.
Это показывает, насколько мощным элементом является цинк и насколько он полезен для латунных материалов.
Свинец
Свинец обычно добавляют в латунь в концентрации 2%.
Свинец — удобный элемент, так как он обладает многочисленными преимуществами для любого материала, с которым вступает в контакт. Во-первых, это улучшает обрабатываемость латуни, облегчая производство товаров и предметов в больших масштабах.
Свинец также обеспечивает большую прочность и устойчивость к коррозии. Свинец может даже обеспечить герметичность, герметизируя усадочные поры, когда дело доходит до архитектурной фурнитуры.
Хотя свинец обычно не встречается в латуни, легко понять, почему свинец добавляют в такие материалы, как латунь, поскольку он имеет множество преимуществ.
Заключение
В этой статье мы узнали, что ржавчина не может образоваться, если она не соприкасается с железом, а видя, что латунь не удерживает железо, она не может ржаветь.
Хотя латунь может и не ржаветь, на нее могут воздействовать те же факторы, которые вызывают ржавчину на других металлах, такие как кислород и вода. Это, в свою очередь, вызывает окисление и коррозию и то, как это влияет на латунь в долгосрочной перспективе.
Это, в свою очередь, вызывает окисление и коррозию и то, как это влияет на латунь в долгосрочной перспективе.
Наконец, мы рассмотрели материалы, которые вы найдете в латуни, включая медь, цинк и иногда свинец. Мы обсудили, как каждый из этих элементов способствует прочности, долговечности, обрабатываемости и коррозионной стойкости латуни.
Итак, выбираете ли вы инструмент или ищете новый декор для улицы, качественная латунная деталь может быть именно тем, что вам нужно.
Ржавеет ли латунь? — Почему или почему нет?
Латунь – очень часто используемый металлический сплав. Он используется для различных вещей, таких как украшения, гитарные струны и другие музыкальные инструменты, мебель и инструменты. Поскольку он так часто используется, вы можете задать вопрос: « Ржавеет ли латунь?»
В этой статье я отвечу на этот вопрос, а также на некоторые другие вопросы, которые могут возникнуть.
Итак, ржавеет ли латунь? Прямой ответ — нет. Латунь не ржавеет. Ржавчина обычно возникает из-за реакции металла внутри сплава и окружающей среды вокруг него. В латуни нет металла, необходимого для образования ржавчины. Значит, не ржавеет. Однако латунь из-за окисления тускнеет и образует на своей поверхности черноватый, зеленоватый налет.
Латунь не ржавеет. Ржавчина обычно возникает из-за реакции металла внутри сплава и окружающей среды вокруг него. В латуни нет металла, необходимого для образования ржавчины. Значит, не ржавеет. Однако латунь из-за окисления тускнеет и образует на своей поверхности черноватый, зеленоватый налет.
Подробнее о том, почему именно латунь не ржавеет, я расскажу в статье. И укажите, не подвергается ли оно коррозии из-за других факторов. А также более подробно рассмотрим металлы, входящие в состав латуни.
И упомяните о некоторых маленьких хитростях, с помощью которых можно придать блеск любой латуни, которая, кажется, потускнела от времени.
Почему латунь не ржавеет?
Основная причина, почему латунь не ржавеет, это отсутствие железа. Ржавчина образуется из-за окисления железа.
Это происходит, когда вы подвергаете утюг воздействию воды и кислорода. Но латунь не содержит железа, поэтому на ней не может образоваться оксид железа (ржавчина).
Латунь — это сплав, который обычно изготавливается из меди и цинка. В отличие от железа они не образуют ржавчины.
Однако, в зависимости от количества меди или цинка, используемых в металле, он может сделать его прочнее или слабее. Основное преимущество латуни в том, что она не ржавеет. Но как насчет других эффектов?
Что происходит с латунью
Ржавчина — не единственное, что влияет на металл. Фактически, устойчивость к ржавчине не означает, что латунь невосприимчива к другим воздействиям.
Коррозия для латуни
Тот факт, что латунь не ржавеет, не означает, что она не будет подвергаться коррозии.
Некоторые думают, что коррозия и ржавчина — это одно и то же. Это неверно, ржавчина — это средство, при помощи которого разъедается железо. Это всего лишь одна из форм коррозии. Как и железо, медь также подвергается коррозии.
Основной причиной коррозии латуни является воздействие воды на медь или олово, присутствующие в латуни.
Вместо ржавчины медь или олово, реагирующие с водой, вызывают изменение цвета. В результате на поверхности могут образовываться розоватые или красноватые пятна.
В основном это касается инструментов и т.п., подвергающихся воздействию воды. Другим примером могут быть латунные трубы. Они будут постоянно подвергаться воздействию воды. В результате вы должны заметить красноватые или розоватые пятна на поверхности.
Окисление латуни
Я рассмотрел, как латунь может реагировать на воду, что приводит к коррозии. Но что делать при длительном контакте с кислородом? Окисляется ли латунь, как железо, без образования ржавчины? Да, латунь окисляется. Окисление происходит на цинке, присутствующем в латуни.
Окисление латуни может быть для нее как положительным, так и отрицательным фактором. Окисление может помочь предотвратить дальнейшую коррозию латуни. Однако это приводит к тому, что поверхность латуни становится менее привлекательной.
Окисление также может повлиять на структурную целостность латуни. Так как окисление латуни может разрушить присутствующий в ней цинк. Главной обязанностью цинка является прочность латуни. Таким образом, окисление может ослабить латунь.
Так как окисление латуни может разрушить присутствующий в ней цинк. Главной обязанностью цинка является прочность латуни. Таким образом, окисление может ослабить латунь.
Окисление очень заметно. Поверхность латуни покроется чешуйчатым черным, синим или зеленым слоем.
Из чего сделана латунь?
Будучи сплавом, латунь представляет собой комбинацию более чем одного отдельного металла. Это делается для того, чтобы усилить некоторые качества, которых может не хватать каждому металлу, за счет заимствования у другого элемента.
В этой статье я расскажу о некоторых наиболее часто используемых металлах для изготовления латунных сплавов.
Медь
Медь играет самую важную роль в производстве латуни. Это основной компонент латуни. Составляя около 67% в наши дни. Латунь может многое выиграть от меди. Вот почему он составляет большую часть.
Одной из наиболее примечательных характеристик, которые медь придает латуни, является низкая обитаемость бактерий.
Эта черта делает латунь полезной при изготовлении медицинского оборудования. А также дверные ручки или любые поверхности, к которым вы будете регулярно прикасаться. Таким образом, снижается вероятность распространения болезни.
Цинк
Цинк — еще один известный металл, используемый для создания латуни, составляющий 33% его. Латунь получает свою силу и устойчивость от цинка. Таким образом, увеличение количества цинка может привести к получению более прочного сплава.
Прочность латуни позволяет использовать ее в трубах для удержания воды и в болтах для их удержания на месте. И в отличие от обычных труб, они не ржавеют и не ломаются.
Использование цинка в латуни также повышает ее пластичность. Это означает, что из него можно сделать тонкую проволоку, но она все равно сохранит свою первоначальную прочность и долговечность. Таким образом, добавляя больше преимуществ латуни.
Свинец
Среди металлов, добавляемых в латунь, свинец присутствует в довольно небольшом количестве. Составляя всего около 2% от общего количества латуни. Однако свинец не всегда присутствует в латуни. Но он добавляется, чтобы получить дополнительные преимущества.
Составляя всего около 2% от общего количества латуни. Однако свинец не всегда присутствует в латуни. Но он добавляется, чтобы получить дополнительные преимущества.
Добавление свинца в латунь может укрепить ее и облегчить производство. Таким образом, массовое производство изделий из латуни значительно упрощается.
Еще одним преимуществом, которое латунь получает от свинца, является повышение коррозионной стойкости. Это может даже обеспечить герметичность латуни. Это достигается за счет герметизации усадочных пор.
Ниже представлена таблица состава латуни. Несколько дополнительных металлов добавляются в небольшой пропорции в зависимости от требований к латуни.
Очистка потускневшей латуни
Окисление и коррозия могут привести к потускнению латуни. Но это не значит, что его нельзя исправить. Прежде всего вам нужно сначала узнать, с каким типом латуни вы работаете. Если это латунь с покрытием или цельный кусок латуни.
Обнаружение и очистка потускневшего латунного покрытия
Это можно определить с помощью простого магнита. Поместите его напротив латунного предмета. А если не липнет, то это сплошная латунь. Но если и липнет, то скорее всего из латуни. Очистить латунное украшение или инструмент очень легко.
Поместите его напротив латунного предмета. А если не липнет, то это сплошная латунь. Но если и липнет, то скорее всего из латуни. Очистить латунное украшение или инструмент очень легко.
Все, что вам нужно сделать, это помыть его горячей водой с мылом. Будьте осторожны, чтобы не использовать что-то грубое для чистки. Так как вы можете поцарапать покрытие.
Удаление лака с цельной латуни
Однако очистка цельной латуни немного сложнее. Во-первых, они обычно поставляются с предварительно нанесенным слоем лака. Сначала вам нужно будет удалить лак, прежде чем вы сможете правильно очистить его.
Погрузите ненадолго в горячую воду, затем охладите и снова погрузите. Это может привести к тому, что лаковое покрытие начнет отслаиваться. После этого можно попробовать отклеить его ногтями.
Очистка от потускнения твердой латуни
После удаления лака замочите его в небольшом количестве горячей мыльной воды, чтобы очистить. После этого используйте старую зубную щетку, чтобы соскоблить лишнюю грязь и пыль, которые могут остаться. После этого промойте и высушите его, чтобы вы могли, наконец, начать избавляться от потускнения.
После этого промойте и высушите его, чтобы вы могли, наконец, начать избавляться от потускнения.
Используйте пищевую соду и белый уксус, чтобы сделать пасту. Эта паста может немного шипеть, но должна успокоиться. Теперь у вас есть паста. Нанесите его на поверхность латунного предмета кистью или даже рукой.
После тщательного нанесения пасты дайте ей постоять около 30 минут. По прошествии 30 минут смойте пасту и вытрите насухо тряпкой. Тусклый вид должен исчезнуть, а старый, полированный блеск должен вернуться.
Если на нем все еще есть следы потускнения, повторяйте процесс, пока не получите желаемый результат. Это работает, потому что кислота в уксусе и натрий, присутствующий в пищевой соде, создают химическую реакцию для растворения потускнения.
Ниже прилагается видео, показывающее, как очистить потускневшую латунь.
Обычное использование латуни
Тот факт, что латунь не ржавеет, позволяет нам использовать ее во многих сферах нашей жизни. Ранее я упоминал о полезных свойствах, которые латунь получает от меди, цинка и свинца.
Ранее я упоминал о полезных свойствах, которые латунь получает от меди, цинка и свинца.
Давайте посмотрим, где можно использовать латунь.
Музыкальные инструменты
Одно из наиболее распространенных применений латуни – это изготовление музыкальных инструментов. Это связано с тем, что он податлив и устойчив к коррозии.
И тот факт, что на нем не могут размножаться бактерии, делает его отличным выбором для изготовления любого музыкального инструмента.
Декорации
Латунь очень часто используется для декорирования. В отличие от большинства металлов, он не будет спешить и оставлять некрасивый след.
Цвет может варьироваться от светло-золотистого или серебристого до более красноватого оттенка. Универсальность позволяет вам делать больше с ним во время украшения.
Инструменты
Благодаря своей долговечности и прочности инструменты из латуни очень популярны. Они не подвержены коррозии и не ржавеют. А болты, сделанные из латуни, довольно прочные, что обеспечивает надежную фиксацию.
Заключение
Вы пришли к этой статье с простым вопросом « Ржавеет ли латунь?» А я ответил и объяснил, почему латунь не ржавеет. А также вдаваться в подробности о том, каким другим эффектам он подвергается. Как и из чего сделана латунь.
Надеюсь, эта статья оказалась для вас информативной. Спасибо за прочтение статьи. До свидания и удачи.
По теме: Латунь против бронзы
Является ли латунь магнитной
Проводит ли латунь электричествоКраска ингибитора коррозии меди 0019
для покрытия медного сплава и латуни, Бес
– Покрытия STEEL-IT
Превратите медные сплавы в нержавеющую сталь с помощью Steel-It®!
Коррозия темнеет, затем чернеет, затем зеленеет на ярко-красной медной поверхности, не только портя, но во многих случаях и разрушая медный сплав. Так? Напыляемые антикоррозионные защитные покрытия Steel-It® для меди и всех ее сплавов позволяют легко и недорого преобразовать любую медную поверхность в промышленно прочную, твердую, долговечную, коррозионно-стойкую, термостойкую, устойчивую к истиранию и химическим веществам. , долговечная отделка из нержавеющей стали 316L. Если вы сегодня воспользуетесь контактной формой слева, чтобы сообщить нам о своих потребностях в промышленной защите меди, мы незамедлительно направим вас к продукту, который лучше всего им соответствует.
, долговечная отделка из нержавеющей стали 316L. Если вы сегодня воспользуетесь контактной формой слева, чтобы сообщить нам о своих потребностях в промышленной защите меди, мы незамедлительно направим вас к продукту, который лучше всего им соответствует.
Защита от коррозии меди и латуни
Нелегированная медь (Cu) представляет собой химически активный и подверженный коррозии металл, который окисляется на воздухе. В простой воде медь образует естественный стойкий слой оксидов меди, так называемый пассивирующий слой. Медь медленно корродирует в чистом воздухе и воде и проявляет хорошую устойчивость к некоторым кислотам (неокисляющим, деаэрированным кислотам). Сплавы с высоким содержанием меди (C 10100–C 19600 и C 80100–C 82800) сталкиваются с такими же проблемами коррозии, как и чистая медь. Как мягкий металл, медь подвержена точечной коррозии. Другие сплавы с низким содержанием меди демонстрируют хорошую устойчивость к ряду солевых и щелочных растворов, а также к органическим химическим веществам. Различные медные сплавы привлекательны в промышленном отношении из-за простоты изготовления, тепло- и электропроводности, возможности соединения, формуемости, обрабатываемости, обрабатываемости, особых механических свойств и устойчивости к определенным химическим веществам и морской воде.
Различные медные сплавы привлекательны в промышленном отношении из-за простоты изготовления, тепло- и электропроводности, возможности соединения, формуемости, обрабатываемости, обрабатываемости, особых механических свойств и устойчивости к определенным химическим веществам и морской воде.
Тем не менее коррозия меди резко ускоряется в присутствии окисляющих кислот, солей тяжелых металлов, цианидов и/или серы, аммиака или их соединений. Коррозия также может увеличиваться в некоторых «купросольвентных» водах, как правило, богатых CO2, которые часто добываются из частных скважин. соединение медных сплавов с алюминием или сталью часто вызывает быструю и сильную гальваническую коррозию.
Сплав меди с цинком представляет собой латунь. Латуни (C 20500 – C 28580) имеют многочисленные промышленные применения, но они не лишены собственных проблем с коррозией. Латуни с низким содержанием цинка (менее 15%) и высоким содержанием меди демонстрируют почти такую же устойчивость к растворам на водной основе, что и нелегированная медь. Однако в латунях с высоким содержанием цинка такое воздействие может привести к обесцинковыванию латуни, что приведет к ухудшению качества сплава.
Однако в латунях с высоким содержанием цинка такое воздействие может привести к обесцинковыванию латуни, что приведет к ухудшению качества сплава.
В большинстве коррозионных сред на помощь приходят системы покрытий Steel-It®. Они образуют чрезвычайно прочный слой микроскопических чешуек из стали 316L, которые плотно прилегают к защищаемой поверхности. Металлическая конструкция, покрытая Steel-It, во многих практических целях становится практически неотличимой от нержавеющей стали (за исключением недостатков последней, таких как высокая стоимость и большой объем). С Steel-It превратите свою медь в нержавеющую сталь по цене краски! Пожалуйста, используйте нашу веб-форму для связи, чтобы точно узнать, как Steel-It решит вашу потребность в защите поверхностей из меди и медных сплавов от разрушения в результате коррозии.
Ингибитор коррозии медных труб: краска для наружных работ в сантехнической промышленности
Медные трубы использовались в сантехнической промышленности примерно в течение последних двух столетий. Сегодня медные трубы постепенно вытесняются пластиковыми. Однако медные водопроводные трубы все еще производятся и используются во всем мире. Важно отметить, что очень обширный массив устаревших медных труб остается на месте и с течением времени подвергается значительной и усиливающейся коррозии, что является постоянной и дорогостоящей проблемой. Большая часть этой коррозии происходит внутри труб, но большая часть возникает снаружи из-за сырости, пара, конденсата, присутствия химических веществ и т. д. Точечные утечки, вызванные как внутренней, так и внешней коррозией, могут нанести серьезный ущерб зданиям еще до того, как их обнаружат.
Сегодня медные трубы постепенно вытесняются пластиковыми. Однако медные водопроводные трубы все еще производятся и используются во всем мире. Важно отметить, что очень обширный массив устаревших медных труб остается на месте и с течением времени подвергается значительной и усиливающейся коррозии, что является постоянной и дорогостоящей проблемой. Большая часть этой коррозии происходит внутри труб, но большая часть возникает снаружи из-за сырости, пара, конденсата, присутствия химических веществ и т. д. Точечные утечки, вызванные как внутренней, так и внешней коррозией, могут нанести серьезный ущерб зданиям еще до того, как их обнаружат.
Продукты Steel-It имеют выдающийся послужной список в области замедления коррозии на всех видах металлических поверхностей, от медных водопроводных труб до промышленного оборудования. Во многих случаях правила требуют, чтобы трубы не имели видимых внешних дефектов — еще одна функция, которую Steel-It выполняет исключительно хорошо, придавая трубам чистый промышленный вид полированной нержавеющей стали.
Экологическая и пищевая безопасность красок Steel-It для медных сплавов
Недостатком меди, связанным с ее коррозионной активностью, является токсичность меди, когда она выщелачивается в вещества, используемые людьми, например в пищу. Защитная краска Steel-It герметизирует медный сплав под ней. Steel-It® безопасен для пищевых продуктов и одобрен Министерством сельского хозяйства США для случайного контакта с пищевыми продуктами. Кроме того, некоторые продукты Steel-It, которые подходят для защиты медных поверхностей, представляют собой покрытия с высоким содержанием твердых частиц и низким содержанием летучих органических соединений, которые соответствуют строгим экологическим стандартам и требованиям (включая требования штата Калифорния). Пожалуйста, свяжитесь с нами сейчас через веб-форму для получения дополнительной информации или для размещения заказа.
Вернуться к информации
Предотвратите потускнение духовых инструментов с помощью капсул против потускнения Zerust
В латуни есть что-то, что дает великолепный, богатый тембр – идеально подходит для музыкальных инструментов. Латунь — это цветной металл, то есть она не содержит железа и поэтому не ржавеет. Однако он состоит из цинка и меди, которые со временем могут тускнеть и подвергаться коррозии под воздействием кислорода и влаги. Хороший духовой инструмент может прослужить 100 и более лет, но только при правильном уходе. Лучший способ предотвратить потускнение латунных инструментов — содержать инструмент в чистоте и использовать капсулы против потускнения Zerust VCI. (VCI означает ингибитор паровой коррозии.)
Латунь — это цветной металл, то есть она не содержит железа и поэтому не ржавеет. Однако он состоит из цинка и меди, которые со временем могут тускнеть и подвергаться коррозии под воздействием кислорода и влаги. Хороший духовой инструмент может прослужить 100 и более лет, но только при правильном уходе. Лучший способ предотвратить потускнение латунных инструментов — содержать инструмент в чистоте и использовать капсулы против потускнения Zerust VCI. (VCI означает ингибитор паровой коррозии.)
Потускнение делает медные инструменты более тусклыми и даже может привести к ухудшению качества некоторых компонентов, что может снизить устойчивость звука. Перепродажная стоимость потускневшего музыкального инструмента часто значительно снижается. Повреждение отделки может быть ускорено воздействием масла и грязи на руки и лица. Вот почему многие музыканты так тщательно моют руки перед тем, как взяться за них.
Хотя Zerust исторически обслуживал больше механиков, чем музыкантов, в последние годы нам написали несколько музыкантов, которые рассказали нам, как наши паровые капсулы против потускнения помогли им защитить их ценные инструменты от потускнения, ржавчины и коррозии.
Надлежащее хранение медных духовых инструментов
Музыкальные магазины и мастера рекомендуют регулярную чистку как ключ к поддержанию блестящей золотой поверхности медных духовых инструментов и обеспечению их хорошего рабочего состояния. Тщательная очистка один раз в месяц, а то и после каждого использования, может замедлить или предотвратить потускнение медных инструментов. Однако одна только очистка не остановит потускнение полностью, если инструмент подвергается воздействию кислорода и влаги. Подготовка тубы, валторны или саксофона перед отправкой на хранение важна, но хранить их нужно правильно. (И да, мы знаем, что саксофоны технически являются деревянными духовыми инструментами, но на самом деле большинство из них сделаны из меди.)
Как указано в книге Медные духовые инструменты: покупка, техническое обслуживание, устранение неполадок и прочее Салли Вагнер и Дэвида Феддерли, правильное хранение духовых инструментов включает:
- Хранение в футляре, специально предназначенном для этого инструмента.

- Избегайте экстремальных температур (включая оставление инструмента в машине на ночь).
- Очистка прибора и его полное высыхание перед повторной сборкой для хранения. Некоторые музыканты предпочитают смазывать слайды и клапаны перед тем, как положить инструмент в футляр, в то время как другие не смазывают свои инструменты.
- Убедитесь, что внутри футляра для хранения нет резиновых, эластичных лент или латекса, так как они содержат серу, которая быстро потускнеет медные инструменты.
Почему капсулы Zerust Anti-Tarnish рекомендуются для хранения медных духовых инструментов
Как указано в Руководстве по консервации музыкальных инструментов Стюарда Полленса, некоторые футляры для хранения, демонстрации и переноски (а именно, сделанные из дерева, фанеры, ДСП, мазонит, картон, ткани, краски и клеи) могут содержать едкие пары, способные обесцветить инструменты из латуни, мельхиора и серебра. Герметичное хранение мешков, как правило, также не рекомендуется, потому что в случае сбоя климат-контроля внутри мешка может образоваться конденсат, что увеличивает вероятность потускнения.
Капсулы против потускнения Zerust гарантируют, что ваш инструмент не потускнеет, когда вы достанете его из хранилища. Капсулы недороги, нетоксичны, просты в использовании и обеспечивают защиту до одного года, если их поместить в закрытый футляр или место для хранения. Они имеют клейкую основу, поэтому их можно легко прикрепить к внутренней части ящиков, контейнеров, ящиков, сейфов и шкафов, и они могут предотвратить ржавчину латунных инструментов в радиусе двух футов от закрытого помещения. Для более крупного инструмента может потребоваться более одного.
Важно предпринять этот дополнительный шаг, чтобы предотвратить потускнение медных инструментов, особенно инструментов из желтой латуни и золотых медных инструментов. Они содержат больше цинка, чем меди, в отличие от розовой латуни, которая на 90 процентов состоит из меди и на 10 процентов из цинка. Цинк, как известно, подвергается коррозии и тускнеет намного быстрее, но он важен для качества звука инструмента. Вот почему желтые духовые инструменты известны своей яркой тональностью, в то время как золотые медные инструменты производят более широкий/глубокий звук, а резонанс розовых медных духовых инструментов мягче.
