Медь температура плавления: Температура плавления меди – при какой температуре плавится медь
Содержание
Как производится плавление меди
Одним из красивейших при декорировании материалом является медь. Однако осуществить плавление меди в мастерской довольно проблематично. Поэтому люди придумывают различные ухищрения и способы, чтоб осуществить плавление меди дома. Это связано с тем, что медь очень «благородно» смотрится, ее благородный внешний вид украсит любую поделку. Например, медные детали прекрасно украсят рукоятки ножей (охотничьих, так и бытовых), шкатулки, зажигалки, брелоки, дамские сумочки и кошельки и т.д. Однако, при изготовлении таких поделок дома, человек сталкивается с целым рядом проблем: начиная от вопроса «где достать металл?», заканчивая вопросом «как его расплавить?» и «как придать нужную форму элементу?». Где найти медь в быту, как осуществить плавление меди в бытовых условиях и как приготовить формы для заливки детали, будет рассказано ниже.
Медь: где ее достать
Все помнят из школьного курса химии то, что медь это 11 элемент таблицы Менделеева, с температурой плавления порядка 1083,5 градусов Цельсия. Но помимо всего прочего, медь не широко распространена в природе, поэтому на данный момент стоимость меди достигает 9000 долларов США за тонну (при этом исторический рекорд по цене – 12000 долларов за тонну в 2011 году). Высокая стоимость вызвана небольшим количеством месторождений. Основные месторождения меди находятся в Южной Америке (Чили и Перу), Казахстане, Китае, Австралии и США. Именно этим обоснована высокая стоимость чистого металла. Поэтому возникает вопрос: где достать медь в быту?
Но помимо всего прочего, медь не широко распространена в природе, поэтому на данный момент стоимость меди достигает 9000 долларов США за тонну (при этом исторический рекорд по цене – 12000 долларов за тонну в 2011 году). Высокая стоимость вызвана небольшим количеством месторождений. Основные месторождения меди находятся в Южной Америке (Чили и Перу), Казахстане, Китае, Австралии и США. Именно этим обоснована высокая стоимость чистого металла. Поэтому возникает вопрос: где достать медь в быту?
Общая схема выплавки меди.
Медь может находиться в электронике и электротехнических изделиях. Из меди изготавливают провода и кабели, обмотки для трансформаторов и электрических машин (электродвигателей и электрогенераторов), небольшое количество металла содержится в печатных платах.
Другие бытовые изделия – это радиаторы и нагреватели. В продаже имеются полотенцесушители, трубы, радиаторы (в том числе и автомобильные), которые выполнены из чистой меди. Их достаточно легко определить по желтому (специфическому) цвету материала и массе (медь довольно тяжела).
В продаже (на барахолках или в магазинах) можно встретить медные дверные ручки, столовые приборы, различные поделки и, естественно, монеты, гильзы от артиллерийских снарядов и от стрелкового оружия.
При этом количество металла в тех или иных элементах бывает недостаточно, поэтому многие люди смешивают металл из одного изделия с другим. Однако это неправильно, поскольку столовая медь является очищенной, а электротехническая или металл из труб токсичен, и не годиться для приготовления пищи (если конечное изделие планируется использовать на кухне).
График температуры плавления меди.
Другим вариантом получения меди является использование сплавов меди, таких как латунь или бронза. Так, латунью называют сплав меди и цинка в соотношении примерно 5 к 8 (на 5 частей меди 8 частей цинка). Из латуни изготавливают широкий спектр изделий, связанных с водопроводом: краны, вентиля, патрубки и т.д. Латунь может использоваться в смесителях. Из латуни также делают метизы (гайки, шайбы, болты), манометрические трубки и т. д. Обычно латунь имеет желтый или золотистый цвет, однако существуют сплавы и зеленого цвета. Ее температура плавления около 900 градусов Цельсия.
д. Обычно латунь имеет желтый или золотистый цвет, однако существуют сплавы и зеленого цвета. Ее температура плавления около 900 градусов Цельсия.
Бронзой называют сплав меди с оловом в соотношении 90% к 10%. Температура плавления бронзы составляет порядка 1000-1100 градусов Цельсия. В современном мире встретить изделия из бронзы довольно сложно, поскольку ее используют только для отливки украшений и элементов декора. Некоторые бронзовые сплавы применяются для изготовления смесителей.
Выплавить медь из деталей или из сплавов (латуни, бронзы) примерно одинаково по материальным затратам и по времени. Поэтому любая деталь, изготовленная из вышеперечисленных металлов годиться для плавки.
Вернуться к оглавлению
Организация рабочего места
Поскольку медь является тугоплавким металлом, то необходимо приобрести некоторое оборудование для ее плавления. Рассмотрим вариант плавки заготовки весом более 0,5 кг. Что для этого потребуется:
Цветовые характеристики сплавов меди.
- Первое, с чего следует начать – это постройка горна. Есть много способов построить горн своими руками. Его выкладывают из огнеупорных кирпичей полностью. При этом не следует гнаться за большим объемом плавильной камеры, для переплавки небольшого объема металла потребуется небольшой объем. Так объема в 0,5 кубометра хватить для переплавки 1 кг меди. Самый примитивный горн делается следующим образом: огнеупорными кирпичами (без раствора) складывается небольшая камера (для этого потребуется 25-30 кирпичей), в которую подводиться газ. При этом особое внимание стоит уделить системе подачи газа и горелке. Естественно, что такая конструкция не предназначена для большого количества плавок, однако на 2-3 плавки.
- Муфельная печь. Ею обзаводятся, если лень строить горн. Ее можно свободно приобрести у специализированных фирм. Для малого объема плавки в продаже имеются лабораторные муфельные печи. Стоит отметить, что приобрести готовую муфельную печь менее трудозатратно и не сильно дорого по сравнению с горном.
 Так стоимость материалов для самостоятельного строительства горна может составлять 70% от стоимости готового изделия.
Так стоимость материалов для самостоятельного строительства горна может составлять 70% от стоимости готового изделия. - Далее следует тигель и щипцы к нему. Тиглем называют емкость из тугоплавкого материала, в которой переноситься и плавиться металл. Тигель и щипцы для него рекомендуется купить (их свободно продают для лабораторных нужд).
- Бытовой пылесос или компрессор – для нагнетания воздуха в горн и печь. Реконструкторы могут построить кузнечные меха.
- Формы для заливки изделий. Их часто изготавливают (вырезают) из дерева или камня. Форма должна быть идентична желаемой детали.
- Крюк из стали. Подбирается по диаметру тигля. Крюк должен быть немного меньше диаметра.
- Расходные материала. Сюда относится топливо: дрова, кокс и газ.
Вернуться к оглавлению
Как производится плавка
После того, как все необходимое построено, собрано и проверено на работоспособность, можно осуществить плавление меди.
Сначала внутрь тигля укладываются детали и элементы, которые идут на переплавку. После чего тигель помещается внутрь муфельной печи. Далее задается необходимая температура плавки. При этом важно постоянно контролировать металл, чтобы он не сгорел и не выгорел. Для наблюдения в печи имеется смотровое окошко. При этом стоит помнить, что на поверхности металла может образовываться пленка окиси.
После чего тигель помещается внутрь муфельной печи. Далее задается необходимая температура плавки. При этом важно постоянно контролировать металл, чтобы он не сгорел и не выгорел. Для наблюдения в печи имеется смотровое окошко. При этом стоит помнить, что на поверхности металла может образовываться пленка окиси.
Когда температура в печи достигла выставленного значения, дверь печи открывают и при помощи щипцов достают тигель.
Плавка меди в тигле.
Далее следует отодвинуть окисную пленку стальной проволокой, после чего выливают расплавленную медь внутрь стоящей рядом формы. Важно, чтобы форма находилась недалеко от печи, чтобы не дать застыть металлу в процессе переноски. После заливки металлу дают время, чтобы остыть, после чего извлекают готовое изделие. Плавки с использованием муфельной печи очень удобны, требуют минимум вмешательства человека.
В случае, если печь отсутствует, медные детали можно переплавить в горне. Здесь в качестве топлива можно использовать древесные угли, каменные угли, кокс и другие виды топлива. Перед плавкой тигель с металлом устанавливается на слой угля и обкладывается углем. К горну приставляется компрессорная установка для нагнетания воздуха внутрь. В качестве компрессора отлично подойдут бытовые пылесосы, которые работают на выдув. Далее топливо поджигается, и запускается компрессорная установка. Главное отличие плавки в горне от муфельной печи заключается в постоянном участии в процессе плавки (топливо добавить, увеличить напор воздуха и т.д.). При этом стоит постоянно контролировать плавление металла. После того, как медь расплавилась, тигель вынимают щипцами, и металл заливают в форму.
Перед плавкой тигель с металлом устанавливается на слой угля и обкладывается углем. К горну приставляется компрессорная установка для нагнетания воздуха внутрь. В качестве компрессора отлично подойдут бытовые пылесосы, которые работают на выдув. Далее топливо поджигается, и запускается компрессорная установка. Главное отличие плавки в горне от муфельной печи заключается в постоянном участии в процессе плавки (топливо добавить, увеличить напор воздуха и т.д.). При этом стоит постоянно контролировать плавление металла. После того, как медь расплавилась, тигель вынимают щипцами, и металл заливают в форму.
Если объем меди для переплавки небольшой, то можно воспользоваться автогеном. Для этого струю пламени направляют от днища тигля вверх. При этом необходимо защитить металл от чрезмерного окисления. Для этого поверхность металла в тигле присыпают древесным углем (растолченным в пыль). После расплавления металла его также заливают в форму.Небольшие детали из сплавов меди (латунь и бронза) могут быть расплавлены на паяльной лампе.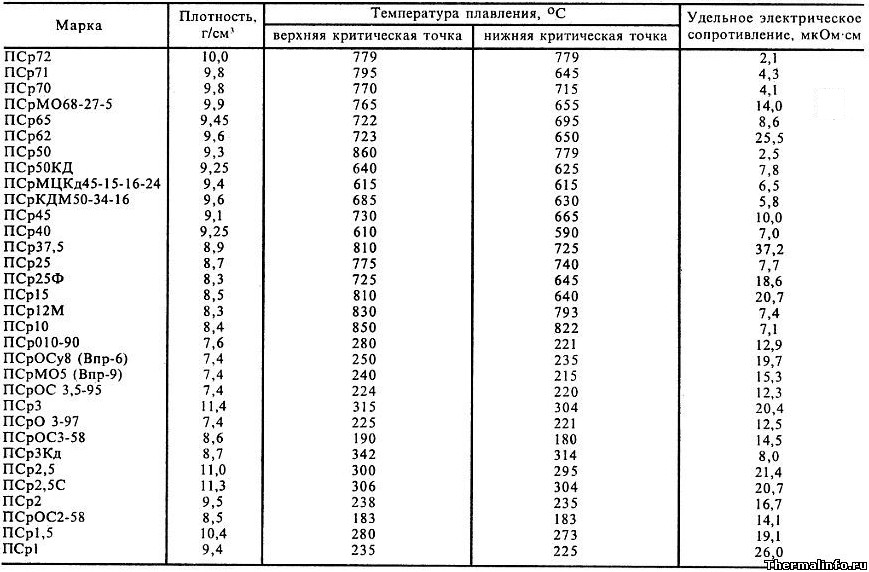
Вернуться к оглавлению
Заключение по теме
Если планируется регулярно осуществлять плавку меди, то настоятельно рекомендуется построить горн или купить муфельную печь.
Температура плавления меди
Историки предполагают, что первобытные люди находили медь в виде самородков, порой достигающих значительных размеров. Свое название на латинском языке медь (Cuprum) получила от острова Кипр, где ее добывали древние греки. Благодаря тому, что температура плавления меди не слишком высока и составляет 1083 °С, самородки или руду, содержащую медь, можно было плавить на костре. Это обеспечивало получение меди и позволяло использовать ее для изготовления оружия и предметов быта.
Несмотря на то, что медь широко применялась людьми еще с древних времен, по распространению в земной коре она занимает 23 место среди других элементов. Чаще всего она в природе встречается в виде соединений, входящих в состав сульфидных руд. Наиболее распространенные из них – медный блеск и медный колчедан.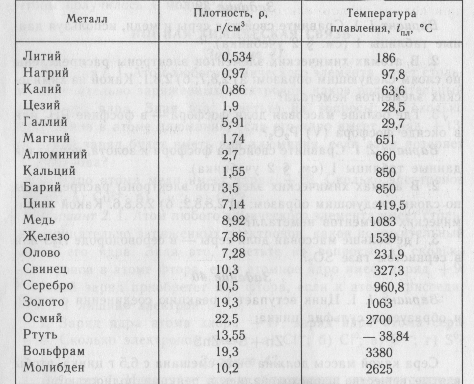 Существует несколько технологий получения меди из руды, причем по каждой из них процесс происходит в несколько этапов.
Существует несколько технологий получения меди из руды, причем по каждой из них процесс происходит в несколько этапов.
Как уже отмечалось, невысокая температура плавления меди позволяла успешно ее обрабатывать еще на самом начальном этапе развития цивилизации. И надо отдать должное древним металлургам, ими были найдены варианты получения и использования не только чистой меди, но и ее сплавов. Плавление – это переход металла из твердого состояния в жидкое. Для этого использовали нагрев, и низкая температура плавления меди позволяла успешно проводить подобную операцию.
Затем в жидкую медь добавляли олово или производили его восстановление из касситерита (руды, содержащей олово) на поверхности меди. В итоге получали бронзу, по прочности превосходящую Cuprum и применяемую для изготовления оружия. Однако сейчас хотелось бы остановиться более подробно на операции плавления, позволяющей получить достаточно чистый материал из руды.
Температура плавления у каждого металла своя и зависит от наличия примесей в составе исходного материала.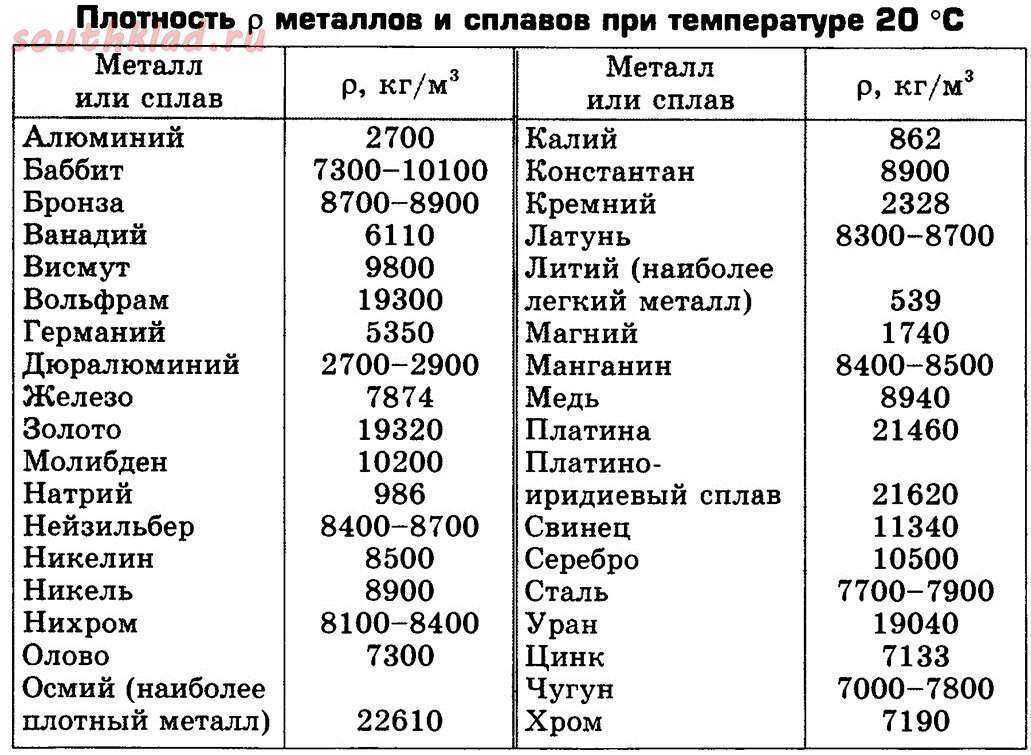 Так, медь, температура плавления которой составляет 1083 °С, после добавления олова образует бронзу, которая плавится при температуре 930-1140°С в зависимости от содержания олова. Латунь же, сплав меди и цинка, имеет температуру плавления 900-1050°С.
Так, медь, температура плавления которой составляет 1083 °С, после добавления олова образует бронзу, которая плавится при температуре 930-1140°С в зависимости от содержания олова. Латунь же, сплав меди и цинка, имеет температуру плавления 900-1050°С.
В процессе нагрева металла происходит разрушение кристаллической решетки. Первоначально, по мере нагрева, температура возрастает, а затем, начиная с некоторого значения, остается постоянной, хотя нагрев и продолжается. В этот момент и происходит плавление. Так продолжается в течение всего времени, пока весь металл не расплавится, и только потом температура начнет повышаться. Это справедливо для всех металлов, температура плавления меди также не изменяется.
При охлаждении картина обратная: сначала температура снижается до начала затвердевания металла, потом держится постоянной и после полного отвердения металла начинает опять понижаться. Такое поведение металла, если его изобразить на графике, называется фазовой диаграммой, показывающей, в каком состоянии находится вещество при конкретной температуре.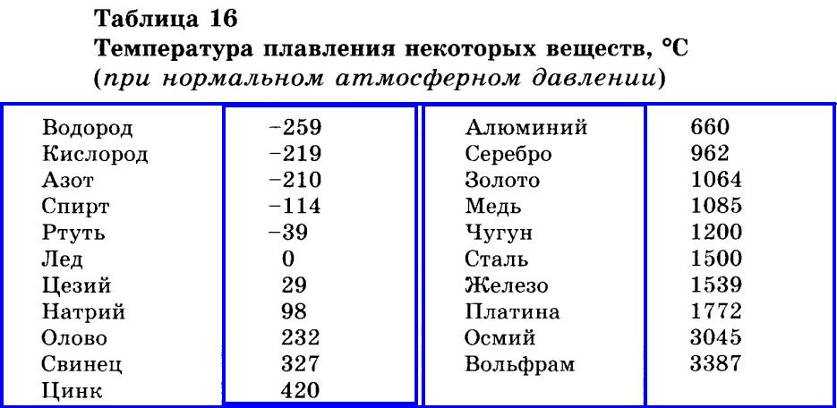 Для ученых фазовая диаграмма является одним из инструментов в изучении поведения металлов при плавлении.
Для ученых фазовая диаграмма является одним из инструментов в изучении поведения металлов при плавлении.
Если продолжить нагрев расплавленного металла, то при некоторой температуре начинается процесс, похожий на кипение. Так, температура кипения меди составляет 2560 °С. Это название процесс получил за внешнее сходство с кипением жидкости, когда из нее начинают выделяться пузырьки газа. То же самое происходит и с металлом, например, при достаточно высокой температуре из жидкого железа начинает выходить углерод, образующийся в ходе его окисления.
В статье рассмотрен процесс плавления металлов, описано понятие температуры плавления, ее поведение в процессе проведения плавки. Объясняется, какое влияние низкая температура плавления меди оказала на развитие цивилизации и металлургии.
Плавление и перекристаллизация наночастиц меди, полученных восстановлением в микроволновой печи в присутствии триэтилентетрамина
1. Хань З.Х., Ян Б., Ци Ю., Камингс Дж. Синтез легкоплавких металлических наночастиц методом ультразвуковой наноэмульсии . Ультразвук. 2011; 51: 485–488. doi: 10.1016/j.ultras.2010.11.015. [PubMed] [CrossRef] [Google Scholar]
Ультразвук. 2011; 51: 485–488. doi: 10.1016/j.ultras.2010.11.015. [PubMed] [CrossRef] [Google Scholar]
2. Zhang M., Efremov M., Schiettekatte F., Olson E.A., Kwan A.T., Lai S.L., Wisleder T., Greene J.E., Allen L.H. Снижение температуры плавления в зависимости от размера наноструктур: Нанокалориметрические измерения. физ. Ред. Б. 2000; 620:10548–10557. doi: 10.1103/PhysRevB.62.10548. [Перекрестная ссылка] [Академия Google]
3. Sun J., Wang W., Yue Q. Обзор основ взаимодействия микроволн с веществом и эффективных стратегий нагрева, связанных с микроволнами. Материалы. 2016;9:231. дои: 10.3390/ma9040231. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
4. Мишра Р.Р., Шарма А.К. Явления взаимодействия микроволн и материала: механизмы нагрева, проблемы и возможности в обработке материалов. Композиции Часть А. 2016; 81:78–97. doi: 10.1016/j.compositesa.2015.10.035. [Перекрестная ссылка] [Академия Google]
5. Figlarz M., Fievet F., Lagier J.P. Способ восстановления соединений металлов полиолами и металлические порошки, полученные этим способом. № 4 539 041. Патент США. 1985 г., 3 сентября;
№ 4 539 041. Патент США. 1985 г., 3 сентября;
6. Чоу Г.М., Шон П.Е., Курихара Л.К. Наноструктурированные металлические порошки и пленки в спиртовом растворителе. № 5 759 230. Патент США. 1998 г., 2 июня;
7. Курихара Л.К., Чоу Г.М., Шон П.Е. Нанокристаллические металлические порошки и пленки, полученные полиольным методом. НанаШучуед Матер. 1995;5:607–613. doi: 10.1016/0965-9773(95)00275-J. [CrossRef] [Google Scholar]
8. Чжу Х.Т., Линь Ю.С., Инь Ю.С. Новый одностадийный химический метод приготовления медных наножидкостей. J. Коллоидный интерфейс Sci. 2004; 277:100–103. doi: 10.1016/j.jcis.2004.04.026. [PubMed] [CrossRef] [Google Scholar]
9. Данг Т.М.Д., Ле Т.Т.Т., Блан Э.Ф., Данг М.К. Синтез и оптические свойства наночастиц меди, полученных методом химического восстановления. Доп. Нац. науч. Наноски. нанотехнологии. 2011; 2:1–6. дои: 10.1088/2043-6262/2/1/015009. [CrossRef] [Google Scholar]
10. Huang H.H., Yan F.Q., Kek Y.M., Chew C.H., Xu G. Q., Ji W., Oh P.S., Tang S.H. Синтез, характеристика и нелинейно-оптические свойства наночастиц меди. Ленгмюр. 1997; 13: 172–175. doi: 10.1021/la9605495. [CrossRef] [Google Scholar]
Q., Ji W., Oh P.S., Tang S.H. Синтез, характеристика и нелинейно-оптические свойства наночастиц меди. Ленгмюр. 1997; 13: 172–175. doi: 10.1021/la9605495. [CrossRef] [Google Scholar]
11. Аслам М., Гопакумар Г., Шоба Т.Л., Мулла И.С., Виджаямоханан К., Кулкарни С.К., Урбан Дж., Фогель В. Формирование наночастиц Cu и Cu 2 O с помощью изменение поверхностного лиганда: получение, структура и переход из изолирующего в металлический. J. Коллоидный интерфейс Sci. 2002;255:79–90. doi: 10.1006/jcis.2002.8558. [PubMed] [CrossRef] [Google Scholar]
12. Ещенко О.А., Дмитрук И.М. Размерозависимое плавление сферических наночастиц меди, внедренных в кремнеземную матрицу. физ. Ред. Б. 2007; 75:1–6. doi: 10.1103/PhysRevB.75.085434. [CrossRef] [Google Scholar]
13. Блоси М., Альбонетти С., Донди М., Мартелли С., Балди Г. Синтез полиолов наночастиц меди с помощью микроволн. Дж. Нанопарт. Рез. 2011; 13:127–138. doi: 10.1007/s11051-010-0010-7. [Перекрестная ссылка] [Академия Google]
14. Висуррага Дж.Д., Плессинг К.В., Даза С., Позо С., Бесерра А., Гарсия А. Исследование антибактериальных наночастиц меди, стабилизированных альгинатом, с помощью FT-IR и 2D-IR корреляционной спектроскопии. Междунар. Дж. Наномед. 2012;7:3597–3612. doi: 10.2147/IJN.S32648. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
Висуррага Дж.Д., Плессинг К.В., Даза С., Позо С., Бесерра А., Гарсия А. Исследование антибактериальных наночастиц меди, стабилизированных альгинатом, с помощью FT-IR и 2D-IR корреляционной спектроскопии. Междунар. Дж. Наномед. 2012;7:3597–3612. doi: 10.2147/IJN.S32648. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
15. Salzemann C., Lisiecki I., Urban J., Pileni M.P. Анизотропные нанокристаллы меди, синтезированные в пересыщенной среде: рост нанокристаллов. Ленгмюр. 2004; 20:11772–11777. дои: 10.1021/la0492862. [PubMed] [CrossRef] [Google Scholar]
16. Kawasaki H., Kosaka Y., Myoujin Y., Narushima T., Yonezawa T., Arakawa R. Синтез полиолов с помощью микроволнового излучения нанокристаллов меди без использования дополнительных защитные агенты. хим. коммун. 2011;47:7740–7742. doi: 10.1039/c1cc12346g. [PubMed] [CrossRef] [Google Scholar]
17. Кредер К.Дж., Мантирам А. Металлические нанопены с помощью легкого сольвотермического процесса с помощью микроволновой печи. хим. коммун. 2016; 53: 865–868. doi: 10.1039/C6CC08322F. [PubMed] [CrossRef] [Академия Google]
хим. коммун. 2016; 53: 865–868. doi: 10.1039/C6CC08322F. [PubMed] [CrossRef] [Академия Google]
18. Анзлвар А., Орел З.К., Зигон М. Оксид меди(I) и частицы металлической меди, образованные в 1,2-пропандиоле. Дж. Евр. Керам. соц. 2007; 27: 987–991. doi: 10.1016/j.jeurceramsoc.2006.04.131. [CrossRef] [Google Scholar]
19. Годселахи Т., Весаги М.А., Шафиехани А. Исследование поверхностного плазмонного резонанса наночастиц ядро–оболочка Cu@Cu 2 O методом теории Ми. Дж. Физ. Д заявл. физ. 2009; 42:1–6. doi: 10.1088/0022-3727/42/1/015308. [CrossRef] [Google Scholar]
20. Cottancin E., Celep G., Leré J., Pellarin M., Huntzinger J.R., Vialle J.L., Broyer M. Оптические свойства кластеров благородных металлов в зависимости от размера: сравнение между экспериментами и полуквантовой теорией. Теор. хим. Акк. 2006; 116: 514–523. doi: 10.1007/s00214-006-0089-1. [CrossRef] [Google Scholar]
21. Wei W., Lu Y., Chen W., Chen S. Однореакторный синтез, фотолюминесценция и электрокаталитические свойства кластеров меди субнанометрового размера. Варенье. хим. соц. 2011;133:2060–2063. doi: 10.1021/ja109303z. [PubMed] [CrossRef] [Google Scholar]
Варенье. хим. соц. 2011;133:2060–2063. doi: 10.1021/ja109303z. [PubMed] [CrossRef] [Google Scholar]
22. Видаль Н.В., Бланко М.С., Лопес-Кинтела М.А., Ривас Дж., Серра С. Электрохимический синтез очень стабильных фотолюминесцентных кластеров меди. Дж. Физ. хим. С. 2010; 114:15924–15930. дои: 10.1021/jp911380с. [CrossRef] [Google Scholar]
23. Васкес С., Банобре-Лопес М., Митра А., Лопес-Квинтела М.А., Ривас Дж. Синтез малых атомарных кластеров меди в микроэмульсиях. Ленгмюр. 2009; 25:8208–8216. doi: 10.1021/la
0w. [PubMed] [CrossRef] [Google Scholar]
24. Харам С.К., Махадешвар А.Р., Диксит С.Г. Синтез и характеристика наночастиц сульфида меди в микроэмульсиях Triton-X 100 вода-в-масле. Дж. Физ. хим. 1996; 100: 5868–5873. doi: 10.1021/jp952391n. [Перекрестная ссылка] [Академия Google]
25. Лисецкий И., Пилени М.П. Синтез металлических кластеров меди с использованием обратных мицелл в качестве микрореакторов. Варенье. хим. соц. 1993; 115:3887–3896. doi: 10.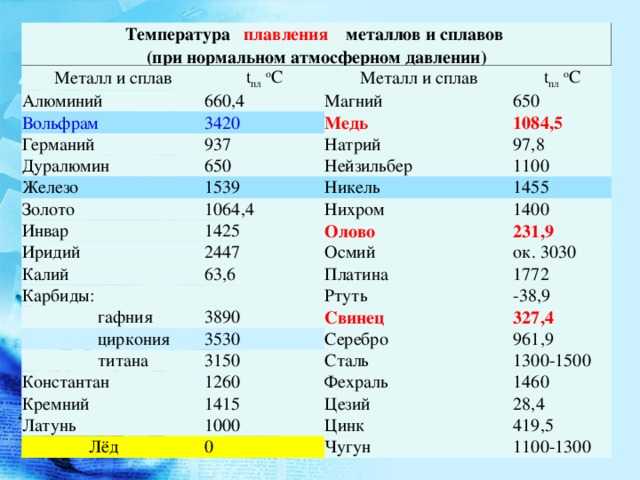 1021/ja00063a006. [CrossRef] [Google Scholar]
1021/ja00063a006. [CrossRef] [Google Scholar]
26. Пилени М.П., Лисецкий И. Синтез нанометровых частиц металлической меди в обратных мицеллах. Коллоидный прибой. Физикохим. англ. Асп. 1993; 80: 63–68. doi: 10.1016/0927-7757(93)80224-3. [CrossRef] [Google Scholar]
27. Балог Л., Томалия Д.А. Нанокомпозиты на основе поли(амидоаминовых) дендримеров. 1. Синтез нанокластеров нульвалентной меди. Варенье. хим. соц. 1998;120:7355–7356. doi: 10.1021/ja980861w. [CrossRef] [Google Scholar]
28. Ohde H., Hunt F., Wai C.M. Синтез наночастиц серебра и меди в микроэмульсии вода-в-сверхкритическом диоксиде углерода. хим. Матер. 2001; 13:4130–4135. doi: 10.1021/cm010030g. [CrossRef] [Google Scholar]
29. Cheon J.M., Lee J.H., Song Y., Kim J. Синтез наночастиц Ag методом электролиза и применение в струйной печати. Коллоидный прибой. Физикохим. англ. Асп. 2011; 389: 175–179. doi: 10.1016/j.colsurfa.2011.08.032. [CrossRef] [Google Scholar]
30. Кумар Р.В., Мастай Ю. , Диамант Ю., Геданкен А. Сонохимический синтез аморфной меди и нанокристаллической меди 2 O, встроенной в полианилиновую матрицу. Дж. Матер. хим. 2001; 11:1209–1213. doi: 10.1039/b005769j. [CrossRef] [Google Scholar]
, Диамант Ю., Геданкен А. Сонохимический синтез аморфной меди и нанокристаллической меди 2 O, встроенной в полианилиновую матрицу. Дж. Матер. хим. 2001; 11:1209–1213. doi: 10.1039/b005769j. [CrossRef] [Google Scholar]
31. Ценг П.Х., Ван Ю.З., Се Т.Х., Хо К.С., Цай Ч.Х., Чен К.Т. Получение наночастиц меди малого размера с помощью микроволнового облучения в присутствии триэтилентетрамина. Нанотехнологии. 2018;29:085603. doi: 10.1088/1361-6528/aaa35e. [PubMed] [CrossRef] [Google Scholar]
32. Шмид Г., Корейн Б.Е. Наночастицы золота: синтезы, структуры, электроника и реактивность. Евро. Дж. Неорг. хим. 2003; 2003: 3081–3098. doi: 10.1002/ejic.200300187. [CrossRef] [Google Scholar]
33. Castro T., Reifenberger R., Choi E., Andres R.P. Температура плавления отдельных нанометровых металлических кластеров в зависимости от размера. физ. Ред. Б. 1990; 13:8548–8556. doi: 10.1103/PhysRevB.42.8548. [PubMed] [CrossRef] [Академия Google]
34. Сиснерос Р., Рамирес С. , Ван С.-М. Эллипсометрия и неэмпирические подходы к показателю преломления пористого кремния. Дж. Физ. Конденс. Иметь значение. 2007;19:395015. doi: 10.1088/0953-8984/19/39/395010. [CrossRef] [Google Scholar]
, Ван С.-М. Эллипсометрия и неэмпирические подходы к показателю преломления пористого кремния. Дж. Физ. Конденс. Иметь значение. 2007;19:395015. doi: 10.1088/0953-8984/19/39/395010. [CrossRef] [Google Scholar]
35. Зола А.С., Рибейро Р.У., Буэно Дж.М.С., Занчет Д., Арройо П.А. Наночастицы кобальта получены тремя различными способами. Дж. Эксп. Наноски. 2014; 9: 398–405. doi: 10.1080/17458080.2012.662723. [CrossRef] [Google Scholar]
36. Kelton K.F., Lee G.W., Gangopadhyay A.K., Hyers R.W., Rathz T.J., Rogers J.R., Robinson M.B., Robinson D.S. икосаэдрический порядок на барьере зародышеобразования. физ. Преподобный Летт. 2003;90:19550. doi: 10.1103/PhysRevLett.90.195504. [PubMed] [CrossRef] [Google Scholar]
37. Мэй К.С., Лу К. Плавление и перегрев кристаллических твердых тел: от объема к нанокристаллам. прог. Матер. науч. 2007; 52:1175–1262. doi: 10.1016/j.pmatsci.2007.01.001. [CrossRef] [Google Scholar]
38. Dash J.G. История поиска непрерывной плавки. Преподобный Мод. физ. 1999; 71: 1737–1743. doi: 10.1103/RevModPhys.71.1737. [CrossRef] [Google Scholar]
физ. 1999; 71: 1737–1743. doi: 10.1103/RevModPhys.71.1737. [CrossRef] [Google Scholar]
39. Шидпур Р., Делавари Х.Х., Воссуги М. Аналитическая модель, основанная на энергии когезии, для определения краевых и угловых эффектов на температуру плавления металлических наночастиц. хим. физ. 2010; 378:14–18. doi: 10.1016/j.chemphys.2010.09.007. [CrossRef] [Google Scholar]
40. Qi W.H., Huang B.Y., Wang M.P., Li Z., Yu Z.M. Обобщенная модель энергии связи для энергии когезии малых металлических частиц. физ. лат. А. 2007; 370: 494–498. doi: 10.1016/j.physleta.2007.06.062. [CrossRef] [Google Scholar]
41. Шандиз М.А., Сафаеи А., Санджаби С., Барбер З.Х. Моделирование энергии когезии и температуры плавления наночастиц по их среднему координационному числу. Твердотельный коммун. 2008; 145:432–437. doi: 10.1016/j.ssc.2007.12.021. [Перекрестная ссылка] [Академия Google]
42. Chakravarty C., Debenedetti P.G., Stillinger F.H. Lindemann измеряет фазовый переход твердое тело-жидкость. Дж. Хим. физ. 2007;126:204508. дои: 10.1063/1.2737054. [PubMed] [CrossRef] [Google Scholar]
Дж. Хим. физ. 2007;126:204508. дои: 10.1063/1.2737054. [PubMed] [CrossRef] [Google Scholar]
43. Полинг Л. Так называемые икосаэдрические и декагональные квазикристаллы являются двойниками кубического кристалла из 820 атомов. физ. Преподобный Летт. 1987; 58: 365–368. doi: 10.1103/PhysRevLett.58.365. [PubMed] [CrossRef] [Google Scholar]
44. Фраундорф П., Бишоп К. Эффективное обнаружение икосаэдрических близнецов с помощью изображения решетки. микроск. Микроанал. 2013;19: 1804–1805. doi: 10.1017/S143192761301101X. [CrossRef] [Google Scholar]
45. Цзян М.Л., Цзэн К., Чжан Т.Т., Ян М.Л., Джексон К.А. Переход медных кластеров из икосаэдрической в двойно-икосаэдрическую форму. Дж. Хим. физ. 2012;136:104501. doi: 10.1063/1.3689442. [PubMed] [CrossRef] [Google Scholar]
Какова температура плавления меди? – Wazeesupperclub.com
Какова температура плавления меди?
1 984 °F (1 085 °C) Медь / точка плавления
Это сплав Pb и Sn с низкой температурой плавления?
Сплав Pb-Sn с уникальным составом, называемым эвтектическим составом (самый низкоплавкий состав), ниже температуры плавления каждого из отдельных металлов, встречается при ~62% Sn в системе сплава Pb-Sn и имеет самая низкая температура плавления 183°C при этом эвтектическом составе.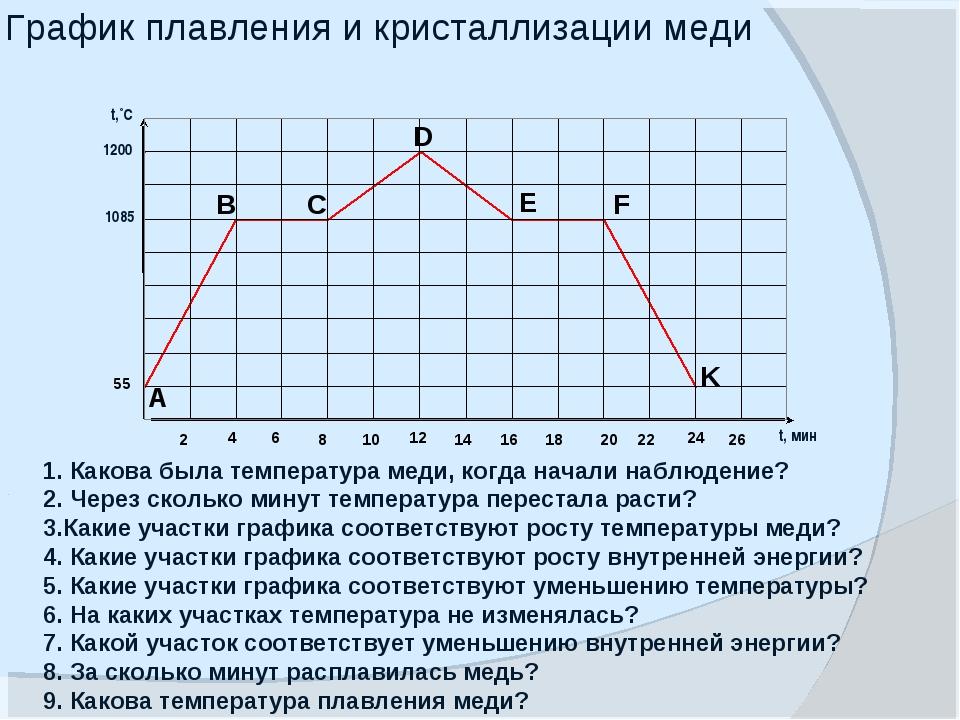
При какой температуре плавятся медь и олово?
Температура плавления обычных металлов Латунь: 930°C (1710°F) Алюминий Бронза*: 1027-1038°C (1881-1900°F) Хром: 1860°C (3380°F) Медь: 1084°C (1983°F)
Что такое плавление температура свинца?
621,5°F (327,5°C) Свинец / точка плавления
Как плавить медь?
Если вы плавите небольшое количество меди, вы можете сделать это с помощью паяльной лампы или на плите. Вы можете использовать его для домашних поделок или переплавить в слитки для хранения. Медь быстро проводит тепло и электричество, поэтому следует проявлять большую осторожность, если вы пытаетесь расплавить медь в домашних условиях.
Какой металл плавится при 95 градусах?
Температуры плавления металлов и чистых элементов
| Атомный # | Элемент | Температура плавления (°С) |
|---|---|---|
| 95 | Америций | 1176 °С |
| 51 | Сурьма | 630,63 °С |
| 18 | Аргон | -189,35 °С |
| 33 | Мышьяк | 817 °С |
Почему SN имеет более низкую температуру плавления, чем Pb?
Температуры плавления и температуры кипения Тенденции отражают растущую слабость ковалентных или металлических связей по мере того, как атомы становятся больше, а связи становятся длиннее. Низкое значение температуры плавления олова по сравнению со свинцом, по-видимому, связано с тем, что олово образует искаженную 12-координационную структуру, а не чистую.
Низкое значение температуры плавления олова по сравнению со свинцом, по-видимому, связано с тем, что олово образует искаженную 12-координационную структуру, а не чистую.
Какова температура кипения Sn?
4 716°F (2 602°C)Олово / точка кипения
При каких температурах плавятся металлы?
Температура плавления металлов и сплавов
| Металл | Точка плавления | |
|---|---|---|
| (оС) | (оф) | |
| Углеродистая сталь | 1425 – 1540 | 2600 – 2800 |
| Нержавеющая сталь | 1510 | 2750 |
| Тантал | 2980 | 5400 |
Расплавится ли медь в огне?
Медь плавится почти при 2000 градусов по Фаренгейту. Костер разогревается примерно до 1100 градусов по Фаренгейту. Чтобы достичь температуры, при которой плавится медь, вам нужно увеличить скорость горения. Один из способов сделать это — переместить огонь в камеру сгорания, а затем вдуть в камеру воздух.
