Питтинговая коррозия: Питтинг – суть процесса, методы борьбы с питтинговой коррозией стали
Содержание
Питтинговая коррозия — что это? Распространение, особенности и методы защиты
Виды коррозии достаточно обширны и разнообразны, у каждого свои причины и последствия. Одним из распространенных проявлений коррозии является питтинговая коррозия или, как ее еще называют, точечная коррозия.
Коррозийному разрушению подвергаются практически все металлы, какие-то более восприимчивы, а какие-то нет. Сегодня в мире существуют технологии, которые помогают замедлить процессы разрушения, происходящие с элементами, но не избавить от них полностью.
Питтинговая коррозия – это непредсказуемый и наиболее опасный вид процессов коррозийного разрушения.
Особенности питтинговой коррозии
Внешнее проявление точечной коррозии – это точечные язвы буро-рыжего цвета.
Отличительными чертами данного вида разрушения является то, что она возникает и распространяется в верхних слоях элемента, поражает участки ранее полученных дефектов, также питтинг обычно распространяется в слоях верхнего антикоррозийного покрытия.
Точечной коррозии металла подвергаются в большей степени пассивные металлы, к которым относится: медь, сурьма, ртуть, платина, также часто питтинг наблюдается на алюминии, никеле, цинке. Поэтому все изделия из данных материалов подвержены такому виду разрушения (микросхемы, агрегаты, сплавы этих металлов и др.).
Факторы, влияющие на образование питтинга на поверхности металлических материалов:
- Перепады температур или постоянное действие повышенных температур.
- Плохо обработанная поверхность (шероховатости, потертости, рыхлости и т.д.).
- Действие кислотных сред.
- Действие веществ с примесями соли.
Классификация точечных повреждений
По размеру бывают:
- Микропиттинги величиной до 0,1 мм;
- Обычные размером до 1 мм;
- Язвенный питтинг имеет размеры более 1 мм.
Также различают открытые, закрытые и поверхностные точечные язвы.
В открытом виде ржавые пятна хорошо просматриваются на поверхности материала, достаточно человеческого зрения. Если язвенных образований слишком много, то в процессе своего распространения они сливаются в одну сплошную диффузную составляющую. Закрытый вид питтинга самый опасный, так как его невозможно рассмотреть с внешней стороны, так как они увеличиваются не наружу, а вглубь материала изделия. Такие язвы могут быть найдены только с использование специальных просвечивающих приборов.
Если язвенных образований слишком много, то в процессе своего распространения они сливаются в одну сплошную диффузную составляющую. Закрытый вид питтинга самый опасный, так как его невозможно рассмотреть с внешней стороны, так как они увеличиваются не наружу, а вглубь материала изделия. Такие язвы могут быть найдены только с использование специальных просвечивающих приборов.
Поверхностный питтинг встречается наиболее редко, разрушение происходит не вглубь или наружу элемента, а вширь, что способствует образованию не просто точек, а выбоин на поверхности элемента.
Питтинговая коррозия — причины образования
Интенсивное образование ржавчины происходит при контакте металлического изделия с солеными растворами и различными химически агрессивными средами.
Нужно понимать, что питтинговая коррозия это точечные язвы там, где происходило нарушение технологий производства, механические повреждения, приводящие к микроскопическим дефектам. Если сплав был произведен с нарушением технологии, то в нем могут быть инородные включения, поры, которые нарушают работу изделия.
Если сплав был произведен с нарушением технологии, то в нем могут быть инородные включения, поры, которые нарушают работу изделия.
Важной причиной появления питтингов можно назвать среду, в которой эксплуатируется материал. При частых динамических воздействиях, нарушается структурная целостность зерен металла, что приводит, к внутренним разрушениям и распространению коррозийных процессов.
Проявление точечных язв
Чтобы более полно понимать, что такое питтинговая коррозия, необходимо разобрать процесс ее появления и развития:
- Начальная стадия или зарождение – отмечалось выше, что питтинги образуются в местах ранее полученных дефектов в виде трещин, сколов, рыхлостей от удара и т.п. Также на поверхности металла существует естественная защитная пленка, от воздействия факторов окружающей среды, она может истончаться или пропадать вовсе, что содействует более быстрому процессу разрушения.
- Процесс роста – рост происходит вследствие электрохимических реакций и полного растворения защитной оксидной пленки.

- С момента зарождения коррозия в определенном месте развивается очень быстро, но со временем ее распространение замедляется и все больше углубляется внутрь материала элемента для полного разрушения металлической решетки.
Имеются случаи, когда питтинг не развивается, а наоборот происходит его замедление – процесс репассивации. Но это может произойти только на ранних этапах развития ржавчины.
Формы питтингового повреждения
Если рассматривать питтинг более тщательно, то можно обратить внимание, что одни точки имеют правильную округлую форму, другие могут быть: многогранниками, объединенными многогранниками, пирамидальные, призматические. В некоторых многогранников наблюдается блестящее дно язвы.
Форма питинговой коррозии металлов будет напрямую зависеть от формы частиц кристаллической решетки, так как продукты разрушения повреждают именно кристаллическую решетку материала, и образуются пустоты.
По форме точечных язв на изделии, можно понять, из какого именно металла оно сделано.
Методы защиты металлов и сплавов от коррозии
Защита металлов и сплавов от питтинговой коррозии:
- Электрохимическая защита. Этот вид защиты часто применяется вместе с применением ингибиторов.
- Так как наиболее подвержены питтинговым образованиям пассивные сплавы, то наилучшим решением будет минимизировать их величину в составе сплавов или совсем заменить на другой, более устойчивый к разрушению материал.
Существуют вещества, введение которых в сплав, повышает его антикоррозийную стойкость (например, кремний и хром).
- Применение ингибиторов, которые в замкнутой системе подавляют или задерживают развитие разрушающих процессов, вследствие химических и физико-химических воздействий (вещества на сульфатной основе, щелочи, нитраты).
- Нанесения защитного антикоррозийного покрытия на предварительно очищенную и подготовленную поверхность элемента.

Важно понимать, что представленные методы борьбы с точечной коррозией металла возможны только на производстве или на начальном этапе создания сплава для конструкции или детали.
Таким образом, наличие питтингов не ставит крест на работоспособности конструкции, если они были замечены вовремя. Стоит всегда тщательно следить за состоянием изделий, включенных в работ, во время проводить технические обследования и не скупиться на качественную антикоррозийную защиту для металлов.
Питтинговая коррозия металлов — причины и этапы образования
Многие считают, что любой металл можно защитить с помощью специального оксидного покрытия, которое будет препятствовать возникновению коррозии. Однако существует особый тип коррозии под названием питтинг, который затрагивает металлы с защитным покрытием. В большинстве случаев питтинговая коррозия затрагивает лишь верхний оксидный слой металла, а вглубь проникает достаточно медленно.
Но как именно возникает питтинг-ржавчина? Правда ли то, что существует коррозия нержавеющих сталей? Ниже мы узнаем ответы на эти вопросы.
Что такое питтинговая коррозия?
Питтинговая коррозия — такая разновидность, при которой на поверхности металла образуются так называемые питтинги.
Подобная коррозия затрагивает железные сплавы, медные, алюминиевые, на основе хрома и так далее. Питтинговая коррозия возможна даже на нержавеющей стали.
Питтинг обычно затрагивает различные металлоконструкции, которые контактируют с соленой водой (обычно это различные прибрежные участки). Связано это с тем, что для запуска реакции питтинга нужен избыток так называемых ионов-активаторов, которые будут вытеснять кислород из оксидной защитной пленки — а подобные вещества в обильных количествах содержатся именно в воде.
Обратите внимание, что сперва питтинг обычно затрагивает внешние слои оксидной пленки металла, однако по мере распространения ржавчины он может захватывать весь металл целиком. Питтинговая коррозия нержавеющих сталей возникает обычно в случае комбинации сразу нескольких факторов.
Питтинговая коррозия нержавеющих сталей возникает обычно в случае комбинации сразу нескольких факторов.
Причины
Основные причины появления питтинг-коррозии:
Механическая деформация
Это может быть вмятина, царапина, растрескивание в области удара и прочее. Этот фактор является ключевым, поскольку на многих металлических сплавах на поверхности есть достаточно тонкий защитный слой, который предотвращает коррозию. Соответственно при повреждении этого слоя металл становится беззащитным перед ржавчиной.
Неоднородность структуры
Этот фактор тоже является очень важным, поскольку неоднородности часто создают небольшие очаги, где со временем заводится ржавчина. Неопытному инженеру может показаться, что этот фактор опасен только для низкокачественного металла и стали, однако это не совсем так.
Действительно, низкокачественные сплавы имеют неоднородную структуру и ржавеют значительно чаще, однако неоднородная структура может появиться также у обработанных деталей, на которые забыли нанести защитное покрытие. Простой пример: при сверлении отверстия была нарушена целостность внешней антикоррозийной пленки — это привело к появлению ржавчины.
Простой пример: при сверлении отверстия была нарушена целостность внешней антикоррозийной пленки — это привело к появлению ржавчины.
Высокая шероховатость поверхности
Если поверхность какого-либо объект является очень шероховатой, то в таком случае на ней вряд ли сможет удержаться антикоррозийное покрытие. Поэтому появление на такой поверхности ржавчины — лишь дело времени.
Также обратите внимание, что здесь действует одно простое правило — чем более шероховатая поверхность будет у металла, тем скорее она начнет покрываться питтинг-коррозией. Однородный гладкий металл обладает большой устойчивостью к коррозии.
Агрессивные среды
Контакт с агрессивными средами (кислоты, вода с большим содержанием солей, щелочи и так далее). Агрессивные среды также могут повреждать внешний антикоррозийный слой, что со временем приведет к образованию питтинга.
Обратите внимание, что разные вещества влияют на металл по-разному — если морская вода при краткосрочном контакте не наносит каких-либо повреждений, то при контакте с сильными кислотами повреждение стали может возникнуть моментально. Поэтому нужно соблюдать правила хранения и обработки металлов.
Поэтому нужно соблюдать правила хранения и обработки металлов.
Как защитить металл
Мы рассмотрели вопрос о том, из-за чего возникает питтинговая коррозия. При понимании особенности такого процесса, можно будет определить, как с ней бороться и обеспечить процесс защиты.
Чтобы бороться с такой проблемой, можно будет использовать процесс пассивации.
Он основан на применении специального раствора, в состав которого входят две кислоты – лимонная и азотная. Также для сильного усиления процесса, можно использовать добавки.
Цель, которая ставится при применении пассивации, процесс коррозии может стать медленнее или же прекратиться.
Есть 3 метода, позволяющие защититься от причин возникновения питтинговой коррозии.
К ним относятся:
- Устранение дефектов. Использование современных методов позволяет устранить большинство видов дефектов, которые могут появляться на металле. Применяется полировка, а также другие средства для исправления неровностей.
 Это уменьшает опасность развития коррозии.
Это уменьшает опасность развития коррозии. - Полировка. Помогает устранить шероховатости. Это не позволяет продуктам коррозии скапливаться. На гладком металле могут появиться естественные защитные пленки.
- Использование хромированного покрытия. Оно позволяет оградить материал от контакта с агрессивными средами. Используется цинкование – именно такой подход помогает улучшить общее качество защиты.
Наша компания всегда готова создать защиту от повреждений любых видов металлоконструкций и стальных изделий.
Этапы образования питтинговой коррозии
Главной опасностью питтинг-коррозии является быстрое распространение. Дело все в том, что по мере образования ржавчины разрушается внешний защитный слой, поэтому питтинг-коррозию не удается локализовать на каком-либо участке.
Дело все в том, что по мере образования ржавчины разрушается внешний защитный слой, поэтому питтинг-коррозию не удается локализовать на каком-либо участке.
Даже самый маленький питтинг-фрагмент растет и увеличивается в размерах, а при отсутствии своевременной обработки коррозия очень быстро захватывает весь металл целиком, что делает его бесполезным и даже опасным (скажем, когда речь идет о навесной металлической конструкции).
Питтинговая коррозия по металлу распространяется в несколько этапов:
- Питтинг возникает в местах с поврежденным антикоррозийным покрытием (царапины, трещины, вмятины и так далее), а также в случае неоднородной структуры металла. Еще одна локализация — это обработанный металл, на который по какой-либо причине не нанесли защитное покрытие.
- На химическом уровне питтинг происходит следующим образом: ионы-активаторы под действием электрохимических сил вытесняют кислород из оксидной пленки, которой покрыт металлический лист или изделие.
 Это приводит к постепенному разрушению внешнего слоя металла с образованием характерных язв и пятен коричневато-рыжего цвета.
Это приводит к постепенному разрушению внешнего слоя металла с образованием характерных язв и пятен коричневато-рыжего цвета. - По мере разрушения оксидной пленки ржавчина захватывает все новые участки поверхности металлического объекта, что приводит к ухудшению его физических свойств (теряется плотность, твердость, прочность и так далее). Реакция окисления идет по электрохимическому сценарию за счет вытеснения кислорода из оксидной пленки.
- После полного уничтожения оксидной пленки питтинг начинает проникать вглубь металлического сплава — наступает так называемый диффузный этап. Скорость протекания диффузного питтинга достаточно низкая, а полное ржавление может занять большое количество времени.
Обратите внимание, что иногда может происходить самопроизвольная пассивация металла, что приводит к замедлению образования ржавчины. На практике подобный сценарий встречается достаточно редко, хотя подобные случаи и встречаются. Обратите внимание, что в случае перехода питтинга на диффузный этап пассивация невозможна по физическим причинам.
Подробности
Причины появления
Предлагаем рассмотреть основные причины питтинговой точечной коррозии.
- Деформация механического характера
Это может быть царапина, вмятина, растрескивание в области удара, а также другое. Этот фактор будет ключевым, потому что на большинстве металлических сплавов на поверхность есть весьма тонкий, но все-таки слой защиты, который способствует предотвращению коррозии. Естественно, что при повреждении такого слоя металл будет становиться незащищенным перед ржавчиной.
- Структурная неоднородность
Такой фактор тоже является крайне важным, потому что неоднородности часто будут создавать небольшие по размеру очаги, где спустя время начнет появляться ржавчина. Неопытные инженеры могут подумать, что такой фактор будет опасным лишь для металла и стали низкого качества, но это вовсе не так. Действительно, сплавы низкого качества будут иметь неоднородную структуру и ржавеют намного чаще, но еще структурная неоднородность может появиться и у деталей, которые обработаны, на которые забыли нанести покрытие с защитой. Простой пример – во время сверления отверстия будет нарушена целостность внешней пленки против коррозии – это будет привлекать внимание к появлению повреждений.
Простой пример – во время сверления отверстия будет нарушена целостность внешней пленки против коррозии – это будет привлекать внимание к появлению повреждений.
- Высокая степень шероховатости
Если поверхность объекта из металла является весьма шероховатой, то в подобном случае на ней вряд ли будет удерживаться особое антикоррозийное покрытие. По этой причине появление на подобной поверхности коррозии, но это лишь вопрос времени. Еще обращайте внимание на то, что тут будет действовать одно правило – чем больше шероховатость поверхности металла, тем скорее она станет покрываться коррозией. Гладкий однородный металл будет обладать прекрасной устойчивостью к ржавчине.
- Агрессивная среда
Не поверите, но может случиться даже точечная коррозия нержавеющей стали, если будет контакт с агрессивными средами (кислоты, воды с огромным содержанием солей, щелочей и прочего). Агрессивные среды тоже могут повредить внешний антикоррозийный слой, а это спустя время может привести к появлению питтинга. Также обратите внимание, что различные вещества будут влиять на металл разными способами – если морская вода при не долгосрочном контакте не будет наносить какие-либо повреждения, а вот при контакте с сильными кислотами могут появиться сильные повреждения. По этой причине следует соблюдать правила хранения и обработку металла.
Также обратите внимание, что различные вещества будут влиять на металл разными способами – если морская вода при не долгосрочном контакте не будет наносить какие-либо повреждения, а вот при контакте с сильными кислотами могут появиться сильные повреждения. По этой причине следует соблюдать правила хранения и обработку металла.
Этапы появления точечной коррозии
Основной опасностью такой коррозии будет быстрое распространение. Все дело заключается в том, что по мере появления ржавчины будет разрушаться защитный внешний слой, и поэтому такую коррозию не удастся локализовать на определенном участке. Даже самые малые по размеру фрагменты растут и увеличиваются в размере, а при отсутствии своевременной обработки коррозия очень быстро станет целиком захватывать металл, что сделает его бесполезным и в какой-то мере опасным (к примеру, когда идет речь о навесной конструкции из металла).
Такая коррозия по металлу станет распространяться в несколько этапов:
- Точечная ржавчина начинает появляться в местах, где повреждено антикоррозийное покрытие (трещины, царапины, вмятины и прочее), а еще при неоднородной металлической структуре.
 Еще одной локализацией будет обработанный металл, на который по каким-то причинам не успели нанести защитное покрытие.
Еще одной локализацией будет обработанный металл, на который по каким-то причинам не успели нанести защитное покрытие. - На химическом уровне это будет происходить так – ионы-активаторы под воздействием электрохимической силы станут вытеснять кислород из оксидной пленки, которой покрыт лист металла или изделие. Это приведет к постепенному разрушению внешнего покрытия металла с появлением характерных язв и пятен рыжевато-коричневого цвета.
- По мере того, как будет разрушаться оксидная пленка, ржавчина станет захватывать новые участки поверхности объекта из металла, то это может привести к ухудшению свойств физического характера (теряется твердость/плотность/прочность и прочее). Реакция окисления будет идти по электрохимическому сценарию благодаря вытеснению кислорода из пленки оксида.
- После всецелого уничтожения оксидной пленки питтинг начнет проникать внутрь металлического сплава – и тогда наступит диффузный этап. Скорость протекания такого процесса будет достаточно низкой, а полное ржавление может занимать огромное количество времени.

Стоит обратить внимание на то, что иногда будет происходить пассивация металла самопроизвольного типа, что приведет к замедлению появления ржавчины. На практике такой сценарий встречается весьма редко, хотя подобные случаи можно встретить на практике. Стоит обратить внимание на то, что в случае перехода точечной коррозии на диффузный этап пассивация не будет возможна по физическим причинам.
Классификация
Есть несколько видов питтинга:
Поверхностный. При подобном сценарии ржавчина начнет затрагивать исключительно верхнюю металлическую поверхность. Еще она будет распространяться в виде небольших и тоненьких линий с диаметром от 0.1 до 0.3 см. Поверхностная ржавчина на первоначальном этапе обычно будет захватывать углы, но спустя время она начнет распространяться в горизонтальном направлении по всей поверхности элемента из металла.
- Открытый. При подобном сценарии коррозии начнет появляться в виде частых больших точек, причем их диаметр будет составлять от 0.
 2 до 0.5 см. На поверхности сперва будут появляться несколько точек, которые размещено далеко друг от друга. Спустя время количество точек будет прямопропорционально расти, и они станут захватывать всю поверхность объекта из металла.
2 до 0.5 см. На поверхности сперва будут появляться несколько точек, которые размещено далеко друг от друга. Спустя время количество точек будет прямопропорционально расти, и они станут захватывать всю поверхность объекта из металла. - Закрытый. При подобном сценарии питтинг будет захватывать сначала внутреннюю поверхность пленки из металла, а также распространение коррозии обычно идет виде недлинных линий или больших окружностей со средним диаметром (от 0.5 до 1.5 см). Такой сценарий будет встречаться крайне редко, и является самым опасным, а также губительным в связи со сложностью своевременного обнаружения. Подобная коррозия будет проявляться лишь на позднем этапе роста коррозии, когда металл спасти невозможно.
А теперь немного о том, как защитить объекты.
Защита объектов из металла
Главным методом защиты нержавейки и металла от коррозии питтингового типа будет пассивация. Для обработки обычно применяют особый раствор на основании лимонной и азотной кислоты.
При необходимости кислотный раствор может усиливаться разными вспомогательными добавками. Определенные инженеры добавляют в раствор калия ферроцианид при концентрации 2.5%. Целью пассивации будет замедление коррозии до полного прекращения появления новой ржавчины. Такой кислотный раствор будет играть роль новой защитной пленки, которая будет образовываться на поверхности во время процесса.
Кроме этого можно использовать и другие вспомогательные защитные меры:
- Заделка дефектов и трещин. Одной из основных причин появления коррозии будет нарушение целостности оксидной пленки из-за внешних дефектов. Если такие повреждения заделать вовремя, то ржавчина не успеет появиться.
- Удаление шероховатостей и неровностей. Ржавчина крайне часто появляется на неровной поверхности, а зачистка поверхности металла будет надежно защищать элемент.
- Нанесение хромированного покрытия. Определенные виды стали можно защитить при помощи нанесения дополнительного покрытия на хромовой основе, а еще такой элемент будет препятствовать появлению ржавчины.

Надеемся, теперь вам станет проще защищать металлические элементы.
Классификация питтинговой коррозии
Существует несколько видов питтинга:
- Поверхностный. При таком сценарии ржавчина затрагивает исключительно верхнюю поверхность металла. Распространяется она в виде небольших тонких линий диаметром 1-3 мм. Поверхностная ржавчина на начальном этапе обычно захватывает углы, однако со временем она начинает распространяется в горизонтальном направлении по всей поверхности металлического элемента.
- Открытый. При таком сценарии ржавчина распространяется в виде частых крупных точек, диаметр которых составляет 2-5 мм. На поверхности сперва образуется несколько точек, которые располагаются далеко друг от друга. Со временем количество точек пропорционально растет и они захватывают всею поверхность металлического объекта.
- Закрытый. При таком сценарии питтинг захватывает сперва внутреннюю поверхность металлической пленки. Распространение коррозии обычно идет в виде коротких линий или широких окружностей среднего диаметра (5-15 мм).
 Данный сценарий встречается достаточно редко. Он является самым губительным и опасным в связи со сложностью его своевременного обнаружения. Такая коррозия проявляется на поверхности только на позднем этапе роста ржавчины, когда спасти металл уже невозможно.
Данный сценарий встречается достаточно редко. Он является самым губительным и опасным в связи со сложностью его своевременного обнаружения. Такая коррозия проявляется на поверхности только на позднем этапе роста ржавчины, когда спасти металл уже невозможно.
Классификация точечных повреждений
По размеру бывают:
- Микропиттинги величиной до 0,1 мм;
- Обычные размером до 1 мм;
- Язвенный питтинг имеет размеры более 1 мм.
Также различают открытые, закрытые и поверхностные точечные язвы.
В открытом виде ржавые пятна хорошо просматриваются на поверхности материала, достаточно человеческого зрения. Если язвенных образований слишком много, то в процессе своего распространения они сливаются в одну сплошную диффузную составляющую. Закрытый вид питтинга самый опасный, так как его невозможно рассмотреть с внешней стороны, так как они увеличиваются не наружу, а вглубь материала изделия. Такие язвы могут быть найдены только с использование специальных просвечивающих приборов.
Поверхностный питтинг встречается наиболее редко, разрушение происходит не вглубь или наружу элемента, а вширь, что способствует образованию не просто точек, а выбоин на поверхности элемента.
Защита металлических объектов
Главным способом защиты нержавеющей стали и металла от питтинг-коррозии является пассивация. Для обработки обычно используется специальный раствор на основании азотной и лимонной кислот. При необходимости кислотный раствор для пассивации может усиливаться различными вспомогательными добавками. Некоторые инженеры добавляют в раствор ферроцианид калия в концентрации 2-3%.
Цель пассивации — это замедление коррозии вплоть до полного прекращения образования новой ржавчины. Пассивирующий кислотный раствор в данном случае выполняет роль новой защитной пленки, которая образуется на поверхности во время пассивации.
Помимо пассивации могут применяться другие вспомогательные меры защиты:
- Заделывание трещин и дефектов. Одной из главных причин появления ржавчины является нарушение целостности оксидной пленки в результате внешних дефектов.
 Если такие повреждения вовремя заделывать, то ржавчина не успеет образоваться.
Если такие повреждения вовремя заделывать, то ржавчина не успеет образоваться. - Удаление неровностей и шероховатостей. Ржавчина часто появляется на неровных поверхностях. Зачистка поверхности металла будет надежно защищать деталь.
- Нанесение хромированного покрытия. Некоторые стали можно защитить с помощью нанесения дополнительного покрытия на основе хрома. Этот элемент препятствует образованию ржавчины.
Этапы роста питтинга:
1) Зарождение питтинга происходит в местах дефектов пассивной пленки (царапины, разрывы) или ее слабых местах (если имеет место неоднородность сплава) при достижении определенного потенциала – потенциала питтингообразования (φпо). Ионы-активаторы вытесняют адсорбированный на поверхности кислород или при взаимодействии разрушают оксидную защитную пленку.
2) Рост питтинга – происходит по электрохимическому механизму, вследствии интенсивного растворения пассивной оксидной пленки. Из-за активного растворения пленки происходит усиление анодного процесса в самом питтинге (активационный рост питтинга).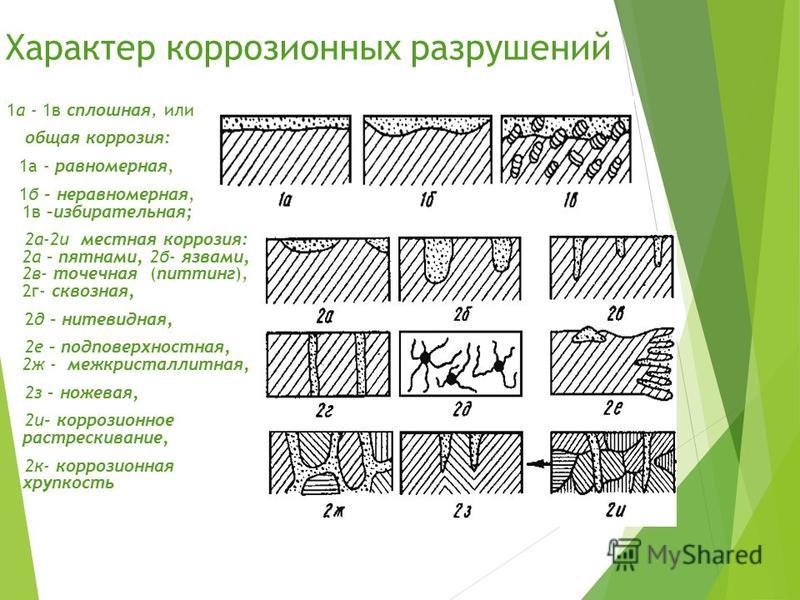 Со временем, когда питтинг будет достаточно расширен, активационный рост замедляется, начинается диффузионный режим роста питтинга.
Со временем, когда питтинг будет достаточно расширен, активационный рост замедляется, начинается диффузионный режим роста питтинга.
3) Иногда рост питтинга прекращается и наступает стадия репассивации. Основной причиной репассивации можно считать сдвиг потенциала поверхности в отрицательную сторону, т.е. сторону пассивации. Питтинг с диффузионным режимом роста (постепенно, стабильно растущий питтинг) не может перейти в стадию репассивации.
Причины, инициирующие питтинг
Часто предпосылкой для появления точечной коррозии становится нарушение технологии производства металла. Например, при несоблюдении правил отливки в стали появляются микропримеси, включения, изменяющие нормальную структуру. Некачественный металл может быть слишком пористым либо в нем появляется остаточная окалина – это тоже способствует возникновению питтинга.
Также питтинг возникает при эксплуатации стали, иных металлов в агрессивной среде: растворах, содержащих окислители и активирующие анионы (соляная, азотная кислоты, морская вода, хлористые соединения).
Прочие причины образования точечной коррозии таковы:
- механическое воздействие, приводящее к появлению сколов, царапин и вызывающее повреждение внешней защитной пленки;
- излишнее внутреннее напряжение металла;
- эксплуатация изделия при высоких температурах.
На шероховатой нержавейке точечная коррозия появится с большей вероятностью, чем на гладкой, отполированной, поэтому неровная текстура поверхности тоже считается фактором риска.
Числовой эквивалент стойкости к точечной коррозии (PREN)
Показатель RREN относится к справочным, он показывает склонность разных видов и марок нержавейки к появлению питтингов. Числовой эквивалент стойкости к точечной коррозии применяют как ориентир, но не как абсолютное руководство для предопределения коррозионной стойкости.
Обычно наиболее устойчивыми к точечному ржавлению оказываются молибден, хром и азот в качестве добавок при легировании. Чем выше цифра RREN, тем более стойкой будет сталь к появлению питтингов.
Вот справочная информация по RREN:
| Марка стали | RREN |
| 444 | 25 |
| 430 | 16 |
| 304 | 19 |
| 316 | 26 |
| 304LN | 21 |
| 904L | 36 |
| 316LN | 27,5 |
| SAF 2507 | 42 |
| Zeron 100 | 41 |
Схема разрушения металла
Для активации питтинговой коррозии необходимо присутствие двух реагентов – активаторов и пассиваторов. В качестве активаторов чаще всего выступают анионы хлора, брома, йода – они содержатся в большинстве сред, в которых эксплуатируются металлические изделия. Они адсорбируются на поверхности металла и образуют с его компонентами растворимые комплексы.
В качестве пассиваторов чаще всего выступает вода или гидроксильная группа. Непосредственно процесс разрушения протекает по следующей схеме:
- Ионы-активаторы адсорбируются на поверхности защитной (оксидной) пленки.

- Происходит процесс замещения ионов кислорода на ионы активатора процесса.
- Образуется большое количество растворимых ионов, в результате чего пленка разрушается.
В результате этого возникает разность потенциалов на поверхности материала, что ведет к появлению локальных токов, активизируется бурный анодный процесс. Ионы-активаторы при этом перемещаются к очагам разрушения, из-за чего питтинговая коррозия прогрессирует.
Питтинговая коррозия алюминия
Питтинговая или точечная коррозия
Питтинговая коррозия является наиболее часто встречающимся видом коррозии алюминия и алюминиевых сплавов. Часто ее называют точечной коррозией. Язвы образуются в оксидной пленке алюминия, подверженной воздействию атмосферы, пресной или соленой воды и других нейтральных электролитов. Поскольку в растворах с высокой кислотностью или высокой щелочностью оксидная пленка обычно не устойчива, то питтинговая коррозия бывает только при интервале величины рН от 4,5 до 9,0.
Язвы могут быть мельчайшими и концентрированными или широко разбросанными и различными по размерам в зависимости от химического состава алюминиевого сплава, качества оксидной пленки и свойств корродирующей среды. Явление питтинга может усиливаться наличием щелей и контактов алюминия с другими металлами.
Морфология питтинговой коррозии алюминия
Известно, что хлоридные ионы способны «прорывать» оксидную пленку. Хлорид алюминия (AlCl3) обычно присутствуют в растворе внутри язвы и его концентрация увеличивается при развитии коррозии или при снижении влажности окружающего воздуха. Насыщенный раствор хлорида алюминия имеет величину рН около 3,5, поэтому на дне коррозионных язв коррозия продолжается до тех пор, пока туда еще могут мигрировать кислород и корродирующий электролит. Форма коррозионных язв может меняться от мелких блюдцеобразных до полусферических и далее – до глубоких круглых цилиндрических отверстий. Это отличает питтинговую коррозию от межкристаллитной коррозии, при которой образуются подповерхностные «туннели» вдоль границ зерен, обычно видимые только в микроскоп.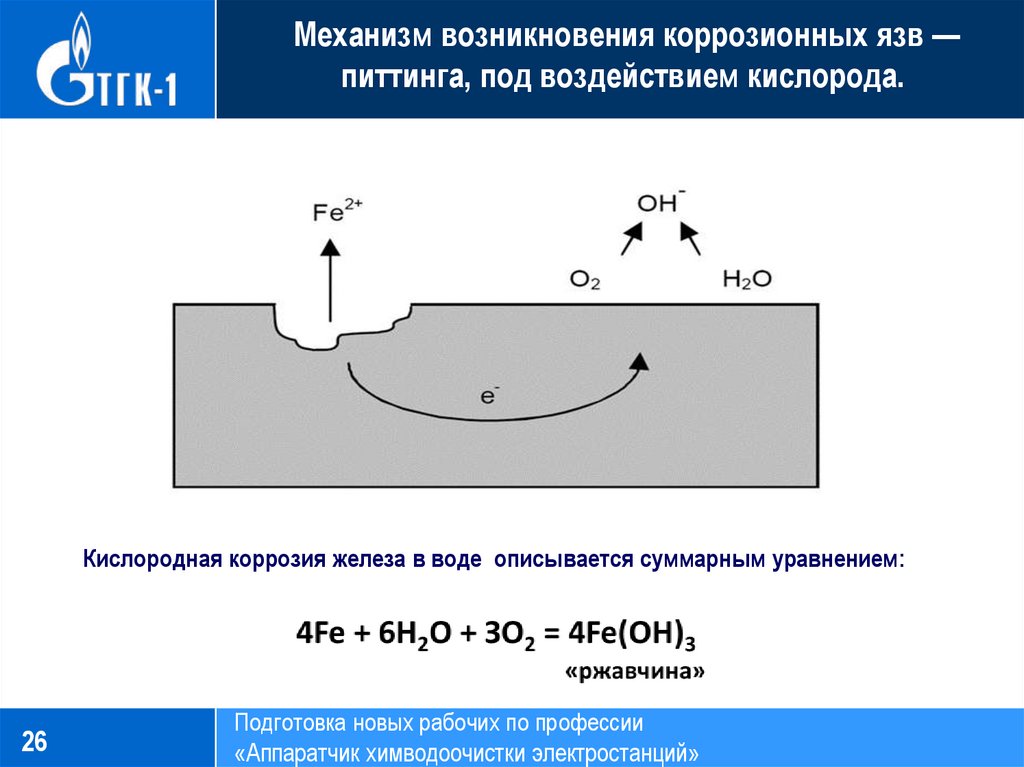
Рисунок – Гальваническая химия точечной коррозии
Рейтинг стойкости к питтинговой коррозии
Сопротивление алюминиевых сплавов питтинговой коррозии существенно зависит от степени их чистоты. Чистый алюминий имеет максимальное сопротивление питтинговой коррозии, а сплавы различных серий по стойкости к питтинговой коррозии располагаются в следующем порядке (в европейских и международных обозначениях): 1ххх – 5ххх – 3ххх – 6ххх – 7ххх – 2ххх.
Технический алюминий
Чистый алюминий (99,00 % и чище) является более стойким к питтинговой коррозии, чем любой из алюминиевых сплавов. Быстрое растворение оксидной пленки происходит только в высоко кислотных или высоко щелочных растворах. В интервале величины рН от 4 до 9 на оксидной пленке могут лишь возникать пятна и легкая локальная питтинговая коррозия. Сверхчистый алюминий (99,999 % и чище) сопротивляется питтинговой коррозии намного более успешно, чем алюминий промышленной чистоты.
Алюминиево-магниевые сплавы
Из всех промышленных алюминиевых сплавов сплавы 5ххх (Al-Mg) с содержанием магния не более 3 % имеют наилучшее сопротивление питтинговой коррозии и самую низкую скорость распространения язв, особенно в морской воде и водных растворах с содержанием хлоридов. Повышение содержания меди всего лишь до 0,2 % резко снижает стойкость этих сплавов к питтинговой коррозии.
Повышение содержания меди всего лишь до 0,2 % резко снижает стойкость этих сплавов к питтинговой коррозии.
Алюминиево-марганцевые сплавы
Следующими по сопротивлению питтинговой коррозии стоят алюминиевые сплавы 3ххх (Al-Mn), такие как 3003 (АМц) и 3004 (Д12). Алюминиево-марганцевые частицы в этих сплавах имеют электрохимический потенциал аналогичный потенциалу алюминия. Поэтому при низком содержании меди (до 0,05 %) сплавы 3003 и 3004 имеют сопротивление питтинговой коррозии почти такое же как у чистого алюминия. Повышение содержания меди повышает склонность к питтинговой коррозии в хлоридных растворах и при содержании меди около 0,15 % это влияние становится явным.
Медь и железо для питтинговой коррозии алюминия
Медь и железо оказывают наибольшее влияние на склонность к питтинговой коррозии всех алюминиевых сплавов. Хотя сплавы 6ххх (Al-Mg-Si), например, сплав АД31, в целом являются умеренно склонными к питтинговой коррозии, их сопротивление к ней может резко снижаться при повышенном содержании меди и железа, например, сплав АД33 (сплав 6061). Алюминиевые сплавы 7ххх (Al-Zn-Mg) и сплавы 2ххх (Al-Cu-Mg и Al-Cu-Mn), особенно те, что содержат много меди, имеют наименьшее сопротивление питтиниговой коррозии. Поэтому поверхность листов из этих сплавов обычно плакируют – покрывают тонким слоем технического алюминия, например, алюминий марки АД1пл (99,30 %) по ГОСТ 4784-97 или специального алюминиевого сплава с содержанием около 1 % цинка (АЦпл) по тому же стандарту. Сплавы 7ххх без меди (с марганцем или без него) показывают лучшее сопротивление питтинговой коррозии из всех высокопрочных сплавов.
Алюминиевые сплавы 7ххх (Al-Zn-Mg) и сплавы 2ххх (Al-Cu-Mg и Al-Cu-Mn), особенно те, что содержат много меди, имеют наименьшее сопротивление питтиниговой коррозии. Поэтому поверхность листов из этих сплавов обычно плакируют – покрывают тонким слоем технического алюминия, например, алюминий марки АД1пл (99,30 %) по ГОСТ 4784-97 или специального алюминиевого сплава с содержанием около 1 % цинка (АЦпл) по тому же стандарту. Сплавы 7ххх без меди (с марганцем или без него) показывают лучшее сопротивление питтинговой коррозии из всех высокопрочных сплавов.
Предотвращение питтинговой коррозии алюминия
Типичные подходы к снижению или минимизации питтинговой коррозии основаны на следующих принципах:
- Снижать агрессивность окружающей среды, например, содержание хлоридных ионов, понижать уровень температуры, кислотности и активных окисляющих веществ.
- Тщательно подбирать материалы алюминиевых конструкций. Например, применять по возможности алюминиевые сплавы 5ххх и 3ххх.
 Высокопрочные алюминиевые сплавы применять только плакированными.
Высокопрочные алюминиевые сплавы применять только плакированными. - Тщательно проектировать конструкции: избегать образования щелей, применять циркуляцию и перемешивание жидкостей для предотвращения их застоя, обеспечивать эффективный дренаж жидкостей из конструкций.
Источник: Corrosion of Aluminum and Aluminum Alloys. Edited by J.R. Davis. – ASM International, 1999.
Моделирование питтинговой коррозии в COMSOL Multiphysics®
Когда капля воды попадает на металлическую поверхность, это может привести к возникновению коррозии. При определённых условиях и достаточно длительном времени коррозионного воздействия на металлической поверхности образуется маленькое углубление. Со временем электрохимические условия в таком углублении меняются, вследствие чего нижняя часть поверхности приобретает анодную поляризацию, а удалённая от неё часть — катодную. В результате этого интенсивность коррозии в донной части углубления возрастает, что приводит к увеличению размеров углубления и образованию так называемого питтинга. Моделирование питтинговой коррозии позволяет проанализировать развитие питтингов, возникающих в различных материалах и конструкциях при определённых условиях. В этой статье мы рассмотрим, как построить модель питтинговой коррозии.
Моделирование питтинговой коррозии позволяет проанализировать развитие питтингов, возникающих в различных материалах и конструкциях при определённых условиях. В этой статье мы рассмотрим, как построить модель питтинговой коррозии.
Коррозионные процессы. Краткое введение
Гальваническая коррозия возникает при наличии электрического контакта между двумя металлами, атомы которых имеют разные значения энергии сродства к электрону. Если два таких металла поместить в электролит, то на их поверхности образуется двойной электрический слой. Потенциал двойного электрического слоя для этих двух металлов будет разным. Таким образом, электроны передаются от металла с меньшим электрохимическим потенциалом к металлу с более высоким потенциалом, как показано на рис. 1.
На поверхности благородных металлов (с высоким электрохимическим потенциалом) электроны участвуют в реакции восстановления (катодная реакция). Металлы с меньшим потенциалом отдают электроны и в результате этой анодной реакции растворяются.
Рисунок 1. Схематическое описание гальванической коррозии.
Если позволить электрохимическому процессу, схема которого показана на рис. 1, осуществляться в течение некоторого времени, то металл с меньшим потенциалом (в данном случае это железо) будет растворяться вблизи поверхности контакта с другим металлом (см. рис. 2), потенциал которого выше.
Рисунок 2. В результате гальванической коррозии железо растворяется вблизи области контакта с медью.
Теперь рассмотрим каплю воды на поверхности металла (см. рис. 3). На микроскопическом уровне металл может состоять из разных фаз с отличающимся сродством к электрону. Это означает, что, например, в кристаллитах будут идти катодные реакции, а в межкристаллитных областях — анодные.
Рисунок 3. Схема микроструктуры металлической поверхности: показаны кристаллиты и межкристаллитные области.
Согласно схеме, показанной на рис. 2, на той поверхности, где растворяется железо, образуется гидроксид железа. Гидроксид железа — один из компонентов ржавчины. Но если электрохимический процесс идёт по схеме, представленной на рис. 3, тогда ржавчина может появляться на всей поверхности металла, поскольку межкристаллитные области распределены очень равномерно. Такую коррозию обычно называют генерализованной.
Гидроксид железа — один из компонентов ржавчины. Но если электрохимический процесс идёт по схеме, представленной на рис. 3, тогда ржавчина может появляться на всей поверхности металла, поскольку межкристаллитные области распределены очень равномерно. Такую коррозию обычно называют генерализованной.
Теперь обратимся к рис. 4, на котором показана схема дальнейшего развития генерализованной коррозии, описанной на рис. 3. В центре капли диффузия кислорода к зернам кристаллита занимает больше времени, чем по краям капли, где диффузионный пробег намного короче. На поверхности металла, расположенной под центром капли, концентрация кислорода понижена, что в свою очередь уменьшает электрохимический потенциал в этой части поверхности по отношению к областям по периметру капли. Таким образом, когда потенциал оказывается меньше потенциала пассивации железа, защитный оксидный слой теряет устойчивость. В итоге, кристаллиты, расположенные в центральной части, из-за снижения концентрации кислорода станут анодами. В результате растворения железа в центральной части капли на поверхности металла появляется углубление. Кроме того, ионы железа вступают в реакцию с водой с образованием протонов, из-за чего в углублении снижается водородный показатель pH. Уменьшение pH повышает кислотность среды и, таким образом, ещё сильнее ускоряет коррозию. Описанный процесс получил название эксперимента Эванса с каплей (Evans drop experiment)[1] в честь учёного, который первым объяснил и воспроизвёл этот процесс.
В результате растворения железа в центральной части капли на поверхности металла появляется углубление. Кроме того, ионы железа вступают в реакцию с водой с образованием протонов, из-за чего в углублении снижается водородный показатель pH. Уменьшение pH повышает кислотность среды и, таким образом, ещё сильнее ускоряет коррозию. Описанный процесс получил название эксперимента Эванса с каплей (Evans drop experiment)[1] в честь учёного, который первым объяснил и воспроизвёл этот процесс.
Рисунок 4. Эксперимент Эванса с каплей. Образование углубления приводит к снижению водородного показателя, что дополнительно ускоряет анодную реакцию.
Образование углубления может происходить и по другому сценарию. Например, механическое воздействие или наличие примесей на поверхности металла могут ослабить оксидную плёнку, которая в некоторой степени защищает поверхность железа от дальнейшей коррозии. Нержавеющая сталь тоже имеет защитную оксидную плёнку, которая может быть повреждена вследствие механического или химического воздействия. —
—
Концентрацию гидроксильных ионов можно исключить при условии равновесия автопротолиза воды. Концентрацию одного из других ионов, а именно протона, можно исключить, приняв условие электронейтральности. Оба допущения в COMSOL Multiphysics® учитываются автоматически при использовании интерфейса Tertiary Current Distribution, Nernst-Planck с выбранной опцией Water-based with electroneutrality. Отметим, что при расчёте плотности тока электролита в уравнение баланса токов включены уравнения переноса для всех ионов. Ещё одной зависимой переменной является электрический потенциал электролита.
Предположим, что в результате электроосаждения внутри углубления образовался пористый слой, поэтому будем рассматривать углубление как пористую структуру, поры которой заполнены электролитом. Это разумное предположение, поскольку из того металла, на месте которого образовалось углубление, с высокой вероятностью сформируется пористое отложение. Задачу будем решать в двумерной осесимметричной постановке, как показано на рис. 5.
5.
Рисунок 5. Геометрическая модель расчётной области.
Реакция растворения металла моделируется на всей границе, обозначенной на рис. 5 как «Fe electrode surface». Будем считать, что скорость анодной реакции пропорциональна концентрации протонов. Такая зависимость характерна для условий повышенной кислотности в присутствии хлорида [2]. Чтобы связать перемещение границы расчётной области с интенсивностью растворения железа, воспользуемся методом подвижной сетки.
Как мы уже отмечали, реакция восстановления кислорода не моделируется. Мы заменяем моделирование этого процесса на граничное условие постоянного электрического потенциала электролита вдали от углубления на горизонтальной границе, которая обозначена как «Bulk electrolyte boundary». Также на этой границе мы зададим концентрацию ионов натрия, хлорида и железа.
Будем считать, что в области, занятой электролитом, в том числе в углублении, идут реакции автопротолиза воды и образования гидроксида железа. Отметим, что гидроксид расходуется в реакции образования Fe(OH)2(s), поэтому, как уже упоминалось выше (см. рис. 4), водородный показатель уменьшается.
Отметим, что гидроксид расходуется в реакции образования Fe(OH)2(s), поэтому, как уже упоминалось выше (см. рис. 4), водородный показатель уменьшается.
Начальные значения концентраций и электрического потенциала электролита рассчитываются с помощью решения стационарной задачи для исходной геометрической модели. То есть для получения начальных значений задача решается для неизменяемой геометрической модели с указанными выше граничными условиями с помощью стационарного решателя. В результате получается некоторое распределение концентраций и электрического потенциала электролита для t = 0. Это решение является начальным условием для нестационарной задачи.
Результаты
Использование стационарного решения в качестве начальных условий является разумным подходом, поскольку изменение состава и электрического потенциала электролита сначала, то есть в течение первых суток, происходит довольно медленно.
На рис. 6 показано, как увеличится углубление по истечении 30 дней.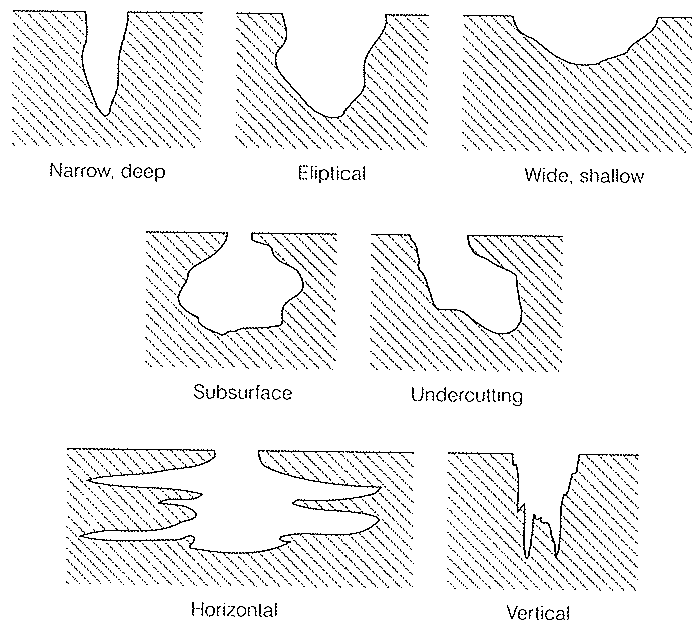 Для области внутри углубления характерен большой градиент потенциала электролита. В углублении потенциал электролита изменяется от 0,43 мВ до 16,5 мВ, тогда как за пределами углубления потенциал изменяется от 0 мВ до 0,43 мВ в течение 30 дней. Отметим, что интенсивность процессов переноса в углублении ниже, поскольку эта область представляет собой пористую среду с более низкими по сравнению с электролитом снаружи эффективными свойствами переноса. Качественно такое же распределение потенциала наблюдается в течение всего моделируемого периода времени, при этом донная часть углубления увеличивается в размерах быстрее, чем устье. По этой причине проходное сечение для переноса заряда в устье углубления сужается, что приводит к большим градиентам потенциала электролита. В результате мы действительно наблюдаем коррозию на плоской поверхности. Через 30 дней поверхность сместится примерно на 0,35 мкм, а смещение донной части углубления составит 1,45 мкм.
Для области внутри углубления характерен большой градиент потенциала электролита. В углублении потенциал электролита изменяется от 0,43 мВ до 16,5 мВ, тогда как за пределами углубления потенциал изменяется от 0 мВ до 0,43 мВ в течение 30 дней. Отметим, что интенсивность процессов переноса в углублении ниже, поскольку эта область представляет собой пористую среду с более низкими по сравнению с электролитом снаружи эффективными свойствами переноса. Качественно такое же распределение потенциала наблюдается в течение всего моделируемого периода времени, при этом донная часть углубления увеличивается в размерах быстрее, чем устье. По этой причине проходное сечение для переноса заряда в устье углубления сужается, что приводит к большим градиентам потенциала электролита. В результате мы действительно наблюдаем коррозию на плоской поверхности. Через 30 дней поверхность сместится примерно на 0,35 мкм, а смещение донной части углубления составит 1,45 мкм.
Рисунок 6. Размеры донной части углубления увеличиваются быстрее, чем размеры устья. Это приводит к большему градиенту потенциала электролита вблизи устья.
Это приводит к большему градиенту потенциала электролита вблизи устья.
Изменение водородного показателя в процессе коррозии показано на рис. 7. Значение водородного показателя в донной части через сутки равно 9,48, а через 30 суток — 9,14. Может показаться, что это незначительное изменение, однако оно соответствует увеличению концентрации протонов в 2,2 раза. Константа скорости коррозионного процесса пропорциональна концентрации протонов, а значит и скорость коррозии тоже возрастает.
Рисунок 7. Водородный показатель в углублении в различные моменты времени.
На рис. 8 приведены значения скорости коррозии в мкм/сут для четырех моментов времени, показанных выше. Максимальная скорость коррозии в донной части углубления через 30 дней в 2,3 раза выше по сравнению со скоростью коррозии через 1 день. Соответственно, концентрация протонов через 30 дней в 2,2 раза выше, чем через 1 день.
Рисунок 8. Скорость коррозии на поверхности металла в разные моменты времени.
Распределение концентрации ионов натрия обратно распределению концентрации ионов железа. Причина — условие электронейтральности. По мере того, как ионы железа попадают в электролит, ионы натрия выталкиваются из углубления. В отличие от ионов натрия, ионы хлорида, наоборот, движутся в углубление, вследствие условия электронейтральности (не показаны).
Рисунок 9. Концентрация ионов натрия в различные моменты времени.
Расчётная модель демонстрирует эффект «порочного круга» питтинговой коррозии. Интенсивность процесса растёт с течением времени, пока углубление не станет достаточно глубоким. Тогда омические потери и продукты коррозии ограничивают скорость реакции.
Заключение
Расчётную модель можно усложнить, если добавить учёт материального баланса осажденных продуктов коррозии. Плотность продуктов реакции меньше, чем плотность железа, поэтому они образуются в углублении, но затем вытесняются из него. Этот процесс можно смоделировать, если пористость сделать зависимой переменной и учесть конвективный перенос оксидов.
Ещё одно направление усложнения модели — введение в неё полной геометрической модели капли, что позволит учесть диффузию и восстановление кислорода.
Кроме того, модель можно дополнить более подробным описанием химическим процессов. Например, можно учесть образование различных ионов железа, описать дополнительные окислительно-восстановительные реакции, а также включить в модель больше различных оксидов и гидроксидов железа, образующихся на поверхности металла. Тем не менее, мы можем поэкспериментировать и с исходной моделью, которая сама по себе уже является достаточно комплексной, несмотря на относительную простоту её построения.
Дальнейшие шаги
Узнайте о функциональных возможностях модуля «Коррозия», кликнув по кнопке:
Описание модуля
Источники
- U.R. Evans, “Corrosion and Oxidation of Metals”, Amolds, p. 118., 1960.
- H.C. Kuo and K. Nobe, “Electrodissolution Kinetics of Iron in Chloride Solutions”, J. of Electrochem.
 Soc, vol. 125, no.6, 1978.
Soc, vol. 125, no.6, 1978.
Скорость — питтинговая коррозия — Большая Энциклопедия Нефти и Газа, статья, страница 1
Cтраница 1
| Коррозия малоуглеродистых сталей на разных глубинах в Атлантическом ( 1 — 4 и Тихом ( 5 — 7 океанах.
[1] |
Скорость питтинговой коррозии в аэрированной морской воде в стальных судовых трубопроводах может составлять до 1300 мкм / год. Питтинг может усиливаться, если на металле остается окалина. Как и в атмосферных условиях, окалина защищает только покрытую поверхность, а свободные участки становятся анодными. Ввиду сравнительно большой, как правило, площади катодных участков, скорость коррозии на локальных анодах очень велика.
[2]
Скорость питтинговой коррозии в присутствии в воде анионов СГ и SO повышается в 7 — 10 раз. При этом не имеет значения получена эта вода из подземного или поверхностного источника.
[3]
Скорость питтинговой коррозии можно определить параллельно с общей скоростью коррозии на том же приборе. В основу определения положен метод амперометрии нулевого сопротивления. В ячейку помещают два электрода одинаковой площади из одного и того же материала. Показатель питтинговой коррозии определяется путем измерения плотности контактного тока, возникающего между электродами, с помощью микроамперметра с нулевым сопротивлением. Согласно законам Фарадея происходит пересчет значений тока в показатель питтинговой коррозии, выраженный в мкм / год. Если величина этого показателя значительно ниже значений скорости общей коррозии, то питтингообразование минимально. В случае обратного соотношения питтинговая или щелевая коррозия будут основными в изучаемом процессе. Если показатели двух видов коррозии соизмеримы, то наблюдают отдельные неглубокие питтинги с пологими краями.
[4]
УПК — скорость питтинговой коррозии в г / ( м2 — ч), Am — суммарная потеря массы металла, a S — суммарная площадь поверхности параллельно испытываемых образцов. Количество и глубина образовавшихся на поверхности металла питтингов являются дополнительными показателями, определяемыми при помощи оптической микроскопии.
Количество и глубина образовавшихся на поверхности металла питтингов являются дополнительными показателями, определяемыми при помощи оптической микроскопии.
[5]
В нейтральных растворах для нержавеющих сталей скорость питтинговой коррозии проходит через максимум при 90 С. Они показали ( рис. 26), что с повышением температуры число питтингов резко возрастает, а глубина питтингов, как средняя, так и максимальная, остается практически постоянной. При температурах 60 — 70 С на поверхности стали образовывалось много мелких питтингов, глубина которых не превышала 0 1 мм.
[6]
Предыдущими опытами [17], а также в настоящем исследовании установлено, что в 0 5 N растворе FeCl3 скорость питтинговой коррозии нержавеющей стали 18 Сг-14 Ni, определенная по потере веса, а также измерением средней глубины питтинга, уменьшается от дополнительного легирования в следующем порядке добавок: V, Si, Mo, Re. В том же порядке, как было показано выше, влияют эти добавки на скорость роста искусственного питтинга при анодной поляризации.
[7]
Так как в растворе хлорного железа при комнатной температуре без наложения внешнего электрического тока нержавеющие стали подвергаются только питтинговой коррозии ( а общая коррозия отсутствует), то скорость питтинговой коррозии Km г / м2ч определялась весовыми потерями.
[8]
На скорость питтинговой коррозии катионнообменная очистка воды не влияет.
[9]
Определение скорости коррозии проводят с использованием портативных приборов — измерителей скорости коррозии Р5035, коррозиометров КАРТЭК-00025 или Эксперт-004. Отличительной особенностью ряда приборов, например, Эксперта-004 является возможность параллельного определения скоростей общей и питтинговой коррозии. Для измерений используют двухэлектрод-ную ячейку, в крышке которой жестко крепятся электроды из исследуемого материала. Форма, размер электродов и способ их крепления определяется видом прибора, используемого в эксперименте. По чувствительности и диапазону измеряемых скоростей коррозии метод МПС превосходит многие другие методы.
[10]
| Зависимость скорости общей коррозии ( / и максимальной глубины питтинговой коррозии ( 2 сплава 6061 — Т6 в морской воде от концентрации растворенного кислорода ( продолжительность экспозиции 1 год.
[11] |
Как и все алюминиевые сплавы, сплав 6061 склонен к питтингу при экспозиции в морской воде. Данные о коррозии этого сплава на разных глубинах, приведенные на рис. 81, показывают, что скорость питтинговой коррозии при глубоком погружении выше, чем в поверхностных водах, хотя дело здесь, по-видимому, не в самой глубине, а в количестве растворенного в морской воде кислорода.
[12]
Скорость общей коррозии у железоникелевого сплава существенно ниже, чем у малоуглеродистой стали ( см. табл. 1.20), а скорость питтинговой коррозии незначительно ниже.
[13]
Коррозия углеродистой стали на среднем уровне прилива. Глубина коррозии рассчитана по потерям массы. Кривая построена по средним значениям для 6 образцов.| Общая ( / и питтин-говая ( 2 коррозия литой ( а и кованой ( б углеродистой сталей при постоянном погружении в морскую воду. Средняя глубина питтинговой коррозии определена по 20 наибольшим питтингам, общей — по потерям массы. Кривые построены по средним значениям для 2 ( а или 6 ( б образцов. Глубина коррозии рассчитана по потерям массы. Кривая построена по средним значениям для 6 образцов.| Общая ( / и питтин-говая ( 2 коррозия литой ( а и кованой ( б углеродистой сталей при постоянном погружении в морскую воду. Средняя глубина питтинговой коррозии определена по 20 наибольшим питтингам, общей — по потерям массы. Кривые построены по средним значениям для 2 ( а или 6 ( б образцов.
[14] |
Для углеродистой стали этот параметр непосредственно связан с уменьшением временного сопротивления материала и, таким образом, является хорошим показателем изменения прочности конструкции. В тех слу-чаях; когда наибольшие неприятности могут быть связаны с перфорацией конструкции или контейнера, важным параметром коррозии становится глубина питтинга. Поэтому интересно рассмотреть и влияние биологической активности на скорость питтинговой коррозии.
[15]
Страницы:
1
2
О новейших методах изучения процессов питтинговой коррозии
Библиографическое описание:
Замалетдинов, И. И. О новейших методах изучения процессов питтинговой коррозии / И. И. Замалетдинов, Е. А. Колобова. — Текст : непосредственный // Техника. Технологии. Инженерия. — 2017. — № 1 (3). — С. 36-45. — URL: https://moluch.ru/th/8/archive/46/1655/ (дата обращения: 04.03.2023).
И. О новейших методах изучения процессов питтинговой коррозии / И. И. Замалетдинов, Е. А. Колобова. — Текст : непосредственный // Техника. Технологии. Инженерия. — 2017. — № 1 (3). — С. 36-45. — URL: https://moluch.ru/th/8/archive/46/1655/ (дата обращения: 04.03.2023).
There are summarizes of current methods for studying pitting (PC), including a method of using neural networks, 3D method for studying the morphology during the growth of pitting, finite element method, ellipsometry method, and others. Get useful information to deepen our understanding of the mechanism and kinetics of growth of pitting corrosion.
Keywords: Pitting corrosion, neural networks, velocity of pitting’s growth
Питтинговая коррозия является опасным видом локального поражения металлов и сплавов, которая, помимо перфорации стенок оболочкового оборудования химических производств, может инициировать процессы коррозионного растрескивания и коррозионной усталости. Поэтому интерес к изучению ПК возрастает в связи с развитием металловедения, с необходимостью создания устойчивых к локальным видам коррозии металлов и сплавов. Прежде чем перейти к новейшим исследованиям в области ПК вкратце охарактеризуем условия возникновения ПК и теоретические представления о ПК, которые базируются на работах научных школ Я. М. Колотыркина [1], И. Л. Розенфельда [2], Н. Д. Томашова [3] и др.
Поэтому интерес к изучению ПК возрастает в связи с развитием металловедения, с необходимостью создания устойчивых к локальным видам коррозии металлов и сплавов. Прежде чем перейти к новейшим исследованиям в области ПК вкратце охарактеризуем условия возникновения ПК и теоретические представления о ПК, которые базируются на работах научных школ Я. М. Колотыркина [1], И. Л. Розенфельда [2], Н. Д. Томашова [3] и др.
Питтинговая коррозия характерна для пассивирующихся металлов в средах, содержащих в первую очередь галиды (Cl—, Br—, I—) металлов. При достижении критического потенциала питтингообразования на активных центрах поверхности металла адсорбируются агрессивные анионы и при достижении критической концентрации Скр вызывают растворение в виде соли. Схематически процесс можно представить в виде следующих последовательных стадий [4]:
Пассивацию металла вызывают молекулы воды, которые к атому металла обращены кислородным концом. Ионы хлора вытесняют молекулы воды с поверхности и образуют с металлом интермедиаты (комплексы), переходящие в раствор. Далее следует быстрая стадия гидролиза с высвобождением хлор-ионов, вступающих в новое поверхностное взаимодействие с атомами металла. Таким образом формируется циклический или автокаталитический путь реакции питтингообразования [4].
Ионы хлора вытесняют молекулы воды с поверхности и образуют с металлом интермедиаты (комплексы), переходящие в раствор. Далее следует быстрая стадия гидролиза с высвобождением хлор-ионов, вступающих в новое поверхностное взаимодействие с атомами металла. Таким образом формируется циклический или автокаталитический путь реакции питтингообразования [4].
В работе [5] изучали ПК на аэрокосмических сплавах (Al-5,6 Zn-2,5 Mg-1,6 Cu) путем использования искусственных нейронных сетей для моделирования процесса. При этом были использованы оптическая профилометрия и функции Вейбулла для характеристики распределения по глубинам и диаметрам питтингов. Авторы использовали временные эмпирические зависимости скорости роста питтингов, полученные ранее исследователями [6,7]:
,(1)
где t — время, d — глубина или диаметр питтинга, К и b — константы, где b принимает значения от 0,3 до 0,5 [6]. Далее применили трехпараметровую Вейбуловскую функцию распределения для определения популяции питтингов по глубине и диаметру:
(2)
где d — глубина питтинга или эквивалентный ей диаметр, α— Вейбуловский параметр формы питтинга, β — параметр масштаба. γ — параметр сдвига (локализации). Методом практической профилометрии установлено, что параметром сдвига можно пренебречь, поэтому выражение (2) авторы [5] упростили:
γ — параметр сдвига (локализации). Методом практической профилометрии установлено, что параметром сдвига можно пренебречь, поэтому выражение (2) авторы [5] упростили:
,(3)
где параметры уравнения такие же, что и в уравнении (2). Вейбуловские параметры глубины и диаметра (обозначенные как αгл, βгл, αдиам, βдиам) были использованы в создании искусственных нейронных сети (ИНС). Входами во все НС были показатели температуры, рН, [Cl—], время экспозиции, в то время как выходами были максимальная глубина питтингов, максимальный диаметр питтинга, αгл, βгл, αдиам, βдиам. Каждый параметр, (т. е. температура, глубина питтинга и т. д.) был нормализован между значениями 0 и 1 перед подачей в ИНС. Поскольку температура и величина рН равномерно распределены по их весам, они были нормализованы в соответствии с линейными правилами. Например, температура была нормализована в соответствии с уравнением
Например, температура была нормализована в соответствии с уравнением
,(4)
где Тнорм— нормализованная температура, Ti — температура i -ого опыта, Tmin,, Tmax— минимальная и максимальная температура соответственно. Аналогичной нормализации была подвергнута величина рН, а концентрация хлорида, время, глубина и диаметр питтинга были нормализованы по логарифмической зависимости:
.(5)
Нейроносетевое моделирование проводилось с помощью программного обеспечения JMP8. Программное обеспечение позволило выбрать определенный процент данных вначале для тренинга ИНС (67 % было использовано для определения βгл и 90 % для остальных).
Рис. 1. Нейроносетевая структура для всех конечных параметров (вид параметра, α; параметр шкалы, β; максимальная глубина питтинга или диаметр dmax. Число нод (Нn) в промежуточном слое варьируется для каждого параметра. Входные параметры: температура, рН, концентрация Cl—, время, ориентация (продольная и поперечная) зерен после прокатки, смещение. Выходные параметры α, β или dмакс.
Входные параметры: температура, рН, концентрация Cl—, время, ориентация (продольная и поперечная) зерен после прокатки, смещение. Выходные параметры α, β или dмакс.
3D — изображение [5], полученное оптической профилометрией представлено на рис. 2.
Рис. 2. Слева: Очерченные круговые контуры групп питтингов для съемки на оптическом профилометре сплава алюминия АА 7075 (время испытаний 720 часов при температуре 60оС в растворе 0,6 М хлорида, рН = 6. Справа: 3D изображение образца после испытания
Каждый питтинг был зафиксирован программой в виде круга, пронумерован, расположение и размеры глубин и диаметров были записаны.
В табл. 1 приведено определенное пользователем число узлов (в скрытом слое), использованное для каждой ИНС.
В циклических условиях возникают напряжения, вызывающие рост трещин из глубоких питтингов. Поэтому измеренная действительная максимальная глубина питтингов была сопоставлена с результатами расчета ИНС. Результаты представлены на рис. 3.
Результаты представлены на рис. 3.
Таблица 1
Число нод искусственной нейронной сети при употреблении входящих параметров
Параметр | Число нод |
αглубина питтинга | 10 |
βглубина питтинга | 10 |
αдиаметр питтинга | 10 |
βдиаметр питтинга | 9 |
Максимальная глубина | 11 |
Максимальный диаметр | 12 |
Видно, что данные обучения/проверки ИНС со средним квадратичным отклонением R2 = 0,71 хорошо согласуются с результатами опытов со средним квадратичным отклонением R2 = 0,90. При анализе результатов использования ИНС было установлено, что на максимальную глубину питтингов оказывало влияние время испытаний, температура и рН раствора, а концентрация хлорида и ориентация тонкой структуры после прокатки сплава не оказывало существенного влияния. Незначительное влияние концентрации хлорида объяснено достаточным количеством хлорида для роста питтингов, влияние хлорида возможно возникнет в опытах при более низких концентрациях.
При анализе результатов использования ИНС было установлено, что на максимальную глубину питтингов оказывало влияние время испытаний, температура и рН раствора, а концентрация хлорида и ориентация тонкой структуры после прокатки сплава не оказывало существенного влияния. Незначительное влияние концентрации хлорида объяснено достаточным количеством хлорида для роста питтингов, влияние хлорида возможно возникнет в опытах при более низких концентрациях.
Рис. 3. Действительные максимальные глубины питтингов и рассчитанные ИНС максимальные глубины ложатся на одну прямую [5]
Временные уравнения роста питтингов были получены обученной ИНС: кинетика t1/4 была характерна для щелочных сред и для повышенных температур, а кинетика t1/2 была свойственна для кислых сред и для пониженных температур, однако для многих промежуточных значений рН и температур кинетика была t1/3. Показатель степени от 0,3 до 0,5 для большинства сред соответствовал литературным данным [6,7]. Кроме того, выявленные закономерности кинетики роста питтингов в литературе и результаты предсказаний нейронной сети по величинам степени b делают ей доверие, несмотря на интерполяционный ее характер.
Кроме того, выявленные закономерности кинетики роста питтингов в литературе и результаты предсказаний нейронной сети по величинам степени b делают ей доверие, несмотря на интерполяционный ее характер.
В работе [8] проводились анализы электрохимического шума с использованием временной и частотной зависимостей и статистических параметров потенциала и значений тока, полученные на нержавеющей стали AISI 316 в процессе питтинговой коррозии в деаэрированном 0,5 М растворе NaCl и в процессе коррозионного растрескивания под напряжением в кипящем подкисленном растворе NaCl. Визуальные наблюдения и статистические анализы значений спектрального оценивания тока и потенциала, использующего метод максимальной энтропии, дали полезную информацию на установление различия между этими коррозионными процессами и на влияние напряжения на усиление питтинговой коррозии. Результаты хорошо согласовывались с оптическими микроскопическими наблюдениями.
Исследователи [9] изучали трехмерную питтинговую коррозию, инициированную на включениях MnS стали А537 при циклических нагрузках. При этом использовали софокусный сканирующий лазерный микроскоп с элементным анализом. Ими установлено, что при циклических механических нагрузках питтинги растут анизотропно, т. е. скорости растворения стенок питтинга и дна различаются. Существенно более высокая скорость роста была обнаружена в перпендикулярном направлении оси нагрузок. Конечный элементный анализ указывает на то, что локальная продольная нагрузка играет важную роль на рост питтинга. Кинетика роста питтинга вширь доминировала в продольном направлении. Слияние питтингов в дальнейшем увеличивает скорость роста питтингов, как и предсказывалось методом конечного анализа.
При этом использовали софокусный сканирующий лазерный микроскоп с элементным анализом. Ими установлено, что при циклических механических нагрузках питтинги растут анизотропно, т. е. скорости растворения стенок питтинга и дна различаются. Существенно более высокая скорость роста была обнаружена в перпендикулярном направлении оси нагрузок. Конечный элементный анализ указывает на то, что локальная продольная нагрузка играет важную роль на рост питтинга. Кинетика роста питтинга вширь доминировала в продольном направлении. Слияние питтингов в дальнейшем увеличивает скорость роста питтингов, как и предсказывалось методом конечного анализа.
Объектом исследования [9] служила горячекатаная плита из стали А537, которая используется для изготовления нефтяной платформы. Химический состав стали, масс. %: 0,13 С; 1,48 Mn; 0,46 Si; 0,012 P; 0,005 S; 0,04 Cr; 0,19 Ni; 0,05 V; 0,17 Cu; 0,016 Mo, остальное железо. Матрица стали состоит из ферритно-перлитной структуры, полученной при прокатке и коротких поперечных перемещениях, включающей в большом количестве включения MnS в феррите. Статистика измерений показала, что размеры включений MnS в длину составила 27,1 ± 16,4 мкм, в ширину — 2,3 ±0,8 мкм с объемной фракцией 0,24 ± 0,11 % [9].
Статистика измерений показала, что размеры включений MnS в длину составила 27,1 ± 16,4 мкм, в ширину — 2,3 ±0,8 мкм с объемной фракцией 0,24 ± 0,11 % [9].
Испытания на растяжение проводили на универсальной испытательной машине (Shimadzu, модели AG-100KNG) при номинальной скорости деформации 4,2∙10–4 с-1 при комнатной температуре на трех прямоугольных стандартных образцах по направлению прокатки оси нагрузки. Во время испытаний на растяжение деформация записывалась тензометром. Механические свойства были следующие: предел текучести 303±3 МПа, прочность на растяжение 513±1 МПа, относительное удлинение 33±1 %, модуль Юнга (Е) 206±5 ГПа [9].
Образцы гантельной формы с калибровочными размерами длиной и шириной соответственно 15 и 6 мм, и толщиной 6 мм были использованы для тестов на усталостную коррозию. Осевая нагрузка была вдоль направления прокатки. Все образцы были отполированы сначала наждачной бумагой с зернами карбида кремния, затем алмазной пастой на полировочной машине. Коррозионные усталостные испытания проводили на установке Shimadzu, модели ENF-EAS с генератором синусоидальных колебаний с частотой 1 Гц с отношением напряжений 0 при комнатной температуре 20–25 оС. Серия усталостных испытаний проводилась при различных количествах циклов (1×104, 4×104, 7×104, 1×105, 2×105) при напряжении 140 МПа. Было установлено, что коррозионная усталость до разрушения составляла примерно 1×106 циклов. Не было коррозионных трещин в питтингах вплоть до 2×105 циклов, как установлено растровой электронной микроскопией. Поэтому это количество циклов являлось идеальным для исследования влияния циклических напряжений на рост питтингов [9]. Схема установки испытаний на коррозионную усталость представлена на рис. 4.
Коррозионные усталостные испытания проводили на установке Shimadzu, модели ENF-EAS с генератором синусоидальных колебаний с частотой 1 Гц с отношением напряжений 0 при комнатной температуре 20–25 оС. Серия усталостных испытаний проводилась при различных количествах циклов (1×104, 4×104, 7×104, 1×105, 2×105) при напряжении 140 МПа. Было установлено, что коррозионная усталость до разрушения составляла примерно 1×106 циклов. Не было коррозионных трещин в питтингах вплоть до 2×105 циклов, как установлено растровой электронной микроскопией. Поэтому это количество циклов являлось идеальным для исследования влияния циклических напряжений на рост питтингов [9]. Схема установки испытаний на коррозионную усталость представлена на рис. 4.
Из резервуара раствор 3,5 % NaCl со скоростью 20 мл/мин центробежным насосом нагнетался через нижний штуцер в сосуд с образцом, при этом жидкость контактировала с площадкой 1 см2 (остальная поверхность изолировалась силиконовым клеем) узкой части испытуемого образца. Через верхний штуцер жидкость самотеком поступала обратно в резервуар.
Через верхний штуцер жидкость самотеком поступала обратно в резервуар.
После коррозионных испытаний продукты коррозии удаляли раствором этилендиаминотетрауксусной кислотой (готовили 200 мл 1,5 % -ный раствор). Раствор не растворял матрицу и включения MnS.
Морфологию питтингов изучали в продольно-поперечном направлении конфокальным сканирующим лазерным микроскопом (OLYMPUS LEXT OLS3000). Тестировалось более 40 окрестностей вокруг включений MnS. На рис. 5 представлена картина поверхности, на которой форма питтингов была нерегулярной. Поэтому 3D — измерения (длина, ширина и глубина) обсчитывалась программным обеспечением, установленном на OLYMPUS LEXT OLS3000. В случае слияния питтингов их рассматривали как один питтинг.
Рис. 4. Схема установки для испытаний на коррозионную усталость
Установлено, что из всех направлений рост в глубину оказался наименьшим после 200 кс испытаний без циклических нагрузок. В условиях циклических нагрузок рост питтинга ускоряется как в ширину, так и в глубину, но со значительным ускорением в ширину. Имеется незначительный рост скорости в длину для циклически напряженных образцов после 100 кс. Явление, по-видимому, связано со слиянием питтингов.
Имеется незначительный рост скорости в длину для циклически напряженных образцов после 100 кс. Явление, по-видимому, связано со слиянием питтингов.
Рис. 5. (а) Поверхность до коррозионных испытаний; (б) питтинги, инициированные после испытаний в растворе 3,5 % NaCl без приложения напряжений
Рис. 5. (с) Питтинги, инициированные после циклических напряжений; (d) 3D — питтинги, снятые софокусным сканирующим микроскопом, обратная картинка с Z фактором 1,5
Кинетику роста питтинга в 3D направлении можно представить в виде уравнения [9]:
, (6)
где f(t) представляет ширину, длину и глубину питтингов, a, b, n экспериментальные константы. Константа a представляет инициативный размер питтинга, возникший на включении MnS. Результаты расчетов кинетических параметров [9] представлены в табл.2.
Таблица 2
Сравнение кинетических данных 3D размеров питтингов, полученных без циклических нагрузок ис ними.
3D размер | Амплитуда напряжений, МПа | α, мкм | b, мкм∙с—n | n | R2 |
Ширина | 0 | 3.6±2,7 | 0,20 | 0,32±0,14 | 0,981 |
140 | 7,5±0,2 | 1,3∙10–5 | 1,15±0,05 | 0,998 | |
Длина | 0 | 20,4±4,9 | 0,84 | 0,28±0,11 | 0,993 |
140 | 31±1,4 | 3,9∙10–3 | 0,72±0,10 | 0,991 | |
Глубина | 0 | 3,4±0,26 | 2,0∙10–4 | 0,76±0,23 | 0,948 |
140 | 4,3±0,8 | 1,7∙10–3 | 0. | 0,963 |
Показано, что константа “a” для ширины питтинга была больше, чем усредненный размер включения (т. е. 2,3 мкм). Это объяснено авторами [9] наличием трещины между включением MnS и матрицей (рис. 5(a)). Относительно большие различия, которые найдены для рассчитанной «оригинальной длины» подтверждают, что оригинальная длина питтингов варьируется на различных образцах.
Рассчитанная экспонента n роста питтинга в ширину увеличивалась от 0,32 до 1,15, когда была приложена циклическая нагрузка. Можно сделать сравнение данных табл. 2 и уравнения (6) скорости роста питтинга для образцов, испытанных без напряжений и с напряжением. Например, для после испытаний продолжительностью 200 кс скорости роста в ширину были 16 и 93 пм/с соответственно без нагрузки и с нагрузкой. Результаты свидетельствуют, что скорость роста в ширину может значительно ускоряться при воздействии циклических нагрузок.
В общем, циклические нагрузки усиливают скорость роста питтингов. Питтинги, инициированные на включениях MnS, продемонстрировали анизотропное поведение роста. Скорости роста питтингов в ширину и глубину после воздействия циклических нагрузок были выше, чем скорость роста в длину. Чтобы понять этот феномен рассчитывали методом анализа конечных элементов напряжения вокруг питтингов и их распределение.
Питтинги, инициированные на включениях MnS, продемонстрировали анизотропное поведение роста. Скорости роста питтингов в ширину и глубину после воздействия циклических нагрузок были выше, чем скорость роста в длину. Чтобы понять этот феномен рассчитывали методом анализа конечных элементов напряжения вокруг питтингов и их распределение.
Локальные напряжения и распределение напряжений одиночного полуэллипсоидного питтинга были промоделированы методом конечных элементов. Выбраны граничные условия, при которых движение левой стороны модели питтинга фиксировалось вдоль направления х, в то время как движения вдоль направлений y и z были свободными, как показано на рис. 6а. Одноосное растягивающее напряжение 280 МПа (нагрузка от 0 до 280 МПа колебаний с синусоидной волной) была приложена к правой стороне модели. Направление нагрузки было параллельно длинной оси полуэллипсоидного питтинга (направление х на рис. 6а). В соответствии со статистическими результатами типичные длина, ширина и глубина питтингов были 45, 15 и 7,5 мкм соответственно. 3D усредненные напряжения отдельного полуэллипсоидного питтинга показано на рис. 6.
3D усредненные напряжения отдельного полуэллипсоидного питтинга показано на рис. 6.
Авторы [10] для изучения процессов ПК сталей 304 и 904L применили метод электрохимической высокочастотной модуляции (ЭВЧМ). Метод заключается в наложении к анодному процессу ПК сигналов возмущения, состоящих из синусоидальных колебаний. Поясняющая схема приведена на рис.7. На корродирующую поверхность подается потенциал, который вырабатывает соответствующий ток (величина тока есть функция потенциала). На нижнем снимке потенциал возмущения состоит из двух синусоидальных волн, наложенных методом ЭВЧМ. В ответ будут получены дополнительные и более высокие частоты, являющиеся нелинейными из-за явлений, протекающие при питтингообразовании. Производится математический анализ токовых сигналов по соответствующим уравнениям для расчета тока коррозии тафелевых наклонов.
Рис. 6. 3D зоны напряжений вокруг единичного полуэллиптического питтинга (длиной 45 мкм, шириной 15 мкм и глубиной 7,5 мкм). Направление деформации показано стрелками. Зона концентраций согласованных напряжений направлена по оси х. Цветовая гамма с цифрами напряжений приведена слева от рисунка
Направление деформации показано стрелками. Зона концентраций согласованных напряжений направлена по оси х. Цветовая гамма с цифрами напряжений приведена слева от рисунка
Соответствующая математическая модель разрабатывалась, чтобы изучить реакцию на возмущение при потенциалах ниже и выше потенциодинамического потенциала питтингообразования. Ставилась цель быстрого нахождения области нелинейного изменения тока с потенциалом. Ток как функция потенциала может определяться по уравнению (7).
, (7)
где icorr — ток коррозии, К2 и К3— параметры, ассоциируемые с ПК, bc — катодный тафелевский наклон. Здесь Е, Еcorr, Epit — cоответствующие приложенный потенциал, потенциал коррозии и потенциал питтингообразования. Параметры К2 и К3 ассоциируются с ПК и их значения выбираются по уравнению (7) для представления стремительного роста тока с потенциалом, происходящего при инициировании питтинга.
В ЭВЧМ технике авторы [10] применяли возмущающий сигнал потенциала, состоящий из двух синусоидальных волн, как показано ниже
,(8)
где Uo — амплитуда потенциала возмущения, f1 и f2— частоты возмущения в Гц и Едс — потенциал двойного слоя. Подстановка уравнения (8) в уравнение (7) дает ток во временной области, который может быть затем преобразован в частотной области. Для определения теоретических значений факторов причин ниже потенциала питтингообразования и вблизи потенциала ПО, были выбраны параметры, приведенные в таблице 3.
Рис. 7. Верхняя часть временной домен тока как функции потенциала; нижняя часть — частотный домен
Таблица 3
Коррозионные параметры, показывающие свои соответствующие входные значения для симуляции цели
Параметр | Характеристика | Входные значения |
icor | Ток коррозии | 1 мкА |
Epit | Потенциал питтингообразования | 0,4 В |
К2 | Питтинговый параметр | 1 мкА |
К3 | Нелинейный параметр | 92 мВ-1 |
U0 | Амплитуда потенциала | 10 мВ |
bc | Катодный тафелевский наклон | 120 мВ на декаду |
Ecorr | Потенциал коррозии | 0 В |
f1 | Первая частота | 2 Гц |
f2 | Вторая частота | 5 Гц |
Edl | Потенциал двойного слоя | -0,3, -0,2…. |
Рис. 8. Поляризационная кривая. Различные нелинейные изменения тока в области роста питтингов и в пассивной области. Потенциал коррозии равен 0 В, а потенциал питтингобразования равен 0,4 В
Видно, что токовые компоненты в области питтинговой коррозии существенно выше, чем токи в пассивной области.
Принимая во внимание данные, полученные с помощью современных методов изучения питтинговой коррозии, можно сделать соответствующие выводы:
- Метод нейронносетевого моделирования позволил выяснить наиболее влиятельные на рост глубины питтингов во время циклических нагрузок входные параметры. Для изучения процесса также использовался метод оптической профилометрии
- В ходе исследования [9] установлен анизотропный характер роста питтингов при циклических механических нагрузках. В период приложения нагрузки, экспонента n роста питтингов в ширину возрастала более чем в 2 раза, что свидетельствует о воздействии циклической нагрузки на скорость роста в ширину
- При приложении одноосного растягивающего напряжения к полу-эллипсообразному питтингу, напряжения, возникающие перпендикулярно оси растяжения, превышают значение приложенной нагрузки, увеличивая скорость роста ПК в ширину и глубину
- Метод электрохимической высокочастотной модуляции позволяет отследить инициирование роста питтинга, в связи со стремительным ростом силы тока и потенциала в этот период.

Литература:
- Колотыркин Я. М. Металл и коррозия. М.: Металлургия, 1985. — 88 с.
- Розенфельд И. Л. Ингибиторы коррозии. Монография. — М.: Химия, 1977. — 352 с.: ил.
- Томашов Н. Д. Коррозия металлов с кислородной деполяризацией. Учебник: — М., Л.: Издательство АН СССР, 1947. — 250 с.
- Розенфельд И. Л. Ускоренные методы коррозионных испытаний металлов (теория и практика)/ И. Л. Розенфельд, К. А. Жигалова. М.: Металлургия, 1966. — 348с.
- Modeling the environmental dependence of pit growth using neural network approaches/ M. K. Cavanaugh, R. G. Buchheit, N. Birbilis//Corrosion Science, Vol.52 (2010), p.3070–3077.
- Pitting corrosion of aluminium/ Z. Szklarska-Smialowska// Corrosion Science, Vol. 41 (1999), p.1743–1767.
- A simplified method for estimating corrosion cavity growth rates/ G Engelhardt, M Urquidi-Macdonald, DD Macdonald// Corrosion Science,Vol.39 (1997), p.419–441.

- Assessment of stress corrosion crack initiation and propagation in AISI type 316 stainless steel by electrochemical noise technique/ T. Anita, M. G. Pujar, H. Shaikh, R. K. Dayal, H. S. Khatak// Corrosion Science, Vol.48, Issue 9, September 2006, p.2689–2710.
- Anisotropic 3D growth of corrosion pits initiated at MnS inclusions for A537 steel during corrosion fatigue/ Jin Ma, Bo Zhang, Jianqiu Wang, Guozhen Wang, En-Hou Han, Wei Ke //Corrosion Science, Vol.52 (2010), p.2867–2877.
- Evolution of current transients and morphology of metastable and stable pitting on stainless steel near the critical pitting temperature/ M. H. Moayed, R. C. Newman// Corrosion Science, Vol.48, Issue 4, April 2006, p.1004–1018.
Основные термины (генерируются автоматически): скорость роста, глубина, параметр, потенциал, ширина, LEXT, OLYMPUS, коррозионная усталость, максимальная глубина, нагрузка.
Питтинг Определение и значение — Merriam-Webster
питтинг
ˈpi-tiŋ
1
: расположение ям
2
: действие или процесс формирования ям
3
: объединение петухов для борьбы
Примеры предложений
На краске автомобиля было видно, что изрыт из-за летящего гравия.
На ее лице были незначительные изъязвления от ветряной оспы.
Недавние примеры в Интернете
Нет ни слова о политике семейных ценностей, которая превратила бы 2000-е годы в войну культур , в которой обиженных, пишущих письма консерваторов против резких анти-ПК братьев.
— Крейг Дженкинс, Стервятник , 29 июля 2021 г.
На последних снимках с «Новых горизонтов» видна неясная шестиугольная рябь, возможно, из-за циркуляции этих мягких льдов, и широко распространенные точечная коррозия , скорее всего, из-за прямого испарения частей твердой поверхности (процесс, известный как сублимация).
— Кори С. Пауэлл, Discover Magazine , 31 декабря 2015 г.
Критики говорят, что Castroville обыграли — фальшивый , противопоставляющий одного недостаточно обслуживаемого сообщества другому.
— Розанна Ксиастафф, писатель, Los Angeles Times , 18 ноября 2022 г.
Чтобы избежать точечная коррозия или другие повреждения поверхности, никогда не используйте абразивные инструменты, агрессивные чистящие средства или кислотные ингредиенты, такие как уксус или лимонный сок, для очистки этих раковин.
— Джессика Беннетт, Better Homes & Gardens , 8 сентября 2022 г.
Чтобы избежать точечной коррозии или других повреждений поверхности, никогда не используйте абразивные инструменты, агрессивные чистящие средства или кислотные ингредиенты, такие как уксус или лимонный сок, для очистки этих раковин.
— Джессика Беннетт, 9 лет.0025 Better Homes & Gardens , 8 сентября 2022 г.
Чтобы избежать точечной коррозии или других повреждений поверхности, никогда не используйте абразивные инструменты, агрессивные чистящие средства или кислотные ингредиенты, такие как уксус или лимонный сок, для очистки этих раковин.
— Джессика Беннетт, Better Homes & Gardens , 8 сентября 2022 г.
Высокая температура и давление также сорвали заземляющий провод на конце свечи зажигания, и даже чугунная гильза цилиндра показала около точечная коррозия .
— Дэйв Вандерверп, Автомобиль и водитель , 26 августа 2022 г.
Войны советов в Чикаго разразились 2 мая 1983 года, когда 29 олдерменов осознали силу излюбленного сценария профессоров политических наук: противопоставили слабого мэра сильному городскому совету.
—Chicago Tribune Staff, Chicago Tribune , 19 июня 2022 г.
Узнать больше
Эти примеры предложений автоматически выбираются из различных онлайн-источников новостей, чтобы отразить текущее использование слова «питтинг». Мнения, выраженные в примерах, не отражают точку зрения Merriam-Webster или ее редакторов. Отправьте нам отзыв.
История слов
Первое известное использование
1593, в значении, определенном во втором смысле
Путешественник во времени
Первое известное использование питтинг был
в 1593 г.
Посмотреть другие слова того же года
питтиды
точечная коррозия
зритель последних рядов партера
Посмотреть другие записи поблизости
Процитировать эту запись0003
«Питтинг». Словарь Merriam-Webster.com , Merriam-Webster, https://www.merriam-webster.com/dictionary/pitting. По состоянию на 3 марта 2023 года.
яма
Медицинское определение
точечная корка
существительное
1
: действие или процесс образования ямок (например, в угревой коже, зубе или зубной реставрации) при надавливании пальцем или тупым предметом и исчезает лишь медленно после снятия давления при некоторых формах отека
Еще от Merriam-Webster на
точечная коррозия
Тезаурус: Все синонимы и антонимы к слову pitting
Английский: Перевод pitting для говорящих на испанском языке
Последнее обновление:
— Обновлены примеры предложений
Подпишитесь на крупнейший словарь Америки и получите тысячи дополнительных определений и расширенный поиск без рекламы!
Merriam-Webster полное определение
в кембриджском словаре английского языка
Ни одна из четырех игр , в которых с 16 посевными против односеменных, не закончилась разочарованием.
Из ВРЕМЕНИ
Теперь это фактически война только на словах, а не на словах.0025 сталкивает армий друг с другом.
Из International Business Times
Сообщение об отсутствии на работе чревато профессиональным и личным компромиссом, противопоставляя подключенной компетентности отдыху без подключения к сети.
Из Business Insider
Разделение людей на группы и противопоставление их друг другу никогда не приведет к системному экономическому росту.
От TechCrunch
Племена были вынуждены создавать виртуальные резервации в своих деревнях, натравливая одну группу на другую, тем самым разрушая традиционные торговые методы.
От Хаффингтон Пост
Инспекторы проводят визуальный осмотр невооруженным глазом или с помощью увеличительного стекла в поисках ржавчины или точечная коррозия .
Из журнала Slate
Но то, что мы наблюдаем сейчас, — это стравливания человек друг против друга, нацеливание на иммигрантов.
Из Лос-Анджелес Таймс
Это , в котором деловых людей противопоставляются либертарианцам и социально сознательным людям.
Из Нью-Йорк Дейли Ньюс
Запугивание, манипулирование и стравливает человек друг с другом.
Из Сиэтл Таймс
Питтинг риски вакцин против рисков болезней действительно находятся в его центре.
Из Атлантики
Наиболее примечательным среди их выводов было то, что точечная коррозия возникла в основном на лобовых стеклах автомобилей, а не на их задних стеклах.
От Хаффингтон Пост
Государственная политика и риторика «угрожают нашей открытой экономике, наносят ущерб нашей международной репутации и разделяют наше общество на противопоставляет сообщество сообществу», — сказала она.
От Блумберга
Дело не в конфликте, не в том, что противопоставляет бизнес рабочим.
От Хаффингтон Пост
Благодаря тому, что сталкивают друг с другом команд с подстановочными знаками, новый формат устраняет некоторые плохие стимулы старого режима.
Из журнала Slate
Обе группы утверждают, что другая противопоставляет небольшое количество тех, у кого есть, против большего числа тех, у кого их нет.
От Хаффингтон Пост
Эти примеры взяты из корпусов и источников в Интернете. Любые мнения в примерах не отражают мнение редакторов Кембриджского словаря, издательства Кембриджского университета или его лицензиаров.
Любые мнения в примерах не отражают мнение редакторов Кембриджского словаря, издательства Кембриджского университета или его лицензиаров.
Что такое точечная коррозия? Как обнаружить и лечить питтинговую коррозию?
Точечная коррозия поражает металлы и сплавы, такие как сталь, железо, алюминий и другие. Обычно он ограничивается определенными областями. Он быстро проникает и атакует, и его трудно обнаружить. Чаще всего это происходит, когда слой пассивного покрытия физически поврежден или подвергся химическому воздействию. Это создает слабое место, где вода или коррозионные растворы воздействуют на подложку.
Соседние материалы часто остаются незатронутыми. Если ее не остановить, точечная коррозия может быть разрушительной для кровельных систем или любой металлической конструкции. Она возникает быстро и ее легко не заметить, поэтому многие считают ее самой опасной формой коррозии.
Точечная коррозия Объяснение
Питтинговая коррозия представляет собой полость, отверстие или ямку, которые образуются на небольшой площади или в точке. Ямки или отверстия закрыты небольшим количеством продуктов коррозии (ржавчины) на поверхности. Когда катодная реакция на большой площади (покрытие) поддерживает анодную реакцию на небольшой площади (открытый металл), образуется ямка, полость или небольшое отверстие. Окисление происходит в металле даже при отсутствии подачи кислорода.
Ямки или отверстия закрыты небольшим количеством продуктов коррозии (ржавчины) на поверхности. Когда катодная реакция на большой площади (покрытие) поддерживает анодную реакцию на небольшой площади (открытый металл), образуется ямка, полость или небольшое отверстие. Окисление происходит в металле даже при отсутствии подачи кислорода.
Высокое потребление электронов большим катодом переносится на маленький анод, что приводит к интенсивной точечной коррозии. Это будет незаметно и произойдет быстро с очень вредными последствиями. На поверхности видно только небольшое пятно ржавчины, в то время как повреждение происходит глубоко в металлической конструкции внизу.
Диаграмма точечной коррозии, показывающая, как ржавчина образуется в небольшой анодной области из-за большого потребления электронов большой катодной площадью, образующей ямку внизу.
Что вызывает точечную коррозию?
Точечная коррозия возникает, когда катод (поврежденное покрытие) большой, а анод (открытый металл) маленький. Обычно поверхностный защитный слой или пленка становится катодом, когда он повреждается и трескается. Затем обнажается небольшой участок металла, который становится анодом.
Обычно поверхностный защитный слой или пленка становится катодом, когда он повреждается и трескается. Затем обнажается небольшой участок металла, который становится анодом.
Питтинг проявляется сильно, когда раствор на поверхности металла содержит ионы хлорида, гипохлорита или бромида. Другими вредными растворами являются те, которые содержат фториды и йодиды. Также известно, что сульфиды и вода усиливают процесс питтинговой коррозии.
Наиболее распространенными причинами точечной коррозии являются;
- Трещины в защитном покрытии
- Царапины, потертости и мелкие сколы
- Неравномерное напряжение
- Дефект металлической подложки
- Турбулентный поток жидкости
- Неоднородное защитное покрытие
- Химическое воздействие на защитное покрытие
Металлы, склонные к точечной коррозии;
- из нержавеющей стали
- Хром
- Пассивный железо
- Mercury
- Cobalt
- Alluminum
- Mopper
- Allumyn
- ASTM G61 Испытание на циклическую поляризацию
- ASTM G150 Электрохимическое испытание на температуру точечной коррозии
- Использование покрытия, предотвращающего точечную коррозию на металлических поверхностях
- Использование более устойчивых к коррозии материалов
- Обеспечение регулярного смывания жидкостей, контактирующих с материалом
- Использование катодных защита
- Предотвращение застойных зон
- Использование ингибитора / контроль химического состава жидкости
- Поддержание защитной пленки материала
- Услуги неразрушающего контроля/инспекции для определения географии повреждений с использованием методов скрининга первого уровня, включая визуальный осмотр (волоконная оптика) и волноводный контроль, в сочетании с более подробными оценками второго уровня с ультразвуковым контролем (UT) для обычных котлов и котлов-утилизаторов в не -оребренная трубка.
- Предоставить рекомендации по выбору мест отбора проб труб для обычных и котлов-утилизаторов, а также провести металлографический анализ для определения степени точечной коррозии.
- Проведите оценку первого уровня для выявления тепловых переходных процессов и определения мест, где в паровых трубопроводах образуется конденсат, который плохо дренируется.
- Предоставить руководство по проведению испытаний на унос пара для выявления присутствия сульфата натрия.
 Осмотрите паровые барабаны, чтобы убедиться в правильности работы уровня барабана и определить, не повреждены ли внутренние части барабана таким образом, что это может способствовать уносу.
Осмотрите паровые барабаны, чтобы убедиться в правильности работы уровня барабана и определить, не повреждены ли внутренние части барабана таким образом, что это может способствовать уносу. - Обзор и сравнительный анализ программы химического цикла предприятия, обычно выполняемые в течение однодневного визита на объект. Оцените заводские методы работы с точки зрения количества повторяющихся ситуаций, которые могут увеличить вероятность точечной коррозии. Предоставьте предлагаемый план действий по устранению недостатков в программе биохимии и повторите ситуации, чтобы включить приборы для надлежащего мониторинга биохимии в течение всего цикла.
- Оцените методы укладки компонентов, чтобы свести к минимуму присутствие застойной, насыщенной кислородом воды, и предоставьте рекомендации по надлежащим краткосрочным и долгосрочным процедурам укладки.
- Поддержка реализации, пересмотра и контроля плана действий и оценка результатов.
- Дайте совет и рекомендации по ремонту.

. частицы. Область под каплей недостаточно насыщена кислородом, в то время как окружающие области хорошо насыщены кислородом. Это приводит к дифференциальной аэрационной коррозии, когда окружающие области являются катодными, а небольшая область под каплями и частицами пыли становится анодной. Электроны проходят через металл и встречают воду и кислород. Ионы образуются и распадаются вместе, образуя ржавчину. По мере образования ржавчины в металле появляются ямки, трещины и щели.
частицы. Область под каплей недостаточно насыщена кислородом, в то время как окружающие области хорошо насыщены кислородом. Это приводит к дифференциальной аэрационной коррозии, когда окружающие области являются катодными, а небольшая область под каплями и частицами пыли становится анодной. Электроны проходят через металл и встречают воду и кислород. Ионы образуются и распадаются вместе, образуя ржавчину. По мере образования ржавчины в металле появляются ямки, трещины и щели.
Типы точечной коррозии
Точечная коррозия может проявляться в различных формах. Форма ямки во многом зависит от затронутого материала и направления зерна в этом материале. Чаще всего страдают пассивные металлы и сплавы, в том числе нержавеющая сталь и алюминий. Однако почти любой металл или материал, подверженный коррозии, может быть затронут.
Желобковая точечная коррозия
Желобовые ямки имеют тенденцию быть полусферическими, чашеобразными или неправильной формы. Точечная коррозия возникает, когда пассивная пленка (защитный слой) разрушается, а металлическая стенка разрушается, образуя узкие и глубокие бороздки. Их плоские стенки обнажают кристаллическую структуру металла. Они могут быстро перфорировать толщину материала, например, кровельного листа, фермы или элемента водосточного желоба.
Их плоские стенки обнажают кристаллическую структуру металла. Они могут быстро перфорировать толщину материала, например, кровельного листа, фермы или элемента водосточного желоба.
Диаграмма поперечного сечения точечной коррозии с вертикальной коррозией зерна.
Диаграмма поперечного сечения узкой и глубокой точечной коррозии.
Диаграмма поперечного сечения точечной коррозии в виде эллиптической желоба.
Неглубокая широкая желобчатая точечная коррозия. Диаграмма поперечного сечения.
Боковая питтинговая коррозия
Боковые ямки покрыты полупроницаемой пленкой продуктов коррозии (ржавчины) и появляются в виде горизонтальных зерен, подрезов и подповерхностных форм. Боковая точечная коррозия может очень быстро проникнуть в металл. Это очень трудно обнаружить, потому что поверхность металла выглядит нетронутой и свободной от коррозии. При наличии лишь нескольких небольших пятен ржавчины может показаться, что повреждение очень незначительное.
Диаграмма сечения поперечного сечения точечной коррозии при горизонтальном воздействии зерен.
Диаграмма поперечного сечения подповерхностной боковой точечной коррозии.
Подрезание боковой точечной коррозии Диаграмма поперечного сечения.
Как проверить на питтинговую коррозию?
Визуальный осмотр корродированной металлической поверхности является первым и основным используемым методом. Подсчитайте количество ямок через окуляр микроскопа на определенной площади поверхности, например, 20 см 2 определить примерный размер и распределение ямок. Количество ям не обязательно является самым важным фактором для рассмотрения. Глубина ямы, безусловно, самая большая опасность. Одна узкая глубокая яма может быть более опасной, чем множество мелких ям. Металлографический поперечный разрез для измерения глубины ямок покажет интенсивность атаки.
Звуковые испытания – это когда ультразвуковые импульсы звуковой энергии передаются через контактную жидкость на масляной или водной основе на поверхность металла. Волны генерируются и отражают эхо, которые преобразуются в электрические сигналы. Эти сигналы можно интерпретировать, чтобы показать расположение ямок, щелей и дефектов в металле. Этот тест обладает хорошей чувствительностью и дает мгновенную информацию о глубине, ширине и расположении ямок и дефектов.
Волны генерируются и отражают эхо, которые преобразуются в электрические сигналы. Эти сигналы можно интерпретировать, чтобы показать расположение ямок, щелей и дефектов в металле. Этот тест обладает хорошей чувствительностью и дает мгновенную информацию о глубине, ширине и расположении ямок и дефектов.
Электромагнитные испытания используются для обнаружения дефектов или неоднородностей в структуре электропроводящих материалов, таких как сталь и железо. Материалы с дефектами будут создавать магнитное поле, отличное от поля эталонного материала без дефектов.
Электрохимические испытания для измерения точечной коррозии в любом металле, такие как циклическая поляризация и потенциостатические испытания, также возможны. Это краткосрочные электрохимические тесты, дающие мгновенные результаты.
Другим вариантом является испытание погружением или метод снижения веса. Эти тесты требуют больше времени для выполнения. Они включают удаление образца металла и погружение в раствор. Через несколько дней его можно снять, чтобы рассчитать скорость коррозии. Вы можете наблюдать за ямками и их глубиной под микроскопом и производить необходимые расчеты.
Они включают удаление образца металла и погружение в раствор. Через несколько дней его можно снять, чтобы рассчитать скорость коррозии. Вы можете наблюдать за ямками и их глубиной под микроскопом и производить необходимые расчеты.
Существует несколько стандартов, которые содержат рекомендации по электрохимическим испытаниям на точечную коррозию нержавеющих сталей, и наиболее популярными из них являются:
Как лечить точечную коррозию?
Рекомендуется использовать рекомендуемые процедуры очистки, чтобы полностью обнажить ямки и удалить продукты коррозии. Избегайте использования растворов, которые чрезмерно воздействуют на основной металл. Желательно во время чистки периодически прощупывать ямки остроконечным инструментом. Это позволит вам определить степень любого подреза или подповерхностной коррозии. Энергичная очистка ямы проволочной щеткой значительно расширит отверстия. Удаление продуктов коррозии и подрезов металла поможет вам оценить степень повреждения.
Удаление продуктов коррозии и подрезов металла поможет вам оценить степень повреждения.
Когда металлический материал будет чистым и свободным от мусора, проведите окончательную проверку повреждений. Если вы довольны тем, что коррозия была обнаружена вовремя, вы можете приступить к нанесению базового грунтовочного покрытия, а затем еще одного или двух верхних слоев. Если повреждение серьезное и компонент слишком слабый, его необходимо заменить.
Цинк-фосфатное грунтовочное покрытие является одним из самых популярных методов покрытия для защиты от точечной коррозии. Специально разработанные грунтовки, такие как фосфат цинка, улучшают коррозионную стойкость.
Металлизация цинковым напылением — это метод, который очень эффективен против коррозии. Он имеет гладкую поверхность, которая эстетически привлекательна и популярна. Он не обеспечивает такую же защиту, как горячее цинкование, но поскольку это холодный процесс, нет риска деформации металла. Металлизация распылением цинка идеально подходит для использования на декоративных металлических предметах, таких как художественные выставки, металлические перила и заборы.
Металлизация распылением цинка идеально подходит для использования на декоративных металлических предметах, таких как художественные выставки, металлические перила и заборы.
Химическое покрытие использует электростатический или сжатый воздух для нанесения специального порошкового материала на стальную поверхность. Затем он плавится, образуя гладкую защитную пленку. Обработанная таким образом сталь не только защищена от коррозии и УФ-повреждений, но и обладает высокой устойчивостью к отслаиванию, царапанью и растрескиванию.
Горячее погружение — это метод покрытия цинком, который можно использовать для стали всех форм и размеров. Он включает погружение стали в ванну с расплавленным цинком при температуре до 450°C. Сталь, оцинкованная таким образом, является особенно популярным подходом для применения в трубах, поскольку она хорошо защищена от коррозии, а также от экстремальных погодных условий.
Как предотвратить и защитить от точечной коррозии?
Факторы окружающей среды, вызывающие точечную коррозию, должны быть по возможности сведены к минимуму. Влажность, температура, содержание хлоридов и кислот pH, а также уровень солей должны контролироваться и сводиться к минимуму.
Влажность, температура, содержание хлоридов и кислот pH, а также уровень солей должны контролироваться и сводиться к минимуму.
Для катодной защиты подвергающийся риску металл следует покрыть химически активным металлом, который легче подвергается коррозии. Это может быть гальванизированное цинковое покрытие или подобное. Реакционноспособный металл будет действовать как анод и сначала подвергаться коррозии, предотвращая образование точечной коррозии на подложке.
Для защиты от химического воздействия лучше подходят устойчивые к коррозии металлы, такие как сплавы. Сплавы, содержащие титан, азот, хром и молибден, очень эффективны в средах с высоким содержанием ионов хлора.
Питтинговую коррозию можно контролировать с помощью:
Подробнее
Точечная коррозия – Википедия
Изучение и оценка точечной коррозии
Различные типы точечной коррозии
Взрыв канализации Гвадалахары из-за точечной коррозии
Точечная коррозия – Служба материалов, обеспечивающих целостность конструкции
Точечная коррозия – это локализованное коррозионное воздействие, сопровождающееся растворением металлической поверхности трубы на небольшой и хорошо очерченной территории. Питтинговая коррозия может возникнуть в любом компоненте, контактирующем с водой в условиях застойного насыщения кислородом. Точечная коррозия в трубках экономайзера обычно является результатом неправильной практики отключения, которая допускает контакт со стоячей водой с высоким содержанием кислорода. Точечная коррозия также может возникать в трубах с водяными стенками в результате кислотного воздействия в результате неудовлетворительной химической очистки или кислотного загрязнения.
Питтинговая коррозия может возникнуть в любом компоненте, контактирующем с водой в условиях застойного насыщения кислородом. Точечная коррозия в трубках экономайзера обычно является результатом неправильной практики отключения, которая допускает контакт со стоячей водой с высоким содержанием кислорода. Точечная коррозия также может возникать в трубах с водяными стенками в результате кислотного воздействия в результате неудовлетворительной химической очистки или кислотного загрязнения.
Ямки, связанные с условиями низкого pH, как правило, многочисленны и расположены довольно близко друг к другу. Ямки, как правило, имеют глубокие стенки по сравнению с длиной дефекта. Разрушение поверхности пассивного металла инициирует процесс точечной коррозии в условиях застоя кислорода. Возникает большая разность потенциалов между небольшой площадью инициированной активной ямки (анод) и пассивной областью вокруг ямки (катод). Яма будет расти в присутствии концентрированной соли или кислых веществ. Соль иона металла (M+A-) соединяется с водой и образует гидроксид металла и соответствующую свободную кислоту (например, соляную кислоту, когда присутствует хлорид). Кислородное восстановление на катоде подавляет коррозию по краям ямки, но внутри ямки скорость атаки увеличивается, поскольку локальная среда внутри ямки становится более кислой. В случае, если поверхности вдоль стенок ямки не репассивированы, скорость роста ямки будет продолжать увеличиваться, так как реакция больше не регулируется средой объемной жидкости. Питтинг часто встречается в застойных условиях, которые позволяют инициировать и концентрировать место, позволяя атаке продолжаться.
Соль иона металла (M+A-) соединяется с водой и образует гидроксид металла и соответствующую свободную кислоту (например, соляную кислоту, когда присутствует хлорид). Кислородное восстановление на катоде подавляет коррозию по краям ямки, но внутри ямки скорость атаки увеличивается, поскольку локальная среда внутри ямки становится более кислой. В случае, если поверхности вдоль стенок ямки не репассивированы, скорость роста ямки будет продолжать увеличиваться, так как реакция больше не регулируется средой объемной жидкости. Питтинг часто встречается в застойных условиях, которые позволяют инициировать и концентрировать место, позволяя атаке продолжаться.
Наиболее частая причина точечной коррозии в трубопроводах, соприкасающихся с паром, возникает из-за богатого кислородом застойного конденсата, образующегося во время останова. Принудительное охлаждение и/или неправильный слив и вентиляция узлов могут привести к избыточной влажности. Граница между жидкостью и воздухом является областью наибольшей восприимчивости. Точечная коррозия также может быть ускорена, если условия допускают отложение солей, таких как сульфат натрия, которые смешиваются с влагой во время останова. Унос летучих веществ зависит от давления в барабане, в то время как механический перенос может увеличиваться при работе с высоким уровнем в барабане или отверстиями в сепараторах барабана. Точечная коррозия из-за воздействия сульфата натрия может возникать в секциях подогревателя обычных установок и установок-утилизаторов, поскольку сульфат менее растворим и откладывается на внутренних поверхностях. Во время остановов образующаяся влага имеет более кислую реакцию.
Точечная коррозия также может быть ускорена, если условия допускают отложение солей, таких как сульфат натрия, которые смешиваются с влагой во время останова. Унос летучих веществ зависит от давления в барабане, в то время как механический перенос может увеличиваться при работе с высоким уровнем в барабане или отверстиями в сепараторах барабана. Точечная коррозия из-за воздействия сульфата натрия может возникать в секциях подогревателя обычных установок и установок-утилизаторов, поскольку сульфат менее растворим и откладывается на внутренних поверхностях. Во время остановов образующаяся влага имеет более кислую реакцию.
В обычных блоках точечная коррозия возникает в местах, где конденсат может образовываться и оставаться в жидком состоянии во время останова, если узлы не вентилируются должным образом, не осушаются или не промываются воздухом или инертным газом. Эти области включают горизонтальные трубы экономайзера и в нижней части наклонных изгибов или в нижних точках провисающих горизонтальных труб в трубах, контактирующих с паром.
В котлах-утилизаторах повреждения возникают на поверхностях любого компонента, который намеренно поддерживается во влажном состоянии в периоды простоя или подвержен задержке воды из-за неполного слива или конденсации во время периодов простоя.
Разрушение вследствие неправильной химической очистки обычно усиливается в зонах термического влияния сварки или в местах, где отложения могли остаться после очистки.
Ямки часто бывают небольшого размера и могут быть заполнены продуктами коррозии или оксидами, поэтому определение серьезности питтинговой коррозии при визуальном осмотре может быть затруднено.
Повреждение пораженных поверхностей имеет тенденцию быть глубоким по отношению к ширине ямки, так что соотношение сторон является отличительной чертой.
Основной фактор, который способствует точечной коррозии в трубах котлов, связан с неправильными методами остановки, которые допускают образование и сохранение стоячей, насыщенной кислородом воды без защитной среды. Подтверждение наличия стоячей воды включает: а) анализ продуктов коррозии внутри и вокруг приямка; б) отбор проб труб на пораженных участках для определения наличия локальной коррозии; и c) оценка процедур останова для проверки наличия условий, способствующих застою воды. Унос сульфата натрия и его отложение в подогревателе может привести к образованию кислых растворов во время незащищенного останова и вызвать точечную коррозию. Точно так же летучая зола может втягиваться в трубы подогревателя под вакуумом и образовывать кислую среду.
Подтверждение наличия стоячей воды включает: а) анализ продуктов коррозии внутри и вокруг приямка; б) отбор проб труб на пораженных участках для определения наличия локальной коррозии; и c) оценка процедур останова для проверки наличия условий, способствующих застою воды. Унос сульфата натрия и его отложение в подогревателе может привести к образованию кислых растворов во время незащищенного останова и вызвать точечную коррозию. Точно так же летучая зола может втягиваться в трубы подогревателя под вакуумом и образовывать кислую среду.
Визуальный осмотр (волоконная оптика) и волноводное исследование могут использоваться для определения поврежденных зон и выявления областей с сильными отложениями, особенно в котлах-утилизаторах. Ультразвуковой контроль можно использовать для определения степени потерь или утончения металла на трубах без внешних ребер.
Точечная коррозия чаще всего устраняется путем замены в натуральной форме на пораженных участках после их выявления. Сварка подушечками не считается приемлемым долгосрочным ремонтом. Цикл питтинга может начаться снова, если не будут приняты надлежащие методы простоя. Эти действия должны сопровождаться анализом и оптимизацией химического цикла агрегата (как питательной воды, так и котловой воды).
Цикл питтинга может начаться снова, если не будут приняты надлежащие методы простоя. Эти действия должны сопровождаться анализом и оптимизацией химического цикла агрегата (как питательной воды, так и котловой воды).
Департамент истории NPR: NPR
Линтон Уикс
Мужчина показывает лобовое стекло с ямками полицейскому в Сиэтле, 1954 год.
Музей истории и промышленности, Seattle Post-Intelligence Collection, 1986.5.571.1
скрыть заголовок
переключить заголовок
Музей истории и промышленности, Seattle Post-Intelligence Collection, 1986.5.571.1
Мужчина показывает лобовое стекло с ямками полицейскому в Сиэтле, 1954 год
Музей истории и промышленности, Seattle Post-Intelligence Collection, 1986. 5.571.1
5.571.1
Общенациональная странность, которая была тайной питтинга ветрового стекла, началась весной 1954 года. Оглядываясь на сегодняшние события, мы можем получить окно — хорошо, ветровое стекло — на состав и образ мышления Америки середины 20-го века.
Эпицентром эпидемии, согласно HistoryLink — онлайн-сборнику истории штата Вашингтон — был город Беллингхэм, где «крошечные дырочки, ямы и вмятины… по-видимому, появлялись на лобовых стеклах автомобилей с беспрецедентной скоростью» в конце Маршировать.
«Жители в панике», сообщает веб-сайт, подозревали «все, от космических лучей до яиц песчаных блох и осадков от испытаний водородных бомб».
В своей книге «Введение в коллективное поведение и коллективные действия » Дэвид Л. Миллер пишет, что «испытания ядерного оружия и угроза ядерной войны» рассматривались как один из источников беспокойства. Газета Huffington Post позже назвала это «массовой истерией».
Стеклянные дыры вскоре были замечены в других общинах Вашингтона, включая Анакортес и Оук-Харбор. Сообщается, что в середине апреля 1954 года по городу Сиэтл прокатилась странная волна звона лобового стекла.
Сообщается, что в середине апреля 1954 года по городу Сиэтл прокатилась странная волна звона лобового стекла.
Губернатор Вашингтона, группа университетских ученых и даже президент Дуайт Д. Эйзенхауэр были уведомлены о массовой тайне.
Это была раздутая истерия? Имитация вандализма? Странные последствия ядерных испытаний?
Ямы и маятник
В конце концов, в Америке произошли все три явления.
Исторически сложилось так, что массовая истерия в этой стране часто связана с судами над ведьмами 17-го века в Салеме, штат Массачусетс. В середине 19-го века вандализм на кладбище был широко распространен в общинах от Пенсильвании до Теннесси и Огайо. А в 1960-х детей по всей стране предупредили, чтобы они не ели снег из-за возможной радиации от ядерных испытаний.
В штате Вашингтон сотрудники правоохранительных органов тщательно проверили ветровые стекла 15 000 автомобилей в течение 1954 эпизода и, по данным HistoryLink, обнаружил, что более 3000 были повреждены.
В ходе расследования сотрудники правоохранительных органов исключили вандализм и радиоактивные осадки. Представитель криминальной лаборатории полиции Сиэтла, согласно HistoryLink, «заявил, что все отчеты о повреждениях состоят из« 5 процентов хулиганства и 95 процентов публичной истерии ». Жители Пьюджет-Саунд невольно стали участниками хрестоматийного коллективного заблуждения.
Никаких оспин ни на одном доме
В Вашингтоне количество наблюдений уменьшилось. Но, несмотря на то, что Сиэтлу уделялось больше всего внимания, сообщения со всей страны продолжали поступать.
19 апреля 1954 г. о выбоинах на ветровых стеклах сообщалось по крайней мере в девяти штатах и Канаде. на лобовых стеклах их автомобилей.В Маунт-Плезант, штат Мичиган, оспины были обнаружены на стеклах теплиц.В других местах, похоже, были затронуты стекла кабин самолетов.
«Сначала в стекле появляется от 10 до 20 ямок с синими краями, хотя позже может быть различимо до 50 «кратеров», — заметил репортер. «Крошечные отверстия не пробивают стекло, но сообщается о глубине ямки 1/16 дюйма».
«Крошечные отверстия не пробивают стекло, но сообщается о глубине ямки 1/16 дюйма».
Любопытно, что на окнах домов, боковых окнах автомобилей или другом вертикально расположенном стекле не образовалось точечной коррозии. «Это заставило одного наблюдателя поверить в то, что то, что вызывает питтинг, — сообщает INS, — падает прямо с неба, вероятно, на большой высоте».
В Кантоне, штат Огайо, около 1000 жителей уведомили полицию о том, что их лобовые стекла были «непонятным образом повреждены», сообщило 17 апреля Daily Mail из Хагерстауна, штат Мэриленд. 20, что «новые сообщения о загадочных питтингах на лобовом стекле появились сегодня почти так же быстро, как и теории о том, что их вызывает». Канадский ученый предположил, что следы были сделаны скелетами мельчайших морских существ, которые были подняты в воздух в результате испытаний водородной бомбы в Тихом океане.
В штате Юта кто-то предположил, что причиной появления вмятин на лобовом стекле может быть кислота от летающих жуков, но биолог из Университета имени Бригама Янга опроверг эту теорию, сообщила газета Provo Daily Herald от 27 июня. Сообщения о точечной коррозии уменьшились повсюду, и страна перешла к строительству убежищ от радиоактивных осадков на заднем дворе.
Сообщения о точечной коррозии уменьшились повсюду, и страна перешла к строительству убежищ от радиоактивных осадков на заднем дворе.
Но вопрос остается: как насчет этих ямок на лобовом стекле?
Подводные камни СМИ
За советом мы обратимся к социологу из Университета штата Миссури Дэвиду Рохоллу, который более десяти лет читает курсы по социальным движениям и коллективному поведению.
Что послужило причиной ямок на лобовом стекле в Сиэтле и других местах?
«Многое из того, что происходит в обществе, — это игра с числами, — говорит Рохолл. «Если у вас больше людей, любое явление начинает казаться более распространенным, если вы сосредоточитесь на каком-то одном событии или поведении».
Даже то, что случается очень редко, может начать казаться тенденцией, говорит он, «если объединить эти события. В штате Вашингтон миллионы автомобилей, но тысячи случаев питтинга. представляет менее 1 процента автомобилей. Если все ищут и сообщают об этом, это может показаться своего рода заговором».
Если все ищут и сообщают об этом, это может показаться своего рода заговором».
Поскольку имелись физические доказательства выбивания лобового стекла, поместило ли это инциденты в категорию, отличную от других невидимых явлений, которые вызвали коллективное поведение?
Выемки на лобовом стекле, говорит Рохолл, «могут быть больше похожи на круги на полях, в которых есть вещественные доказательства того, что «что-то» произошло, но никто не уверен в причине. Конечно, с тех пор мы нашли доказательства того, что в некоторых случаях , люди используют специальное оборудование, чтобы сделать эти круги на полях. Причина появления ямок в другом, потому что было бы очень трудно поймать того, кто их создает».
Америка все еще подвержена своего рода массовой истерии, которая приведет к подобным событиям?
«Большинство специалистов в этой области больше не верят в массовую истерию как в причину поведения больших групп, — говорит Рохолл. «Идея исходила от Гюстава Ле Бона, французского теоретика, пытавшегося объяснить странное поведение больших групп во время Французской революции, когда рядовые граждане начали убивать большое количество людей с помощью гильотины. Что заставило их совершить такой гнусный поступок? ?»
«Идея исходила от Гюстава Ле Бона, французского теоретика, пытавшегося объяснить странное поведение больших групп во время Французской революции, когда рядовые граждане начали убивать большое количество людей с помощью гильотины. Что заставило их совершить такой гнусный поступок? ?»
Даже если бы эта теория была верна, говорит Рохолл, «она предназначена для применения в ситуациях повышенного эмоционального возбуждения — например, в больших толпах. сомневаюсь, что это было эмоциональное заражение, которое заставляло их действовать определенным образом».
Так что же именно заставило большое количество людей сообщить о щербинах на ветровых стеклах?
«Война миров — прекрасный пример того, как средства массовой информации подчеркивают несколько «реальных случаев» истерии, не признавая, что подавляющее большинство людей знали, что радиопрограмма была выдумкой и ничего не делала», — добавляет Рохолл. «Как и круги на полях, мы знаем, что некоторые из них созданы руками человека, так же как и эти ямы. Однако средства массовой информации, возможно, заставили людей начать замечать ямы, которые уже были там».
Однако средства массовой информации, возможно, заставили людей начать замечать ямы, которые уже были там».
Он сравнивает этот опыт со следующим: «Люди очень часто думают, что заразились болезнью, когда слышат, как врач описывает медицинскую проблему и симптомы, связанные с этой проблемой. Я подозреваю, что у большинства людей уже были эти ямки. и приписывали это таинственной причине только тогда, когда слышали, как это делают другие люди.Третья часть могла быть следствием вандализма или новых случаев от простых аварий — обломков дорог.Это истерия или просто логическое мышление с использованием информации из СМИ и их собственная ситуация — машина с ямками? Некоторые исследования предполагаемой «истерии» действительно показывают, что люди вовсе не истеричны».
Следуй за мной @NPRHistoryDept; напишите мне по адресу [email protected]
Модель фазового поля кинетики точечной коррозии в металлических материалах
Рассмотренная система и электрохимические реакции
Исследуемая система состоит из нержавеющей стали 304 (SS304) в разбавленной соленой воде (рис. 1). Предполагается, что в этой системе не будет образовываться новая пассивная пленка. Мы рассмотрим эффекты формирования пассивной пленки в будущем исследовании. В этой модели рассматриваются следующие электрохимические реакции и кинетика. 9-$$
1). Предполагается, что в этой системе не будет образовываться новая пассивная пленка. Мы рассмотрим эффекты формирования пассивной пленки в будущем исследовании. В этой модели рассматриваются следующие электрохимические реакции и кинетика. 9-$$
В дальнейшем M e используется для представления эффективного металла в SS304 со средним зарядовым числом z 1 . Свойства материала SS304, такие как молярная концентрация в твердой фазе ( c твердая фаза = 143 моль / л), 12 концентрация насыщения в электролите ( c насыщенная = 4,1 моль / л), 29349 моль / л эффективный коэффициент диффузии ( D 1 = 8,5 × 10 −10 9-$$
(1)
Предполагается, что анодное растворение металла подчиняется уравнению Батлера–Фольмера,
$$i_a = i_0\left[ {\exp \left( {\frac{{\alpha _az_1F\ varphi _{s,o}}}{{R_gT}}} \right) — \exp \left( { — \frac{{\alpha _cz_1F\varphi _{s,o}}}{{R_gT}}} \ right)} \right]$$
(2)
где F – постоянная Фарадея, R g – газовая постоянная, T – температура, φ 1, с – поляризационное перенапряжение, 9+$$
(8)
Константы равновесия реакций в уравнениях (7) и (8) определяются как К 1 и К 2 соответственно.
$$K_1 = \frac{{k_{1f}}}{{k_{1b}}},\,K_2 = \frac{{k_{2f}}}{{k_{2b}}}$$
где k 1f , k 1b , k 2f и k 2b — скорости прямой и обратной реакции. Таким образом, всего в этой модели рассматривается шесть разновидностей ионов, 9{z_6} = c_6$$
, где z i ( i = 1, 2, ……6) – зарядовые числа соответствующих видов (их значения приведены в табл. 2s), а c i (i = 1, 2, ……6) – нормированные концентрации соответствующих видов. Нормированная концентрация c i определяется по0613 C твердый для i = 1,2,…,6, где C i представляет собой молярную концентрацию ионных частиц. Константы K 1 и K 2 также могут быть выражены как функция C i .
$$K_1 = C_2C_5/C_1,\,K_2 = C_5C_6$$
Модель фазового поля для коррозии
Поверхность металла обычно покрыта пассивирующей пленкой; однако может произойти частичный пробой пленки, что может привести к образованию ямок, подобных показанной на рис. 1. Модель состоит из двух фаз: твердой фазы M e (т.е. металлическая часть) и жидкая фаза (т.е. электролитная часть). Движущей силой коррозии металлов и эволюции микроструктуры является минимизация полной свободной энергии системы, которая обычно состоит из объемной свободной энергии E b , энергии интерфейса E i и энергий дальнодействующего взаимодействия, таких как как энергия упругой деформации E s и электростатическая энергия E e . 36,37 Полная энергия системы может быть выражена как
1. Модель состоит из двух фаз: твердой фазы M e (т.е. металлическая часть) и жидкая фаза (т.е. электролитная часть). Движущей силой коррозии металлов и эволюции микроструктуры является минимизация полной свободной энергии системы, которая обычно состоит из объемной свободной энергии E b , энергии интерфейса E i и энергий дальнодействующего взаимодействия, таких как как энергия упругой деформации E s и электростатическая энергия E e . 36,37 Полная энергия системы может быть выражена как
$$E = E_b + E_i + E_s + E_e$$
(9)
Включение упругой и/или пластической деформации в модель вполне осуществимо, поскольку сделано в других системах. 38,39,40 Может быть даже необходимо включить термин энергии деформации, если во время коррозии образуется объемная несовместимая пассивная пленка. Поскольку на первом этапе данной работы не будет рассматриваться формирование пассивной пленки, для простоты здесь не рассматривается энергия упругой деформации. В следующем разделе влияние приложенного или остаточного напряжения на точечную коррозию будет изучено с использованием концепции перенапряжения, а не энергии деформации. Сейчас у нас 92 + z_1FC_1\varphi } \right]} dV$$
В следующем разделе влияние приложенного или остаточного напряжения на точечную коррозию будет изучено с использованием концепции перенапряжения, а не энергии деформации. Сейчас у нас 92 + z_1FC_1\varphi } \right]} dV$$
(11)
где f b ( c 1 , η ), выводится в следующем локальном разделе плотность свободной энергии, которая является функцией нормированной концентрации ионных частиц c 1 и параметра порядка η ; второй член в уравнении (11) представляет плотность энергии градиента, которая вносит вклад в межфазную энергию, в которой α u — коэффициент энергии градиента, который связан с физическими параметрами в следующем разделе; и третий член в уравнении. (11) представляет плотность электростатической энергии, где C 1 — молярная концентрация иона металла, а φ — электростатический потенциал.
Объемная плотность свободной энергии
Для определения объемной плотности свободной энергии f b ( c 1 , η ) мы используем модель, предложенную Kim et al. для бинарных сплавов. 35 Мы выбрали модель KKS, потому что модель имеет меньше ограничений по толщине интерфейса по сравнению с некоторыми другими моделями, такими как модель, представленная моделью Wheeler et al. 41 Подробные выводы всех функций в модели KKS здесь опущены, и читатели могут обратиться к оригинальной статье. 35 В модели KKS параметры модели могут быть определены аналитически по свойствам материала и экспериментальным условиям для рассматриваемой системы. В модели KKS в каждой точке материал рассматривается как смесь двух сосуществующих фаз, и всегда предполагается локальное равновесие между двумя фазами:
для бинарных сплавов. 35 Мы выбрали модель KKS, потому что модель имеет меньше ограничений по толщине интерфейса по сравнению с некоторыми другими моделями, такими как модель, представленная моделью Wheeler et al. 41 Подробные выводы всех функций в модели KKS здесь опущены, и читатели могут обратиться к оригинальной статье. 35 В модели KKS параметры модели могут быть определены аналитически по свойствам материала и экспериментальным условиям для рассматриваемой системы. В модели KKS в каждой точке материал рассматривается как смесь двух сосуществующих фаз, и всегда предполагается локальное равновесие между двумя фазами:
$$c_1 = h\left( \eta \right)c_s + \left[ {1 — h\left( \eta \right)} \right]c_l$$
(12)
$$\partial f_s\left( {c_s} \right)/\partial c_s = \partial f_l\left( {c_l} \right)/\partial c_l$$
(13)
где c s и c l представляют собой нормированные концентрации твердой и жидкой фаз соответственно; ч(η) — монотонно меняющаяся функция от ч (0) = 0 до ч (1) = 1. В этом исследовании предполагается, что ч ( η ) = η 2 (−2 η ). В уравнении (13) плотности свободной энергии твердой и жидкой фаз выражаются как f s ( c s ) и f l ( c l ) соответственно. Поскольку концентрация считается смесью твердой и жидкой фаз в каждой точке, следуя тому же аргументу, объемная плотность свободной энергии твердой и жидкой фаз выражается аналогичным образом
В этом исследовании предполагается, что ч ( η ) = η 2 (−2 η ). В уравнении (13) плотности свободной энергии твердой и жидкой фаз выражаются как f s ( c s ) и f l ( c l ) соответственно. Поскольку концентрация считается смесью твердой и жидкой фаз в каждой точке, следуя тому же аргументу, объемная плотность свободной энергии твердой и жидкой фаз выражается аналогичным образом
$$f_b(c_1,\eta) = h\left( \eta \right)f_s(c_s) + \left[ {1 — h\left( \eta \right)} \right]f_l(c_l) + wg(\eta )$$
(14)
Это потенциал двойной ямы в энергетическом пространстве. Высота потенциала двойной ямы равна 90 613 w 90 614 и 90 613 g 90 614 ( 90 613 η 90 614 ) = 90 613 η 90 614 90 348 2 90 349 (1 − 90 613 η 90 614 ) 90 343 9
9 . Это выражение имеет два минимума при
η = 0 и η = 1, которые соответствуют фазе электролита и твердой фазе. 92 $$
92 $$
(16)
, где C EQ, S = 1 и C EQ, L = C SAT / C 1111111111111111111111111111111111111 собой СИЛИ. твердая и жидкая фазы соответственно. Зависящая от температуры константа пропорциональности плотности свободной энергии A считается одинаковой как для жидкой, так и для твердой фаз. Его значение рассчитывается таким образом, чтобы движущая сила коррозии металла в аппроксимированной результирующей системе была достаточно близка к силе исходной термодинамической системы. 42
Эволюция параметра фазового порядка η и концентрации ионов металлов c 1 во времени и пространстве подчиняется закону Гинзбурга–Ландау (также известному как Аллена–Кана) 43 и Кана– Хиллиарда 44 уравнений соответственно.
$$\frac{{\partial \eta}}{{\partial t}} = — L\frac{{\delta E}}{{\delta \eta}} = L\left[ {\nabla \ alpha _u\nabla \eta + h\prime \left( \eta \right)\left\{ {f_l\left( {c_l} \right) — f_s\left( {c_s} \right) — \left( {c_l — c_s} \right)\frac{{\partial f_l\left( {c_l} \right)}}{{\partial c_l}}} \right\} — wg\prime \left( \eta \right)} \ справа]$$
(17)
$$\begin{array}{*{20}{l}} {\ frac {{\ partial {\ mathrm {c}} _1}} {{\ partial {\ mathrm {t} }}}} \hfill & = \hfill & {\nabla M\nabla \frac{{\delta E}}{{\delta c_1}} + R_1} \hfill \cr {} \hfill & = \hfill & { \nabla \left[ {D_1\left( \eta \right)\nabla c_1} \right] + \nabla \left[ {D_1\left( \eta \right)h\prime \left( \eta \right)\ влево( {c_l — c_s} \right)\nabla \eta } \right]} \hfill \cr {} \hfill & {} \hfill & {+ \nabla \left[ {\ frac {{z_1Fc_1D_1\left( \ eta \right)}}{{R_gT}}\nabla \varphi } \right]y_1\left( \eta \right) + R_1} \hfill \end{array}$$ 92)\). В уравнении (18), R 1 является членом источника и/или стока для ионов металлов в результате реакции (уравнение (7)), и он принимает форму (− k 1 f c 1 + k 1 b c 2 c 5 ) y 1 ( u ). Функция y 1 (η ), определенная ниже, должна гарантировать, что реакция (уравнение (7)) происходит только в фазе электролита.
В уравнении (18), R 1 является членом источника и/или стока для ионов металлов в результате реакции (уравнение (7)), и он принимает форму (− k 1 f c 1 + k 1 b c 2 c 5 ) y 1 ( u ). Функция y 1 (η ), определенная ниже, должна гарантировать, что реакция (уравнение (7)) происходит только в фазе электролита.
$${\mathrm{y}}_1\left( \eta \right) = \left\{ {\begin{array}{*{20}{l}} {1;} \hfill & {\eta \le 0} \hfill \cr {} \hfill & {0 < \eta < 0,1} \hfill \cr {0;} \hfill & {\eta \ge 0,1} \hfill \end{массив}} \right. \left( {\mathrm{линейно}}\,{\mathrm{изменение}}\,{\mathrm{от}}1\,{\mathrm{к}}\,0} \right)$$
(19)
Сохранение заряда
В этом исследовании мы следуем работе Дассо, а не модели Гайера 45,46 , которая упрощает модель, устраняя необходимость дискретизации двойного слоя на границе металл-электролит. Это позволяет нашей модели PF моделировать процесс коррозии от мезо- до макромасштабов по сравнению с моделью Гайера, которая была ограничена наномасштабом. Также можно учесть влияние ламинарного/турбулентного течения электролита на границу раздела металл-электролит в случае движущегося электролита. 47 Здесь закон сохранения заряда можно выразить как 1 — y_1\left( \eta \right)} \right]\nabla \varphi } \right\} + y_1\left( \eta \right)FC_{solid}{\sum} {z_i} \frac{{\ парциальный c_i}}{{\partial t}}$$
Это позволяет нашей модели PF моделировать процесс коррозии от мезо- до макромасштабов по сравнению с моделью Гайера, которая была ограничена наномасштабом. Также можно учесть влияние ламинарного/турбулентного течения электролита на границу раздела металл-электролит в случае движущегося электролита. 47 Здесь закон сохранения заряда можно выразить как 1 — y_1\left( \eta \right)} \right]\nabla \varphi } \right\} + y_1\left( \eta \right)FC_{solid}{\sum} {z_i} \frac{{\ парциальный c_i}}{{\partial t}}$$
(20)
где ρ e — плотность заряда, а σ e — электропроводность металла в твердой фазе. Функция [1 − y 1 ( η )] интерполирует электропроводность σ e в твердой фазе до нуля в фазе электролита, где y 1 η . (19). Время, необходимое для накопления заряда на границе раздела из-за диффузии ионных частиц, намного больше, чем время, необходимое для достижения стационарного накопления заряда на границе раздела, поэтому сохранение заряда в вышеуказанной системе можно рассматривать в стационарном состоянии. Отношение, данное в уравнении (20) уменьшается до
Отношение, данное в уравнении (20) уменьшается до
$$0 = \nabla \left\{ {\sigma _e\left[ {1 — y_1\left( \eta \right)} \right]\nabla \varphi} \right\} + y_1(\eta)FC_ {solid}{\sum} {z_i} \frac{{\partial c_i}}{{\partial t}}$$
(21)
Коэффициент градиентной энергии
Высота потенциала двойной ямы w а коэффициент энергии градиента α u может быть связан с энергией границы раздела ϱ и толщиной интерфейса l 33
$${\it{\varrho}} = 4\sqrt {w\alpha _u}$$
(22)
$$l = \sqrt 2 \alpha \prime \sqrt {\frac{{ \alpha _u}}{w}}$$
(23)
где α ′ — постоянная величина, определяемая параметром порядка u . Если область интерфейса определяется как 0,05 < η < 0,95; значение α ′ равно 2,94. 35
Уравнения переноса для других ионных частиц в электролите
Основными уравнениями для других пяти ионных частиц являются уравнения Нернста-Планка с членами химической реакции. Они выражены как
Они выражены как
$$\frac{{\partial {\mathrm{c}}_2\left({{\boldsymbol{x}},t} \right)}}{{\partial {\mathrm{t}}}} = \nabla \left[ {D_2\left( \eta \right)\nabla c_2} \right] + \nabla \left[ {\frac{{z_2Fc_2D_2\left( \eta \right)}}{{R_gT}} \nabla \varphi } \right]y_1\left( \eta \right) + R_2$$
(24)
$$\frac{{\partial {\mathrm{c}}_3\left({{\ boldsymbol{x}},t} \right)}}{{\partial {\mathrm{t}}}} = \nabla \left[ {D_3\left( \eta \right)\nabla c_3} \right] + \nabla \left[ {\frac{{z_3Fc_3D_3\left(\eta \right)}}{{R_gT}}\nabla \varphi} \right]y_1\left(\eta \right)$$
(25)
$$\frac{{\partial {\mathrm{c}}_4\left({{\boldsymbol{x}},t} \right)}}{{\partial {\mathrm{ t}}}} = \nabla \left[ {D_4\left( \eta \right)\nabla c_4} \right] + \nabla \left[ {\frac{{z_4Fc_4D_4\left( \eta \right)}} {{R_gT}}\nabla \varphi} \right]y_1\left( \eta \right)$$
(26)
$$\frac{{\partial {\mathrm{c}}_5\left( {{\boldsymbol{x}},t} \right)}}{{\partial {\mathrm{t}}}} = \nabla \left[ {D_5\left( \eta \right)\nabla c_5} \ right] + \nabla \left[ {\frac{{z_5Fc_5D_5\left( \eta \right)}}{{R_gT}}\nabla \varphi} \right]y_1\left(\eta \right) + R_5$$
(27)
$$\frac{{\partial {\mathrm{c}}_6\left({{\boldsymbol{x}},t} \right)}}{{\partial {\mathrm{ t}}}} = \nabla \left[ {D_6\left( \eta \right)\nabla c_6} \right] + \nabla \left[ {\frac{{z_6Fc_6D_6\left( \eta \right)}} {{R_gT}}\nabla \varphi } \right]y_1\left( \eta \right) + R_6$$
(28)
, где R 2 — термин источник/сток, полученный из электрохимической реакция в уравнении (7) которая принимает вид [ k 1 f c 1 − k 1 b c 2 c 5 ] y 1 ( η ). Скорости прямой и обратной реакции выражаются как k 1 f и k 1 b соответственно. Предполагается, что внутри металлической детали не происходит электрохимической реакции. Это обеспечивается b y y 1 ( η ), определенный в уравнении. (19). R 5 и R 6 являются условиями источника/стока, возникающими в результате электрохимических реакций в уравнениях. (7) и (8) и принять вид \(\left[ {k_{1f}c_1 — k_{1b}c_2c_5 + k_{2f} — k_{2b}c_5c_6} \right]y_1\left( \eta \right) — \left( {\frac{{J_5}}{{z_5FC_{solid}}}} \right)y_2\left( \eta \right)\) и \(\left[ {k_{2f} — k_{2b}c_5c_6} \right]y_1\left( \eta \right) — \left( {\frac{{J_6}}{{z_6FC_{solid}}}} \right)y_2\left( \eta \right )\) соответственно. Скорости прямой и обратной реакций гидролиза воды представлены к 2f и к 2b соответственно. Следует отметить, что R 5 и R 6 имеют дополнительный член вблизи границы металл–электролит из-за катодных реакций, рассматриваемых в уравнениях.
Скорости прямой и обратной реакции выражаются как k 1 f и k 1 b соответственно. Предполагается, что внутри металлической детали не происходит электрохимической реакции. Это обеспечивается b y y 1 ( η ), определенный в уравнении. (19). R 5 и R 6 являются условиями источника/стока, возникающими в результате электрохимических реакций в уравнениях. (7) и (8) и принять вид \(\left[ {k_{1f}c_1 — k_{1b}c_2c_5 + k_{2f} — k_{2b}c_5c_6} \right]y_1\left( \eta \right) — \left( {\frac{{J_5}}{{z_5FC_{solid}}}} \right)y_2\left( \eta \right)\) и \(\left[ {k_{2f} — k_{2b}c_5c_6} \right]y_1\left( \eta \right) — \left( {\frac{{J_6}}{{z_6FC_{solid}}}} \right)y_2\left( \eta \right )\) соответственно. Скорости прямой и обратной реакций гидролиза воды представлены к 2f и к 2b соответственно. Следует отметить, что R 5 и R 6 имеют дополнительный член вблизи границы металл–электролит из-за катодных реакций, рассматриваемых в уравнениях. (3) и (5), где J 5 и J 6 определены в уравнениях. (4) и (6) соответственно. Эти члены реакции умножаются на ступенчатую функцию y 2 ( η ), чтобы гарантировать, что эти реакции происходят только в небольшой области вблизи поверхности металла.
(3) и (5), где J 5 и J 6 определены в уравнениях. (4) и (6) соответственно. Эти члены реакции умножаются на ступенчатую функцию y 2 ( η ), чтобы гарантировать, что эти реакции происходят только в небольшой области вблизи поверхности металла.
$${\mathrm{y}}_2\left( \eta \right) = \left\{ {\begin{array}{*{20}{l}} {1;} \hfill & {0,01 \ le \eta < 0,05} \hfill \cr {0;} \hfill & {\eta \ge 0,05} \hfill \cr {0;} \hfill & {\eta < 0,01} \hfill \end{массив}} \ справа.$$
(29)
Следует также отметить, что в уравнениях. (25) и (26) условия источника/стока отсутствуют, поскольку предполагалось, что c 3 (Cl — ) и c 4 (Na + ) ни в каких реакциях не участвует. Это неверно, если может образоваться солевая пленка. Эффект образования солевой пленки будет изучен в будущем исследовании.
Электростатический потенциал φ определяется уравнением (21) в сочетании с управляющими уравнениями. (18) и (24–28). Коэффициент диффузии D i является функцией параметра порядка η . Как известно, диффузионная способность ионных частиц различается в металлической и электролитной фазах. Коэффициенты диффузии всех ионов определялись с помощью ступенчатой функции параметра порядка η . Для иона металла c 1 ступенчатая функция, выраженная в уравнении используется (30), в котором значение коэффициента диффузии в металле принимается в γ раз меньше, чем в электролите. Ступенчатая функция, выраженная в уравнении (31) используется для всех других ионных видов ( C 2 , C 3 , C 4 , C 5 и .
(18) и (24–28). Коэффициент диффузии D i является функцией параметра порядка η . Как известно, диффузионная способность ионных частиц различается в металлической и электролитной фазах. Коэффициенты диффузии всех ионов определялись с помощью ступенчатой функции параметра порядка η . Для иона металла c 1 ступенчатая функция, выраженная в уравнении используется (30), в котором значение коэффициента диффузии в металле принимается в γ раз меньше, чем в электролите. Ступенчатая функция, выраженная в уравнении (31) используется для всех других ионных видов ( C 2 , C 3 , C 4 , C 5 и .
$${\mathrm{D}}_1\left( \eta \right) = \left\{ {\begin{array}{*{20}{l}} {D_1;} \hfill & {\eta < 0,90} \hfill \cr {} \hfill & {0,90 \le \eta \le 0,95} \hfill \cr {D_1/\gamma ;} \hfill & {\eta > 0,95} \hfill \end{массив}} \ вправо. \, \ влево ( {\ mathrm {линейно}} \, {\ mathrm {изменение}} \, {\ mathrm {от}} \, D_1 {\ mathrm {к}} \, D_1/\ gamma} \right)$$
(30)
$${\mathrm{D}}_{\mathrm{i}}\left({\mathrm{\eta}} \right) = \left\{ {\ begin{array}{*{20}{l}} {{\mathrm{D}}_{\mathrm{i}};} \hfill & {\eta < 0,90} \hfill \cr {} \hfill & { 0,90 \le \eta \le 0,95} \hfill \cr {0;} \hfill & {\eta > 0,95} \hfill \end{массив}} \right. \,\left( {\mathrm{linearly}}\,{\mathrm{change}}\,{\mathrm{from}}\,D_i\,{ \mathrm{to}}\,0} \right)$$
\,\left( {\mathrm{linearly}}\,{\mathrm{change}}\,{\mathrm{from}}\,D_i\,{ \mathrm{to}}\,0} \right)$$
(31)
for i = 2,3,….,6.
Перенапряжение
Перенапряжение выражается как
$$\varphi _{s,o} = \varphi _m — \varphi _{m,se} — \varphi _c — \varphi _l$$
(32)
, где φ m — потенциал в металлической фазе, также известный как приложенный потенциал; ф 9{z_1}\) рядом с интерфейсом,
$$c_{1b} = \left\{ {\begin{array}{*{20}{l}} {c_1;} \hfill & {\left( { \eta = 0,05} \right)} \hfill \cr {0;} \hfill & {\left({\eta < 0,05} \right)} \hfill \cr {0;} \hfill & {\left({ \eta > 0.05} \right)} \hfill \end{array}} \right.$$
(34)
Электростатический потенциал вблизи границы раздела равен,
$$\varphi _l = \left\{ { \begin{array}{*{20}{l}} {\varphi;} \hfill & {\left({\eta = 0,05} \right)} \hfill \cr {0;} \hfill & {\left ( {\eta < 0,05} \right)} \hfill \cr {0;} \hfill & {\left( {\eta > 0,05} \right)} \hfill \end{array}} \right.


 68±0,19
68±0,19 .0,6
.0,6