Типы коррозии: Виды коррозии | Руководство по выбору материалов
Содержание
Типы коррозии металла: атмосферная, почвенная, щелевая
В технической терминологии под понятием «коррозия» понимают разрушение разных видов металлов вследствие их взаимодействия с атмосферными факторами. Скорость развития и масштабность распространения коррозии обусловлена разными причинами.
Именно поэтому сегодня не существует универсальных способов защиты металлоконструкций от негативного воздействия коррозийных процессов. Однако в зависимости от разновидности коррозийного процесса используются разные технологические решения.
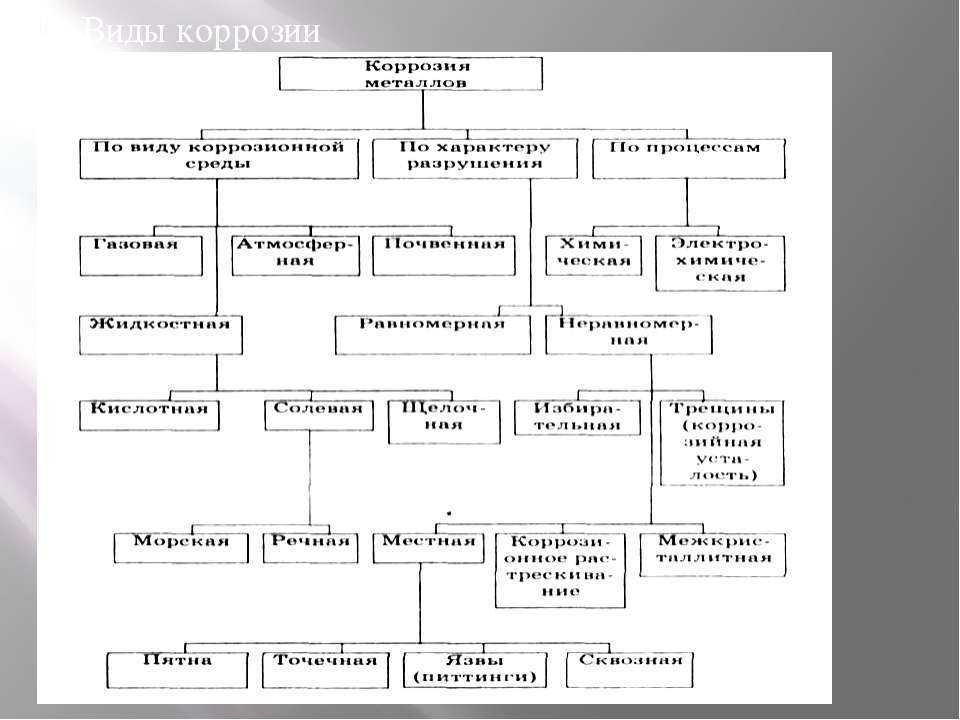
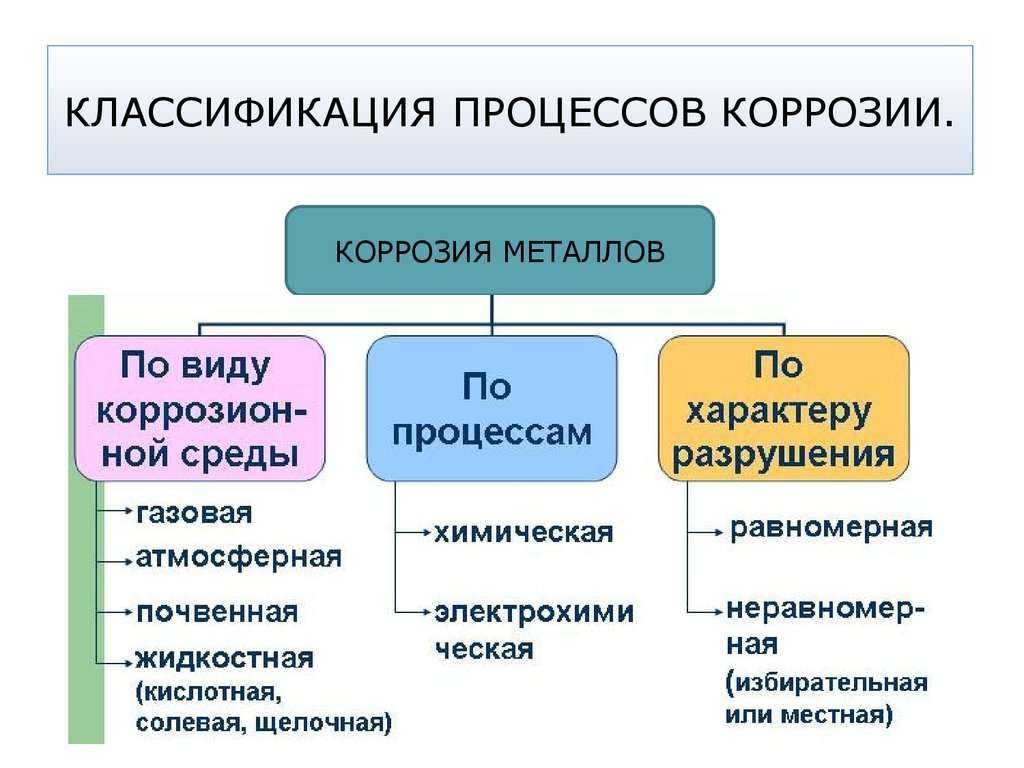
На основании показателя активности и скорости протекания выделяют отдельные типы коррозии металлов – химическая и электрохимическая. В первом случае реакция наблюдается вследствие взаимодействия металла со средой с минимальной электропроводимостью. Благодаря этому во время реакции отсутствует эффект электростатики.
Во втором случае реакция протекает при воздействии на металл среды с высокой электрической проводимостью (электролит). Как правило, электрохимическая реакция возникает в воде, атмосфере и почве, а также в кислотных, солевых и щелочных растворах.
Классификация коррозии в зависимости от типа окружающей среды
Атмосферная коррозия
Это один из самых распространенных видов коррозии, который в зависимости от объема влаги, воздействующей на металлическую поверхность, также классифицируется как мокрая, сухая и влажная коррозия. При этом в зависимости от агрессивности атмосферы выделяют следующие виды атмосферной коррозии, которая может проявляться:
- в промышленности;
- сельской местности;
- приморских районах;
- при специфическом загрязнении окружающей среды.
Главные особенности атмосферной коррозии проявляются в скорости ее распространения. На этот фактор оказывают влияние такие параметры, как температура, уровень влажности, состав металла, качество его поверхности, особенности состава окружающей среды, а также другие параметры.
Почвенная коррозия
Коррозийные процессы, проходящие с металлами в грунте или под землей, оказывают на их эксплуатационные характеристики разрушительное воздействие. Существует не только почвенная коррозия металлов, но также процесс, который возникает после воздействия внешних и блуждающих электротоков.
Существует не только почвенная коррозия металлов, но также процесс, который возникает после воздействия внешних и блуждающих электротоков.
Под напряжением коррозийные процессы протекают вследствие одновременного воздействия на поверхность металлоконструкций коррозийной среды и механических напряжений. Как следствие, на поверхности металлоконструкции может наблюдаться коррозийное растрескивание или коррозийная усталость. Это зависит от вида и интенсивности напряжения.
Щелевая коррозия металла
Щелевая коррозия развивается вследствие контакта изделий в электропроводящих средах, имеющих разные электрохимические характеристики. Помимо этого различают коррозийные процессы в зависимости от разновидности и сложности вызываемых повреждений – это сплошная (или общая) и местная (или локальная) коррозия.
Между тем, сплошная коррозия может быть равномерной (процесс проходит с одинаковой скоростью по всей площади металлоконструкции) и неравномерной (на разных участках детали процесс протекает с разной скоростью).
Локальный коррозийный процесс классифицируют на сосредоточенный (проявляется в виде пятен, язв, точек и др.) и подповерхностный (транс- и межкристаллитный, структурно-избирательный).
Более опасной и разрушительной считается локальная коррозия, поскольку она образует дефекты (свищи и трещины в стенах емкостей и трубопроводов), которые стремительно снижают прочностные и функциональные характеристики конструкции.
Если же говорить об изделиях, поверхность которых обработана по технологии горячего цинкования, то в данном случае большую угрозу несет общая коррозия. Она вызывает разрушение защитного слоя, что приводит к утрате изделием первоначального привлекательного внешнего вида.
Также для продукции, имеющей цинковый слой, нанесенный горячим цинкованием, опасность несет коррозия под напряжением (разрушение происходит на наиболее напряженных участках детали) и точечная (питтинговая) коррозия (по аналогичным причинам).
Заказывайте оцинковку металла в Точинвест Цинк
Каждый клиент при обращении в нашу компанию получает следующие преимущества:
- Компания работает с 2007 года, имеет в своем распоряжении 3 производственных цеха для горячего цинкования.

- Мощность предприятия с многолетним опытом составляет 120 000 тонн в год.
- Оперативное проведение работ, независимо от сложности и объема.
- Наше предприятие является обладателем самой глубокой ванны для горячего цинкования в ЦФО – глубина составляет 3.43 м.
- Наносим цинковое покрытие на различные виды металлоконструкций, включая габаритные.
- Нанесение покрытия по технологии горячего цинкования специалисты выполняют в соответствие с требованиями ГОСТ 307-89.
Работы проводятся на современном оборудовании чешской компании EKOMOR и немецко-австрийской компании KVK KOERNER.
Вернуться к статьям
Поделиться статьей
Типы коррозии
Типы коррозии
Основные причины возникновения коррозии:
- Из-за процессов, связанных с воздействием на металл – очищение, изготовление холодная штамповка, термическая обработка. Любое действие, связанное с затрагиванием структуры, влечет риск появления ржавления.
 Эти факторы запускаются еще на этапе производства, задолго до того, как деталь или прокат будут упакованы и отправлены конечному потребителю;
Эти факторы запускаются еще на этапе производства, задолго до того, как деталь или прокат будут упакованы и отправлены конечному потребителю; - Из-за некорректной упаковки. Такие материалы как гофрокартон и бумага впитывают влагу, удерживают ее, а затем отдают упакованной продукции. В итоге, вместо того, чтобы предохранять товары, тара приносит больше проблем, чем пользы;
- Агрессивное воздействие окружающей среды, перепады температур и влажности, воздействие кислотных сред, и атмосферных осадков также способствуют появлению ржи.
Компания LIKKOR, являясь одним из лидеров в производстве продуктов для защиты от коррозии, признает, что предлагать высококачественный и эффективный продукт – это только половина дела. Качественное обслуживание клиентов, удовлетворение их запросов на получение технологичного продукта, не менее важно и относится к одним из основных постулатов нашей миссии.
Мы постоянно разрабатываем полезные материалы для клиентов, помогая им бороться с возникновением порчи продукции. Мы рекомендуем нашим клиентам идентифицировать вид ржавчины, которая появляется в процессе производства или доставки. Знание типов коррозии помогает определить причину их возникновения.
Мы рекомендуем нашим клиентам идентифицировать вид ржавчины, которая появляется в процессе производства или доставки. Знание типов коррозии помогает определить причину их возникновения.
Красная ржавчина
Представляет собой гидратированный оксид железа трехвалентный Fe2O3 • h3O или Fe2O3
Она имеет красный цвет и считается наиболее опасным вариантом из всех имеющихся. В отличии от других окислений, при этом типе открываются все новые слои для разрушения, а в его толще образуются гидроксид Fe. Порча может продолжать свой «рост» до полнейшего распада металлоконструкции.
- Красные «язвы» итог длительного влияния О2 и влаги, смешанных с загрязнениями (солью).
- Этот тип относится к атмосферным, потому что обычно на металлических деталях и оборудовании, где он появился нет следов разводов;
- При этом окислении наблюдается равномерное разрушение, затрагивающее всю площадь.
Желтая ржавчина
Она также называется оксид-гидроксид железа FeO (OH) h3O
Появляется в среде, где есть влага, но мало кислорода, например, под водой. Вещество, образованное от окисления железа трехвалентного – растворимый оксид, и приводит к желтому ржавлению.
Вещество, образованное от окисления железа трехвалентного – растворимый оксид, и приводит к желтому ржавлению.
- Находят в утопленных участках металлических деталей оборудования, где «течет и капает» (сольватированная коррозия).
- Также образуется от высокого содержания влаги. Например, ее легко увидеть на автомобиле, если машина долго стояла в луже.
Коричневая ржавчина
Имеет название оксид Fe2O3
Ржа от оксидов железа трехвалентного при высоком содержании кислорода и небольшой влажности приводит к бурой.
- Она считается более «сухой», чем упомянутые выше.
- Порча относится к атмосферным. Считается итогом действия жидкости и кислорода, содержащихся в воздушной смеси, и представляет собой красновато-коричневую корку на верхнем слое металла.
- Считается локализованным окислением. Оно проявляется в виде неоднородных пятен только в определенных областях и считается последствием загрязнения на поверхности металла, часто возникающего в процессе производства.

Черная ржавчина
Имеет название оксид железа четырехвалентный Fe3O4
Ржа от трехвалентных продуктов окисления, при ограниченном доступе воздуха и низкой влажности, приводит к «рождению» черной.
- Она визуально идентифицируется как тонкая темная пленка, и является результатом нахождения в среде с низким содержанием О2.
- На участках с ней было что-то, что препятствовало проникновению воздуха.
Сочетание видов
Возможно появление множественных форм коррозии: они часто присутствуют на металлоконструкциях одновременно
- Бурое поражение является итогом действия атмосферных условий.
- В местах, где присутствует черное, влажная бумага часто плотно прилегает к металлоизделию.
- Разрушение желтого цвета часто возникает в среде, где есть жидкости.
Хотите избавиться от коррозии? Обратитесь к специалистам LIKKOR. У нас есть ассортимент продукции, которая надежно предотвратит порчу оборудования, конструкций и деталей.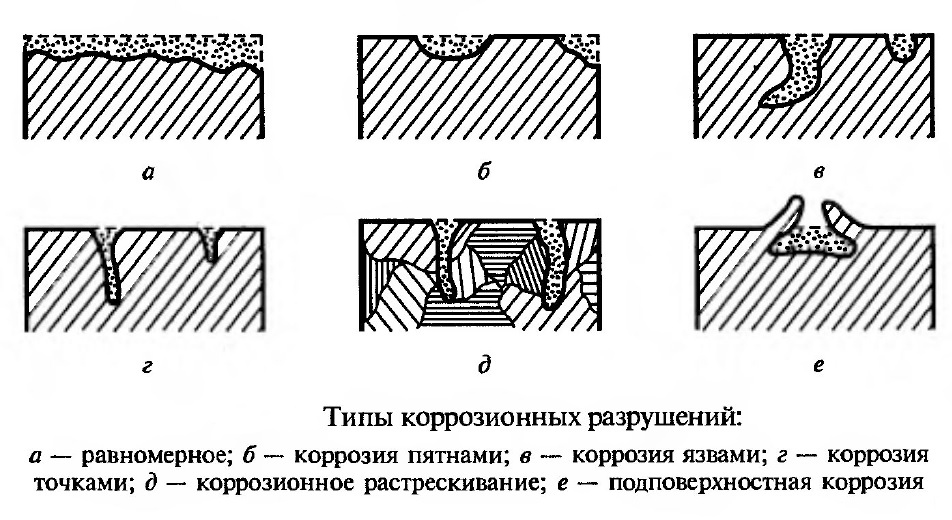 Вы сможете предотвратить убытки, сохранить продукцию при хранении и перевозках. Звоните нам для заказа и консультаций.
Вы сможете предотвратить убытки, сохранить продукцию при хранении и перевозках. Звоните нам для заказа и консультаций.
Обучение технологии
Она достаточно проста, при желании заказчика мы организуем однодневный выездной тренинг и обучим персонал работе с пленкой и оборудованием!
Отправляя заявку вы соглашаетесь с политикой конфиденциальности
Информация
Закажите звонок
Отправляя заявку вы автоматически соглашаетесь с политикой конфиденциальности сайта
Закажите прайс-лист
Отправляя заявку вы автоматически соглашаетесь с политикой конфиденциальности сайта
Закажите тренинг
Отправляя заявку вы автоматически соглашаетесь с политикой конфиденциальности сайта
Название заказа
Описание заказа
Отправляя заявку вы автоматически соглашаетесь с политикой конфиденциальности сайта
Авторизация
Просмотр изображения
Виды коррозии, защита и хранение металлических изделий
Несоблюдение правил хранения может привести к порче продукции. Гарантия производителя на изделия из оцинкованной стали предоставляется только в том случае, если соблюдены все условия транспортировки, хранения и монтажа изделий.
Гарантия производителя на изделия из оцинкованной стали предоставляется только в том случае, если соблюдены все условия транспортировки, хранения и монтажа изделий.
Основой оцинкованных изделий служит стальной лист, на котором под внешним воздействием атмосферы возможно возникновение коррозии. Чтобы этого избежать тонколистый стальной прокат обработан несколькими защитными слоями: цинковым и несколькими полимерными покрытиями, которые препятствуют прямому контакту стали с внешней средой.
Если оцинкованная сталь подвергается воздействию влаги (дождь, роса, конденсат) в среде, где не хватает кислорода, то вода быстро реагирует с цинком и постепенно разъедает покрытие. Наиболее распространённые условия, в которых появляется белая ржавчина, — изделия хранятся в заводской упаковке и/или плотно прижатыми друг к другу.
Физико-химические процессы разрушения металла
Коррозия — это самопроизвольно протекающий процесс разрушения металла, вследствие химического или электрохимического взаимодействия металла с окружающей средой.
Различают химическую и электрохимическую коррозию.
Химическая коррозия — коррозия металла в газовой и жидкостной среде, не проводящей ток. Коррозия этого вида состоит в окислении металла в результате непосредственного его химического взаимодействия с окружающей средой. В таких средах, как воздух, продукты сгорания каменного угля и других видов топлива (нефть, бензин, керосин, смазочные масла) обычно развивается химическая коррозия.
Но наличие даже небольших количеств влаги в указанных веществах может в большей или меньшей степени сообщить коррозии электрохимический характер. Химическая коррозия в чистом виде — достаточно специфическое явление, преобладающее в средах, достаточно закрытых для окружающего природного воздействия. Большое практическое значение имеет электрохимическая коррозия.
Электрохимическая коррозия
Электрохимическая коррозия имеет характер анодного окисления металла, которое может протекать по двум различным механизмам:
– гальванокоррозия — окисление металла, являющегося анодом самопроизвольно возникающей гальванической цепи;
– электрокоррозия — окисление металла, являющегося анодом своеобразной электролизной системы, самопроизвольно возникающей под влиянием тока от внешнего источника.
Гальванокоррозия
При гальванокоррозии основная масса металла обычно играет роль анода. В качестве материала катода могут служить самые разнообразные вещества, но обязательно являющиеся электронными проводниками. Сюда относятся более электронофильные металлы, чем анод. Например, по отношению к железному аноду такими металлами являются Sn, Pb, Cu, Hg, Ag и т.п. Роль катодов может выполнять и ряд электропроводящих неметаллических материалов, среди которых назовём ржавчину, зёрна графита, угля, цементита (карбида железа Fe3C), шлаковые включения в металл и т.д.
Процессы, протекающие при гальванокоррозии, рассмотрим на двух примерах, представляющих практический интерес: коррозию железа в контакте: а) с цинком и б) с оловом во влажном воздухе.
а) Коррозионный процесс в гальванопаре Zn/Fe. Цинк, как сравнительно более химически активный металл, подвергается анодному окислению и переходит в состояние ионов.
Реакция на аноде**: 2Zn – 4e- → 2Zn** (окисление).
Реакция на катоде: 2h3O + O2 + 4e- → 4OH’ (восстановление).
Вторичная реакция: 2Zn** + 4OH’ → 2Zn(OH)2.
В процессе работы коррозионной гальванопары Zn/Fe окисляется, разрушается цинк. За счёт электронов последнего железо предохраняется от коррозии.
б) Коррозионный процесс в гальванопаре Sn/Fe. В данном случае железо более химически активный металл, чем олово. Катодом гальванопары будет олово, а анодом — железо.
Реакция на аноде**: 2Fe – 4e- → 2Fe** (окисление).
Реакция на катоде: 2h3O + O2 + 4e- → 4OH’ (восстановление).
Они приводят к образованию бурой ржавчины.
Таким образом, в процессе работы рассматриваемой гальванопары окисляется и разрушается железо, а олово остается без изменения.
На практике подобные явления встречаются при коррозии оцинкованного и луженого железа. В случае нанесения на железо менее химически активного металла (Sn, Cu, Ni, Cr, Ag, Au), для придания поверхности декоративных и других полезных свойств, защита железа происходит путем его изоляции от внешней среды. При повреждении внешнего защитного слоя начинают протекать описанные реакции и железо ржавеет.
При повреждении внешнего защитного слоя начинают протекать описанные реакции и железо ржавеет.
Коррозионные элементы могут возникать во всех случаях, когда в присутствии электролита соприкасаются металлы, различающиеся между собой электродными потенциалами.
Особо нужно отметить влияние температуры. Повышение температуры ускоряет физические и химические процессы. В водной среде это особенно заметно при температуре около 60°С. При температуре около 70°С в гальванопаре Zn/Fe может произойти изменение потенциала цинка, в результате чего цинковое покрытие становится катодам, а железо анодом. Отмечают, что изменению полярности цинка способствуют низкое содержание в воде кислорода и высокое бикарбонатов. В таких условиях коррозировать будет железо.
Электрокоррозия
К электрокоррозии относятся случаи электрохимической коррозии металлов, протекающие под влиянием электрического тока от внешнего источника. Здесь в основе явления, как уже отмечалось, лежит самопроизвольно возникающий процесс электролиза. В качестве примера рассмотрим электрокоррозию под влиянием так называемых блуждающих токов.
В качестве примера рассмотрим электрокоррозию под влиянием так называемых блуждающих токов.
Металлические листы с полимерным покрытием, сложенные в пачку, представляют собой электрический конденсатор, где металлическая основа листа представляет собой обкладки конденсатора, а полимерное покрытие — диэлектрический слой между обкладками. В следствие неравномерности нагрева листов, воздействия внешних источников энергии и других факторов окружающей среды между различными листами пачки могут возникать разности электрического потенциала.
В воде любого типа в большем или меньшем количестве содержатся растворенные соли, коллоидные и взвешенные вещества, живые микроорганизмы, в воду попадают частицы пыли и дыма. Поэтому при изучении поведения цинка и цинковых покрытий в водных средах воду следует рассматривать как коррозионный электролит. Если торцевую часть листов с разностью электрических потенциалов поместить в раствор соли, которым могут являться атмосферные осадки и конденсат, то возникает естественный процесс электролиза.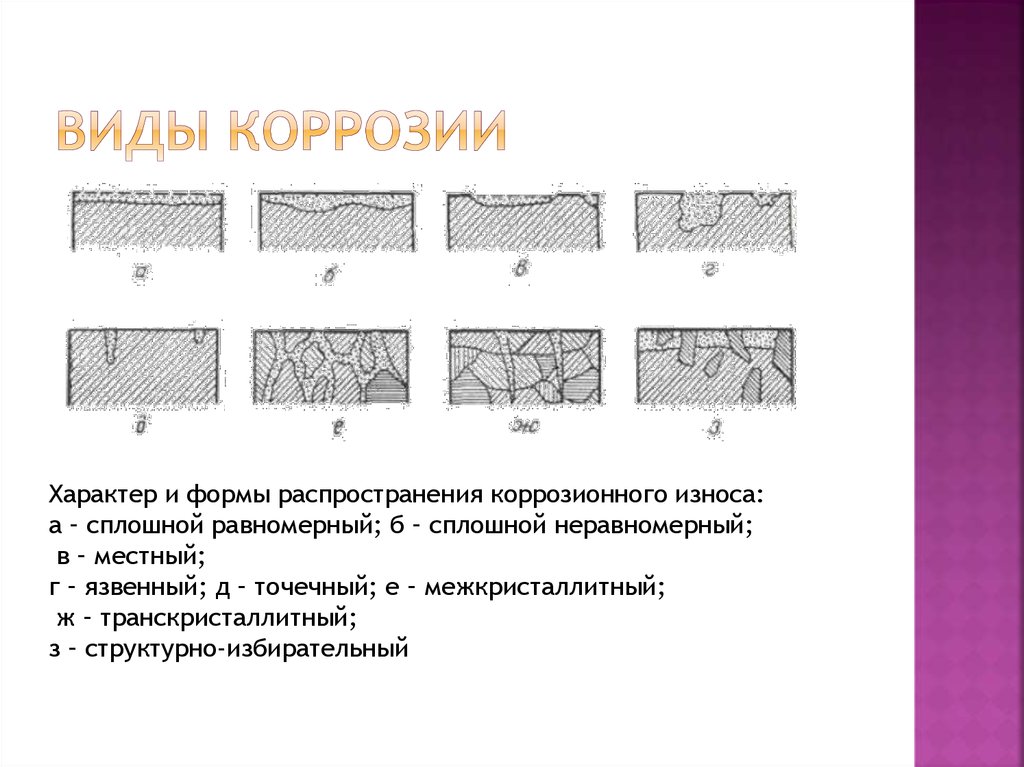 На одном из листов, на его торцевой части, будет происходить анодное окисление металла, т.е. его коррозия.
На одном из листов, на его торцевой части, будет происходить анодное окисление металла, т.е. его коррозия.
Состав электролита, в особенности величина его рН, существенно влияет на скорость коррозии. Так, повышение концентрации Н’-ионов (кислая среда), как правило, резко убыстряет разрушение металла.
Повышение концентрации ОН’-ионов (щелочная среда) в электролите замедляет коррозию таких металлов, как Fe, Mg в следствии образования гидроокисных защитных плёнок.
У металлов Al, Zn, Pb повышение щелочности среды на разрушение этих металлов действует убыстряющим образом т.к. гидроокиси этих металлов растворимы в щелочах. Описанная особенность этих металлов является причиной такого явления как белая ржавчина.
Белая ржавчина на цинковом покрытии
Цинк — сравнительно реактивный металл, он активно реагирует с кислотами и щелочами. Лучше всего он проявляет свои антикоррозионные свойства в рН нейтральной среде. Долговечность цинкового покрытия зависит от формирования оксидно-карбонатной пленки. После окончательного формирования оксидно-карбонатной пленки уровень коррозии цинковых покрытий становится очень низким — не более двух микрон в год в нейтральной среде.
Долговечность цинкового покрытия зависит от формирования оксидно-карбонатной пленки. После окончательного формирования оксидно-карбонатной пленки уровень коррозии цинковых покрытий становится очень низким — не более двух микрон в год в нейтральной среде.
Химические реакции, требуемые для формирования этой плёнки, занимают некоторое время (от нескольких недель до нескольких месяцев):
1. Фаза окисления 2Zn + O2 = 2ZnO
2. Фаза гидратации 2Zn = 2h3O + O2 = 2Zn(OH)2
3. Карбонизации 5Zn(OH)2 = 2CO2 + 2ZnCO3.3Zn(OH)2 + 2h3O
На последнем этапе окончательно формируется трудно растворимый основной карбонат цинка, который обеспечивает надежную антикоррозионную защиту цинковому слою при негативном воздействии влаги. В условиях относительно сухой среды протекают все три реакции, и на поверхности оцинкованного изделия формируется оксидно-карбонатная плёнка, будучи почти непроницаемой для кислорода и влаги, резко ограничивает дальнейший процесс взаимодействия цинка с кислородом.
Иное происходит, если изделие свежеоцинкованное или на нём присутствуют места без сформированного плёночного покрытия (в частности, срезы профилированной продукции) хранится в условиях, когда на него воздействует дождь, роса, конденсат, а подвод углекислого газа и кислорода, способствующего образованию плотной оксидно-карбонатной пленки затруднен. В этом случает происходят только фазы окисления и гидратации. В результате получаются гидроксид и оксид цинка — вещества в виде белого порошка, обладающие низкой адгезионной способностью к поверхности, легко пропускающие кислород к цинку, допускающие его последующее окисление и развитие процессов образования белой ржавчины.
Еще одним случаем, представляющим опасность образования белой ржавчины, являются участки соприкасающихся между собой поверхностей оцинкованных изделий с уже окончательно сформировавшейся оксидно-карбонатной плёнкой. В этих местах задерживается дождевая влага (или конденсируется влага из воздуха при нахождении изделий на воздухе при температуре ниже точки росы), а испаряется она в последнюю очередь.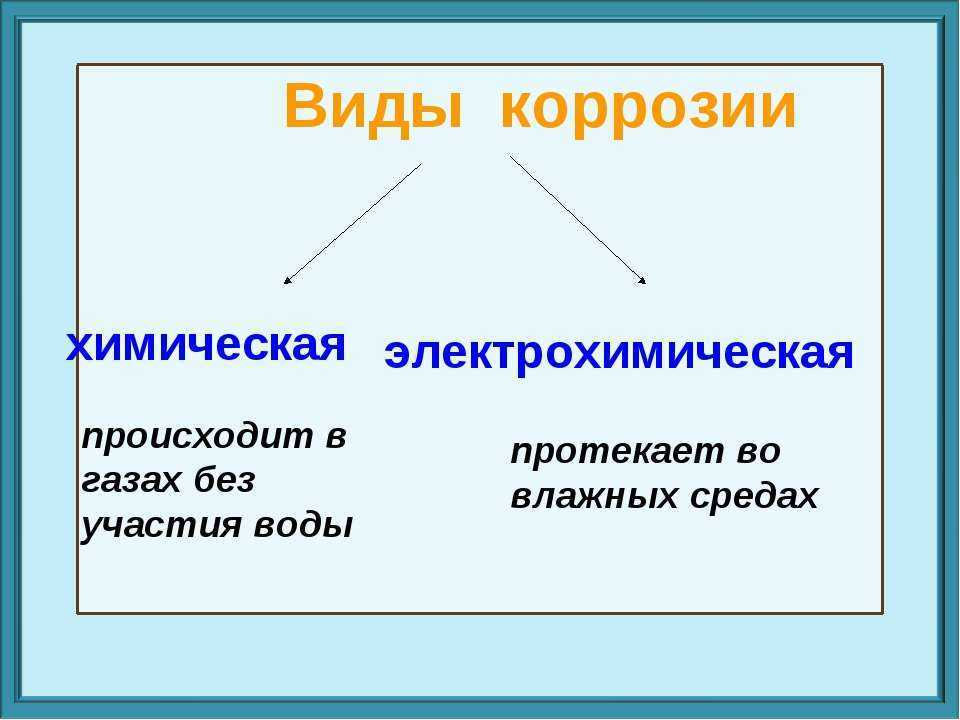 Во всех природных водах присутствует углекислота, которая может находиться в воде в виде растворенного газа СО2 и недиссоциированных молекул Н2СО3 или ионов НСО3- и СО3в2-. Углекислота и присутствующие в воде нитраты, сульфаты, хлориды без доступа кислорода разрушают образующуюся на поверхности цинка оксидно-карбонатную пленку и тем самым усиливают коррозию, приводящую к образованию белой ржавчины.
Во всех природных водах присутствует углекислота, которая может находиться в воде в виде растворенного газа СО2 и недиссоциированных молекул Н2СО3 или ионов НСО3- и СО3в2-. Углекислота и присутствующие в воде нитраты, сульфаты, хлориды без доступа кислорода разрушают образующуюся на поверхности цинка оксидно-карбонатную пленку и тем самым усиливают коррозию, приводящую к образованию белой ржавчины.
При очень длительном хранении (от полугода) оцинкованных изделий с полимерным покрытием в неблагоприятных условиях, оксид и гидроксид цинка — вещества в виде белого порошка может выделяться и на поверхности полимерного покрытия (в особенности на обратной стороне листа, который как правило покрыт только грунтовым полимерным слоем).
В благоприятных (для белой ржавчины) условиях разъедание цинка может происходить при уровнях коррозии в 20–50 раз больших, чем обычно предполагается.
Условия хранения и эксплуатации
Из всего вышеизложенного можно сделать следующие выводы.
Цинковое покрытие стальных изделий хорошо работает как защитный слой в нейтральной сухой или влажной воздушной среде и при кратковременном воздействии воды со свободным доступом кислорода. При таких условиях работает эффект гальванопары Zn/Fe — эффект оксидно-карбонатной пленки. Такие условия соответствуют нормальным условиям эксплуатации изделий.
В случае долговременного нахождения стальных оцинкованных изделий, сложенных в пачку, в водной среде при ограниченном доступе кислорода и повышенной температуре (более 70°С), начинают протекать реакции, при которых защитные эффекты перестают работать. Происходит активное разрушение защитного слоя. Как правило, такие негативные условия складываются при неправильном хранении изделий. При нарушении условий хранения риск поражения коррозией значительно выше, чем при неправильной эксплуатации или монтаже.
Правила хранения оцинкованных изделий:
• Изделия хранятся в заводской упаковке НЕ более 1 (одной) недели с даты поставки. Пачки в заводской упаковке укладываются на ровное место на бруски с шагом 0,5 м.
Пачки в заводской упаковке укладываются на ровное место на бруски с шагом 0,5 м.
• При необходимости хранения профилированной продукции более 1 (одной) недели ее размещают под навесами или в крытых неотапливаемых, сухих помещениях без прямого воздействия солнечных лучей и осадков (в соответствии с ГОСТ 7566).
Изделия следует распаковать (снять заводскую упаковку), расположить на ровной поверхности и переложить каждый лист одинаковыми рейками (штабель высотой до 70 см).
• Хранение на открытом воздухе допускается только на период монтажных работ. Изделия должны быть расположены под небольшим наклоном в 3° так, чтобы между ними обеспечивались свободная циркуляция воздуха и слив воды.
• Максимальный срок хранения во всех вышеперечисленных условиях не должен превышать 2 (двух) месяцев с даты поставки.
Используемая литература:
- «Общая химия» учебники и учебные пособия для высших сельскохозяйственных учебных заведений.
 А.Г. Кульман. Издательство «Колос» 1968.
А.Г. Кульман. Издательство «Колос» 1968. - «Курс общей химии» учебник для студентов вузов. Коровин Н.В., Масленникова Г.Н., Гуськова Л.Г. и др. под ред. Коровина Н.В. Высш. школа 1981.
- «Защита от коррозии, старения и биоповреждений машин, оборудовани и сооружений» Справочник в 2т. Т1. Под ред. Герасименко А.А. М. Машиностроение. 1987.
- «Основы учения о коррозии и защите металлов» Дж. Скалли. Перевод с английского проф. А.В. Шрейдера. Издательство «Мир», Москва 1978.
- СТБ 1527-2005 «Профили металлические холодногнутые для наружной облицовки фасадов зданий и комплектующие изделия к ним».
- СТБ 1382-2003 «Профили металлические холодногнутые для кровель и комплектующие изделия к ним».
- ГОСТ 7566-2018 «Металлопродукция. Правила приемки, маркировка, упаковка, транспортирование и хранение».
Типы коррозии и предотвращение — различные типы коррозии
Опубликовано в июне 2017 г.
В предыдущем посте мы обсудили основы коррозии — от фундаментальной химической реакции до типов сред, в которых может возникнуть коррозия.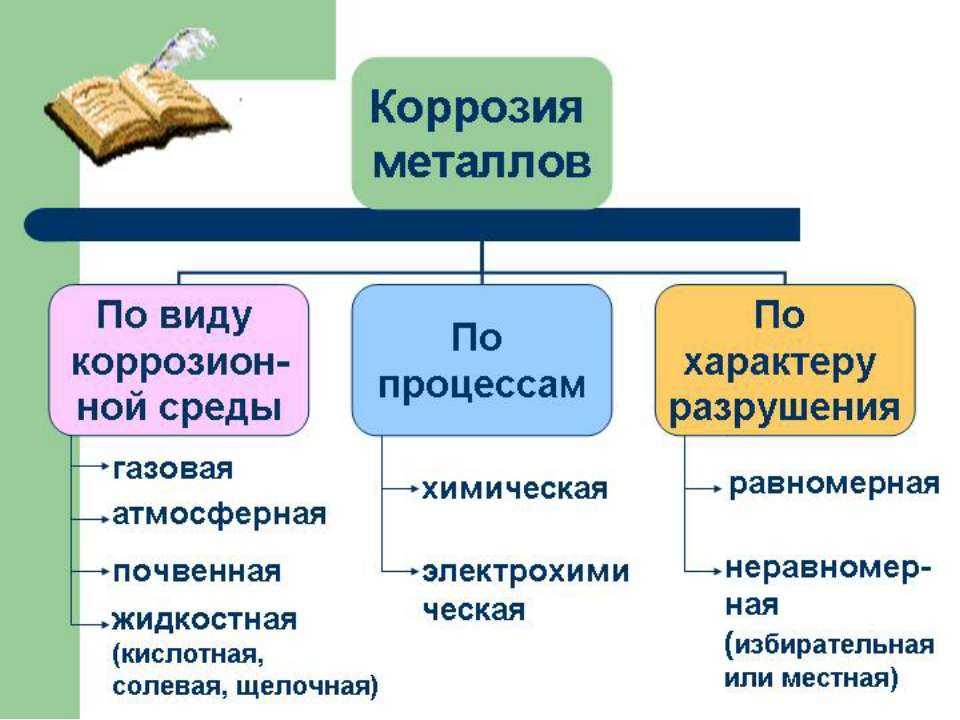 Поскольку коррозия чаще всего возникает в водной среде, теперь мы исследуем различные типы разрушения металла в таких условиях: коррозии. Он также является наиболее безобидным, поскольку степень атаки относительно легко оценить, а результирующее влияние на характеристики материала довольно легко оценить благодаря способности последовательно воспроизводить и тестировать явление. Этот тип коррозии обычно возникает на относительно больших участках поверхности материала.
Поскольку коррозия чаще всего возникает в водной среде, теперь мы исследуем различные типы разрушения металла в таких условиях: коррозии. Он также является наиболее безобидным, поскольку степень атаки относительно легко оценить, а результирующее влияние на характеристики материала довольно легко оценить благодаря способности последовательно воспроизводить и тестировать явление. Этот тип коррозии обычно возникает на относительно больших участках поверхности материала.
Точечная коррозия
Точечная коррозия является одним из наиболее разрушительных видов коррозии, поскольку ее трудно предсказать, обнаружить и охарактеризовать. Точечная коррозия представляет собой локализованную форму коррозии, при которой либо локальная анодная точка, либо, чаще, катодная точка образуют небольшую коррозионную ячейку с окружающей нормальной поверхностью. После образования ямы она превращается в «дыру» или «полость», которая принимает одну из множества различных форм. Ямы обычно проникают с поверхности вниз в вертикальном направлении. Питтинговая коррозия может быть вызвана локальным разрывом или повреждением защитной оксидной пленки или защитного покрытия; это также может быть вызвано неоднородностью самой структуры металла. Точечная коррозия опасна тем, что может привести к разрушению конструкции при относительно небольших общих потерях металла.
Питтинговая коррозия может быть вызвана локальным разрывом или повреждением защитной оксидной пленки или защитного покрытия; это также может быть вызвано неоднородностью самой структуры металла. Точечная коррозия опасна тем, что может привести к разрушению конструкции при относительно небольших общих потерях металла.
Щелевая коррозия
Щелевая коррозия также является локализованной формой коррозии и обычно является результатом застойной микросреды, в которой существует разница в концентрации ионов между двумя участками металла. Щелевая коррозия возникает в защищенных зонах, например, под шайбами, головками болтов, прокладками и т. д., где доступ кислорода ограничен. Эти меньшие площади позволяют проникнуть коррозионному агенту, но не обеспечивают достаточной циркуляции внутри, истощая содержание кислорода, что предотвращает повторную пассивацию. По мере образования застойного раствора pH сдвигается от нейтрального. Этот растущий дисбаланс между щелью (микросреда) и внешней поверхностью (объемная среда) способствует более высокой скорости коррозии.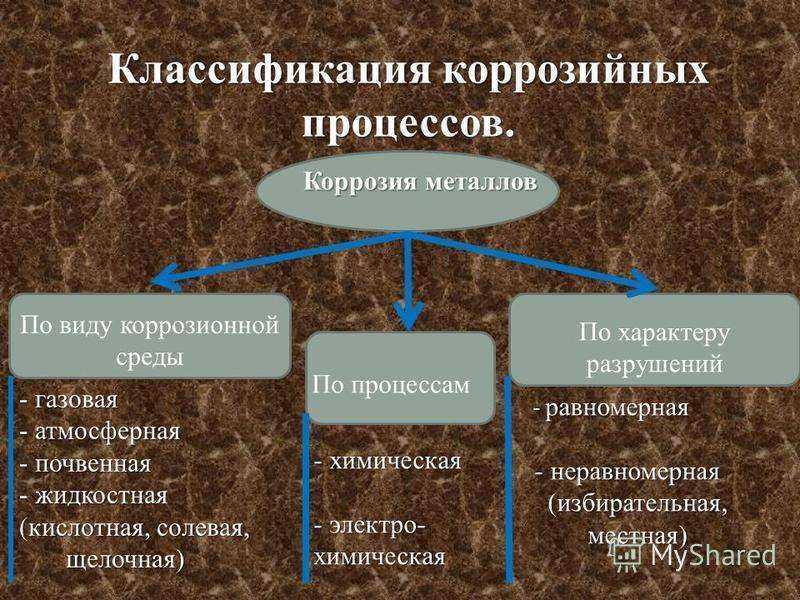 Щелевая коррозия часто может возникать при более низких температурах, чем точечная коррозия. Правильная конструкция соединения помогает свести к минимуму щелевую коррозию.
Щелевая коррозия часто может возникать при более низких температурах, чем точечная коррозия. Правильная конструкция соединения помогает свести к минимуму щелевую коррозию.
Межкристаллитная коррозия
При исследовании микроструктуры металла выявляются зерна, образующиеся при затвердевании сплава, а также границы зерен между ними. Межкристаллитная коррозия может быть вызвана примесями, присутствующими на этих границах зерен, или истощением или обогащением легирующим элементом на границах зерен. Межкристаллитная коррозия происходит вдоль этих зерен или рядом с ними, серьезно влияя на механические свойства металла, в то время как основная часть металла остается неповрежденной.
Примером межкристаллитной коррозии является осаждение карбида, химическая реакция, которая может происходить, когда металл подвергается воздействию очень высоких температур (например, 800°F — 1650°F) и/или локальным горячим работам, таким как сварка. В нержавеющих сталях во время этих реакций углерод «поглощает» хром, образуя карбиды и вызывая падение уровня хрома, оставшегося в сплаве, ниже 11%, необходимых для поддержания спонтанно формирующегося пассивного оксидного слоя. 304L и 316L представляют собой улучшенный химический состав нержавеющей стали 304 и 316, который содержит меньше углерода и обеспечивает наилучшую коррозионную стойкость к осаждению карбида.
304L и 316L представляют собой улучшенный химический состав нержавеющей стали 304 и 316, который содержит меньше углерода и обеспечивает наилучшую коррозионную стойкость к осаждению карбида.
Коррозионное растрескивание под напряжением (SCC)
Коррозионное растрескивание под напряжением (SCC) является результатом сочетания напряжения растяжения и агрессивной среды, часто при повышенных температурах. Коррозия под напряжением может возникнуть в результате внешнего напряжения, такого как фактические растягивающие нагрузки на металл или расширение/сжатие из-за быстрых изменений температуры. Это также может быть результатом остаточного напряжения, возникающего в процессе производства, например, при холодной штамповке, сварке, механической обработке, шлифовке и т. Д. При коррозии под напряжением большая часть поверхности обычно остается неповрежденной; однако в микроструктуре появляются мелкие трещины, из-за чего коррозию трудно обнаружить. Трещины обычно имеют хрупкий вид, формируются и распространяются в направлении, перпендикулярном местонахождению напряжения. Выбор подходящих материалов для данной среды (включая температуру и управление внешними нагрузками) может снизить вероятность катастрофического отказа из-за SCC.
Выбор подходящих материалов для данной среды (включая температуру и управление внешними нагрузками) может снизить вероятность катастрофического отказа из-за SCC.
Гальваническая коррозия
Гальваническая коррозия представляет собой разрушение одного металла вблизи стыка или соединения, которое происходит, когда два электрохимически разнородных металла находятся в электрическом контакте в электролитической среде; например, когда медь находится в контакте со сталью в морской среде. Однако даже при выполнении этих трех условий существует множество других факторов, влияющих на вероятность и степень коррозии, например, температура и качество поверхности металлов. Крупные инженерные системы, в конструкции которых используются различные типы металлов, в том числе различные типы крепежных изделий и материалы, подвержены гальванической коррозии, если не соблюдать осторожность на этапе проектирования. Выбор металлов, которые находятся как можно ближе друг к другу в гальванической серии, помогает снизить риск гальванической коррозии.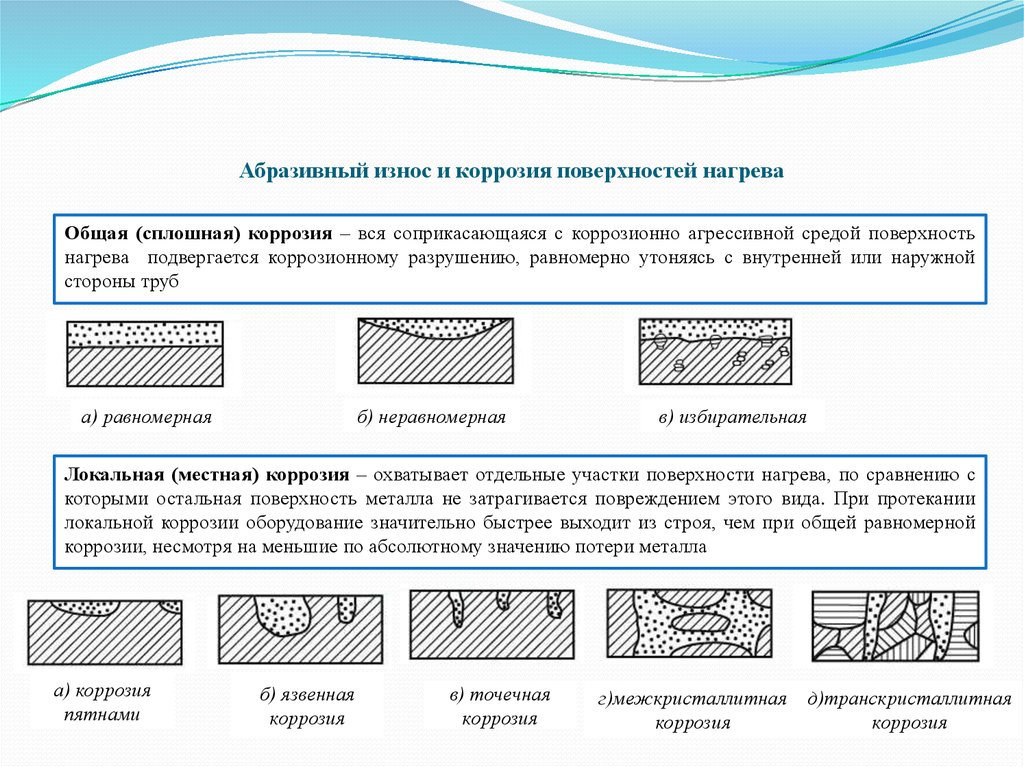
Заключение
В водной среде металлы могут подвергаться не только однородной коррозии, но и различным видам локальной коррозии, включая точечную, щелевую, межкристаллитную, стрессовую и гальваническую коррозию. В областях, где коррозия вызывает беспокойство, изделия из нержавеющей стали предлагают ценность и защиту от этих угроз. Благоприятный химический состав нержавеющей стали делает ее устойчивой ко многим распространенным коррозионным воздействиям, оставаясь при этом значительно более доступным по цене, чем специальные сплавы, такие как титан и сплавы Inconel®.
Нержавеющая сталь представляет собой высоколегированную низкоуглеродистую сталь с высоким (не менее 11%) содержанием хрома. Под воздействием насыщенной кислородом среды хром вступает в реакцию, образуя пассивный оксидный слой на поверхности металла, замедляя дальнейшее окисление и обеспечивая качество самовосстановления, что помогает противостоять равномерной и локальной коррозии. Никель помогает стабилизировать микроструктуру, повышая устойчивость к SCC. Марганец в умеренных количествах и в сочетании с никелем будет выполнять многие функции, присущие никелю, и помогает предотвратить точечную коррозию. Добавление молибдена (дополнительный элемент в нержавеющей стали типа 316, повышающий ее характеристики по сравнению с нержавеющей сталью типа 304) помогает повысить стойкость к точечной и щелевой коррозии. Пониженное содержание углерода, например, в стали 304L и 316L, поможет предотвратить межкристаллитную коррозию. Наконец, азот, хотя и не является основным элементом в составе нержавеющей стали, повышает устойчивость к точечной коррозии. Выбор нержавеющей стали может помочь значительно снизить риск коррозии и обеспечить долгосрочную экономию, избегая затрат, связанных с повторной установкой некачественных продуктов.
Марганец в умеренных количествах и в сочетании с никелем будет выполнять многие функции, присущие никелю, и помогает предотвратить точечную коррозию. Добавление молибдена (дополнительный элемент в нержавеющей стали типа 316, повышающий ее характеристики по сравнению с нержавеющей сталью типа 304) помогает повысить стойкость к точечной и щелевой коррозии. Пониженное содержание углерода, например, в стали 304L и 316L, поможет предотвратить межкристаллитную коррозию. Наконец, азот, хотя и не является основным элементом в составе нержавеющей стали, повышает устойчивость к точечной коррозии. Выбор нержавеющей стали может помочь значительно снизить риск коррозии и обеспечить долгосрочную экономию, избегая затрат, связанных с повторной установкой некачественных продуктов.
По вопросам о различных типах коррозии или о нашем предложении из нержавеющей стали, пожалуйста, обращайтесь к нам.
8 наиболее распространенных форм коррозии металлов
Коррозия ежедневно воздействует на наше общество. Автомобили, здания, инфраструктура, бытовая техника и системы распределения энергии являются примерами некоторых компонентов, на которые отрицательно влияет это явление.
Автомобили, здания, инфраструктура, бытовая техника и системы распределения энергии являются примерами некоторых компонентов, на которые отрицательно влияет это явление.
Реклама
Коррозия определяется как повреждение материала в результате химических реакций между ним и окружающей средой. Хотя коррозия затрагивает множество материалов, включая полимеры и керамику, этот термин чаще всего ассоциируется с деградацией металлов.
В исследовании 2016 года, проведенном NACE (ранее известной как Национальная ассоциация инженеров-коррозионистов) и изложенном в их публикации «Международные меры по предотвращению, применению и экономике технологии коррозии (IMPACT)», коррозия влечет за собой глобальные затраты в размере 2,5 триллиона долларов США. Эта цифра составляет примерно 3,4 процента мирового валового внутреннего продукта (ВВП).
Реклама
Наиболее распространенные типы коррозии
Коррозия состоит из ряда обычно сложных химических реакций и может быть инициирована несколькими различными механизмами, которые зависят от окружающей среды. Это привело к появлению различных классификаций коррозии.
Это привело к появлению различных классификаций коррозии.
Все виды коррозии неодинаковы. Ключ к эффективному предотвращению и смягчению коррозии лежит в базовом понимании типа коррозии, с которой приходится иметь дело, и факторов, ответственных за ее образование. В этой статье мы рассмотрим наиболее распространенные виды коррозии и объясним механизм, лежащий в основе каждого из них.
Равномерная коррозия
Равномерная коррозия является наиболее распространенным типом и характеризуется поражением всей поверхности металла, подвергающегося воздействию коррозионного агента. Этот тип коррозии обычно вызывается химическими или электрохимическими реакциями, в результате которых металл расходуется с образованием оксидов или других соединений на больших видимых участках. Эти реакции вызывают потерю толщины металла с течением времени и могут продолжаться до тех пор, пока металл полностью не растворится. (Узнайте, как авиационная промышленность справляется с этим типом коррозии, в статье «Обнаружение и лечение однородной коррозии в самолетах». )
)
Гальваническая/биметаллическая коррозия
Биметаллическая коррозия, также известная как гальваническая коррозия, представляет собой коррозию, возникающую при прямом или косвенном контакте двух разнородных металлов друг с другом. Визуально этот вид коррозии характеризуется ускоренным износом одного металла, в то время как другой остается нетронутым.
Реклама
Биметаллическая коррозия — это чисто электрохимическая реакция, вызванная разницей электродных потенциалов между двумя металлами. При воздействии электролита два металла образуют тип элемента, известный как биметаллическая пара, где один металл действует как анод, а другой — как катод. Движение электронов от анода к катоду инициирует реакцию окисления на аноде, которая вызывает его растворение, то есть коррозию.
На этот тип коррозии влияет величина разности потенциалов между двумя металлами. Следовательно, чем дальше друг от друга находятся металлы в гальваническом ряду, тем выше скорость коррозии на аноде. (Эта тема рассматривается в разделе «Введение в серию гальванических материалов: гальваническая совместимость и коррозия».)
(Эта тема рассматривается в разделе «Введение в серию гальванических материалов: гальваническая совместимость и коррозия».)
Щелевая коррозия
Щелевая коррозия — это высокопроникающий тип локальной коррозии, который возникает в зазорах или щелях на поверхности или непосредственно рядом с ними. металл. Эти щели могут быть результатом соединения двух поверхностей (металла с металлом или металла с неметаллом) или скопления отложений (грязь, грязь, биообрастание и т. д.). Этот тип коррозии характеризуется разрушением в области щели, в то время как окружающие участки металлической подложки остаются нетронутыми.
Одним из основных критериев развития щелевой коррозии является наличие застоя воды в щели. Это отсутствие движения жидкости приводит к истощению растворенного кислорода и обилию положительных ионов в щели. Это приводит к ряду электрохимических реакций, которые изменяют состав жидкости и делают ее кислой по своей природе. Кислотная жидкость в щели разрушает пассивный слой металла и делает его уязвимым для коррозии.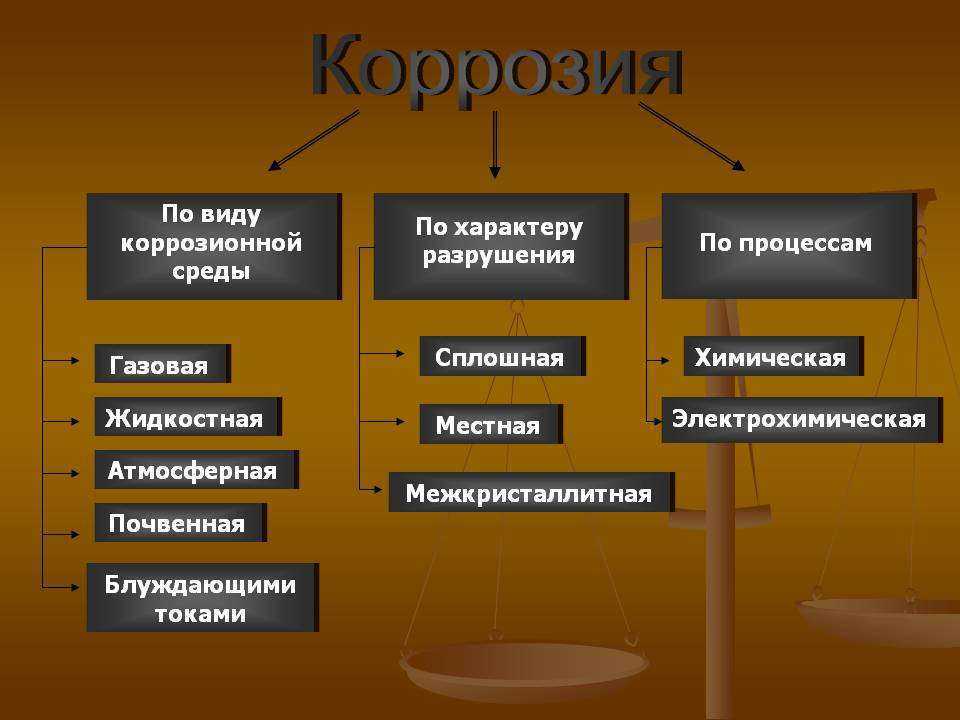
Точечная коррозия
Точечная коррозия, также известная как точечная коррозия, представляет собой еще одну локализованную форму коррозии, возникающую на металлических поверхностях. Питтинг обычно проявляется в виде полостей или отверстий небольшого диаметра на поверхности объекта, в то время как остальная часть металлической поверхности остается нетронутой. Эта форма коррозии также обладает высокой проникающей способностью и считается одним из наиболее опасных видов коррозии, поскольку ее трудно предсказать и она имеет тенденцию вызывать внезапные и экстремальные отказы.
Точечная коррозия обычно возникает на участках металлической поверхности, где существуют несоответствия защитной пассивной пленки. Эти несоответствия могут быть вызваны повреждением пленки, некачественным нанесением покрытия или посторонними отложениями на поверхности металла. Области, где пассивность была уменьшена или потеряна, теперь становятся анодом, а окружающие области действуют как катод. В присутствии влаги анод и катод образуют коррозионную ячейку, в которой анод (т. е. незащищенные пассивирующей пленкой области) подвергается коррозии. Поскольку коррозия ограничивается локализованной областью, точечная коррозия имеет тенденцию проникать в толщу материала.
В присутствии влаги анод и катод образуют коррозионную ячейку, в которой анод (т. е. незащищенные пассивирующей пленкой области) подвергается коррозии. Поскольку коррозия ограничивается локализованной областью, точечная коррозия имеет тенденцию проникать в толщу материала.
Межкристаллитная коррозия
Межкристаллитная коррозия включает ускоренную коррозию по границам зерен металла, в то время как основная часть поверхности металла остается свободной от коррозии. Некоторые сплавы при неправильной термообработке могут иметь сегрегацию примесей на границах зерен, что может затруднить пассивирование этих областей. Границы зерен теперь представляют собой путь высокой коррозионной уязвимости.
Например, аустенитные нержавеющие стали могут быть подвержены межкристаллитному разрушению, если их нагревают от 500°С до 800°С (9от 30°F до 1470°F). При этих температурах карбид хрома может выделяться на границах зерен, что снижает локальную концентрацию хрома на границах. (Дополнительную информацию по этой теме см. в разделе «Роль хрома в межкристаллитной коррозии».) Маловероятно, что граница зерен образует эффективную пассивную пленку и теперь подвержена коррозии.
(Дополнительную информацию по этой теме см. в разделе «Роль хрома в межкристаллитной коррозии».) Маловероятно, что граница зерен образует эффективную пассивную пленку и теперь подвержена коррозии.
Селективное выщелачивание
В определенных агрессивных средах некоторые металлические сплавы могут подвергаться коррозии, при которой только один элемент сплава разрушается и удаляется в результате коррозии. Это дискриминационное удаление определенного элемента известно как селективное выщелачивание или удаление примесей.
Наиболее распространенным примером этого явления является селективное удаление менее благородного элемента цинка из латунных сплавов, также известное как обесцинкование. Сплавы, состоящие из металлических элементов, наиболее удаленных друг от друга в гальваническом ряду, наиболее подвержены этому типу коррозии.
Эрозионная коррозия
Эрозионная коррозия определяется как ускоренное ухудшение состояния металла в результате относительного движения между коррозионной жидкостью и поверхностью металла.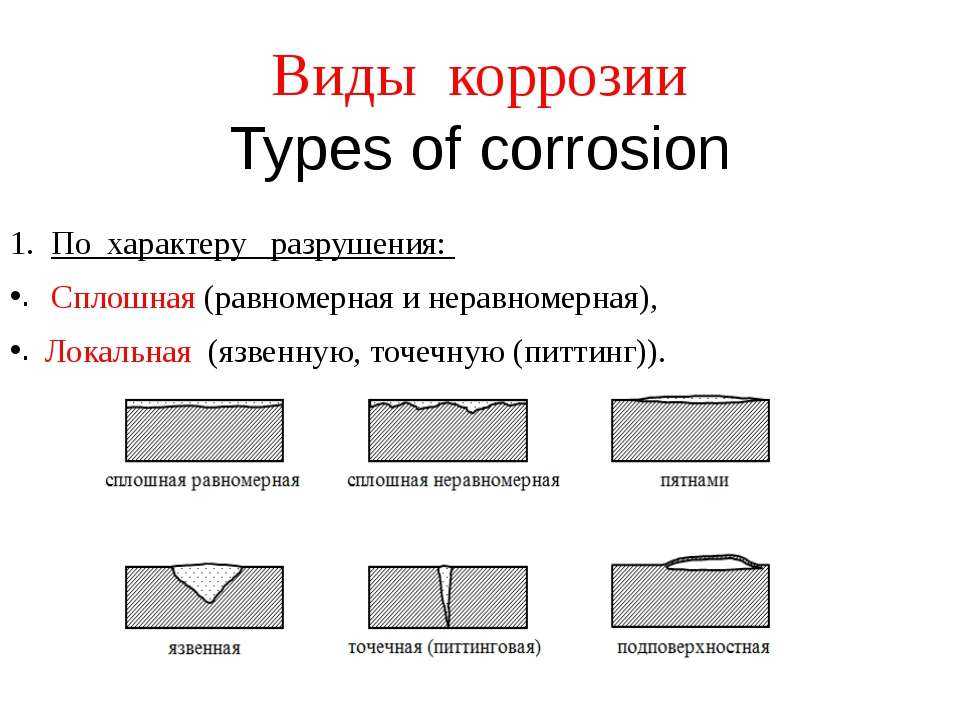 По мере того, как жидкость течет по поверхности (обычно с высокой скоростью), пассивный оксидный слой металла может быть удален или растворен, в результате чего сплав может быть поврежден. Во время этого процесса металл может удаляться в виде растворенных ионов или в виде продуктов коррозии, которые механически смываются с поверхности металла под действием протекающей жидкости.
По мере того, как жидкость течет по поверхности (обычно с высокой скоростью), пассивный оксидный слой металла может быть удален или растворен, в результате чего сплав может быть поврежден. Во время этого процесса металл может удаляться в виде растворенных ионов или в виде продуктов коррозии, которые механически смываются с поверхности металла под действием протекающей жидкости.
Эрозионная коррозия визуально распознается по появлению канавок, канав, кратеров и впадин в направленном узоре на металлической основе. (Узнайте, как предотвратить эрозионную коррозию, в статье «Эрозионная коррозия: покрытия и другие профилактические меры».) поверхности металла, в то время как металл остается незатронутым на большей части своей поверхности. Это растрескивание обычно происходит из-за одновременного наличия растягивающих напряжений в агрессивной среде. SCC считается коварной формой коррозии, потому что повреждение иногда не сразу обнаруживается во время осмотра и может привести к внезапным катастрофическим отказам.
Сварка, термическая обработка и холодная деформация могут вызвать остаточные напряжения в объекте, которые могут вызвать SCC. Одной из ситуаций, когда может возникнуть SCC, являются границы зерен, подвергшихся коррозии в результате межкристаллитной коррозии. Поскольку границы зерен ослабли из-за сегрегации примесей, приложенные остаточные силы растяжения могут привести к мелкому растрескиванию микроструктуры.
Заключение
Коррозия существует во многих формах и может быть вызвана многочисленными механизмами. Есть много других, хотя и менее известных, видов коррозии, не упомянутых в этой статье.
Тип коррозии, которая может образоваться на конкретной металлической поверхности, зависит в первую очередь от окружающей среды и физических и химических свойств металла. Поэтому очень важно понимать механизмы, задействованные в каждом типе коррозии, чтобы гарантировать, что при необходимости будут применяться наиболее эффективные меры предотвращения и смягчения последствий.
Реклама
Связанные термины
- Тип коррозии
- Равномерная коррозия
- Гальваническая коррозия
- Щелевая коррозия
- Питтинговая коррозия
- Межкристаллитная коррозия
- Эрозия Коррозия
- Потенциал электрода
- Локальная коррозия
- Коррозионное растрескивание под напряжением
Поделиться этой статьей
Типы коррозии | Американская ассоциация гальваников
Типы коррозии | Американская ассоциация гальванистов
•
Быстрые ссылки •
Поиск
Поиск не дал результатов
Страницы сайта
База знаний Dr. Galv
Галерея проектов
Нажмите ESC, чтобы выйти
Забыли пароль?
Дом »
Коррозия »
Процесс коррозии металла »
Типы коррозии
Существует несколько типов коррозии, и наука и понимание этих процессов постоянно развиваются. Вот краткий обзор некоторых распространенных типов коррозии:
Вот краткий обзор некоторых распространенных типов коррозии:
- Гальваническая коррозия является наиболее распространенной и опасной формой коррозии. Это происходит при контакте двух разнородных (разных) металлов в присутствии электролита. В гальваническом элементе (биметаллическая пара) корродирует более активный металл (анод) и защищается более благородный металл (катод). Существует ряд факторов, влияющих на гальваническую коррозию, включая типы металлов, относительный размер анода и окружающую среду (температура, влажность, соленость и т. д.)
- Питтинговая коррозия возникает при определенных условиях, что приводит к ускоренной коррозии в определенных областях, а не к равномерной коррозии по всей детали. Такие условия включают низкие концентрации кислорода или высокие концентрации хлоридов (анионов), которые мешают способности сплавов образовывать пассивирующую пленку. В худшем случае большая часть поверхности остается защищенной, но крошечные флуктуации разрушают пленку в нескольких критических областях.
 Коррозия в этих точках усиливается и может вызвать ямки.
Коррозия в этих точках усиливается и может вызвать ямки. - Микробная коррозия , обычно называемая микробиологической коррозией (MIC), вызывается микроорганизмами. Это относится как к металлическим, так и к неметаллическим материалам с кислородом или без него. Когда кислород отсутствует, сульфатредуцирующие бактерии активны и производят сероводород, вызывая сульфидное растрескивание под напряжением. При наличии кислорода некоторые бактерии могут непосредственно окислять железо до оксидов и гидроксидов железа. В отложениях продуктов коррозии могут образовываться концентрационные ячейки, приводящие к локальной коррозии.
- Высокотемпературная коррозия , как следует из названия, представляет собой повреждение металла из-за нагревания. Это может произойти, когда металл подвергается воздействию горячей атмосферы в присутствии кислорода, серы или другого соединения, способного окислять материал.
- Щелевая коррозия возникает в замкнутых пространствах, где ограничен доступ жидкости из окружающей среды, например, в зазорах и зонах контакта между деталями, под прокладками или уплотнениями, внутри трещин и швов и в пространствах, заполненных отложениями.
Необходимо (Обязательно)
Файлы cookie, без которых сайт не может нормально функционировать. Это включает файлы cookie для доступа к безопасным областям и безопасности CSRF. Обратите внимание, что файлы cookie по умолчанию Craft не собирают никакой личной или конфиденциальной информации. Файлы cookie по умолчанию Craft не собирают IP-адреса. Информация, которую они хранят, не отправляется Pixel & Tonic или каким-либо третьим сторонам.
Имя : CraftSessionId
Описание : Craft использует сеансы PHP для поддержки сеансов через веб-запросы. Это делается с помощью файла cookie сеанса PHP. По умолчанию имя файла cookie «CraftSessionId», но его можно переименовать с помощью настройки конфигурации phpSessionId. Срок действия этого файла cookie истечет, как только завершится сеанс.
Провайдер : этот сайт
Срок действия : Сеанс
Имя : *_identity
Описание : При входе в панель управления будет использоваться аутентифицированный файл cookie. Имя файла cookie начинается с длинной случайно сгенерированной строки, за которой следует _identity. Файл cookie хранит только информацию, необходимую для поддержания безопасного аутентифицированного сеанса, и будет существовать только до тех пор, пока пользователь аутентифицируется в Craft.
Имя файла cookie начинается с длинной случайно сгенерированной строки, за которой следует _identity. Файл cookie хранит только информацию, необходимую для поддержания безопасного аутентифицированного сеанса, и будет существовать только до тех пор, пока пользователь аутентифицируется в Craft.
Провайдер : этот сайт
Срок действия : Постоянный
Имя : *_username
Описание : Если вы отметите этот куки-файл во время входа в систему, я запомню параметр «Сохранить в системе». имя пользователя для вашей следующей аутентификации.
Поставщик : этот сайт
Срок действия : Постоянный
Имя : CRAFT_CSRF_TOKEN
Описание Cross-Site Forger : Защищает вас как пользователя от атак Forger.
Поставщик : этот сайт
Срок действия : Сеанс
Статистика
Статистические файлы cookie помогают нам понять, как посетители взаимодействуют с веб-сайтами, собирая и сообщая информацию анонимно.
